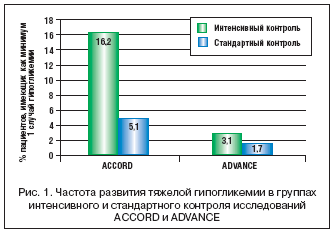
Пристальное внимание к проблеме влияния гипогликемии на развитие осложнений было привлечено после оглашения результатов исследования ACCORD (Action to Control Cardiovascular Risk in Diabetes), которое имело целью оценить влияние интенсивного (с целевым значением HbA1с 6,0%) и стандартного (с целевым значением HbA1с 7,0–7,0%) лечения на риск развития осложнений у пациентов с HbA1с≥7,5% и наличием макрососудистых осложнений в анамнезе. В группе интенсивного лечения HbA1c удалось снизить спустя 4 мес. до 6,7%, спустя 1 год – до 6,4%. Однако главным результатом исследования стало увеличение смертности в группе интенсивной терапии на 22% по сравнению с группой стандартной терапии. Среди главных причин, вызвавших неблагоприятное развитие событий, обсуждались частые гипогликемические состояния (16,2% тяжелых гипогликемий в группе интенсивного контроля по сравнению с 5,1% – в группе стандартного контроля) (рис. 1). Ретроспективный анализ, проведенный в рамках данного исследования, подтвердил четкую взаимосвязь между частотой развития тяжелых гипогликемий и повышенным риском смертности, что было выявлено как в группе интенсивной, так и традиционной терапии. В то же время, другое базовое исследование ADVANCE продемонстрировало благоприятный исход в группе интенсивного контроля (цель – HbA1c – 6,5%), где снижение риска микро– и макрососудистых осложнений составило 10% (p<0,013), сердечно–сосудистой смертности –12% (p<0,12), риск развития нефропатии был равен 21% (p<0,006), макроальбуминурии – 30% (p<0,001), что было сопряжено с низким риском развития гипогликемий (0,7 на 100 пациентов в год) (табл. 1). По данным зарубежных авторов, 5% пожилых больных СД 2–го типа, получающих инсулин, при уровне HbA1c 8,5% имеют как минимум одну тяжелую гипогликемию в год.
В настоящее время не существует единого определения гипогликемии. У человека без СД гипогликемией считают снижение уровня гликемии менее 2,8 ммоль/л, сопровождающееся определенной клинической симптоматикой, или до уровня 2,2 ммоль/л вне зависимости от наличия симптоматики. К пациенту с СД это определение применимо не всегда, т.к. больные, у которых длительно наблюдается близкий к нормальному уровень гликемии или имеющие вегетативную нейропатию, не ощущают снижения гликемии до уровня 2 ммоль/л. В то же время, длительно декомпенсированные больные чувствуют симптомы гипогликемии при уровне глюкозы крови 4–5 ммоль/л. Американская диабетическая ассоциация определила гипогликемию как «любое снижение уровня глюкозы крови, способное принести вред», с минимальным показателем для глюкозы плазмы крови 3,9 ммоль/л при наличии или отсутствии симптомов активации нейроэндокринной контррегуляции. Согласно данным ВОЗ, нормальные значения глюкозы крови находятся в пределах 3,3–5,5 ммоль/л, при этом стандарт для нижней границы также не установлен. Однако известно, что первый контррегуляторный механизм, а именно – угнетение эндогенной секреции инсулина, активируется при достижении значения уровня плазмы крови 4,0–4,2 ммоль/л. Дальнейшее снижение уровня глюкозы ниже 3,7 ммоль/л ведет к повышению уровня контринсулярных гормонов. В связи с этими механизмами, вероятно, гипогликемию следует определять как снижение уровня глюкозы крови ниже 4,0–4,2 ммоль/л [4].
Основной причиной развития гипогликемии является дисбаланс между уровнем инсулина и поступлением углеводов извне (с пищей) или из эндогенных источников (продукция глюкозы печенью). Пусковыми факторами, провоцирующими дисбаланс между уровнем инсулина и глюкозой крови у пациентов с СД 2–го типа, являются передозировка инсулина, препаратов СМ и глинидов, изменение фармакокинетики инсулина или ПССП (вследствие замедленного клиренса, неправильной техники инъекции, лекарственного взаимодействия препаратов СМ), а также повышение чувствительности к инсулину (длительная физическая нагрузка).
В физиологических условиях при достижении порогового уровня гликемии 3,7 ммоль/л запускается гормональный контррегуляторный ответ на гипогликемию, который состоит из нескольких событий. Первым этапом является подавление секреции инсулина β–клетками поджелудочной железы и стимуляция секреции α–клеток с выделением глюкагона, который в свою очередь стимулирует гликогенолиз и глюконеогенез. Лишь при недостаточном эффекте глюкагона происходит стимуляция высвобождения адреналина мозговым веществом надпочечника и норадреналина нервными окончаниями постганглионарных симпатических нервных волокон. Кортизол и СТГ реагируют только при более длительной гипогликемии при недостаточном эффекте от предыдущих механизмов [1,4] (табл. 2).
Таким образом, система контррегуляторного ответа функционирует и у пациентов, имеющих небольшой стаж СД. С увеличением длительности заболевания развивается нарушение функционирования системы контррегуляции, при этом самым ранним нарушением гормонального ответа является снижение секреции глюкагона, позднее – и адреналина, что повышает риск тяжелых гипогликемий. Причинами нарушения системы контррегуляции часто являются автономная нейропатия и снижение распознавания гипогликемии. Кроме этого, гормональный ответ на гипогликемию нарушается на фоне высокой концентрации инсулина крови.
Немаловажным является тот факт, что сама гипогликемия способна вызывать снижение нейроэндокринного ответа на последующие эпизоды гипогликемии. В исследовании S. Heller и P. Cryer с помощью измерения контррегуляторных ответов было установлено, что два эпизода умеренной гипогликемии приводят к значительному снижению уровней глюкагона, адреналина и кортизола в плазме крови на следующий день после гипогликемии [10]. Параллельно с этим ослабевают нейрогенные симптомы. Таким образом, однократный эпизод продолжительной гипогликемии снижает гормональный ответ на следующую гипогликемию, а каждая новая гипогликемия вносит свой губительный вклад в прогрессирующее снижение контррегуляторного ответа. Это дает основания для формирования мотивации к предупреждению минимальной вероятности развития гипогликемии у пациентов с СД 2–го типа.
Указанные механизмы нарушения контррегуляторного ответа у пациентов с СД 2–го типа осложняют подбор сахароснижающей терапии (ССТ), ведь хорошо известно, что применение инсулина, ПСМ и глинидов сопровождается увеличением риска развития гипогликемий (рис. 2). В то же время доказано, что интенсификация ССТ должна проводиться своевременно, с целью не получить реализацию «эффекта метаболической памяти», что, как известно, значительно ухудшает прогноз пациентов с СД 2–го типа. При этом исходы упомянутых выше базовых исследований свидетельствуют о необходимости поиска терапевтических возможностей, которые помимо достаточного сахароснижающего эффекта сопряжены с низким риском развития гипогликемии.
Физиологичность действия и, как следствие, низкий риск побочных эффектов, в том числе и гипогликемии, обусловливают интерес к препаратам из группы ингибиторов дипептидилпептидазы – 4 (ДПП–4).
В основе их действия лежит реализация физиологических сахароснижающих механизмов гормонов ЖКТ глюкагоноподобного пептида–1 (ГПП–1) и глюкозозависимого инсулинотропного полипептида (ГИП) путем ингибирования фермента дипептидилпептидазы–IV (DPP–IV), который в течение нескольких минут расщепляет ГПП–1 и ГИП, тем самым препятствуя их действию. Больший интерес при СД 2–го типа вызывает ГПП–1, т.к. его секреция у пациентов с СД 2–го типа сохранена, а ГИП – снижена. Инактивация фермента DPP–IV позволяет осуществить эффекты ГПП–1 [4,5]. Воздействие ГПП–1 на β–клетку поджелудочной железы состоит в потенцировании секреции инсулина, которая зависит от уровня гликемии: при достижении уровня сахара крови около 4,5 ммоль/л инсулинстимулирующий эффект не реализуется [5,7,15]. Воздействие на рецепторы к ГПП–1 в α–клетках поджелудочной железы приводит к снижению секреции глюкагона, что, в свою очередь, снижает продукцию глюкозы печенью. При этом важно, что и данный эффект глюкозозависим.
Таким образом, глюкозозависимая стимуляция секреции инсулина и глюкозозависимое подавление секреции глюкагона, осуществляемые ГПП–1, являются механизмами защиты от гипогликемии [2,7]. Инактивация фермента ДПП–IV дает возможность реализовать эффекты ГПП–1, что ведет к восстановлению чувствительности α– и β–клеток и баланса уровней инсулина и глюкагона, предотвращая тем самым развитие гипогликемии.
Одним из наиболее изученных препаратов из группы ингибиторов ДПП–4 является вилдаглиптин, клиническое изучение которого доказало высокую эффективность и достоверную безопасность. Препарат обеспечивает улучшение гликемического контроля при назначении как в монотерапии, так и в комбинации, что сопряжено с низким риском гипогликемии и нейтральным влиянием на массу тела.
Среди всех факторов контррегуляции гипогликемии глюкагон играет наиболее значимую роль, в первую очередь потому, что его секреция является первым физиологическим ответом на патологическое снижение гликемии. Однако даже при небольшой длительности СД 2–го типа уже проявляются дефекты в гормональном ответе на гипогликемии, и выражаются они в замедлении инсулиновой реакции и неадекватном уровне глюкагона. В связи с этим основная возможность снижения риска гипогликемии заключается в восстановлении баланса гормонов, участвующих в контррегуляторном ответе. В исследовании B. Ahrén, A. Schweizer, S. Dejager, посвященном изучению влияния вилдаглиптина на уровень глюкагона при гипер– и гипогликемии в сравнении с плацебо после приема стандартного завтрака у 28 пациентов с СД 2–го типа, не получающих ПССТ и имеющих HbA1c≥7,5% [6], было установлено, что вилдаглиптин увеличивает на 38% (р<0,03) уровень глюкагона при проведении гипогликемического клэмпа и на 41% (р<0,019) снижает уровень глюкагона на фоне гипергликемии после приема стандартного завтрака (рис. 3). Таким образом, вилдаглиптин усиливает чувствительность α–клеток к супрессивному действию при гипергликемии и стимулирующему действию при гипогликемии. Эти эффекты, вероятно, и обусловливают эффективность как в уменьшении выраженности гипергликемии, так и в способности снижать риск гипогликемии.
S. Dejager и соавт. изучали эффективность препарата в ходе плацебо–контролируемого исследования длительностью 24 нед. у 632 пациентов. После рандомизации пациенты основной группы получали вилдаглиптин в дозе 50 мг 2 р./сут. или 50–100 мг однократно. По сравнению с исходными данными отмечено снижение HbA1c в среднем на 0,8% в группах, получающих вилдаглиптин. При этом за 24 нед. исследования зарегистрировано 3 случая гипогликемии легкой степени у пациентов, получавших вилдаглиптин [15].
Исследование E. Ferrannini, V. Fonseca длительностью 52 нед. имело целью выявить эффективность и безопасность вилдаглиптина (50 мг 2 р./сут.) по сравнению с глимепиридом (средняя доза – 4 мг/сут.) у пациентов, имеющих недостаточный контроль (HbA1c 6,5–8,5%) на фоне монотерапии метформином. Через 52 нед. пациенты обеих групп продемонстрировали достоверное снижение HbA1c, при этом равное число пациентов в группах достигли уровня HbA1c 7%. Однако в отношении частоты возникновения гипогликемии были зафиксированы существенные различия. Частота развития гипогликемий в группе, получающей вилдаглиптин, оказалась в 10 раз ниже по сравнению с группой, получающей глимепирид (30 эпизодов против 554, р<0,01). При этом в группе вилдаглиптина не было зафиксировано ни одного тяжелого эпизода гипогликемии, в то время как в группе глимепирида отмечено 10 эпизодов тяжелой гипогликемии (р<0,01) (рис. 4). Изучение секреции глюкагона в этом же исследовании показало, что вилдаглиптин подавляет ее в 3,5 раза, а на фоне приема глимепирида отмечено увеличение уровня глюкагона в 4 раза [7].
V. Fonseca и соавт. изучали эффективность вилдаглиптина (50 мг/сут.) по сравнению с плацебо у пациентов с неудовлетворительным контролем гликемии (HbA1с 7,5–11%) на фоне терапии инсулином НПХ в дозе более 30 ЕД/сут. в течение 24 нед. К концу наблюдения уровень HbA1с в основной группе снизился на 0,5%, в группе контроля – всего на 0,2%. Необходимо отметить, что эпизоды гипогликемии регистрировались существенно реже в основной группе, что, вероятно, обусловлено повышением чувствительности α–клеток поджелудочной железы к глюкозе [15]. Добавление вилдаглиптина к инсулину достоверно уменьшало риск гипогликемий по сравнению с терапией только НПХ. Общее число эпизодов гипогликемии составило 113 и 185 в группе вилдаглиптин + НПХ и группе НПХ соответственно (р<0,05). Более того, не наблюдалось ни одного случая тяжелой гипогликемии в группе терапии вилдаглиптином по сравнению с 6 эпизодами в группе плацебо + инсулин НПХ [14].
Таким образом, применение нового класса препаратов, ингибиторов ДПП–4, позволяет получить адекватный гликемии сахароснижающий эффект за счет глюкозозависимого характера стимуляции β–клетки и способности снижать патологически повышенный уровень глюкагона. При этом восстановление чувствительности α–клеток и глюкозозависимая стимуляция секреции глюкагона обеспечивают защиту от гипогликемии.
Статья опубликована по заказу и при финансовой поддержке ООО «Новартис Фарма» (Россия) в соответствии с внутренней политикой общества и действующим законодательством Российской Федерации. Согласно договоренности с ООО «Новартис Фарма», авторам статьи не следовало иметь никаких относящихся к данной статье договоренностей или финансовых соглашений с любыми третьими лицами, статья подлежала написанию без посторонней помощи со стороны любых третьих лиц




Литература
1. Дедов И.И., Шестакова М.В. Инкретины: новая веха в лечении сахарного диабета 2 типа. – М.: ФГУ ЭНЦ, 2010.
2. Аметов А.С. Физиология метаболизма глюкозы // Сахарный диабет 2 типа: проблемы и решения, 2011. – С. 21–51.
3. Аметов А.С., Карпова Е.В. Инкретиномиметики – новый этап в лечении сахарного диабета 2–го типа // РМЖ. – 2010. – Т. 18, № 23 (387). – С. 1410–1415.
4. Аметов А.С., Иванова Е.В. Гипогликемия // Сахарный диабет 2 типа: проблемы и решения, 2011. – С. 115–143.
5. Workgroup on Hypoglycemia, American Diabetes Association. Defining and reporting hypoglycemia in diabetes: a report from the American Diabetes Association Workgroup on Hypoglycemia // Diabetes Care. 2005. Vol. 28. P. 1245–1249.
6. Ahran B., Schweizer A., Dejager S. et al. Vildagliptinenhancesisletresponsiveness to both hyper– and hypoglycemia in patients with type 2 diabetes // J. Clin. Endocrinol. Metab.2009. Vol. 94(4). P. 1236–1243.
7. Ferrannini E., Fonseca V., Zinman B. et al. Fifty–two–week efficacy and safety of vildagliptin vs. glimepiride in patients with type 2 diabetes mellitus inadequately controlled on metformin monotherapy // Diabetes. Obes. Metab. 2009. Vol. 11(2). P. 157–166.
8. Desouza C.V., Bolli G.B., Fonseca V. Hypoglycemia, diabetes, andcardiovascularevents // Diabetes Care. 2010. Vol. 33. P. 1389–1394.
9. Barnett A.H. Avoiding hypoglycaemia while achieving good glycaemic control in type 2 diabetes through optimal use of oral agent therapy // Curr. Med. Res. Opin. 2010. Vol. 26. P. 1333–1342.
10. Heller S., Chapman J., McCloud J., Ward J. Unreliability of reports of hypoglycaemia bydiabetic patients // BMJ. 1995. Vol. 310. P. 440.
11. Wild D., von Maltzahn R., Brohan E. et al. A critical review of the literature on fear of hypoglycemia in diabetes: implications for diabetes management and patient education // Patient Educ. Couns. 2007. Vol. 68. P. 10–15.
12. Vexiau P., Mavros P., Krishnarajah G. et al. Hypoglycaemia in patients with type 2 diabetes treated with a combination of metformin and sulphonylurea therapy in France // Diabetes Obes. Metab. 2008. Vol. 10 (suppl. 1). P. 16–24.
13. Davis S.N., Mann S., Briscoe V. J. et al. Effects of intensive therapy and antecedent hypoglycemia on counterregulatory responses to hypoglycemia in type 2 diabetes // Diabetes. 2009. Vol. 58. P. 701–709.
14. Fonseca V., Baron M., Shao Q., Dejager S. Sustained efficacy and reduced hypoglycemia during one year of treatment with vildagliptin added to insulin in patients with type 2 diabetes mellitus // New Orleans, Louisiana: Endocrinology Department, Tulane University Health Sciences Center, 70112, USA.
15. Dejager S., Razac S., Foley J.E., Schweizer A. Vildagliptin in drug–naive patients with type 2 diabetes: a 24–week, double–blind, randomized, placebo–controlled, multiple–dose study // Horm. Metab. Res. 2007. Vol. 39. P. 218–223.












