–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–µ–Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ–Њ—Б—В—М –Є —А–∞–Ј–љ–Њ—А–µ—З–Є–≤–Њ—Б—В—М –і–∞–љ–љ—Л—Е –њ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є —В–Є–њ–∞–Љ–Є –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Л—Е –Њ—В–≤–µ—В–Њ–≤, –љ–∞—А—П–і—Г —Б –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М—О —Б–Њ–≤–µ—А—И–µ–љ—Б—В–≤–Њ–≤–∞–љ–Є—П –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–Њ–і—Е–Њ–і–Њ–≤ –Ї —В–µ—А–∞–њ–Є–Є –°–Я–Ъ–ѓ —П–≤–Є–ї–Є—Б—М –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П.
–¶–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П – –Њ—Ж–µ–љ–Ї–∞ –Ї–ї–Є–љ–Є–Ї–Њ––ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Я–Ъ–ѓ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –љ–∞–ї–Є—З–Є—П –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є—П —Г –љ–Є—Е –У–Ш.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –≤–Ї–ї—О—З–µ–љ–Њ 58 –±–Њ–ї—М–љ—Л—Е (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В – 25,0±1,0 –ї–µ—В, –Ш–Ь–Ґ– 26,0±0,7 –Ї–≥/–Љ2) —Б –°–Я–Ъ–ѓ, –Ї–Њ—В–Њ—А—Л–µ –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б—П—Ж–µ–≤ –њ–Њ–ї—Г—З–∞–ї–Є –Љ–µ—В—Д–Њ—А–Љ–Є–љ (–°–Є–Њ—Д–Њ—А–500, «Berlin–Chemie AG» –У–µ—А–Љ–∞–љ–Є—П) –њ–Њ 500 –Љ–≥ 3 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Е–∞—А–∞–Ї—В–µ—А–∞ —Б–µ–Ї—А–µ—Ж–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞ –±—Л–ї–Є —Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ—Л 2 –≥—А—Г–њ–њ—Л: –≤ 1–—О –±—Л–ї–∞ –≤–Ї–ї—О—З–µ–љ–∞ 31 –±–Њ–ї—М–љ–∞—П (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В – 23,9±0,9 –ї–µ—В, –Ш–Ь–Ґ 29,3±0,9 –Ї–≥/–Љ2) —Б –У–Ш, –≤–Њ 2–—О – 27 –±–Њ–ї—М–љ—Л—Е (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В – 26,2±1,2 –ї–µ—В, –Ш–Ь–Ґ 22,7±0,8 –Ї–≥/–Љ2) —Б –љ–Њ—А–Љ–Њ–Є–љ—Б—Г–ї–Є–љ–µ–Љ–Є–µ–є (–Э–Ш).
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є –∞–љ–і—А–Њ–≥–µ–љ–Є–Ј–∞—Ж–Є–Є –±—Л–ї–Є –Њ—В–Љ–µ—З–µ–љ—Л —Г 28 (90,3%) –±–Њ–ї—М–љ—Л—Е 1––є –≥—А—Г–њ–њ—Л –Є —Г 22 (81,5%) 2––є –≥—А—Г–њ–њ—Л; —Б—А–µ–і–љ–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≥–Є—А—Б—Г—В–љ–Њ–≥–Њ —З–Є—Б–ї–∞ –њ–Њ —И–Ї–∞–ї–µ –§–µ—А—А–Є–Љ–∞–љ–∞––У–Њ–ї–ї–≤–µ—П —Б–Њ—Б—В–∞–≤–Є–ї–Њ 15,3±0,7 –Є 12,9±0,8.
–Э–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є —П–Є—З–љ–Є–Ї–Њ–≤ –±—Л–ї–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ–Њ —Г –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–Ї. –£ 12,9% –±–Њ–ї—М–љ—Л—Е 1––є –≥—А—Г–њ–њ—Л –Є —Г 11,1% –±–Њ–ї—М–љ—Л—Е 2––є –≥—А—Г–њ–њ—Л –±—Л–ї–∞ –≤—Л—П–≤–ї–µ–љ–∞ –∞–љ–Њ–≤—Г–ї—П—Ж–Є—П –љ–∞ —Д–Њ–љ–µ —А–µ–≥—Г–ї—П—А–љ–Њ–≥–Њ —А–Є—В–Љ–∞ –Љ–µ–љ—Б—В—А—Г–∞—Ж–Є–Є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ —Г 77,4 –Є 70,4% – –Њ–ї–Є–≥–Њ–Љ–µ–љ–Њ—А–µ—П, —Г 16,1 –Є —Г 11,1% – –∞–Љ–µ–љ–Њ—А–µ—П.
–°—А–µ–і–љ—П—П –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –љ–∞—А—Г—И–µ–љ–Є–є –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–≥–Њ —Ж–Є–Ї–ї–∞ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 8,5±1,2 –ї–µ—В –≤ 1––є –≥—А—Г–њ–њ–µ –Є 7,7±1,3 –ї–µ—В –≤–Њ 2––є –≥—А—Г–њ–њ–µ. –Ш–Ј —З–Є—Б–ї–∞ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е 27 (87,1%) –±–Њ–ї—М–љ—Л—Е –≤ 1––є –≥—А—Г–њ–њ–µ –Є 18 (66,7%) –±–Њ–ї—М–љ—Л—Е –≤–Њ 2––є –≥—А—Г–њ–њ–µ –±—Л–ї–Є –Ј–∞–Є–љ—В–µ—А–µ—Б–Њ–≤–∞–љ—Л –≤ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є.
–Т—Б–µ –њ–∞—Ж–Є–µ–љ—В–Ї–Є, –≤–Ї–ї—О—З–µ–љ–љ—Л–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –≤ —В–µ—З–µ–љ–Є–µ –њ—А–µ–і—Л–і—Г—Й–Є—Е 3 –Љ–µ—Б—П—Ж–µ–≤ –љ–µ –њ–Њ–ї—Г—З–∞–ї–Є –≥–Њ—А–Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—О. –Э–∞—А—Г—И–µ–љ–Є–є —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є –њ–Њ –і–∞–љ–љ—Л–Љ –∞–љ–∞–Љ–љ–µ–Ј–∞, –£–Ч–Ш –Є –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ –љ–Є —Г –Њ–і–љ–Њ–є –±–Њ–ї—М–љ–Њ–є.
–Ъ–ї–Є–љ–Є–Ї–Њ––ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –Є—Б—Е–Њ–і–љ–Њ, —З–µ—А–µ–Ј 3 –Є 6 –Љ–µ—Б—П—Ж–µ–≤ –Њ—В –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є (–Є—Б–Ї–ї—О—З–µ–љ–Є–µ —Б–Њ—Б—В–∞–≤–Є–ї–Є –±–Њ–ї—М–љ—Л–µ, —Г –Ї–Њ—В–Њ—А—Л—Е –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –љ–∞—Б—В—Г–њ–Є–ї–∞ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М). –У–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –љ–∞ 2–3 –і–µ–љ—М —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ–≥–Њ –Є–ї–Є –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–≥–Њ —Ж–Є–Ї–ї–∞. –Ъ–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –Ы–У, –§–°–У, —Б–Њ–Љ–∞—В–Њ—В—А–Њ–њ–љ–Њ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞ (–°–Ґ–У), —В–µ—Б—В–Њ—Б—В–µ—А–Њ–љ–∞ (–Ґ), —Н—Б—В—А–∞–і–Є–Њ–ї–∞ (–≠2), —В–µ—Б—В–Њ—Б—В–µ—А–Њ–љ–—Н—Б—В—А–∞–і–Є–Њ–ї —Б–≤—П–Ј—Л–≤–∞—О—Й–µ–≥–Њ –≥–ї–Њ–±—Г–ї–Є–љ–∞ (–Ґ–≠–°–У), 17––Њ–Ї—Б–Є–њ—А–Њ–≥–µ—Б—В–µ—А–Њ–љ–∞ (17––Ю–Э), –і–µ–≥–Є–і—А–Њ—Н–њ–Є–∞–љ–і—А–Њ—Б—В–µ—А–Њ–љ–∞ —Б—Г–ї—М—Д–∞—В–∞ (–Ф–≠–Р–°) –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Њ–њ—А–µ–і–µ–ї—П–ї–Є —А–∞–і–Є–Њ–Є–Љ–Љ—Г–љ–љ—Л–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —В–µ—Б—В–—Б–Є—Б—В–µ–Љ «Immunotech» (–І–µ—Е–Є—П) –Є–ї–Є –Ш–С–Ю–• (–С–µ–ї–∞—А—Г—Б—М), –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –∞–љ–і—А–Њ—Б—В–µ–љ–і–Є–Њ–љ–∞ (–Р) – –Є–Љ–Љ—Г–љ–Њ—Д–µ—А–Љ–µ–љ—В–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Б—В–∞–љ–і–∞—А—В–љ—Л—Е —В–µ—Б—В–—Б–Є—Б—В–µ–Љ «Diagnostics Biohem Canada Inc.» (–Ъ–∞–љ–∞–і–∞).
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Ш–†–Ш –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –Љ–µ—В–Њ–і–Њ–Љ IRMA, c –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —В–µ—Б—В–—Б–Є—Б—В–µ–Љ –Ш–С–Ю–• (–С–µ–ї–∞—А—Г—Б—М), –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –њ—А–Є–ї–∞–≥–∞–µ–Љ—Л–Љ–Є –Ї –љ–Є–Љ –Є–љ—Б—В—А—Г–Ї—Ж–Є—П–Љ. –Ю—Ж–µ–љ–Ї–∞ —Е–∞—А–∞–Ї—В–µ—А–∞ —Б–µ–Ї—А–µ—Ж–Є–Є –Ш–†–Ш –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–∞—Б—М –љ–∞ —Д–Њ–љ–µ 2–—З–∞—Б–Њ–≤–Њ–≥–Њ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –У–Ґ–Ґ. –Ъ–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Ш–†–Ш –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М –љ–∞—В–Њ—Й–∞–Ї –Є –Ї–∞–ґ–і—Л–µ 30 –Љ–Є–љ—Г—В –≤ —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і—Г—О—Й–Є—Е 2 —З–∞—Б–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Ъ–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Є—Е –Є –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Л—Е –Њ—В–≤–µ—В–Њ–≤ –љ–∞ –≥–ї—О–Ї–Њ–Ј–љ—Г—О –љ–∞–≥—А—Г–Ј–Ї—Г –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —А–∞—Б—З–µ—В–љ—Л–Љ –њ—Г—В–µ–Љ –њ–Њ –≤–µ–ї–Є—З–Є–љ–∞–Љ –Љ–Њ–ї—П—А–љ—Л—Е –њ–ї–Њ—Й–∞–і–µ–є (S) –њ–Њ–і —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–Љ–Є —Б–µ–Ї—А–µ—В–Њ—А–љ—Л–Љ–Є –Ї—А–Є–≤—Л–Љ–Є, —А–∞—Б—Б—З–Є—В–∞–љ–љ—Л–Љ–Є –њ–Њ —В—А–∞–њ–µ—Ж–µ–≤–Є–і–љ–Њ–Љ—Г –њ—А–∞–≤–Є–ї—Г. –£—А–Њ–≤–љ–Є –Є—Б—Е–Њ–і–љ–Њ–≥–Њ –Ш–†–Ш, –њ—А–µ–≤—Л—И–∞—О—Й–Є–µ 25 –Љ–Ї–Х–Ф/–Љ–ї, —А–∞—Б—Ж–µ–љ–Є–≤–∞–ї–Є—Б—М, –Ї–∞–Ї –њ—А–Њ—П–≤–ї–µ–љ–Є–µ —В–Њ—Й–∞–Ї–Њ–≤–Њ–є –≥–Є–њ–µ—А–Є–љ—Б—Г–ї–Є–љ–µ–Љ–Є–Є, –∞ –Ј–љ–∞—З–µ–љ–Є—П –≤–µ–ї–Є—З–Є–љ—Л –Љ–Њ–ї—П—А–љ–Њ–є –њ–ї–Њ—Й–∞–і–Є –њ–Њ–і –Ї—А–Є–≤–Њ–є –Ш–†–Ш, –њ—А–µ–≤—Л—И–∞—О—Й–Є–µ 100 –Љ–Ї–Х–Ф/–Љ–ї —Е 120 –Љ–Є–љ, –Ї–∞–Ї –≥–Є–њ–µ—А—Б–µ–Ї—А–µ—В–Њ—А–љ—Л–є —В–Є–њ –Њ—В–≤–µ—В–∞ –љ–∞ –≤–≤–µ–і–µ–љ–Є–µ –µ—Б—В–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б—В–Є–Љ—Г–ї—П—В–Њ—А–∞. –†–∞—Б—З–µ—В –Є–љ–і–µ–Ї—Б–Њ–≤ –Ш–† –њ—А–Њ–Є–Ј–≤–Њ–і–Є–ї—Б—П –њ–Њ —Д–Њ—А–Љ—Г–ї–∞–Љ: HOMA=–Є–љ—Б—Г–ї–Є–љ 00(–Љ–Ї–Х–Ф/–Љ–ї) —Е –≥–ї—О–Ї–Њ–Ј–∞ 00 (–Љ–Љ–Њ–ї—М/–ї)/22,5, –≥–і–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М > 3 —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –Ш–†; CARO=–≥–ї—О–Ї–Њ–Ј–∞ 00(–Љ–≥/–і–ї)/ –Є–љ—Б—Г–ї–Є–љ 00 (–Љ–Ї–Х–Ф/–Љ–ї), –≥–і–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М 4,5 —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –Ш–†.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
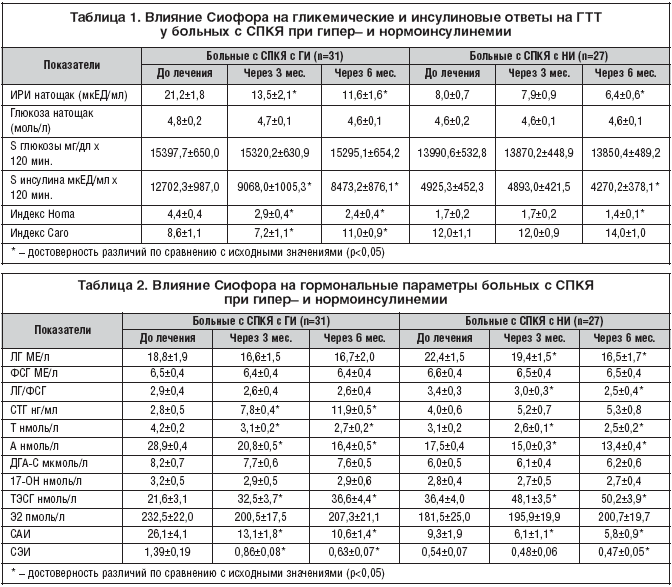
–Ф–∞–љ–љ—Л–µ, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–µ –≤ —В–∞–±–ї–Є—Ж–µ 1, —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ —Г–Љ–µ–љ—М—И–µ–љ–Є–Є –Ш–† –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б –У–Ш –Є –°–Я–Ъ–ѓ.
–Ґ–∞–Ї, –Є–љ–і–µ–Ї—Б Homa –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Г–Љ–µ–љ—М—И–Є–ї—Б—П –њ–Њ—Б–ї–µ 3–—Е (p<0,05) –Є –Њ—Б–Њ–±–µ–љ–љ–Њ –њ–Њ—Б–ї–µ 6 –Љ–µ—Б—П—Ж–µ–≤ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –°–Є–Њ—Д–Њ—А–∞. –Ъ –Ї–Њ–љ—Ж—Г –Ї—Г—А—Б–∞ —В–µ—А–∞–њ–Є–Є –Є–љ–і–µ–Ї—Б Homa –≤ —Ж–µ–ї–Њ–Љ –њ–Њ–љ–Є–Ј–Є–ї—Б—П –≤ 1,8 —А–∞–Ј–∞, –Є–љ–і–µ–Ї—Б Caro – —Г–≤–µ–ї–Є—З–Є–ї—Б—П –≤ 2,1 —А–∞–Ј–∞ (p<0,05). –£ –±–Њ–ї—М–љ—Л—Е —Б –Э–Ш —В–∞–Ї–ґ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г–ї—Г—З—И–µ–љ–Є–µ —В–Ї–∞–љ–µ–≤–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –Є–љ—Б—Г–ї–Є–љ—Г, —Е–Њ—В—П –Є –љ–µ —Б—В–Њ–ї—М –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ: —Б—А–µ–і–љ–Є–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –Є–љ–і–µ–Ї—Б–∞ Homa —Г–Љ–µ–љ—М—И–Є–ї—Б—П –ї–Є—И—М –љ–∞ 17,6% (p<0,05), –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Є–љ–і–µ–Ї—Б–∞ Caro –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ (p>0,05). –Э–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –Њ—В–Љ–µ—З–µ–љ–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ї–∞–Ї –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Ш–†–Ш, —В–∞–Ї –Є –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Л—Е –Њ—В–≤–µ—В–Њ–≤ –љ–∞ –У–Ґ–Ґ. –Ю–і–љ–∞–Ї–Њ –µ—Б–ї–Є –≤ 1––є –≥—А—Г–њ–њ–µ —Н—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Њ—Б—В–∞–≤–Є–ї–Њ 45,3 –Є 45,6%, —В–Њ –≤–Њ 2––є –≥—А—Г–њ–њ–µ – 20,0 –Є 13,3% (p<0,05).
–Р–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –ї–µ—З–µ–љ–Є—П —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –њ–Њ —Б—А–µ–і–љ–Є–Љ —Г—А–Њ–≤–љ—П–Љ —В–Њ—Й–∞–Ї–Њ–≤–Њ–є –≥–ї—О–Ї–Њ–Ј—Л –Є –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Є–Љ –Њ—В–≤–µ—В–∞–Љ –љ–∞ –љ–∞–≥—А—Г–Ј–Њ—З–љ—Л–є —В–µ—Б—В (—В–∞–±–ї. 1) –Ї–∞–Ї –і–Њ –ї–µ—З–µ–љ–Є—П, —В–∞–Ї –Є –њ–Њ—Б–ї–µ 6 –Љ–µ—Б—П—Ж–µ–≤, –Ј–∞ –Ї–Њ—В–Њ—А—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≥–ї—О–Ї–Њ–Ј—Л –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–∞—Б—М.
–Ь–Њ–љ–Є—В–Њ—А–Є–љ–≥ –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ —Б—А–µ–і–љ–Є–µ —Г—А–Њ–≤–љ–Є –Ы–У –Є –§–°–У —Г –±–Њ–ї—М–љ—Л—Е —Б –У–Ш –љ–µ –њ—А–µ—В–µ—А–њ–µ–ї–Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є, —В–Њ–≥–і–∞ –Ї–∞–Ї —Г –±–Њ–ї—М–љ—Л—Е —Б –Э–Ш –њ–Њ—Б–ї–µ 6 –Љ–µ—Б—П—Ж–µ–≤ –њ—А–Є–µ–Љ–∞ –°–Є–Њ—Д–Њ—А–∞ —Б—А–µ–і–љ–Є–є —Г—А–Њ–≤–µ–љ—М –Ы–У –Є –Є–љ–і–µ–Ї—Б –Ы–У/–§–°–У —Г–Љ–µ–љ—М—И–Є–ї–Є—Б—М –≤ 1,4 —А–∞–Ј–∞ (p<0,05) (—В–∞–±–ї. 2). –Ю–±—А–∞—В–љ–∞—П —Б–Є—В—Г–∞—Ж–Є—П –љ–∞–±–ї—О–і–∞–ї–∞—Б—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –°–Ґ–У: —Г –±–Њ–ї—М–љ—Л—Е —Б –У–Ш –Њ–љ –±—Л–ї –Є—Б—Е–Њ–і–љ–Њ –љ–Є–Ј–Ї–Є–Љ –Є —Г–≤–µ–ї–Є—З–Є–ї—Б—П –≤ 4,3 —А–∞–Ј–∞ –њ–Њ—Б–ї–µ 6 –Љ–µ—Б—П—Ж–µ–≤ —В–µ—А–∞–њ–Є–Є, —Г –±–Њ–ї—М–љ—Л—Е —Б –Э–Ш –Є—Б—Е–Њ–і–љ—Л–µ —Г—А–Њ–≤–љ–Є –°–Ґ–У –±—Л–ї–Є –≤ –њ—А–µ–і–µ–ї–∞—Е –љ–Њ—А–Љ–∞—В–Є–≤–љ—Л—Е –Ј–љ–∞—З–µ–љ–Є–є –Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–Є—Б—М –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П. –Ю—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ –Ї–Њ—А—А–µ–ї—П—Ж–Є–Є –°–Ґ–У —Б –Ш–†–Ш –Є —Б S –Ш–†–Ш (r=–0,293 –Є r=–0,339, p<0,05) –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В –љ–∞–ї–Є—З–Є–µ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є —Н—В–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є.
–Ъ–∞–Ї –≤–Є–і–љ–Њ –Є–Ј –і–∞–љ–љ—Л—Е, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –≤ —В–∞–±–ї–Є—Ж–µ 2, –њ—А–Є –њ–µ—А–≤–Є—З–љ–Њ–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б—А–µ–і–љ–Є–µ —Г—А–Њ–≤–љ–Є –Ґ –Є –Р –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–Љ–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –У–Ш, —З–µ–Љ —Б –Э–Ш. –Э–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –°–Є–Њ—Д–Њ—А–∞ —Г—А–Њ–≤–љ–Є –∞–љ–і—А–Њ–≥–µ–љ–Њ–≤ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–Ј–Є–ї–Є—Б—М. –£ –±–Њ–ї—М–љ—Л—Е —Б –У–Ш —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Ґ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є —Г–Љ–µ–љ—М—И–Є–ї–Њ—Б—М –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 31,0%, –Р – –љ–∞ 41,8% (p<0,05), —Г –±–Њ–ї—М–љ—Л—Е —Б –Э–Ш – –љ–∞ 18,8 –Є –љ–∞ 26,7% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ (p<0,05). –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г, —Г 16,1% –±–Њ–ї—М–љ—Л—Е –≤ 1––є –≥—А—Г–њ–њ–µ –Є —Г 11,1% –≤–Њ 2––є –≥—А—Г–њ–њ–µ —Г—А–Њ–≤–љ–Є –∞–љ–і—А–Њ–≥–µ–љ–Њ–≤ –љ–µ –і–Њ—Б—В–Є–≥–ї–Є –љ–Њ—А–Љ–∞—В–Є–≤–љ—Л—Е –Ј–љ–∞—З–µ–љ–Є–є. –Э–∞—А—П–і—Г —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Б–µ–Ї—А–µ—Ж–Є–Є –∞–љ–і—А–Њ–≥–µ–љ–Њ–≤ 6––Љ–µ—Б—П—З–љ—Л–є –Ї—Г—А—Б —В–µ—А–∞–њ–Є–Є –°–Є–Њ—Д–Њ—А–Њ–Љ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї –њ–Њ–≤—Л—И–µ–љ–Є—О —Б—А–µ–і–љ–µ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –Ґ–≠–°–У, –Ї–Њ—В–Њ—А—Л–є —Г –±–Њ–ї—М–љ—Л—Е 1––є –≥—А—Г–њ–њ—Л —Г–≤–µ–ї–Є—З–Є–ї—Б—П –≤ 1,7 —А–∞–Ј–∞, —Г –±–Њ–ї—М–љ—Л—Е 2––є –≥—А—Г–њ–њ—Л – –≤ 1,4 —А–∞–Ј–∞ (p<0,05). –≠—В–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ–Њ –њ—А–Є–≤–µ–ї–Є –Ї —Б–љ–Є–ґ–µ–љ–Є—О –°–Р–Ш (–≤ 2,5 —А–∞–Ј–∞ –≤ 1––є –≥—А—Г–њ–њ–µ –Є –≤ 1,6 —А–∞–Ј–∞ – –≤–Њ 2––є) –Є –°–≠–Ш (—Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –≤ 2,2 –Є 1,2 —А–∞–Ј–∞) (p>0,05).
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є –°–Є–Њ—Д–Њ—А–Њ–Љ, –Њ—Ж–µ–љ–Є–≤–∞–µ–Љ–∞—П –њ–Њ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—О —А–Є—В–Љ–∞ –Љ–µ–љ—Б—В—А—Г–∞—Ж–Є–є, –±—Л–ї–∞ –і–Њ—Б—В–Є–≥–љ—Г—В–∞ –њ—А–Є–Љ–µ—А–љ–Њ —Г –Ї–∞–ґ–і–Њ–є 2––є –Є–Ј –њ—А–Њ–ї–µ—З–µ–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е, –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –љ–∞–ї–Є—З–Є—П –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є—П —Г –љ–Є—Е –У–Ш (—А–Є—Б. 1). –Я—А–Є–Љ–µ—А–љ–Њ —Б –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є —З–∞—Б—В–Њ—В–Њ–є –Њ—В–Љ–µ—З–µ–љ—Л –Њ–≤—Г–ї—П—В–Њ—А–љ—Л–µ —Ж–Є–Ї–ї—Л (45,2% – –≤ 1––є –≥—А—Г–њ–њ–µ –Є 37,0% – –≤–Њ 2––є –≥—А—Г–њ–њ–µ) –Є –љ–∞—Б—В—Г–њ–ї–µ–љ–Є–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є (—Г 33,3 –Є 27,8%).
–Э–∞ —Д–Њ–љ–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Г 21 (36,2%) –±–Њ–ї—М–љ–Њ–є –Њ—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Њ—В 1,5 –Ї–≥ –і–Њ 6 –Ї–≥ (–≤ —Б—А–µ–і–љ–µ–Љ 2,6±0,5 –Ї–≥). –Ч–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ —Г–ї—Г—З—И–µ–љ–Є—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –У–Р –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М, —Б—А–µ–і–љ–Є–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –У–І –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ–Є–ї—Б—П –Є —Б–Њ—Б—В–∞–≤–Є–ї –≤ 1––є –≥—А—Г–њ–њ–µ 14,8±0,7, –≤–Њ 2––є – 12,7±0,7. –Э–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –°–Є–Њ—Д–Њ—А–∞ (–≤ –њ–µ—А–≤—Г—О –љ–µ–і–µ–ї—О) –ґ–∞–ї–Њ–±—Л –љ–∞ —В–Њ—И–љ–Њ—В—Г, –Љ–µ—В–µ–Њ—А–Є–Ј–Љ –Є –і–Є–∞—А–µ—О –њ—А–µ–і—К—П–≤–ї—П–ї–Є 8 (13,8%) –±–Њ–ї—М–љ—Л—Е, —З—В–Њ, –Њ–і–љ–∞–Ї–Њ, –љ–µ —П–≤–Є–ї–Њ—Б—М –њ—А–Є—З–Є–љ–Њ–є –Њ—В–Ї–∞–Ј–∞ –Њ—В –ї–µ—З–µ–љ–Є—П.
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ
–°–Я–Ъ–ѓ –≤—Б—В—А–µ—З–∞–µ—В—Б—П —Г 5–10% [2,8], –∞ –њ–Њ –љ–µ–Ї–Њ—В–Њ—А—Л–Љ –і–∞–љ–љ—Л–Љ, —Г 13% [17] –ґ–µ–љ—Й–Є–љ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –≤—Л—Б–Њ–Ї—Г—О —З–∞—Б—В–Њ—В—Г —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є –Є –≤—Б–µ—Б—В–Њ—А–Њ–љ–љ–µ–µ –Є–Ј—Г—З–µ–љ–Є–µ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–љ–Њ–≤ –°–Я–Ъ–ѓ, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є—Е —Б–Њ–≤–µ—А—И–µ–љ—Б—В–≤–Њ–≤–∞–љ–Є—О —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є –і–∞–љ–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –і–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –њ—А–Њ–±–ї–µ–Љ–∞ –≤—Л–±–Њ—А–∞ –Љ–µ—В–Њ–і–∞ –ї–µ—З–µ–љ–Є—П –Њ—Б—В–∞–µ—В—Б—П —З—А–µ–Ј–≤—Л—З–∞–є–љ–Њ –∞–Ї—В—Г–∞–ї—М–љ–Њ–є. –Ґ—А–∞–і–Є—Ж–Є–Њ–љ–љ–∞—П —В–µ—А–∞–њ–Є—П –±–Њ–ї—М–љ—Л—Е —Б –°–Я–Ъ–ѓ, –≤–Ї–ї—О—З–∞—О—Й–∞—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ъ–Ю–Ъ, –њ—А–Њ–≥–µ—Б—В–∞–≥–µ–љ–Њ–≤ –Є–ї–Є –Є–љ–і—Г–Ї—В–Њ—А–Њ–≤ –Њ–≤—Г–ї—П—Ж–Є–Є, –љ–µ –≤—Б–µ–≥–і–∞ —Б–њ–Њ—Б–Њ–±–љ–∞ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В—М —А–Є—В–Љ –Љ–µ–љ—Б—В—А—Г–∞—Ж–Є–є –Є —Д–µ—А—В–Є–ї—М–љ–Њ—Б—В—М. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –≤ —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Г—Б—Г–≥—Г–±–ї–µ–љ–Є–µ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є, –Ї–Њ—А—А–µ–Ї—Ж–Є—П –Ї–Њ—В–Њ—А—Л—Е –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ –Ї–∞–Ї —Б —Ж–µ–ї—М—О –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Њ—В–і–∞–ї–µ–љ–љ—Л—Е –њ–Њ—Б–ї–µ–і—Б—В–≤–Є–є, —В–∞–Ї –Є –і–ї—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П —А–∞–љ–љ–Є—Е –њ–Њ—В–µ—А—М –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–µ–є, –≥–µ—Б—В–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞, –≥–µ—Б—В–Њ–Ј–Њ–≤. –Ю—В–Ї—А—Л—В–Є–µ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є –Ш–† –Є –У–Ш —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ –°–Я–Ъ–ѓ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ —Б –љ–Њ–≤—Л—Е –њ–Њ–Ј–Є—Ж–Є–є, –њ—Г—В–µ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–љ—Б—Г–ї–Є–љ–Њ—Б–µ–љ—Б–Є—В–∞–є–Ј–µ—А–Њ–≤, –њ–Њ–і–Њ–є—В–Є –Ї —В–µ—А–∞–њ–Є–Є –і–∞–љ–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ф–µ—Б—П—В–Є–ї–µ—В–љ–Є–є –Њ–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е –°–Я–Ъ–ѓ –і–Њ–Ї–∞–Ј–∞–ї –µ–≥–Њ –≤—Л—Б–Њ–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Г –±–Њ–ї—М–љ—Л—Е —Б –љ–∞—А—Г—И–µ–љ–Є–µ–Љ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є —Б–µ–Ї—А–µ—Ж–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞. –†–µ–Ј—Г–ї—М—В–∞—В—Л –љ–∞—Г—З–љ—Л—Е —А–∞–±–Њ—В –Њ –µ–≥–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Г –±–Њ–ї—М–љ—Л—Е –±–µ–Ј –У–Ш –љ–Њ—Б—П—В –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤—Л–є —Е–∞—А–∞–Ї—В–µ—А, —З—В–Њ –Є–љ–Є—Ж–Є–Є—А–Њ–≤–∞–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–є –Њ—Ж–µ–љ–Ї–µ –і–µ–є—Б—В–≤–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Я–Ъ–ѓ –њ—А–Є –≥–Є–њ–µ—А– –Є –љ–Њ—А–Љ–Њ–Є–љ—Б—Г–ї–Є–љ–µ–Љ–Є–Є.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–є —А–∞–±–Њ—В—Л —Б–Њ–≥–ї–∞—Б—Г—О—В—Б—П —Б –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –≤ –Ї–Њ—В–Њ—А—Л—Е –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ —Г–ї—Г—З—И–µ–љ–Є–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –Є–љ—Б—Г–ї–Є–љ—Г —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Я–Ъ–ѓ –Є –У–Ш –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ [9,26,30]. –°–Њ–≥–ї–∞—Б–љ–Њ –њ–Њ–ї—Г—З–µ–љ–љ—Л–Љ –і–∞–љ–љ—Л–Љ 6––Љ–µ—Б—П—З–љ—Л–є –Ї—Г—А—Б —В–µ—А–∞–њ–Є–Є –°–Є–Њ—Д–Њ—А–Њ–Љ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –Є–љ–і–µ–Ї—Б–∞ Homa –≤ 1,8 —А–∞–Ј –Є —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Є–љ–і–µ–Ї—Б–∞ Caro –≤ 2,1 —А–∞–Ј–∞, —З—В–Њ –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ–Њ –Њ—В—А–∞–Ј–Є–ї–Њ—Б—М –≤ —Б–љ–Є–ґ–µ–љ–Є–Є –Ї–∞–Ї –±–∞–Ј–∞–ї—М–љ–Њ–є —Б–µ–Ї—А–µ—Ж–Є–Є –Ш–†–Ш (–љ–∞ 45,3%), —В–∞–Ї —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Њ–є (–љ–∞ 45,6%). –£ –±–Њ–ї—М–љ—Л—Е —Б –Э–Ш –ї–µ—З–µ–љ–Є–µ –°–Є–Њ—Д–Њ—А–Њ–Љ —В–∞–Ї–ґ–µ –њ—А–Є–≤–µ–ї–Њ –Ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ—Г, —Е–Њ—В—П –Є –≤ 2–3 —А–∞–Ј–∞ –Љ–µ–љ–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ—Г, —Г–Љ–µ–љ—М—И–µ–љ–Є—О –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ –Є —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Ш–†–Ш (–љ–∞ 20,0% –Є –љ–∞ 13,3%). –°—Е–Њ–і–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–µ–і—Б—В–∞–≤–Є–ї–Є –≤ —Б–≤–Њ–µ–є —А–∞–±–Њ—В–µ Baillargeon –Є —Б–Њ–∞–≤—В. [4]. –Т–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –њ—Г—В–Є —А–µ–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–Њ–і–Њ–±–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –°–Є–Њ—Д–Њ—А–∞ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В—Б—П —Б –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –њ–Њ–Ј–Є—Ж–Є–є: –≤–Њ––њ–µ—А–≤—Л—Е, –њ—Г—В–µ–Љ –њ–Њ–і–∞–≤–ї–µ–љ–Є—П –≥–ї—О–Ї–Њ–љ–µ–Њ–≥–µ–љ–µ–Ј–∞ –≤ –њ–µ—З–µ–љ–Є, —Г–ї—Г—З—И–µ–љ–Є—П –µ–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –Є–љ—Б—Г–ї–Є–љ—Г, –≤—Б–ї–µ–і—Б—В–≤–Є–µ —З–µ–≥–Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–µ–Ї—А–µ—Ж–Є–Є –Ш–†–Ш –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –Є—Б—Е–Њ–і–љ–Њ–є —В–Ї–∞–љ–µ–≤–Њ–є –Ш–†; –≤–Њ––≤—В–Њ—А—Л—Е, –њ—Г—В–µ–Љ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М —В–Ї–∞–љ–µ–є –Ї –Є–љ—Б—Г–ї–Є–љ—Г [18].
–Э–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –°–Є–Њ—Д–Њ—А–Њ–Љ —Б—А–µ–і–љ–Є–µ —Г—А–Њ–≤–љ–Є —В–Њ—Й–∞–Ї–Њ–≤–Њ–є –≥–ї—О–Ї–Њ–Ј—Л –Є –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Є—Е –Њ—В–≤–µ—В–Њ–≤ –љ–∞ –≥–ї—О–Ї–Њ–Ј–љ—Г—О –љ–∞–≥—А—Г–Ј–Ї—Г –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–Є—Б—М –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е. –Я—А–Є —Н—В–Њ–Љ –љ–µ –±—Л–ї–Њ –љ–Є –Њ–і–љ–Њ–≥–Њ —Б–ї—Г—З–∞—П —А–∞–Ј–≤–Є—В–Є—П –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–є —А–µ–∞–Ї—Ж–Є–Є. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –Є–Љ–µ—О—В—Б—П –і–∞–љ–љ—Л–µ –Њ —В–Њ–Љ, —З—В–Њ –°–Є–Њ—Д–Њ—А –љ–µ —В–Њ–ї—М–Ї–Њ –њ–Њ–≤—Л—И–∞–µ—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–Ї–∞–љ–µ–є –Ї –Є–љ—Б—Г–ї–Є–љ—Г, –љ–Њ –Є, –і–µ–є—Б—В–≤—Г—П –љ–∞ b––Ї–ї–µ—В–Ї–Є –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л, –Є—Б–њ—А–∞–≤–ї—П–µ—В –і–µ—Д–µ–Ї—В—Л –µ–≥–Њ —Б–µ–Ї—А–µ—Ж–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–Ґ–У [1].
–°–Њ–≥–ї–∞—Б–љ–Њ –њ–Њ–ї—Г—З–µ–љ–љ—Л–Љ –і–∞–љ–љ—Л–Љ, 6––Љ–µ—Б—П—З–љ—Л–є –Ї—Г—А—Б —В–µ—А–∞–њ–Є–Є –°–Є–Њ—Д–Њ—А–Њ–Љ –Њ–Ї–∞–Ј—Л–≤–∞–ї –љ–µ–Њ–і–љ–Њ–Ј–љ–∞—З–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Л–µ –њ–∞—А–∞–Љ–µ—В—А—Л —Г –±–Њ–ї—М–љ—Л—Е —Б –≥–Є–њ–µ—А– –Є –љ–Њ—А–Љ–Њ–Є–љ—Б—Г–ї–Є–љ–µ–Љ–Є–µ–є, —З—В–Њ –≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–є —Б—В–µ–њ–µ–љ–Є —Б–≤—П–Ј–∞–љ–Њ —Б —А–∞–Ј–ї–Є—З–Є—П–Љ–Є –Є—Б—Е–Њ–і–љ–Њ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Д–Њ–љ–∞. –Ґ–∞–Ї, –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е —Б –Э–Ш –Є—Б—Е–Њ–і–љ—Л–µ —Г—А–Њ–≤–љ–Є –Ы–У –±—Л–ї–Є –≤—Л—И–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ —Б –У–Ш – —Н—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В –і–∞–љ–љ—Л–µ –Њ —В–Њ–Љ, —З—В–Њ –У–Ш —З–∞—Б—В–Њ —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –Ы–У —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Я–Ъ–ѓ [5]. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Ш–†–Ш —Г –±–Њ–ї—М–љ—Л—Е —Б –У–Ш, —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Г—А–Њ–≤–љ—П –Ы–У –њ–Њ—Б–ї–µ 6 –Љ–µ—Б—П—Ж–µ–≤ –њ—А–Є–µ–Љ–∞ –°–Є–Њ—Д–Њ—А–∞ –≤ —Н—В–Њ–є –≥—А—Г–њ–њ–µ –љ–µ –Њ—В–Љ–µ—З–µ–љ–Њ, —В–Њ–≥–і–∞ –Ї–∞–Ї —Г –±–Њ–ї—М–љ—Л—Е —Б –Э–Ш —Н—В–Њ—В –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–Ј–Є–ї—Б—П –Є —Г–ґ–µ –љ–µ –Њ—В–ї–Є—З–∞–ї—Б—П –Њ—В —В–∞–Ї–Њ–≤–Њ–≥–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б –У–Ш. –Я—А–Є–≤–µ–і–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –њ–Њ–Ј–≤–Њ–ї—П—О—В –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Ы–У –љ–µ –Ј–∞–≤–Є—Б–Є—В –Њ—В —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Б–µ–Ї—А–µ—Ж–Є–Є –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –Є–љ—Б—Г–ї–Є–љ—Г –Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –љ–∞–ї–Є—З–Є–Є –Є–љ–Њ–≥–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞ —А–µ–∞–ї–Є–Ј–∞—Ж–Є–Є –і–∞–љ–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П. –°—Е–Њ–і–љ—Л–µ –і–∞–љ–љ—Л–µ –Њ–±–љ–∞—А—Г–ґ–Є–ї –≤ —Б–≤–Њ–µ–є —А–∞–±–Њ—В–µ Ulloa–Aguirre [27], —В–Њ–≥–і–∞ –Ї–∞–Ї –≤ –і—А—Г–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –і–∞–љ–љ–∞—П –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ–Њ—Б—В—М –љ–µ –±—Л–ї–∞ –≤—Л—П–≤–ї–µ–љ–∞ [12,13].
–Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –≤ —А–∞–±–Њ—В–µ –і–∞–љ–љ—Л–µ —Г–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞ —В–µ—Б–љ—Г—О –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Ш–†–Ш –Є –°–Ґ–У, –Ї–Њ—В–Њ—А–∞—П –њ—А–Њ—П–≤–ї—П–ї–∞—Б—М –Є—Б—Е–Њ–і–љ–Њ –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –°–Ґ–У —Г –±–Њ–ї—М–љ—Л—Е —Б –У–Ш, –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ –°–Ґ–У –≤ 4,3 —А–∞–Ј–∞ –њ–Њ—Б–ї–µ –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –У–Ш, –∞ —В–∞–Ї–ґ–µ –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–Љ–Є –Ї–Њ—А—А–µ–ї—П—Ж–Є—П–Љ–Є –°–Ґ–У —Б –Ш–†–Ш –Є —Б S –Ш–†–Ш (r=–0,293 –Є r=–0,339, p<0,05). –£ –±–Њ–ї—М–љ—Л—Е —Б –Э–Ш –Є—Б—Е–Њ–і–љ—Л–µ —Г—А–Њ–≤–љ–Є –°–Ґ–У –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–Љ–Є –Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–Є—Б—М –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є.
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –≤ —А–∞–Ј–≤–Є—В–Є–Є —П–Є—З–љ–Є–Ї–Њ–≤–Њ–є –У–Р –њ—А–Є –°–Я–Ъ–ѓ –њ—А–Є–Њ—А–Є—В–µ—В–љ–∞—П —А–Њ–ї—М –Њ—В–≤–Њ–і–Є—В—Б—П –У–Ш [9,26]. –Ф–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ, —Б–Њ–≥–ї–∞—Б–љ–Њ –њ–Њ–ї—Г—З–µ–љ–љ—Л–Љ –і–∞–љ–љ—Л–Љ —Г –±–Њ–ї—М–љ—Л—Е —Б –У–Ш –Є—Б—Е–Њ–і–љ—Л–µ —Г—А–Њ–≤–љ–Є –∞–љ–і—А–Њ–≥–µ–љ–Њ–≤ (–Ґ –Є –Р) –±—Л–ї–Є –≤—Л—И–µ, —З–µ–Љ —Г –±–Њ–ї—М–љ—Л—Е —Б –Э–Ш, –Є –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Б–љ–Є–ґ–∞–ї–Є—Б—М –њ–Њ—Б–ї–µ —В–µ—А–∞–њ–Є–Є –°–Є–Њ—Д–Њ—А–Њ–Љ. –Ґ–∞–Ї, —Б—А–µ–і–љ–Є–є —Г—А–Њ–≤–µ–љ—М –Ґ —Г–Љ–µ–љ—М—И–Є–ї—Б—П –љ–∞ 31,0%, –Р – –љ–∞ 41,8%, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Г –±–Њ–ї—М–љ—Л—Е —Б –Э–Ш –і–∞–љ–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–Є 18,8 –Є 26,7%. –Э–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—О —Г—А–Њ–≤–љ–µ–є –Ґ –Є –Р, —Б–Њ—З–µ—В–∞—О—Й—Г—О—Б—П —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Ш–†–Ш, —Б–≤—П–Ј—Л–≤–∞—О—В —Б —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –≤–ї–Є—П–љ–Є—П –Ш–†–Ш –љ–∞ —Д–µ—А–Љ–µ–љ—В–∞—В–Є–≤–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–ї–µ—В–Њ–Ї —П–Є—З–љ–Є–Ї–∞, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –љ–∞ —Ж–Є—В–Њ—Е—А–Њ–Љ –†–450 [22]. –Р–љ—В–Є–∞–љ–і—А–Њ–≥–µ–љ–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –°–Є–Њ—Д–Њ—А–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Я–Ъ–ѓ –њ—А–Є –Э–Ш –Њ–±—К—П—Б–љ—П—О—В —Б —А–∞–Ј–љ—Л—Е –њ–Њ–Ј–Є—Ж–Є–є [4,23]:
– –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –±–Њ–ї—М–љ—Л–µ –Є–Љ–µ—О—В –љ–∞—А—Г—И–µ–љ–Є–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –Є–љ—Б—Г–ї–Є–љ—Г –Є —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –У–Ш, –Ї–Њ—В–Њ—А—Л–µ –љ–µ –≤—Л—П–≤–ї—П—О—В—Б—П –Є—Б–њ–Њ–ї—М–Ј—Г—О—Й–Є–Љ–Є—Б—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Љ–µ—В–Њ–і–∞–Љ–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –Ш–†;
– –Є–љ—Б—Г–ї–Є–љ —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В —Б–Є–љ—В–µ–Ј –∞–љ–і—А–Њ–≥–µ–љ–Њ–≤ –≤ —П–Є—З–љ–Є–Ї–∞—Е –і–∞–ґ–µ –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –У–Ш – –Ј–∞ —Б—З–µ—В –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є —В–Ї–∞–љ–Є —П–Є—З–љ–Є–Ї–Њ–≤ –Ї –µ–≥–Њ –і–µ–є—Б—В–≤–Є—О;
– –љ–µ –Є—Б–Ї–ї—О—З–µ–љ–Њ –њ—А—П–Љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –°–Є–Њ—Д–Њ—А–∞ –љ–∞ —Б—В–µ—А–Њ–Є–і–Њ–≥–µ–љ–µ–Ј –≤ —П–Є—З–љ–Є–Ї–∞—Е, –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ–µ –Њ—В —Г—А–Њ–≤–љ—П –Є–љ—Б—Г–ї–Є–љ–∞. –≠—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В –і–∞–љ–љ—Л–µ –Њ —Б–љ–Є–ґ–µ–љ–Є–Є –њ—А–Њ–і—Г–Ї—Ж–Є–Є –∞–љ–і—А–Њ–≥–µ–љ–Њ–≤ –≤ –Њ–њ—Г—Е–Њ–ї–µ–≤—Л—Е —В–µ–Ї–∞––Ї–ї–µ—В–Ї–∞—Е —З–µ–ї–Њ–≤–µ–Ї–∞ –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ [3].
–Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –≤ —А–∞–±–Њ—В–µ –і–∞–љ–љ—Л–µ –Њ —Б–љ–Є–ґ–µ–љ–Є–Є —Г—А–Њ–≤–љ—П –Ш–†–Ш —Г –±–Њ–ї—М–љ—Л—Е —Б –Э–Ш –і–∞—О—В –Њ—Б–љ–Њ–≤–∞–љ–Є–µ –Њ–±—К—П—Б–љ–Є—В—М —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –У–Р —З–∞—Б—В–Є—З–љ–Њ –Є –Ј–∞ —Б—З–µ—В —Н—В–Њ–≥–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞. –° –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Б–µ–Ї—А–µ—Ж–Є—П –∞–љ–і—А–Њ–≥–µ–љ–Њ–≤ –≤ —П–Є—З–љ–Є–Ї–∞—Е —А–µ–≥—Г–ї–Є—А—Г–µ—В—Б—П –Ы–У. –Ъ–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –±–Є–Њ—Б–Є–љ—В–µ–Ј–∞ –∞–љ–і—А–Њ–≥–µ–љ–Њ–≤ –Ј–∞ —Б—З–µ—В –њ–Њ–і–∞–≤–ї–µ–љ–Є—П –Ы–У –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –Є –µ–≥–Њ –њ—А—П–Љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ —П–Є—З–љ–Є–Ї –±—Л–ї–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–Њ Veldhuis [29] –љ–∞ –Ї—Г–ї—М—В—Г—А–µ –Ї–ї–µ—В–Њ–Ї –Є Mitwally [20] –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е –љ–∞ –ґ–Є–≤–Њ—В–љ—Л—Е. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Ы–У —Г –±–Њ–ї—М–љ—Л—Е —Б –Э–Ш —В–∞–Ї–ґ–µ –Љ–Њ–ґ–µ—В –≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–є —Б—В–µ–њ–µ–љ–Є —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є—О —Б–Є–љ—В–µ–Ј–∞ –∞–љ–і—А–Њ–≥–µ–љ–Њ–≤.
–£ –±–Њ–ї—М–љ—Л—Е —Б –°–Я–Ъ–ѓ —Б—В–µ–њ–µ–љ—М –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –У–Р –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –Є –Ј–∞ —Б—З–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—П —Б–≤–Њ–±–Њ–і–љ—Л—Е —Д—А–∞–Ї—Ж–Є–є –∞–љ–і—А–Њ–≥–µ–љ–Њ–≤ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є—П –Є–љ—Б—Г–ї–Є–љ–Њ–Љ —Б–Є–љ—В–µ–Ј–∞ –Ґ–≠–°–У –≤ –њ–µ—З–µ–љ–Є [16, 25]. –†–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–є —А–∞–±–Њ—В—Л –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—О—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ –і–∞–љ–љ–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –љ–∞ —Д–Њ–љ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П —Г—А–Њ–≤–љ—П –Ш–†–Ш. –Ґ–∞–Ї, —Г –±–Њ–ї—М–љ—Л—Е —Б –У–Ш —Б—А–µ–і–љ–Є–є —Г—А–Њ–≤–µ–љ—М –Ґ–≠–°–У —Г–≤–µ–ї–Є—З–Є–ї—Б—П –≤ 1,7 —А–∞–Ј, —З—В–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–Њ—Б—М –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ—Л–Љ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –∞–љ–і—А–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞ –Ї—А–Њ–≤–Є –≤ 2,5 —А–∞–Ј. –£ –±–Њ–ї—М–љ—Л—Е —Б –Э–Ш —Б–љ–Є–ґ–µ–љ–Є–µ —Б–µ–Ї—А–µ—Ж–Є–Є –Ш–†–Ш –±—Л–ї–Њ –љ–µ —Б—В–Њ–ї—М —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ, —Б—А–µ–і–љ–Є–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –Ґ–≠–°–У –њ–Њ–≤—Л—Б–Є–ї—Б—П –ї–Є—И—М –≤ 1,4 —А–∞–Ј–∞, –∞ –°–Р–Ш – –≤ 1,6 —А–∞–Ј–∞.
–Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ —Б–Њ–≥–ї–∞—Б—Г—О—В—Б—П —Б —А—П–і–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—О—Й–Є—Е, —З—В–Њ –Ї–Њ—А—А–µ–Ї—Ж–Є—П –У–Ш –Є —П–Є—З–љ–Є–Ї–Њ–≤–Њ–є –У–Р —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —А–Є—В–Љ–∞ –Љ–µ–љ—Б—В—А—Г–∞—Ж–Є–є –Є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—О —Д–µ—А—В–Є–ї—М–љ–Њ—Б—В–Є [25,30]. –Т —А—П–і–µ –љ–∞—Г—З–љ—Л—Е –њ—Г–±–ї–Є–Ї–∞—Ж–Є–є —Г–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П, —З—В–Њ –ї–µ—З–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –ї–Є—И—М —Г –±–Њ–ї—М–љ—Л—Е —Б –У–Ш [10,24], –≤ —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –і–µ–ї–∞–µ—В—Б—П –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ –Њ —В–Њ–Љ, —З—В–Њ –Ш–† –Є –У–Ш —П–≤–ї—П—О—В—Б—П –Љ–∞—А–Ї–µ—А–∞–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –љ–µ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Є –≤—Л—П–≤–Є—В—М –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П —А–Є—В–Љ–∞ –Љ–µ–љ—Б—В—А—Г–∞—Ж–Є–є –Њ—В –љ–∞–ї–Є—З–Є—П –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є—П –Є—Б—Е–Њ–і–љ–Њ–є –У–Ш –Є –Ш–†. –Ы–µ—З–µ–љ–Є–µ –°–Є–Њ—Д–Њ—А–Њ–Љ –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М –≤ —А–∞–≤–љ–Њ–є —Б—В–µ–њ–µ–љ–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –Ї–∞–Ї —Г –±–Њ–ї—М–љ—Л—Е —Б –У–Ш (61,3%), —В–∞–Ї –Є —Б –Э–Ш (55,6%). –£ –Ї–∞–ґ–і–Њ–є 2–3––є (45,2% –Є 37,0%) –Є–Ј –њ—А–Њ–ї–µ—З–µ–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е –≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є–ї–∞—Б—М –Њ–≤—Г–ї—П—Ж–Є—П, —Г –Ї–∞–ґ–і–Њ–є 3–4––є (33,3% –Є 27,8%) – –љ–∞—Б—В—Г–њ–Є–ї–∞ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М. –Я–Њ–і–Њ–±–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –±—Л–ї–Є –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ—Л Liu –Є –Ї–Њ–ї–ї–µ–≥–∞–Љ–Є [19], –Ї–Њ—В–Њ—А—Л–µ –Њ—В–Љ–µ—В–Є–ї–Є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ –Њ–≤—Г–ї—П—Ж–Є–Є –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П —Г 48,8% –±–Њ–ї—М–љ—Л—Е —Б –У–Ш –Є —Г 44,7% –±–Њ–ї—М–љ—Л—Е —Б –Э–Ш.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —И–µ—Б—В–Є–Љ–µ—Б—П—З–љ—Л–є –Ї—Г—А—Б —В–µ—А–∞–њ–Є–Є –°–Є–Њ—Д–Њ—А–Њ–Љ –Ї–Њ—А—А–Є–≥–Є—А—Г–µ—В –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Я–Ъ–ѓ –Ї–∞–Ї —Б –У–Ш, —В–∞–Ї –Є —Б –Э–Ш. –Ф–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—Б–Њ–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є, –њ—А–Њ—П–≤–ї—П—О—Й–∞—П—Б—П –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–µ–є —Д—Г–љ–Ї—Ж–Є–Є —П–Є—З–љ–Є–Ї–Њ–≤ –Є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ–Љ —Д–µ—А—В–Є–ї—М–љ–Њ—Б—В–Є, –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М, –і–Њ–Ї–∞–Ј–∞–љ–љ–∞—П –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є, –і–∞—О—В –Њ—Б–љ–Њ–≤–∞–љ–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞—В—М –°–Є–Њ—Д–Њ—А –і–ї—П –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б –°–Я–Ъ–ѓ –Є –∞–љ–Њ–≤—Г–ї—П—В–Њ—А–љ—Л–Љ –±–µ—Б–њ–ї–Њ–і–Є–µ–Љ –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –љ–∞–ї–Є—З–Є—П –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є—П –У–Ш.

–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Ahren B. et al. Improved meal–related beta–cell function and insulin sensitivity by the dipeptidyl peptidase–IV inhibitor vildagliptin in metformin–treated patients with type 2 diabetes over 1 year. / Diabetes Care.– 2005.–Vol.28., N 8. – p.1936–1940. 157
2. Asuncion M.J. et al. A prospective study of the prevalence of the polycystic ovary syndrome in unselected Caucasian women from Spain. / Clin Endocrinol Metab.–2000.– Vol.85., N 7.– p.2434– 2438.
3. Attia G.R. et al. Metformin directly inhibits androgen production in human thecal cells. / Fertil Steril.–2001.– Vol.76., N 3.– p.517–524.
4. Baillargeon J.P. et al. Effects of metformin and rosiglitazone, alone and in combination, in nonobese women with polycystic ovary syndrome and normal indices of insulin sensitivity. / Fertil Steril.–2004.–Vol.82., N 4.– p.893–990.
5. Banaszewska B. et al. Incidence of elevated LH/FSH ratio in polycystic ovary syndrome women with normo– and hyperinsulinemia. / Rocz Akad Med Bialymst.–2003.– Vol.48.–p.131–134.
6. Burghen G.A. et al. Correlation of hyperandrogenism with hiperinsulinism in polycystic ovarian disease. / J Clin Endocrinol Metab.–1980.– Vol.50., N 1.– p.113–116.
7. Carmina E., Lobo R.A. Does metformin induce ovulation in normoandrogenic ovulatory women / Am J Obstet Gynecol.–2004.–Vol.191., N 5.– p.1580–1584.
8. Diamani– Kandarakis E. et al. A survey of the polycystic ovary syndrome in the Greek island of Lesbos: hormonal and metabolic profile. / J Clin. Endocrinol. Metab.–1999.– Vol.84., N 11.– p.4006–4011.
9. Ehrmann D.A. et al. Effects of metformin on insulin secretion, insulin action, and ovarian steroidogenesis in women with polycystic ovary syndrome. / J Clin Endocrinol Metab.–1997.–Vol. 82., N 2.– p.24–30.
10. Eisenhardt S.J. et al. Early effects of metformin in women with polycystic ovary syndrome (PCOS): a prospective randomized double–blind placebo–controlled trial. / Clin Endocrinol Metab.–2006.– Vol.91., N 3.– p.946–952.
11. Elkind–Hirsch K.E. et al. Androgen responses to acutely increased endogenous insulin levels in hyperandrogenic and normally cycling women. / Fertil Steril.–1991.– Vol. 55., N 3.– p.486–491.
12. Garmes H.M. et al. Endocrine–vetabolic effects of the treatment with pioglitazonein obese patients with polycystic ovary syndrome. / Gynecol Endocrinol.–2005.– Vol.21., N 6.– p.317–323. 139
13. Genazzani A.D. et al. Metformin administration modulates and restores luteinizing hormone spontaneous episodic secretion and ovarian function in nonobese patients with polycystic ovary syndrome. / Fertil Steril.–2004.– Vol. 81., N 1.– p.114–119. 13
14. Glueck C. et al. Pregnancy outcomes among women with polycystic ovary syndrome treated with metformin. / Hum Reprod.–2002.– Vol.17., N 11.– p.2858–2864.
15. Glueck C.J. et al. Treatment of polycystic ovary syndrome with insulin–lowering agents. / Expert Opin Pharmacother.–2002.– Vol.3., N 8.– p.1177–1189.
16. Glueck G.J. et al. Pioglitazone and metformin in obese women with polycystic ovary syndrome not optimally responsive to metformin. / Hum Reprod.–2003.– Vol.18., N 8.– p.1618–1625.
17. Goodarzi M.O. et al. Polycystic ovary syndrome in Mexican–Americans: prevalence and association with the severity of insulin resistance. / Fertil Steril. – 2005. – Vol.84, N 3.– p.766–769.
18. Hundal R.S. et al. Mechanism by which metformin reduces glucose prodactin in type 2 diabetes. / Diabetes.–2000.– Vol.49., N 12.–p.2063–2069. 215
19. Liu K.E. et al. Use of metformin for ovulation induction in women who have polycystic ovary syndrome with or without evidence of insulin resistance. / J Obstet Gynaecol Can.–2006.–Vol.28., N 7. – p.595–599.
20. Mitwally M.F. et al. Troglitazone: a possible modulator of ovarian steroidogenesis. / J Soc Gynecol Investig.–2002.– Vol.9., N 3.– p.163–167.
21. Morin–Papunen L. et al. Metformin versus ethinyl estradiol–cyproterone acetate in the treatment of nonobese women with polycystic ovary syndrome: a randomized study. / J Clin Endocrinol Metab.–2003.– Vol.88., N 1.– p.148–156.
22. Nestler J.E. et al. Decreases in ovarian P450c17 activity and serum free testosterone after reduction in insulin secretion in women with polycystic ovary syndrome. / N Engl J Med. 1996.– Vol.29;335., N 9.– p.617–623.
23. Nestler J.E., Jakubowicz D.J. Lean women with polycystic ovary syndrome respond to insulin reduction with decreases in ovarian P450cl7 activity and serum androgens. / J Clin Endocrinol Metab.–1997.– Vol.82.– p.4075–4079.
24. Onalan G. et al. Predictive value of glucose–insulin ratio in PCOS and profile of women who benefit from metformin therapy: Obese, lean, hyper or normoinsulinemic / Eur J Obstet Gynecol Reprod Biol 2005.– Vol.1;123., N 2.– p.204–211.
25. Romualdi D. et al. Selective effects of pioglitazone on insulin and androgen abnormalities in normo– and hyperinsulinaemic obese patients with polycystic ovary syndrome. / Hum reprod.–2003.– Vol.18., N 6.–p. 1210–1218.
26. Sepilian V., Nagamani M.J. Effects of rosiglitazone in obese women with polycystic ovary syndrome and severe insulin resistance. / J Clin Endocrinol Metab.–2005.– Vol.90., N 1.– p.60–65.
27. Ulloa–Aguirre A. et al. Effects of metformin on inappropriate LH release in women with polycystic ovarian syndrome and insulin resistance. / Reprod Biomed Online.– 2006.– Vol.12., N 6. – p.669–683.
28. Velazquez E.M. et al. Metformin therapy in polycystic ovary syndrome reduces hyperinsulinemia, insulin resistance, hyperandrogenemia, and systolic blood pressure, while facilitating normal menses and pregnancy. / Metabolism.–1994.–Vol.43., N 5. – p.647–654.
29. Veldhuis J.D. et al. Troglitazone, an insulin–sensitizing thiazolidinedione, represses combined stimulation by LH and insulin of de novo androgen biosynthesis by thecal cells in vitro. / J Clin Endocrinol Metab.–2002.– Vol.87., N 3.– p.1129–1133.
30. Zheng Z. et al. Effect of rosiglitazone on insulin resistance and hyperandrogenism in polycystic ovary syndrome. / Zhonghua Fu Chan Ke Za Zhi.–2002.– Vol.37., N 5.– p.271–273.












