–Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П —П–≤–ї—П–µ—В—Б—П –њ—А–Є—З–Є–љ–Њ–є —А–∞–Ј–≤–Є—В–Є—П –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –∞ –Љ–∞–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П – –Њ—Б–љ–Њ–≤–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є —Б–Љ–µ—А—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф [2].
–†–µ–Ј—Г–ї—М—В–∞—В—Л –љ–µ–і–∞–≤–љ–µ–≥–Њ –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–∞, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ Stettler –Є –Ї–Њ–ї–ї–µ–≥–∞–Љ–Є [3], –њ–Њ–і—В–≤–µ—А–і–Є–ї–Є, —З—В–Њ —Г–ї—Г—З—И–µ–љ–Є–µ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Б–љ–Є–ґ–∞–µ—В —З–∞—Б—В–Њ—В—Г –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –Љ–∞–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 1 –Є–ї–Є 2 —В–Є–њ–∞. –Ф–Њ –љ–µ–і–∞–≤–љ–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –і–Њ–Љ–Є–љ–Є—А—Г—О—Й–Є–є —Д–Њ–Ї—Г—Б —В–µ—А–∞–њ–Є–Є –Ј–∞–Ї–ї—О—З–∞–ї—Б—П –≤ —Б–љ–Є–ґ–µ–љ–Є–Є —Г—А–Њ–≤–љ–µ–є HbA1c —Б –Њ—Б–Њ–±—Л–Љ –∞–Ї—Ж–µ–љ—В–Њ–Љ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї [4]. –Ю–і–љ–∞–Ї–Њ, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ —З—В–Њ –Ї–Њ–љ—В—А–Њ–ї—М –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї –љ–µ–Њ–±—Е–Њ–і–Є–Љ, –Њ–±—Л—З–љ–Њ –µ–≥–Њ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ–Њ–ї—Г—З–µ–љ–Њ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –і–∞–љ–љ—Л—Е, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є (–њ–Њ—Б–ї–µ –µ–і—Л) –≥–ї—О–Ї–Њ–Ј—Л –њ–ї–∞–Ј–Љ—Л –Є–Љ–µ–µ—В –≤–µ–і—Г—Й—Г—О —А–Њ–ї—М [5] –Є –љ–µ –Љ–µ–љ–µ–µ –≤–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≥–ї–Є–Ї–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞ (HbA1c) [6–11].
–Т–∞–ґ–љ–Њ—Б—В—М –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є —А–µ–≥—Г–ї—П—Ж–Є–Є —Б—В–∞–ї–∞ –Њ–і–љ–Њ–є –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е —В–µ–Љ –і–Є—Б–Ї—Г—Б—Б–Є–є –≤–Њ –≤—А–µ–Љ—П 43––≥–Њ –µ–ґ–µ–≥–Њ–і–љ–Њ–≥–Њ —Б–Њ–±—А–∞–љ–Є—П –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–є –Р—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О –і–Є–∞–±–µ—В–∞ –≤ —Б–µ–љ—В—П–±—А–µ 2007 –≥–Њ–і–∞ –≤ –Р–Љ—Б—В–µ—А–і–∞–Љ–µ. –®–Є—А–Њ–Ї–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –Њ–±—Й–µ—Б—В–≤–µ–љ–љ–Њ—Б—В–Є –±—Л–ї–Њ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ «–†—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –њ–Њ –≤–µ–і–µ–љ–Є—О –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є», —А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ–Њ–µ –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–є —Д–µ–і–µ—А–∞—Ж–Є–µ–є –і–Є–∞–±–µ—В–∞ –≤ 2007 –≥. –њ—А–Є —Г—З–∞—Б—В–Є–Є —Г—З–µ–љ—Л—Е —Б –±–Њ–ї—М—И–Є–Љ –Њ–њ—Л—В–Њ–Љ –≤ –њ–Њ–і–Њ–±–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –Є –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є—Е –≤—А–∞—З–µ–є, –∞ —В–∞–Ї–ґ–µ –ї–Є—Ж —Б –ґ–Є–Ј–љ–µ–љ–љ—Л–Љ –Њ–њ—Л—В–Њ–Љ –°–Ф. –Т–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ —Б–Њ–Ј–і–∞–≤–∞–ї–Њ—Б—М —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Њ—Б–љ–Њ–≤–љ—Л—Е –њ—А–Є–љ—Ж–Є–њ–Њ–≤ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л, —Б –Њ–њ–Њ—А–Њ–є –љ–∞ –Њ–±–Ј–Њ—А—Л, —Б–і–µ–ї–∞–љ–љ—Л–µ —А–∞–љ–µ–µ, –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј—Л, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ, –Ї–Њ–≥–Њ—А—В–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –∞ —В–∞–Ї–ґ–µ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞ –ґ–Є–≤–Њ—В–љ—Л—Е –Є —Д—Г–љ–і–∞–Љ–µ–љ—В–∞–ї—М–љ—Л–µ —А–∞–±–Њ—В—Л, –Њ—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–ї–Њ–ґ–µ–љ–Є—П –Є —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–∞.
–Т –Є—В–Њ–≥–µ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –њ—А–Є–Ј–љ–∞–љ–Њ, —З—В–Њ –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П —П–≤–ї—П–µ—В—Б—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Љ–∞–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Ґ–∞–Ї–ґ–µ —Б –≤—Л—Б–Њ–Ї–Њ–є —Б—В–µ–њ–µ–љ—М—О –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Љ–Њ–ґ–љ–Њ —Г—В–≤–µ—А–ґ–і–∞—В—М, —З—В–Њ –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–∞—П –≥–ї–Є–Ї–µ–Љ–Є—П (–Я–Я–У) –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П:
• —Б –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ —А–Є—Б–Ї–Њ–Љ —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є [7];
• —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —В–Њ–ї—Й–Є–љ—Л intima–media —Б–Њ–љ–љ—Л—Е –∞—А—В–µ—А–Є–є [11];
• —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Љ–Є–Њ–Ї–∞—А–і–Є–∞–ї—М–љ–Њ–≥–Њ –Њ–±—К–µ–Љ–∞ –Ї—А–Њ–≤–Є –Є –Љ–Є–Њ–Ї–∞—А–і–Є–∞–ї—М–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞;
• —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —А–∞–Ї–∞ [12–16];
• —Б –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –Ї–Њ–≥–љ–Є—В–Є–≤–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є —Г –ї–Є—Ж —Б—В–∞—А—И–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ —Б –°–Ф 2 —В–Є–њ–∞ [17];
• –∞ —В–∞–Ї–ґ–µ –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј–≤–Є—В–Є—О –Њ–Ї—Б–Є–і–∞—В–Є–≤–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞, –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Є —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є [18–20].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–∞—П –≥–ї–Є–Ї–µ–Љ–Є—П –≤—Л–Ј—Л–≤–∞–µ—В —Б–µ—А—М–µ–Ј–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П, –Є –µ–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М.
–Ь–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б–љ–Є–ґ–∞—О—Й–Є—Е –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –≥–ї—О–Ї–Њ–Ј—Л –њ–ї–∞–Ј–Љ—Л, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –Є —Б–љ–Є–ґ–µ–љ–Є—О —З–∞—Б—В–Њ—В—Л —А–∞–Ј–≤–Є—В–Є—П —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —В–µ—А–∞–њ–Є—П, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–∞—П –љ–∞ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї–∞–Ї –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї (–У–Ъ–Э), —В–∞–Ї –Є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є, —П–≤–ї—П–µ—В—Б—П —Б—В—А–∞—В–µ–≥–Є—З–µ—Б–Ї–Є –≤–∞–ґ–љ–Њ–є –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П —З–µ—А–µ–Ј –њ—А–Є–Ј–Љ—Г –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –°—В–∞–љ–Њ–≤–Є—В—Б—П —П—Б–љ–Њ, —З—В–Њ –≤–љ–µ–і—А–µ–љ–Є–µ –≤ –њ—А–∞–Ї—В–Є–Ї—Г —Б—В—А–∞—В–µ–≥–Є–Є, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–є –љ–∞ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—О –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є, –∞–±—Б–Њ–ї—О—В–љ–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ.
–Ъ –Ї–∞–Ї–Є–Љ –ґ–µ —Ж–µ–ї–µ–≤—Л–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є —Б–ї–µ–і—Г–µ—В —Б—В—А–µ–Љ–Є—В—М—Б—П? –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Г—А–Њ–≤–µ–љ—М –≥–ї—О–Ї–Њ–Ј—Л –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є –њ–Њ—Б–ї–µ –µ–і—Л —А–µ–і–Ї–Њ –њ–Њ–≤—Л—И–∞–µ—В—Б—П –≤—Л—И–µ 7,8 –Љ–Љ–Њ–ї—М/–ї —Г –ї–Є—Ж —Б –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В—М—О –Ї –≥–ї—О–Ї–Њ–Ј–µ –Є –Њ–±—Л—З–љ–Њ –≤–Њ–Ј–≤—А–∞—Й–∞–µ—В—Б—П –Ї –Є—Б—Е–Њ–і–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ —З–µ—А–µ–Ј –і–≤–∞ —З–∞—Б–∞ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–∞—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П —Д–µ–і–µ—А–∞—Ж–Є—П –Є –і—А—Г–≥–Є–µ –Ї–Њ–Љ–њ–µ—В–µ–љ—В–љ—Л–µ –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–Є –Њ–њ—А–µ–і–µ–ї—П—О—В –љ–Њ—А–Љ–∞–ї—М–љ—Г—О –≥–ї—О–Ї–Њ–Ј–Њ—В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В—М –Ї–∞–Ї —Г—А–Њ–≤–µ–љ—М –≥–ї–Є–Ї–µ–Љ–Є–Є –Љ–µ–љ–µ–µ 7,8 –Љ–Љ–Њ–ї—М/–ї —З–µ—А–µ–Ј –і–≤–∞ —З–∞—Б–∞ –њ–Њ—Б–ї–µ –љ–∞–≥—А—Г–Ј–Ї–Є —Б 75 –≥ –≥–ї—О–Ї–Њ–Ј—Л. –° —Г—З–µ—В–Њ–Љ —В–Њ–≥–Њ, —З—В–Њ –Њ—В—Б—Г—В—Б—В–≤—Г—О—В –і–∞–љ–љ—Л–µ –Њ —Б—Г—Й–µ—Б—В–≤–Њ–≤–∞–љ–Є–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–≥–Њ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–Њ–≥–∞ –і–ї—П —Б–љ–Є–ґ–µ–љ–Є—П —З–∞—Б—В–Њ—В—Л –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є [21,22], —Ж–µ–ї—М—О —В–µ—А–∞–њ–Є–Є –°–Ф –і–Њ–ї–ґ–љ–Њ –±—Л—В—М –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ –Ї–∞–Ї –Љ–Њ–ґ–љ–Њ –±–Њ–ї–µ–µ –±–ї–Є–Ј–Ї–Њ–≥–Њ –Ї –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ –њ–Њ –≤—Б–µ–Љ —В—А–µ–Љ –Ї—А–Є—В–µ—А–Є—П–Љ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П: —Г—А–Њ–≤–љ—О HbA1c, —Г—А–Њ–≤–љ—О –≥–ї—О–Ї–Њ–Ј—Л –њ–ї–∞–Ј–Љ—Л –љ–∞—В–Њ—Й–∞–Ї –Є –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є. –° —Г—З–µ—В–Њ–Љ —Н—В–Є—Е —Ж–µ–ї–µ–є –Є –њ–Њ–≤—Л—И–µ–љ–Є—П –і–Њ—Б—В—Г–њ–љ–Њ—Б—В–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–∞—А–Є–∞–љ—В–Њ–≤ —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є, –∞ —В–∞–Ї–ґ–µ —В–µ—Е–љ–Њ–ї–Њ–≥–Є–є –і–ї—П –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Є –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Ж–µ–ї–µ–≤–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –≥–ї—О–Ї–Њ–Ј—Л –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є —З–µ—А–µ–Ј 2 —З–∞—Б–∞ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є –Љ–µ–љ–µ–µ 7,8 –Љ–Љ–Њ–ї—М/–ї –Љ–Њ–ґ–љ–Њ —Б—З–Є—В–∞—В—М —А–µ–Ј–Њ–љ–љ—Л–Љ –Є –і–Њ—Б—В–Є–ґ–Є–Љ—Л–Љ.
–Э–∞–і–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П —П–≤–ї—П–µ—В—Б—П —З–∞—Б—В–Њ –≤—Б—В—А–µ—З–∞—О—Й–Є–Љ—Б—П —Д–µ–љ–Њ–Љ–µ–љ–Њ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф –Ї–∞–Ї 1, —В–∞–Ї –Є 2 —В–Є–њ–∞ [37–40] –Є –Љ–Њ–ґ–µ—В –≤—Л—П–≤–ї—П—В—М—Б—П –і–∞–ґ–µ –µ—Б–ї–Є —Б—А–µ–і–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В—Б—П –∞–і–µ–Ї–≤–∞—В–љ—Л–Љ–Є –њ—А–Є –Њ—Ж–µ–љ–Ї–µ –њ–Њ —Г—А–Њ–≤–љ—О HbA1c [23,24]. –Ґ–∞–Ї, –≤ –њ–µ—А–µ–Ї—А–µ—Б—В–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б —Г—З–∞—Б—В–Є–µ–Љ 443 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ —Г 71% –Њ–±—Б–ї–µ–і—Г–µ–Љ—Л—Е –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л —Б—А–µ–і–љ–Є–µ –і–≤—Г—Е—З–∞—Б–Њ–≤—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≥–ї–Є–Ї–µ–Љ–Є–Є –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є –њ–Њ—Б–ї–µ –µ–і—Л –±–Њ–ї–µ–µ 14 –Љ–Љ–Њ–ї—М/–ї [25]. –Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [26] —Б –Њ—Ж–µ–љ–Ї–Њ–є —Б—Г—В–Њ—З–љ—Л—Е –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Д–Є–ї–µ–є —Г 3284 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –љ–∞ –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є –≤ —В–µ—З–µ–љ–Є–µ –Њ–і–љ–Њ–є –љ–µ–і–µ–ї–Є –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Г—А–Њ–≤–µ–љ—М –≥–ї–Є–Ї–µ–Љ–Є–Є –њ–ї–∞–Ј–Љ—Л –њ–Њ—Б–ї–µ –µ–і—Л –±–Њ–ї–µ–µ 8,9 –Љ–Љ–Њ–ї—М/–ї —Д–Є–Ї—Б–Є—А—Г–µ—В—Б—П, –њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ, –≤ 84% —Б–ї—Г—З–∞–µ–≤.
–Ф–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –љ–µ—В –Ј–∞–≤–µ—А—И–µ–љ–љ—Л—Е —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е –љ–∞ –Є–Ј—Г—З–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Њ–≤ –Ї–Њ–љ—В—А–Њ–ї—П –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞ —А–∞–Ј–≤–Є—В–Є–µ –Љ–∞–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Ю–і–љ–∞–Ї–Њ, –Ї –њ—А–Є–Љ–µ—А—Г, —В–µ—А–∞–њ–Є—П –∞–љ–∞–ї–Њ–≥–∞–Љ–Є –Є–љ—Б—Г–ї–Є–љ–∞ —Г–ї—М—В—А–∞–Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –і–ї—П –Ї–Њ–љ—В—А–Њ–ї—П –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –љ–∞ –Љ–∞—А–Ї–µ—А—Л —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, —В–∞–Ї–Є—Е –Ї–∞–Ї –љ–Є—В—А–Њ—В–Є—А–Њ–Ј–Є–љ [27], –Љ–µ—В–Є–ї–≥–ї–Є–Њ–Ї—Б–∞–ї—М (–Ь–У) –Є 3––і–µ–Њ–Ї—Б–Є–≥–ї—О–Ї–Њ–Ј–Њ–љ (3––Ф–У) [28].
–С–Њ–ї–µ–µ —В–Њ–≥–Њ, –≤ –Њ–і–љ–Њ–Љ –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Ї–Њ–љ—В—А–Њ–ї—М —В–Њ–ї—М–Ї–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –±—Л—Б—В—А–Њ–і–µ–є—Б—В–≤—Г—О—Й–µ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ –њ–Њ–≤—Л—И–∞–ї –Љ–Є–Њ–Ї–∞—А–і–Є–∞–ї—М–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї, –Ї–Њ—В–Њ—А—Л–є –Њ–±—Л—З–љ–Њ —Б–љ–Є–ґ–µ–љ –њ—А–Є –°–Ф 2 —В–Є–њ–∞ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є [29]. –Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –њ—А–Є –Њ—Ж–µ–љ–Ї–µ –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є, –Ь–У –Є 3––Ф–У —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 1 —В–Є–њ–∞ [28]. –£ —Н—В–Њ–є –ґ–µ –≥—А—Г–њ–њ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —В–µ—А–∞–њ–Є—П –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –ї–Є–Ј–њ—А–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Б–љ–Є–ґ–∞–ї–∞ –Ї–Њ–ї–µ–±–∞–љ–Є—П —Г—А–Њ–≤–љ–µ–є –Ь–У –Є 3––Ф–У, –Є —Н—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ—А—А–µ–ї–Є—А–Њ–≤–∞–ї–Њ —Б –љ–Є–Ј–Ї–Є–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –Ї–Њ–ї–µ–±–∞–љ–Є–є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –њ—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є —Б —В–µ—А–∞–њ–Є–µ–є –Њ–±—Л—З–љ—Л–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ.
–Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —И–Є—А–Њ–Ї–Њ –Є–Ј–≤–µ—Б—В–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П Kumamoto [30], –≤ –Ї–Њ—В–Њ—А–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П —А–µ–ґ–Є–Љ –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ—Л—Е –Є–љ—К–µ–Ї—Ж–Є–є –Є–љ—Б—Г–ї–Є–љ–∞ –і–ї—П –Ї–Њ–љ—В—А–Њ–ї—П –Ї–∞–Ї –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї, —В–∞–Ї –Є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–µ–Љ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞, –љ–µ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ —А–∞–Ј–≤–Є—В–Є—П –Є–ї–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є –Є–ї–Є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є –њ—А–Є —Г—А–Њ–≤–љ–µ –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї <6,1 –Љ–Љ–Њ–ї—М/–ї –Є —Г—А–Њ–≤–љ–µ –≥–ї–Є–Ї–µ–Љ–Є–Є —З–µ—А–µ–Ј 2 —З–∞—Б–∞ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є <10 –Љ–Љ–Њ–ї—М/–ї. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В—Б—П, —З—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –Є —Б–љ–Є–ґ–µ–љ–Є–µ –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї –≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –њ—А–Є–≤–Њ–і—П—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є –Є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є.
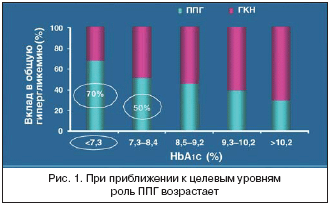
–Ф–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є –≤–Ї–ї–∞–і —Г—А–Њ–≤–љ—П –≥–ї—О–Ї–Њ–Ј—Л –њ–ї–∞–Ј–Љ—Л –њ–Њ—Б–ї–µ –µ–і—Л –≤ —Б—А–µ–і–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≥–ї–Є–Ї–µ–Љ–Є–Є —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –њ–Њ –Љ–µ—А–µ —Б–љ–Є–ґ–µ–љ–Є—П —Г—А–Њ–≤–љ—П HbA1c. Monnier –Є –Ї–Њ–ї–ї–µ–≥–Є [31] –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Г—А–Њ–≤–љ—П–Љ–Є HbA1c <7,3% –≤–Ї–ї–∞–і –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –≤ —Г—А–Њ–≤–µ–љ—М HbA1c —Б–Њ—Б—В–∞–≤–ї—П–ї –Њ–Ї–Њ–ї–Њ 70%, –Ї–Њ–≥–і–∞ –ґ–µ —Г—А–Њ–≤–љ–Є HbA1c –±—Л–ї–Є –≤—Л—И–µ 9,3%, –≤–Ї–ї–∞–і –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є —Б–Њ—Б—В–∞–≤–ї—П–ї –Њ–Ї–Њ–ї–Њ 40% [32] (—А–Є—Б. 1).
Woerle –Є –Ї–Њ–ї–ї–µ–≥–Є [33] –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є –≤–Ї–ї–∞–і –Ї–Њ–љ—В—А–Њ–ї—П –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї –Є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Є —Г—А–Њ–≤–љ–µ–Љ HbA1c?7,5%. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —В–Њ–ї—М–Ї–Њ —Г 64% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –і–Њ—Б—В–Є–≥—И–Є—Е —Г—А–Њ–≤–љ—П –≥–ї—О–Ї–Њ–Ј—Л –њ–ї–∞–Ј–Љ—Л –љ–∞—В–Њ—Й–∞–Ї <5,6 –Љ–Љ–Њ–ї—М/–ї, –љ–∞–±–ї—О–і–∞–ї—Б—П —Г—А–Њ–≤–µ–љ—М HbA1c<7%, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —В–∞–Ї–Њ–≥–Њ –ґ–µ —Г—А–Њ–≤–љ—П HbA1c –і–Њ—Б—В–Є–≥–ї–Є 94% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –Є–Љ–µ–ї–Є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ—Л–µ —Г—А–Њ–≤–љ–Є –≥–ї–Є–Ї–µ–Љ–Є–Є –Љ–µ–љ–µ–µ 7,8 –Љ–Љ–Њ–ї—М/–ї. –°–љ–Є–ґ–µ–љ–Є–µ –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –њ—А–Є–≤–µ–ї–Њ –Ї —Б–љ–Є–ґ–µ–љ–Є—О –≤ –і–≤–∞ —А–∞–Ј–∞ —Г—А–Њ–≤–љ—П HbA1c –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї. –Т–Ї–ї–∞–і –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≥–ї–Є–Ї–µ–Љ–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї –њ—А–Є–Љ–µ—А–љ–Њ 80% HbA1c –њ—А–Є —Г—А–Њ–≤–љ–µ HbA1c –Љ–µ–љ–µ–µ 6,2% –Є –њ—А–Є–Љ–µ—А–љ–Њ 40% –≤ —В–Њ–Љ —Б–ї—Г—З–∞–µ, –Ї–Њ–≥–і–∞ HbA1c –±—Л–ї –≤—Л—И–µ 9,0%.
–≠—В–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В —В–Њ—З–Ї—Г –Ј—А–µ–љ–Є—П –Њ —В–Њ–Љ, —З—В–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ –Ї–Њ–љ—В—А–Њ–ї—М –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї, –љ–Њ –Њ–±—Л—З–љ–Њ —Н—В–Њ–≥–Њ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є HbA1c<7%, –њ–Њ—Н—В–Њ–Љ—Г –Ї–Њ–љ—В—А–Њ–ї—М –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є –∞–±—Б–Њ–ї—О—В–љ–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–љ—Л—Е —Ж–µ–ї–µ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є HbA1c. –Ъ—А–∞–є–љ–µ –≤–∞–ґ–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Ж–µ–ї–µ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–µ –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ —А–Є—Б–Ї–Њ–Љ –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є. –° –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є –Љ–Њ–ґ–µ—В –њ–Њ–≤—Л—И–∞—В—М—Б—П –њ—А–Є –њ–Њ–њ—Л—В–Ї–∞—Е —Б–љ–Є–Ј–Є—В—М —Г—А–Њ–≤–µ–љ—М HbA1c –і–Њ —Ж–µ–ї–µ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є –Љ–µ–љ–µ–µ 7% –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П —В–Њ–ї—М–Ї–Њ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –њ—А–Њ–≤–Њ–і–Є–≤—И–µ–Љ—Б—П –њ–Њ –њ—А–Є–љ—Ж–Є–њ—Г «–ї–µ—З–µ–љ–Є–µ –і–Њ —Ж–µ–ї–Є» («treat–to–target») [34] —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–≤ —Б—А–µ–і–љ–µ–є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –і–µ–є—Б—В–≤–Є—П –Є –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –і–ї—П –Ї–Њ–љ—В—А–Њ–ї—П –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї, —В–Њ–ї—М–Ї–Њ 25% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –љ–∞—Е–Њ–і–Є–≤—И–Є—Е—Б—П –љ–∞ —В–µ—А–∞–њ–Є–Є –≥–ї–∞—А–≥–Є–љ–Њ–Љ —Б –≤–≤–µ–і–µ–љ–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –Њ–і–Є–љ —А–∞–Ј –≤ —Б—Г—В–Ї–Є, –і–Њ—Б—В–Є–≥–ї–Є —Г—А–Њ–≤–љ—П HbA1c –Љ–µ–љ–µ–µ 7% –±–µ–Ј –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л—Е —Н–њ–Є–Ј–Њ–і–Њ–≤ –љ–Њ—З–љ—Л—Е –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є. Bastyr –Є –Ї–Њ–ї–ї–µ–≥–Є [35] –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Ж–µ–ї–µ–≤–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –≤ –њ—А–Њ—В–Є–≤–Њ–њ–Њ–ї–Њ–ґ–љ–Њ—Б—В—М –≤–ї–Є—П–љ–Є—О –љ–∞ —Г—А–Њ–≤–µ–љ—М –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–ї–Њ—Б—М —Б –∞–љ–∞–ї–Њ–≥–Є—З–љ–Њ–є –Є–ї–Є –Љ–µ–љ—М—И–µ–є —З–∞—Б—В–Њ—В–Њ–є —А–∞–Ј–≤–Є—В–Є—П –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–є. –Ґ–∞–Ї–ґ–µ –љ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Б–ї—Г—З–∞–µ–≤ —В—П–ґ–µ–ї—Л—Е –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Woerle –Є –Ї–Њ–ї–ї–µ–≥, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –±—Л–ї–Њ –і–Њ—Б—В–Є–≥–љ—Г—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ —Б—А–µ–і–љ–µ–≥–Њ —Г—А–Њ–≤–љ—П HbA1c –Њ—В 8,7% –і–Њ 6,5%. –Я—А–Є —Н—В–Њ–Љ —Ж–µ–ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤–Ї–ї—О—З–∞–ї–Є –≤–ї–Є—П–љ–Є–µ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≥–ї—О–Ї–Њ–Ј—Л –њ–ї–∞–Ј–Љ—Л –њ–Њ—Б–ї–µ –µ–і—Л [36].
–Ъ –њ—А–µ–њ–∞—А–∞—В–∞–Љ, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є–Љ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Я–Я–У, –Њ—В–љ–Њ—Б—П—В—Б—П: –Є–љ–≥–Є–±–Є—В–Њ—А—Л ?––≥–ї—О–Ї–Њ–Ј–Є–і–∞–Ј—Л, –≥–ї–Є–љ–Є–і—Л (—Б–µ–Ї—А–µ—В–∞–≥–Њ–≥–Є –Є–љ—Б—Г–ї–Є–љ–∞ –±—Л—Б—В—А–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П) –Є –Є–љ—Б—Г–ї–Є–љ (–∞–љ–∞–ї–Њ–≥–Є –Є–љ—Б—Г–ї–Є–љ–∞ —Г–ї—М—В—А–∞–Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –і–≤—Г—Е—Д–∞–Ј–љ—Л–µ [–≥–Њ—В–Њ–≤—Л–µ —Б–Љ–µ—Б–Є] –Є–љ—Б—Г–ї–Є–љ—Л, –Є–љ–≥–∞–ї—П—Ж–Є–Њ–љ–љ—Л–є –Є–љ—Б—Г–ї–Є–љ, –Њ–±—Л—З–љ—Л–є —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–є –Є–љ—Б—Г–ї–Є–љ).
–Р–љ–∞–ї–Њ–≥–Є –Є–љ—Б—Г–ї–Є–љ–∞ —Г–ї—М—В—А–∞–Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –±—Л–ї–Є —А–∞–Ј—А–∞–±–Њ—В–∞–љ—Л –і–ї—П –Є–Љ–Є—В–∞—Ж–Є–Є –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б–µ–Ї—А–µ—Ж–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞. –Ф–ї—П –љ–Є—Е —Е–∞—А–∞–Ї—В–µ—А–љ–Њ –±—Л—Б—В—А–Њ–µ –љ–∞—З–∞–ї–Њ –і–µ–є—Б—В–≤–Є—П –Є –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ –њ–Є–Ї–Њ–≤–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, –∞ —В–∞–Ї–ґ–µ –±–Њ–ї–µ–µ –Ї–Њ—А–Њ—В–Ї–∞—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–µ–є—Б—В–≤–Є—П.
–Т –і–≤—Г—Е—Д–∞–Ј–љ—Л—Е (–≥–Њ—В–Њ–≤—Л—Е —Б–Љ–µ—Б—П—Е) –Є–љ—Б—Г–ї–Є–љ–Њ–≤ —Б–Њ—З–µ—В–∞–µ—В—Б—П –∞–љ–∞–ї–Њ–≥ –Є–љ—Б—Г–ї–Є–љ–∞ —Г–ї—М—В—А–∞–Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П —Б –Є–љ—Б—Г–ї–Є–љ–Њ–Љ —Б—А–µ–і–љ–µ–є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –і–µ–є—Б—В–≤–Є—П –і–ї—П –Є–Љ–Є—В–∞—Ж–Є–Є –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б–µ–Ї—А–µ—Ж–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞ –Є —Б–љ–Є–ґ–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є [37–40].
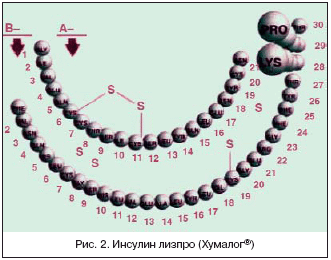
–Ь–µ–і–Є—Ж–Є–љ—Б–Ї–∞—П —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ–∞–ї–Њ–≥–Њ–≤ –Є–љ—Б—Г–ї–Є–љ–∞ –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ —В–Њ–Љ, —З—В–Њ –Њ–љ–Є –±–Њ–ї–µ–µ –±–ї–Є–Ј–Ї–Є –Ї —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –њ–∞—А–∞–Љ–µ—В—А–∞–Љ –і–Є–љ–∞–Љ–Є–Ї–Є –Є–љ—Б—Г–ї–Є–љ–∞, —З—В–Њ –љ–∞—А—П–і—Г —Б –і—А—Г–≥–Є–Љ–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞–Љ–Є –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–ї—Г—З—И–µ–љ–Є—О –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–≥–Њ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –Є —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –љ–Є–Ј–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–Ј–і–љ–µ–є –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є. –Ґ–∞–Ї, –Ј–∞–Љ–µ–љ–∞ –њ—А–Є—А–Њ–і–љ–Њ–є –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В–Є –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В —Б –њ–Њ–Љ–Њ—Й—М—О —А–µ–Ї–Њ–Љ–±–Є–љ–∞–љ—В–љ–Њ–є –Ф–Э–Ъ–—В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є –њ—А–Њ–ї–Є–љ––ї–Є–Ј–Є–љ –Т28 –Є –Т29 –Т–—Ж–µ–њ–Є –Є–љ—Б—Г–ї–Є–љ–Њ–≤–Њ–є –Љ–Њ–ї–µ–Ї—Г–ї—Л –љ–∞ –Њ–±—А–∞—В–љ—Г—О (—А–Є—Б. 2) –њ—А–Є–≤–µ–ї–∞ –Ї –њ–Њ—П–≤–ї–µ–љ–Є—О –∞–љ–∞–ї–Њ–≥–∞ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ [–Ы–Є–Ј(–Т28), –Я—А–Њ (–Т29)] (–Є–љ—Б—Г–ї–Є–љ –ї–Є–Ј–њ—А–Њ (–•—Г–Љ–∞–ї–Њ–≥®).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–Њ–ї–µ–Ї—Г–ї—Л –Є–љ—Б—Г–ї–Є–љ–∞ –•—Г–Љ–∞–ї–Њ–≥® –Є–Љ–µ—О—В —Е–∞—А–∞–Ї—В–µ—А–љ—Г—О –±–Њ–ї–µ–µ –±—Л—Б—В—А—Г—О —Б–Ї–Њ—А–Њ—Б—В—М –∞–±—Б–Њ—А–±—Ж–Є–Є –Є –±–Њ–ї–µ–µ –Ї–Њ—А–Њ—В–Ї—Г—О –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–µ–є—Б—В–≤–Є—П –≤—Б–ї–µ–і—Б—В–≤–Є–µ –Љ–µ–љ–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є —В–µ–љ–і–µ–љ—Ж–Є–Є –Ї —Б–∞–Љ–Њ–∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–Љ–Є –Є–љ—Б—Г–ї–Є–љ–∞–Љ–Є –Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П. –Э–∞—З–∞–ї–Њ –і–µ–є—Б—В–≤–Є—П –Є–љ—Б—Г–ї–Є–љ–∞ –•—Г–Љ–∞–ї–Њ–≥® –љ–∞—Б—В—Г–њ–∞–µ—В —З–µ—А–µ–Ј 0–15 –Љ–Є–љ. –њ–Њ—Б–ї–µ –Є–љ—К–µ–Ї—Ж–Є–Є, –њ–Є–Ї –і–µ–є—Б—В–≤–Є—П –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П —З–µ—А–µ–Ј 45–60 –Љ–Є–љ., –∞ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–µ–є—Б—В–≤–Є—П –Њ–≥—А–∞–љ–Є—З–µ–љ–∞ 3–4 —З–∞—Б–∞–Љ–Є.
–°—В–Њ–Є—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –њ–Њ–ї–Њ–ґ–µ–љ–Є—П –ї–Є–Ј–Є–љ–∞ –Є –њ—А–Њ–ї–Є–љ–∞ –≤ –Љ–Њ–ї–µ–Ї—Г–ї–µ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ –љ–µ –Є–Ј–Љ–µ–љ—П–µ—В –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –∞–Ї—В–Є–≤–љ–Њ–є –Р–—Ж–µ–њ–Є, –љ–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —В–Њ–Љ—Г, —З—В–Њ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–∞ –•—Г–Љ–∞–ї–Њ–≥–∞® –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ –њ—А–Є–±–ї–Є–ґ–∞–µ—В—Б—П –Ї —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ—Г –і–µ–є—Б—В–≤–Є—О –Є–љ—Б—Г–ї–Є–љ–∞ —Г –Ј–і–Њ—А–Њ–≤–Њ–≥–Њ —З–µ–ї–Њ–≤–µ–Ї–∞. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –Є–љ—Б—Г–ї–Є–љ –ї–Є–Ј–њ—А–Њ –Њ–±–ї–∞–і–∞–µ—В —В–∞–Ї–Є–Љ –ґ–µ –њ—А–Њ—Д–Є–ї–µ–Љ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є, –Ї–∞–Ї –њ—А–Њ—Б—В–Њ–є —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–є –Є–љ—Б—Г–ї–Є–љ. –Ґ–∞–Ї, –≤ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –љ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –љ–Є–Ї–∞–Ї–Є—Е –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е —П–≤–ї–µ–љ–Є–Є, —Б–њ–µ—Ж–Є—Д–Є—З–љ—Л—Е –і–ї—П –Є–љ—Б—Г–ї–Є–љ–∞ –ї–Є–Ј–њ—А–Њ [41]: –њ—А–µ–њ–∞—А–∞—В –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –Њ—В–ї–Є—З–∞–µ—В—Б—П –Њ—В —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Б—В–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ –њ–Њ –µ–≥–Њ –Є–Љ–Љ—Г–љ–Њ–≥–µ–љ–љ–Њ—Б—В–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ [42], —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–Љ —Н—Д—Д–µ–Ї—В–∞–Љ –≤ –њ–µ—А–Є–Њ–і —А–µ–њ—А–Њ–і—Г–Ї—Ж–Є–Є –Є —А–∞–Ј–≤–Є—В–Є—П —Г –ґ–Є–≤–Њ—В–љ—Л—Е [43] –Є –њ–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞—В—М –Ї–ї–µ—В–Њ—З–љ—Л–є —А–Њ—Б—В [44].
–†–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—П —А–∞–Ј–≤–Є—В–Є–µ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є, —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Є–Ј–Љ–µ–љ–Є–ї–∞—Б—М –Є —В–µ—А–Љ–Є–љ–Њ–ї–Њ–≥–Є—П. –Ґ–∞–Ї, –≤–Љ–µ—Б—В–Њ «–Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є» –њ—А–µ–і–ї–∞–≥–∞–µ—В—Б—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —В–µ—А–Љ–Є–љ «–≥–Є–±–Ї–∞—П –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є—П», –∞ –њ—А–µ–њ–∞—А–∞—В—Л –Є–љ—Б—Г–ї–Є–љ–∞ –њ–Њ–і—А–∞–Ј–і–µ–ї—П—В—М –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–љ—Ж–Є–њ–Њ–≤ –Ј–∞–Љ–µ—Б—В–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ–∞ –њ—А–∞–љ–і–Є–∞–ї—М–љ—Л–є –Є–љ—Б—Г–ї–Є–љ –Є –њ–Њ—Б—В–∞–±—Б–Њ—А–±—Ж–Є–Њ–љ–љ—Л–є –Є–љ—Б—Г–ї–Є–љ.
–Ы—Г—З—И–Є–є –Ї–Њ–љ—В—А–Њ–ї—М –њ–Њ—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–љ–Є–Є –•—Г–Љ–∞–ї–Њ–≥–∞® –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥–µ–љ–љ–Њ–Є–љ–ґ–µ–љ–µ—А–љ—Л–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –њ–Њ–і—В–≤–µ—А–і–Є–ї–Є –Є –±–Њ–ї—М—И–Є–µ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б —Г—З–∞—Б—В–Є–µ–Љ –±–Њ–ї–µ–µ 2000 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–ї–Є–ї–Є—Б—М –і–Њ 12 –Љ–µ—Б—П—Ж–µ–≤ –Є –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –≥–ї–Є–Ї–µ–Љ–Є–Є –±—Л–ї –љ–∞ 1,5–2,5 –Љ–Љ–Њ–ї—М/–ї –љ–Є–ґ–µ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –•—Г–Љ–∞–ї–Њ–≥–∞® [Zinman B.,1997; Melki,1998; De Verga, 1998; Garg S.K.,1999].
–Ю—В–Љ–µ—В–Є–Љ –µ—Й–µ —А–∞–Ј, —З—В–Њ —Ж–µ–ї—М –ї–µ—З–µ–љ–Є—П –і–Є–∞–±–µ—В–∞ —Б–Њ—Б—В–Њ–Є—В –≤ –і–Њ—Б—В–Є–ґ–µ–љ–Є–Є —Е–Њ—А–Њ—И–µ–є –Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –±–µ–Ј —Г–≤–µ–ї–Є—З–µ–љ–Є—П —А–Є—Б–Ї–∞ –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є. –†–µ–Ј—Г–ї—М—В–∞—В—Л, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –≤ —А–∞–Љ–Ї–∞—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П Diabetes Control and Complications Trial («–Ъ–Њ–љ—В—А–Њ–ї—М –Ј–∞ –і–Є–∞–±–µ—В–Њ–Љ –Є –µ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П–Љ–Є») –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є —Б–ї–Њ–ґ–љ–Њ—Б—В—М –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л—Е –Ј–љ–∞—З–µ–љ–Є–є HbA1c –±–µ–Ј –њ–Њ–≤—Л—И–µ–љ–Є—П —А–Є—Б–Ї–∞ –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є [45], –≤ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –≤ –љ–Њ—З–љ–Њ–µ –≤—А–µ–Љ—П [46]. –У–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є—П —П–≤–ї—П–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ –Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –Њ–њ–∞—Б–љ—Л–Љ –њ–Њ–±–Њ—З–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П. –Я–Њ –Њ—Ж–µ–љ–Ї–∞–Љ, –±–Њ–ї—М–љ–Њ–є –°–Ф 1 —В–Є–њ–∞ –Ј–∞ 40–45 –ї–µ—В –ґ–Є–Ј–љ–Є —Б –і–Є–∞–±–µ—В–Њ–Љ –Є—Б–њ—Л—В—Л–≤–∞–µ—В –≤ —Б—А–µ–і–љ–µ–Љ 3500 –њ—А–Є—Б—В—Г–њ–Њ–≤ –ї–µ–≥–Ї–Њ–є –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є, 30–70 – —В—П–ґ–µ–ї–Њ–є –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є –Є 3–7 —Б–ї—Г—З–∞–µ–≤ –Ї–Њ–Љ—Л [46,47]. –Я–∞—Ж–Є–µ–љ—В—Л –±–Њ—П—В—Б—П —В—П–ґ–µ–ї–Њ–є –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є –љ–µ –Љ–µ–љ—М—И–µ, —З–µ–Љ —В–∞–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –Ї–∞–Ї –њ–Њ—З–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –Є —Б–ї–µ–њ–Њ—В–∞.
–°–Њ–њ–Њ—Б—В–∞–≤–ї–µ–љ–Є–µ –Є–љ—Б—Г–ї–Є–љ–∞ –ї–Є–Ј–њ—А–Њ —Б –њ—А–Њ—Б—В—Л–Љ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –≤ –±–Њ–ї—М—И–Њ–Љ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б —Г—З–∞—Б—В–Є–µ–Љ 1008 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 1 —В–Є–њ–∞ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 6 –Љ–µ—Б—П—Ж–µ–≤ –њ–Њ–Ї–∞–Ј–∞–ї–Њ [48], —З—В–Њ –≤ —В–µ—З–µ–љ–Є–µ –≤—Б–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ—Л–є –њ–Њ–і—К–µ–Љ —Г—А–Њ–≤–љ—П –≥–ї—О–Ї–Њ–Ј—Л –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –ї–Є–Ј–њ—А–Њ –±—Л–ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Љ–µ–љ—М—И–µ. –Ъ –Ї–Њ–љ—Ж—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Є–љ—Б—Г–ї–Є–љ –ї–Є–Ј–њ—А–Њ, –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ—Л–є –њ–Њ–і—К–µ–Љ –≥–ї—О–Ї–Њ–Ј—Л –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –±—Л–ї –љ–Є–ґ–µ —З–µ—А–µ–Ј 1 —З. –љ–∞ 1,3 –Љ–Љ–Њ–ї—М/–ї, –∞ —З–µ—А–µ–Ј 2 —З. – –љ–∞ 2,0 –Љ–Љ–Њ–ї—М/–ї (p<0,001). –° –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, —З–∞—Б—В–Њ—В–∞ –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –ї–Є–Ј–њ—А–Њ –±—Л–ї–∞ –љ–∞ 12% –Љ–µ–љ—М—И–µ (6,4±0,2 vs. 7,2±0,3 —Н–њ–Є–Ј–Њ–і–Њ–≤ –Ј–∞ 30 –і–љ–µ–є, p<0,001) –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В —Б—Е–µ–Љ—Л –≤–≤–µ–і–µ–љ–Є—П –±–∞–Ј–Є—Б–љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ –Є —Г—А–Њ–≤–љ—П HbA1c. –≠—В–Є —Б–љ–Є–ґ–µ–љ–Є—П –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –і–ї—П —Н–њ–Є–Ј–Њ–і–Њ–≤ –Ї–∞–Ї —Б —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є, —В–∞–Ї –Є –і–ї—П –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ—Л—Е. –Я—А–Є –∞–љ–∞–ї–Є–Ј–µ —Б—Г–Љ–Љ–∞—А–љ–Њ–≥–Њ —З–Є—Б–ї–∞ —Н–њ–Є–Ј–Њ–і–Њ–≤ –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є –њ–Њ –Ї–∞–ґ–і–Њ–Љ—Г –њ–∞—Ж–Є–µ–љ—В—Г –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≤—А–µ–Љ–µ–љ–Є –Є—Е —А–∞–Ј–≤–Є—В–Є—П –Њ–±–љ–∞—А—Г–ґ–Є–ї–Њ—Б—М, —З—В–Њ —Н—В–Њ —З–Є—Б–ї–Њ –≤ —В–µ—З–µ–љ–Є–µ 3––є –Є 4––є —З–µ—В–≤–µ—А—В–µ–є –і–љ—П –±—Л–ї–Њ –Љ–µ–љ—М—И–µ —Г –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Є–љ—Б—Г–ї–Є–љ –ї–Є–Ј–њ—А–Њ, —З–µ–Љ —Г —В–µ—Е, –Ї—В–Њ –њ–Њ–ї—Г—З–∞–ї –њ—А–Њ—Б—В–Њ–є —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–є –Є–љ—Б—Г–ї–Є–љ (p<0,001). –°–∞–Љ–Њ–µ –±–Њ–ї—М—И–Њ–µ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –љ–Њ—З—М—О. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —З—В–Њ –Ї—А–∞–є–љ–µ –≤–∞–ґ–љ–Њ, –Є–љ—Б—Г–ї–Є–љ –ї–Є–Ј–њ—А–Њ —Г–ї—Г—З—И–∞–µ—В –Ї–Њ–љ—В—А–Њ–ї—М –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є –Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В —З–Є—Б–ї–Њ —Н–њ–Є–Ј–Њ–і–Њ–≤ –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є, —П–≤–ї—П—П—Б—М –±–Њ–ї–µ–µ —Г–і–Њ–±–љ—Л–Љ –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–Э–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ —В–∞–Ї–ґ–µ, —З—В–Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –Є–љ—К–µ–Ї—Ж–Є–Є –•—Г–Љ–∞–ї–Њ–≥–∞® –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –њ–µ—А–µ–і –њ—А–Є–µ–Љ–Њ–Љ –њ–Є—Й–Є –Є–ї–Є —Б—А–∞–Ј—Г –њ–Њ—Б–ї–µ –µ–і—Л –і–µ–ї–∞–µ—В –µ–≥–Њ –±–Њ–ї–µ–µ –њ—А–Є–≤–ї–µ–Ї–∞—В–µ–ї—М–љ—Л–Љ –Є–Љ–µ–љ–љ–Њ –≤ –і–µ—В—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ, –Ї–Њ–≥–і–∞ —А–µ–ґ–Є–Љ –њ–Є—В–∞–љ–Є—П –Є —Г–≥–ї–µ–≤–Њ–і–љ–∞—П –љ–∞–≥—А—Г–Ј–Ї–∞ –љ–µ–њ–Њ—Б—В–Њ—П–љ–љ—Л.
–Ь—Л –Ј–љ–∞–µ–Љ, —З—В–Њ —Б –њ–Њ–Ј–Є—Ж–Є–Є —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Ї—А–Є—В–µ—А–Є–µ–≤ –Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞ –њ–µ—А–µ–≤–Њ–і –љ–∞ –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є—О –і–ї—П –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Ї–∞–Ї —В–Њ—Й–∞–Ї–Њ–≤–Њ–є, —В–∞–Ї –Є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є —П–≤–ї—П–µ—В—Б—П –Њ–њ—А–∞–≤–і–∞–љ–љ—Л–Љ –њ–Њ–і—Е–Њ–і–Њ–Љ. –Ф–Њ—Б—В–∞—В–Њ—З–љ–Њ —З–∞—Б—В–Њ –љ–µ–≥–∞—В–Є–≤–љ–∞—П —В–Њ—З–Ї–∞ –Ј—А–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞ —Н—В–Њ—В –Љ–µ—В–Њ–і —В–µ—А–∞–њ–Є–Є –Њ—Б–љ–Њ–≤–∞–љ–∞ –љ–∞ –±–Њ—П–Ј–љ–Є –Є–љ—К–µ–Ї—Ж–Є–є, –љ–µ–ґ–µ–ї–∞–љ–Є–Є —В–µ—А—П—В—М –≤—А–µ–Љ—П –љ–∞ –Њ–±—Г—З–µ–љ–Є–µ —В–µ—Е–љ–Є–Ї–µ –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є, –∞ —В–∞–Ї–ґ–µ –љ–∞ —Б—В—А–∞—Е–µ –њ–µ—А–µ–і –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–µ–є –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ –Љ–∞—Б—Б—Л —В–µ–ї–∞. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –њ–µ—А—Б–Њ–љ–∞–ї –њ–Њ–ї–Є–Ї–ї–Є–љ–Є–Ї – –њ–µ—А–≤–Њ–≥–Њ –Ј–≤–µ–љ–∞ –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П – –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –љ–µ –Є–Љ–µ–µ—В –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –≤—А–µ–Љ–µ–љ–Є –Є —А–µ—Б—Г—А—Б–Њ–≤ –і–ї—П –Њ–±—Г—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —В–µ—Е–љ–Є–Ї–µ –Є–љ—К–µ–Ї—Ж–Є–є –Є, —З—В–Њ —Б–∞–Љ–Њ–µ –≤–∞–ґ–љ–Њ–µ, –і–ї—П —В—Й–∞—В–µ–ї—М–љ–Њ–≥–Њ –љ–∞–±–ї—О–і–µ–љ–Є—П –Ј–∞ –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є, –њ–µ—А–µ–≤–µ–і–µ–љ–љ—Л–Љ–Є –љ–∞ –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є—О.
–Ю—З–µ–≤–Є–і–љ–Њ, —З—В–Њ –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї–∞–Ї –њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–≥–Њ, —В–∞–Ї –Є –њ–Њ—Б—В–∞–±—Б–Њ—А–±—Ж–Є–Њ–љ–љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ —Б–Љ–µ—И–∞–љ–љ—Л–µ —Д–Њ—А–Љ—Л –Є–љ—Б—Г–ї–Є–љ–∞, —Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –•—Г–Љ–∞–ї–Њ–≥® —Б –Є–љ—Б—Г–ї–Є–љ–∞–Љ–Є –њ—А–Њ–і–ї–µ–љ–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –Љ–Њ–≥—Г—В —Г–њ—А–Њ—Б—В–Є—В—М —Б–Є—В—Г–∞—Ж–Є—О. –•—Г–Љ–∞–ї–Њ–≥® –Ь–Є–Ї—Б™ 25 –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –≥–Њ—В–Њ–≤—Г—О —Б–Љ–µ—Б—М –Є–Ј 75% –њ—А–Њ—В–∞–Љ–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–є —Б—Г—Б–њ–µ–љ–Ј–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞ –ї–Є–Ј–њ—А–Њ –Є 25% –Є–љ—Б—Г–ї–Є–љ–∞ –ї–Є–Ј–њ—А–Њ. –Я—А–Њ—В–∞–Љ–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –±–∞–Ј–∞–ї—М–љ—Г—О –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М, —В–∞–Ї –Ї–∞–Ї —П–≤–ї—П–µ—В—Б—П –∞–љ–∞–ї–Њ–≥–Њ–Љ –Є–љ—Б—Г–ї–Є–љ–∞ —Б—А–µ–і–љ–µ–є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –і–µ–є—Б—В–≤–Є—П, –∞ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В —Б —Г–ї—М—В—А–∞–Ї–Њ—А–Њ—В–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ—В –Ї–Њ–ї–µ–±–∞–љ–Є—П –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є.
–Я–Њ –∞–љ–∞–ї–Њ–≥–Є–Є —Г–ї—М—В—А–∞–Ї–Њ—А–Њ—В–Ї–Є–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –≤ —Б–Љ–µ—Б–Є –і–µ–є—Б—В–≤—Г–µ—В –≥–Њ—А–∞–Ј–і–Њ –±—Л—Б—В—А–µ–µ –Є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –ї—Г—З—И–Є–є –Ї–Њ–љ—В—А–Њ–ї—М –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–Њ—Б—В—Л–Љ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –≤ —Б–Љ–µ—Б–Є [49], —В–Њ –µ—Б—В—М –њ–Є–Ї –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–є –Є–љ—Б—Г–ї–Є–љ–∞ –њ–ї–∞–Ј–Љ—Л –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –•—Г–Љ–∞–ї–Њ–≥® –Ь–Є–Ї—Б™ 25 –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–є –Є –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –±—Л—Б—В—А–µ–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥–Њ—В–Њ–≤—Л–Љ–Є —Б–Љ–µ—Б—П–Љ–Є —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є—Е –Є–љ—Б—Г–ї–Є–љ–Њ–≤ [50].
–Ґ–∞–Ї –Ї–∞–Ї —Г–ї—М—В—А–∞–Ї–Њ—А–Њ—В–Ї–Є–є –Є–љ—Б—Г–ї–Є–љ –і–µ–є—Б—В–≤—Г–µ—В –±—Л—Б—В—А–µ–µ, —З–µ–Љ –њ—А–Њ—Б—В–Њ–є —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–є –Є–љ—Б—Г–ї–Є–љ, –њ–∞—Ж–Є–µ–љ—В—Л –Љ–Њ–≥—Г—В –њ—А–Є–Љ–µ–љ—П—В—М –Є –≥–Њ—В–Њ–≤—Л–µ —Б–Љ–µ—Б–Є –∞–љ–∞–ї–Њ–≥–Њ–≤ –≤ –Є–љ—В–µ—А–≤–∞–ї–µ 15 –Љ–Є–љ. –і–Њ –љ–∞—З–∞–ї–∞ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є –Є–ї–Є –і–∞–ґ–µ –њ–Њ—Б–ї–µ –µ–і—Л. –Я–Њ–і–Њ–±–љ–∞—П –≥–Є–±–Ї–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Г–ї—Г—З—И–∞–µ—В –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –Є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –≤—Л—Б–Њ–Ї—Г—О –Ї–Њ–Љ–њ–ї–∞–є–µ–љ—В–љ–Њ—Б—В—М [51].
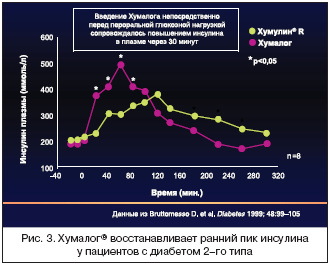
–Ю—Б–љ–Њ–≤—Л–≤–∞—П—Б—М –љ–∞ –і–∞–љ–љ—Л—Е –Њ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Є —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞—Е, –Љ–Њ–ґ–љ–Њ —Б–Ї–∞–Ј–∞—В—М, —З—В–Њ –≥–Њ—В–Њ–≤—Л–µ —Б–Љ–µ—Б–Є –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Л—Е –∞–љ–∞–ї–Њ–≥–Њ–≤ –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –Ї–Њ–љ—В—А–Њ–ї—П –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є, —З–µ–Љ –≥–Њ—В–Њ–≤—Л–µ —Б–Љ–µ—Б–Є —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є—Е –Є–љ—Б—Г–ї–Є–љ–Њ–≤. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф —В–Є–њ–∞ 2 –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Г–ї—М—В—А–∞–Ї–Њ—А–Њ—В–Ї–Є–є –∞–љ–∞–ї–Њ–≥ –Є–љ—Б—Г–ї–Є–љ–∞ –•—Г–Љ–∞–ї–Њ–≥®, –≤—Е–Њ–і—П—Й–Є–є –≤ —Б–Њ—Б—В–∞–≤ —Б–Љ–µ—Б–Є, –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ—А–Њ—В–Ї–Є–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В —А–∞–љ–љ–Є–є –њ–Є–Ї —Б–µ–Ї—А–µ—Ж–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є, —З—В–Њ –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ–Њ –і–ї—П –Ї–Њ–љ—В—А–Њ–ї—П –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є, –Є –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –њ–Њ–і–∞–≤–ї—П–µ—В —Н–љ–і–Њ–≥–µ–љ–љ—Г—О —Б–µ–Ї—А–µ—Ж–Є—О –≥–ї—О–Ї–Њ–Ј—Л –њ–µ—З–µ–љ—М—О (—А–Є—Б. 3 –Є 4).
–Я—А–Є –≤–≤–µ–і–µ–љ–Є–Є –•—Г–Љ–∞–ї–Њ–≥® –Ь–Є–Ї—Б™ 25 –Ј–∞ 5 –Љ–Є–љ. –і–Њ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є —Г—А–Њ–≤–µ–љ—М –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є —Б–љ–Є–ґ–∞–ї—Б—П –љ–∞ 27% –±–Њ–ї—М—И–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ 30/70 –≤ –і–≤–Њ–є–љ–Њ–Љ —Б–ї–µ–њ–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Ї—А–Њ—Б—Б–Њ–≤–µ—А–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б —Г—З–∞—Б—В–Є–µ–Љ 177 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 1 –Є 2 —В–Є–њ–∞ [52]. –Т –і—А—Г–≥–Њ–Љ –Њ—В–Ї—А—Л—В–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Ї—А–Њ—Б—Б–Њ–≤–µ—А–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г 33 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф —В–Є–њ–∞ 2 –љ–∞ —Б—В–∞–љ–і–∞—А—В–љ–Њ–є –Є—В–∞–ї—М—П–љ—Б–Ї–Њ–є –і–Є–µ—В–µ (—Б –њ–Њ–љ–Є–ґ–µ–љ–љ—Л–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ –ґ–Є—А–Њ–≤ –Є —Б –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ —Б–ї–Њ–ґ–љ—Л—Е —Г–≥–ї–µ–≤–Њ–і–Њ–≤) –Є–љ—Б—Г–ї–Є–љ –•—Г–Љ–∞–ї–Њ–≥® –Ь–Є–Ї—Б™ 25 –њ—А–Є–Љ–µ–љ—П–ї—Б—П –Ј–∞ 5 –Љ–Є–љ. –і–Њ —Г—В—А–µ–љ–љ–µ–є –Є –≤–µ—З–µ—А–љ–µ–є –µ–і—Л, –∞ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–є –Є–љ—Б—Г–ї–Є–љ 30/70 – –Ј–∞ 30 –Љ–Є–љ. –і–Њ –њ—А–Є–µ–Љ–Њ–≤ –њ–Є—Й–Є. –Т —В–µ—З–µ–љ–Є–µ 12 –і–љ–µ–є –ї–µ—З–µ–љ–Є—П –Ї–Њ–ї–µ–±–∞–љ–Є—П –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –њ–Њ—Б–ї–µ —Г–ґ–Є–љ–∞ —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–Љ–µ–љ—П–≤—И–Є—Е –•—Г–Љ–∞–ї–Њ–≥® –Ь–Є–Ї—Б™ 25, –±—Л–ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–Є–ґ–µ, —З–µ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–Љ–µ–љ—П–≤—И–Є—Е —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–є –Є–љ—Б—Г–ї–Є–љ 30/70 (—А–∞–Ј–љ–Є—Ж–∞ –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є – 66%, p<0,05) [53].
–Ш–љ—В–µ—А–µ—Б–љ—Л –і–∞–љ–љ—Л–µ, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –≤ –Њ—В–Ї—А—Л—В–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Ї—А–Њ—Б—Б–Њ–≤–µ—А–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є–љ—Б—Г–ї–Є–љ–∞ –•—Г–Љ–∞–ї–Њ–≥® –Ь–Є–Ї—Б™ 25 –Є —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ 30/70 —Г 151 –њ–∞—Ж–Є–µ–љ—В–∞ —Б –°–Ф 2 —В–Є–њ–∞, –Ї–Њ—В–Њ—А—Л–µ —Б–Њ–±–ї—О–і–∞–ї–Є –њ–Њ—Б—В –≤–Њ –≤—А–µ–Љ—П –†–∞–Љ–∞–і–∞–љ–∞ –Є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –љ–µ –њ—А–Є–љ–Є–Љ–∞–ї–Є –њ–Є—Й—Г –≤ —В–µ—З–µ–љ–Є–µ –і–љ—П. –Э–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 14 –і–љ–µ–є —Б–Љ–µ—Б—М –њ—А–Є–Љ–µ–љ—П–ї–∞—Б—М —Б—А–∞–Ј—Г –њ–µ—А–µ–і —Г—В—А–µ–љ–љ–Є–Љ –Є –≤–µ—З–µ—А–љ–Є–Љ –њ—А–Є–µ–Љ–Њ–Љ –њ–Є—Й–Є, —В–Њ–≥–і–∞ –Ї–∞–Ї –њ–∞—Ж–Є–µ–љ—В—Л, –њ—А–Є–Љ–µ–љ—П–≤—И–Є–µ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–є –Є–љ—Б—Г–ї–Є–љ 30/70, —Б—В–∞–љ–і–∞—А—В–љ–Њ –і–µ–ї–∞–ї–Є —Н—В–Њ –Ј–∞ 30–40 –Љ–Є–љ. –і–Њ –µ–і—Л. –Я–Њ—Б–ї–µ –Њ—Ж–µ–љ–Ї–Є –≥–ї–Є–Ї–µ–Љ–Є–Є –≤ —В–µ—З–µ–љ–Є–µ —Б—Г—В–Њ–Ї –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є–µ –Њ–±—Й–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –≥–ї–Є–Ї–µ–Љ–Є–Є (–5,9%, p=0,004) –Є –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –≥–ї–Є–Ї–µ–Љ–Є–Є –њ–µ—А–µ–і –≤–µ—З–µ—А–љ–Є–Љ –њ—А–Є–µ–Љ–Њ–Љ –њ–Є—Й–Є (–5,5%; p=0,034) –±—Л–ї–Є –≤ –≥—А—Г–њ–њ–µ –•—Г–Љ–∞–ї–Њ–≥® –Ь–Є–Ї—Б™ 25 –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–Љ–µ–љ—П–ї–Є —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–є –Є–љ—Б—Г–ї–Є–љ 30/70. –Ф–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є–µ –Ї–Њ–ї–µ–±–∞–љ–Є—П –≥–ї–Є–Ї–µ–Љ–Є–Є –њ–Њ—Б–ї–µ –≤–µ—З–µ—А–љ–µ–≥–Њ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є —В–∞–Ї–ґ–µ –±—Л–ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–Љ–µ–љ—П–≤—И–Є—Е –Є–љ—Б—Г–ї–Є–љ –•—Г–Љ–∞–ї–Њ–≥® –Ь–Є–Ї—Б™ 25 (–15%; p=0,007). –£—В—А–µ–љ–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –≥–ї–Є–Ї–µ–Љ–Є–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ –Њ—В–ї–Є—З–∞–ї–Є—Б—М [54].
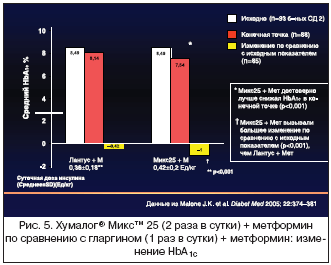
–Т 32––љ–µ–і–µ–ї—М–љ–Њ–Љ (–њ–Њ 16 –љ–µ–і–µ–ї—М –љ–∞ –Ї–∞–ґ–і—Л–є –њ–µ—А–Є–Њ–і) —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Њ—В–Ї—А—Л—В–Њ–Љ –Ї—А–Њ—Б—Б–Њ–≤–µ—А–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б —Г—З–∞—Б—В–Є–µ–Љ 105 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞, –Ї–Њ—В–Њ—А—Л–µ –љ–∞—З–∞–ї–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–љ—Б—Г–ї–Є–љ–∞, –љ–Њ –њ—А–Њ–і–Њ–ї–ґ–∞–ї–Є –њ—А–Є–µ–Љ –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞, 42% –Є–Ј –≥—А—Г–њ–њ—Л –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Б–Љ–µ—Б—М –•—Г–Љ–∞–ї–Њ–≥® –Ь–Є–Ї—Б™ 25 –і–≤–∞–ґ–і—Л –≤ —Б—Г—В–Ї–Є –і–Њ—Б—В–Є–≥–∞–ї–Є HbA1c<7% –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 18% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є –Є–љ—Б—Г–ї–Є–љ –≥–ї–∞—А–≥–Є–љ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ (—А<0,001). –Ъ–Њ–ї–µ–±–∞–љ–Є—П –Я–Я–У –њ–Њ—Б–ї–µ –Ј–∞–≤—В—А–∞–Ї–∞ –Є —Г–ґ–Є–љ–∞ –±—Л–ї–Є –љ–∞ 65% –Є 70% –љ–Є–ґ–µ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –•—Г–Љ–∞–ї–Њ–≥® –Ь–Є–Ї—Б™ 25 –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –≥–ї–∞—А–≥–Є–љ (—А<0,005), —А–∞–Ј–ї–Є—З–Є–є –њ–Њ—Б–ї–µ –Њ–±–µ–і–∞ –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ. –І–∞—Б—В–Њ—В–∞ –ї–µ–≥–Ї–Є—Е –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є –±—Л–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞ –•—Г–Љ–∞–ї–Њ–≥® –Ь–Є–Ї—Б™ 25, —З–µ–Љ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞ –≥–ї–∞—А–≥–Є–љ (—А=0,041) [55]. –Ф—А—Г–≥–Њ–µ 32––љ–µ–і–µ–ї—М–љ–Њ–µ –Њ—В–Ї—А—Л—В–Њ–µ –Ї—А–Њ—Б—Б–Њ–≤–µ—А–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б —Г—З–∞—Б—В–Є–µ–Љ 97 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г—О—Й–Є—Е—Б—П –љ–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Њ–і–љ–Њ– –Є–ї–Є –і–≤—Г–Ї—А–∞—В–љ–Њ–≥–Њ —А–µ–ґ–Є–Љ–∞ –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є (–≤ –≤–Є–і–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Є–ї–Є –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –Я–°–Я), –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –Є–љ—Б—Г–ї–Є–љ –•—Г–Љ–∞–ї–Њ–≥® –Ь–Є–Ї—Б™ 25 —Б–љ–Є–ґ–∞–µ—В HbA1c –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ –љ–∞ 0,6% –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –≥–ї–∞—А–≥–Є–љ, –њ—А–Є–Љ–µ–љ—П–≤—И–Є–Љ—Б—П –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ (—А<0,001). –Т –Њ–±—Й–µ–Љ –Є —Ж–µ–ї–Њ–Љ –Ї–Њ–ї–µ–±–∞–љ–Є—П –≥–ї–Є–Ї–µ–Љ–Є–Є –±—Л–ї–Є –љ–∞ 25% –љ–Є–ґ–µ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞ –•—Г–Љ–∞–ї–Њ–≥® –Ь–Є–Ї—Б™ 25 (—А<0,001), –љ–Њ –Њ–±—Й–∞—П —З–∞—Б—В–Њ—В–∞ –ї–µ–≥–Ї–Є—Е –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ –Њ—В–ї–Є—З–∞–ї–∞—Б—М –Љ–µ–ґ–і—Г –ї–µ—З–µ–±–љ—Л–Љ–Є —А–µ–ґ–Є–Љ–∞–Љ–Є (0,61 –њ—А–Њ—В–Є–≤ 0,44 —Н–њ–Є–Ј–Њ–і–∞ –љ–∞ –њ–∞—Ж–Є–µ–љ—В–∞ –Ј–∞ 30 –і–љ–µ–є; —А=NS) [56]. –≠–њ–Є–Ј–Њ–і–Њ–≤ —В—П–ґ–µ–ї–Њ–є –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є –љ–µ –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–Њ –љ–Є –≤ –Њ–і–љ–Њ–Љ, –љ–Є –≤ –і—А—Г–≥–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [55,56] (—А–Є—Б. 5 –Є 6).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –•—Г–Љ–∞–ї–Њ–≥® –≤ —Б–Њ—Б—В–∞–≤–µ —Б–Љ–µ—Б–Є –•—Г–Љ–∞–ї–Њ–≥®a –Ь–Є–Ї—Бa™ 25 –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–Њ–≤–Њ–і–Є—В—М –Ї–Њ—А—А–µ–Ї—Ж–Є—О –Я–Я–У –±–Њ–ї–µ–µ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–љ–Њ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ—А–Њ—В–Ї–Є–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ, –≤—Е–Њ–і—П—Й–Є–Љ –≤ —Б–Њ—Б—В–∞–≤ –њ—А–Њ—Б—В–Њ–є —Б–Љ–µ—Б–Є 30/70.
–Т–Њ –≤—Б–µ—Е –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –≥–Њ—В–Њ–≤—Л–µ —Б–Љ–µ—Б–Є –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Л—Е –∞–љ–∞–ї–Њ–≥–Њ–≤ –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –і–≤–∞–ґ–і—Л –≤ –і–µ–љ—М – –њ–µ—А–µ–і —Г—В—А–µ–љ–љ–Є–Љ –Є –≤–µ—З–µ—А–љ–Є–Љ –њ—А–Є–µ–Љ–Њ–Љ –њ–Є—Й–Є –Ј–∞ 0–15 –Љ–Є–љ. –і–Њ –µ–і—Л. –≠—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–ї–Њ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є–љ—Б—Г–ї–Є–љ–∞ –і–ї—П —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–µ–љ–Є—П –±–∞–Ј–∞–ї—М–љ–Њ–є –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є –Є –њ–Њ–Ї—А—Л—В–Є—П –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ—Л—Е –Ї–Њ–ї–µ–±–∞–љ–Є–є –≥–ї–Є–Ї–µ–Љ–Є–Є –њ–Њ—Б–ї–µ –Ј–∞–≤—В—А–∞–Ї–∞ –Є —Г–ґ–Є–љ–∞, –Ї–Њ—В–Њ—А—Л–µ —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ —П–≤–ї—П—О—В—Б—П —Б–∞–Љ—Л–Љ–Є –±–Њ–ї—М—И–Є–Љ–Є –њ—А–Є–µ–Љ–∞–Љ–Є –њ–Є—Й–Є. –Ю–і–љ–Њ–Ї—А–∞—В–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≥–Њ—В–Њ–≤—Л—Е —Б–Љ–µ—Б–µ–є –∞–љ–∞–ї–Њ–≥–Њ–≤ –Є–љ—Б—Г–ї–Є–љ–∞ —В–∞–Ї–ґ–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –Ї–∞–Ї —Б—В–∞—А—В–Њ–≤—Л–є —А–µ–ґ–Є–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –≤ –љ–∞—З–∞–ї–µ –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є. –Я—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –і–ї—П –њ–Њ–Ї—А—Л—В–Є—П –Ї–Њ–ї–µ–±–∞–љ–Є–є –≥–ї–Є–Ї–µ–Љ–Є–Є –≤ –Њ–±–µ–і–µ–љ–љ–Њ–µ –≤—А–µ–Љ—П –Љ–Њ–≥—Г—В –±—Л—В—М –і–Њ–±–∞–≤–ї–µ–љ—Л –Є–ї–Є –±—Л—Б—В—А–Њ–і–µ–є—Б—В–≤—Г—О—Й–Є–µ —Б–µ–Ї—А–µ—В–∞–≥–Њ–≥–Є, –Є–ї–Є –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Л–µ –∞–љ–∞–ї–Њ–≥–Є —Г–ї—М—В—А–∞–Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –Є–ї–Є —В—А–µ—В—М—П –Є–љ—К–µ–Ї—Ж–Є—П —Б–Љ–µ—И–∞–љ–љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞. –Я–Њ—Б–ї–µ–і–љ–Є–є —А–µ–ґ–Є–Љ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ –њ—А–Є–±–ї–Є–ґ–∞–µ—В –ї–µ—З–µ–љ–Є–µ –Ї –±–∞–Ј–Є—Б–љ–Њ––±–Њ–ї—О—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–Ъ–∞–Ї –Є –њ—А–Є –ї—О–±–Њ–Љ —А–µ–ґ–Є–Љ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–љ—Б—Г–ї–Є–љ–∞, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—Б—В–∞–љ–Њ–≤–Є—В—М –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Л–µ —Ж–µ–ї–Є –≥–ї–Є–Ї–µ–Љ–Є–Є –і–ї—П –Ї–∞–ґ–і–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ –≤–Њ –Є–Ј–±–µ–ґ–∞–љ–Є–µ –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є –Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є—А–Њ—Б—В–∞ –Љ–∞—Б—Б—Л —В–µ–ї–∞.
–° —Ж–µ–ї—М—О –њ–Њ–і–±–Њ—А–∞ –і–Њ–Ј—Л –Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –Љ–µ—В–Њ–і–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Б–Љ–µ—И–∞–љ–љ—Л—Е –Є–љ—Б—Г–ї–Є–љ–Њ–≤ 30/70. –°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ —Д–µ–і–µ—А–∞–ї—М–љ–Њ–є —Ж–µ–ї–µ–≤–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ—Л «–°–∞—Е–∞—А–љ—Л–є –Ф–Є–∞–±–µ—В», –љ–∞—З–∞–ї—М–љ–Њ–є –і–Њ–Ј–Њ–є –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ 12 –Ь–Х –њ–µ—А–µ–і –Ј–∞–≤—В—А–∞–Ї–Њ–Љ –Є 8 –Ь–Х –њ–µ—А–µ–і —Г–ґ–Є–љ–Њ–Љ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–µ–є –і–Њ–Ј—Л —З–µ—А–µ–Ј 2–3 –і–љ—П (–њ–Њ 2 –Є–ї–Є 4 –Ь–Х) –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —Б–∞–Љ–Њ–Ї–Њ–љ—В—А–Њ–ї—П –і–Њ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ—Л—Е –і–ї—П –і–∞–љ–љ–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ —Ж–µ–ї–µ–≤—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤.
–•–Њ—З–µ—В—Б—П –∞–Ї—Ж–µ–љ—В–Є—А–Њ–≤–∞—В—М –≤–љ–Є–Љ–∞–љ–Є–µ –љ–∞ —В–Њ–Љ, —З—В–Њ —Б —В–µ—З–µ–љ–Є–µ–Љ –≤—А–µ–Љ–µ–љ–Є –Љ–Њ–ґ–µ—В –њ–Њ—В—А–µ–±–Њ–≤–∞—В—М—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л –Є–љ—Б—Г–ї–Є–љ–∞, —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–Є–Љ —В–µ—З–µ–љ–Є–µ–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –∞ –љ–µ —В–µ–Љ, —З—В–Њ –њ–∞—Ж–Є–µ–љ—В –љ–µ —Б—В—А–Њ–≥–Њ –њ—А–Є–і–µ—А–ґ–Є–≤–∞–ї—Б—П –ї–µ—З–µ–љ–Є—П.
–Т –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Б–Ї–∞–Ј–∞—В—М, —З—В–Њ —А–∞–Ј—А–∞–±–Њ—В–Ї–∞ –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Л—Е –∞–љ–∞–ї–Њ–≥–Њ–≤ —Г–ї—М—В—А–∞–Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –њ–Њ–Ј–≤–Њ–ї–Є–ї–∞ –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є —Б—В–∞—В—М –±–Њ–ї–µ–µ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–љ–Њ–є. –Ъ–∞–Ї –±–∞–Ј–∞–ї—М–љ–∞—П, —В–∞–Ї –Є –њ—А–∞–љ–і–Є–∞–ї—М–љ–∞—П –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –Є–љ—Б—Г–ї–Є–љ–µ –Љ–Њ–≥—Г—В –±—Л—В—М –њ–Њ–ї–љ–Њ—Б—В—М—О –њ–Њ–Ї—А—Л—В—Л –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –Њ–і–љ–Њ–є –Є–љ—К–µ–Ї—Ж–Є–Є –≥–Њ—В–Њ–≤–Њ–є —Б–Љ–µ—Б–Є –Є–љ—Б—Г–ї–Є–љ–Њ–≤–Њ–≥–Њ –∞–љ–∞–ї–Њ–≥–∞, —З—В–Њ –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б–ї—Г—З–∞—П—Е –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–њ—А–Њ—Й–∞–µ—В –њ—А–∞–Ї—В–Є—З–µ—Б–Ї—Г—О —А–µ–∞–ї–Є–Ј–∞—Ж–Є—О –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –Є–љ—Б—Г–ї–Є–љ–∞ –ї–Є–Ј–њ—А–Њ (–•—Г–Љ–∞–ї–Њ–≥®) –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ –µ–≥–Њ –њ–Њ—П–≤–ї–µ–љ–Є–µ –Љ–Њ–ґ–љ–Њ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М –Ї–∞–Ї —И–∞–≥ –≤–њ–µ—А–µ–і –≤ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–Є –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є –Є –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –≥–ї–Є–Ї–µ–Љ–Є–Є.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Diabetes Atlas, 3rd edition. International Diabetes Federation, 2006.
2. Niskanen L, Turpeinen A, Penttila I, Uusitupa MI. Hyperglycemia and compositional lipoprotein abnormalities as predictors of cardiovascular mortality in type 2 diabetes: a 15–year follow–up from the time of diagnosis. Diabetes Care 1998; 21(11):1861–1869.
3. Stettler (14) Diabetes Control and Complications Trial (DCCT) Research Group. The absence of a glycemic threshold for the development of longterm complications: the perspective of the Diabetes Control and Complications Trial. Diabetes 1996; 45(10):1289–1298.
4. Nathan DM, Buse JB, Davidson MB, Heine RJ, Holman RR, Sherwin R et al. Management of Hyperglycemia in Type 2 Diabetes: A Consensus Algorithm for the Initiation and Adjustment of Therapy: A consensus statement from the American Diabetes Association and the European Association for the Study of Diabetes. Diabetes Care 2006; 29(8):1963–1972.
5. Sorkin JD, Muller DC, Fleg JL, Andres R. The relation of fasting and 2–h postchallenge plasma glucose concentrations to mortality: data from the Baltimore Longitudinal Study of Aging with a critical review of the literature. Diabetes Care 2005; 28(11):2626–2632.
6. Ohkubo Y, Kishikawa H, Araki E, Miyata T, Isami S, Motoyoshi S et al. Intensive insulin therapy prevents the progression of diabetic microvascular complications in Japanese patients with non–insulin–dependent diabetes mellitus: a randomized prospective 6–year study. Diabetes Res Clin Pract 1995; 28(2):103–117.
7. Shiraiwa T, Kaneto H, Miyatsuka T, Kato K, Yamamoto K, Kawashima A et al. Post–prandial
hyperglycemia is an important predictor of the incidence of diabetic microangiopathy in Japanese type 2 diabetic patients. Biochem Biophys Res Commun 2005; 336(1):339–345.
8. Levitan EB, Song Y, Ford ES, Liu S. Is nondiabetic hyperglycemia a risk factor for
cardiovascular disease? A meta–analysis of prospective studies. Arch Intern Med 2004; 164(19):2147–2155.
9. Hanefeld M, Cagatay M, Petrowitsch T, Neuser D, Petzinna D, Rupp M. Acarbose reduces
the risk for myocardial infarction in type 2 diabetic patients: meta–analysis of seven long–term studies. Eur Heart J 2004; 25(1):10–16.
10. Woerle HJ, Neumann C, Zschau S, Tenner S, Irsigler A, Schirra J et al. Impact of fasting and
postprandial glycemia on overall glycemic control in type 2 diabetes Importance of postprandial glycemia to achieve target HbA1c levels. Diabetes Res Clin Pract 2007.
11. Hanefeld M, Koehler C, Schaper F, Fuecker K, Henkel E, Temelkova–Kurktschiev T. Postprandial plasma glucose is an independent risk factor for increased carotid intima–media thickness in non–diabetic individuals. Atherosclerosis 1999; 144(1):229–235.
12. Gapstur SM, Gann PH, Lowe W, Liu K, Colangelo L, Dyer A. Abnormal glucose metabolism and pancreatic cancer mortality. JAMA 2000; 283(19):2552–2558.
13. Larsson SC, Bergkvist L, Wolk A. Consumption of sugar and sugar–sweetened foods and the risk of pancreatic cancer in a prospective study. Am J Clin Nutr 2006; 84(5):1171–1176.
14. Michaud DS, Liu S, Giovannucci E, Willett WC, Colditz GA, Fuchs CS. Dietary sugar, glycemic load, and pancreatic cancer risk in a prospective study. J Natl Cancer Inst 2002; 94(17):1293–1300.
15. Michaud DS, Fuchs CS, Liu S, Willett WC, Colditz GA, Giovannucci E. Dietary glycemic load, carbohydrate, sugar, and colorectal cancer risk in men and women. Cancer Epidemiol Biomarkers Prev 2005; 14(1):138–147.
16. Lajous M, Willett W, Lazcano–Ponce E, Sanchez–Zamorano LM, Hernandez–Avila M, Romieu I. Glycemic load, glycemic index, and the risk of breast cancer among Mexican women. Cancer Causes Control 2005; 16(10):1165–1169.
17. Abbatecola AM, Rizzo MR, Barbieri M, Grella R, Arciello A, Laieta MT et al. Postprandial plasma glucose excursions and cognitive functioning in aged type 2 diabetics. Neurology 2006; 67(2):235–240.
18. Ceriello A, Quagliaro L, Piconi L, Assaloni R, Da RR, Maier A et al. Effect of postprandial hypertriglyceridemia and hyperglycemia on circulating adhesion molecules and oxidative stress generation and the possible role of simvastatin treatment. Diabetes 2004; 53(3):701–710.
19. Williams SB, Goldfine AB, Timimi FK, Ting HH, Roddy MA, Simonson DC et al. Acute hyperglycemia attenuates endothelium–dependent vasodilation in humans in vivo. Circulation 1998; 97(17):1695–1701.
20. Kawano H, Motoyama T, Hirashima O, Hirai N, Miyao Y, Sakamoto T et al. Hyperglycemia rapidly suppresses flow–mediated endothelium–dependent vasodilation of brachial artery. J Am Coll Cardiol 1999; 34(1):146–154.
21. Diabetes Control and Complications Trial (DCCT) Research Group. The absence of a glycemic threshold for the development of longterm complications: the perspective of the Diabetes Control and Complications Trial. Diabetes 1996; 45(10):1289–1298.
22. Stratton IM, Adler AI, Neil HA, Matthews DR, Manley SE, Cull CA et al. Association of glycaemia with macrovascular and microvascular complications of type 2 diabetes (UKPDS 35): prospective observational study. BMJ 2000; 321(7258):405–412.
23. Erlinger TP, Brancati FL. Postchallenge hyperglycemia in a national sample of U.S. adults with type 2 diabetes. Diabetes Care 2001; 24(10):1734–1738.
24. Bonora E, Corrao G, Bagnardi V, Ceriello A, Comaschi M, Montanari P et al. Prevalence and correlates of post–prandial hyperglycaemia in a large sample of patients with type 2 diabetes mellitus. Diabetologia 2006; 49(5):846–854.
25. Akbar DH. Sub–optimal postprandial blood glucose level in diabetics attending the outpatient clinic of a University Hospital. Saudi Med J 2003; 24(10):1109–1112.
26. Bonora E, Corrao G, Bagnardi V, Ceriello A, Comaschi M, Montanari P et al. Prevalence and correlates of post–prandial hyperglycaemia in a large sample of patients with type 2 diabetes mellitus. Diabetologia 2006; 49(5):846–854.
27. Ceriello A, Quagliaro L, Catone B, Pascon R, Piazzola M, Bais B et al. Role of hyperglycemia in nitrotyrosine postprandial generation. Diabetes Care 2002; 25(8):1439–1443.
28. Beisswenger PJ, Howell SK, O’Dell RM, Wood ME, Touchette AD, Szwergold BS. alpha–dicarbonyls increase in the postprandial period and reflect the degree of hyperglycemia. Diabetes Care 2001; 24(4):726–732.
29. Scognamiglio R, Negut C, De Kreutzenberg SV, Tiengo A, Avogaro A. Effects of different insulin regimes on postprandial myocardial perfusion defects in type 2 diabetic patients. Diabetes Care 2006; 29(1):95–100.
30. Ohkubo Y, Kishikawa H, Araki E, Miyata T, Isami S, Motoyoshi S et al. Intensive insulin therapy prevents the progression of diabetic microvascular complications in Japanese patients with non–insulin–dependent diabetes mellitus: a randomized prospective 6–year study. Diabetes Res Clin Pract 1995; 28(2):103–117.
31. Monnier L, Lapinski H, Colette C. Contributions of fasting and postprandial plasma glucose increments to the overall diurnal hyperglycemia of type 2 diabetic patients: variations with increasing levels of HbA(1c). Diabetes Care 2003; 26(3):881–885.
32. Monnier L, Colette C, Dunseath GJ, Owens DR. The loss of postprandial glycemic control precedes stepwise deterioration of fasting with worsening diabetes. Diabetes Care 2007; 30(2):263–269.
33. Woerle HJ, Neumann C, Zschau S, Tenner S, Irsigler A, Schirra J et al. Impact of fasting and postprandial glycemia on overall glycemic control in type 2 diabetes Importance of postprandial glycemia to achieve target HbA1c levels. Diabetes Res Clin Pract 2007.
34. Riddle MC, Rosenstock J, Gerich J. The treat–to–target trial: randomized addition of glargine or human NPH insulin to oral therapy of type 2 diabetic patients. Diabetes Care 2003; 26(11):3080–3086.
35. Bastyr EJ, III, Stuart CA, Brodows RG, Schwartz S, Graf CJ, Zagar A et al. Therapy focused on lowering postprandial glucose, not fasting glucose, may be superior for lowering HbA1c. IOEZ Study Group. Diabetes Care 2000; 23(9):1236–1241.
36. Woerle HJ, Neumann C, Zschau S, Tenner S, Irsigler A, Schirra J et al. Impact of fasting and postprandial glycemia on overall glycemic control in type 2 diabetes Importance of postprandial glycemia to achieve target HbA1c levels. Diabetes Res Clin Pract 2007.
37. Halimi S, Raskin P, Liebl A, Kawamori R, Fulcher G, Yan G. Efficacy of biphasic insulin aspart in patients with type 2 diabetes. Clin Ther 2005; 27 Suppl 2:S57–S74.
38. Kazda C, Hulstrunk H, Helsberg K, Langer F, Forst T, Hanefeld M. Prandial insulin substitution with insulin lispro or insulin lispro mid mixture vs. basal therapy with insulin glargine: a randomized controlled trial in patients with type 2 diabetes beginning insulin
therapy. J Diabetes Complications 2006; 20(3):145–152.
39. Schernthaner G, Kopp HP, Ristic S, Muzyka B, Peter L, Mitteregger G. Metabolic control in patients with type 2 diabetes using Humalog Mix50 injected three times daily: crossover comparison with human insulin 30/70. Horm Metab Res 2004;
36(3):188–193.
40. Roach P, Malone JK. Comparison of insulin lispro mixture 25/75 with insulin glargine during a 24–h standardized test–meal period in patients with Type 2
diabetes. Diabet Med 2006; 23(7):743–749.
41. Anderson J. et al.Reduction of postprandial hyperglycemia and frequency of hypoglycemia in IDDM patients on insulin–analog treatment. Multicenter Insulin Lispro Study Group Diabetes 46: 265–270
42.Fineberg SE, Fineberg NS, Anderson J.H., Birkett M:Insulin immune response to lispro human insulin therapy in insulin naive type I and type II patients (Abstract.) Diabetologia 38 (Suppl.1):A4,1995
43. Buelke–Sam J, Byrd RA, Hayt JA, Zimmerman JL: A reproductive and developmental toxicity study in CD rats of LY275585, (Lys(B28),Pro(B29)) human insulin. J Am Coll Toxicol 13:247–260, 1994
44. Slieker LJ, Brooke GS, Chance RE, Fan L, Hoffmann JA, Howey DC, Long HB, Mayer J, Shields JE, Sundell KL, DiMarshi RD: Insulin and IGF–1 analogs: novel approach to improved insulin pharmacokinetics. In Current Directions in Insulin–like Growth Factors Research. LeRoith D, Raizada MK, eds. New York, Plenum Press, 1994, p.25–32
45. The DCCT Research Group: Adverse events and their accosiation with treatment
regimens in the Diabetes Control and Complications Trial. Diabetes Care
18:1415–1427, 1995
46. The DCCT Research Group: Epidemiology of severe hypoglycemia in the
Diabetes Control and Complications Trial. Am J Med 90:450–459,1991
47. Pramming S, Thorsteinsson B, Bendtson I, Binder C: The relationship between
symptomatic and biochemical hypoglycemia in insulin–dependent diabetic
patients. J Int Med 228:641–646, 1990
48. Anderson J. et al.Reduction of postprandial hyperglycemia and frequency of hypoglycemia in IDDM patients on insulin–analog treatment. Multicenter Insulin Lispro Study Group Diabetes 46: 265–270
49. Rolla AR. Insulin analog mixes in the management of type 2 diabetes mellitus. Pract Diabetol. 2002;21:36–43.
50. DeWitt DE, Dugdale DC. Using new insulin strategies in the outpatient treatment of diabetes: Clinical applications.JAMA.2003;289:2265–2269.
51. Owens DR, Zinman B, Bolli GB. Insulins today and beyond [published correction appears in Lancet. 2001;358:1374]. Lancet. 2001;358: 739–746.
52. MaloneJK, Yang H, WoodworthJR, et al. Humalog Mix25 offers better mealtime glycemic control in patients with type 1 or type 2 diabetes. Diabetes Metab.2000;26:481–487.
53. Coscelli C, lacobellis G, Calderini C, et al. Importance of premeal injection time in insulin therapy: Humalog Mix25 is convenient for improved post–prandial glycemic control in type 2 diabetic patients with Italian dietary habits. Acta Diabetol. 2003; 40:187–192.
54. Mattoo V, Milicevic Z, MaloneJK, et al, for the Ramadan Study Group. A comparison of insulin lispro Mix25 and human insulin 30/70 in the treatment of type 2 diabetes during Ramadan. Diabetes Res C/in Pract. 2003;59:137–143.
55. MaloneJK, Kerr LF, Campaigne BN, et al, for the Lispro Mixture–Glargine Study Group. Combined therapy with insulin lispro Mix 75/25 plus metformin or insulin glargine plus metformin: A 16–week, randomized, open–label, crossover study in patients with type 2 diabetes beginning insulin therapy. Clin Ther. 2004;26: 2034–2044.
56. MaloneJK, Bai S, Campaigne BN, et al. Twice–daily pre–mixed insulin rather than basal insulin therapy alone results in better overall glycaemic control in patients with type 2 diabetes. Diabet Med. 2005;22:374–381.












