С другой стороны, непрерывный длительный мониторинг гликемии с использованием прибора CGMSOGold (Continuous Glucose Monitoring SystemO Gold, производства «Медтроник», США) и данные дневника самоконтроля обеспечивают наиболее полную информацию о направлении, величине, продолжительности, частоте и причинах изменений глюкозы в крови в течение суток, позволяя, таким образом, более адекватно оценивать степень компенсации углеводного обмена больных СД и рационально корректировать терапию [1] (рис. 1).
Система состоит из трех основных частей: чувствительного сенсора (рис. 2), монитора (рис. 3) и устройства передачи данных на персональный компьютер (рис. 4).
Сенсор представляет собой тонкий и гибкий стерильный платиновый электрод, который практически безболезненно устанавливается пациенту подкожно при помощи автоматического устройства в амбулаторных условиях (рис. 5).
Принцип работы сенсора основан на глюкозооксидазном методе (рис. 6). Фермент глюкозооксидаза используется для того, чтобы конвертировать глюкозу на поверхности датчика в электронные сигналы. Последняя под воздействием фермента (на сенсоре) превращается в глюконовую кислоту с выделением двух электронов. Электроны образуют электрический потенциал, который фиксируется электродом и передается на монитор через кабель. Чем выше содержание глюкозы в интерстициальной жидкости, тем больше появляется электронов, тем выше электрический потенциал.
Монитор производит выборку сигналов каждые 10 секунд и делает запись среднего сигнала каждые 5 минут. Устройство монитора позволяет фиксировать факты приема пищи, приема лекарственных средств, эпизоды физических нагрузок и др. После окончания исследования полученные данные загружаются в персональный компьютер и обрабатываются с помощью специальной программы. Результаты измерений после компьютерной обработки могут быть представлены как в виде цифровых данных (288 измерений в сутки с указанием времени, границ колебания и средних значений уровня гликемии, а также уровня гликемии за день и за трое суток), так и в виде графиков, на которых отмечены колебания уровня гликемии за время исследования.
О необходимости проведения непрерывного длительного мониторинга гликемии для оценки контроля углеводного обмена у больных СД убедительно свидетельствуют результаты исследования, проведенного Bruce W. Bode с соавт. [2]. В нем принимал участие 101 пациент, причем каждый участник прошел мониторинг глюкозы в среднем в течение 12 дней. Полученная в конечном итоге информация стала беспрецедентной по количеству данных непрерывного мониторинга в опубликованной литературе на сегодняшний день. Это исследование уникально тем, что пациенты не были осведомлены о данных измерений глюкозы, полученных с помощью устройства в течение периода наблюдения, и тем самым эти данные были лишены влияния терапевтических вмешательств. Авторы представили результаты пациентов с интенсивным управлением и контролем диабета, проводивших самоконтроль в среднем 9 раз в сутки.
Шокирующим открытием стал тот факт, что пациенты, использующие столь частые измерения гликемии и имеющие широкий спектр терапевтических возможностей, находились в эугликемическом диапазоне всего около 65% времени в сутки, а временной интервал, в течение которого они достигали строгого гликемического контроля (по критериям Американской диабетической ассоциации), составлял менее 30% в сутки. Это свидетельствует о том, что существующие методы мониторинга и терапии диабета недостаточны для ежедневного поддержания нормогликемии. Почти 30% времени пациенты находились в гипергликемическом диапазоне с более выраженной тенденцией к гипергликемии в дневные часы, что, вероятно, было обусловлено вкладом постпрандиальной гипергликемии. В предыдущих исследованиях, использовавших длительный непрерывный мониторинг глюкозы, также были отмечены характерные эпизоды явной постпрандиальной гипергликемии, несмотря на успешные препрандиальные уровни, значения которых были внутри или около целевого диапазона [2,3]. Этот феномен, к сожалению, ранее недооценивался при использовании традиционного мониторинга гликемии [4]. Кроме того, были получены данные о периодах гипогликемии, на которые приходилось около 8% времени. Этот результат подтверждали предыдущие исследования, оценивавшие распространенность гипогликемии [2]. Важно, что периоды низкого сахара крови чаще имели место в ночное время. Столь частые гипогликемические эпизоды ранее редко определялись стандартными средствами самоконтроля уровня сахара в крови.
Важно отметить, что даже при частоте контроля 8–10 раз в сутки могут не регистрироваться бессимптомные ночные гипогликемии, а также максимальный подъем гликемии после еды. Становится понятно, что отдельные результаты не обеспечивают понимания частоты, интенсивности и продолжительности суточных колебаний гликемии [2] (рис. 1).
Хорошо известно, что отрицательное воздействие на организм человека создают как острые подъемы (постпрандиальные), так и острые снижения (межпрандиальные) уровня глюкозы крови относительно средних значений. Это наблюдение, вероятно, могло бы объяснить некоторые данные, полученные в ходе Американского исследования по изучению контроля диабета и его осложнений Diabetes Control and Complications Trial (DCCT). Например, в подгруппах пациентов с сохранявшимся в течение всего исследования HbA1c на уровне 9% риск ретинопатии снижался более чем на 50% в группе интенсивного контроля, по сравнению с группой обычного контроля, несмотря на то, что в обеих группах наблюдался одинаковый уровень гликированного гемоглобина [5] (рис. 7). Различие, как теперь предполагается, могло быть связано с более низкой вариабельностью уровня глюкозы в течение дня в группе интенсивного контроля.
Хотя оценка средней амплитуды колебаний гликемии требует постоянного мониторинга уровня глюкозы, считается, что именно этот индекс должен использоваться в качестве золотого стандарта для оценки колебаний уровня глюкозы и вариабельности гликемии. Следующий пример может объяснить превосходство индекса средней амплитуды колебаний гликемии при оценке вариабельности уровня глюкозы, по сравнению со стандартным отклонением от профиля глюкозы, построенного, к примеру, по семи точкам. Рассмотрим двух пациентов с СД 2 типа, у которых наблюдаются одинаковые значения HbA1c и стандартные отклонения уровня глюкозы от среднего. Предположим, что у одного пациента отмечаются множественные небольшие колебания уровня глюкозы и один или два выраженных отклонения в день, в то время как у другого пациента отмечаются умеренные колебания уровня глюкозы в течение суток. Несмотря на одинаковые стандартные отклонения уровня глюкозы от среднего, у этих двух пациентов должны наблюдаться сильно различающиеся показатели индекса средней амплитуды колебаний гликемии.
Непрерывный мониторинг обеспечивает детальную информацию о характере и тенденциях изменения уровня глюкозы и обещает стать одним из значительных достижений в контроле диабета [2,3]. Важно, что профили постоянного измерения гликемии и записи, полученные при помощи мониторов, позволяют идентифицировать периоды скрытых ночных гипогликемий, постпрандиальных гипергликемий и корректировать дозу сахароснижающего препарата, время его приема, вносить изменения в план питания и график физической активности, регулировать время и частоту измерений сахара в крови [2,3,6–10].
Итак, на сегодняшний день известно, что патофизиология осложнений СД рассматривается, как результат двух основных вредоносных метаболических нарушений (избыточного гликозилирования и активации окислительного стресса), которые активируются тремя основными гликемическими нарушениями: гипергликемией натощак и в постпрандиальном периоде и острыми колебаниями уровня глюкозы. Не подвергается сомнению тот факт, что повышенный уровень глюкозы натощак и во время постпрандиального периода приводит к активации процесса гликозилирования, который можно комплексно оценивать по уровню НвA1с. Кроме гипергликемии натощак, острая или хроническая гипергликемия в постпрандиальном периоде и в общем – острые колебания глюкозы относительно средних значений уровня глюкозы приводят к активации окислительного стресса. Результирующее влияние в виде риска развития осложнений описывается диагональной стрелкой геометрического куба, в котором в трехмерных координатах по трем осям расположены уровень глюкозы в плазме натощак, уровень постпрандиальной глюкозы и колебания уровня глюкозы.
В соответствии с этой моделью глобальная стратегия лечения СД на современном уровне должна быть направлена на снижение значений по всем трем осям координат (т.е. на снижение объема куба) и, следовательно, величины диагональной стрелки, которая отражает риск развития осложнений диабета (рис. 8).
Таким образом, непрерывное измерение концентрации глюкозы в крови с определением продолжительности нормо–, гипо– и гипергликемии, а также амплитуды колебаний гликемии в течение суток может значительно дополнить HbA1c, как интегрированную оценку гликемического контроля.
Например, в исследовании Einhorn с соавт. [2] результаты 88% пациентов, прошедших мониторирование глюкозы крови с помощью системы непрерывного мониторинга гликемии, потребовали такого изменения схемы инсулинотерапии, которое невозможно было прогнозировать, несмотря на интенсивное исследование глюкозы крови с помощью глюкометра.
Специфический подбор терапии может включать переход на применение другого сахароснижающего препарата, изменение углеводного состава питания, режима введения инсулина, корректировку целевых уровней пре– и постпрандиальной гликемии или даже направление пациента на консультацию к психологу, чтобы усилить мотивацию на соблюдение режима лечения (рис. 9 а, б).
Например, Donicova c cоавт. [1] исследовали плазменный уровень глюкозы у 30 пациентов с СД 2 типа, получающих монотерапию глимепиридом при помощи метода непрерывного мониторинга гликемии. Исследование продемонстрировало, что гипергликемия после завтрака отмечается даже у тех пациентов с СД 2 типа, которые имеют хороший гликемический контроль. Практической рекомендацией стало снижение количества углеводов в утренний прием пищи до 15 г.
Таким образом, основная цель непрерывного мониторинга – получение достоверной и подробной картины, позволяющей при подборе терапии качественно улучшить контроль гликемии и тем самым снизить риск развития осложнений заболевания, влияющих на продолжительность и качество жизни пациентов.
Важно, что постоянный мониторинг гликемии наряду с определением среднего уровня глюкозы крови позволяет новыми способами регистрировать динамику его изменения. После назначения нового лечения средний уровень глюкозы может измениться быстро, а на практике не всегда предоставляется возможность ждать месяцы и недели, чтобы оценить изменение уровня HbA1c или фруктозамина, соответственно. С этой точки зрения метод непрерывного мониторинга гликемии позволяет точнее оценить изменение соотношения отрезков времени, когда пациент находился в состоянии нормо–, гипо– и гипергликемии, и это более достоверно, чем интегрированные данные, такие как HbA1c или фруктозамин. Увеличение периода нормогликемии значительно снижает риск развития осложнений заболевания, в отличие от ситуации постоянно чередующихся гипогликемических «долин» и гипергликемических «пиков», особенно если учесть, что последние, как правило, не отображаются при измерении маркеров (фруктозамин и HbA1c), дающих усредненные значения.
Общеизвестна отрицательная роль гипогликемических эпизодов, и метод непрерывного мониторинга гликемии играет важную роль не только в идентификации этих эпизодов, но и в подборе терапевтических режимов, которые снизят вероятность их появления и которые также влияют на развитие осложнений диабета.
Известно, что важнейшим компонентом оказания помощи при диабете является разработка и внедрение системы обучения больных самоконтролю и управлению этим заболеванием. Пациент должен вовлекаться в программу лечения на регулярной, ежедневной основе, так как достижение стабильной компенсации диабета требует внимательного отношения к питанию, расходу энергии и медикаментозному лечению.
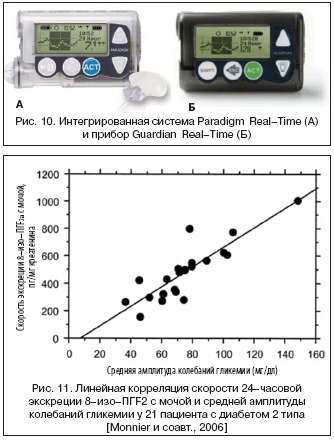
В отличие от прибора CGMSO Gold, ретроспективные данные о гликемии с которого врач может получить только после проведения исследования, такие портативные устройства, как интегрированная система инсулиновой помпы с измерением глюкозы в интерстициальной жидкости ParadigmO Real–Time и монитор для визуализации гликемии GuardianO Real–Time («Медтроник», США) (рис. 10), позволяют пациенту с СД не только видеть изменения гликемии на дисплее в режиме реального времени, но и получать предупреждающие сигналы об опасных уровнях сахара крови и оперативно изменять терапию, достигая хорошего контроля диабета с низкой вариабельностью гликемии в кратчайшие сроки.
Таким образом, вариабельность уровня глюкозы, определяемая с помощью приборов непрерывного длительного мониторинга гликемии ретроспективно или в режиме реального времени, должна быть одной из целей лечения нарушений углеводного обмена, имеющих место у пациентов с СД. В качестве целевого показателя вариабельности уровня глюкозы, на основании проведенных исследований скорости экскреции 8–изо–простагландин –F2 2α c мочой, установлен уровень 2,2 ммоль/л (40 мг/дл) (рис. 11).
Однако не вызывает сомнения, что для уточнения стандартов вариабельности глюкозы при СД необходимо проведение дальнейших крупномасштабных исследований с использованием метода непрерывного мониторинга гликемии, результаты которых будут призваны ответить на многочисленные вопросы, для того чтобы мы смогли обеспечить пациентам действительно высокое качество жизни при диабете. s
Медтроник Б.В.
www.medtronic–diabetes.ru
Телефон линиии поддержки: 8 (495) 225–76–36




Литература
1. Шилов А.М., Авшалумов А.С., Синицина Е.Н., Марковский В.Б.. «Клиническое значение суточного мониторирования гликемии у больных с нарушением углеводного обмена». Эффективная фармакотерапия в эндокринологии, 1–2008, с.32–35.
2. Kannel WB, Mc Gee DL: Diabetes and cardiovascular diseases: the Framingham Study. JAMA 241:2035–2038, 1979.
3. Laakso L, Lehto S: Epidemiology of macrovascular disease in diabetes. Diabetes Rev 5:294–315, 1997.
4. Boland E., Monsod T., Delucia M. et al. Limitations of conventional methods of self–monitoring of blood glucose: lessons learned from 3 days of continuous glucose sensing in pediatric patients with type 1 diabetes // Diabetes Care. – 2001. – Vol. 24. – P. 1858–1862.
5. DCCT Research Group: The relationship of a glycemic exposure (HbA1c) to the risk of development and progression of retinopathy in the Diabetes Control and Complications Trial. Diabetes 44:968–983, 1995.
6. Diabetes Control and Complications Trial Research Group: The effect of intensive treatment of diabetes on the development and progression of long–term complications in insulin–dependent diabetes mellitus. N Engl J Med 329:977–986, 1993.
7. Hay L., Wilmshurst E., Fulcher G. Unrecognized hypo– and hyperglycemia in well–controlled patients with type 2 diabetes mellitus: the results of continuous glucose monitoring // Diabetes Thechnol. Ther. – 2003. – Vol. 5. – P. 19–26.
8. Stratton IM, Adler AI, Neil HA, Matthews DR, Manley SE, Cull CA, Hadden D, Turner RC, Holman RR: Association of glycaemia with macrovascular and microvascular complications of type 2 diabetes (UKPDS 35): prospective observational study. BMJ 321:405–412, 2000.
9. Eastman RC, Javitt JC, Herman WH, Dasbach EJ, Zbrozek AS, Dong F, Manninen D, Gardfield SA, Copley–Merriman C, Maier W, Eastman JF, Kotsanos J, Cowie CC, Harris M: Model of complications of NIDDM 1: Model constructions and assumptions. Diabetes Care 20:725–734, 1997.
10. Gaede P, Vedel P, Larsen N, Jensen GVH, Parving HH, Pedersen O: Multifactorial intervention and cardiovascular disease in patients with type 2 diabetes. N Engl J Med 348:383–393, 2003.
11. Monnier L, Mas E, Ginet C, Michel F, Villon L, Cristol JP, Colette C: Activation of oxidative stress by acute glucose fluctuations compared with sustained chronic hyperglycemia in patients with type 2 diabetes. JAMA 295:1681–1687, 2006.












