–†–Ķ–≤–ľ–į—ā–ĺ–ł–ī–Ĺ—č–Ļ –į—Ä—ā—Ä–ł—ā – —ć—ā–ĺ –į—É—ā–ĺ–ł–ľ–ľ—É–Ĺ–Ĺ–ĺ–Ķ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ķ, –ļ–ĺ—ā–ĺ—Ä–ĺ–Ķ —Ö–į—Ä–į–ļ—ā–Ķ—Ä–ł–∑—É–Ķ—ā—Ā—Ź —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł–ľ –≤–ĺ—Ā–Ņ–į–Ľ–Ķ–Ĺ–ł–Ķ–ľ —Ā—É—Ā—ā–į–≤–ĺ–≤ —Ā –ĺ–Ī–ĺ—Ā—ā—Ä–Ķ–Ĺ–ł—Ź–ľ–ł, —á—ā–ĺ –ľ–ĺ–∂–Ķ—ā –Ņ—Ä–ł–≤–ĺ–ī–ł—ā—Ć –ļ —ā—Ź–∂–Ķ–Ľ–ĺ–Ļ –ł –ł–Ĺ–≤–į–Ľ–ł–ī–ł–∑–ł—Ä—É—é—Č–Ķ–Ļ –į—Ä—ā—Ä–ĺ–Ņ–į—ā–ł–ł —Ā –Ņ–ĺ—Ā–Ľ–Ķ–ī—É—é—Č–ł–ľ–ł –ī–Ķ—Ą–ĺ—Ä–ľ–į—Ü–ł—Ź–ľ–ł –ł –Ņ–ĺ—ā–Ķ—Ä–Ķ–Ļ –ī–Ķ–Ķ—Ā–Ņ–ĺ—Ā–ĺ–Ī–Ĺ–ĺ—Ā—ā–ł [1, 2]. –ü—Ä–ł –Ľ–Ķ—á–Ķ–Ĺ–ł–ł —ć—ā–ĺ–Ļ –Ī–ĺ–Ľ–Ķ–∑–Ĺ–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ—Ź—é—ā—Ā—Ź –Ĺ–ĺ–≤—č–Ķ –ł —ā—Ä–į–ī–ł—Ü–ł–ĺ–Ĺ–Ĺ—č–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā—č –ļ–Ľ–į—Ā—Ā–į DMARD (disease-modifying anti-rheumatic drugs – –į–Ĺ—ā–ł—Ä–Ķ–≤–ľ–į—ā–ł—á–Ķ—Ā–ļ–ł–Ķ –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č–Ķ —Ā—Ä–Ķ–ī—Ā—ā–≤–į (–õ–°), –≤–Ľ–ł—Ź—é—Č–ł–Ķ –Ĺ–į —Ö–ĺ–ī –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź) [3], –ļ–ĺ—ā–ĺ—Ä—č–Ķ –ľ–ĺ–≥—É—ā —Ä–Ķ–į–Ľ—Ć–Ĺ–ĺ –ł–∑–ľ–Ķ–Ĺ—Ź—ā—Ć –Ķ–≥–ĺ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ. –Ę–į–ļ–∂–Ķ –ī–Ľ—Ź –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź —ć—ā–ĺ–Ļ –Ī–ĺ–Ľ–Ķ–∑–Ĺ–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ—Ź—é—ā—Ā—Ź –Ĺ–Ķ—Ā—ā–Ķ—Ä–ĺ–ł–ī–Ĺ—č–Ķ –Ņ—Ä–ĺ—ā–ł–≤–ĺ–≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā—č (–Ě–ü–í–ü), –ļ–ĺ—ā–ĺ—Ä—č–Ķ –ĺ–Ī–Ľ–Ķ–≥—á–į—é—ā —Ā–ł–ľ–Ņ—ā–ĺ–ľ—č –∑–į —Ā—á–Ķ—ā —Ā–Ĺ—Ź—ā–ł—Ź –Ī–ĺ–Ľ–ł –ł –≤–ĺ—Ā–Ņ–į–Ľ–Ķ–Ĺ–ł—Ź. –•–ĺ—ā—Ź –Ě–ü–í–ü – —ć—ā–ĺ –ĺ—á–Ķ–Ĺ—Ć —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ—č–Ķ –õ–°, –ł—Ö –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ —Ā–≤—Ź–∑–į–Ĺ–ĺ —Ā —Ü–Ķ–Ľ—č–ľ —Ä—Ź–ī–ĺ–ľ –Ĺ–Ķ–∂–Ķ–Ľ–į—ā–Ķ–Ľ—Ć–Ĺ—č—Ö –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č—Ö —Ä–Ķ–į–ļ—Ü–ł–Ļ —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ņ–Ķ—á–Ķ–Ĺ–ł, –Ņ–ĺ—á–Ķ–ļ, –ļ–ĺ–∂–ł –ł –ļ–ł—ą–Ķ—á–Ĺ–ł–ļ–į [4, 5]. –Ě–į–ł–Ī–ĺ–Ľ–Ķ–Ķ —á–į—Ā—ā–ĺ –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –õ–° —ć—ā–ĺ–≥–ĺ –ļ–Ľ–į—Ā—Ā–į –≤–ĺ–∑–Ĺ–ł–ļ–į—é—ā –Ĺ–Ķ–∂–Ķ–Ľ–į—ā–Ķ–Ľ—Ć–Ĺ—č–Ķ —Ä–Ķ–į–ļ—Ü–ł–ł —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ė–ö–Ę [6, 10]. –Ě–Ķ–∂–Ķ–Ľ–į—ā–Ķ–Ľ—Ć–Ĺ—č–Ķ —Ź–≤–Ľ–Ķ–Ĺ–ł—Ź (–Ě–Į) –≤–į—Ä—Ć–ł—Ä—É—é—ā –ĺ—ā —Ā–ł–ľ–Ņ—ā–ĺ–ľ–ĺ–≤ —Ā—Ä–Ķ–ī–Ĺ–Ķ–Ļ —Ā—ā–Ķ–Ņ–Ķ–Ĺ–ł —ā—Ź–∂–Ķ—Ā—ā–ł, —ā–į–ļ–ł—Ö –ļ–į–ļ –ī–ł—Ā–Ņ–Ķ–Ņ—Ā–ł—Ź, –ł–∑–∂–ĺ–≥–į –ł –ī–ł—Ā–ļ–ĺ–ľ—Ą–ĺ—Ä—ā –≤ –∂–ł–≤–ĺ—ā–Ķ, –ī–ĺ –Ī–ĺ–Ľ–Ķ–Ķ —Ā–Ķ—Ä—Ć–Ķ–∑–Ĺ—č—Ö —Ź–≤–Ľ–Ķ–Ĺ–ł–Ļ, —ā–į–ļ–ł—Ö –ļ–į–ļ –Ņ–Ķ–Ņ—ā–ł—á–Ķ—Ā–ļ–į—Ź —Ź–∑–≤–į –ł —Ā–ĺ–Ņ—É—ā—Ā—ā–≤—É—é—Č–ł–Ķ –∂–ł–∑–Ĺ–Ķ—É–≥—Ä–ĺ–∂–į—é—Č–ł–Ķ –ĺ—Ā–Ľ–ĺ–∂–Ĺ–Ķ–Ĺ–ł—Ź, –ļ—Ä–ĺ–≤–ĺ—ā–Ķ—á–Ķ–Ĺ–ł—Ź –ł –Ņ—Ä–ĺ–Ī–ĺ–ī–Ĺ–į—Ź —Ź–∑–≤–į. –°–Ľ–ł–∑–ł—Ā—ā–į—Ź –ĺ–Ī–ĺ–Ľ–ĺ—á–ļ–į (–°–ě) –ł–ľ–Ķ–Ķ—ā –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–Ĺ—č–Ķ –∑–į—Č–ł—ā–Ĺ—č–Ķ –ľ–Ķ—Ö–į–Ĺ–ł–∑–ľ—č, –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –Ě–ü–í–ü –Ĺ–į—Ä—É—ą–į–Ķ—ā—Ā—Ź —Ą—É–Ĺ–ļ—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ –Ī–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–į –ł–∑ —ć—ā–ł—Ö –ľ–Ķ—Ö–į–Ĺ–ł–∑–ľ–ĺ–≤ [11].
–ü—Ä–Ķ–ī—Ā—ā–į–≤–Ľ—Ź–Ķ—ā—Ā—Ź, —á—ā–ĺ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź –Ė–ö–Ę –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ —ć—ā–ł—Ö –õ–° –ĺ–Ņ–ĺ—Ā—Ä–Ķ–ī–ĺ–≤–į–Ĺ—č 2-–ľ—Ź –ĺ—Ā–Ĺ–ĺ–≤–Ĺ—č–ľ–ł –ľ–Ķ—Ö–į–Ĺ–ł–∑–ľ–į–ľ–ł: —Ą–ł–∑–ł–ļ–ĺ-—Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ł–ľ –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł–Ķ–ľ –Ī–į—Ä—Ć–Ķ—Ä–Ĺ–ĺ–Ļ —Ą—É–Ĺ–ļ—Ü–ł–ł –°–ě –∂–Ķ–Ľ—É–ī–ļ–į –ł —Ā–ł—Ā—ā–Ķ–ľ–Ĺ—č–ľ –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł–Ķ–ľ –∑–į—Č–ł—ā—č –°–ě –∂–Ķ–Ľ—É–ī–ļ–į –≤—Ā–Ľ–Ķ–ī—Ā—ā–≤–ł–Ķ –ł–Ĺ–≥–ł–Ī–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł —Ü–ł–ļ–Ľ–ĺ–ĺ–ļ—Ā–ł–≥–Ķ–Ĺ–į–∑—č (–¶–ě–ď) (–Ņ—Ä–ĺ—Ā—ā–į–≥–Ľ–į–Ĺ–ī–ł–Ĺ (–ü–ď) —ć–Ĺ–ī–ĺ–Ņ–Ķ—Ä–ĺ–ļ—Ā–ł–ī G/H —Ā–ł–Ĺ—ā–į–∑—č – –¶–ě–ď) –≤ –°–ě –Ė–ö–Ę. –£–ľ–Ķ–Ĺ—Ć—ą–Ķ–Ĺ–ł–Ķ –ł–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –≤—č—Ä–į–Ī–ĺ—ā–ļ–ł —Ā–Ľ–ł–∑–ł –ł –Ī–ł–ļ–į—Ä–Ī–ĺ–Ĺ–į—ā–į, –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł–Ķ –ļ—Ä–ĺ–≤–ĺ—ā–ĺ–ļ–į –≤ –°–ě –ł —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł–Ķ —Ā–Ķ–ļ—Ä–Ķ—Ü–ł–ł –ļ–ł—Ā–Ľ–ĺ—ā—č —Ź–≤–Ľ—Ź—é—ā—Ā—Ź –ĺ—Ā–Ĺ–ĺ–≤–Ĺ—č–ľ–ł –Ņ–ĺ—Ā–Ľ–Ķ–ī—Ā—ā–≤–ł—Ź–ľ–ł –Ě–ü–í–ü-–ł–Ĺ–ī—É—Ü–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–≥–ĺ –ī–Ķ—Ą–ł—Ü–ł—ā–į –ü–ď [12]. –Ę–į–ļ–∂–Ķ –Ī—č–Ľ–ł –Ņ—Ä–ĺ–ī–Ķ–ľ–ĺ–Ĺ—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ—č –ī–ĺ–Ņ–ĺ–Ľ–Ĺ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ķ –ľ–Ķ—Ö–į–Ĺ–ł–∑–ľ—č —Ä–į–∑–≤–ł—ā–ł—Ź –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–Ļ: –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł–Ķ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–į –ĺ–ļ–ł—Ā–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ —Ą–ĺ—Ā—Ą–ĺ—Ä–ł–Ľ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź (—Ä–į–∑—Ä—č–≤ —Ü–Ķ–Ņ–ł –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–į —ć–Ľ–Ķ–ļ—ā—Ä–ĺ–Ĺ–ĺ–≤), —É–ľ–Ķ–Ĺ—Ć—ą–Ķ–Ĺ–ł–Ķ –ł–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ņ—Ä–ĺ–Ľ–ł—Ą–Ķ—Ä–į—Ü–ł–ł –ļ–Ľ–Ķ—ā–ĺ–ļ –°–ě –ł —Ä–Ķ–Ņ–Ľ–ł–ļ–į—Ü–ł–ł –Ē–Ě–ö, –į–ļ—ā–ł–≤–į—Ü–ł—Ź –Ĺ–Ķ–Ļ—ā—Ä–ĺ—Ą–ł–Ľ–ĺ–≤ [12].
–Ě–į–ł–Ī–ĺ–Ľ–Ķ–Ķ –≤–Ķ—Ä–ĺ—Ź—ā–Ĺ–ĺ, —á—ā–ĺ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–Ķ —ā–ļ–į–Ĺ–Ķ–Ļ –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –Ě–ü–í–ü –ĺ–Ī—É—Ā–Ľ–ĺ–≤–Ľ–Ķ–Ĺ–ĺ –ł–Ĺ–≥–ł–Ī–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ–ľ –¶–ě–ď-1, —ā. –ļ. –≤—Ā–Ķ –Ě–ü–í–ü (–≤ –ĺ—ā–Ľ–ł—á–ł–Ķ –ĺ—ā –ī—Ä—É–≥–ł—Ö —Ā—Ä–Ķ–ī—Ā—ā–≤) –ł–Ĺ–≥–ł–Ī–ł—Ä—É—é—ā –¶–ě–ď-1, –ł –Ņ—Ä–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–ł –≤—Ā–Ķ—Ö –Ě–ü–í–ü –ĺ—ā–ľ–Ķ—á–į—é—ā—Ā—Ź —Ā—Ö–ĺ–∂–ł–Ķ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź. –ü—Ä–ł–≤–Ľ–Ķ–ļ–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā—Ć —ć—ā–ĺ–Ļ –≥–ł–Ņ–ĺ—ā–Ķ–∑—č – –≤ –Ķ–Ķ –Ņ—Ä–ĺ—Ā—ā–ĺ—ā–Ķ; —Ā—É—Č–Ķ—Ā—ā–≤—É–Ķ—ā –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–Ĺ–į—Ź –ļ–ĺ—Ä—Ä–Ķ–Ľ—Ź—Ü–ł—Ź –ľ–Ķ–∂–ī—É –Ņ—Ä–ł–Ķ–ľ–ĺ–ľ –Ě–ü–í–ü –ł —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ–ľ —É—Ä–ĺ–≤–Ĺ—Ź –ü–ď –≤ –°–ě. –í –ĺ–ī–Ĺ–ĺ–Ļ —Ā—ā–į—ā—Ć–Ķ [13] –Ņ—Ä–Ķ–ī–Ņ–ĺ–Ľ–į–≥–į–Ķ—ā—Ā—Ź, —á—ā–ĺ –į–Ĺ—ā–ł-–¶–ě–ď –į–Ĺ—ā–ł—ā–Ķ–Ľ–į –≤—č–∑—č–≤–į—é—ā –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–Ķ –Ė–ö–Ę —É –ļ—Ä–ĺ–Ľ–ł–ļ–ĺ–≤, –ł–ī–Ķ–Ĺ—ā–ł—á–Ĺ–ĺ–Ķ —ā–į–ļ–ĺ–≤–ĺ–ľ—É –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –Ě–ü–í–ü. –ü–ĺ—Ā–Ľ–Ķ –ĺ—ā–ļ—Ä—č—ā–ł—Ź 2-—Ö –ł–∑–ĺ—Ą–ĺ—Ä–ľ –¶–ě–ď (–¶–ě–ď-1 –ł –¶–ě–ď-2) –Ī—č–Ľ–ł —Ä–į–∑—Ä–į–Ī–ĺ—ā–į–Ĺ—č –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č–Ķ –≤–Ķ—Č–Ķ—Ā—ā–≤–į, —Ā–Ņ–ĺ—Ā–ĺ–Ī–Ĺ—č–Ķ –≤ —ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–ł—á–Ķ—Ā–ļ–ł—Ö –ī–ĺ–∑–į—Ö —Ā–Ņ–Ķ—Ü–ł—Ą–ł—á–Ķ—Ā–ļ–ł –ł–Ĺ–≥–ł–Ī–ł—Ä–ĺ–≤–į—ā—Ć –¶–ě–ď-2 –ł –≤ –ľ–Ķ–Ĺ—Ć—ą–Ķ–Ļ —Ā—ā–Ķ–Ņ–Ķ–Ĺ–ł –ł–Ĺ–≥–ł–Ī–ł—Ä–ĺ–≤–į—ā—Ć –¶–ě–ď-1. –•–ĺ—ā—Ź –ł–ľ–Ķ—é—ā—Ā—Ź —Ā–≤–Ķ–ī–Ķ–Ĺ–ł—Ź –ĺ —ā–ĺ–ľ, —á—ā–ĺ –¶–ě–ď-2 –≤ –Ĺ–ĺ—Ä–ľ–Ķ —ć–ļ—Ā–Ņ—Ä–Ķ—Ā—Ā–ł—Ä—É–Ķ—ā—Ā—Ź –≤ –°–ě –Ė–ö–Ę –ł —Ā–ĺ–≤–ľ–Ķ—Ā—ā–Ĺ–ĺ —Ā –¶–ě–ď-1 —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź —á–į—Ā—ā—Ć—é –∑–į—Č–ł—ā–Ĺ–ĺ–Ļ —Ā–ł—Ā—ā–Ķ–ľ—č –Ė–ö–Ę [14, 15], —ā–į–ļ –Ĺ–į–∑—č–≤–į–Ķ–ľ—č–Ķ «—Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č–Ķ –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä—č –¶–ě–ď-2» –ĺ–Ī–Ķ—Ā–Ņ–Ķ—á–ł–≤–į—é—ā –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –Ľ—É—á—ą–Ķ–Ķ –ĺ—ā–Ĺ–ĺ—ą–Ķ–Ĺ–ł–Ķ —Ä–ł—Ā–ļ/–Ņ–ĺ–Ľ—Ć–∑–į –Ņ–ĺ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—é —Ā –Ĺ–Ķ—Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č–ľ–ł –Ě–ü–í–ü. –¶–ě–ď-1 —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –ī–ĺ–ľ–ł–Ĺ–į–Ĺ—ā–Ĺ–ĺ–Ļ –ł–∑–ĺ—Ą–ĺ—Ä–ľ–ĺ–Ļ –≤ –Ĺ–ĺ—Ä–ľ–į–Ľ—Ć–Ĺ–ĺ–Ļ –°–ě [14], —ā–į–ļ —á—ā–ĺ –ü–ď, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –≤—č—Ä–į–Ī–į—ā—č–≤–į—é—ā—Ā—Ź –Ņ—Ä–ł —É—á–į—Ā—ā–ł–ł –¶–ě–ď-2, –ł–≥—Ä–į—é—ā –ļ–Ľ—é—á–Ķ–≤—É—é —Ä–ĺ–Ľ—Ć —ā–ĺ–Ľ—Ć–ļ–ĺ –Ņ—Ä–ł –∑–į–∂–ł–≤–Ľ–Ķ–Ĺ–ł–ł —Ź–∑–≤ [14, 15] –ł –Ņ—Ä–ł –Ĺ–į–Ľ–ł—á–ł–ł –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–≥–ĺ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź, –ĺ–Ī—É—Ā–Ľ–ĺ–≤–Ľ–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ Helicobacter pylori [14, 16].
–Ę–į–ļ–∂–Ķ –ľ–ĺ–∂–Ĺ–ĺ –ĺ—ā–ľ–Ķ—ā–ł—ā—Ć, —á—ā–ĺ –Ņ—Ä–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–ł —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–ĺ–≤ –¶–ě–ď-2, —ā–į–ļ–ł—Ö –ļ–į–ļ —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī –ł —Ä–ĺ—Ą–Ķ–ļ–ĺ–ļ—Ā–ł–Ī, –Ņ–ĺ–ľ–ł–ľ–ĺ –Ņ–ĺ–ī–į–≤–Ľ–Ķ–Ĺ–ł—Ź –Ī–ł–ĺ—Ā–ł–Ĺ—ā–Ķ–∑–į –ü–ď –≤ –°–ě –Ė–ö–Ę, –Ĺ–Ķ –Ĺ–į–Ī–Ľ—é–ī–į–Ķ—ā—Ā—Ź –ļ–į–ļ–ĺ–Ķ-–Ľ–ł–Ī–ĺ –ľ–Ķ—Ā—ā–Ĺ–ĺ–Ķ —Ä–į–∑–ī—Ä–į–∂–Ķ–Ĺ–ł–Ķ. –ě—ā—Ā—É—ā—Ā—ā–≤–ł–Ķ —Ä–į–∑–ī—Ä–į–∂–Ķ–Ĺ–ł—Ź —Ā–≤—Ź–∑–į–Ĺ–ĺ —Ā —ā–Ķ–ľ, —á—ā–ĺ –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ—č —ć—ā–ł—Ö –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č—Ö –≤–Ķ—Č–Ķ—Ā—ā–≤ —Ā–į–ľ–ł –Ņ–ĺ —Ā–Ķ–Ī–Ķ –Ĺ–Ķ –ļ–ł—Ā–Ľ—č–Ķ –ł –Ĺ–Ķ –≤—č–∑—č–≤–į—é—ā —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł—Ź –Ņ—Ä–ĺ–Ĺ–ł—Ü–į–Ķ–ľ–ĺ—Ā—ā–ł –∂–Ķ–Ľ—É–ī–ļ–į –ł–Ľ–ł –ļ–ł—ą–Ķ—á–Ĺ–ł–ļ–į –ł–Ľ–ł –≤–ĺ—Ā–Ņ–į–Ľ–Ķ–Ĺ–ł–Ķ –°–ě [17]. –Ę–į–ļ–ł–ľ –ĺ–Ī—Ä–į–∑–ĺ–ľ, –Ņ—Ä–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–ł —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–ĺ–≤ –¶–ě–ď-2 –Ĺ–Ķ –į–ļ—ā–ł–≤–ł—Ä—É—é—ā—Ā—Ź 2 –ļ–Ľ—é—á–Ķ–≤—č—Ö –Ī–ł–ĺ—Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ł—Ö –ľ–Ķ—Ö–į–Ĺ–ł–∑–ľ–į –Ě–ü–í–ü-–ł–Ĺ–ī—É—Ü–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–≥–ĺ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź – —ć—ā–ĺ —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –Ņ—Ä–ł—á–ł–Ĺ–ĺ–Ļ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –Ľ—É—á—ą–Ķ–Ļ –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā–ł —ć—ā–ł—Ö –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –ī–Ľ—Ź –Ė–ö–Ę.
–í –ľ–į—Ā—ą—ā–į–Ī–Ĺ—č—Ö –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł—Ö –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź—Ö –Ī—č–Ľ–ĺ –Ņ—Ä–ĺ–ī–Ķ–ľ–ĺ–Ĺ—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ–ĺ, —á—ā–ĺ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–ĺ–≤ –¶–ě–ď-2 —ć–ļ–≤–ł–≤–į–Ľ–Ķ–Ĺ—ā–Ĺ–į —ā–į–ļ–ĺ–≤–ĺ–Ļ –ī–Ľ—Ź –ĺ–Ī—č—á–Ĺ—č—Ö –Ě–ü–í–ü [18, 19] –Ņ—Ä–ł –Ľ—É—á—ą–ł—Ö –Ņ–į—Ä–į–ľ–Ķ—ā—Ä–į—Ö –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł –≤ –ĺ—ā–Ĺ–ĺ—ą–Ķ–Ĺ–ł–ł –Ė–ö–Ę [20, 21]. –í —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł—á–Ķ—Ā–ļ–ł—Ö –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź—Ö –Ī—č–Ľ–ĺ –Ņ—Ä–ĺ–ī–Ķ–ľ–ĺ–Ĺ—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ–ĺ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ —É–ľ–Ķ–Ĺ—Ć—ą–Ķ–Ĺ–ł–Ķ —á–į—Ā—ā–ĺ—ā—č —Ä–į–∑–≤–ł—ā–ł—Ź —Ź–∑–≤—č –∂–Ķ–Ľ—É–ī–ļ–į –ł –ī–≤–Ķ–Ĺ–į–ī—Ü–į—ā–ł–Ņ–Ķ—Ä—Ā—ā–Ĺ–ĺ–Ļ –ļ–ł—ą–ļ–ł (–Ē–ü–ö) [22, 23] –ł –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–į –ĺ—Ā–Ľ–ĺ–∂–Ĺ–Ķ–Ĺ–ł–Ļ –Ņ—Ä–ł –Ņ–Ķ–Ņ—ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ —Ź–∑–≤–Ķ.
–ź–ľ—ā–ĺ–Ľ–ľ–Ķ—ā–ł–Ĺ –≥—É–į—Ü–ł–Ľ (2-–ľ–Ķ—ā–ĺ–ļ—Ā–ł—Ą–Ķ–Ĺ–ł–Ľ-1-–ľ–Ķ—ā–ł–Ľ-5-–Ņ-–ľ–Ķ—ā–ł–Ľ–Ī–Ķ–Ĺ–∑–ĺ–Ľ-–Ņ–ł—Ä—Ä–ĺ–Ľ-2-–į—Ü–Ķ—ā–į–ľ–ł–ī–ĺ–į—Ü–Ķ—ā–į—ā, –ź–ú–ď) – —ć—ā–ĺ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā –ļ–Ľ–į—Ā—Ā–į –Ě–ü–í–ü [24], –ļ–ĺ—ā–ĺ—Ä—č–Ļ —Ā –Ĺ–Ķ–ī–į–≤–Ĺ–Ķ–≥–ĺ –≤—Ä–Ķ–ľ–Ķ–Ĺ–ł –Ĺ–į—Ö–ĺ–ī–ł—ā—Ā—Ź –≤ —Ā–≤–ĺ–Ī–ĺ–ī–Ĺ–ĺ–Ļ –Ņ—Ä–ĺ–ī–į–∂–Ķ –≤ –ė—ā–į–Ľ–ł–ł –ł —É—ā–≤–Ķ—Ä–∂–ī–Ķ–Ĺ –ī–Ľ—Ź —ā–Ķ—Ä–į–Ņ–ł–ł —Ä–Ķ–≤–ľ–į—ā–ĺ–ł–ī–Ĺ–ĺ–≥–ĺ –į—Ä—ā—Ä–ł—ā–į, –ĺ—Ā—ā–Ķ–ĺ–į—Ä—ā—Ä–ł—ā–į, –≤–Ĺ–Ķ—Ā—É—Ā—ā–į–≤–Ĺ–ĺ–≥–ĺ —Ä–Ķ–≤–ľ–į—ā–ł–∑–ľ–į –ł –Ņ–ĺ—Ā–Ľ–Ķ–ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–Ļ –Ī–ĺ–Ľ–ł. –ź–ú–ď –ł–Ĺ–≥–ł–Ī–ł—Ä—É–Ķ—ā –¶–ě–ď-1 –ł –¶–ě–ď-2, –Ņ—Ä–ł —ć—ā–ĺ–ľ –ĺ—ā–Ĺ–ĺ—ą–Ķ–Ĺ–ł–Ķ —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –ł–Ĺ–≥–ł–Ī–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –¶–ě–ď-2/–¶–ě–ď-1 –≤ —ć–ļ—Ā–Ņ–Ķ—Ä–ł–ľ–Ķ–Ĺ—ā–Ķ —Ā –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ–ľ –ļ–Ľ–Ķ—ā–ĺ–ļ —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł—Ź –Ī—č—á—Ć–Ķ–Ļ –į–ĺ—Ä—ā—č –ł –ľ–į–ļ—Ä–ĺ—Ą–į–≥–ĺ–≤, —Ā—ā–ł–ľ—É–Ľ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö –Ľ–ł–Ņ–ĺ–Ņ–ĺ–Ľ–ł—Ā–į—Ö–į—Ä–ł–ī–į–ľ–ł, —Ā–ĺ—Ā—ā–į–≤–Ľ—Ź–Ľ–ĺ 4,4 [Vane et al., –Ĺ–Ķ–ĺ–Ņ—É–Ī–Ľ–ł–ļ–ĺ–≤–į–Ĺ–Ĺ—č–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā—č]. –ü–ĺ–ī–ĺ–Ī–Ĺ–ĺ —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č–ľ –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–į–ľ –¶–ě–ď-2 –ź–ú–ď –ĺ–Ī–Ľ–į–ī–į–Ķ—ā —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ—č–ľ –Ņ—Ä–ĺ—ā–ł–≤–ĺ–≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–ľ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ–ľ —Ā —É–Ľ—É—á—ą–Ķ–Ĺ–Ĺ–ĺ–Ļ –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā—Ć—é –ī–Ľ—Ź –Ė–ö–Ę. –ě–ī–Ĺ–į–ļ–ĺ –≤ –ĺ—ā–Ľ–ł—á–ł–Ķ –ĺ—ā —ć—ā–ł—Ö –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –ź–ú–ď –ĺ–ļ–į–∑—č–≤–į–Ķ—ā –į–Ĺ—ā–ł—ā—Ä–ĺ–ľ–Ī–ĺ—Ü–ł—ā–į—Ä–Ĺ–ĺ–Ķ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ [25, 26].
–í –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł—Ö –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź—Ö –Ī—č–Ľ–ĺ –Ņ—Ä–ĺ–ī–Ķ–ľ–ĺ–Ĺ—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ–ĺ, —á—ā–ĺ –Ņ—Ä–ĺ—ā–ł–≤–ĺ–≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ, –ĺ–Ī–Ķ–∑–Ī–ĺ–Ľ–ł–≤–į—é—Č–ł–Ļ –ł –∂–į—Ä–ĺ–Ņ–ĺ–Ĺ–ł–∂–į—é—Č–ł–Ļ —ć—Ą—Ą–Ķ–ļ—ā—č –ź–ú–ď —Ā—Ä–į–≤–Ĺ–ł–ľ—č —Ā —ā–į–ļ–ĺ–≤—č–ľ–ł –ī–Ľ—Ź —ā—Ä–į–ī–ł—Ü–ł–ĺ–Ĺ–Ĺ—č—Ö –Ě–ü–í–ü [27–29]. –í 2-—Ö –ľ–Ķ—ā–į–į–Ĺ–į–Ľ–ł–∑–į—Ö [30, 31] –Ī—č–Ľ–ĺ —É—Ā—ā–į–Ĺ–ĺ–≤–Ľ–Ķ–Ĺ–ĺ, —á—ā–ĺ –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –ź–ú–ď –Ĺ–į–Ī–Ľ—é–ī–į–Ķ—ā—Ā—Ź –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –ľ–Ķ–Ĺ—Ć—ą–Ķ (7,2 –ł 28,3% —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ) –Ě–Į —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –∂–Ķ–Ľ—É–ī–ļ–į, —á–Ķ–ľ –Ņ—Ä–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–ł —ā—Ä–į–ī–ł—Ü–ł–ĺ–Ĺ–Ĺ—č—Ö –Ě–ü–í–ü. –ß–į—Ā—ā–ĺ—ā–į –ł —Ā—ā–Ķ–Ņ–Ķ–Ĺ—Ć —ā—Ź–∂–Ķ—Ā—ā–ł –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź –°–ě –∂–Ķ–Ľ—É–ī–ļ–į, –Ņ–ĺ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł–ł, –Ī—č–Ľ–ł –ľ–Ķ–Ĺ—Ć—ą–Ķ –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –ź–ú–ď –Ņ–ĺ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—é —Ā —ā–į–ļ–ĺ–≤—č–ľ–ł –Ņ—Ä–ł –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–ł –ī—Ä—É–≥–ł—Ö –Ě–ü–í–ü, –ĺ—ā–Ĺ–ĺ—ą–Ķ–Ĺ–ł–Ķ —ą–į–Ĺ—Ā–ĺ–≤ —Ā–ĺ—Ā—ā–į–≤–Ľ—Ź–Ķ—ā 0,3 (95%, CI 0,1–0,7) –ī–Ľ—Ź —ā—Ź–∂–Ķ–Ľ–ĺ–≥–ĺ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź –ł 0,1 (95%, CI 0,1–0,4) –ī–Ľ—Ź —Ā—Ä–Ķ–ī–Ĺ–Ķ–≥–ĺ –ł —ā—Ź–∂–Ķ–Ľ–ĺ–≥–ĺ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ [30].
–í —Ą–į—Ä–ľ–į–ļ–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł—Ö –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź—Ö, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –Ī—č–Ľ–ł –≤—č–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ—č –Ĺ–į —Ä–į–∑–Ľ–ł—á–Ĺ—č—Ö –∂–ł–≤–ĺ—ā–Ĺ—č—Ö, –Ī—č–Ľ–ĺ –Ņ—Ä–ĺ–ī–Ķ–ľ–ĺ–Ĺ—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ–ĺ, —á—ā–ĺ –ź–ú–ď –Ĺ–Ķ —ā–ĺ–Ľ—Ć–ļ–ĺ –Ĺ–Ķ –Ņ–ĺ–≤—Ä–Ķ–∂–ī–į–Ķ—ā –°–ě –∂–Ķ–Ľ—É–ī–ļ–į, –Ĺ–ĺ –ł —Ä–Ķ–į–Ľ—Ć–Ĺ–ĺ –ĺ–ļ–į–∑—č–≤–į–Ķ—ā –≥–į—Ā—ā—Ä–ĺ–Ņ—Ä–ĺ—ā–Ķ–ļ—ā–ł–≤–Ĺ—č–Ļ —ć—Ą—Ą–Ķ–ļ—ā [26], –ļ–ĺ—ā–ĺ—Ä—č–Ļ —Ä–į—Ā–Ņ—Ä–ĺ—Ā—ā—Ä–į–Ĺ—Ź–Ķ—ā—Ā—Ź —ā–į–ļ–∂–Ķ –Ĺ–į –ĺ–Ī–Ľ–į—Ā—ā—Ć –ļ–ł—ą–Ķ—á–Ĺ–ł–ļ–į [32]. –≠—ā–ĺ —ā–į–ļ–∂–Ķ –Ĺ–į–Ī–Ľ—é–ī–į–Ķ—ā—Ā—Ź —É —á–Ķ–Ľ–ĺ–≤–Ķ–ļ–į – –ź–ú–ď –∑–į—Č–ł—Č–į–Ķ—ā –°–ě –∂–Ķ–Ľ—É–ī–ļ–į –ĺ—ā –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź —ć—ā–į–Ĺ–ĺ–Ľ–ĺ–ľ, –Ņ—Ä–ł —ć—ā–ĺ–ľ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –ź–ú–ď —Ā—Ä–į–≤–Ĺ–ł–ľ–į —Ā —ā–į–ļ–ĺ–≤–ĺ–Ļ –ľ–ł–∑–ĺ–Ņ—Ä–ĺ—Ā—ā–ĺ–Ľ–į [33]. –ó–į—Č–ł—ā–į –°–ě –∂–Ķ–Ľ—É–ī–ļ–į, –Ņ–ĺ-–≤–ł–ī–ł–ľ–ĺ–ľ—É, –ĺ–Ī—É—Ā–Ľ–ĺ–≤–Ľ–Ķ–Ĺ–į –Ĺ–į–Ľ–ł—á–ł–Ķ–ľ –≤–į–Ĺ–ł–Ľ–ł–Ĺ–ĺ–≤–ĺ–Ļ –≥—Ä—É–Ņ–Ņ—č –≤ –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ–Ķ –ź–ú–ď, –Ī–Ľ–į–≥–ĺ–ī–į—Ä—Ź –ļ–ĺ—ā–ĺ—Ä–ĺ–Ļ –ź–ú–ď —Ā–≤—Ź–∑—č–≤–į–Ķ—ā—Ā—Ź —Ā —Ä–Ķ—Ü–Ķ–Ņ—ā–ĺ—Ä–į–ľ–ł –ļ–į–Ņ—Ā–į–ł—Ü–ł–Ĺ–į –ł –≤—č–∑—č–≤–į–Ķ—ā –≤—č—Ā–≤–ĺ–Ī–ĺ–∂–ī–Ķ–Ĺ–ł–Ķ –Ī–Ķ–Ľ–ļ–į CGRP (Calcitonin Gene Related Peptide – –Ņ–Ķ–Ņ—ā–ł–ī, —Ä–ĺ–ī—Ā—ā–≤–Ķ–Ĺ–Ĺ—č–Ļ –ļ–į–Ľ—Ć—Ü–ł—ā–ĺ–Ĺ–ł–Ĺ—É) —Ā –Ņ–ĺ—Ā–Ľ–Ķ–ī—É—é—Č–ł–ľ —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł–Ķ–ľ –≤—č—Ä–į–Ī–ĺ—ā–ļ–ł –ĺ–ļ—Ā–ł–ī–į –į–∑–ĺ—ā–į (NO), —á—ā–ĺ –ļ–ĺ–ľ–Ņ–Ķ–Ĺ—Ā–ł—Ä—É–Ķ—ā —ć—Ą—Ą–Ķ–ļ—ā –ī–Ķ—Ą–ł—Ü–ł—ā–į –ü–ď –ł–∑-–∑–į –ł–Ĺ–≥–ł–Ī–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –¶–ě–ď [34]. –ź–ļ—ā–ł–≤–į—Ü–ł—Ź —Ä–Ķ—Ü–Ķ–Ņ—ā–ĺ—Ä–ĺ–≤ –ļ–į–Ņ—Ā–į–ł—Ü–ł–Ĺ–į –Ņ—Ä–ĺ–ł—Ā—Ö–ĺ–ī–ł—ā –Ņ—Ä–ł –Ņ—Ä—Ź–ľ–ĺ–ľ –ļ–ĺ–Ĺ—ā–į–ļ—ā–Ķ –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ —ć—ā–ĺ–≥–ĺ –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –≤–Ķ—Č–Ķ—Ā—ā–≤–į —Ā–ĺ –°–ě –∂–Ķ–Ľ—É–ī–ļ–į, –Ņ–ĺ—ć—ā–ĺ–ľ—É –ľ–į–ļ—Ā–ł–ľ–į–Ľ—Ć–Ĺ–ĺ–Ķ –Ņ—Ä–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł–Ķ –ī–į–Ĺ–Ĺ–ĺ–≥–ĺ —ć—Ą—Ą–Ķ–ļ—ā–į –Ĺ–į–Ī–Ľ—é–ī–į–Ķ—ā—Ā—Ź –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –ź–ú–ď –Ĺ–į—ā–ĺ—Č–į–ļ. –í —Ā–≤—Ź–∑–ł —Ā —ć—ā–ł–ľ –≤ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ņ—Ä–į–ļ—ā–ł–ļ–Ķ –ľ–ĺ–∂–Ĺ–ĺ —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–ĺ–≤–į—ā—Ć –Ņ—Ä–ł–Ķ–ľ –ź–ú–ď –Ĺ–į—ā–ĺ—Č–į–ļ –ī–Ľ—Ź –ī–ĺ—Ā—ā–ł–∂–Ķ–Ĺ–ł—Ź –Ľ—É—á—ą–Ķ–Ļ –≥–į—Ā—ā—Ä–ĺ–Ņ—Ä–ĺ—ā–Ķ–ļ—ā–ł–≤–Ĺ–ĺ–Ļ –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł. –° —É—á–Ķ—ā–ĺ–ľ –≤—Ā–Ķ—Ö –ĺ–Ņ–ł—Ā–į–Ĺ–Ĺ—č—Ö –≤—č—ą–Ķ —Ą–į–ļ—ā–ĺ—Ä–ĺ–≤ –Ĺ–į—ą–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –Ī—č–Ľ–ĺ —Ä–į–∑—Ä–į–Ī–ĺ—ā–į–Ĺ–ĺ —Ā —Ü–Ķ–Ľ—Ć—é —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—Ź –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł –ī–Ľ—Ź –Ė–ö–Ę –ł –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –ź–ú–ď –ł —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į – —ą–ł—Ä–ĺ–ļ–ĺ —Ä–į—Ā–Ņ—Ä–ĺ—Ā—ā—Ä–į–Ĺ–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –ł –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ–≥–ĺ –ī–Ľ—Ź –Ė–ö–Ę —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ–ĺ–≥–ĺ –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–į –¶–ě–ď-2 –ī–Ľ—Ź –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā —Ä–Ķ–≤–ľ–į—ā–ĺ–ł–ī–Ĺ—č–ľ –į—Ä—ā—Ä–ł—ā–ĺ–ľ.
–ü–į—Ü–ł–Ķ–Ĺ—ā—č –ł –ľ–Ķ—ā–ĺ–ī—č
–ü–į—Ü–ł–Ķ–Ĺ—ā—č
–í –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –Ī—č–Ľ–ł –≤–ļ–Ľ—é—á–Ķ–Ĺ—č –į–ľ–Ī—É–Ľ–į—ā–ĺ—Ä–Ĺ—č–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č –Ľ—é–Ī–ĺ–≥–ĺ –Ņ–ĺ–Ľ–į –≤ –≤–ĺ–∑—Ä–į—Ā—ā–Ķ –Ī–ĺ–Ľ–Ķ–Ķ 18 –Ľ–Ķ—ā, –ļ–ĺ—ā–ĺ—Ä—č–Ķ —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤—É—é—ā –ļ—Ä–ł—ā–Ķ—Ä–ł—Ź–ľ –ź–ľ–Ķ—Ä–ł–ļ–į–Ĺ—Ā–ļ–ĺ–≥–ĺ –ļ–ĺ–ľ–ł—ā–Ķ—ā–į —Ä–Ķ–≤–ľ–į—ā–ĺ–Ľ–ĺ–≥–ł–ł (ACR) –Ņ–ĺ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ī–ł–į–≥–Ĺ–ĺ—Ā—ā–ł–ļ–Ķ —Ä–Ķ–≤–ľ–į—ā–ĺ–ł–ī–Ĺ–ĺ–≥–ĺ –į—Ä—ā—Ä–ł—ā–į –≤ –ĺ—Ā—ā—Ä–ĺ–Ļ —Ą–į–∑–Ķ —Ā —Ą—É–Ĺ–ļ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ–ĺ–Ļ –ļ–Ľ–į—Ā—Ā–ł—Ą–ł–ļ–į—Ü–ł–Ķ–Ļ I–III, –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–ĺ—Ā—ā—Ć—é –Ņ—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ–ł—Ź –Ī–ĺ–Ľ–Ķ–Ķ –Ņ—Ä–ĺ–ī–ĺ–Ľ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł —Ā –Ņ—Ä–ł–Ķ–ľ–ĺ–ľ –Ě–ü–í–ü.
–ü–į—Ü–ł–Ķ–Ĺ—ā—č –Ĺ–Ķ –Ī—č–Ľ–ł –≤–ļ–Ľ—é—á–Ķ–Ĺ—č –≤ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ, –Ķ—Ā–Ľ–ł —É –Ĺ–ł—Ö –Ī—č–Ľ–ł –ĺ–Ī–Ĺ–į—Ä—É–∂–Ķ–Ĺ—č –ī—Ä—É–≥–ł–Ķ —Ä–Ķ–≤–ľ–į—ā–ł—á–Ķ—Ā–ļ–ł–Ķ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź, –Ņ—Ā–ĺ—Ä–ł–į–∑, –Ĺ–Ķ–ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ–ł—Ä—É–Ķ–ľ—č–Ļ –ī–ł–į–Ī–Ķ—ā, –≥–ł–Ņ–Ķ—Ä—ā–ł—Ä–Ķ–ĺ–∑ —Ā –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł–Ķ–ľ –į–ī–Ķ–ļ–≤–į—ā–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł, —Ā–Ķ—Ä—Ć–Ķ–∑–Ĺ–ĺ–Ķ –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł–Ķ —Ą—É–Ĺ–ļ—Ü–ł–ł –Ņ–ĺ—á–Ķ–ļ (—É—Ä–ĺ–≤–Ķ–Ĺ—Ć –ļ—Ä–Ķ–į—ā–ł–Ĺ–ł–Ĺ–į –≤ –Ņ–Ľ–į–∑–ľ–Ķ >1,5 –ľ–≥/–ī–Ľ), –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł–Ķ —Ą—É–Ĺ–ļ—Ü–ł–ł –Ņ–Ķ—á–Ķ–Ĺ–ł (–∑–Ĺ–į—á–Ķ–Ĺ–ł—Ź –į—Ā–Ņ–į—Ä—ā–į—ā–į–ľ–ł–Ĺ–ĺ—ā—Ä–į–Ĺ—Ā—Ą–Ķ—Ä–į–∑—č –ł–Ľ–ł –į–Ľ–į–Ĺ–ł–Ĺ–į–ľ–ł–Ĺ–ĺ—ā—Ä–į–Ĺ—Ā—Ą–Ķ—Ä–į–∑—č –Ī–ĺ–Ľ–Ķ–Ķ —á–Ķ–ľ –≤ 2 —Ä–į–∑–į –Ī–ĺ–Ľ—Ć—ą–Ķ –≤–Ķ—Ä—Ö–Ĺ–Ķ–≥–ĺ –Ņ—Ä–Ķ–ī–Ķ–Ľ–į –Ĺ–ĺ—Ä–ľ—č), –Ĺ–Ķ–≤—Ä–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł–Ķ, –≥–Ķ–ľ–į—ā–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł–Ķ –ł–Ľ–ł –į—É—ā–ĺ–ł–ľ–ľ—É–Ĺ–Ĺ—č–Ķ (–ĺ—ā–Ľ–ł—á–Ĺ—č–Ķ –ĺ—ā —Ä–Ķ–≤–ľ–į—ā–ĺ–ł–ī–Ĺ–ĺ–≥–ĺ –į—Ä—ā—Ä–ł—ā–į) –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź, —Ä–į–ļ –ł–Ľ–ł –ļ–į–ļ–ł–Ķ-–Ľ–ł–Ī–ĺ —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ķ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź. –ü–į—Ü–ł–Ķ–Ĺ—ā—č —ā–į–ļ–∂–Ķ –Ĺ–Ķ –Ī—č–Ľ–ł –≤–ļ–Ľ—é—á–Ķ–Ĺ—č –≤ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –Ņ—Ä–ł –Ĺ–į–Ľ–ł—á–ł–ł –≤ –į–Ĺ–į–ľ–Ĺ–Ķ–∑–Ķ —Ź–∑–≤—č, –∂–Ķ–Ľ—É–ī–ĺ—á–Ĺ–ĺ–≥–ĺ –ļ—Ä–ĺ–≤–ĺ—ā–Ķ—á–Ķ–Ĺ–ł—Ź –ł–Ľ–ł –ļ–į–ļ–ĺ–≥–ĺ-–Ľ–ł–Ī–ĺ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź –°–ě –≤–Ķ—Ä—Ö–Ĺ–ł—Ö –ĺ—ā–ī–Ķ–Ľ–ĺ–≤ –Ė–ö–Ę (—ā. –Ķ. >10 —Ź–∑–≤ –≤ –∂–Ķ–Ľ—É–ī–ļ–Ķ –ł/–ł–Ľ–ł –≤ –Ē–ü–ö; —Ź–∑–≤—č –Ņ–ł—Č–Ķ–≤–ĺ–ī–į, –∂–Ķ–Ľ—É–ī–ļ–į –ł–Ľ–ł –Ē–ü–ö). –Ē—Ä—É–≥–ł–ľ–ł –ļ—Ä–ł—ā–Ķ—Ä–ł—Ź–ľ–ł –ł—Ā–ļ–Ľ—é—á–Ķ–Ĺ–ł—Ź —Ź–≤–Ľ—Ź–Ľ–ł—Ā—Ć —ā–Ķ—Ä–į–Ņ–ł—Ź —Ā –Ņ—Ä–ł–Ķ–ľ–ĺ–ľ —Ā—ā–Ķ—Ä–ĺ–ł–ī–ĺ–≤ –≤ –ī–ĺ–∑–į—Ö –Ī–ĺ–Ľ—Ć—ą–Ķ, —á–Ķ–ľ —ć–ļ–≤–ł–≤–į–Ľ–Ķ–Ĺ—ā 7,5 –ľ–≥/—Ā—É—ā –Ņ—Ä–Ķ–ī–Ĺ–ł–∑–ĺ–Ľ–ĺ–Ĺ–į; –ł–Ĺ–ł—Ü–ł–į—Ü–ł—Ź —ā–Ķ—Ä–į–Ņ–ł–ł –ł–Ľ–ł –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ –Ņ—Ä–ł–Ķ–ľ–į –ī–ĺ–∑—č –ļ–į–ļ–ĺ–≥–ĺ-–Ľ–ł–Ī–ĺ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į –ļ–Ľ–į—Ā—Ā–ĺ–≤ DMARD –ł/–ł–Ľ–ł DCARD (Disease–Controlling Anti-Rheumatic Drug – –į–Ĺ—ā–ł—Ä–Ķ–≤–ľ–į—ā–ł—á–Ķ—Ā–ļ–ł–Ļ –õ–°, –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ–ł—Ä—É—é—Č–ł–Ļ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ķ) –≤ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ 90 –ī–Ĺ–Ķ–Ļ –Ņ–Ķ—Ä–Ķ–ī –Ĺ–į—á–į–Ľ–ĺ–ľ –ł –≤ —Ö–ĺ–ī–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź; –Ņ—Ä–ł–Ķ–ľ –Ņ—Ä–ĺ—ā–ł–≤–ĺ—Ź–∑–≤–Ķ–Ĺ–Ĺ—č—Ö –õ–°; –į–Ľ–Ľ–Ķ—Ä–≥–ł—Ź, —á—É–≤—Ā—ā–≤–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā—Ć –ł–Ľ–ł –Ĺ–Ķ–Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā—Ć –ł—Ā—Ā–Ľ–Ķ–ī—É–Ķ–ľ—č—Ö –õ–° –ł/–ł–Ľ–ł –ł—Ö –ł–Ĺ–≥—Ä–Ķ–ī–ł–Ķ–Ĺ—ā–ĺ–≤; –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ –Ņ—Ä–ĺ—ā–ł–≤–ĺ–ĺ–Ņ—É—Ö–ĺ–Ľ–Ķ–≤—č—Ö –õ–° (–ĺ—ā–Ľ–ł—á–Ĺ—č—Ö –ĺ—ā –ľ–Ķ—ā–ĺ—ā—Ä–Ķ–ļ—Ā–į—ā–į –ī–Ľ—Ź —ā–Ķ—Ä–į–Ņ–ł–ł –į—Ä—ā—Ä–ł—ā–į) –≤ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ 30 –ī–Ĺ–Ķ–Ļ –ī–ĺ –Ĺ–į—á–į–Ľ–į –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź; –Ĺ–į–Ľ–ł—á–ł–Ķ –≤ –į–Ĺ–į–ľ–Ĺ–Ķ–∑–Ķ –∑–Ľ–ĺ—É–Ņ–ĺ—ā—Ä–Ķ–Ī–Ľ–Ķ–Ĺ–ł—Ź –į–Ľ–ļ–ĺ–≥–ĺ–Ľ–Ķ–ľ –ł–Ľ–ł –õ–°; –Ī–Ķ—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ–ĺ—Ā—ā—Ć –ł–Ľ–ł –Ľ–į–ļ—ā–į—Ü–ł—Ź.
–ö–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤
–í—Ā–Ķ–≥–ĺ 304 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į (–Ņ–ĺ 152 –≤ –ļ–į–∂–ī–ĺ–Ļ –≥—Ä—É–Ņ–Ņ–Ķ —ā–Ķ—Ä–į–Ņ–ł–ł) –Ī—č–Ľ–ł —Ä–į–Ĺ–ī–ĺ–ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ—č –ī–Ľ—Ź –ī–ĺ—Ā—ā–ł–∂–Ķ–Ĺ–ł—Ź 90% –ľ–ĺ—Č–Ĺ–ĺ—Ā—ā–ł —Ā —É—á–Ķ—ā–ĺ–ľ –Ņ—Ä–ĺ—Ü–Ķ–Ĺ—ā–į –Ě–Į —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ė–ö–Ę –Ņ—Ä–ł –ĺ–Ī–ĺ–ł—Ö –≤–į—Ä–ł–į–Ĺ—ā–į—Ö —ā–Ķ—Ä–į–Ņ–ł–ł –ł –ĺ–∂–ł–ī–į–Ķ–ľ–ĺ–ľ –≤—č—Ö–ĺ–ī–Ķ –ł–∑ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –ĺ—ā–ī–Ķ–Ľ—Ć–Ĺ—č—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤. –í —Ā–≤—Ź–∑–ł —Ā —ā–Ķ–ľ, —á—ā–ĺ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –≤—č—ą–Ľ–ł –ł–∑ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź, –Ī—č–Ľ–ĺ –ľ–Ķ–Ĺ—Ć—ą–Ķ, —á–Ķ–ľ –ĺ–∂–ł–ī–į–Ľ–ĺ—Ā—Ć, —Ä–į–∑–ľ–Ķ—Ä –Ņ–ĺ–Ņ—É–Ľ—Ź—Ü–ł–ł –Ī—č–Ľ –Ņ–Ķ—Ä–Ķ—Ā—á–ł—ā–į–Ĺ, –ł –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –Ī—č–Ľ–ĺ –Ņ—Ä–Ķ–ļ—Ä–į—Č–Ķ–Ĺ–ĺ –Ņ–ĺ—Ā–Ľ–Ķ —Ä–į–Ĺ–ī–ĺ–ľ–ł–∑–į—Ü–ł–ł 235 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ (118 – –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į –ź–ú–ď –ł 117 – –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į).
–Ē–ł–∑–į–Ļ–Ĺ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź
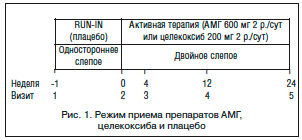
–≠—ā–ĺ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ —Ź–≤–Ľ—Ź–Ľ–ĺ—Ā—Ć –ľ–Ĺ–ĺ–≥–ĺ—Ü–Ķ–Ĺ—ā—Ä–ĺ–≤—č–ľ –ī–≤–ĺ–Ļ–Ĺ—č–ľ —Ā–Ľ–Ķ–Ņ—č–ľ —Ā –ī–≤–ĺ–Ļ–Ĺ—č–ľ –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ–Ķ–ľ –Ņ–Ľ–į—Ü–Ķ–Ī–ĺ, –į–ļ—ā–ł–≤–Ĺ–ĺ–ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ–ł—Ä—É–Ķ–ľ—č–ľ, —Ä–į–Ĺ–ī–ĺ–ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–ľ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ–ľ –≤ –Ņ–į—Ä–į–Ľ–Ľ–Ķ–Ľ—Ć–Ĺ—č—Ö –≥—Ä—É–Ņ–Ņ–į—Ö. –ě–Ĺ–ĺ —Ā–ĺ—Ā—ā–ĺ—Ź–Ľ–ĺ –ł–∑ 2-—Ö —Ą–į–∑: —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł—Ź –≤–Ķ—Ä—Ö–Ĺ–ł—Ö –ĺ—ā–ī–Ķ–Ľ–ĺ–≤ –Ė–ö–Ę – —Ā–Ľ–Ķ–Ņ–ĺ–Ļ –Ņ–Ľ–į—Ü–Ķ–Ī–ĺ-–ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ–ł—Ä—É–Ķ–ľ—č–Ļ –Ņ–Ķ—Ä–ł–ĺ–ī (1 –Ĺ–Ķ–ī.) –ł –ī–≤–ĺ–Ļ–Ĺ–ĺ–Ļ —Ā–Ľ–Ķ–Ņ–ĺ–Ļ –Ņ–Ķ—Ä–ł–ĺ–ī –į–ļ—ā–ł–≤–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł (24 –Ĺ–Ķ–ī.). –ü—Ä–ł –Ņ–ĺ–ľ–ĺ—Č–ł –ļ–ĺ–ľ–Ņ—Ć—é—ā–Ķ—Ä–Ĺ–ĺ–≥–ĺ —Ä–į–Ĺ–ī–ĺ–ľ–ł–∑–į—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–≥–ĺ —Ā–Ņ–ł—Ā–ļ–į (1:1) –≤ –ļ–ĺ–ĺ—Ä–ī–ł–Ĺ–ł—Ä—É—é—Č–Ķ–ľ —Ü–Ķ–Ĺ—ā—Ä–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į–ľ –Ī—č–Ľ –Ĺ–į–∑–Ĺ–į—á–Ķ–Ĺ –ĺ–ī–ł–Ĺ –ł–∑ –≤–į—Ä–ł–į–Ĺ—ā–ĺ–≤ —ā–Ķ—Ä–į–Ņ–ł–ł: –Ņ—Ä–ł–Ķ–ľ —ā–į–Ī–Ľ–Ķ—ā–ĺ–ļ –ź–ú–ď 600 –ľ–≥ 2 —Ä./—Ā—É—ā –ł–Ľ–ł –ļ–į–Ņ—Ā—É–Ľ —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į 200 –ľ–≥ 2 —Ä./—Ā—É—ā. –ü—Ä–ł–Ķ–ľ —ā–į–Ī–Ľ–Ķ—ā–ĺ–ļ –ź–ú–ď –ĺ—Ā—É—Č–Ķ—Ā—ā–≤–Ľ—Ź–Ľ—Ā—Ź —á–Ķ—Ä–Ķ–∑ 2–3 —á –Ņ–ĺ—Ā–Ľ–Ķ –Ķ–ī—č, –į –Ņ—Ä–ł–Ķ–ľ –ļ–į–Ņ—Ā—É–Ľ —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į – –Ĺ–Ķ–∑–į–≤–ł—Ā–ł–ľ–ĺ –ĺ—ā –Ņ—Ä–ł–Ķ–ľ–į –Ņ–ł—Č–ł (—Ä–ł—Ā. 1).
–ü–Ķ—Ä–Ķ–ī –≤–ļ–Ľ—é—á–Ķ–Ĺ–ł–Ķ–ľ –≤ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –Ņ–ĺ–Ľ—É—á–ł–Ľ–ł –Ņ–ĺ–ī—Ä–ĺ–Ī–Ĺ—č–Ķ –ĺ–Ī—ä—Ź—Ā–Ĺ–Ķ–Ĺ–ł—Ź –ĺ —Ö–į—Ä–į–ļ—ā–Ķ—Ä–Ķ –ł —Ü–Ķ–Ľ–ł –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź, –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–ł–Ľ–ł –Ņ–ł—Ā—Ć–ľ–Ķ–Ĺ–Ĺ–ĺ–Ķ –ł–Ĺ—Ą–ĺ—Ä–ľ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–Ķ —Ā–ĺ–≥–Ľ–į—Ā–ł–Ķ –ł –Ņ—Ä–ĺ—ą–Ľ–ł —Ą–ł–∑–ł–ļ–į–Ľ—Ć–Ĺ–ĺ–Ķ –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ, —Ā–ī–į–Ľ–ł –Ľ–į–Ī–ĺ—Ä–į—ā–ĺ—Ä–Ĺ—č–Ķ –į–Ĺ–į–Ľ–ł–∑—č. –í–ł–∑–ł—ā—č –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ł—Ā—Ć –Ĺ–į 4, 12 –ł 24 –Ĺ–Ķ–ī. –Ņ–ĺ—Ā–Ľ–Ķ –Ĺ–į—á–į–Ľ–į –ĺ–Ī–ĺ–ł—Ö –≤–į—Ä–ł–į–Ĺ—ā–ĺ–≤ —ā–Ķ—Ä–į–Ņ–ł–ł. –≠—ā–ĺ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –Ī—č–Ľ–ĺ –Ņ—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ–ĺ –≤ —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–ł–ł —Ā —ā–Ķ–ļ—É—Č–Ķ–Ļ –≤–Ķ—Ä—Ā–ł–Ķ–Ļ —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–į—Ü–ł–Ļ ICH-GCP –ł –•–Ķ–Ľ—Ć—Ā–ł–Ĺ–ļ—Ā–ļ–ĺ–Ļ –ī–Ķ–ļ–Ľ–į—Ä–į—Ü–ł–Ķ–Ļ, —É—ā–≤–Ķ—Ä–∂–ī–Ķ–Ĺ–ĺ –Ĺ–į—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ—č–ľ–ł —Ä–Ķ–≥—É–Ľ—Ź—ā–ĺ—Ä–Ĺ—č–ľ–ł –ĺ—Ä–≥–į–Ĺ–į–ľ–ł –≤ –ļ–į–∂–ī–ĺ–Ļ —Ā—ā—Ä–į–Ĺ–Ķ –ł –ĺ–ī–ĺ–Ī—Ä–Ķ–Ĺ–ĺ –ľ–Ķ—Ā—ā–Ĺ—č–ľ —ć—ā–ł—á–Ķ—Ā–ļ–ł–ľ –ļ–ĺ–ľ–ł—ā–Ķ—ā–ĺ–ľ –ł –ļ–ĺ–ľ–ł—ā–Ķ—ā–ĺ–ľ –Ņ–ĺ –õ–° –≤ –ļ–į–∂–ī–ĺ–ľ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–ľ —Ü–Ķ–Ĺ—ā—Ä–Ķ.
–°–ĺ–Ņ—É—ā—Ā—ā–≤—É—é—Č–į—Ź —ā–Ķ—Ä–į–Ņ–ł—Ź
–ü—Ä–ł–Ķ–ľ —Ā–ĺ–Ņ—É—ā—Ā—ā–≤—É—é—Č–ł—Ö –õ–° (–∑–į –ł—Ā–ļ–Ľ—é—á–Ķ–Ĺ–ł–Ķ–ľ –õ–°, –Ņ–Ķ—Ä–Ķ—á–ł—Ā–Ľ–Ķ–Ĺ–Ĺ—č—Ö –≤ –ļ—Ä–ł—ā–Ķ—Ä–ł—Ź—Ö –ł—Ā–ļ–Ľ—é—á–Ķ–Ĺ–ł—Ź), –ļ–ĺ—ā–ĺ—Ä—č–Ķ –Ī—č–Ľ–ł —Ä–į—Ā—Ü–Ķ–Ĺ–Ķ–Ĺ—č –ļ–į–ļ –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ—č–Ķ –ī–Ľ—Ź –∑–ī–ĺ—Ä–ĺ–≤—Ć—Ź –ł —Ö–ĺ—Ä–ĺ—ą–Ķ–≥–ĺ —Ā–į–ľ–ĺ—á—É–≤—Ā—ā–≤–ł—Ź –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į, –ĺ—Ā—É—Č–Ķ—Ā—ā–≤–Ľ—Ź–Ľ—Ā—Ź –Ņ—Ä–ł —Ā–ĺ–≥–Ľ–į—Ā–ł–ł –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į—ā–Ķ–Ľ—Ź.
–ě—Ü–Ķ–Ĺ–ļ–į –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł
–ü–Ķ—Ä–≤–ł—á–Ĺ—č–ľ–ł –ļ—Ä–ł—ā–Ķ—Ä–ł—Ź–ľ–ł –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł —Ź–≤–Ľ—Ź–Ľ–ł—Ā—Ć –∂–Ķ–Ľ—É–ī–ĺ—á–Ĺ—č–Ķ –ł/–ł–Ľ–ł –ī—É–ĺ–ī–Ķ–Ĺ–į–Ľ—Ć–Ĺ—č–Ķ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź (—ć—Ä–ĺ–∑–ł–ł, —Ź–∑–≤—č), –ī–ł–į–≥–Ĺ–ĺ—Ā—ā–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–Ķ –ľ–Ķ—ā–ĺ–ī–ĺ–ľ —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł–ł –≤–Ķ—Ä—Ö–Ĺ–ł—Ö –ĺ—ā–ī–Ķ–Ľ–ĺ–≤ –Ė–ö–Ę, –≤—č–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ–Ĺ–ĺ–Ļ –≤ –Ĺ–į—á–į–Ľ–Ķ –ł –≤ –ļ–ĺ–Ĺ—Ü–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź; –ĺ—Ü–Ķ–Ĺ–ļ–į –Ī—č–Ľ–į —Ā–ī–Ķ–Ľ–į–Ĺ–į –Ĺ–į –ĺ—Ā–Ĺ–ĺ–≤–į–Ĺ–ł–ł –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –Ņ–ł—Č–Ķ–≤–ĺ–ī–į, –∂–Ķ–Ľ—É–ī–ļ–į, –Ņ–ł–Ľ–ĺ—Ä–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –ļ–į–Ĺ–į–Ľ–į –ł –Ē–ü–ö.
–†–Ķ–∑—É–Ľ—Ć—ā–į—ā—č —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł–ł –Ī—č–Ľ–ł –ĺ—Ü–Ķ–Ĺ–Ķ–Ĺ—č –≤ –Ī–į–Ľ–Ľ–į—Ö –ĺ—ā 0 –ī–ĺ 7 —Ā–Ľ–Ķ–ī—É—é—Č–ł–ľ –ĺ–Ī—Ä–į–∑–ĺ–ľ:
0 – –Ĺ–ĺ—Ä–ľ–į–Ľ—Ć–Ĺ–į—Ź –°–ě;
1 – 1–10 –Ņ–Ķ—ā–Ķ—Ö–ł–Ļ;
2 – >10 –Ņ–Ķ—ā–Ķ—Ö–ł–Ļ;
3 – 1–3 —ć—Ä–ĺ–∑–ł–ł;
4 – 4–10 —ć—Ä–ĺ–∑–ł–Ļ;
5 – >10 —ć—Ä–ĺ–∑–ł–Ļ;
6 – –≤—č–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź –ł–Ľ–ł –Ĺ–į–Ľ–ł—á–ł–Ķ –ļ—Ä–ĺ–≤–ł –≤ –Ņ—Ä–ĺ—Ā–≤–Ķ—ā–Ķ –Ė–ö–Ę;
7 – —Ź–∑–≤–į –ł–Ľ–ł –ĺ–Ī–Ĺ–į–∂–Ķ–Ĺ–Ĺ—č–Ķ –ļ—Ä–ĺ–≤–Ķ–Ĺ–ĺ—Ā–Ĺ—č–Ķ —Ā–ĺ—Ā—É–ī—č.
–†–į–∑—Ä—č–≤ –°–ě –Ī–Ķ–∑ —Ą–ł–Ī—Ä–ĺ–∑–Ĺ—č—Ö –ĺ–Ī—Ä–į–∑–ĺ–≤–į–Ĺ–ł–Ļ –Ī—č–Ľ —Ä–į—Ā—Ü–Ķ–Ĺ–Ķ–Ĺ –ļ–į–ļ —ć—Ä–ĺ–∑–ł—Ź, –į –Ņ—Ä–ł –Ĺ–į–Ľ–ł—á–ł–ł —Ą–ł–Ī—Ä–ĺ–∑–Ĺ—č—Ö –ĺ–Ī—Ä–į–∑–ĺ–≤–į–Ĺ–ł–Ļ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–Ķ –°–ě –Ī—č–Ľ–ĺ –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ĺ –ļ–į–ļ —Ź–∑–≤–į. –Ď–į–Ľ–Ľ—č 0–2 –Ī—č–Ľ–ł —Ä–į—Ā—Ü–Ķ–Ĺ–Ķ–Ĺ—č –ļ–į–ļ –Ĺ–ĺ—Ä–ľ–į–Ľ—Ć–Ĺ—č–Ļ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā, –į –Ī–į–Ľ–Ľ—č 3–7 – –ļ–į–ļ –į–Ĺ–ĺ–ľ–į–Ľ—Ć–Ĺ—č–Ļ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā.
–Ē–Ľ—Ź –ļ–į–∂–ī–ĺ–≥–ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į —É—á–ł—ā—č–≤–į–Ľ—Ā—Ź –∂–Ķ–Ľ—É–ī–ĺ—á–Ĺ—č–Ļ –Ī–į–Ľ–Ľ (–Ĺ–į –ĺ—Ā–Ĺ–ĺ–≤–į–Ĺ–ł–ł —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–ĺ–≤ –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –°–ě –∂–Ķ–Ľ—É–ī–ļ–į) –ł –ī—É–ĺ–ī–Ķ–Ĺ–į–Ľ—Ć–Ĺ—č–Ļ –Ī–į–Ľ–Ľ (–Ĺ–į –ĺ—Ā–Ĺ–ĺ–≤–į–Ĺ–ł–ł —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–ĺ–≤ –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –Ņ–ł–Ľ–ĺ—Ä–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –ļ–į–Ĺ–į–Ľ–į –ł –ī—É–ĺ–ī–Ķ–Ĺ–į–Ľ—Ć–Ĺ–ĺ–Ļ –°–ě). –ö—Ä–ĺ–ľ–Ķ —ā–ĺ–≥–ĺ, –ī–Ľ—Ź –ļ–į–∂–ī–ĺ–≥–ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į —É—á–ł—ā—č–≤–į–Ľ—Ā—Ź –ľ–į–ļ—Ā–ł–ľ–į–Ľ—Ć–Ĺ—č–Ļ –≥–į—Ā—ā—Ä–ĺ–ī—É–ĺ–ī–Ķ–Ĺ–į–Ľ—Ć–Ĺ—č–Ļ –Ī–į–Ľ–Ľ – –Ĺ–į–ł–Ī–ĺ–Ľ–Ķ–Ķ –≤—č—Ā–ĺ–ļ–ł–Ļ –ł–∑ –∂–Ķ–Ľ—É–ī–ĺ—á–Ĺ–ĺ–≥–ĺ –ł–Ľ–ł –ī—É–ĺ–ī–Ķ–Ĺ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –Ī–į–Ľ–Ľ–į. –í—ā–ĺ—Ä–ł—á–Ĺ—č–ľ–ł –ļ—Ä–ł—ā–Ķ—Ä–ł—Ź–ľ–ł –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł —Ź–≤–Ľ—Ź–Ľ–ł—Ā—Ć: —Ā–ł–ľ–Ņ—ā–ĺ–ľ—č —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ė–ö–Ę, –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł—Ź —Ä–į–Ī–ĺ—ā—č —Ā–Ķ—Ä–ī—Ü–į —Ā–ĺ–≥–Ľ–į—Ā–Ĺ–ĺ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ –≠–ö–ď, –ĺ—ā–ļ–Ľ–ĺ–Ĺ–Ķ–Ĺ–ł—Ź –ĺ—ā –Ĺ–ĺ—Ä–ľ—č —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–ĺ–≤ –Ľ–į–Ī–ĺ—Ä–į—ā–ĺ—Ä–Ĺ—č—Ö –į–Ĺ–į–Ľ–ł–∑–ĺ–≤ –ļ—Ä–ĺ–≤–ł –ł –ľ–ĺ—á–ł, –Ě–Į. –°–ł–ľ–Ņ—ā–ĺ–ľ—č —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ė–ö–Ę (—ā–į–ļ–ł–Ķ –ļ–į–ļ –ł–∑–∂–ĺ–≥–į, —ć–Ņ–ł–≥–į—Ā—ā—Ä–į–Ľ—Ć–Ĺ–į—Ź –Ī–ĺ–Ľ—Ć –ł/–ł–Ľ–ł –Ī–ĺ–Ľ—Ć –≤ –∂–ł–≤–ĺ—ā–Ķ, —ā–ĺ—ą–Ĺ–ĺ—ā–į, —Ä–≤–ĺ—ā–į, –ī–ł—Ā–Ņ–Ķ–Ņ—Ā–ł—Ź, –ľ–Ķ—ā–Ķ–ĺ—Ä–ł–∑–ľ, –ī–ł–į—Ä–Ķ—Ź) –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–ł—Ā—Ć —Ā –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ–ľ —Ā–Ņ–Ķ—Ü–ł—Ą–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –ĺ–Ņ—Ä–ĺ—Ā–Ĺ–ł–ļ–į –≤ –Ĺ–į—á–į–Ľ–Ķ –ł –Ņ–ĺ—Ā–Ľ–Ķ 4, 12 –ł 24 –Ĺ–Ķ–ī. —ā–Ķ—Ä–į–Ņ–ł–ł.
–≠–ö–ď –≤ 12 –ĺ—ā–≤–Ķ–ī–Ķ–Ĺ–ł—Ź—Ö, –≥–Ķ–ľ–į—ā–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł–Ķ –ł –Ī–ł–ĺ—Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ł–Ķ –į–Ĺ–į–Ľ–ł–∑—č –ĺ–Ī—Ä–į–∑—Ü–ĺ–≤ –ļ—Ä–ĺ–≤–ł –ł –ľ–ĺ—á–ł –Ī—č–Ľ–ł –≤—č–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ—č –Ĺ–į—ā–ĺ—Č–į–ļ, –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–ł—Ā—Ć –≤ –Ĺ–į—á–į–Ľ–Ķ, –ļ–ĺ–Ĺ—Ü–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –ł–Ľ–ł –Ņ—Ä–ł –≤—č—Ö–ĺ–ī–Ķ –ł–∑ –Ĺ–Ķ–≥–ĺ. –í—Ā–Ķ –Ě–Į, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ł –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į—ā–Ķ–Ľ–ł –ł–Ľ–ł –ĺ –ļ–ĺ—ā–ĺ—Ä—č—Ö —Ā–ĺ–ĺ–Ī—Č–į–Ľ–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č, –Ī—č–Ľ–ł –∑–į—Ä–Ķ–≥–ł—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ—č –≤ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ –≤—Ā–Ķ–≥–ĺ –Ņ–Ķ—Ä–ł–ĺ–ī–į –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź.
–ě—Ü–Ķ–Ĺ–ļ–į —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł
–≠—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–į—Ā—Ć –≤ –Ĺ–į—á–į–Ľ–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –ł –Ņ–ĺ—Ā–Ľ–Ķ 4, 12 –ł 24 –Ĺ–Ķ–ī. —ā–Ķ—Ä–į–Ņ–ł–ł. –ú–Ķ—Ä–ĺ–Ļ –Ņ–Ķ—Ä–≤–ł—á–Ĺ–ĺ–≥–ĺ –ł—Ā—Ö–ĺ–ī–į –Ī—č–Ľ –ł–Ĺ–ī–Ķ–ļ—Ā ACR-20 [35, 36], –ļ–ĺ—ā–ĺ—Ä—č–Ļ –ĺ—ā—Ä–į–∂–į–Ķ—ā –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –ī–ĺ—Ā—ā–ł–≥–į—é—Č–ł—Ö 20% —É–Ľ—É—á—ą–Ķ–Ĺ–ł—Ź –Ņ–ĺ —á–ł—Ā–Ľ—É –Ī–ĺ–Ľ–Ķ–∑–Ĺ–Ķ–Ĺ–Ĺ—č—Ö –ł–Ľ–ł –ĺ–Ņ—É—Ö—ą–ł—Ö —Ā—É—Ā—ā–į–≤–ĺ–≤ –ł 20% —É–Ľ—É—á—ą–Ķ–Ĺ–ł–Ķ 3-—Ö –ł–∑ 5 —Ā–Ľ–Ķ–ī—É—é—Č–ł—Ö –ļ–Ľ—é—á–Ķ–≤—č—Ö –Ņ–į—Ä–į–ľ–Ķ—ā—Ä–ĺ–≤, —ā–į–ļ–ł—Ö –ļ–į–ļ –ĺ–Ī—Č–į—Ź –ĺ—Ü–Ķ–Ĺ–ļ–į –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–ľ, –ĺ–Ī—Č–į—Ź –ĺ—Ü–Ķ–Ĺ–ļ–į –≤—Ä–į—á–ĺ–ľ, –Ī–ĺ–Ľ—Ć, —Ą—É–Ĺ–ļ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ–į—Ź –Ĺ–Ķ–ī–Ķ–Ķ—Ā–Ņ–ĺ—Ā–ĺ–Ī–Ĺ–ĺ—Ā—ā—Ć, –ĺ–Ī–ĺ—Ā—ā—Ä–Ķ–Ĺ–ł–Ķ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź.
–ě–Ī—Č–į—Ź –ĺ—Ü–Ķ–Ĺ–ļ–į –≤—Ä–į—á–ĺ–ľ –ł –ĺ–Ī—Č–į—Ź –ĺ—Ü–Ķ–Ĺ–ļ–į –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–ľ –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–ł—Ā—Ć –≤ –Ī–į–Ľ–Ľ–į—Ö –ĺ—ā 1 (–ĺ—á–Ķ–Ĺ—Ć —Ö–ĺ—Ä–ĺ—ą–ĺ) –ī–ĺ 5 (–ĺ—á–Ķ–Ĺ—Ć –Ņ–Ľ–ĺ—Ö–ĺ); –Ņ—Ä–ł —ć—ā–ĺ–ľ –Ī–ĺ–Ľ–Ķ–Ķ –≤—č—Ā–ĺ–ļ–ł–Ķ –Ī–į–Ľ–Ľ—č –Ņ–ĺ–ļ–į–∑—č–≤–į–Ľ–ł –Ī–ĺ–Ľ—Ć—ą—É—é —Ā—ā–Ķ–Ņ–Ķ–Ĺ—Ć —ā—Ź–∂–Ķ—Ā—ā–ł –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź. –Ď–ĺ–Ľ—Ć –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–ł—Ā—Ć –≤ –Ī–į–Ľ–Ľ–į—Ö –Ņ–ĺ 4-–Ī–į–Ľ–Ľ—Ć–Ĺ–ĺ–Ļ —ą–ļ–į–Ľ–Ķ (—Ā—Ä–Ķ–ī–Ĺ—Ź—Ź, —É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ–į—Ź, —ā—Ź–∂–Ķ–Ľ–į—Ź, –ĺ–Ī–Ķ—Ā—Ā–ł–Ľ–ł–≤–į—é—Č–į—Ź). –§—É–Ĺ–ļ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ–į—Ź –ī–Ķ–Ķ—Ā–Ņ–ĺ—Ā–ĺ–Ī–Ĺ–ĺ—Ā—ā—Ć –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–į—Ā—Ć –≤ —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–ł–ł —Ā –ļ–Ľ–į—Ā—Ā–ł—Ą–ł–ļ–į—Ü–ł–Ķ–Ļ ACR [36].
–°—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ł–Ļ –į–Ĺ–į–Ľ–ł–∑
–°—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ł–Ļ –į–Ĺ–į–Ľ–ł–∑ –Ī—č–Ľ –≤—č–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ –ī–Ľ—Ź –≥—Ä—É–Ņ–Ņ—č –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ Per Protocol (PP), –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–Ĺ–ĺ–Ļ –ļ–į–ļ –≤—Ā–Ķ –Ņ–ĺ–Ľ—É—á–į–≤—ą–ł–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –∑–į–≤–Ķ—Ä—ą–ł–Ľ–ł –ī–į–Ĺ–Ĺ–ĺ–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ. –ü—Ä–ł –ĺ—Ü–Ķ–Ĺ–ļ–Ķ –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł –ī–Ľ—Ź –Ė–ö–Ę —ā–į–ļ–∂–Ķ –Ī—č–Ľ –≤—č–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ –į–Ĺ–į–Ľ–ł–∑ –ī–Ľ—Ź –≥—Ä—É–Ņ–Ņ—č –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ Intent-to-Treat (ITT), —ā. –Ķ. –≤—Ā–Ķ —Ä–į–Ĺ–ī–ĺ–ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –Ņ–ĺ–Ľ—É—á–ł–Ľ–ł –ļ–į–ļ –ľ–ł–Ĺ–ł–ľ—É–ľ –ĺ–ī–Ĺ—É –ī–ĺ–∑—É –ł—Ā—Ā–Ľ–Ķ–ī—É–Ķ–ľ–ĺ–≥–ĺ –õ–°. –°–ł–ľ–Ņ—ā–ĺ–ľ—č —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ė–ö–Ę –ł –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–Ķ –°–ě –ľ–ĺ–≥—É—ā —Ä–į–∑–≤–ł–≤–į—ā—Ć—Ā—Ź –ī–į–∂–Ķ –Ņ–ĺ—Ā–Ľ–Ķ –ĺ–ī–Ĺ–ĺ–ļ—Ä–į—ā–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ł–Ķ–ľ–į –Ě–ü–í–ü [8, 10]. –ü—Ä–ł –Ĺ–į–Ľ–ł—á–ł–ł –ĺ—ā—Ā—É—ā—Ā—ā–≤—É—é—Č–ł—Ö –ł–Ľ–ł –Ĺ–Ķ–ī–ĺ—Ā—ā—É–Ņ–Ĺ—č—Ö —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–ĺ–≤ –Ņ—Ä–ł–ľ–Ķ–Ĺ—Ź–Ľ—Ā—Ź –ľ–Ķ—ā–ĺ–ī —ć–ļ—Ā—ā—Ä–į–Ņ–ĺ–Ľ—Ź—Ü–ł–ł LOCF (Last Observation Carried Forward – –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–Ķ–≥–ĺ –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł—Ź –≤–Ņ–Ķ—Ä–Ķ–ī). –Ē–Ľ—Ź –≤—Ā–Ķ—Ö –ī–Ķ–ľ–ĺ–≥—Ä–į—Ą–ł—á–Ķ—Ā–ļ–ł—Ö –Ņ–Ķ—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ—č—Ö –Ī—č–Ľ –≤—č–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ –ĺ–Ņ–ł—Ā–į—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ –į–Ĺ–į–Ľ–ł–∑. –ź–Ĺ–į–Ľ–ł–∑ –ĺ—Ü–Ķ–Ĺ–ļ–ł –Ĺ–ĺ—Ä–ľ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ —Ä–į—Ā–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź –Ī—č–Ľ –Ņ—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ —Ā –Ņ–ĺ–ľ–ĺ—Č—Ć—é —ā–ĺ—á–Ĺ–ĺ–≥–ĺ —ā–Ķ—Ā—ā–į –§–ł—ą–Ķ—Ä–į –ł–Ľ–ł, –≥–ī–Ķ –Ņ—Ä–ł–ľ–Ķ–Ĺ–ł–ľ–ĺ, —Ā –Ņ–ĺ–ľ–ĺ—Č—Ć—é —ā–Ķ—Ā—ā–į –í–ł–Ľ–ļ–ĺ–ļ—Ā–ĺ–Ĺ–į –ī–Ľ—Ź 2-—Ö –ĺ–Ī—Ä–į–∑—Ü–ĺ–≤, —Ā —Ü–Ķ–Ľ—Ć—é –ĺ—Ü–Ķ–Ĺ–ļ–ł –≥–ĺ–ľ–ĺ–≥–Ķ–Ĺ–Ĺ–ĺ—Ā—ā–ł —Ā—Ä–Ķ–ī–Ĺ–ł—Ö –∑–Ĺ–į—á–Ķ–Ĺ–ł–Ļ –Ĺ–į –ł—Ā—Ö–ĺ–ī–Ĺ–ĺ–ľ —É—Ä–ĺ–≤–Ĺ–Ķ. –Ē–į–Ĺ–Ĺ—č–Ķ –ī–Ľ—Ź –į–Ĺ–į–Ľ–ł–∑–į –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł –Ī—č–Ľ–ł –ĺ—Ā–Ĺ–ĺ–≤–į–Ĺ—č –Ĺ–į —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł–ł –ī–ĺ–Ľ–Ķ–Ļ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź–ľ–ł –Ė–ö–Ę –ł –Ī–Ķ–∑ –Ĺ–ł—Ö. –ď–ł–Ņ–ĺ—ā–Ķ–∑–į –ĺ–Ī —ć–ļ–≤–ł–≤–į–Ľ–Ķ–Ĺ—ā–Ĺ–ĺ—Ā—ā–ł —á–į—Ā—ā–ĺ—ā –Ī—č–Ľ–į –Ņ—Ä–ĺ–≤–Ķ—Ä–Ķ–Ĺ–į —Ā –Ņ–ĺ–ľ–ĺ—Č—Ć—é —ā–ĺ—á–Ĺ–ĺ–≥–ĺ —ā–Ķ—Ā—ā–į –§–ł—ą–Ķ—Ä–į –ī–Ľ—Ź —ā–į–Ī–Ľ–ł—Ü –≤–Ķ—Ä–ĺ—Ź—ā–Ĺ–ĺ—Ā—ā–ł; —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—Ź –Ņ–į—Ä–į–ľ–Ķ—ā—Ä–ĺ–≤ –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł –≤–Ĺ—É—ā—Ä–ł –ł –ľ–Ķ–∂–ī—É –≥—Ä—É–Ņ–Ņ–į–ľ–ł –Ī—č–Ľ–ł –Ņ—Ä–ĺ—ā–Ķ—Ā—ā–ł—Ä–ĺ–≤–į–Ĺ—č —Ā –Ņ–ĺ–ľ–ĺ—Č—Ć—é —ā–ĺ—á–Ĺ–ĺ–≥–ĺ —ā–Ķ—Ā—ā–į –§–ł—ą–Ķ—Ä–į –ł, –≥–ī–Ķ –Ņ—Ä–ł–ľ–Ķ–Ĺ–ł–ľ–ĺ, —Ā –Ņ–ĺ–ľ–ĺ—Č—Ć—é —ā–Ķ—Ā—ā–į –ú–į–ļ-–Ě–Ķ–ľ–į—Ä –ł t-—ā–Ķ—Ā—ā–į –ī–Ľ—Ź –Ņ–į—Ä–Ĺ—č—Ö –ĺ–Ī—Ä–į–∑—Ü–ĺ–≤. –ü–į—Ä–į–ľ–Ķ—ā—Ä—č —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–ł—Ā—Ć —Ā –Ņ–ĺ–ľ–ĺ—Č—Ć—é —ā–ĺ—á–Ĺ–ĺ–≥–ĺ —ā–Ķ—Ā—ā–į –§–ł—ą–Ķ—Ä–į.
–°—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ł–Ķ —ā–Ķ—Ā—ā—č –Ī—č–Ľ–ł 2-—Ā—ā–ĺ—Ä–ĺ–Ĺ–Ĺ–ł–ľ–ł, —Ā 5% —É—Ä–ĺ–≤–Ĺ–Ķ–ľ –∑–Ĺ–į—á–ł–ľ–ĺ—Ā—ā–ł. –°—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ł–Ļ –į–Ĺ–į–Ľ–ł–∑ –Ī—č–Ľ –≤—č–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ —Ā –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ–ľ —Ā—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ņ—Ä–ĺ–≥—Ä–į–ľ–ľ—č SAS 8.2 –≤ —Ā—Ä–Ķ–ī–Ķ Windows.
–†–Ķ–∑—É–Ľ—Ć—ā–į—ā—č
–ü–į—Ü–ł–Ķ–Ĺ—ā—č
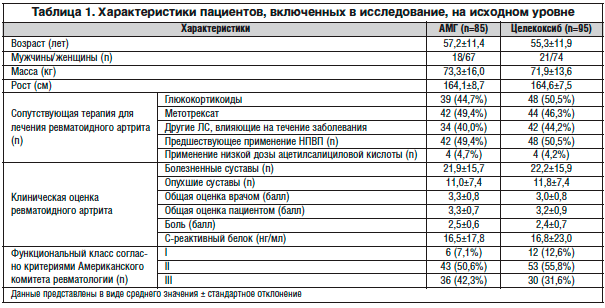
–Ē–į–Ĺ–Ĺ—č–Ļ –į–Ĺ–į–Ľ–ł–∑ –Ī—č–Ľ –≤—č–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ –ī–Ľ—Ź 180 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –∑–į–≤–Ķ—Ä—ą–ł–Ľ–ł –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ (85 – –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į –ź–ú–ď –ł 95 – –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į). –ü–į—Ü–ł–Ķ–Ĺ—ā—č, –Ĺ–Ķ –≤–ļ–Ľ—é—á–Ķ–Ĺ–Ĺ—č–Ķ –≤ –į–Ĺ–į–Ľ–ł–∑, –Ī—č–Ľ–ł —Ä–į—Ā—Ü–Ķ–Ĺ–Ķ–Ĺ—č –ļ–į–ļ –≤—č—ą–Ķ–ī—ą–ł–Ķ –ł–∑ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź. –Ē–Ķ–ľ–ĺ–≥—Ä–į—Ą–ł—á–Ķ—Ā–ļ–ł–Ķ –ł –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ķ —Ö–į—Ä–į–ļ—ā–Ķ—Ä–ł—Ā—ā–ł–ļ–ł —ć—ā–ł—Ö 2-—Ö –≥—Ä—É–Ņ–Ņ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ (—ā–į–Ī–Ľ. 1) —Ā–≤–ł–ī–Ķ—ā–Ķ–Ľ—Ć—Ā—ā–≤–ĺ–≤–į–Ľ–ł, —á—ā–ĺ –ĺ–Ĺ–ł –Ī—č–Ľ–ł –≤–Ņ–ĺ–Ľ–Ĺ–Ķ –≥–ĺ–ľ–ĺ–≥–Ķ–Ĺ–Ĺ—č.
–Ď–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā—Ć
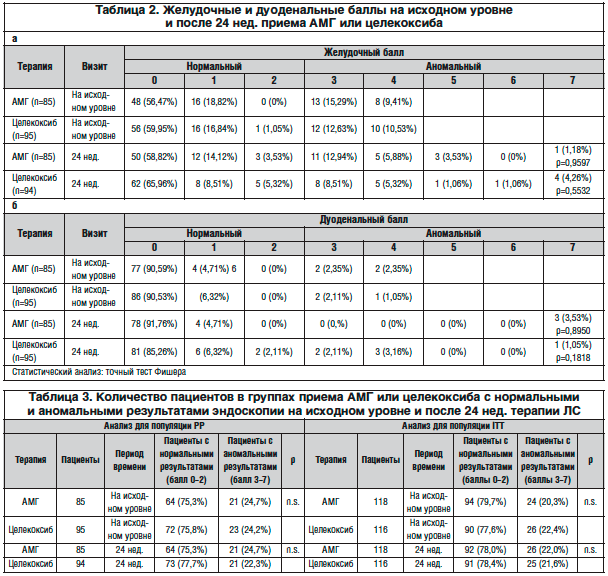
–≠–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł—Ź. –Ė–Ķ–Ľ—É–ī–ĺ—á–Ĺ—č–Ķ –ł –ī—É–ĺ–ī–Ķ–Ĺ–į–Ľ—Ć–Ĺ—č–Ķ –Ī–į–Ľ–Ľ—č –Ī—č–Ľ–ł –ĺ—Ü–Ķ–Ĺ–Ķ–Ĺ—č –Ņ–ĺ –ĺ—ā–ī–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā–ł –ł –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ–Ķ–Ĺ—č –≤ —ā–į–Ī–Ľ–ł—Ü–į—Ö 2a –ł 2–Ī, –į –≤ —ā–į–Ī–Ľ–ł—Ü–Ķ 3 –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ–Ķ–Ĺ—č –ī–į–Ĺ–Ĺ—č–Ķ –ĺ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ĺ–ĺ—Ä–ľ–į–Ľ—Ć–Ĺ—č–ľ–ł –ł–Ľ–ł –į–Ĺ–ĺ–ľ–į–Ľ—Ć–Ĺ—č–ľ–ł —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ–ł —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł–ł. –†–į–∑–Ľ–ł—á–ł—Ź –ľ–Ķ–∂–ī—É –ī–≤—É–ľ—Ź –≤–į—Ä–ł–į–Ĺ—ā–į–ľ–ł —ā–Ķ—Ä–į–Ņ–ł–ł –Ĺ–Ķ –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ł—Ā—Ć: —Ą–į–ļ—ā–ł—á–Ķ—Ā–ļ–ł –ĺ–Ī–Ķ –≥—Ä—É–Ņ–Ņ—č, –≥–ĺ–ľ–ĺ–≥–Ķ–Ĺ–Ĺ—č–Ķ –Ĺ–į –ł—Ā—Ö–ĺ–ī–Ĺ–ĺ–ľ —É—Ä–ĺ–≤–Ĺ–Ķ, –ĺ—Ā—ā–į–≤–į–Ľ–ł—Ā—Ć —Ā—Ä–į–≤–Ĺ–ł–ľ—č–ľ–ł –≤ –ļ–ĺ–Ĺ—Ü–Ķ —ā–Ķ—Ä–į–Ņ–ł–ł; –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –ź–ú–ď –ł —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į –Ĺ–Ķ –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ĺ—Ā—Ć —É—Ö—É–ī—ą–Ķ–Ĺ–ł–Ķ —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł—á–Ķ—Ā–ļ–ł—Ö —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–ĺ–≤. –ü—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –ĺ–Ī–ĺ–ł—Ö –õ–° –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ĺ–ĺ—Ä–ľ–į–Ľ—Ć–Ĺ—č–ľ –∂–Ķ–Ľ—É–ī–ĺ—á–Ĺ—č–ľ –Ī–į–Ľ–Ľ–ĺ–ľ —É–≤–Ķ–Ľ–ł—á–ł–≤–į–Ľ–ĺ—Ā—Ć, —Ö–ĺ—ā—Ź –ł –Ĺ–Ķ–∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ. –Ě–į –ł—Ā—Ö–ĺ–ī–Ĺ–ĺ–ľ —É—Ä–ĺ–≤–Ĺ–Ķ —É –≤—Ā–Ķ—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –į–Ĺ–ĺ–ľ–į–Ľ—Ć–Ĺ—č–ľ–ł –Ī–į–Ľ–Ľ–į–ľ–ł –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–į—Ā—Ć —ā–ĺ–Ľ—Ć–ļ–ĺ –∂–Ķ–Ľ—É–ī–ĺ—á–Ĺ–į—Ź —ć—Ä–ĺ–∑–ł—Ź (—ā. –Ķ. –Ī–į–Ľ–Ľ 3 –ł–Ľ–ł 4); –≤ –ļ–ĺ–Ĺ—Ü–Ķ —ā–Ķ—Ä–į–Ņ–ł–ł 1 –Ņ–į—Ü–ł–Ķ–Ĺ—ā –ł–∑ –≥—Ä—É–Ņ–Ņ—č –Ņ—Ä–ł–Ķ–ľ–į –ź–ú–ď –ł 4 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į –ł–∑ –≥—Ä—É–Ņ–Ņ—č –Ņ—Ä–ł–Ķ–ľ–į —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į –Ņ–ĺ–Ľ—É—á–ł–Ľ–ł –Ī–į–Ľ–Ľ 7, —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤—É—é—Č–ł–Ļ –Ĺ–į–Ľ–ł—á–ł—é —Ź–∑–≤—č –ł–Ľ–ł –ĺ–Ī–Ĺ–į–∂–Ķ–Ĺ–Ĺ—č—Ö –ļ—Ä–ĺ–≤–Ķ–Ĺ–ĺ—Ā–Ĺ—č—Ö —Ā–ĺ—Ā—É–ī–ĺ–≤. –í –ĺ—ā–Ĺ–ĺ—ą–Ķ–Ĺ–ł–ł –ī—É–ĺ–ī–Ķ–Ĺ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –Ī–į–Ľ–Ľ–į –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ĺ–ĺ—Ä–ľ–į–Ľ—Ć–Ĺ—č–ľ –Ī–į–Ľ–Ľ–ĺ–ľ —Ā–Ĺ–ł–∂–į–Ľ–ĺ—Ā—Ć –Ņ–ĺ—Ā–Ľ–Ķ —ā–Ķ—Ä–į–Ņ–ł–ł —Ā –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ–ľ –ź–ú–ď, –Ĺ–ĺ –Ņ–ĺ–≤—č—ą–į–Ľ–ĺ—Ā—Ć –Ņ–ĺ—Ā–Ľ–Ķ —ā–Ķ—Ä–į–Ņ–ł–ł —Ā –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ–ľ —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į. –í –ļ–ĺ–Ĺ—Ü–Ķ —ā–Ķ—Ä–į–Ņ–ł–ł –Ī—č–Ľ–ĺ 3 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į —Ā –į–Ĺ–ĺ–ľ–į–Ľ—Ć–Ĺ—č–ľ–ł –Ī–į–Ľ–Ľ–į–ľ–ł –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į –ź–ú–ď –ł 6 – –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į.
–•–į—Ä–į–ļ—ā–Ķ—Ä–ł—Ā—ā–ł–ļ–ł –Ĺ–į –ł—Ā—Ö–ĺ–ī–Ĺ–ĺ–ľ —É—Ä–ĺ–≤–Ĺ–Ķ –ľ–Ķ–∂–ī—É –≥—Ä—É–Ņ–Ņ–į–ľ–ł –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –Ĺ–Ķ –ĺ—ā–Ľ–ł—á–į–Ľ–ł—Ā—Ć. –ü—Ä–ł –ĺ—Ü–Ķ–Ĺ–ļ–Ķ –ľ–į–ļ—Ā–ł–ľ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –≥–į—Ā—ā—Ä–ĺ–ī—É–ĺ–ī–Ķ–Ĺ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –Ī–į–Ľ–Ľ–į –ł–∑ 64 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į –ź–ú–ď —Ā –Ĺ–ĺ—Ä–ľ–į–Ľ—Ć–Ĺ—č–ľ–ł —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ–ł —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł–ł –Ĺ–į –ł—Ā—Ö–ĺ–ī–Ĺ–ĺ–ľ —É—Ä–ĺ–≤–Ĺ–Ķ —É 54 —Ā–ĺ—Ö—Ä–į–Ĺ–ł–Ľ–ł—Ā—Ć –Ĺ–ĺ—Ä–ľ–į–Ľ—Ć–Ĺ—č–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –Ĺ–į –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–Ķ–ľ –≤–ł–∑–ł—ā–Ķ. –ė–∑ 21 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į, —É –ļ–ĺ—ā–ĺ—Ä—č—Ö —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā—č —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł–ł –Ĺ–į –ł—Ā—Ö–ĺ–ī–Ĺ–ĺ–ľ —É—Ä–ĺ–≤–Ĺ–Ķ –Ī—č–Ľ–ł –į–Ĺ–ĺ–ľ–į–Ľ—Ć–Ĺ—č–ľ–ł, —É 10 –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ĺ—Ā—Ć —É–Ľ—É—á—ą–Ķ–Ĺ–ł–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–ĺ–≤, –Ņ–ĺ –ł—ā–ĺ–≥–į–ľ –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–Ķ–≥–ĺ –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –ł—Ö —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā –Ĺ–į—Ö–ĺ–ī–ł–Ľ—Ā—Ź –≤ –Ņ—Ä–Ķ–ī–Ķ–Ľ–į—Ö –Ĺ–ĺ—Ä–ľ—č. –í –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į –ł–∑ 71 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į —Ā –Ĺ–ĺ—Ä–ľ–į–Ľ—Ć–Ĺ—č–ľ–ł —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ–ł —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł–ł –Ĺ–į –ł—Ā—Ö–ĺ–ī–Ĺ–ĺ–ľ —É—Ä–ĺ–≤–Ĺ–Ķ —É 61 —Ā–ĺ—Ö—Ä–į–Ĺ–ł–Ľ–ł—Ā—Ć –Ĺ–ĺ—Ä–ľ–į–Ľ—Ć–Ĺ—č–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –Ĺ–į –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–Ķ–ľ –≤–ł–∑–ł—ā–Ķ (1 –Ņ–į—Ü–ł–Ķ–Ĺ—ā –Ī—č–Ľ –ł—Ā–ļ–Ľ—é—á–Ķ–Ĺ –ł–∑-–∑–į –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł—Ź –ī–į–Ĺ–Ĺ—č—Ö –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–Ķ–Ļ —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł–ł). –ė–∑ 23 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, —É –ļ–ĺ—ā–ĺ—Ä—č—Ö —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā—č —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł–ł –Ĺ–į –ł—Ā—Ö–ĺ–ī–Ĺ–ĺ–ľ —É—Ä–ĺ–≤–Ĺ–Ķ –Ī—č–Ľ–ł –į–Ĺ–ĺ–ľ–į–Ľ—Ć–Ĺ—č–ľ–ł, —É 12 –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ĺ—Ā—Ć —É–Ľ—É—á—ą–Ķ–Ĺ–ł–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–ĺ–≤; –Ņ–ĺ –ł—ā–ĺ–≥–į–ľ –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–Ķ–≥–ĺ –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –ł—Ö —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā –Ĺ–į—Ö–ĺ–ī–ł–Ľ—Ā—Ź –≤ –Ņ—Ä–Ķ–ī–Ķ–Ľ–į—Ö –Ĺ–ĺ—Ä–ľ—č. –ü—Ä–ł —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł–ł –ľ–Ķ–∂–ī—É –≥—Ä—É–Ņ–Ņ–į–ľ–ł –Ĺ–Ķ –ĺ–Ī–Ĺ–į—Ä—É–∂–ł–Ľ–ł—Ā—Ć —Ā—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ł –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ķ —Ä–į–∑–Ľ–ł—á–ł—Ź –Ĺ–ł –Ņ–ĺ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ –≥–į—Ā—ā—Ä–ĺ–ī—É–ĺ–ī–Ķ–Ĺ–į–Ľ—Ć–Ĺ–ĺ–Ļ —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł–ł –Ĺ–į –ł—Ā—Ö–ĺ–ī–Ĺ–ĺ–ľ —É—Ä–ĺ–≤–Ĺ–Ķ, –Ĺ–ł –Ņ—Ä–ł –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–Ķ–ľ –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł, —ā–į–ļ –∂–Ķ –ļ–į–ļ –ł –Ņ—Ä–ł —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł–ł –≤–Ĺ—É—ā—Ä–ł –≥—Ä—É–Ņ–Ņ (—ā–Ķ—Ā—ā –ú–į–ļ-–Ě–Ķ–ľ–į—Ä, p=0,6698 –ī–Ľ—Ź —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į –ł p=1,0000 –ī–Ľ—Ź –ź–ú–ď). –ö–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ĺ–ĺ—Ä–ľ–į–Ľ—Ć–Ĺ—č–ľ–ł –ł –į–Ĺ–ĺ–ľ–į–Ľ—Ć–Ĺ—č–ľ–ł —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ–ł —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł–ł –Ņ–ĺ–ļ–į–∑–į–Ĺ–ĺ –≤ —ā–į–Ī–Ľ–ł—Ü–Ķ 3. –ü—Ä–ł –į–Ĺ–į–Ľ–ł–∑–Ķ –Ņ–ĺ–Ņ—É–Ľ—Ź—Ü–ł–Ļ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ PP –ł ITT –Ĺ–Ķ –Ī—č–Ľ–ł –ĺ–Ī–Ĺ–į—Ä—É–∂–Ķ–Ĺ—č –ļ–į–ļ–ł–Ķ-–Ľ–ł–Ī–ĺ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ķ –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –Ņ–ĺ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—é —Ā –ł—Ā—Ö–ĺ–ī–Ĺ—č–ľ —É—Ä–ĺ–≤–Ĺ–Ķ–ľ –Ņ–ĺ—Ā–Ľ–Ķ –Ņ—Ä–ł–Ķ–ľ–į –ź–ú–ď –ł–Ľ–ł —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į.
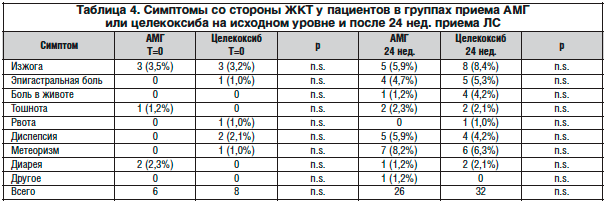
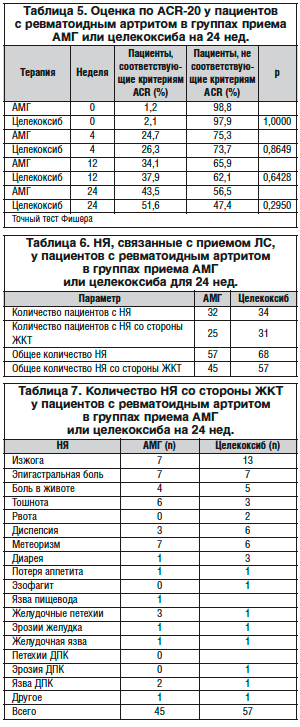
–°–ł–ľ–Ņ—ā–ĺ–ľ—č —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ė–ö–Ę. –í —ā–į–Ī–Ľ–ł—Ü–Ķ 4 –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ–Ķ–Ĺ—č —Ā–ł–ľ–Ņ—ā–ĺ–ľ—č —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ė–ö–Ę (–Ņ–ĺ —Ā–ĺ–ĺ–Ī—Č–Ķ–Ĺ–ł—Ź–ľ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤) –≤ –Ĺ–į—á–į–Ľ–Ķ –ł –≤ –ļ–ĺ–Ĺ—Ü–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź. –ü–ĺ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ —Ā—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –į–Ĺ–į–Ľ–ł–∑–į –Ĺ–Ķ –Ī—č–Ľ–ĺ –Ņ—Ä–ĺ–ī–Ķ–ľ–ĺ–Ĺ—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ–ĺ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö —Ä–į–∑–Ľ–ł—á–ł–Ļ –ľ–Ķ–∂–ī—É —ć—ā–ł–ľ–ł –ī–≤—É–ľ—Ź –≤–į—Ä–ł–į–Ĺ—ā–į–ľ–ł —ā–Ķ—Ä–į–Ņ–ł–ł. –ě–ī–Ĺ–į–ļ–ĺ –Ņ—Ä–ł –ĺ—Ü–Ķ–Ĺ–ļ–Ķ —Ā–ł–ľ–Ņ—ā–ĺ–ľ–ĺ–≤ –Ņ–ĺ—Ā–Ľ–Ķ 4 –Ĺ–Ķ–ī. —ā–Ķ—Ä–į–Ņ–ł–ł –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į –ź–ú–ď –Ī—č–Ľ–į –ĺ–Ī–Ĺ–į—Ä—É–∂–Ķ–Ĺ–į –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –ľ–Ķ–Ĺ—Ć—ą–į—Ź —á–į—Ā—ā–ĺ—ā–į –ī–ł—Ā–Ņ–Ķ–Ņ—Ā–ł–ł (—ā–ĺ—á–Ĺ—č–Ļ —ā–Ķ—Ā—ā –§–ł—ą–Ķ—Ä–į, p=0,0301).
–≠–Ľ–Ķ–ļ—ā—Ä–ĺ–ļ–į—Ä–ī–ł–ĺ–≥—Ä–į—Ą–ł—á–Ķ—Ā–ļ–į—Ź –ĺ—Ü–Ķ–Ĺ–ļ–į. –ü—Ä–ł —Ā–ļ—Ä–ł–Ĺ–ł–Ĺ–≥–Ķ –Ĺ–ĺ—Ä–ľ–į–Ľ—Ć–Ĺ—č–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –Ī—č–Ľ–ł –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į –ź–ú–ď —É 92,9% –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į – —É 90,5%; –Ĺ–į –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–Ķ–ľ –≤–ł–∑–ł—ā–Ķ –Ĺ–ĺ—Ä–ľ–į–Ľ—Ć–Ĺ—č–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į –ź–ú–ď –ł –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į –ĺ—ā–ľ–Ķ—á–į–Ľ–ł—Ā—Ć —É 94,1 –ł 93,6% –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ. –°—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ł –∑–Ĺ–į—á–ł–ľ—č–Ķ —Ä–į–∑–Ľ–ł—á–ł—Ź —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–ĺ–≤ –≠–ö–ď –Ĺ–Ķ –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ł—Ā—Ć –Ĺ–ł –Ņ—Ä–ł –ľ–Ķ–∂–≥—Ä—É–Ņ–Ņ–ĺ–≤–ĺ–ľ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł–ł (—ā–ĺ—á–Ĺ—č–Ļ —ā–Ķ—Ā—ā –§–ł—ą–Ķ—Ä–į –Ĺ–į –ł—Ā—Ö–ĺ–ī–Ĺ–ĺ–ľ —É—Ä–ĺ–≤–Ĺ–Ķ, p=0,6004 –ł –Ņ—Ä–ł –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–Ķ–ľ –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł, —ā–ĺ—á–Ĺ—č–Ļ —ā–Ķ—Ā—ā –§–ł—ą–Ķ—Ä–į, p=1,0000), –Ĺ–ł –Ņ—Ä–ł –≤–Ĺ—É—ā—Ä–ł–≥—Ä—É–Ņ–Ņ–ĺ–≤–ĺ–ľ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł–ł (—ā–Ķ—Ā—ā –ú–į–ļ-–Ě–Ķ–ľ–į—Ä: p=0,5637 –ź–ú–ď –ł p=0,797 –ī–Ľ—Ź –≥—Ä—É–Ņ–Ņ—č –Ņ—Ä–ł–Ķ–ľ–į —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į).
–õ–į–Ī–ĺ—Ä–į—ā–ĺ—Ä–Ĺ—č–Ķ –į–Ĺ–į–Ľ–ł–∑—č. –ü—Ä–ł –ĺ—Ü–Ķ–Ĺ–ļ–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–ĺ–≤ –Ľ–į–Ī–ĺ—Ä–į—ā–ĺ—Ä–Ĺ—č—Ö –į–Ĺ–į–Ľ–ł–∑–ĺ–≤ –ļ—Ä–ĺ–≤–ł –ł –ľ–ĺ—á–ł –Ĺ–Ķ –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ł—Ā—Ć –ļ–į–ļ–ł–Ķ-–Ľ–ł–Ī–ĺ —Ā—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ł –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ķ –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –ł—Ā—Ā–Ľ–Ķ–ī—É–Ķ–ľ—č—Ö –Ņ–į—Ä–į–ľ–Ķ—ā—Ä–ĺ–≤, –∑–į –ł—Ā–ļ–Ľ—é—á–Ķ–Ĺ–ł–Ķ–ľ –ľ–ĺ—á–Ķ–≤–ĺ–Ļ –ļ–ł—Ā–Ľ–ĺ—ā—č –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į –ź–ú–ď (–ĺ—ā–ľ–Ķ—á–į–Ľ–ĺ—Ā—Ć –Ľ–Ķ–≥–ļ–ĺ–Ķ –Ņ–ĺ–≤—č—ą–Ķ–Ĺ–ł–Ķ —É—Ä–ĺ–≤–Ĺ—Ź –ľ–ĺ—á–Ķ–≤–ĺ–Ļ –ļ–ł—Ā–Ľ–ĺ—ā—č) –Ī–Ķ–∑ –Ņ—Ä–Ķ–≤—č—ą–Ķ–Ĺ–ł—Ź –≤ –ļ–į–ļ–ĺ–ľ-–Ľ–ł–Ī–ĺ —Ā–Ľ—É—á–į–Ķ –≤–Ķ—Ä—Ö–Ĺ–Ķ–≥–ĺ –Ņ—Ä–Ķ–ī–Ķ–Ľ–į –Ĺ–ĺ—Ä–ľ—č –ł –≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ–Ļ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –∑–Ĺ–į—á–ł–ľ–ĺ—Ā—ā–ł.
–°—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ł–Ļ –į–Ĺ–į–Ľ–ł–∑: —ā–ĺ—á–Ĺ—č–Ļ —ā–Ķ—Ā—ā –§–ł—ą–Ķ—Ä–į. –Ě–Ķ –Ī—č–Ľ–ĺ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö —Ä–į–∑–Ľ–ł—á–ł–Ļ —É—Ä–ĺ–≤–Ĺ—Ź –≥–Ķ–ľ–ĺ–≥–Ľ–ĺ–Ī–ł–Ĺ–į –≤ –ļ—Ä–ĺ–≤–ł –ī–ĺ –ł –Ņ–ĺ—Ā–Ľ–Ķ —ā–Ķ—Ä–į–Ņ–ł–ł —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –ł–∑ –ĺ–Ī–Ķ–ł—Ö –≥—Ä—É–Ņ–Ņ; —Ā–Ľ–Ķ–ī–ĺ–≤–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ, –ľ–ĺ–∂–Ĺ–ĺ –Ņ—Ä–Ķ–ī–Ņ–ĺ–Ľ–ĺ–∂–ł—ā—Ć –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł–Ķ –ļ–į–ļ–ł—Ö-–Ľ–ł–Ī–ĺ –ļ—Ä–ĺ–≤–ĺ—ā–Ķ—á–Ķ–Ĺ–ł–Ļ –≤ –Ė–ö–Ę –≤ –Ņ–Ķ—Ä–ł–ĺ–ī –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź. –°—Ä–Ķ–ī–Ĺ–ł–Ķ –∑–Ĺ–į—á–Ķ–Ĺ–ł—Ź —Ā–ł—Ā—ā–ĺ–Ľ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –ł –ī–ł–į—Ā—ā–ĺ–Ľ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –ī–į–≤–Ľ–Ķ–Ĺ–ł—Ź, —ā–į–ļ –∂–Ķ –ļ–į–ļ –ł —á–į—Ā—ā–ĺ—ā–į —Ā–Ķ—Ä–ī–Ķ—á–Ĺ—č—Ö —Ā–ĺ–ļ—Ä–į—Č–Ķ–Ĺ–ł–Ļ, –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –Ĺ–Ķ –ł–∑–ľ–Ķ–Ĺ–ł–Ľ–ł—Ā—Ć –≤ –Ņ–Ķ—Ä–ł–ĺ–ī —ā–Ķ—Ä–į–Ņ–ł–ł –ł—Ā—Ā–Ľ–Ķ–ī—É–Ķ–ľ—č–ľ–ł –õ–°.
–≠—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć
–ö–į–ļ–ł—Ö-–Ľ–ł–Ī–ĺ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö —Ä–į–∑–Ľ–ł—á–ł–Ļ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —É–Ľ—É—á—ą–Ķ–Ĺ–ł—Ź, –ĺ—Ü–Ķ–Ĺ–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –Ņ–ĺ –ł–Ĺ–ī–Ķ–ļ—Ā—É ACR-20 (—ā–į–Ī–Ľ. 5), –ľ–Ķ–∂–ī—É –ī–≤—É–ľ—Ź –≥—Ä—É–Ņ–Ņ–į–ľ–ł –≤ —Ä–į–∑–Ľ–ł—á–Ĺ—č—Ö –≤—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ—č—Ö –ł–Ĺ—ā–Ķ—Ä–≤–į–Ľ–į—Ö –Ĺ–Ķ –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ĺ—Ā—Ć. –í —á–į—Ā—ā–Ĺ–ĺ—Ā—ā–ł, –ī–Ľ—Ź –ĺ–Ī–ĺ–ł—Ö –õ–° –Ī—č–Ľ–į –Ņ—Ä–ĺ–ī–Ķ–ľ–ĺ–Ĺ—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ–į —Ā—Ö–ĺ–∂–į—Ź —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –Ĺ–į 4, 12 –ł 24 –Ĺ–Ķ–ī. –Ņ—Ä–ł–Ķ–ľ–į. –ü–ĺ–Ľ—É—á–Ķ–Ĺ–Ĺ—č–Ķ –∑–Ĺ–į—á–Ķ–Ĺ–ł—Ź –Ī—č–Ľ–ł —Ā—Ä–į–≤–Ĺ–ł–ľ—č —Ā –Ņ—Ä–ł–≤–Ķ–ī–Ķ–Ĺ–Ĺ—č–ľ–ł –≤ –Ľ–ł—ā–Ķ—Ä–į—ā—É—Ä–Ķ –ī–Ľ—Ź —Ä–į—Ā–Ņ—Ä–ĺ—Ā—ā—Ä–į–Ĺ–Ķ–Ĺ–Ĺ—č—Ö –Ě–ü–í–ü –Ņ—Ä–ł —ā–Ķ—Ä–į–Ņ–ł–ł —Ä–Ķ–≤–ľ–į—ā–ĺ–ł–ī–Ĺ–ĺ–≥–ĺ –į—Ä—ā—Ä–ł—ā–į [37].
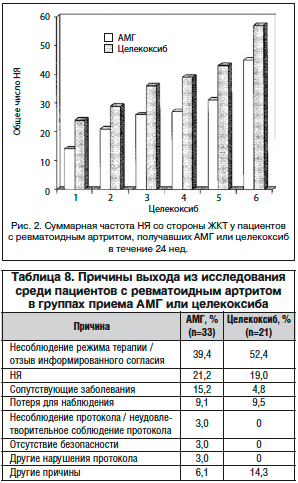
–Ě–Į. –ß–į—Ā—ā–ĺ—ā–į –≤–ĺ–∑–Ĺ–ł–ļ–Ĺ–ĺ–≤–Ķ–Ĺ–ł—Ź –Ě–Į, —Ä–į—Ā—Ā—á–ł—ā–į–Ĺ–Ĺ–į—Ź –ī–Ľ—Ź –≤—Ā–Ķ—Ö —Ä–į–Ĺ–ī–ĺ–ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –Ī—č–Ľ–į —Ā—Ö–ĺ–∂–Ķ–Ļ –ī–Ľ—Ź –ĺ–Ī–ĺ–ł—Ö –õ–° –≤ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ –≤—Ā–Ķ–≥–ĺ –Ņ–Ķ—Ä–ł–ĺ–ī–į –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź (—ā–į–Ī–Ľ. 6). –ü—Ä–ĺ—Ü–Ķ–Ĺ—ā –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ě–Į —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ė–ö–Ę, —Ā–≤—Ź–∑–į–Ĺ–Ĺ—č–ľ–ł —Ā —ā–Ķ—Ä–į–Ņ–ł–Ķ–Ļ (–ļ–į–ļ –Ņ–ĺ–ļ–į–∑–į–Ĺ–ĺ –≤ —ā–į–Ī–Ľ–ł—Ü–Ķ 7), —Ā–ĺ—Ā—ā–į–≤–Ľ—Ź–Ľ 21,2% –ī–Ľ—Ź –≥—Ä—É–Ņ–Ņ—č –Ņ—Ä–ł–Ķ–ľ–į –ź–ú–ď –ł 26,5% – –ī–Ľ—Ź –≥—Ä—É–Ņ–Ņ—č –Ņ—Ä–ł–Ķ–ľ–į —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į. –Ě–į —Ä–ł—Ā—É–Ĺ–ļ–Ķ 2 –Ņ–ĺ–ļ–į–∑–į–Ĺ–į –ļ—É–ľ—É–Ľ—Ź—ā–ł–≤–Ĺ–į—Ź —á–į—Ā—ā–ĺ—ā–į –Ě–Į —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ė–ö–Ę –≤ –Ņ–Ķ—Ä–ł–ĺ–ī –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź.
–Ě–Ķ —Ā–≤—Ź–∑–į–Ĺ–Ĺ—č–Ķ —Ā –Ė–ö–Ę –Ě–Į –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ł—Ā—Ć —É 12 –ł 11 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≤ –≥—Ä—É–Ņ–Ņ–į—Ö –Ņ—Ä–ł–Ķ–ľ–į –ź–ú–ď –ł —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ. –£ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –Ņ–ĺ–Ľ—É—á–į–≤—ą–ł—Ö –ź–ú–ď, –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ł—Ā—Ć –≥–ĺ–Ľ–ĺ–≤–Ĺ–į—Ź –Ī–ĺ–Ľ—Ć (n=3), –į–Ľ–Ľ–Ķ—Ä–≥–ł—á–Ķ—Ā–ļ–ł–Ķ —Ä–Ķ–į–ļ—Ü–ł–ł –ļ–ĺ–∂–ł (n=3), —É—Ö—É–ī—ą–Ķ–Ĺ–ł–Ķ —Ā–į–ľ–ĺ—á—É–≤—Ā—ā–≤–ł—Ź (n=3), –≥–ł–Ņ–ĺ—ā–Ķ–Ĺ–∑–ł—Ź (n=1) –ł –į–Ĺ–ĺ–ľ–į–Ľ—Ć–Ĺ—č–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –Ľ–į–Ī–ĺ—Ä–į—ā–ĺ—Ä–Ĺ—č—Ö –į–Ĺ–į–Ľ–ł–∑–ĺ–≤ (n=2). –£ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –Ņ–ĺ–Ľ—É—á–į–≤—ą–ł—Ö —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī, –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ł—Ā—Ć —ā–ł–Ĺ–Ĺ–ł—ā—É—Ā (n=1), –ĺ—ā–ļ–Ľ–ĺ–Ĺ–Ķ–Ĺ–ł—Ź –ĺ—ā –Ĺ–ĺ—Ä–ľ—č –Ņ–ĺ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ –≠–ö–ď (n=1), –į–Ľ–Ľ–Ķ—Ä–≥–ł—á–Ķ—Ā–ļ–ł–Ķ —Ä–Ķ–į–ļ—Ü–ł–ł –ļ–ĺ–∂–ł (n=3), –į–Ĺ–ĺ–ľ–į–Ľ—Ć–Ĺ—č–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –Ľ–į–Ī–ĺ—Ä–į—ā–ĺ—Ä–Ĺ—č—Ö –į–Ĺ–į–Ľ–ł–∑–ĺ–≤ (n= 4), –≥–ł–Ņ–Ķ—Ä—ā–Ķ–Ĺ–∑–ł—Ź (n=1), –ļ—Ä–ĺ–≤–ĺ—ā–Ķ—á–Ķ–Ĺ–ł–Ķ (n=1).
–°–Ķ—Ä—Ć–Ķ–∑–Ĺ—č–Ķ –Ě–Į. –í –Ņ–Ķ—Ä–ł–ĺ–ī –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź —É 7 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ł—Ā—Ć 11 –Ě–Į (4 – –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į –ź–ú–ď –ł 3 – –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ—Ä–ł–Ķ–ľ–į —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į). –≠—ā–ł —Ź–≤–Ľ–Ķ–Ĺ–ł—Ź –Ĺ–Ķ –Ī—č–Ľ–ł —Ä–į—Ā—Ü–Ķ–Ĺ–Ķ–Ĺ—č –ļ–į–ļ —Ā–≤—Ź–∑–į–Ĺ–Ĺ—č–Ķ —Ā –Ņ—Ä–ł–Ķ–ľ–ĺ–ľ –ź–ú–ď, –ł —ā–ĺ–Ľ—Ć–ļ–ĺ 1 –Ě–Į (–į–Ĺ–≥–ł–ĺ–Ĺ–Ķ–≤—Ä–ĺ—ā–ł—á–Ķ—Ā–ļ–ł–Ļ –ĺ—ā–Ķ–ļ) –Ī—č–Ľ–ĺ —Ā–≤—Ź–∑–į–Ĺ–ĺ —Ā –Ņ—Ä–ł–Ķ–ľ–ĺ–ľ —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į.
–í—č—Ö–ĺ–ī –ł–∑ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź. 54 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į –ł–∑ 235 –ī–ĺ—Ā—Ä–ĺ—á–Ĺ–ĺ –≤—č—ą–Ľ–ł –ł–∑ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź, –Ĺ–į–ł–Ī–ĺ–Ľ–Ķ–Ķ —á–į—Ā—ā–ĺ–Ļ –Ņ—Ä–ł—á–ł–Ĺ–ĺ–Ļ –≤—č—Ö–ĺ–ī–į –Ī—č–Ľ–ĺ –Ĺ–Ķ—Ā–ĺ–Ī–Ľ—é–ī–Ķ–Ĺ–ł–Ķ —Ä–Ķ–∂–ł–ľ–į —ā–Ķ—Ä–į–Ņ–ł–ł –ł–Ľ–ł –ĺ—ā–∑—č–≤ –ł–Ĺ—Ą–ĺ—Ä–ľ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–≥–ĺ —Ā–ĺ–≥–Ľ–į—Ā–ł—Ź (—ā–į–Ī–Ľ. 8). –Ę–ĺ–Ľ—Ć–ļ–ĺ 11 —Ā–Ľ—É—á–į–Ķ–≤ –≤—č—Ö–ĺ–ī–į –ł–∑ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –Ī—č–Ľ–ł –ĺ–Ī—É—Ā–Ľ–ĺ–≤–Ľ–Ķ–Ĺ—č –Ě–Į, —Ā–≤—Ź–∑–į–Ĺ–Ĺ—č–ľ–ł —Ā –Ņ—Ä–ł–Ķ–ľ–ĺ–ľ –õ–°: 7 – –Ņ—Ä–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–ł –ź–ú–ď –ł 4 – —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į. –ö –Ě–Į –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –ź–ú–ď –ĺ—ā–Ĺ–ĺ—Ā–ł–Ľ–ł—Ā—Ć –Ě–Į —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ė–ö–Ę (n=4), –į–Ľ–Ľ–Ķ—Ä–≥–ł—á–Ķ—Ā–ļ–ł–Ķ —Ä–Ķ–į–ļ—Ü–ł–ł (n=1), –≥–ł–Ņ–ĺ—ā–Ķ–Ĺ–∑–ł—Ź (n=1) –ł –≥–ĺ–Ľ–ĺ–≤–Ĺ–į—Ź –Ī–ĺ–Ľ—Ć (n=1). –ö –Ě–Į –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į –ĺ—ā–Ĺ–ĺ—Ā–ł–Ľ–ł—Ā—Ć –Ě–Į —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ė–ö–Ę (n=2) –ł –į–Ľ–Ľ–Ķ—Ä–≥–ł—á–Ķ—Ā–ļ–ł–Ķ —Ä–Ķ–į–ļ—Ü–ł–ł (n=2).
–ě–Ī—Ā—É–∂–ī–Ķ–Ĺ–ł–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–ĺ–≤
–Ę–ĺ–ļ—Ā–ł—á–Ĺ–ĺ—Ā—ā—Ć –ī–Ľ—Ź –Ė–ö–Ę –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –Ě–ü–í–ü —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –ĺ–ī–Ĺ–ł–ľ –ł–∑ –Ĺ–į–ł–Ī–ĺ–Ľ–Ķ–Ķ —Ä–į—Ā–Ņ—Ä–ĺ—Ā—ā—Ä–į–Ĺ–Ķ–Ĺ–Ĺ—č—Ö —Ā–Ķ—Ä—Ć–Ķ–∑–Ĺ—č—Ö –Ě–Į, —Ā–≤—Ź–∑–į–Ĺ–Ĺ—č—Ö —Ā –Ņ—Ä–ł–Ķ–ľ–ĺ–ľ –õ–° –≤ —Ä–į–∑–≤–ł—ā—č—Ö —Ā—ā—Ä–į–Ĺ–į—Ö. –Ē–į–Ĺ–Ĺ–ĺ–Ķ —Ź–≤–Ľ–Ķ–Ĺ–ł–Ķ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –≤–Ľ–ł—Ź–Ķ—ā –Ĺ–į –∑–ī–ĺ—Ä–ĺ–≤—Ć–Ķ –Ĺ–į—Ā–Ķ–Ľ–Ķ–Ĺ–ł—Ź –ł —Ā–ĺ–Ņ—Ä—Ź–∂–Ķ–Ĺ–ĺ —Ā –ī–ĺ–Ņ–ĺ–Ľ–Ĺ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–ľ–ł –∑–į—ā—Ä–į—ā–į–ľ–ł –Ĺ–į –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ –Ě–Į. –Ē–Ľ—Ź –Ņ—Ä–ĺ—Ą–ł–Ľ–į–ļ—ā–ł–ļ–ł –Ņ–ĺ–≤—Ä–Ķ–∂–ī–Ķ–Ĺ–ł–Ļ –∂–Ķ–Ľ—É–ī–ļ–į –ł –Ē–ü–ö, —Ā–≤—Ź–∑–į–Ĺ–Ĺ—č—Ö —Ā –Ņ—Ä–ł–Ķ–ľ–ĺ–ľ –Ě–ü–í–ü, –Ņ—Ä–ł–ľ–Ķ–Ĺ—Ź–Ľ–ł—Ā—Ć —Ä–į–∑–Ľ–ł—á–Ĺ—č–Ķ —Ā—ā—Ä–į—ā–Ķ–≥–ł–ł: –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ –≥–į—Ā—ā—Ä–ĺ–Ņ—Ä–ĺ—ā–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č—Ö –≤–Ķ—Č–Ķ—Ā—ā–≤, —ā–į–ļ–ł—Ö –ļ–į–ļ –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä—č –Ņ—Ä–ĺ—ā–ĺ–Ĺ–Ĺ–ĺ–≥–ĺ –Ĺ–į—Ā–ĺ—Ā–į –ł–Ľ–ł –ľ–ł–∑–ĺ–Ņ—Ä–ĺ—Ā—ā–ĺ–Ľ, —Ā–ł–Ĺ—ā–Ķ—ā–ł—á–Ķ—Ā–ļ–ł–Ķ –Ņ—Ä–ĺ–ł–∑–≤–ĺ–ī–Ĺ—č–Ķ PG–ē1, –ł–Ľ–ł —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–ĺ–≤ –¶–ě–ď-2. –°–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č–Ķ –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä—č –¶–ě–ď-2 –ĺ–Ī–Ľ–į–ī–į—é—ā —Ā—Ö–ĺ–∂–ł–ľ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ–ľ —Ā —Ä–į—Ā–Ņ—Ä–ĺ—Ā—ā—Ä–į–Ĺ–Ķ–Ĺ–Ĺ—č–ľ–ł –Ě–ü–í–ü – —Ā–Ĺ–ł–∂–į—é—ā —É—Ä–ĺ–≤–Ķ–Ĺ—Ć –Ī–ĺ–Ľ–ł –ł –≤–ĺ—Ā–Ņ–į–Ľ–Ķ–Ĺ–ł—Ź –Ņ—Ä–ł –į—Ä—ā—Ä–ł—ā–Ķ, –į —ā–į–ļ–∂–Ķ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ —É–Ľ—É—á—ą–į—é—ā –ļ–į—á–Ķ—Ā—ā–≤–ĺ –∂–ł–∑–Ĺ–ł, —Ā–≤—Ź–∑–į–Ĺ–Ĺ–ĺ–Ķ —Ā —Ā–ĺ—Ā—ā–ĺ—Ź–Ĺ–ł–Ķ–ľ –∑–ī–ĺ—Ä–ĺ–≤—Ć—Ź [38, 39], –Ī–Ľ–į–≥–ĺ–ī–į—Ä—Ź –Ľ—É—á—ą–Ķ–Ļ –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā–ł —ć—ā–ł—Ö –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –ī–Ľ—Ź –Ė–ö–Ę. –í –Ņ—Ä–ĺ—Ā–Ņ–Ķ–ļ—ā–ł–≤–Ĺ–ĺ–ľ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł [40] –Ņ–ĺ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—é —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ņ—Ä–ł–Ķ–ľ–į –Ě–ü–í–ü –≤ —Ä–Ķ–∂–ł–ľ–Ķ –ľ–ĺ–Ĺ–ĺ—ā–Ķ—Ä–į–Ņ–ł–ł —Ā —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć—é –Ņ—Ä–ł–Ķ–ľ–į –Ě–ü–í–ü –ł –ľ–ł–∑–ĺ–Ņ—Ä–ĺ—Ā—ā–ĺ–Ľ–į –Ī—č–Ľ–ĺ —É—Ā—ā–į–Ĺ–ĺ–≤–Ľ–Ķ–Ĺ–ĺ, —á—ā–ĺ —É 0,95% –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā —Ä–Ķ–≤–ľ–į—ā–ĺ–ł–ī–Ĺ—č–ľ –į—Ä—ā—Ä–ł—ā–ĺ–ľ, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –Ņ–ĺ–Ľ—É—á–į–Ľ–ł —ā–ĺ–Ľ—Ć–ļ–ĺ –Ě–ü–í–ü, –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ł—Ā—Ć –ĺ—Ā–Ľ–ĺ–∂–Ĺ–Ķ–Ĺ–ł—Ź —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –≤–Ķ—Ä—Ö–Ĺ–ł—Ö –ĺ—ā–ī–Ķ–Ľ–ĺ–≤ –Ė–ö–Ę —á–Ķ—Ä–Ķ–∑ 6 –ľ–Ķ—Ā. –Ņ–ĺ—Ā–Ľ–Ķ –Ĺ–į—á–į–Ľ–į —ā–Ķ—Ä–į–Ņ–ł–ł. –ü—Ä–ł –ļ–ĺ–ľ–Ī–ł–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł –Ī—č–Ľ–ĺ –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ–ĺ —É–ľ–Ķ–Ĺ—Ć—ą–Ķ–Ĺ–ł–Ķ —Ä–ł—Ā–ļ–į –Ĺ–į 40%. –í –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź—Ö –ī–Ķ–Ļ—Ā—ā–≤–ł—Ź —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–ĺ–≤ –¶–ě–ď-2, —ā–į–ļ–ł—Ö –ļ–į–ļ —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī [22] –ł —Ä–ĺ—Ą–Ķ–ļ–ĺ–ļ—Ā–ł–Ī [23], –Ī—č–Ľ–ĺ –Ņ—Ä–ĺ–ī–Ķ–ľ–ĺ–Ĺ—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ–ĺ –≤ —Ā—Ä–Ķ–ī–Ĺ–Ķ–ľ 50% —É–ľ–Ķ–Ĺ—Ć—ą–Ķ–Ĺ–ł–Ķ —á–į—Ā—ā–ĺ—ā—č –≤–ĺ–∑–Ĺ–ł–ļ–Ĺ–ĺ–≤–Ķ–Ĺ–ł—Ź —Ź–∑–≤ –ł –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö –Ě–Į —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –≤–Ķ—Ä—Ö–Ĺ–ł—Ö –ĺ—ā–ī–Ķ–Ľ–ĺ–≤ –Ė–ö–Ę –Ņ–ĺ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—é —Ā —ā–į–ļ–ĺ–≤—č–ľ–ł –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –Ĺ–Ķ—Ā–Ņ–Ķ—Ü–ł—Ą–ł—á–Ķ—Ā–ļ–ł—Ö –Ě–ü–í–ü. –°—Ä–Ķ–ī–ł —Ä–į–∑–Ľ–ł—á–Ĺ—č—Ö —Ā–ĺ–≤—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ—č—Ö –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–ĺ–≤ –¶–ě–ď-2 —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –Ņ—Ä–ł —Ā–≤—Ź–∑—č–≤–į–Ĺ–ł–ł —Ā –ł–∑–ĺ—Ą–ĺ—Ä–ľ–į–ľ–ł –¶–ě–ď —Ā—É—Č–Ķ—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ –≤–į—Ä—Ć–ł—Ä—É–Ķ—ā –≤ –∑–į–≤–ł—Ā–ł–ľ–ĺ—Ā—ā–ł –ĺ—ā –ľ–Ķ—ā–ĺ–ī–į (in vivo, ex vivo –ł–Ľ–ł in vitro, —Ü–Ķ–Ľ—č–Ķ –ļ–Ľ–Ķ—ā–ļ–ł –ł–Ľ–ł –ĺ—á–ł—Č–Ķ–Ĺ–Ĺ—č–Ķ —Ą–Ķ—Ä–ľ–Ķ–Ĺ—ā—č –≤ –ļ–į—á–Ķ—Ā—ā–≤–Ķ —ć–ļ—Ā–Ņ–Ķ—Ä–ł–ľ–Ķ–Ĺ—ā–į–Ľ—Ć–Ĺ–ĺ–Ļ —Ā–ł—Ā—ā–Ķ–ľ—č, –≤–į—Ä–ł–į—Ü–ł–ł –ļ–ĺ–Ĺ—Ü–Ķ–Ĺ—ā—Ä–į—Ü–ł–ł —Ā—É–Ī—Ā—ā—Ä–į—ā–į –ł –≤—Ä–Ķ–ľ–Ķ–Ĺ–ł –ł–Ĺ–ļ—É–Ī–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź) [41, 42]. –°–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ, –ļ–Ľ–į—Ā—Ā–ł—Ą–ł–ļ–į—Ü–ł—Ź —ć—ā–ł—Ö —Ā—Ä–Ķ–ī—Ā—ā–≤ –∑–į—ā—Ä—É–ī–Ĺ–Ķ–Ĺ–į –ł–∑-–∑–į –Ĺ–Ķ–ī–ĺ—Ā—ā–į—ā–ĺ—á–Ĺ–ĺ—Ā—ā–ł –ī–į–Ĺ–Ĺ—č—Ö –ī–Ľ—Ź –Ņ—Ä–Ķ–ī—Ā–ļ–į–∑–į–Ĺ–ł—Ź —Ā–≤—Ź–∑–ł –ľ–Ķ–∂–ī—É –Ī–ł–ĺ—Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ł–ľ–ł/—Ą–į—Ä–ľ–į–ļ–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł–ľ–ł —Ā–≤–ĺ–Ļ—Ā—ā–≤–į–ľ–ł –ł –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł–ľ —ć—Ą—Ą–Ķ–ļ—ā–ĺ–ľ –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –≤–Ķ—Č–Ķ—Ā—ā–≤–į. –í –Ľ—é–Ī–ĺ–ľ —Ā–Ľ—É—á–į–Ķ –ī–Ľ—Ź –ī–ĺ—Ā—ā–ł–∂–Ķ–Ĺ–ł—Ź –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –Ņ—Ä–Ķ–ł–ľ—É—Č–Ķ—Ā—ā–≤–į —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č–Ļ –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä –¶–ě–ď-2 –ī–ĺ–Ľ–∂–Ķ–Ĺ –ĺ–Ī–Ľ–į–ī–į—ā—Ć –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ—č–ľ –Ņ—Ä–ĺ—ā–ł–≤–ĺ–≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–ľ –ł –ĺ–Ī–Ķ–∑–Ī–ĺ–Ľ–ł–≤–į—é—Č–ł–ľ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ–ľ –Ņ—Ä–ł –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł–ł –Ĺ–Ķ–≥–į—ā–ł–≤–Ĺ—č—Ö –Ņ—Ä–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł–Ļ –ł–Ĺ–≥–ł–Ī–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –¶–ě–ď-1 – –Ņ–ĺ–ī–į–≤–Ľ–Ķ–Ĺ–ł—Ź –Ī–ł–ĺ—Ā–ł–Ĺ—ā–Ķ–∑–į –ü–ď –≤ –°–ě –ł –į–≥—Ä–Ķ–≥–į—Ü–ł–ł —ā—Ä–ĺ–ľ–Ī–ĺ—Ü–ł—ā–ĺ–≤ [42, 43].
–í –Ĺ–Ķ–ļ–ĺ—ā–ĺ—Ä—č—Ö —ć–ļ—Ā–Ņ–Ķ—Ä–ł–ľ–Ķ–Ĺ—ā–į—Ö –Ī—č–Ľ–į –Ņ—Ä–ĺ–ī–Ķ–ľ–ĺ–Ĺ—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ–į –Ĺ–ł–∑–ļ–į—Ź —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į [44, 45], –ĺ–ī–Ĺ–į–ļ–ĺ —ć—ā–ĺ—ā —Ą–į–ļ—ā –Ĺ–Ķ –Ņ—Ä–ĺ—ā–ł–≤–ĺ—Ä–Ķ—á–ł—ā –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–ľ—É –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł—é —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–ĺ–≤ –¶–ě–ď-2. –ü—Ä–ł —ć—ā–ĺ–ľ –≤ –ľ–į—Ā—ą—ā–į–Ī–Ĺ—č—Ö –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł—Ö –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź—Ö [19, 20] –ł –Ņ–ĺ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ –ľ–Ķ—ā–į–į–Ĺ–į–Ľ–ł–∑–į [22] –Ī—č–Ľ–į —É–Ī–Ķ–ī–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –Ņ–ĺ–ī—ā–≤–Ķ—Ä–∂–ī–Ķ–Ĺ–į –≥–į—Ā—ā—Ä–ĺ–Ņ—Ä–ĺ—ā–Ķ–ļ—ā–ł–≤–Ĺ–į—Ź –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć. –í –Ĺ–į—Ā—ā–ĺ—Ź—Č–Ķ–ľ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł –ĺ—ā–ľ–Ķ—á–į–Ķ—ā—Ā—Ź, —á—ā–ĺ –ź–ú–ď –ł —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī —Ź–≤–Ľ—Ź—é—ā—Ā—Ź —Ā—Ö–ĺ–∂–ł–ľ–ł –Ņ–ĺ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –õ–° –ī–Ľ—Ź –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ź —Ā–ł–ľ–Ņ—ā–ĺ–ľ–ĺ–≤ —Ä–Ķ–≤–ľ–į—ā–ĺ–ł–ī–Ĺ–ĺ–≥–ĺ –į—Ä—ā—Ä–ł—ā–į. –ź–ú–ď –ł —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī –ĺ–Ī–Ľ–į–ī–į—é—ā —Ā—Ö–ĺ–∂–Ķ–Ļ —ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć—é, –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā—Ć—é –ī–Ľ—Ź –Ė–ö–Ę –ł –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā—Ć—é, —á—ā–ĺ –Ņ–ĺ–ī—ā–≤–Ķ—Ä–∂–ī–į–Ķ—ā —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –Ņ—Ä–Ķ–ī—ą–Ķ—Ā—ā–≤—É—é—Č–ł—Ö —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł—á–Ķ—Ā–ļ–ł—Ö –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ļ –Ņ–ĺ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—é –ź–ú–ď —Ā —Ä–į—Ā–Ņ—Ä–ĺ—Ā—ā—Ä–į–Ĺ–Ķ–Ĺ–Ĺ—č–ľ–ł –Ě–ü–í–ü [27, 28, 46].
–ě—ā—Ā—É—ā—Ā—ā–≤–ł–Ķ –ļ–ĺ—Ä—Ä–Ķ–Ľ—Ź—Ü–ł–ł –ľ–Ķ–∂–ī—É —Ā–ł–ľ–Ņ—ā–ĺ–ľ–į–ľ–ł –ł –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–Ķ–ľ –°–ě –Ņ–ĺ—Ā–Ľ–Ķ –Ņ—Ä–ł–Ķ–ľ–į –Ě–ü–í–ü –Ī—č–Ľ–ĺ –Ĺ–Ķ–ĺ–ī–Ĺ–ĺ–ļ—Ä–į—ā–Ĺ–ĺ –Ņ—Ä–ĺ–ī–Ķ–ľ–ĺ–Ĺ—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ–ĺ –≤ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł—Ö –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź—Ö. –°–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ, –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł–Ķ —Ā–ł–ľ–Ņ—ā–ĺ–ľ–ĺ–≤ –Ĺ–Ķ –ľ–ĺ–∂–Ķ—ā –Ī—č—ā—Ć —Ä–į—Ā—Ü–Ķ–Ĺ–Ķ–Ĺ–ĺ –ļ–į–ļ –ĺ–ī–Ĺ–ĺ–∑–Ĺ–į—á–Ĺ—č–Ļ –Ņ—Ä–ł–∑–Ĺ–į–ļ –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł—Ź –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–Ļ –°–ě. –§–į–ļ—ā–ł—á–Ķ—Ā–ļ–ł –ľ–Ĺ–ĺ–≥–ł–Ķ —Ā–Ķ—Ä—Ć–Ķ–∑–Ĺ—č–Ķ –ĺ—Ā–Ľ–ĺ–∂–Ĺ–Ķ–Ĺ–ł—Ź —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ė–ö–Ę, —Ā–≤—Ź–∑–į–Ĺ–Ĺ—č–Ķ —Ā –Ņ—Ä–ł–Ķ–ľ–ĺ–ľ –Ě–ü–í–ü, –ľ–ĺ–≥—É—ā –Ņ—Ä–ĺ—ā–Ķ–ļ–į—ā—Ć –Ī–Ķ–∑ —Ā–ł–ľ–Ņ—ā–ĺ–ľ–ĺ–≤ [47, 48]. –í —ć—ā–ĺ–ľ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł —Ā–ł–ľ–Ņ—ā–ĺ–ľ—č –ł –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–Ķ –°–ě –ł–∑—É—á–į–Ľ–ł—Ā—Ć —Ā –Ņ–ĺ–ľ–ĺ—Č—Ć—é —Ā–Ņ–Ķ—Ü–ł–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ĺ–Ņ—Ä–ĺ—Ā–Ĺ–ł–ļ–į –ł —ć–Ĺ–ī–ĺ—Ā–ļ–ĺ–Ņ–ł–ł –Ė–ö–Ę. –ü–ĺ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ —Ā—É–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ł –ĺ–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ĺ—Ü–Ķ–Ĺ–ĺ–ļ –ĺ—ā–ľ–Ķ—á–į–Ķ—ā—Ā—Ź —Ö–ĺ—Ä–ĺ—ą–į—Ź –≥–į—Ā—ā—Ä–ĺ–ī—É–ĺ–ī–Ķ–Ĺ–į–Ľ—Ć–Ĺ–į—Ź –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā—Ć –ź–ú–ď –ł —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į —Ā–ĺ —Ā—Ö–ĺ–∂–Ķ–Ļ —á–į—Ā—ā–ĺ—ā–ĺ–Ļ –Ě–Į, –≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ –ł–Ľ–ł –≤–Ķ—Ä–ĺ—Ź—ā–Ĺ–ĺ —Ā–≤—Ź–∑–į–Ĺ–Ĺ—č—Ö —Ā —ā–Ķ—Ä–į–Ņ–ł–Ķ–Ļ. –í —á–į—Ā—ā–Ĺ–ĺ—Ā—ā–ł, –ī–Ľ—Ź —ć—ā–ł—Ö –õ–° —á–į—Ā—ā–ĺ—ā–į, –ł–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –ł —ā–ł–Ņ –Ě–Į —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ė–ö–Ę –Ī—č–Ľ–ł —Ā—Ö–ĺ–∂–ł–ľ–ł.
–Ě–Ķ—Ā–ľ–ĺ—ā—Ä—Ź –Ĺ–į –ł–Ĺ–≥–ł–Ī–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ –¶–ě–ď –ł –ī–Ķ—Ą–ł—Ü–ł—ā –ü–ď, –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –ź–ú–ď –Ĺ–Ķ –Ņ—Ä–ĺ–ł—Ā—Ö–ĺ–ī–ł—ā –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–Ķ –°–ě –Ė–ö–Ę –ł –Ĺ–į–Ī–Ľ—é–ī–į–Ķ—ā—Ā—Ź –∑–į—Č–ł—ā–į –ĺ—ā –≤–ĺ–∑–ī–Ķ–Ļ—Ā—ā–≤–ł—Ź —Ä–į–∑–ī—Ä–į–∂–į—é—Č–ł—Ö —Ą–į–ļ—ā–ĺ—Ä–ĺ–≤.
–ó–į—Č–ł—ā–į –°–ě –ī–ĺ—Ā—ā–ł–≥–į–Ľ–į—Ā—Ć –Ņ—É—ā–Ķ–ľ –ł–Ĺ–≥–ł–Ī–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –≤—č—Ä–į–Ī–ĺ—ā–ļ–ł –ļ–ł—Ā–Ľ–ĺ—ā—č, —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł—Ź –≤—č—Ä–į–Ī–ĺ—ā–ļ–ł –Ī–ł–ļ–į—Ä–Ī–ĺ–Ĺ–į—ā–į –ł —Ā—ā–ł–ľ—É–Ľ—Ź—Ü–ł–ł –ļ—Ä–ĺ–≤–ĺ—ā–ĺ–ļ–į –≤ –°–ě. –≠—ā–ł —ć—Ą—Ą–Ķ–ļ—ā—č –ĺ–Ņ–ĺ—Ā—Ä–Ķ–ī–ĺ–≤–į–Ĺ—č —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł–Ķ–ľ –≤—č—Ä–į–Ī–ĺ—ā–ļ–ł CGRP –ł NO [26, 49–51]. –í –Ĺ–į—Ā—ā–ĺ—Ź—Č–Ķ–Ķ –≤—Ä–Ķ–ľ—Ź –ĺ—á–Ķ–≤–ł–ī–Ĺ–ĺ, —á—ā–ĺ –ľ–ł–ļ—Ä–ĺ–≤–į—Ā–ļ—É–Ľ—Ź—Ä–Ĺ—č–Ķ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź —Ź–≤–Ľ—Ź—é—ā—Ā—Ź –Ĺ–į–ł–Ī–ĺ–Ľ–Ķ–Ķ —Ä–į–Ĺ–Ĺ–ł–ľ –Ņ—Ä–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł–Ķ–ľ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź –Ė–ö–Ę –Ņ–ĺ—Ā–Ľ–Ķ –Ņ—Ä–ł–Ķ–ľ–į –Ě–ü–í–ü [52]. –≠—ā–ł –Ņ—Ä–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł—Ź –Ņ—Ä–Ķ–ī—ą–Ķ—Ā—ā–≤—É—é—ā –Ņ–ĺ–≤—Ä–Ķ–∂–ī–Ķ–Ĺ–ł—Ź–ľ —ć–Ņ–ł—ā–Ķ–Ľ–ł—Ź –ł —Ā–Ņ–ĺ—Ā–ĺ–Ī—Ā—ā–≤—É—é—ā –ł—Ö —Ä–į–∑–≤–ł—ā–ł—é. –í –Ĺ–Ķ–ī–į–≤–Ĺ–Ķ–ľ —ć–ļ—Ā–Ņ–Ķ—Ä–ł–ľ–Ķ–Ĺ—ā–į–Ľ—Ć–Ĺ–ĺ–ľ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł [53] –Ņ—É—ā–Ķ–ľ –ľ–ł–ļ—Ä–ĺ—Ā–ļ–ĺ–Ņ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –°–ě –∂–Ķ–Ľ—É–ī–ļ–į –Ī—č–Ľ–ĺ —É—Ā—ā–į–Ĺ–ĺ–≤–Ľ–Ķ–Ĺ–ĺ, —á—ā–ĺ –ī–į–∂–Ķ —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č–Ļ –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä –¶–ě–ď-2 – —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī, –Ņ–ĺ–ī–ĺ–Ī–Ĺ–ĺ —Ä–į—Ā–Ņ—Ä–ĺ—Ā—ā—Ä–į–Ĺ–Ķ–Ĺ–Ĺ—č–ľ –Ě–ü–í–ü, –≤—č–∑—č–≤–į–Ķ—ā —Ā—É—Č–Ķ—Ā—ā–≤–Ķ–Ĺ–Ĺ—č–Ķ –Ņ–ĺ–≤—Ä–Ķ–∂–ī–Ķ–Ĺ–ł—Ź —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł—Ź. –ě–ī–Ĺ–į–ļ–ĺ –Ņ—Ä–ł —ā–Ķ—Ö –∂–Ķ —ć–ļ—Ā–Ņ–Ķ—Ä–ł–ľ–Ķ–Ĺ—ā–į–Ľ—Ć–Ĺ—č—Ö —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö –Ņ–ĺ–ī –≤–Ľ–ł—Ź–Ĺ–ł–Ķ–ľ –ļ—Ä–į—ā–ļ–ĺ—Ā—Ä–ĺ—á–Ĺ–ĺ–≥–ĺ –ł –Ņ—Ä–ĺ–ī–ĺ–Ľ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ł–Ķ–ľ–į –ź–ú–ď –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ł—Ā—Ć –Ľ–ł—ą—Ć –≤–Ķ—Ā—Ć–ľ–į –ĺ–≥—Ä–į–Ĺ–ł—á–Ķ–Ĺ–Ĺ—č–Ķ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –Ĺ–į–ł–Ī–ĺ–Ľ–Ķ–Ķ –≤–Ķ—Ä–ĺ—Ź—ā–Ĺ–ĺ —Ā–≤—Ź–∑–į–Ĺ—č —Ā –≤—č—Ā–≤–ĺ–Ī–ĺ–∂–ī–Ķ–Ĺ–ł–Ķ–ľ –≤–į–∑–ĺ–ī–ł–Ľ–į—ā–į—ā–ĺ—Ä–ĺ–≤ –ł NO, —á—ā–ĺ —Ā–Ņ–ĺ—Ā–ĺ–Ī—Ā—ā–≤—É–Ķ—ā –∑–į—Č–ł—ā–Ķ —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł—Ź.
–ě–Ī–Ķ –ł–∑–ĺ—Ą–ĺ—Ä–ľ—č –¶–ě–ď (–¶–ě–ď-1 –ł –¶–ě–ď-2) –Ņ–ĺ—Ā—ā–ĺ—Ź–Ĺ–Ĺ–ĺ —ć–ļ—Ā–Ņ—Ä–Ķ—Ā—Ā–ł—Ä—É—é—ā—Ā—Ź –≤ –Ņ–ĺ—á–ļ–į—Ö —É –≤–∑—Ä–ĺ—Ā–Ľ—č—Ö –ľ–Ľ–Ķ–ļ–ĺ–Ņ–ł—ā–į—é—Č–ł—Ö –ł —É—á–į—Ā—ā–≤—É—é—ā –≤ –Ī–ł–ĺ—Ā–ł–Ĺ—ā–Ķ–∑–Ķ –Ņ—Ä–ĺ—Ā—ā–į–Ĺ–ĺ–ł–ī–ĺ–≤. –ė–Ĺ–≥–ł–Ī–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ –¶–ě–ď –≤ –Ņ–ĺ—á–ļ–į—Ö –Ņ–ĺ–ī –≤–Ľ–ł—Ź–Ĺ–ł–Ķ–ľ –Ě–ü–í–ü –ł–ľ–Ķ–Ķ—ā —É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ—č–Ķ –Ņ–ĺ—Ā–Ľ–Ķ–ī—Ā—ā–≤–ł—Ź –ī–Ľ—Ź –∑–ī–ĺ—Ä–ĺ–≤—č—Ö –ī–ĺ–Ī—Ä–ĺ–≤–ĺ–Ľ—Ć—Ü–Ķ–≤, –ĺ–ī–Ĺ–į–ļ–ĺ –ľ–ĺ–∂–Ķ—ā –Ņ—Ä–ł–≤–ĺ–ī–ł—ā—Ć –ļ —Ā–Ķ—Ä—Ć–Ķ–∑–Ĺ—č–ľ –Ě–Į —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –∑–į–≤–ł—Ā—Ź—ā –ĺ—ā –ü–ď. –í –Ī–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ļ –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ĺ—Ā—Ć –≤—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ–ĺ–Ķ —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ –ł–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –≤—č–≤–Ķ–ī–Ķ–Ĺ–ł—Ź –Ĺ–į—ā—Ä–ł—Ź –Ņ—Ä–ł —ā–Ķ—Ä–į–Ņ–ł–ł —Ā –Ņ—Ä–ł–Ķ–ľ–ĺ–ľ –ļ–į–ļ–ĺ–≥–ĺ-–Ľ–ł–Ī–ĺ —ā—Ä–į–ī–ł—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–≥–ĺ –Ě–ü–í–ü –ł–Ľ–ł –ļ–ĺ–ļ—Ā–ł–Ī–ĺ–≤, —á—ā–ĺ —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł—Ź–ľ–ł —Ą—É–Ĺ–ļ—Ü–ł–ł –Ņ–ĺ—á–Ķ–ļ, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –∑–į–≤–ł—Ā—Ź—ā –ĺ—ā –Ņ—Ä–ł–Ķ–ľ–į –Ņ—Ä–ĺ—Ā—ā–į–Ĺ–ĺ–ł–ī–ĺ–≤, –ľ–ĺ–∂–Ķ—ā –Ņ—Ä–ł–≤–Ķ—Ā—ā–ł –ļ –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—é —Ā–ļ–ĺ—Ä–ĺ—Ā—ā–ł –ļ–Ľ—É–Ī–ĺ—á–ļ–ĺ–≤–ĺ–Ļ —Ą–ł–Ľ—Ć—ā—Ä–į—Ü–ł–ł. –Ě–į—Ä—É—ą–Ķ–Ĺ–ł–Ķ —Ą—É–Ĺ–ļ—Ü–ł–ł –Ņ–ĺ—á–Ķ–ļ –ľ–ĺ–∂–Ķ—ā –Ņ—Ä–ĺ–ł—Ā—Ö–ĺ–ī–ł—ā—Ć –≤ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–Ķ –≥–ł–Ņ–Ķ—Ä—ā–Ķ–Ĺ–∑–ł–ł –ł –ĺ—ā–Ķ–ļ–į. –Ę–į–ļ–ł–ľ –ĺ–Ī—Ä–į–∑–ĺ–ľ, –Ņ—Ä–ł –Ľ–Ķ—á–Ķ–Ĺ–ł–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā —Ä–ł—Ā–ļ–ĺ–ľ —Ä–į–∑–≤–ł—ā–ł—Ź –Ě–Į —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ņ–ĺ—á–Ķ–ļ (–Ņ–į—Ü–ł–Ķ–Ĺ—ā—č —Ā –∑–į—Ā—ā–ĺ–Ļ–Ĺ–ĺ–Ļ —Ā–Ķ—Ä–ī–Ķ—á–Ĺ–ĺ–Ļ –Ĺ–Ķ–ī–ĺ—Ā—ā–į—ā–ĺ—á–Ĺ–ĺ—Ā—ā—Ć—é, –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź–ľ–ł –Ņ–Ķ—á–Ķ–Ĺ–ł –ł –Ņ–ĺ—á–Ķ–ļ –ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č –Ņ–ĺ–∂–ł–Ľ–ĺ–≥–ĺ –≤–ĺ–∑—Ä–į—Ā—ā–į, –Ņ—Ä–ł–Ĺ–ł–ľ–į–≤—ą–ł–Ķ –ī–ł—É—Ä–Ķ—ā–ł–ļ–ł –ł–Ľ–ł –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä—č –ź–ü–§) —Ā–Ľ–Ķ–ī—É–Ķ—ā —Ā–ĺ–Ī–Ľ—é–ī–į—ā—Ć –ĺ—Ā—ā–ĺ—Ä–ĺ–∂–Ĺ–ĺ—Ā—ā—Ć –Ņ—Ä–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–ł –ļ–į–ļ —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–ĺ–≤ –¶–ě–ď-2, —ā–į–ļ –ł –ĺ–Ī—č—á–Ĺ—č—Ö –Ě–ü–í–ü. –Ę–į–ļ–ł–ľ –ĺ–Ī—Ä–į–∑–ĺ–ľ, –ĺ—á–Ķ–≤–ł–ī–Ĺ–ĺ, —á—ā–ĺ –¶–ě–ď-2-—Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č–Ķ –Ě–ü–í–ü –Ĺ–Ķ –ĺ–Ī–Ľ–į–ī–į—é—ā –ļ–į–ļ–ł–ľ-–Ľ–ł–Ī–ĺ –Ņ—Ä–Ķ–ł–ľ—É—Č–Ķ—Ā—ā–≤–ĺ–ľ –Ĺ–į–ī –Ĺ–Ķ—Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č–ľ–ł –Ě–ü–í–ü –≤ –ĺ—ā–Ĺ–ĺ—ą–Ķ–Ĺ–ł–ł –Ņ–ĺ—á–Ķ—á–Ĺ–ĺ–Ļ –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł [54]. –ü—Ä–ł —ć—ā–ĺ–ľ –ź–ú–ď –Ĺ–Ķ –≤—č–∑—č–≤–į–Ķ—ā –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–Ķ –Ņ–ĺ—á–Ķ–ļ –Ņ—Ä–ł –ľ–Ĺ–ĺ–≥–ĺ–ļ—Ä–į—ā–Ĺ–ĺ–ľ –Ņ—Ä–ł–Ķ–ľ–Ķ, —á—ā–ĺ –Ņ–ĺ–ī—ā–≤–Ķ—Ä–∂–ī–į–Ķ—ā—Ā—Ź –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł–ľ–ł –ł –Ī–ł–ĺ—Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ł–ľ–ł –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ź–ľ–ł [55]. –ú–Ķ—Ö–į–Ĺ–ł–∑–ľ–ĺ–ľ –Ņ–ĺ—á–Ķ—á–Ĺ–ĺ–Ļ –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł –ź–ú–ď, –Ņ–ĺ-–≤–ł–ī–ł–ľ–ĺ–ľ—É, —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź —É—Ā–ł–Ľ–Ķ–Ĺ–ł–Ķ –ļ—Ä–ĺ–≤–ĺ—ā–ĺ–ļ–į –≤ –Ņ–ĺ—á–ļ–į—Ö –ł–∑-–∑–į –Ņ–ĺ–≤—č—ą–Ķ–Ĺ–Ĺ–ĺ–Ļ –≤—č—Ä–į–Ī–ĺ—ā–ļ–ł NO.
–•–ĺ—ā—Ź –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–ĺ–≤ –¶–ě–ď-2 –≤–ľ–Ķ—Ā—ā–ĺ –ĺ–Ī—č—á–Ĺ—č—Ö –Ě–ü–í–ü –ī–Ľ—Ź —ā–Ķ—Ä–į–Ņ–ł–ł –į—Ä—ā—Ä–ł—ā–į –Ņ—Ä–ł–≤–ĺ–ī–ł—ā –ļ —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł—é —Ä–ł—Ā–ļ–į —Ä–į–∑–≤–ł—ā–ł—Ź —Ā–Ķ—Ä—Ć–Ķ–∑–Ĺ—č—Ö –Ě–Į —Ā–ĺ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č –Ė–ö–Ę, —Ä–ĺ–Ľ—Ć —ć—ā–ł—Ö –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–ĺ–≤ –≤ –≤–ĺ–∑–Ĺ–ł–ļ–Ĺ–ĺ–≤–Ķ–Ĺ–ł–ł –ł–Ľ–ł –ĺ–Ī–ĺ—Ā—ā—Ä–Ķ–Ĺ–ł–ł –ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ł—Ö –ļ–į—Ä–ī–ł–ĺ–≤–į—Ā–ļ—É–Ľ—Ź—Ä–Ĺ—č—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ –Ĺ–į –ī–į–Ĺ–Ĺ—č–Ļ –ľ–ĺ–ľ–Ķ–Ĺ—ā –Ĺ–Ķ—Ź—Ā–Ĺ–į. –í –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł—Ö –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź—Ö –Ī—č–Ľ–ĺ –Ņ—Ä–ĺ–ī–Ķ–ľ–ĺ–Ĺ—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ–ĺ, —á—ā–ĺ –≥–ł–Ņ–Ķ—Ä—ā–Ķ–Ĺ–∑–ł—Ź –ľ–ĺ–∂–Ķ—ā –Ī—č—ā—Ć –ł–Ĺ–ī—É—Ü–ł—Ä–ĺ–≤–į–Ĺ–į –ł–Ľ–ł —É—Ā–ł–Ľ–Ķ–Ĺ–į –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–į–ľ–ł –¶–ě–ď–2 –≤ —Ā—ā–Ķ–Ņ–Ķ–Ĺ–ł —Ā—Ö–ĺ–∂–Ķ–Ļ –ł–Ľ–ł –Ī–ĺ–Ľ–Ķ–Ķ –≤—č—Ā–ĺ–ļ–ĺ–Ļ, —á–Ķ–ľ –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –Ĺ–Ķ—Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –õ–° [56].
–ü—Ä–ł –ł–Ĺ–≥–ł–Ī–ł—Ä–ĺ–≤–į–Ĺ–ł–ł –¶–ě–ď-2 –ľ–ĺ–∂–Ķ—ā —É—Ā–ł–Ľ–ł–≤–į—ā—Ć—Ā—Ź –Ņ–ĺ–≤—Ä–Ķ–∂–ī–Ķ–Ĺ–ł–Ķ —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł—Ź (–ł–Ĺ–ī–ł–ļ–į—ā–ĺ—Ä —Ā–Ķ—Ä–ī–Ķ—á–Ĺ–ĺ–Ļ –ł—ą–Ķ–ľ–ł–ł) [57]; –ĺ–Ī—Ā—É–∂–ī–į–Ķ—ā—Ā—Ź –≤–ĺ–Ņ—Ä–ĺ—Ā –ĺ —ā–ĺ–ľ, –Ņ—Ä–ł–≤–ĺ–ī—Ź—ā –Ľ–ł —ć—ā–ł –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –ļ –į–Ī—Ā–ĺ–Ľ—é—ā–Ĺ–ĺ–ľ—É —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł—é —á–į—Ā—ā–ĺ—ā—č –ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ł—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ —Ā–Ķ—Ä–ī—Ü–į [58]. –≠—ā–ĺ –≤–Ľ–ł—Ź–Ĺ–ł–Ķ –Ĺ–į –ļ–į—Ä–ī–ł–ĺ–≤–į—Ā–ļ—É–Ľ—Ź—Ä–Ĺ—č–Ķ —Ą–į–ļ—ā–ĺ—Ä—č —Ä–ł—Ā–ļ–į –Ī–ĺ–Ľ–Ķ–Ķ –≤–į–∂–Ĺ–ĺ –ī–Ľ—Ź –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā —Ä–Ķ–≤–ľ–į—ā–ĺ–ł–ī–Ĺ—č–ľ –į—Ä—ā—Ä–ł—ā–ĺ–ľ, –ļ–ĺ—ā–ĺ—Ä—č–Ļ —Ā–ĺ–Ņ—Ä–ĺ–≤–ĺ–∂–ī–į–Ķ—ā—Ā—Ź —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł–Ķ–ľ —á–į—Ā—ā–ĺ—ā—č –ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ł—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ —Ā–Ķ—Ä–ī—Ü–į [59].
–í—Ā–ļ–ĺ—Ä–Ķ –Ņ–ĺ—Ā–Ľ–Ķ –Ĺ–į—á–į–Ľ–į –Ņ—Ä–ĺ–ī–į–∂–ł —Ü–Ķ–Ľ–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į –ł —Ä–ĺ—Ą–Ķ–ļ–ĺ–ļ—Ā–ł–Ī–į –Ī—č–Ľ–ĺ —É—Ā—ā–į–Ĺ–ĺ–≤–Ľ–Ķ–Ĺ–ĺ, —á—ā–ĺ –ĺ–Ī–į –õ–° –Ņ–ĺ–ī–į–≤–Ľ—Ź—é—ā –≤—č—Ä–į–Ī–ĺ—ā–ļ—É –Ņ—Ä–ĺ—Ā—ā–į—Ü–ł–ļ–Ľ–ł–Ĺ–į I2 (–ü–ďI2) —É –∑–ī–ĺ—Ä–ĺ–≤—č—Ö –ī–ĺ–Ī—Ä–ĺ–≤–ĺ–Ľ—Ć—Ü–Ķ–≤ [60]. –†–į–Ĺ–Ķ–Ķ –Ī—č–Ľ–ĺ –Ņ—Ä–ĺ–ī–Ķ–ľ–ĺ–Ĺ—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ–ĺ, —á—ā–ĺ –ü–ďI2 —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –Ņ—Ä–Ķ–ĺ–Ī–Ľ–į–ī–į—é—Č–ł–ľ –Ņ—Ä–ĺ–ī—É–ļ—ā–ĺ–ľ, –ļ–ĺ—ā–ĺ—Ä—č–Ļ —Ā–ł–Ĺ—ā–Ķ–∑–ł—Ä—É–Ķ—ā—Ā—Ź –Ņ—Ä–ł —É—á–į—Ā—ā–ł–ł –¶–ě–ď –≤ —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł–ł –ł –ł–Ĺ–≥–ł–Ī–ł—Ä—É–Ķ—ā –į–≥—Ä–Ķ–≥–į—Ü–ł—é —ā—Ä–ĺ–ľ–Ī–ĺ—Ü–ł—ā–ĺ–≤, –≤—č–∑—č–≤–į–Ķ—ā –≤–į–∑–ĺ–ī–ł–Ľ–į—ā–į—Ü–ł—é –ł –Ņ—Ä–Ķ–ī–ĺ—ā–≤—Ä–į—Č–Ķ–Ĺ–ł–Ķ –Ņ—Ä–ĺ–Ľ–ł—Ą–Ķ—Ä–į—Ü–ł–ł –≤–į—Ā–ļ—É–Ľ—Ź—Ä–Ĺ—č—Ö –ļ–Ľ–Ķ—ā–ĺ–ļ –≥–Ľ–į–ī–ļ–ĺ–Ļ –ľ—É—Ā–ļ—É–Ľ–į—ā—É—Ä—č in vitro [61]. –†–į–Ĺ–Ķ–Ķ –Ņ—Ä–Ķ–ī–Ņ–ĺ–Ľ–į–≥–į–Ľ–ĺ—Ā—Ć, —á—ā–ĺ –ü–ďI2 —Ā–ł–Ĺ—ā–Ķ–∑–ł—Ä—É–Ķ—ā—Ā—Ź –≤ –ĺ—Ā–Ĺ–ĺ–≤–Ĺ–ĺ–ľ –Ņ—Ä–ł —É—á–į—Ā—ā–ł–ł –¶–ě–ď-1 –ł —á—ā–ĺ –¶–ě–ď-1 —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –Ķ–ī–ł–Ĺ—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ–Ļ –ł–∑–ĺ—Ą–ĺ—Ä–ľ–ĺ–Ļ, –ļ–ĺ—ā–ĺ—Ä–į—Ź –Ņ–ĺ—Ā—ā–ĺ—Ź–Ĺ–Ĺ–ĺ —ć–ļ—Ā–Ņ—Ä–Ķ—Ā—Ā–ł—Ä—É–Ķ—ā—Ā—Ź –≤ –ļ–Ľ–Ķ—ā–ļ–į—Ö —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł—Ź.
–í–Ņ–ĺ—Ā–Ľ–Ķ–ī—Ā—ā–≤–ł–ł –Ī—č–Ľ–ĺ —É—Ā—ā–į–Ĺ–ĺ–≤–Ľ–Ķ–Ĺ–ĺ, —á—ā–ĺ —ć—ā–į –≥–ł–Ņ–ĺ—ā–Ķ–∑–į –Ĺ–Ķ–≤–Ķ—Ä–Ĺ–į: –≤ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł –Ĺ–į –ľ—č—ą–į—Ö –ł –≤ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł—Ö –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź—Ö –Ī—č–Ľ–ĺ –Ņ—Ä–ĺ–ī–Ķ–ľ–ĺ–Ĺ—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ–ĺ, —á—ā–ĺ –¶–ě–ď-2 —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –Ņ—Ä–Ķ–ĺ–Ī–Ľ–į–ī–į—é—Č–Ķ–Ļ –ł–∑–ĺ—Ą–ĺ—Ä–ľ–ĺ–Ļ [62, 63]. –ö–į—Ä–ī–ł–ĺ–≤–į—Ā–ļ—É–Ľ—Ź—Ä–Ĺ—č–Ļ —ć—Ą—Ą–Ķ–ļ—ā –ü–ďI2 in vitro –Ņ—Ä–ĺ—ā–ł–≤–ĺ–Ņ–ĺ–Ľ–ĺ–∂–Ķ–Ĺ —ć—Ą—Ą–Ķ–ļ—ā—É —ā—Ä–ĺ–ľ–Ī–ĺ–ļ—Ā–į–Ĺ–į A2 (TXA2) – –ĺ—Ā–Ĺ–ĺ–≤–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ĺ–ī—É–ļ—ā–į –¶–ě–ď-1 –≤ —ā—Ä–ĺ–ľ–Ī–ĺ—Ü–ł—ā–į—Ö, –ļ–ĺ—ā–ĺ—Ä—č–Ļ –≤—č–∑—č–≤–į–Ķ—ā –į–≥—Ä–Ķ–≥–į—Ü–ł—é —ā—Ä–ĺ–ľ–Ī–ĺ—Ü–ł—ā–ĺ–≤, —Ā—É–∂–Ķ–Ĺ–ł–Ķ –ļ—Ä–ĺ–≤–Ķ–Ĺ–ĺ—Ā–Ĺ—č—Ö —Ā–ĺ—Ā—É–ī–ĺ–≤ –ł –≤–į—Ā–ļ—É–Ľ—Ź—Ä–Ĺ—É—é –Ņ—Ä–ĺ–Ľ–ł—Ą–Ķ—Ä–į—Ü–ł—é [64]. –ü—Ä–ł —ć—ā–ĺ–ľ —ā—Ä–į–ī–ł—Ü–ł–ĺ–Ĺ–Ĺ—č–Ķ –Ě–ü–í–ü –ł–Ĺ–≥–ł–Ī–ł—Ä—É—é—ā –Ī–ł–ĺ—Ā–ł–Ĺ—ā–Ķ–∑ TXA2 –ł –ü–ďI2, –į –ļ–ĺ–ļ—Ā–ł–Ī—č –Ĺ–Ķ –≤–Ľ–ł—Ź—é—ā –Ĺ–į –Ī–ł–ĺ—Ā–ł–Ĺ—ā–Ķ–∑ TXA2, —á—ā–ĺ —Ā–≤—Ź–∑–į–Ĺ–ĺ —Ā –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł–Ķ–ľ –¶–ě–ď-2 –≤ —ā—Ä–ĺ–ľ–Ī–ĺ—Ü–ł—ā–į—Ö. –Ę–į–ļ–ł–ľ –ĺ–Ī—Ä–į–∑–ĺ–ľ, –Ņ—Ä–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–ł —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–ĺ–≤ –¶–ě–ď-2 —É–≤–Ķ–Ľ–ł—á–ł–≤–į–Ķ—ā—Ā—Ź —Ä–ł—Ā–ļ —Ä–į–∑–≤–ł—ā–ł—Ź —ā—Ä–ĺ–ľ–Ī–ĺ–∑–į, –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č —Ā—ā–į–Ĺ–ĺ–≤—Ź—ā—Ā—Ź –Ī–ĺ–Ľ–Ķ–Ķ –Ņ—Ä–Ķ–ī—Ä–į—Ā–Ņ–ĺ–Ľ–ĺ–∂–Ķ–Ĺ–Ĺ—č–ľ–ł –ļ –ł–Ĺ—Ā—É–Ľ—Ć—ā—É –ł –ł–Ĺ—Ą–į—Ä–ļ—ā—É [64]. –í —ć–Ņ–ł–ī–Ķ–ľ–ł–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł—Ö –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź—Ö [65, 66] —ā–į–ļ–∂–Ķ –ł–∑—É—á–į–Ľ–į—Ā—Ć –ļ–į—Ä–ī–ł–ĺ–≤–į—Ā–ļ—É–Ľ—Ź—Ä–Ĺ–į—Ź –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā—Ć –ļ–ĺ–ļ—Ā–ł–Ī–ĺ–≤. –ź–≥–Ķ–Ĺ—ā—Ā—ā–≤–į FDA –≤ –°–®–ź –ł EMEA –≤ –ē–≤—Ä–ĺ–Ņ–Ķ [67, 68], –į —ā–į–ļ–∂–Ķ –ź–≥–Ķ–Ĺ—ā—Ā—ā–≤–ĺ –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č—Ö –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –ė—ā–į–Ľ–ł–ł (AIFA) [69] –≤—č–Ņ—É—Ā—ā–ł–Ľ–ł –Ņ—Ä–Ķ–ī—É–Ņ—Ä–Ķ–∂–ī–Ķ–Ĺ–ł–Ķ –ĺ –ļ–į—Ä–ī–ł–ĺ–≤–į—Ā–ļ—É–Ľ—Ź—Ä–Ĺ–ĺ–ľ —Ä–ł—Ā–ļ–Ķ –Ņ—Ä–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–ł —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–ĺ–≤ –¶–ě–ď-2, —ā–į–ļ –∂–Ķ –ļ–į–ļ –ł –Ņ—Ä–ł –Ņ—Ä–ł–Ķ–ľ–Ķ –Ĺ–Ķ—Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –Ě–ü–í–ü. –°–Ľ–Ķ–ī—É–Ķ—ā —É—á–ł—ā—č–≤–į—ā—Ć —ć—ā—É –ł–Ĺ—Ą–ĺ—Ä–ľ–į—Ü–ł—é –Ņ—Ä–ł –Ľ–Ķ—á–Ķ–Ĺ–ł–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –ļ–į—Ä–ī–ł–ĺ–≤–į—Ā–ļ—É–Ľ—Ź—Ä–Ĺ—č–ľ–ł —Ą–į–ļ—ā–ĺ—Ä–į–ľ–ł —Ä–ł—Ā–ļ–į. –í –ĺ—ā–Ľ–ł—á–ł–Ķ –ĺ—ā –¶–ě–ď-2-—Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –Ě–ü–í–ü, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –Ĺ–Ķ –≤–Ľ–ł—Ź—é—ā –Ĺ–į –į–≥—Ä–Ķ–≥–į—Ü–ł—é —ā—Ä–ĺ–ľ–Ī–ĺ—Ü–ł—ā–ĺ–≤ [70–72], –ź–ú–ď –ĺ–Ī–Ľ–į–ī–į–Ķ—ā –į–Ĺ—ā–ł—ā—Ä–ĺ–ľ–Ī–ĺ—Ü–ł—ā–į—Ä–Ĺ–ĺ–Ļ –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć—é in vitro –ł ex vivo, —Ā—Ä–į–≤–Ĺ–ł–ľ–ĺ–Ļ —Ā –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ–ľ –į—Ü–Ķ—ā–ł–Ľ—Ā–į–Ľ–ł—Ü–ł–Ľ–ĺ–≤–ĺ–Ļ –ļ–ł—Ā–Ľ–ĺ—ā—č [25]. –Ď–Ľ–į–≥–ĺ–ī–į—Ä—Ź —ć—ā–ĺ–ľ—É —Ą–į—Ä–ľ–į–ļ–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ĺ–ľ—É —ć—Ą—Ą–Ķ–ļ—ā—É –ī–į–Ĺ–Ĺ–ĺ–Ķ –õ–° —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –Ī–ĺ–Ľ–Ķ–Ķ –Ņ–ĺ–ī—Ö–ĺ–ī—Ź—Č–ł–ľ, —á–Ķ–ľ —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č–Ļ –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä –¶–ě–ď-2, –ī–Ľ—Ź –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –ĺ–ī–Ĺ–ł–ľ –ł–Ľ–ł –Ī–ĺ–Ľ–Ķ–Ķ –ļ–į—Ä–ī–ł–ĺ–≤–į—Ā–ļ—É–Ľ—Ź—Ä–Ĺ—č–ľ–ł —Ą–į–ļ—ā–ĺ—Ä–į–ľ–ł —Ä–ł—Ā–ļ–į.
–í —Ü–Ķ–Ľ–ĺ–ľ –Ĺ–į –ĺ—Ā–Ĺ–ĺ–≤–į–Ĺ–ł–ł –≤—Ā–Ķ–Ļ –ł–∑–Ľ–ĺ–∂–Ķ–Ĺ–Ĺ–ĺ–Ļ –≤—č—ą–Ķ –ł–Ĺ—Ą–ĺ—Ä–ľ–į—Ü–ł–ł –ľ–ĺ–∂–Ĺ–ĺ —Ā–ī–Ķ–Ľ–į—ā—Ć –≤—č–≤–ĺ–ī –ĺ —ā–ĺ–ľ, —á—ā–ĺ –ź–ú–ď —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ—č–ľ –Ņ—Ä–ĺ—ā–ł–≤–ĺ–≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–ľ –õ–° —Ā —Ö–ĺ—Ä–ĺ—ą–ł–ľ–ł –Ņ–į—Ä–į–ľ–Ķ—ā—Ä–į–ľ–ł –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł –ī–Ľ—Ź –Ė–ö–Ę, –Ņ–ĺ—á–Ķ–ļ –ł —Ā–Ķ—Ä–ī–Ķ—á–Ĺ–ĺ-—Ā–ĺ—Ā—É–ī–ł—Ā—ā–ĺ–Ļ —Ā–ł—Ā—ā–Ķ–ľ—č. –Ď–Ľ–į–≥–ĺ–ī–į—Ä—Ź —ć—ā–ł–ľ —Ā–≤–ĺ–Ļ—Ā—ā–≤–į–ľ –ł —Ā–Ņ–Ķ—Ü–ł—Ą–ł—á–Ķ—Ā–ļ–ĺ–ľ—É –ľ–Ķ—Ö–į–Ĺ–ł–∑–ľ—É –ī–Ķ–Ļ—Ā—ā–≤–ł—Ź –ź–ú–ď —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –Ĺ–į–ł–Ī–ĺ–Ľ–Ķ–Ķ –Ņ–ĺ–ī—Ö–ĺ–ī—Ź—Č–ł–ľ –ī–Ľ—Ź –Ņ—Ä–ĺ–ī–ĺ–Ľ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź, –ĺ—Ā–ĺ–Ī–Ķ–Ĺ–Ĺ–ĺ —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –Ņ–ĺ–∂–ł–Ľ–ĺ–≥–ĺ –≤–ĺ–∑—Ä–į—Ā—ā–į –ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź–ľ–ł –Ņ–ĺ—á–Ķ–ļ –ł–Ľ–ł —Ā–Ķ—Ä–ī–Ķ—á–Ĺ–ĺ-—Ā–ĺ—Ā—É–ī–ł—Ā—ā–ĺ–Ļ —Ā–ł—Ā—ā–Ķ–ľ—č.
–†–Ķ—Ą–Ķ—Ä–į—ā –Ņ–ĺ–ī–≥–ĺ—ā–ĺ–≤–ł–Ľ –ļ.–ľ.–Ĺ. –Ě.–ď. –õ—é—ā–ĺ–≤ –Ņ–ĺ –ľ–į—ā–Ķ—Ä–ł–į–Ľ–į–ľ —Ā—ā–į—ā—Ć–ł Z. Jajic, M. Malaise, K. Nekam et al. «Gastrointestinal safety of amtolmetin guacyl in comparison with celecoxib in patients with rheumatoid arthritis» // Clinical and Experimental Rheumatology. 2005. Vol. 23, –†. 809–818
–õ–ł—ā–Ķ—Ä–į—ā—É—Ä–į
1. Sokka T. Work disability in yearly rheumatoid arthritis // Clin Exp Rheumatol 2003. Vol. 21 (Suppl. 31). –†. 571–574.
2. Scott D.L., Smith C., Kingsley G. Joint damage and disability in rheumatoid arthritis: an updated systematic review // Clin Exp Rheumatol. 2003. Vol. 21 (Suppl. 31). –†. 520–527.
3. Pincus T., Kavanaugh A., Sokka T. Benefit/ risk of therapies for rheumatoid arthritis: underestimation of the “side effects” or risks of RA leads to underestimation of the benefit/ risk of therapies // Clin Exp Rheumatol. 2004. Vol. 22 (Suppl. 35). P. 2–11.
4. Henry D.A. Side effects of non steroidal anti-inflammatory drugs // Balliere’s Clin Rheumatol. 1988. Vol. 2. P. 425–454.
5. Brater D.C. Anti-inflammatory agents and renal function // Semin Arthritis Rheum. 2002. Vol. 32 (Suppl. 1). P. 33–42.
6. Wolfe M.M., Lichtenstein D.R., Singh G. Gastrointestinal toxicity of non-steroidal anti-inflammatory drugs // N Eng J Med. 1999. Vol. 340. P. 1888–1899.
7. Macdonald T.M., Morant S.V., Robinson G.C. et al. Association of upper gastrointestinal toxicity of non-steroidal anti-inflammatory drugs with continued exposure: cohort study // BMJ. 1997. Vol. 315. P. 1333–1337.
8. Langman M.J., Weil J., Wainwright P. et al. Risks of bleeding peptic ulcer associated with individual non-steroidal anti-inflammatory drugs // Lancet. 1994. Vol. 343. P. 1075–1058.
9. Haslock I. Review of induced upper gastrointestinal morbidity and mortality. In CHELI R (Ed.): Treatment and Prevention of NSAID Induced Gastropathy // Royal Society of Medicine Services International Congress and Symposium Series. 1989. Vol. 147. P. 3–10.
10. Garcia-Rodriguez L.A., Jick H. Risk of upper gastrointestinal bleeding and perforation associated with individual non steroidal anti-inflammatory drugs // Lancet. 1994. Vol. 343. P. 769–772.
11. Scarpignato C., Pelosini I. Prevention and treatment of non-steroidal anti-inflammatory drug-induced gastro-duodenal damage: rationale for the use of antisecretory compounds // Ital J Gastroenterol Hepatol. 1999. Vol. 31 (Suppl. 1). P. 63–72.
12. Scarpignato C. Non steroidal anti-inflammatory drugs: how do they damage gastroduodenal mucosa? // Dig Dis. 1995. Vol. 13 (Suppl. 1). P. 9–39.
13. Redfern J.S., Feldman M. Role of prostaglandins in preventing gastrointestinal ulceration: Induction of ulcers by antibodies to prostaglandins // Gastroenterology. 1989. Vol. 96. P. 596–605.
14. Halter F., Tarnawski A.S., Schmassmann A., Peskar B.M. Cyclooxygenase 2- implications on maintenance of gastric mucosa integrity and ulcer healing: controversial issues and perspectives // Gut. 2001. Vol. 49. P. 443–453.
15. Wallace J.L., Devchand P.R. Emerging roles for cyclooxygenase-2 in gastrointestinal mucosal defence // Br J Pharmacol. 2005. Vol. 145. P. 275–282.
16. Wu C.Y., Wu M.S., Chen C.J., Li M.C., Lin J.T., Chen G.H. The interaction of H. pylori infection and NSAIDs in cyclooxygenase-2 mRNA expression in gastric antral, corpus mucosa, and gastric ulcer // J Clin Gastroenterol. 2005. Vol. 39. P. 50–55.
17. Scarpignato C., Bjarnason I., Bretagne J.-F. et al. Working Team Report: Towards a GI Safer Antiinflammatory Therapy // Gastroenterology Int. 1999. Vol. 12. P. 186–215.
18. Bensen W.G., Fiechtner J.J., Mcmillen J.I. et al. Treatment of osteoarthritis with celecoxib, a cyclooxygenase 2 inhibitor: a randomized, controlled trial // Mayo Clin Proc. 1999. Vol. 74. P. 1095–1105.
19. Emery P., Zeidler H., Kwien T. et al. Celecoxib versus diclofenac in long term management of rheumatoid arthritis: randomized, double blind comparison // Lancet. 1999. Vol. 354. P. 2106–2611.
20. Silverstein F.E., Faich G., Goldstein J.L. et al. Gastrointestinal toxicity with celecoxib vs non steroidal anti-inflammatory drugs for osteoarthritis and rheumatoid arthritis. The CLASS study: a randomized, controlled trial // JAMA. 2000. Vol. 284 (10). P. 1247–1255.
21. Bombardier C., Laine L., Reicin A. et al. Comparison of upper gastrointestinal toxicity of rofecoxib and naproxen in patients with rheumatoid arthritis // N Engl J Med. 2000. Vol. 343. P. 1520–1528.
22. Deeks J.J., Smith L.A., Bradley M.D. Efficacy, tolerability, and upper gastrointestinal safety of celecoxib for treatment of osteoarthritis and rheumatoid arthritis: systematic review of randomised controlled trials // BMJ. 2002. Vol. 325. P. 619–624.
23. Watson D.J., Yu Q., Bolognese J.A., Reicin A.S., Simon T.J. The upper gastrointestinal safety of rofecoxib vs. NSAIDs: an updated combined analysis // Curr Med Res Opin. 2004. Vol. 20. P. 1539–1548.
24. Tubaro E., Belogi L., Mezzadri C.M., Ruco L., Stopacciaro A. Studies on the gastric tolerability of the new non steroidal anti-inflammatory drug amtolmetin guacyl // Arzneim Forsch/Drug Res. 1995. Vol. 45. P. 1298–1302.
25. Tubaro E., Belogi L., Mezzadri C.M. Anti-inflammatory and antiplatelet effect of Amtolmetin Guacyl, a new gastroprotective non-steroidal anti-inflammatory drug // Arzneim Forsch/Drug Res. 2001. Vol. 51. P. 737–742.
26. Tubaro E., Belogi L., Mezzadri C.M. The mechanism of action of amtolmetin guacyl, a new gastroprotective non-steroidal anti-inflammatory drug. Eur J Pharmacol. 2000. Vol. 387. P. 233–244.
27. Bianchi Porro G., Montrone F., Lazzaroni M., Manzionna G., Caruso I. Clinical and gastroscopic evaluation of amtolmetin guacyl versus diclofenac in patients with rheumatoid arthritis // Ital J Gastroenterol Hepatol. 1999. Vol. 3. P. 378–385.
28. Tavella G., Ursini G. Studio clinico sull’attivita antinfiammatoria e sulla tollerabilita gastroenterica di amtolmetin guacil, un nuovo FANS, in confronto a diclofenac, su pazienti anziani con patologie osteoarticolari // Clin Ter. 1997. Vol. 148. P. 543–548.
29. Montrone F., Santandrea S., Caruso I. et al. Amtolmetin guacyl versus piroxicam in patients with osteoarthritis. J Int Med Res. 2000. Vol. 28. P. 91–100.
30. Marcolongo R., Frediani B., Biasi G., Minari C., Barreca C. Metanalysis of the tolerability of amtolmetin guacyl, a new, efficacious, non-steroidal anti-inflammatory drug, compared with traditional NSAIDs // Clin Drug Invest. 1999. Vol. 17. P. 89–96.
31. De Pretis G., Tasini E. Tollerabilita gastrica dell’antiinfiammatorio Amtolmetina Guacil: meta-analisi dei trials terapeutici. Medicina Terapia. 2002.
32. Tubaro E., Belogi L., Mezzadri C.M., Bettelli E. Impact on the bowel of amtolmetin guacyl, a new gastroprotective non-steroidal anti-inflammatory drug // Eur J Pharmacol. 2003. Vol. 467. P. 173–183.
33. Riezzo G., Chiloiro M., Montanaro S. Protective effect of amtolmetin guacyl versus placebo, a typical NSAID and misoprostol in healthy volunteers evaluated as gastric electrical activity in alcohol induced stomach damage // Dig Dis Sci. 2001. Vol. 46. P. 1797–1804.
34. Pisano C., Grandi D., Morini G. et al. Gastrosparing effect of new anti-inflammatory drug amtolmetin guacyl in the rat: involvement of nitric oxide // Dig Dis Sci. 1999. Vol. 44. P. 713–724.
35. Felson D.T., Anderson J.J., Boers M. et al. The American College of Rheumatology preliminary core Set of disease activity measures for rheumatoid arthritis clinical trials // Arthritis Rheum. 1993. Vol. 36. P. 729–740.
36. Felson D.T. et al. American College of Rheumatology. Preliminary definition of improvement in rheumatoid arthritis // Arthritis Rheum. 1996. Vol. 39. P. 535–537.
37. Simon L.S., Weawer A.L., Graham D.Y. et al. The anti-inflammatory and upper gastrointestinal effects of celecoxib in rheumatoid arthritis: a randomized, controlled trial // JAMA. 2000. Vol. 82. P. 1921–1928.
38. Mitchell J.A., Warner T.D. Cyclooxygenase 2: pharmacology, physiology, biochemistry and relevance to NSAID therapy // Br J Pharmacol. 1999. Vol. 128. P. 1121–1132.
39. Zhao S.S., Mcmillen J.I., Markenson J.A. et al. Evaluation of functional status aspects of health related quality of life of patients with osteoarthritis treated with celecoxib // Pharmacotherapy. 1999. Vol. 19. P. 1269–1278.
40. Silverstein F.E., Graham D.Y., Senior J.R. et al. Misoprostol reduces serious gastrointestinal complications in patients with rheumatoid arthritis receiving non-steroidal anti-inflammatory drugs: a randomized, double blind, placebo controlled trial // Ann Intern Med. 1995. Vol. 123. P. 241–249.
41. Scarpignato C., Lazzaroni M., Pelosini I., Bianchi Porro G. Selective inhibitors of cyclooxyganase-2: myth or reality ? [in Italian]. Arg Gastroenterol Clin. 1997. Vol. 10. P. 53–75.
42. Brooks P., Emery P., Evans J.F. et al. Interpreting the clinical significance of the differential inhibition of cyclooxygenase-1 and cyclooxygenase-2 // Rheumatology. 1999. Vol. 38. P. 779–788.
43. Lipsky L.P., Abramson S.B., Crofford L., Dubois R.N., Simon L.S., Van D.E., Putte L.B. The classification of cyclooxygenase inhibitors. J Rheumatol. 1998. Vol. 25. P. 2298–2303.
44. Warner T.D., Giuliano F., Vojnovic I., Bukasa A., Mitchell J.A., Vane J.R. Nonsteroid drug selectivities for cyclo-oxygenase-1 rather than cyclo-oxygenase-2 are associated with human gastrointestinal toxicity: a full in vitro analysis // Proc Natl Acad Sci USA. 1999. Vol. 96. P. 7563–7568.
45. Tacconelli S., Capone M.L., Sciulli M.G., Ricciotti E., Patrignani P. The biochemical selectivity of novel COX-2 inhibitors in whole blood assays of COX-isozyme activity // Curr Med Res Opin. 2002. Vol. 18. P. 503–511.
46. Lazzaroni M., Anderloni A., Bianchi Porro G. The effects on gastroduodenal mucosa of a new non-steroidal anti-inflammatory drug, amtolmetin guacyl, versus piroxicam in healthy volunteers: a short term, double blind, endoscopically controlled study // Eur J Gastroenterol Pathol. 2001. Vol. 13. P. 833–839.
47. Hawkey C.J., Langstrom G., Naesdal J. et al. Significance of dyspeptic symptoms during healing and maintenance of NSAID associated gastroduodenal lesions with omeprazole, misoprostol and ranitidine // Gastroenterology. 1997. Vol. 112. P. 144.
48. Singh G., Ramey D.R., Morfeld D., Shi H., Hatoum H.T., Fries J.F. Gastrointestinal tract complications of non-steroidal anti-inflammatory drug treatment in rheumatoid arthritis // Arch Intern Med. 1996. Vol. 156. P. 1530–1536.
49. Coruzzi G., Coppelli G., Spaggiari S. et al. Gastroprotective effects of amtolmetin guacyl: a new non-steroidal anti-inflammatory drug that activates inducible gastric nitric oxide synthase // Dig Liv Dis. 2002. Vol. 34. P. 403–410.
50. Brzozowski T., Konturek P.C., Konturek S.J. et al. Gastroprotective and ulcer healing effects of nitric oxide releasing nonsteroidal anti-inflammatory drugs // Dig Liv Dis. 2000. Vol. 32. P. 583–594.
51. Teppermann B.L., Soper B.D. Nitric oxide synthase induction and cytoprotection of rat gastric mucosa from injury by ethanol // Can J Physiol Pharmacol. 1994. Vol. 72. P. 1308–1312.
52. Lopez-Belmonte J., Whittle B.J.R., Moncada S. The actions of nitric oxide donors in the prevention or induction of injury to the rat gastric mucosa // Br J Pharmacol. 1993. Vol. 108. P. 73–78.
53. Morini G., Guaiata E., Lazzaretti M., Grandi D., Coruzzi G. Morphological features of rat gastric mucosa after acute and chronic treatment with amtolmetin guacyl: comparison with non-selective and COX2 selective NSAIDs. Digestion. 2003. Vol. 68. P. 124–132.
54. Schnitzer T.J. Cyclooxygenase-2-specific inhibitors: are they safe? // Am J Med. 2001. Vol. 110 (1A). P. 46–49.
55. Niccoli L., Bellino S., Cantini F. Renal tolerability of three commonly employed non-steroidal anti-inflammatory drugs in elderly patients with osteoarthritis // Clin Exp Rheumatol. 2002. Vol. 20. P. 201–207.
56. Aw T.J., Haas S.J., Liew D., Krum H.: Metaanalysis of cyclooxygenase-2 inhibitors and their effects on blood pressure // Arch Intern Med. 2005. Vol. 165. P. 490–496.
57. Justice E., Carruthers D.M. Cardiovascular risk and COX-2 inhibition in rheumatology practice // J Hum Hypertens. 2005. Vol. 19. P. 1–5.
58. Wong D., Wang M., Cheng Y., Fitzgerald G.A. Cardiovascular hazard and nonsteroidal anti-inflammatory drugs // Curr Opin Pharmacol. 2005. Vol. 5. P. 204–210.
59. Wallberg-Jonsson S., Cederfelt M., Rantapaa Dahlqvisp S. Hemostatic factors and cardiovascular disease in active rheumatoid arthritis: an 8-year follow-up study // J Rheumatol. 2000. Vol. 27. P. 71–75.
60. Fitzgerald G.A. COX-2 and beyond: approaches to prostaglandin inhibition in human disease // Nat Rev Drug Discov. 2003. Vol. 2. P. 879–899.
61. Schror K., Weber A.A. Roles of vasodilatatory prostaglandins in mitogenesis of vascular smooth muscle cells // Agents Actions. 1997. Vol. 48 (Suppl.). P. 63–91.
62. Egan K.M., Lawson J.A., Fries S. et al. Cyclooxygenase-2-derived prostacyclin confers atheroprotection on female mice // Obstet Gynecol Surv. 2005. Vol. 60. P. 309–310.
63. Mcadam B.F., Catella-Lawson F., Mardini I.A., Kapoor S., Lawson J.A., Fitzgerald G.A. Systemic biosynthesis of prostacyclin by cyclooxygenase (COX)-2: the human pharmacology of a selective inhibitor of COX // Proc Natl Acad Sci USA. 1999. Vol. 96. P. 272–277.
64. Fitzgerald G.A. Coxibs and cardiovascular disease // N Eng J Med. 2004. Vol. 351. P. 1709–1711.
65. Mukherjee D., Nissen S.E., Topol E.J. Risk of cardiovascular events associated with selective Cox-2 inhibitors // JAMA. 2001. Vol. 286. P. 954–959.
66. Ray W.A., Stein C.M., Daugherty J.R., Hall K., Arbogast P.G., Griffin M.R. COX-2 selective non-steroidal anti-inflammatory drugs and risk of serious coronary heart disease // Lancet. 2002. Vol. 360. P. 1071–1073.
67. EMEA/62838/2005 Public statement: European Medicines Agency announces regulatory action on COX-2 inhibitors [http://www.emea.eu.int/htms/hotpress/d6275705.htm].
68. FDA Public Health Advisory: FDA announces important changes and additional warnings for COX-2 selective and non-selective non-steroidal anti-inflammatory drugs (NSAIDs) [http://www.fda.gov/cder/drug/advisory/COX2.htm].
69. AIFA: Comunicato n. 5 del 17 febbraio 2005. COX 2, AIFA adotta misure a tutela salute cittadini [http://www.agenziafarmaco.it/com_n5_17_02_2005.html].
70. Leese P.T., Hubbard R.C., Karim A., Isakson P.C., Yu S.S., Geis G.S. Effects of celecoxib, a novel cyclooxygenase-2 inhibitor, on platelet function in healthy adults: a randomized, controlled trial // J Clin Pharmacol. 2000. Vol. 40. P. 124–132.
71. Wilner K.D., Rushing M., Walden C. et al. Celecoxib does not affect the antiplatelet activity of aspirin in healthy volunteers // J Clin Pharmacol. 2002. Vol. 42. P. 1027–1030.
72. Catella-Lawson F., Reilly M.P., Kapoor S.C. et al. Cyclooxygenase inhibitors and the antiplatelet effects of aspirin // N Engl J Med. 2001. Vol. 345. P.1809.












