Диагностическая и лечебная стратегия при острой и хронической диарее имеет существенные различия. Они обусловлены тем, что острая диарея разрешается самостоятельно и лечебная стратегия ограничивается эмпирическим выбором противодиарейных препаратов, тогда как для успешной терапии хронической диареи принципиально важно определение специфических причин, лежащих в основе заболевания [1,2]. Это может потребовать простых мер – таких как прекращение приема слабительных при их передозировке или более сложных – как назначение безглютеновой диеты при целиакии, иммуносупрессивных препаратов при воспалительных заболеваниях толстой кишки или хирургическое удаление гормонально продуцирующей опухоли. Тем не менее у многих больных, несмотря на предпринимаемые усилия, установить точный диагноз длительное время не удается, что заставляет врача искать оптимальные средства симптоматической или патогенетической терапии для коррекции имеющихся нарушений.
Диарея субъективно определяется больным, как учащение частоты стула более 3 раз в сутки в сочетании с изменением консистенции фекалий, появлением ургентных позывов на дефекацию. Однако с медицинских позиций критериями диареи является стойкое повышение содержания жидкости в фекалиях с 60–75% до 85–90% или увеличение их массы более 200 г в сутки на фоне Западной диеты [3,4]. Таким образом, больной может жаловаться на наличие диареи, но количественная оценка массы фекалий не подтверждает данного факта. Это имеет важное клиническое значение. Помимо этого, с практической точки зрения выделяют острую диарею, продолжающуюся 7–10 дней, затяжную диарею – от 2 до 11 недель и хроническую – 3 месяца и более [5]. Дифференциально–диагностический круг и терапия в каждом случае будет различной. Отличаются и патофизиологические механизмы диарейного синдрома. Они включают секрецию криптами анионов («секреторная» диарея), повышенную внутрипросветную осмолярность («осмотическая»диарея), нарушенную всасывательную функцию и ускоренный транзит. Роль двигательных нарушений, как первичной причины диареи, оспаривается, но большинство исследователей все же полагают, что ускоренное время транзита способствует тяжести диареи, уменьшая время контакта между внутрипросветной жидкостью и абсорбтивной поверхностью [6]. Хотя в развитии диареи могут быть задействованы сразу несколько механизмов, для простоты можно считать, что в большинстве случаев речь идет о дисбалансе между абсорбтивными и секреторными процессами. На протяжении многих лет доминирует догмат, объясняющий диарею стимулированной секрецией. Эта концепция построена на том, что кишечный эпителий функционально не поврежден, но «трудится» максимально усердно в направлении активной секреции. Эта концепция верна для диареи, вызванной эндокринными опухолями и бактериальными токсинами и, отчасти, воспалительными заболеваниями толстой кишки [7,8].
Острая диарея
Факторами, приводящими к развитию острой диареи, являются диетические погрешности и пищевая аллергия (непереносимость цитрусовых, клубники, молока, злоупотребление кофе, пивом, клетчаткой), прием некоторых лекарственных препаратов (магнийсодержащие препараты, колхицин, теофиллин, антибиотики) и, конечно же, инфекционные агенты – бактерии, вирусы и простейшие. Истинная водянистая диарея развивается вследствие вирусного гастроэнтерита (ротовирусы, Норфолк вирусы и др.) или воздействия бактериальных токсинов (золотистый стафилококк энтеротоксигенная E.coli, Vibrio cholerae, криптоспоридии и др.).
Невоспалительная диарея [9,10]. Как правило, у больных не отмечается лихорадки, интоксикации, выделения крови и обилия лейкоцитов в фекалиях, но из–за вовлечения в процесс тонкой кишки наблюдается значительная масса кала, потеря жидкости и электролитов. Для диареи воспалительного характера типичны частые дефекации с выделением малого объема каловых масс, лихорадка, кровь и лейкоциты в фекалиях, интоксикация, но не дегидратация (шигеллы, сальмонеллы, кампилобактер, иерсинии, энтерогеморрагическая кишечная палочка, E.histolitica, C.difficile). Если в первом случае при ректороманоскопии обычно не обнаруживается воспалительных изменений, то при инфекциях, вызванных инвазивными штаммами микроорганизмов, определяется выраженный отек, гиперемия слизистой оболочки, контактная кровоточивость, а в более поздние сроки и изъязвления.
Замещение жидкости и солей
Необходимость в возмещении жидкости и солей возникает в том случае, если масса фекалий превышает 500 мл в сутки. Одним из главных достижений в терапии диареи стало наблюдение, что сопряженное всасывание глюкозы и натрия в ворсинчатых клетках кишечника может не нарушаться даже тогда, когда имеет место повышенная секреция в криптах слизистой тонкой кишки. Следовательно, оральное применение глюкозо–солевых растворов может повысить всасывание, несмотря на продолжающуюся секрецию, и тем самым восстановить у больного положительный баланс воды, натрия и калия. Корригируя нарушенный водно–электролитный баланс, эти растворы не уменьшают объема стула и могут даже увеличить массу фекалий. Больной об этом должен быть предупрежден. Наилучшим образом для этой цели подходит состав, рекомендованный ВОЗ (табл. 1). Для этого может использоваться Регидрон, а при недоступности растворов промышленного производства рекомендуется раствор собственного приготовления (8 чайных ложек сахара, 1 чайная ложка поваренной соли, сок 2 апельсинов на 1 литр воды [9]. В настоящее время применяются различные модификации этой формулы, но растворы для оральной регидратации на основе рисового отвара представляются наиболее перспективными, т.к. гидролиз крахмала при многих формах диареи активно поддерживается ферментами щеточной каймы, а часть углеводов, поступающих в толстую кишку, может метаболизироваться в короткоцепочечные жирные кислоты [12]. Их всасывание стимулирует абсорбцию в толстой кишке воды и солей и обеспечивает дополнительное поступление энергии.

Антибиотики
Невоспалительная острая диарея не является показанием к назначению антибактериальных препаратов. Их следует применять при инфекциях, вызванных инвазивными микроорганизмами, когда в клинической картине заболевания имеется интоксикация, лихорадка, примесь крови в фекалиях. Антибиотики в этом случае назначают эмпирически еще до верификации патогенного агента при микробиологическом исследовании [10]. Такая тактика оправданна, т.к. процесс скоротечен, а причины острой бактериальной диареи удается установить лишь в 60% случаев [14]. Еще реже обнаруживаются лямблии и другие простейшие (менее 50%), для чего приходится многократно исследовать образцы [15]. Препаратами выбора признаны для бактериальной диареи – фторхинолоны (ципрофлоксацин, норфлоксацин) , при амебиазе – метронидазол, при гельминтозах – соответствующие антигельминтные препараты. В старой литературе высказывалось предположение, что антибиотикотерапия сальмонеллеза может служить причиной формирования носительства. Однако этого не установлено для Salmonella enteridis.
Опиаты
Опиаты применяли на протяжении нескольких столетий для терапии любых форм диареи, однако сегодня их используют в качестве средства симптоматического лечения хронической секреторной диареи [16]. Хотя опиаты и демонстрируют прямое стимулирующее действие на кишечную абсорбцию электролитов in vitro, наиболее вероятно, что решающим является антиперистальтический эффект, снижающий объем и частоту стула у больных с диареей [17]. Чаще других с этой целью используют дифеноксилат с атропином, кодеин и лоперамид. Последние чуть более эффективны. Лоперамид вызывает меньшее привыкание и седативный эффект в высоких дозах в сравнении с кодеином. Он также повышает давление в анальном сфинктере, что может быть полезным у больных с инконтиненцией [3]. Тем не менее применение опиатов у больных с острой инфекционной диареей нежелательно, поскольку это может удлинить сроки элиминации патогенных микроорганизмов, а следовательно, и продолжительность заболевания.
Адсорбирующие агенты
Продолжительность и тяжесть диареи уменьшаются под влиянием препаратов висмута и диосмектита. Соли висмута плохо всасываются. Присутствуя в просвете, висмут проявляет антибактериальную активность, что и объясняет его положительный эффект, например, при диарее путешественников [18,19]. Его применяют в виде субсалицилата висмута. Что касается диосмектита (Смекта), то он связывает вирусы, бактерии и бактериальные токсины, создавая предпосылки для уменьшения воспаления в слизистой оболочке кишечника [20]. Взаимодействуя с гликопротеинами, диосмектит повышает сопротивляемость барьера слизь–IgA и улучшает ее качество. Он успешно защищает слизистую оболочку от действия микроорганизмов и желчных солей [21]. Динамика частоты и объема стула свидетельствует, что Смекта столь же эффективна, как и лоперамид, в купировании этих симптомов [22], но безопасна при пролонгированном приеме, в том числе и у детей [23]. Имеются свидетельства, что диосмектит может быть полезен в контроле хронической диареи, связанной с ВИЧ–инфекцией [24], лучевым поражением [25], а также у больных, подвергшихся резекции части толстой кишки [26]. Сегодня Смекта применяется для лечения любого типа диареи в качестве стартовой терапии.
Plantago ovata (Psyllium)
Препараты из семян подорожника чаще используются в широкой клинической практике для лечения запоров, но благодаря выраженной водосвязывающей способности они могут быть полезны и при диарее [27]. Масса фекалий в этом случае не уменьшается, но уплотнение фекалий и устранение жидкой консистенции облегчает переносимость диареи. Это особенно важно при воспалительном ее варианте с частым стулом небольшого объема. За счет полноты опорожнения ампулы прямой кишки заметно снижаются ложные императивные позывы на дефекацию и частота стула [28]. Как и крахмал, входящие в состав Psyllium гемицеллюлозы расщепляются анаэробной кишечной микрофлорой до короткоцепочечных жирных кислот, что важно для лечения хронической диареи.
Saccharomyces boulardi
Во многих странах Европы и США широко применяются препараты лиофилизированных лактобацилл и E.coli, хотя их эффективность в лечении диареи не подтверждена контролируемыми клиническими испытаниями. В отличие от них Saccharomyces boulardi, как было показано, стимулирует абсорбцию натрия in vitro и даже в одном клиническом исследовании предотвращает антибиотико–ассоциированную диарею [29]. Тем не менее, препарат не признан в качестве противодиарейного средства, т.к. оказался не эффективным у больных с начинающейся острой диареей.
Затяжная диарея
Почему острый процесс, вызванный бактериальными токсинами или вирусами не разрешается в положенные сроки, до конца не ясно. Однако в ряде случае течение заболевания затягивается до 2–3 недель и более. Имеется ряд гипотез, объясняющих пролонгированное течение болезни. Длительное течение объясняют сниженной всасывательной функцией относительно незрелого кишечного эпителия [30], нарушением проницаемости вследствие снижения объема циркулирующей крови в брыжеечных артериях [31], дефицитом короткоцепочечных жирных кислот [4]. Во всех случаях затяжной диареи показана антибиотикотерапия. Причем у больных, у которых дважды выделены патогенные микроорганизмы и имеется пролонгированное течение диареи, следует определить чувствительность к антибиотикам. Терапия, таким образом, уже приобретает направленный характер.
Хроническая диарея
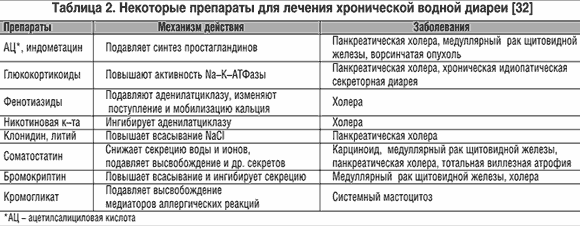
Под маской хронической диареи могут скрываться разнообразные заболевания – синдром раздраженного кишечника, неязвенная диспепсия, хологенная диарея, целиакия, язвенный колит, болезнь Крона, микроскопический колит и другие. Уточняющая диагностика становится обязательным элементом лечебной стратегии. Секреторная диарея является кардинальным симптомом многих эндокриннологических заболеваний. Она наблюдается при VIPоме, карциноиде, медуллярном раке щитовидной железы, сахарном диабете и др. [32]. Соматостатинома и тиреотоксикоз могут быть ассоциированы со стеатореей. Как правило, масса фекалий менее 1 л/сут, но при VIPоме она выше и достигает 3 л/сут. Каждый из указанных патологических процессов требует своего медикаментозного обеспечения. Для ведения хронической водной диареи применяются нестероидные противовоспалительные препараты, глюкокортикоиды, фенотиазиды, кромогликат, никотиновая кислота, клонидин, бромокриптин, соматостатин (табл. 2). Специального упоминания заслуживает соматостатин, т.к. аналоги этого пептида уже доступны для клинического применения [33]. Соматостатин способен специфически снижать высвобождение секрета из опухоли, таких как VIP при синдроме панкреатической холеры или серотонин при злокачественном карциноиде [34,35,36]. Он также оказывает неспецифическое действие на тонкую кишку, удлиняя время транзита и пролонгируя контакт между внутрипросветным содержимым и слизистой, подавляя в ней и секреторные процессы. Сегодня соматостатин успешно применяется при широком спектре диарейных состояний, таких как энтеропатия при СПИДе, илеостомии, диабетической диарее, при энтерокожных свищах.
1. Ивашкин В.Т., Шептулин А.А. Синдром диареи. Москва: Гэотар Медицина; 2000: 135 с.
2. Парфенов А.И. Энтерология. Москва:Триада–Х; 2002: 724 с.
3. Шептулин А.А. Современные возможности применения различных форм имодиума в лечении больных с острой диареей и синдромом раздраженного кишечника (функциональной диареей). Ж.Клинические перспективы гастроэнтерологии, гепатологии 2001; 3 : 26–30.
4. Binder Y.J. Speculations on the pathophysiology of functional diarrhoea. In: Goebell H., Holtmann G., Talley N. (eds); Functional dyspepsia and irritable bowel syndrome. Concepts and controversies. Dodrecht: Kluwer Academic Publishers; 1997: 233–235.
5. Blackstone M.O., Kirsner J.B. Clinical application of diagnostic tests in selected colonic disorders. In: Phillips S.F., Pemberton J.H., Shoster R.G. (eds); The large intestine: physiology, pathophysiology and disease; New York : Raven Press; 1991: 253–302.
6. Chang E.B., Rao M.C. Physiology of the gastrointestinal tract. New York: Leonard R. Johnson; 1994: 2027–2082.
7. Madara J.L., Stafford J. Interferon–gamma directly affects barrier function of cultured intestinal epithelial monolayers. J Clin Invest 1989; 83 (2): 724–727.
8. Barrett K.E. Bowditch lecture. Integrated regulation of intestinal epithelial transport: intercellular and intracellular pathways. Am J Physiol 1997; 272 (4 Pt 1): 1069–1076.
9. Krejs G.J. Secretory diarrhea. In: Bayless T.M. (ed.); Current therapy in Gastroenterology and Liver Disease. Philadelphia–Toronto: Decker Inc.; 1984: 255–259.
10. Секачева М.И. Современные подходы к лечению острой диареи. Ж. Лечащий врач 2001; 5–6 : 38–41.
11. DuPont H.L. Practice Parameters Committee of the American College of Gastroenterology. Guidelines on acute infectious diarrhoea in adults. Am J Gastroenterol 1997; 92: 1962–1975.
12. Ahmed H.S., Molla A.M. Rice–based oral rehydratation. J Diarrhoeal Dis Res 1987; 5 (1): 1–6.
13. Krejs G.J. Antidiarrhoeal therapy. In: Domschke W., Stoll R., Brasitus T.A., Kagnoff M.F. (eds); Intestinal mucosa and its diseases. Pathophysiology and clinics. Dodrecht : Kluver Academic Publishers; 1999: 77–82.
14. Jewkes J., Larson H.E., Price A.B. et al. Aetiology of acute diarrhoea in adults. Gut 1981; 22: 388–392.
15. Thompson R.B.Jr., Haas R.A. Intestinal parasites: the necessity of examining multiple stool specimens. Mayo Clin Proc 1984; 59: 641–642.
16. American Gastroenterological Association medical position statement: guidlines for the evaluation and management of chronic diarrhea. Gastroenterology 1999; 116: 1461–1464.
17. Read N.W., Krejs G.J., Read M.G. et al. Chronic diarrhea of unknown origin. Gastroenterology 1980; 78: 264–271.
18. Johnson P.C., Ericsson C.D., Du Pont H.L. Comparison of loperamide with bismuth subsalicylate for the treatment of acute traveler’s diarrhea. JAMA 1986; 255: 757–760.
19. Du Pont H.L., Ericsson C.D. Prevention and treatment of traveler’s diarrhea. N Engl J Med 1993; 328: 1821–1827.
20. Milocco C., Bolis A., Rizzo V. Evaluation of diosmectite in acute doarrhea in children. Pediatr Med Chir 1999; 21: 129–133.
21. De Sola Pool N., Loehle K., Radzik A.J., Kinsley J. Comparing of sistemic and unsistemic effects antidiarrheal drugs in the treatment of acute unspecific diarrhea in adults. Today’s therapeutic Trends 1987; 5 (2): 31–38.
22. Drov M.T., Drouet Y., Geraud G., Schatz B. La filance: nouvelle approche de l’agression intestinale et de sa therapeutique. Gastroenterol Clin Biol, 1985, 19, 119–121.
23. Vivatvakin B., Jongpipatvanish S., Haricul S. et al. Control study of oral regidratation solution (ORS) / ORS + dioctahedral smectite in hospitalized thai infants with acute secretory diarrhea. South asean J trop med public health, 1992, 23, 3, 414–419.
24. Mastroianni A., Cancellieri C., Coronado O. et al. Diosmectite for the treatment of chronic idiopathic diarrhea in patients with HIV disease. J Antimicrob Chemother, 1999, 44, Suppl A, 116–117.
25. Hombrink J., Voss A.C., Frohlich D. et al. Therapy trends in the prevention of radiation induced diarrhea after pelvic and abdominal irradiation. Results of a tricenter study. Strahlenther Oncol, 1995, 174, 1, 49–53.
26. Lukes M. Our experience with administration of Smektit (hydrated magnesium aluminium silicate) in the treatment of diarrhoea with a non–infectious etiology and of diarrhoea after resections of the large bowel on account of colorectal carcinoma pour cancer colorectal. Rozhl Chir, 1999, 188–190.
27. Румянцев В.Г. Препараты Plantago в регуляции деятельности пищеварительного тракта. Ж.Клин.мед. 1997; 11: 19–23.
28. Румянцев В.Г., Киркин Б.В., Калинская Т.Ю. и др. Мукофальк – новый препарат для нормализации моторики толстой кишки. Матер.конференции «Новое в гастроэнтерологии»; М. 1996: 82–84.
29. Surawicz C.M., Elmer G.W., Speelman P. et al. Prevention of antibiotic–associated diarrhea by Saccharomyces boulardii: A prospective study. Gastroenterology 1989; 96: 981–988.
30. Cantey J.R. Infectious diarrhea: pathogenesis and risk factors. Am J Med 1985; 27 (Suppl 6 B): 65–75.
31. Socinski M.A., Francal J.P., Vorrow P.L. et al. Painless diarrhea secondary to intestinal ishemia. Diagnosis of atheromatous emboli by jejunal biopsy. Dig Dis Sci 1984; 29: 674–677.
32. Schiller L.R. Review article: anti–diarrheal pharmacology and therapeutics. Aliment Pharmacol Ther 1995; 9: 87–106.
33. Белоусова Е.А., Румянцев В.Г., Мишуровская Т.С. и др. Новые возможности применения сандостатина (октреотида) в гастроэнтерологии. Ж.Клин фармакология и терапия 2000; 1: 36–39.
34. Krejs G.J. VIPoma syndrome. Am J Med 1987; 82 (Suppl 5 B): 37–48.
35. Davis G.R., Camp R.C., Raskin P., Krejs G.J. Effect of sandostatin infusion on jejunal water and electrolyte transport in a patient with secretory diarrhea due to malignant carcinosis syndrome. Gastroenterology 1980; 78: 346–349.
36. Degen L., Beglinger C. The role of octreotide in the treatment of gastroenteropancreatic endocrine tumors. Digestion 1999; 60 (Suppl 2): 9–14.
37. Holzer–Petsche U., Petritsch W., Hinterleitner T. et al. Effect of neuropeptide Y on jejunal water and ion transport in man. Gastroenterology 1991; 101: 325–330.
38. Hinterleitner T.A., Petritsch W., Dimsity G. et al. Acetorphan prevents cholera toxin–induced water and electrolyte secretion in the human jejunum. Eur J Gastroenterol 1997; 9: 887–891.








.gif)



