Анализ заболеваемости НАЖДП свидетельствует о значительной распространенности НАДЖП и НАСГ. При СД 2–го типа гепатостеатоз и стеатогепатит выявлены у 34–75% обследованных. Среди пациентов с ожирением эта патология определена в 39–100% [2].
Распространенность АЖДП и АСГ зависит от количества употребляемого алкоголя. Вопрос о роли алкоголя в генезе ЖДП и стеатогепатита является основополагающим
Также как при ЖДП алкогольного генеза, при неалкогольной жировой дистрофии печени (НАЖДП) четко прослеживается патологическая негативная динамика: НАЖДП переходит в НАСГ, потом в фиброз, а затем в цирроз печени. Такая негативная эволюция позволяет высказать предположение, что в происхождении криптогенных циррозов печени участвует НАСГ.
НАСГ заметно уступает по распространенности алкогольному стеатогепатиту (АСГ), соотношение составляет НАСГ/АСГ = 1/10–15. При гистологических исследованиях доля НАСГ 7–9% [10–12], в настоящее время НАСГ и АСГ анализируются в литературе раздельно, но общая морфологическая картина позволяет предполагать наличие общих патогенетических звеньев и, естественно, общих лечебных подходов. Патогенез ЖДП включает механизмы:
• увеличение поступления СЖК в печень;
• повышение синтеза СЖК в митохондриях гепатоцитов;
• снижение активности βокисления СЖК в митахондриях гепатоцитов;
• замедление элиминации триглицеридов из печени.
При различных этиологических факторах отмечаются особенности развития ЖДП и стеатогепатита. Ведущим фактором в развитии АЖДП является высокая концентрация ацетальдегида – токсического деривата алкоголя, продуцирующегося при воздействии алкогольдегидрогеназы (АДГ). Механизм можно представить следующим образом.
В развитии некроза гепатоцита и последующих явлений воспалений и фиброза участвует стеатонекроз, когда жировые включения фатально нарушают метаболизм клетки, явлении «эффект ацетальдегида», заключающийся в запуске перекисного окисления липидов (ПОЛ). Активация ПОЛ приводит к увеличению потребности в кислороде, гипоксии в центролобулярной зоне и дальнейшему некрозу гепатоцитов. Ацетальдегид также связывается с фосфолипидами, разрушает клеточную мембрану, сенсибилизирует Т–клетки, увеличивая продукцию провоспалительных цитокинов, повреждает микротрубочки цитоскелета и нарушает репаративные процессы в ядре гепатоцита.
В этой схеме остается неясным вопрос «толчка». Что запускает «оксидантный стресс» ПОЛ? Логично предположить, что при ХАИ возможно это резкое увеличение в печени ацетальдегида – интенсивный алкогольный эксцесс [5].
Этиологические (предрасполагающие) факторы НАЖДП и НАСГ разнообразны. Ведущими, т.е. приводящими, в большинстве случаев к НАСГ, являются:
• ожирение, особенно абдоминальное;
• СД 2–го типа;
• гиперлипидемия всех типов.
НАЖДП очень часто сопровождает метаболический синдром (МС), при этом НАЖДП в критерии МС не входит. Инсулинорезистентность является решающим звеном МС; заметна роль инсулинорезистентности и в генезе НАЖДП [13–15].
Ряд авторов вышеперечисленные этиологически обусловленные варианты НАЖДП и НАСГ определяет, как первичные. Накопление жира в печени – в гепатоцитах и клетках ИТО – происходит при сочетании следующих факторов:
• повышение поступления СЖК;
• снижение β–окисления СЖК;
• повышенное образование жирных килот;
• снижение удаления триглицеридов.
Больные ожирением СД 2–го типа и МС демонстрируют высокое содержание триглицеридов (ТГ), липопротеинов и СЖК в крови и в печени. Накопление СЖК в печени способствует высокому уровню инсулина в крови, гиперинсулинизм, сопровождающий ожирение, СД 2–го типа и МС, является патогенетическим фактором, поскольку инсулин стимулирует синтез СЖК, ТГ, а также снижает β–окисление СЖК и эвакуацию липидов из печени.
Предполагается, что «первым толчком» НАСГ является накопление СЖ в гепатоците. СЖК являются высокореактивным субстратом перекисного окисления липидов (ПОЛ). Процесс ПОЛ с образованием активных радикалов приводит к повреждению митохондрий и клеточных мембран.
Клинический опыт свидетельствует, что список состояний (этиологических факторов), при которых возникают НАЖДП и НАСГ, весьма широк и включает также:
• лекарственные препараты;
• синдром нарушенного всасывания;
• интенсивное снижение массы тела;
• длительное, несбалансированное парентеральное питание;
• болезнь Вильсона – Коновалова.
Выделены лекарства, прием которых весьма часто сопровождается развитием НАСГ, в первую очередь, амодарон, глюкокортикостероиды, тетрациклин, НПВП, метотрексат, синтетические эстрогены, тамоксифен.
Особое внимание заслуживает синдром нарушенного всасывания, приводящий к НАСГ. Обсуждаются следующие причины синдрома нарушенного всасывания, способствующие возникновению НАСГ:
• внешнесекреторная недостаточность поджелудочной железы;
• болезнь Крона;
• обширная резекция тонкой кишки;
• синдром избыточного бактериального роста тонкой кишки;
• операции по поводу ожирения (гастропластика, илеоеюнальный анастамоз).
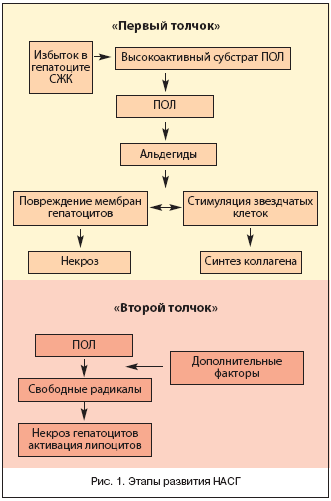
В настоящее время рассматриваются два этапа (два «толчка») развития НАСГ (рис. 1).
Возникло понимание, что только избыточное накопление в печени СЖК является необходимым, но недостаточным для возникновения «оксидантного стресса» ПОЛ. Сформулировалось представление о «втором толчке», приводящем к НАСГ.
Индукторами, дополнительными факторами «второго толчка» рассматривают воздействие лекарств, дефицит в пище антиоксидантов, гормональный дисбаланс гастроитестинальных гормонов, гипоксию. Так, тетрациклин снижает скорость β–окисления СЖК, амиодарон угнетает процесс β–окисления и способствует образованию активных кислородных радикалов, а также подавляет лизосомальный метаболизм липидов. Эстрогены снижают β–окисление, влияя на функцию и структуру митохондрий.
Патология пищеварения, представленная в перечне причин НАСГ, сопровождается снижением поступления в печень метионина, холина, участвующих в метаболизме липидов, а также снижением уровня антиоксидантов.
Критериями диагноза НАСГ являются:
• данные пункционной биопсии: ЖДП + воспалительные изменения, сходные с алкогольным гепатитом;
• отсутствие употребления алкоголя в гепатотоксичных дозах;
• отсутствие другой патологии печени (HCV, АИГ).
Идентификация НАСГ основана на определении негепатотоксичной дозы. Идеальным было бы включить в критерии НАСГ позицию «исключение употребления алкоголя». Но это невозможно. Известно, что в России высокий уровень среднедушевого потребления алкоголя (18 л в год на человека) сочетается с широкой распространенностью употребления. Алкоголизация населения в РФ – тяжелая медицинская проблема.
Среди госпитализированных в возрасте 20–59 лет ХАИ выявлена в 27,0–46,6%. Среди пациентов, госпитализированных по поводу патологии печени и заболевания желудочно–кишечного тракта, количество лиц с ХАИ значительно выше [16].
Для объективизации факта алкоголизации и оценки влияния употребления алкоголя целесообразно на этапе сбора данных анамнеза задать вопросы, входящие в опросник CAGE:
• «У Вас когда–нибудь возникало чувство, что Вы должны постараться уменьшить потребление алкоголя или наркотиков?»
• «У Вас когда–нибудь люди вызывали раздражение своими упреками в отношении Вашего употребления алкоголя или наркотиков?»
• «Испытывали ли Вы когда–нибудь чувство вины по поводу своего употребления алкоголя или наркотиков?»
• «Вы когда–нибудь утром опохмелялись / употребляли наркотики, чтобы успокоить свои нервы, или избавиться от плохого самочувствия, или чтобы обрести способность что–нибудь делать?»
Учитывая, что больные, употребляющие даже умеренное количество алкоголя, склонны уменьшать в диалоге с врачом количество выпитого, целесообразно получить сведения от родственников.
Возможность соблюдения режима отказа от алкоголя прямо связана с наличием или отсутствием алкогольной зависимости. Заподозрить возникновение алкогольной зависимости помогают следующие положения:
• доза оказывается больше планируемой;
• постоянное желание выпить;
• безуспешность осуществления отказа от приема алкоголя;
– употребление в неподходящих ситуациях;
– продолжение употребления несмотря на то, что пациент знает о негативных последствиях;
• дефекты социальной и профессиональной деятельности;
• изменение толерантности;
• похмельный синдром.
Определив, даже с некоторой неточностью, дозу употребляемого алкоголя, следует решить важный вопрос о токсичности данного количества для конкретного индивидуума. Известно, что токсичность алкоголя зависит от пола (для женщин порог токсичности ниже), возраста и массы тела. Известно, что лица, принадлежащие к азиатской расе, вследствие особенностей алкогольдегидрогеназы более чувствительны (поражаемы) к этанолу.
Из клинических признаков ХАИ следует обратить внимание на:
• расширение сосудов носа, инъецированность склер;
• увеличение околоушных желез;
• геникомастию;
• контрактуру Дюпюитрена.
Объективным методом документирования ХАИ служат результаты лабораторных исследований:
• повышение активности в крови Г–ГТ;
• повышение содержания в крови IgA;
• увеличение среднего объема эритроцитов;
• повышение в крови активности АСТ, превышающее АЛТ;
• повышение содержания в крови трансферрина.
Чаще всего оказывается, что ЖДП имеет смешанный генез с преобладанием алкогольных или неалкогольных факторов.
Пациенты с АЖДП и НАЖДП обычно жалоб, обусловленных патологией печени, не предъявляют. В поле зрения врача эти пациенты попадают при выявлении гепатомегалии.
Боли могут иметь как минимум две причины. Одни имеют характер тяжести в правом подреберье и возникают при увеличении органа, растяжении капсулы, эти боли не связаны с приемом пищи, могут усиливаться при физической нагрузке.
Чаще к врачу–терапевту на УЗИ приводят боли в правом подреберье, возникающие при употреблении жиров и жареной пищи. Больные обследуются по поводу ХБХ, ЖКБ, ХБП.
Гепатомегалия может быть выявлена в следующих ситуациях:
• нацеленное выявление:
– при жалобах и анамнезе, позволяющих предположить патологию печени;
– при «патологических» биохимических и вирусологических исследованиях;
• ожидаемая – при болезнях, сопровождающихся гепатомегалией;
• случайная – при УЗИ, диспансерном осмотре и физическом исследовании при заболеваниях, не сопровождающихся гепатомегалией
При НАДЖП и АЖДП пациенты чаще предъявляют жалобы, обусловленные сопутствующей патологией. Сами НАЖДП и АЖДП не имеют специфических клинических признаков. Жалобы могут следствием других причин.
Следует отметить, что в группах больных НАСГ и АСГ имеется различие в излагаемых жалобах и клинических данных. Пациенты с АСГ реже испытывают боли в правом подреберье (или меньше жалуются на них). Известно, что больные с алкоголь–ассоциированной патологией отличаются такой особенностью: эффект обезболивающего, антидепрессивного, эйфорирующего действия алкоголя и висцеральной полинейропатии [17]. Астенические жалобы встречаются чаще у лиц с АСГ. Гепатомегалия в других группах определяется в 80–86%. Спленомегалия несколько чаще встречается при НАСГ – в 22%. Малые внепеченочные знаки в 2 раза чаще встречаются при АСГ.
При АЖДП могут быть жалобы, входящие в «синдром выходного дня», когда в понедельник (после употребления алкоголя в пятницу и субботу) имеет место астенический синдром и синдромы желудочной и кишечной диспепсии.
При НАЖДП пациенты предъявляют жалобы, обусловленные чаще всего дискинезией желчного пузыря, и жалобы, характерные для функциональной желудочной диспепсии по варианту либо синдрома эпигастральной боли, либо постпрандиального дистрес–синдрома.
При АСГ чаще наблюдали симптомы кишечной диспепсии. При НАСГ чаще отмечали признаки «вовлечения» желчного пузыря. При лечении НАЖДП и НАСГ важно учесть факторы, рассматриваемые у данного пациента как этиологические.
Особое внимание требуют лекарственные препараты, длительность приема, характер питания, перенесенные операции.
Физическое обследование начинается с поиска «малых» внепеченочных знаков и стигматов ХАИ. Определение индекса массы тела, объема талии, объема бедра обязательны, что позволяет определить степень и форму ожирения.
При АСГ печень умеренно плотная, пальпация ее края вызывает легкую болезненность. При АЖДП воздержание от алкоголя приводит к нормализации размеров. Результаты лабораторных исследований позволяют определить активность печеночного цитолитического синдрома, биохимических показателей холестаза, исключить вирусную этиологию гепатопатии и провести скрининг других факторов. Лабораторные показатели при НАСГ зависят от выраженности печеночного цитолиза. Обязательным является ультразвуковое исследование (УЗИ). В настоящее время УЗИ помимо размеров, структуры, характера паренхимы, с применением специальной аппаратуры позволяет определить степень жировой инфильтрации и фиброза. Пункционная биопсия позволяет выявить этиологию, определить степень активности (воспаление), определить стадии прогрессирования (фиброз), провести верификацию цирроза, оценить эффективность лечения. Активность АСТ и АЛТ обычно превышает норму в 2–3 раза. Активность АСТ превышает активность АЛТ у 30–40% больных. Гипербилирубинемия наблюдается у 15–20%.
Лабораторные показатели печени при АСГ зависят от времени, прошедшего с момента употребления алкоголя, но четко уровень ГГТ при АСГ заметно выше, чем при НАСГ.
Течение и прогноз НАСГ и АСГ во многом определяет наличие факторов прогрессирования:
– высокая степень ожирения;
– гипертриглицеридемия;
– декомпенсация СД;
– повышение активности печеночных ферментов крови;
– пожилой возраст.
Отмечено, что за 10 лет прогрессирование НАСГ с развитием фиброза и цирроза печени происходит у 10% больных.
Прогрессирование АСГ зависит от длительности ХАИ, дозы употребляемого алкоголя, типа употребления, характера питания. Главная задача – отказ от употребления алкоголя.
Больные прекращают употреблять алкоголь: при невысокой толерантности, при отсутствии или слабой выраженности алкоголь–ассоциируемых синдромов, при высоком социальном статусе, при наличии тревожно–мнительных черт характера.
Прогноз при АСГ значительно хуже, так при НАСГ 10–летняя выживаемость 59%, а при АСГ – 15%.
Лечение АСГ и НАСГ имеет много общего. Поскольку ожирение и инсулинорезистентность – главные факторы развития НАЖДП и НАСГ основной задачей немедикаментозной терапии является уменьшение калорий в диете за счет главным образом жиров и углеводов, увеличение физической нагрузки. Снижение массы тела идивидуализированно. Общими принципами – снижение массы тела медленное (1,5–2 кг в месяц), резко ограничивают прием простых углеводов, насыщенных жиров [18].
Диета должна включать достаточное количество пищевых растительных волокон (30–40 г/сут.), целесообразно использовать пшеничные отруби, семя льна.
Для достижения снижения веса применяют ингибиторы панкреатической и желудочной липазы, средства, повышающие чувство насыщения, увеличивающие чувствительность к инсулину.
С большой осторожностью следует относиться к назначению препаратов, направленных на устранение гипертриглицеридемии и дислипидемии. Важным является использование препаратов с гепатопротективным и антиоксидантным эффектом.
Медикаментозная терапия НАСГ:
– эссенциальные фосфолипиды:
– α–липоевая кислота;
– адеметионин;
– флаваноиды;
– усодезоксихолиевая кислота;
– витамин Е;
– витамин С.
Можно говорить о традиционно назначаемых препаратах, прием которых сопровождается улучшением клинической картины и улучшением биохимических показателей – эссенциальные фосфолипиды (ЭФЛ). К ним относится Эссенциале® форте Н.
Механизм действия Эссенциале® форте Н:
– восстановление целостности мембраны гепатоцитов;
– активация мембранных ферментов;
– повышение текучести мембраны;
– снижение повреждающего эффекта при ПОЛ;
– увеличение синтеза эндогенных фосфолипидов;
– уменьшение трансформации клеток Ито в миофибринобластоподобных клетках;
– уменьшение синтеза провоспалительных цитокинов;
– обратное развитие ЖДП;
– торможение окисления ЛПНП.
Известно, что соблюдают рекомендации отказа от алкоголя не более 1/3 пациентов. Лечение алкогольной болезни печени включает следующее: отказ от алкоголя, увеличение белка в диете (1,0–1,5 г/кг), увеличение ненасыщенных жирных кислот, применение эссенциальных фосфолипидов, применение средств растительного происхождения, содержащих флавоноиды, препаратов урсодезоксихолиевой кислоты, адеметионин, колхицин.
При АСГ и НАСГ существуют общие факторы, влияющие на стеатоз печени. Это прежде всего несбалансированный рацион питания.
Около трети лиц, злоупотребляющих алкоголем, имеют избыток массы тела, что в первую очередь обусловлено повышением аппетита при стимуляции кислотопродукции алкоголем, снижением контроля за рационом и высокоэнергетической ценности алкоголя (1 г этанола = 7 ккал). Другая категория, входящая в группу «голодного пьянства», имеет дефицит массы тела и рацион без белка и витаминов.
В России широкое применение нашли лекарственные средства на основе эссенциальных фосфолипидов (Эссенциале® форте Н), эффективность которых доказана многолетним положительным опытом их применения. Механизм их действия многогранен и складывается из нескольких основных компонентов [19,20].
• Мембранопротективное действие: поддержание нормальной текучести и репарации мембран гепатоцитов за счет восстановления их фосфолипидного состава путем встраивания экзогенных молекул фофолипидов в поврежденные клеточные мембраны.
• Антиоксидантный эффект: уменьшение окислительного стресса за счет предотвращения окисления липидов в гепатоцитах.
• Подавление процессов воспаления и фиброзообразования в паренхиме печени посредством уменьшения синтеза провоспалительных цитокинов (ФНО–α и ИЛ–1β).
• Защита митохондриальных и миросомальных ферментов от повреждения.
• Усиление детоксикационного, экскреторного и обменного потенциала гепатоцитов.
• Антифибротический эффект: препятствие развитию фиброза и ускорение его обратного развития за счет замедления синтеза и коллагена, повышения активности коллагеназы, а также подавления трансформации звездчатых клеток печени в продуцирующие коллаген миофибробласты.
Таким образом, наличие этиологических компонентов общих этиологических факторов, схожие звенья патогенеза позволяют в терапии АСГ и НАСГ использовать патогенетически эффективные средства, содержащие эссенциальные фосфолипиды, такие как «Эссенциале® форте Н». Рекомендуемый курс состоит из введения 5–10 мл (1–2 ампулы) внутривенно в течение 10–15 дней с последующим приемом по 2 капсулы 3 раза/сут. в течение 2 мес. Препарат хорошо переносится и эффективно влияет на основные звенья патогенеза. Эффективен при АСГ и НАСГ. Целесообразно проведение 2–3 курсов в год.
![Таблица 1. Оценка гепатотоксичности количества ежедневного потребления алкоголя взрослым мужским населением [6]](/data/articles/Image/t19/n5/282-1.gif)
Литература
1. Подымова С.Д. Болезни печени. М.: Медицина, 2005. 768 с.
2. Герок В., Блюм Х.Е. Заболевания печени и желчевыделительной системы. М.: «МЕДпресс–информ», 2009. 199 с.
3. Майер К.П Гепатит и последствия гепатита. М.: Издательский дом «Гэотар–Мед», 2004. С. 479–489.
4. Рациональная фармакотерапия заболеваний органов пищеварения / Под ред. В.Т. Ивашкина, Т.Л. Лапиной. М.: «Литтера», 2003. С. 407–422.
5. Подымова С.Д. Патогенетическая роль эссенциальных фосфолипидов в терапии алкогольной болезни печени // Consilium medicum: Экстра выпуск. 2001. С. 3–5.
6. Хазанов А.И. Важная проблема современности — алкогольная болезнь печени // Рос. журн. гастроэнтерологии и гепатологии. 2003. 2. С. 13–20.
7. Павлов Ч., Золотаревский В.Б, Ивашкин В.Т. Структура хронических заболеваний печени по данным биопсии и морфологические исследования ее ткани // Российский журнал гастроэнтерологии, гепатологии, колопрактологии. 2007. 1. С. 90–95.
8. Angulo P., Deach J.C., Batts K.P., et al. Independent predictors of liver fibrosis in patients with nonalcoholic steatohepatitis. Hepatology. 1999. 30. 1356–62.
9. Bacon B., Faravash M.J., Janney C.G., et al. Nonalcoholic steatohepatitis; An expandedclinical entiny // Gastroenterology. 1994. 107. С. 1103–1106.
10. Ивашкин В.Т., Шульпекова Ю.О. Неалкогольный стеатогепатит // Болезни органов пищеварения. 2000. № 2. С. 41–45. С. 13.
11. Ferenci P. Clinical spectrum of alcoholic hepatitis. In: Leuschner U, James OFW, Dancygier H (eds). Steatohepatitis (NASH and ASH). Dordrecht: Kluwer Academ Publ 2001.
12. Sanyal AJ (ed). Nonalcoholic fatty liver disease. Clinics in Liver Disease 2004. Vol. 8, Nr. 3.
13. Маколкин В.И. Метаболический синдром. М.: МИА, 2010. С. 142.
14. Larter CZ, Farrell GC. Insulin resistance, adiponectin, cytokines in NASH: Which is the best target to treat. J. Hepatol. 2006. 44. 253–261.
15. Neuschwander–tetri BA, Caldwell SH. Nonalcoholic steatohepatitis: Summary of an AASLD singletopic conference. Hepatology. 2003. 37. 1202–1219.
16. Гундерманн К. Новейшие данные о механизмах действия и клинической эффективности эссенциальных фосфолипидов // Клин. перспективы гастроэнтерологии, гепатологии. 2002. 2. С. 28–31.
17. Махов В.М. Диагностика и лечение алкоголь–зависимой патологии органов пищеварения. М., 2005. 24 с.
18. Минушкин О.Н. Опыт терапии заболеваний печени эссенциальными фосфолипидами / Consilium–medicum: Экстра–выпуск. М., 2001. С. 9–11.
19. Калинин А.В. Эссенциале форте Н – опыт применения препарата при алкогольной болезни печени // Consilium–medicum: Экстра–выпуск. М., 2001. С. 6–8.
20. Буеверов А.О. Место гепатопротекторов в лечении заболевании печени // Болезни органов пищеварения. 2001. № 1. С. 16–18.
RU.PCH.11.03.01












