–≠—В–Є–Њ–ї–Њ–≥–Є—П –Є –њ–∞—В–Њ–≥–µ–љ–µ–Ј
–У–ї—О—В–µ–љ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–∞—П —Ж–µ–ї–Є–∞–Ї–Є—П (–У–¶) – –Њ–і–љ–∞ –Є–Ј –љ–µ–Љ–љ–Њ–≥–Є—Е –љ–µ–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –±–Њ–ї–µ–Ј–љ–µ–є, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–є –Є–Ј–≤–µ—Б—В–µ–љ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —Д–∞–Ї—В–Њ—А – –±–µ–ї–Њ–Ї –≥–ї—О—В–µ–љ. –£–і–∞–ї–µ–љ–Є–µ —Н—В–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ –Є–Ј —А–∞—Ж–Є–Њ–љ–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞—В—М —Н—Д—Д–µ–Ї—В —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П – –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –Є –≤—Л–Ј–і–Њ—А–Њ–≤–ї–µ–љ–Є–µ. –Я–Њ—Б–ї–µ–і—Г—О—Й–µ–µ –≤–≤–µ–і–µ–љ–Є–µ –≥–ї—О—В–µ–љ–∞ –≤ —В–µ—З–µ–љ–Є–µ –і–∞–ї—М–љ–µ–є—И–µ–є –ґ–Є–Ј–љ–Є –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В —А–∞–Ј–≤–Є—В–Є–µ —А–µ—Ж–Є–і–Є–≤–∞ –±–Њ–ї–µ–Ј–љ–Є.
–Ь–µ—Е–∞–љ–Є–Ј–Љ —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –≥–ї—О—В–µ–љ–∞ –љ–∞ —Б–ї–Є–Ј–Є—Б—В—Г—О –Њ–±–Њ–ї–Њ—З–Ї—Г —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –ї—О–і–µ–є, –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л—Е –Ї –У–¶, –і–Њ —Б–Є—Е –њ–Њ—А –њ—А–Њ–і–Њ–ї–ґ–∞–µ—В –Є–Ј—Г—З–∞—В—М—Б—П. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ї–∞—Б–∞—О—В—Б—П —Б–∞–Љ–Њ–≥–Њ –≥–ї—О—В–µ–љ–∞, –Њ—В–≤–µ—В–∞ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –љ–∞ –µ–≥–Њ –≤–≤–µ–і–µ–љ–Є–µ –Є –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є –±–Њ–ї—М–љ—Л—Е —Ж–µ–ї–Є–∞–Ї–Є–µ–є.
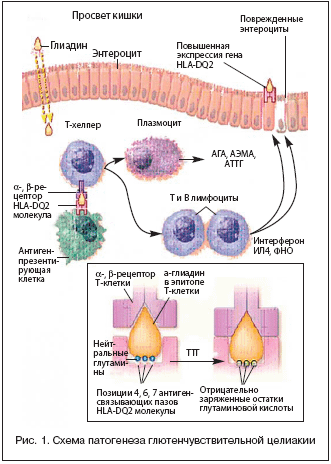
–У–µ–љ—Л –У–¶ —В–µ—Б–љ–Њ —Б–≤—П–Ј–∞–љ—Л —Б –ї–Њ–Ї—Г—Б–Њ–Љ DQ HLA –Ї–ї–∞—Б—Б–∞ II –Є –µ–≥–Њ –≥–µ—В–µ—А–Њ–і–Є–Љ–µ—А–∞–Љ–Є HLA–DQ2 –Є–ї–Є HLA–DQ8. –У–µ—В–µ—А–Њ–і–Є–Љ–µ—А DQ2, –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л–є –Ј–∞ –≤–Њ—Б–њ—А–Є–Є–Љ—З–Є–≤–Њ—Б—В—М –Ї –У–¶, –њ—А–Є—Б—Г—В—Б—В–≤—Г–µ—В –њ—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ —Г 90–95% –±–Њ–ї—М–љ—Л—Е. –У–µ—В–µ—А–Њ–і–Є–Љ–µ—А DQ8, —Б–≤—П–Ј–∞–љ–љ—Л–є c –У–¶, –њ—А–Є—Б—Г—В—Б—В–≤—Г–µ—В —Г 5–10% –±–Њ–ї—М–љ—Л—Е. –£ –ї–Є—Ж, –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л—Е –Ї —Ж–µ–ї–Є–∞–Ї–Є–Є, —Б DQ2 –Є–ї–Є DQ8 —Б–≤—П–Ј—Л–≤–∞—О—В—Б—П «–±–µ–ї–Ї–Є –≥–ї—О—В–µ–љ–∞», —Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –≥–ї—Г—В–∞–Љ–Є–љ –Є –њ—А–Њ–ї–Є–љ, –Ї–Њ—В–Њ—А—Л–µ –Њ–±—А–∞–Ј—Г—О—В—Б—П –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –≥–Є–і—А–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–≥–Њ —А–∞—Б—Й–µ–њ–ї–µ–љ–Є—П –≥–ї–Є–∞–і–Є–љ–∞ –≤ –њ—А–Њ—Б–≤–µ—В–µ –Ї–Є—И–Ї–Є [1]. –Ъ–Њ–Љ–њ–ї–µ–Ї—Б «DQ––њ–µ–њ—В–Є–і –≥–ї–Є–∞–і–Є–љ–∞» —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –∞–Ї—В–Є–≤–Є–Ј–Є—А—Г–µ—В T––Ї–ї–µ—В–Ї–Є –≤ —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ–є –њ–ї–∞—Б—В–Є–љ–Ї–µ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –Ї–Є—И–Ї–Є. –°—Е–µ–Љ–∞ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –У–¶ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –љ–∞ —А–Є—Б—Г–љ–Ї–µ 1.
–Ь–Њ–ґ–љ–Њ –њ—А–µ–і—Б—В–∞–≤–Є—В—М –њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ –і–≤–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –≤–∞—А–Є–∞–љ—В–∞ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є—В–µ–ї –≤ —Н–Ї—Б—В—А–∞—Ж–µ–ї–ї—О–ї—П—А–љ–Њ–Љ –Љ–∞—В—А–Є–Ї—Б–µ —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ–є –њ–ї–∞—Б—В–Є–љ–Ї–Є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є. –Я–µ—А–≤—Л–є –њ—Г—В—М –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П —З–µ—А–µ–Ј –Љ–∞–Ї—А–Њ—Д–∞–≥–Є, –Ї–Њ—В–Њ—А—Л–µ –Ј–∞—Е–≤–∞—В—Л–≤–∞—О—В –≥–ї–Є–∞–і–Є–љ –Є –њ–µ—А–µ–і–∞—О—В –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—О –Ґ– –Є –Т––ї–Є–Љ—Д–Њ—Ж–Є—В–∞–Љ. –Ґ–—Е–µ–ї–њ–µ—А—Л –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ —Н–Ї—Б–њ—А–µ—Б—Б–Є—А—Г—О—В –∞–љ—В–Є–≥–µ–љ—Л –≥–Є—Б—В–Њ—Б–Њ–≤–Љ–µ—Б—В–Є–Љ–Њ—Б—В–Є –ЭL–Р DR, –Ї–Њ—В–Њ—А—Л–µ –∞–Ї—В–Є–≤–Є—А—Г—О—В —А–µ—Ж–µ–њ—В–Њ—А—Л –°D40L –љ–∞ –Т –ї–Є–Љ—Д–Њ—Ж–Є—В–∞—Е –Є –≤—Л–Ј—Л–≤–∞—О—В –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—О –Є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї—Г –њ–ї–∞–Ј–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Ї–ї–µ—В–Њ–Ї, –њ—А–Њ–і—Г—Ж–Є—А—Г—О—Й–Є—Е –∞–љ—В–Є—В–µ–ї–∞ –Ї –≥–ї–Є–∞–і–Є–љ—Г.
–Ф—А—Г–≥–Њ–є –њ—Г—В—М –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ –љ–∞ –≥–ї–Є–∞–і–Є–љ —Б–≤—П–Ј–∞–љ —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –≥–ї–Є–∞–і–Є–љ–∞ —Б —В–Ї–∞–љ–µ–≤–Њ–є —В—А–∞–љ—Б–≥–ї—Г—В–∞–Љ–Є–љ–∞–Ј–Њ–є (–Ґ–Ґ–У) – —Д–µ—А–Љ–µ–љ—В–Њ–Љ, –і–µ–Ј–∞–Љ–Є–љ–Є—А—Г—О—Й–Є–Љ –µ–≥–Њ. –Ъ–Њ–Љ–њ–ї–µ–Ї—Б –Њ–±–ї–∞–і–∞–µ—В —Б—А–Њ–і—Б—В–≤–Њ–Љ –Ї HLA DQ2 –Є–ї–Є HLA DQ8 –љ–∞ –Т––ї–Є–Љ—Д–Њ—Ж–Є—В–∞—Е –Є –∞–Ї—В–Є–≤–Є–Ј–Є—А—Г–µ—В –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—О –Є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї—Г –њ–ї–∞–Ј–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Ї–ї–µ—В–Њ–Ї, –Ї–Њ—В–Њ—А—Л–µ —Б–Є–љ—В–µ–Ј–Є—А—Г—О—В —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –∞–љ—В–Є—В–µ–ї–∞. –Т–љ–Њ–≤—М –Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л–є –Ї–Њ–Љ–њ–ї–µ–Ї—Б –≥–ї–Є–∞–і–Є–љ–∞ —Б –Ґ–Ґ–У –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –∞–љ—В–Є–≥–ї–Є–∞–і–Є–љ–Њ–≤—Л—Е –∞–љ—В–Є—В–µ–ї (–Р–У–Р), –∞–љ—В–Є—В–µ–ї –Ї –Ґ–Ґ–У (–Р–Ґ–Ґ–У) –Є —Н–љ–і–Њ–Љ–Є–Ј–Є–Є (–Р–≠–Р).
–Ф–µ–Ј–∞–Љ–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–є –≥–ї–Є–∞–і–Є–љ –∞–Ї—В–Є–≤–Є—А—Г–µ—В —Б–Є–љ—В–µ–Ј –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ –Ґ––ї–Є–Љ—Д–Њ—Ж–Є—В–∞–Љ–Є. –Ш–љ—В–µ—А—Д–µ—А–Њ–љ–g, –Ш–Ы–4 –Є –§–Э–Ю–a –њ–Њ–≤—А–µ–ґ–і–∞—О—В —Н–љ—В–µ—А–Њ—Ж–Є—В—Л.
–£–≤–µ–ї–Є—З–µ–љ–Є–µ —З–Є—Б–ї–∞ –Љ–µ–ґ—Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ (–Ь–≠–Ы) – –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–є –Њ—В–≤–µ—В –љ–∞ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ —Н–њ–Є—В–µ–ї–Є–Њ—Ж–Є—В–Њ–≤ – —П–≤–ї—П–µ—В—Б—П —Б–∞–Љ—Л–Љ —А–∞–љ–љ–Є–Љ –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ —Ж–µ–ї–Є–∞–Ї–Є–Є.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Д–Њ—А–Љ—Л
–Ґ–Є–њ–Є—З–љ–∞—П —Д–Њ—А–Љ–∞ –љ–∞—З–Є–љ–∞–µ—В—Б—П –≤ –і–µ—В—Б—В–≤–µ, –њ—А–Њ—В–µ–Ї–∞–µ—В —Б —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –љ–∞—А—Г—И–µ–љ–љ–Њ–≥–Њ –≤—Б–∞—Б—Л–≤–∞–љ–Є—П (–°–Э–Т) III —Б—В. —В—П–ґ–µ—Б—В–Є (–і–Є–∞—А–µ—П, –њ–Њ–ї–Є—Д–µ–Ї–∞–ї–Є—П, –Є—Б—В–Њ—Й–µ–љ–Є–µ, –Њ—В–µ–Ї–Є, –Њ—В—Б—В–∞–≤–∞–љ–Є–µ –≤ —А–∞–Ј–≤–Є—В–Є–Є –Є —В.–і.).
–Ы–∞—В–µ–љ—В–љ–∞—П —Д–Њ—А–Љ–∞ —Ж–µ–ї–Є–∞–Ї–Є–Є —Б –Љ–∞–ї–Њ—Б–Є–Љ–њ—В–Њ–Љ–љ—Л–Љ —В–µ—З–µ–љ–Є–µ–Љ. –Э–∞–±–ї—О–і–∞–µ—В—Б—П —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –≤–Ј—А–Њ—Б–ї—Л—Е, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –ґ–µ–љ—Й–Є–љ. –•–∞—А–∞–Ї—В–µ—А–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л: —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –і–Є–∞—А–µ—П, –Љ–∞–ї–µ–љ—М–Ї–Є–є —А–Њ—Б—В, –ґ–µ–ї–µ–Ј–Њ–і–µ—Д–Є—Ж–Є—В–љ–∞—П –∞–љ–µ–Љ–Є—П, –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј.
–Ь–µ–љ–µ–µ —Е–∞—А–∞–Ї—В–µ—А–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л: –±–µ—Б–њ–ї–Њ–і–Є–µ, –∞–Љ–µ–љ–Њ—А–µ—П, –≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Є–є —Б–Є–љ–і—А–Њ–Љ, –љ–µ–є—А–Њ–њ–∞—В–Є–Є –Є –і—А.
–С–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ—Л–µ —Д–Њ—А–Љ—Л —Ж–µ–ї–Є–∞–Ї–Є–Є. 1) –°–Ї—А—Л—В–∞—П —Ж–µ–ї–Є–∞–Ї–Є—П: —Б–Є–Љ–њ—В–Њ–Љ—Л –Љ–∞–ї–∞–±—Б–Њ—А–±—Ж–Є–Є –Њ—В—Б—Г—В—Б—В–≤—Г—О—В, –љ–Њ —Б–ї–Є–Ј–Є—Б—В–∞—П –Њ–±–Њ–ї–Њ—З–Ї–∞ —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є —Б —Е–∞—А–∞–Ї—В–µ—А–љ—Л–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –≥–Є–њ–µ—А—А–µ–≥–µ–љ–µ—А–∞—В–Њ—А–љ–Њ–є –∞—В—А–Њ—Д–Є–Є –Є/–Є–ї–Є —Г–≤–µ–ї–Є—З–µ–љ–љ—Л–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –Ь–≠–Ы.
2) –Я–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–∞—П —Ж–µ–ї–Є–∞–Ї–Є—П: —Б–ї–Є–Ј–Є—Б—В–∞—П –Њ–±–Њ–ї–Њ—З–Ї–∞ —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –љ–Њ—А–Љ–∞–ї—М–љ–∞—П, –љ–Њ —Г–≤–µ–ї–Є—З–µ–љ–Њ —З–Є—Б–ї–Њ g/l (gamma/delta) –Ь–≠–Ы, —Г–≤–µ–ї–Є—З–µ–љ–Њ —З–Є—Б–ї–Њ –Љ–Є—В–Њ–Ј–Њ–≤ –≤ –Ї–ї–µ—В–Ї–∞—Е –Ї—А–Є–њ—В, –≤—Л—П–≤–ї—П–µ—В—Б—П —Н–Ї—Б–њ—А–µ—Б—Б–Є—П HLA –Ї–ї–∞—Б—Б–∞ II. –≠—В—Г —Д–Њ—А–Љ—Г –Њ–±—Л—З–љ–Њ –∞–Ї—В–Є–≤–љ–Њ –≤—Л—П–≤–ї—П—О—В —Г –±–ї–Є–ґ–∞–є—И–Є—Е —А–Њ–і—Б—В–≤–µ–љ–љ–Є–Ї–Њ–≤ –±–Њ–ї—М–љ—Л—Е —Ж–µ–ї–Є–∞–Ї–Є–µ–є. –Я—А–Њ—П–≤–ї—П–µ—В—Б—П –≤–љ–µ–Ї–Є—И–µ—З–љ—Л–Љ–Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є, —Б–≤—П–Ј–∞–љ–љ—Л–Љ–Є —Б –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –≤—Б–∞—Б—Л–≤–∞–љ–Є—П –Є–ї–Є –Є–Љ–Љ—Г–љ–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є (–≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Є–є —Б–Є–љ–і—А–Њ–Љ, –Њ—Б—В–µ–Њ–Љ–∞–ї—П—Ж–Є—П, –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л–є —В–Є—А–µ–Њ–Є–і–Є—В, –≥–µ–њ–∞—В–Є—В –Є –і—А.).
–Ъ–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П
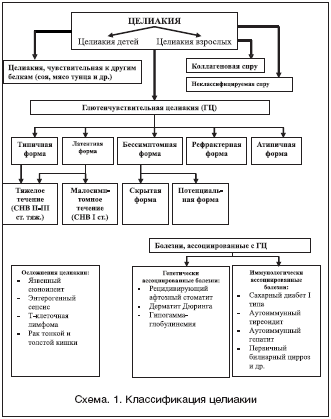
–Э–∞ —Б—Е–µ–Љ–µ 1 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П —Ж–µ–ї–Є–∞–Ї–Є–Є [2]. –Ь–љ–Њ–≥–Њ–ї–Є–Ї–Њ—Б—В—М –У–¶ –Њ–±—К—П—Б–љ—П–µ—В—Б—П —А–∞–Ј–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –±–Њ–ї—М–љ—Л—Е –Ї –≥–ї–Є–∞–і–Є–љ—Г, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М—О –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л—Е –Љ–∞–љ–Є—Д–µ—Б—В–∞—Ж–Є–є –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М—О –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є. –°—Г—Й–µ—Б—В–≤—Г—О—В —В—А–Є —Б—В–µ–њ–µ–љ–Є –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –≥–ї–Є–∞–і–Є–љ—Г: –≤—Л—А–∞–ґ–µ–љ–љ–∞—П, —Г–Љ–µ—А–µ–љ–љ–∞—П –Є —Б–ї–∞–±–∞—П.
–Т—Л—А–∞–ґ–µ–љ–љ–∞—П —Б—В–µ–њ–µ–љ—М –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –≥–ї–Є–∞–і–Є–љ—Г –њ—А–Њ—П–≤–ї—П–µ—В—Б—П —В–Є–њ–Є—З–љ–Њ–є —Д–Њ—А–Љ–Њ–є –У–¶. –Ф–ї—П –љ–µ–µ —Е–∞—А–∞–Ї—В–µ—А–љ—Л –∞) –≤—Л—А–∞–ґ–µ–љ–љ–∞—П –Є–Љ–Љ—Г–љ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П —А–µ–∞–Ї—Ж–Є—П –Ї–Є—И–Ї–Є –љ–∞ –≥–ї–Є–∞–і–Є–љ: –±) –≤—Л—Б–Њ–Ї–Є–µ —В–Є—В—А—Л –∞–љ—В–Є—В–µ–ї –Ї –≥–ї–Є–∞–і–Є–љ—Г, —Н–љ–і–Њ–Љ–Є–Ј–Є—О –Є —В–Ї–∞–љ–µ–≤–Њ–є —В—А–∞–љ—Б–≥–ї—Г—В–∞–Љ–Є–љ–∞–Ј–µ: –≤) –Ј–љ–∞—З–Є—В–µ–ї—М–љ–∞—П –њ—А–Њ—В—П–ґ–µ–љ–љ–Њ—Б—В—М –њ–Њ—А–∞–ґ–µ–љ–Є—П —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є: –≥) –°–Э–Т III —Б—В. —В—П–ґ–µ—Б—В–Є.
–£–Љ–µ—А–µ–љ–љ–∞—П —Б—В–µ–њ–µ–љ—М –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –≥–ї–Є–∞–і–Є–љ—Г –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –Љ–∞–ї–Њ—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є –У–¶. –Ф–ї—П –љ–µ–µ —Е–∞—А–∞–Ї—В–µ—А–љ—Л: –∞) —Б–ї–∞–±–∞—П –Є–Љ–Љ—Г–љ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П —А–µ–∞–Ї—Ж–Є—П –Ї–Є—И–Ї–Є –љ–∞ –≥–ї–Є–∞–і–Є–љ; –±) –њ–Њ–≤—Л—И–µ–љ–љ—Л–µ —В–Є—В—А—Л –∞–љ—В–Є—В–µ–ї –Ї —Н–љ–і–Њ–Љ–Є–Ј–Є—О –Є —В–Ї–∞–љ–µ–≤–Њ–є —В—А–∞–љ—Б–≥–ї—Г—В–∞–Љ–Є–љ–∞–Ј–µ; –≤) –Њ—В—Б—Г—В—Б—В–≤–Є–µ –∞—В—А–Њ—Д–Є–Є –≤–Њ—А—Б–Є–љ–Њ–Ї —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є; –≥) –≥–Є–њ–µ—А–њ–ї–∞–Ј–Є—П –Ї—А–Є–њ—В; –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Љ–µ–ґ—Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ (–Ь–≠–Ы); –і) –°–Э–Т I–II —Б—В. —В—П–ґ–µ—Б—В–Є
–Я—А–Є —Б–ї–∞–±–Њ–є —Б—В–µ–њ–µ–љ–Є –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –≥–ї–Є–∞–і–Є–љ—Г —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–∞—П –У–¶. –Ф–ї—П –љ–µ–µ —Б–≤–Њ–є—Б—В–≤–µ–љ–љ—Л: –∞) –љ–µ–≤—Л—Б–Њ–Ї–Є–є —В–Є—В—А –∞–љ—В–Є—В–µ–ї –Ї —Н–љ–і–Њ–Љ–Є–Ј–Є—О –Є —В–Ї–∞–љ–µ–≤–Њ–є —В—А–∞–љ—Б–≥–ї—Г—В–∞–Љ–Є–љ–∞–Ј–µ; –±) –Њ—В—Б—Г—В—Б—В–≤–Є–µ –∞—В—А–Њ—Д–Є–Є –Є –≥–Є–њ–µ—А–њ–ї–∞–Ј–Є–Є –Ї—А–Є–њ—В; –≤) —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —З–Є—Б–ї–∞ g/l —Д–Њ—А–Љ –Ґ –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ CD4+ –Є –°D8+ –≤ —Н–њ–Є—В–µ–ї–Є–Є –Є —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ–є –њ–ї–∞—Б—В–Є–љ–Ї–µ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –љ–∞—З–∞–ї—М–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤ —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є; –≥) –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Љ–∞–ї–∞–±—Б–Њ—А–±—Ж–Є–Є.
–°–њ–µ–Ї—В—А –Ї–Є—И–µ—З–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –њ—А–Є –У–¶ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –Є –Љ–Њ–ґ–µ—В –≤–∞—А—М–Є—А–Њ–≤–∞—В—М –Њ—В —В—П–ґ–µ–ї—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –≤—Б–∞—Б—Л–≤–∞–љ–Є—П —Б –Є—Б—В–Њ—Й–µ–љ–Є–µ–Љ –Є –≥–Є–њ–Њ–њ—А–Њ—В–µ–Є–љ–µ–Љ–Є—З–µ—Б–Ї–Є–Љ–Є –Њ—В–µ–Ї–∞–Љ–Є –і–Њ —Б–Ї—А—Л—В—Л—Е —Д–Њ—А–Љ (—А–Є—Б. 2). –Т —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е –±–Њ–ї–µ–Ј–љ—М –Љ–∞–љ–Є—Д–µ—Б—В–Є—А—Г–µ—В –≤–љ–µ–Ї–Є—И–µ—З–љ—Л–Љ–Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є, –љ–∞–њ—А–Є–Љ–µ—А, –∞–љ–µ–Љ–Є–µ–є, –Њ—Б—В–µ–Њ–њ–µ–љ–Є–µ–є, –±–µ—Б–њ–ї–Њ–і–Є–µ–Љ –Є —В.–і. –Ґ—П–ґ–µ–ї–∞—П —Д–Њ—А–Љ–∞ —Ж–µ–ї–Є–∞–Ї–Є–Є —Б –°–Э–Т III —Б—В. —В—П–ґ–µ—Б—В–Є –≤—Б—В—А–µ—З–∞–µ—В—Б—П —А–µ–і–Ї–Њ, —З—В–Њ –Є —Б–ї—Г–ґ–Є–ї–Њ –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –Њ—В–љ–Њ—Б–Є—В—М —Ж–µ–ї–Є–∞–Ї–Є—О –Ї —А–µ–і–Ї–Є–Љ —Д–Њ—А–Љ–∞–Љ –њ–∞—В–Њ–ї–Њ–≥–Є–Є. –Ы–Є—И—М —В–µ–њ–µ—А—М —Б—В–∞–ї–Њ —П—Б–љ–Њ, —З—В–Њ –≥–Њ—А–∞–Ј–і–Њ —З–∞—Й–µ –±–Њ–ї–µ–Ј–љ—М –њ—А–Њ—В–µ–Ї–∞–µ—В –≤ –Љ–∞–ї–Њ—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є –Є–ї–Є –і–∞–ґ–µ –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є —Д–Њ—А–Љ–µ.
–†–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Є –≥—А—Г–њ–њ—Л —А–Є—Б–Ї–∞
–Ґ–Є–њ–Є—З–љ–∞—П —Д–Њ—А–Љ–∞ —Ж–µ–ї–Є–∞–Ї–Є–Є –≤—Б—В—А–µ—З–∞–µ—В—Б—П –њ—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ —Г 1:1000 –Є —А–µ–ґ–µ. –Э–Њ —Б–Ї—А—Л—В—Л–µ –Є –∞—В–Є–њ–Є—З–љ—Л–µ —Д–Њ—А–Љ—Л –≤—Л—П–≤–ї—П—О—В –њ—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ –≤ 10 —А–∞–Ј —З–∞—Й–µ. –Я–Њ—Н—В–Њ–Љ—Г –≤ —Ж–µ–ї–Њ–Љ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М —Ж–µ–ї–Є–∞–Ї–Є–Є –Љ–Њ–ґ–µ—В –≤–∞—А—М–Є—А–Њ–≤–∞—В—М –Њ—В 1:200 [3] –і–Њ 1:100 [4]. –£—Б–њ–µ—Е–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Њ–±—К—П—Б–љ—П—О—В—Б—П –∞–Ї—В–Є–≤–љ—Л–Љ –≤—Л—П–≤–ї–µ–љ–Є–µ–Љ –∞—В–Є–њ–Є—З–љ—Л—Е —Д–Њ—А–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –њ—А–Њ—В–µ–Ї–∞—О—Й–Є—Е –±–µ–Ј –Ї–Є—И–µ—З–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Є –љ–∞—А—Г—И–µ–љ–Є–є –≤—Б–∞—Б—Л–≤–∞–љ–Є—П.
–Ю—Б–Њ–±–µ–љ–љ–Њ —З–∞—Б—В–Њ –У–¶ –≤—Б—В—А–µ—З–∞–µ—В—Б—П –≤ –≥—А—Г–њ–њ–∞—Е —А–Є—Б–Ї–∞. –Ъ –љ–Є–Љ –Њ—В–љ–Њ—Б—П—В—Б—П: 1) –±–ї–Є–ґ–∞–є—И–Є–µ —А–Њ–і—Б—В–≤–µ–љ–љ–Є–Ї–Є –±–Њ–ї—М–љ—Л—Е —Ж–µ–ї–Є–∞–Ї–Є–µ–є; 2) –±–Њ–ї—М–љ—Л–µ —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є–Љ–Є –њ–Њ–і–Њ–Ј—А–µ–≤–∞—В—М –љ–∞—А—Г—И–µ–љ–Є–µ –≤—Б–∞—Б—Л–≤–∞–љ–Є—П –≤ –Ї–Є—И–µ—З–љ–Є–Ї–µ: –і–µ—В–Є, –Њ—В—Б—В–∞—О—Й–Є–µ –≤ —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є–Є, –∞–љ–µ–Љ–Є—П, –Њ—Б—В–µ–Њ–њ–µ–љ–Є—П, –Ј–∞–і–µ—А–ґ–Ї–∞ –њ–Њ–ї–Њ–≤–Њ–≥–Њ —Б–Њ–Ј—А–µ–≤–∞–љ–Є—П, –∞–Љ–µ–љ–Њ—А–µ—П, –±–µ—Б–њ–ї–Њ–і–Є–µ, –њ—А–Є—З–Є–љ—Г –Ї–Њ—В–Њ—А—Л—Е –≤—Л—П—Б–љ–Є—В—М –љ–µ —Г–і–∞–ї–Њ—Б—М; 3) –±–Њ–ї—М–љ—Л–µ, —Б—В—А–∞–і–∞—О—Й–Є–µ –≥–µ—А–њ–µ—В–Є—Д–Њ—А–Љ–љ—Л–Љ –і–µ—А–Љ–∞—В–Є—В–Њ–Љ –Ф—О—А–Є–љ–≥–∞ –Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –±—Л—В—М —Б–≤—П–Ј–∞–љ—Л —Б —Ж–µ–ї–Є–∞–Ї–Є–µ–є: –Є–љ—Б—Г–ї–Є–љ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 1 —В–Є–њ–∞ –Є –і—А—Г–≥–Є–Љ–Є –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є, —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–Є–Љ –Ї–Њ–љ—К—О–љ–Ї—В–Є–≤–Є—В–Њ–Љ, —П–Ј–≤–µ–љ–љ—Л–Љ —Б—В–Њ–Љ–∞—В–Є—В–Њ–Љ, –і–µ—Д–µ–Ї—В–∞–Љ–Є –Ј—Г–±–љ–Њ–є —Н–Љ–∞–ї–Є, —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–Љ –і–µ—Д–Є—Ж–Є—В–Њ–Љ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–∞ A (–Ш–У–Р). –І–∞—Б—В–Њ—В–∞ —Ж–µ–ї–Є–∞–Ї–Є–Є –≤ –≥—А—Г–њ–њ–∞—Е —А–Є—Б–Ї–∞ –≤ —Б—А–µ–і–љ–µ–Љ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 5–10%.
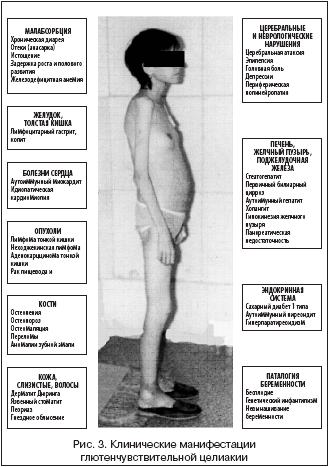
–Э–∞ —А–Є—Б—Г–љ–Ї–µ 3 –њ–Њ–Ї–∞–Ј–∞–љ—Л –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Љ–∞–љ–Є—Д–µ—Б—В–∞—Ж–Є–Є –У–¶, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–µ –Љ–∞–ї–∞–±—Б–Њ—А–±—Ж–Є–µ–є –Є –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ–Є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є—П–Љ–Є —Б –і—А—Г–≥–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є.
–£ 4–8% –ґ–µ–љ—Й–Є–љ —Б –љ–µ–Њ–±—К—П—Б–љ–µ–љ–љ—Л–Љ –±–µ—Б–њ–ї–Њ–і–Є–µ–Љ –љ–µ–Ї–Њ—В–Њ—А—Л–µ –∞–≤—В–Њ—А—Л –Њ–±–љ–∞—А—Г–ґ–Є–ї–Є —Ж–µ–ї–Є–∞–Ї–Є—О [5]. –£—Б–њ–µ—И–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –±–µ—Б–њ–ї–Њ–і–Є—П –њ—А–Њ–Є–Ј–Њ—И–ї–Њ –њ–Њ—Б–ї–µ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –∞–≥–ї—О—В–µ–љ–Њ–≤–Њ–є –і–Є–µ—В—Л (–Р–У–Ф) [6].
–Х. Lindh –Є –і—А. –≤ 1992 –≥. –љ–∞—И–ї–Є —Г 3,2% –±–Њ–ї—М–љ—Л—Е –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ –і–Њ–Ї–∞–Ј–∞–љ–љ—Г—О –±–Є–Њ–њ—Б–Є–µ–є —Ж–µ–ї–Є–∞–Ї–Є—О [7]. –Я–Њ–Ј–ґ–µ —Б–≤—П–Ј—М –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–∞ —Б —Ж–µ–ї–Є–∞–Ї–Є–µ–є –њ–Њ–і–≤–µ—А–і–Є–ї–Є –Љ–љ–Њ–≥–Є–µ –∞–≤—В–Њ—А—Л.
–†–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –У–¶ —Б—А–µ–і–Є –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е —Б –ґ–µ–ї–µ–Ј–Њ–і–µ—Д–Є—Ж–Є—В–љ–Њ–є –∞–љ–µ–Љ–Є–µ–є (–Ц–Ф–Р) –Ї–Њ–ї–µ–±–ї–µ—В—Б—П –Њ—В 2,2% –і–Њ 15,9% [8], –∞ —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ц–Ф–Р –љ–µ—П—Б–љ–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–Є —Ж–µ–ї–Є–∞–Ї–Є—П —Б–Њ—Б—В–∞–≤–ї—П–µ—В 20–57,8% [9]. –Я—А–Є —Н—В–Њ–Љ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–µ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Њ–±—Б–ї–µ–і—Г–µ–Љ—Л—Е –љ–µ –Є–Љ–µ–ї–Є –Ї–∞–Ї–Є—Е––ї–Є–±–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Љ–∞–ї–∞–±—Б–Њ—А–±—Ж–Є–Є.
–Я–Њ –і–∞–љ–љ—Л–Љ J.A. Murray (2005), –Є—Б—Б–ї–µ–і–Њ–≤–∞–≤—И–µ–≥–Њ –±–Њ–ї—М–љ—Л—Е —Ж–µ–ї–Є–∞–Ї–Є–µ–є –Є –і–Є–∞–±–µ—В–Њ–Љ 1 —В–Є–њ–∞ —А–∞–Ј–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –У–¶ –њ—А–µ–і—И–µ—Б—В–≤–Њ–≤–∞–ї–∞ –і–Є–∞–±–µ—В—Г —В–Њ–ї—М–Ї–Њ —Г 1%, –љ–Њ —Б–Њ–њ—Г—В—Б—В–≤–Њ–≤–∞–ї–∞ –µ–Љ—Г —Г 6,5% –±–Њ–ї—М–љ—Л—Е [10]. –†–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –У–¶ —Б—А–µ–і–Є –љ–∞—Б–µ–ї–µ–љ–Є—П —Б 1 —В–Є–њ–Њ–Љ –і–Є–∞–±–µ—В–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤—Л—И–µ, —З–µ–Љ –≤ –Њ–±—Й–µ–Љ –љ–∞—Б–µ–ї–µ–љ–Є–Є. –Ю–і–љ–∞–Ї–Њ –њ–Њ–ї–Њ–≤–Є–љ–∞ –Є—Е –љ–µ –Є–Љ–µ–ї–∞ –љ–Є–Ї–∞–Ї–Є—Е –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤. –Ю—Б—В–∞–ї—М–љ—Л–µ –Є–Љ–µ–ї–Є —В–Њ–ї—М–Ї–Њ —Г–Љ–µ—А–µ–љ–љ—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є. –Ъ–∞–Ј–∞–ї–Њ—Б—М –±—Л, –±–Њ–ї—М–љ—Л–µ –і–Є–∞–±–µ—В–Њ–Љ – –±–Њ–≥–∞—В—Л–є –Є—Б—В–Њ—З–љ–Є–Ї –і–ї—П –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є—П –У–¶. –Ф–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ, –Љ–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–і–≤–µ—А–≥–∞—О—В—Б—П —Н–љ–і–Њ—Б–Ї–Њ–њ–Є–Є, —З—В–Њ–±—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞—В—М –њ—А–Є—З–Є–љ—Г —З–∞—Б—В—Л—Е –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –љ–∞–±–ї—О–і–∞—О—В—Б—П —Г –љ–Є—Е. –≠—В–Њ —В—А–µ–±–Њ–≤–∞–ї–Њ –±—Л –љ–µ–Љ–љ–Њ–≥–Њ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е —Г—Б–Є–ї–Є–є, —З—В–Њ–±—Л –њ–Њ–ї—Г—З–Є—В—М –±–Є–Њ–њ—В–∞—В—Л –Є –њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ –Њ–і–љ–∞–ґ–і—Л –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –У–¶, —В–µ–Љ –±–Њ–ї–µ–µ, —З—В–Њ —А–µ–Ј—Г–ї—М—В–∞—В –±–Є–Њ–њ—Б–Є–Є –Љ–Њ–ґ–µ—В –Њ–±—К—П—Б–љ—П—В—М –њ—А–Є–Ј–љ–∞–Ї–Є –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –і–ї—П –Ї–Њ—В–Њ—А—Л—Е –њ—А–Њ—Ж–µ–і—Г—А–∞ –Є –±—Л–ї–∞ —Б–і–µ–ї–∞–љ–∞. –Э–µ —П—Б–љ–Њ, –Ї–∞–Ї–Њ–≤–∞ –њ—А–Є—З–Є–љ–∞ —Н—В–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, —Е–Њ—В—П –Њ–љ–Є, –Ї–∞–ґ–µ—В—Б—П, —Б—В–Є—Е–∞—О—В –љ–∞ —Д–Њ–љ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Б–Њ–±–ї—О–і–µ–љ–Є—П –Р–У–Ф.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М —Б–Ї—А—Л—В–Њ–є —Д–Њ—А–Љ—Л –У–¶ –њ—А–Є–±–ї–Є–ґ–∞–µ—В—Б—П –Ї 1% –Њ—В –Њ–±—Й–µ–є —З–Є—Б–ї–µ–љ–љ–Њ—Б—В–Є –љ–∞—Б–µ–ї–µ–љ–Є—П. –¶–µ–љ–љ–Њ—Б—В—М –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –≤—Л—П–≤–ї–µ–љ–Є—П —Б–Ї—А—Л—В—Л—Е —Д–Њ—А–Љ —Ж–µ–ї–Є–∞–Ї–Є–Є –Њ–±—К—П—Б–љ—П–µ—В—Б—П —В–µ–Љ, —З—В–Њ –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –Р–У–Ф –Є—Б—З–µ–Ј–∞—О—В –Є–ї–Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г–Љ–µ–љ—М—И–∞—О—В—Б—П –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –±–Њ–ї–µ–Ј–љ–µ–є, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б —Ж–µ–ї–Є–∞–Ї–Є–µ–є (–Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј, –±–µ—Б–њ–ї–Њ–і–Є–µ, –Ј–∞–і–µ—А–ґ–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Є —В.–і.).
–Ш—Б—Е–Њ–і—П –Є–Ј –≤—Л—И–µ–Є–Ј–ї–Њ–ґ–µ–љ–љ–Њ–≥–Њ, —Б—В–∞–љ–Њ–≤–Є—В—Б—П —П—Б–љ–Њ, —З—В–Њ –∞–Ї—В–Є–≤–љ—Л–є –њ–Њ–Є—Б–Ї —Ж–µ–ї–Є–∞–Ї–Є–Є —Б—А–µ–і–Є –Њ–±—Й–µ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є –љ–∞—Б–µ–ї–µ–љ–Є—П, –Є –≤ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –≤ –≥—А—Г–њ–њ–∞—Е —А–Є—Б–Ї–∞, –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ—В–љ–µ—Б–µ–љ –Ї —Б–њ–Њ—Б–Њ–±—Г –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –±–Њ–ї–µ–Ј–љ–µ–є, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л—Е —Б —Ж–µ–ї–Є–∞–Ї–Є–µ–є.
–Э–µ–Ї–Њ—В–Њ—А—Л–µ –±–Њ–ї–µ–Ј–љ–Є, –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ —З–∞—Б—В–Њ —Б–Њ—З–µ—В–∞—О—Й–Є–µ—Б—П —Б —Ж–µ–ї–Є–∞–Ї–Є–µ–є, –Њ–±—К—П—Б–љ—П—О—В—Б—П –Њ–±—Й–љ–Њ—Б—В—М—О –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є —Б–≤—П–Ј–Є. –Ґ–∞–Ї, –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є—П —Б –≥–µ—А–њ–µ—В–Є—Д–Њ—А–Љ–љ—Л–Љ –і–µ—А–Љ–∞—В–Є—В–Њ–Љ –Є —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –Ф–∞—Г–љ–∞ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –±–ї–Є–Ј–Њ—Б—В—М—О –Є—Е –≥–µ–љ–Њ–≤. –°—Г—Й–µ—Б—В–≤—Г–µ—В –≥–Є–њ–Њ—В–µ–Ј–∞, —З—В–Њ —Б–≤—П–Ј—М —Б –±–Њ–ї–µ–Ј–љ—М—О –Ф–∞—Г–љ–∞ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В—Б—П –≥–µ–љ–Њ–Љ –≤–Њ—Б–њ—А–Є–Є–Љ—З–Є–≤–Њ—Б—В–Є –Ї –У–¶, –Ї–Њ—В–Њ—А—Л–є –љ–∞—Е–Њ–і–Є—В—Б—П –≤ —Е—А–Њ–Љ–Њ—Б–Њ–Љ–µ 21. C–≤—П–Ј—М –і–µ—А–Љ–∞—В–Є—В–∞ –Ф—О—А–Є–љ–≥–∞ —Б –У–¶ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Г –љ–Є—Е –∞–љ—В–Є–≥–µ–љ–Њ–≤ –≥–Є—Б—В–Њ—Б–Њ–≤–Љ–µ—Б—В–Є–Љ–Њ—Б—В–Є: —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М HLA–DQ2 –Є–DQ8 —Г –±–Њ–ї—М–љ—Л—Е –≥–µ—А–њ–µ—В–Є—Д–Њ—А–Љ–љ—Л–Љ –і–µ—А–Љ–∞—В–Є—В–Њ–Љ —В–∞ –ґ–µ —Б–∞–Љ–∞—П, —З—В–Њ –Є —Г –±–Њ–ї—М–љ—Л—Е –У–¶.
–Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞
–°–њ–µ–Ї—В—А —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Є —В—П–ґ–µ—Б—В—М —Б–Њ—Б—В–Њ—П–љ–Є—П –±–Њ–ї—М–љ–Њ–≥–Њ –њ—А–Є —Ж–µ–ї–Є–∞–Ї–Є–Є –Ј–∞–≤–Є—Б—П—В –Њ—В –њ—А–Њ—В—П–ґ–µ–љ–љ–Њ—Б—В–Є, —Б—В–µ–њ–µ–љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –Є –Њ—В —А–∞–Ј–≤–Є—В–Є—П –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є.
–£ –±–Њ–ї—М–љ—Л—Е —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –і–Є–∞—А–µ–µ–є —Б –°–Э–Т III —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є –Њ–±—Л—З–љ–Њ –њ–Њ—А–∞–ґ–µ–љ–∞ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–∞—П –Є —В–Њ—Й–∞—П –Ї–Є—И–Ї–Є. –£ –±–Њ–ї—М–љ—Л—Е —Б –Љ–µ–љ–µ–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є –њ—А–Њ—В—П–ґ–µ–љ–љ–Њ—Б—В—М—О –∞—В—А–Њ—Д–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Ї–∞—А—В–Є–љ–∞ –Љ–Њ–ґ–µ—В –Њ–≥—А–∞–љ–Є—З–Є–≤–∞—В—М—Б—П —Н–њ–Є–Ј–Њ–і–∞–Љ–Є –і–Є–∞—А–µ–Є, –њ–Є—Й–µ–≤—Л–Љ–Є –Є–љ—В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В—П–Љ–Є –Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–Љ–Є –Є–Ј–±–Є—А–∞—В–µ–ї—М–љ—Л–Љ –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –≤—Б–∞—Б—Л–≤–∞–љ–Є—П –љ—Г—В—А–Є–µ–љ—В–Њ–≤, –љ–∞–њ—А–Є–Љ–µ—А –ґ–µ–ї–µ–Ј–∞ –Є–ї–Є –Ї–∞–ї—М—Ж–Є—П. –Я—А–∞–≤–Є–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј –≤ —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е –Љ–Њ–ґ–µ—В –±—Л—В—М —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ –ї–Є—И—М —В–Њ–≥–і–∞, –Ї–Њ–≥–і–∞ —Г –≤—А–∞—З–∞ –њ–Њ—П–≤–Є—В—Б—П –Љ—Л—Б–ї—М –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є —Б–≤—П–Ј–Є –≤–љ–µ–Ї–Є—И–µ—З–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ —Б —Ж–µ–ї–Є–∞–Ї–Є–µ–є.
–Х—Й–µ —Б–ї–Њ–ґ–љ–µ–µ —Г—Б—В–∞–љ–Њ–≤–Є—В—М –њ—А–∞–≤–Є–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј —Г –±–Њ–ї—М–љ—Л—Е –∞—В–Є–њ–Є—З–љ–Њ–є —Ж–µ–ї–Є–∞–Ї–Є–µ–є. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Ї–∞—А—В–Є–љ–∞ —Г –љ–Є—Е –њ—А–Њ—П–≤–ї—П–µ—В—Б—П —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П. –Ґ—А—Г–і–љ–Њ—Б—В–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —Г—Б—Г–≥—Г–±–ї—П—О—В—Б—П —В–µ–Љ, —З—В–Њ –Ї–Є—И–µ—З–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –Љ–Њ–≥—Г—В –Њ—В—Б—В—Г–њ–∞—В—М –љ–∞ –≤—В–Њ—А–Њ–є –њ–ї–∞–љ –њ–µ—А–µ–і –≤–љ–µ–Ї–Є—И–µ—З–љ—Л–Љ–Є –Љ–∞–љ–Є—Д–µ—Б—В–∞—Ж–Є—П–Љ–Є –Є–ї–Є –ґ–µ –≤–Њ–≤—Б–µ –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞—В—М. –≠—В–Є–Љ–Є –Њ–±—Б—В–Њ—П—В–µ–ї—М—Б—В–≤–∞–Љ–Є –Њ–±—К—П—Б–љ—П–µ—В—Б—П –Њ–і–љ–∞ –Є–Ј –≤–∞–ґ–љ–µ–є—И–Є—Е –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –У–¶. –Х–µ —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—О—В —В–Њ–ї—М–Ї–Њ —В–µ –≤—А–∞—З–Є, –Ї–Њ—В–Њ—А—Л–Љ –Є–Ј–≤–µ—Б—В–љ—Л –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –∞—В–Є–њ–Є—З–љ–Њ–≥–Њ —В–µ—З–µ–љ–Є—П –Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є (–Љ–Њ–ї—З–∞—Й–µ–є) —Ж–µ–ї–Є–∞–Ї–Є–Є. –Т–∞–ґ–љ–Њ –Њ–±—А–∞—В–Є—В—М –≤–љ–Є–Љ–∞–љ–Є–µ –љ–∞ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–µ –Ј–љ–∞–љ–Є—П –≤—А–∞—З–∞–Љ–Є –њ—А–Њ–±–ї–µ–Љ, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Њ–є –У–¶. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, —А–µ–і–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–∞—А–Ї–µ—А—Л –Є –і—Г–Њ–і–µ–љ–Њ–±–Є–Њ–њ—Б–Є—О –і–ї—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —Ж–µ–ї–Є–∞–Ї–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –і–Є–∞—А–µ–µ–є. –Ь–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –Њ—Ж–µ–љ–Ї–∞ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є —З–∞—Б—В–Њ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П –±–µ–Ј –і–Њ–ї–ґ–љ–Њ–≥–Њ —Г—З–µ—В–∞ –Ї–∞—З–µ—Б—В–≤–∞ –Њ—А–Є–µ–љ—В–∞—Ж–Є–Є –±–Є–Њ–њ—В–∞—В–Њ–≤ –Є —Б—В–∞–љ–і–∞—А—В–∞ –Њ—Ж–µ–љ–Ї–Є –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–Ь–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є
–Ф–Є–∞–≥–љ–Њ–Ј —Ж–µ–ї–Є–∞–Ї–Є–Є – –Њ—З–µ–љ—М –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л–є, —В–∞–Ї –Ї–∞–Ї —В—А–µ–±—Г–µ—В –њ–Њ–ґ–Є–Ј–љ–µ–љ–љ–Њ–≥–Њ —Б–Њ–±–ї—О–і–µ–љ–Є—П –Р–У–Ф. –Я–Њ—Н—В–Њ–Љ—Г –µ–≥–Њ –Љ–Њ–ґ–љ–Њ —Б—З–Є—В–∞—В—М –њ—А–∞–≤–Њ–Љ–Њ—З–љ—Л–Љ —В–Њ–ї—М–Ї–Њ –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є. –Ф—Г–Њ–і–µ–љ–∞–ї—М–љ–∞—П –±–Є–Њ–њ—Б–Є—П –і–Њ–ї–ґ–љ–∞ –±—Л—В—М –≤—Л–њ–Њ–ї–љ–µ–љ–∞ –≤—Б–µ–Љ –±–Њ–ї—М–љ—Л–Љ, —Г –Ї–Њ—В–Њ—А—Л—Е –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В—Б—П –У–¶ –Є–ї–Є —В—А–µ–±—Г–µ—В—Б—П –Є—Б–Ї–ї—О—З–Є—В—М —Н—В—Г –±–Њ–ї–µ–Ј–љ—М. –С–Є–Њ–њ—Б–Є–Є –і–Њ–ї–ґ–љ—Л –±—Л—В—М —Б–і–µ–ї–∞–љ—Л –≤—Б–µ–Љ –ї–Є—Ж–∞–Љ —Б –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ–Є –Р–У–Р, –Р–≠–Р –Є–ї–Є –Р–Ґ–Ґ–У, –Ц–Ф–Р, –Њ—Б—В–µ–Њ–Љ–∞–ї—П—Ж–Є–µ–є, –Љ–∞–ї–∞–±—Б–Њ—А–±—Ж–Є–µ–є –Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–є –љ–µ–Њ–±—К—П—Б–љ–µ–љ–љ–Њ–є –њ–Њ—В–µ—А–µ–є –Љ–∞—Б—Б—Л —В–µ–ї–∞. –Ю—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Б–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Ї—А–Є–љ–Є–љ–≥–∞ –љ–µ —П–≤–ї—П—О—В—Б—П –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П –Њ—В–Ї–∞–Ј–∞ –Њ—В –±–Є–Њ–њ—Б–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б —В–µ–Љ–Є –Є–ї–Є –Є–љ—Л–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –У–¶.
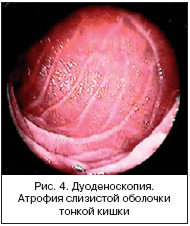
–Ь–∞–Ї—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ—А–Є —Ж–µ–ї–Є–∞–Ї–Є–Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П –±–ї–µ–і–љ–Њ—Б—В—М—О —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є, —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –≤—Л—Б–Њ—В—Л —Б–Ї–ї–∞–і–Њ–Ї, –Ї–Њ—В–Њ—А—Л–µ —Б—В–∞–љ–Њ–≤—П—В—Б—П —А–µ–і–Ї–Є–Љ–Є. –Т–Њ –≤—А–µ–Љ—П –і—Г–Њ–і–µ–љ–Њ—Б–Ї–Њ–њ–Є–Є –Љ–Њ–ґ–љ–Њ –≤–Є–і–µ—В—М –њ—А–Є–Ј–љ–∞–Ї–Є –∞—В—А–Њ—Д–Є–Є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є: –Є—Б—В–Њ–љ—З–µ–љ–Є–µ –Є –њ–Њ–≤—Л—И–µ–љ–љ—Г—О —В—А–∞–≤–Љ–Є—А—Г–µ–Љ–Њ—Б—В—М –µ–µ, —А–µ–і–Ї–Є–µ –Ї–µ—А–Ї—А–Є–љ–≥–Њ–≤—Л —Б–Ї–ї–∞–і–Ї–Є, –Є–Љ–µ—О—Й–Є–µ –Ј–∞–Ј—Г–±—А–Є–љ–Ї–Є –љ–∞ –≤–µ—А—И–Є–љ–∞—Е (—Д–µ—Б—В–Њ–љ—З–∞—В—Л–µ —Б–Ї–ї–∞–і–Ї–Є) (—А–Є—Б. 4).
–•–∞—А–∞–Ї—В–µ—А–љ—Л–µ –і–ї—П –У–¶ –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤–Њ–Ј–љ–Є–Ї–∞—О—В –≤ –Љ–µ—Б—В–µ –њ–µ—А–≤–Њ–≥–Њ –Ї–Њ–љ—В–∞–Ї—В–∞ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –Ї–Є—И–µ—З–љ–Є–Ї–∞ —Б –≥–ї—О—В–µ–љ–Њ–Љ: –≤ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Є —В–Њ—Й–µ–є –Ї–Є—И–Ї–∞—Е. –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –і–ї—П –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –≤–њ–Њ–ї–љ–µ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –±–Є–Њ–њ—В–∞—В—Л, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –Њ–±—Л—З–љ—Л–Љ –і—Г–Њ–і–µ–љ–Њ—Б–Ї–Њ–њ–Њ–Љ –Є–Ј –і–Є—Б—В–∞–ї—М–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ–Њ–ї—Г—З–Є—В—М –љ–µ –Љ–µ–љ–µ–µ —В—А–µ—Е —Д—А–∞–≥–Љ–µ–љ—В–Њ–≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –Є–Ј —А–∞–Ј–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤ —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є.
–Х—Б–ї–Є –Є–Љ–µ—О—В—Б—П —Н–Ї–Ј–µ–Љ–њ–ї—П—А—Л —Б –ґ–µ–ї–µ–Ј–∞–Љ–Є –С—А—Г–љ–љ–µ—А–∞ –Є–ї–Є –ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –Љ–µ—В–∞–њ–ї–∞–Ј–Є–µ–є, —В–Њ —Н—В–Є –Њ–±—А–∞–Ј—Ж—Л –Є–≥–љ–Њ—А–Є—А—Г—О—В –Є –њ–Њ–≤—В–Њ—А—П—О—В –±–Є–Њ–њ—Б–Є—О –Є–Ј –±–Њ–ї–µ–µ –і–Є—Б—В–∞–ї—М–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є.
–Т —Ж–µ–ї—П—Е —Г–љ–Є—Д–Є–Ї–∞—Ж–Є–Є –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–њ–Є—Б–∞–љ–Є—П –Є –Ј–∞–Ї–ї—О—З–µ–љ–Є–є –Њ –љ–∞–ї–Є—З–Є–Є –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є —Ж–µ–ї–Є–∞–Ї–Є–Є –≤ 1992 –≥. M.N. Marsh –њ—А–µ–і–ї–Њ–ґ–Є–ї –њ–∞—В–Њ–Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—О —Ж–µ–ї–Є–∞–Ї–Є–Є. –Т –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є –Њ–њ–Є—Б–∞–љ—Л —Б—В–∞–і–Є–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –њ—А–Є —Ж–µ–ї–Є–∞–Ї–Є–Є [11]. –Я–Њ–Ј–ґ–µ, –≤ 1999 –≥. –Ь.–Э. –Ь–∞—А—И –±–Њ–ї–µ–µ –њ–Њ–і—А–Њ–±–љ–Њ —Б–Є—Б—В–µ–Љ–∞—В–Є–Ј–Є—А–Њ–≤–∞–ї —Б—В–∞–і–Є–Є –±–Њ–ї–µ–Ј–љ–Є, –Є –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П —Б—В–∞–ї–∞ –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ.
–°—В–∞–і–Є–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –њ—А–Є —Ж–µ–ї–Є–∞–Ї–Є–Є:
–Ь–∞—А—И I (–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–∞—П) – —Б—В—А—Г–Ї—В—Г—А–∞ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –љ–Њ—А–Љ–∞–ї—М–љ–∞—П, –љ–Њ —Б –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ–Љ –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ –≤ —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л–є —Б–ї–Њ–є –≤–Њ—А—Б–Є–љ–Њ–Ї. –Т –љ–Њ—А–Љ–µ —З–Є—Б–ї–Њ –Ь–≠–Ы –і–Њ–ї–ґ–љ–Њ –±—Л—В—М –љ–µ –±–Њ–ї–µ–µ 30–40 –љ–∞ 100 –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л—Е —Н–љ—В–µ—А–Њ—Ж–Є—В–Њ–≤. –Ф–ї—П –Њ–±–ї–µ–≥—З–µ–љ–Є—П –Є–і–µ–љ—В–Є—Д–Є–Ї–∞—Ж–Є–Є –Є –њ–Њ–і—Б—З–µ—В–∞ –Ь–≠–Ы —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ—А–Є–Љ–µ–љ—П—В—М –Њ–Ї—А–∞—Б–Ї—Г –љ–∞ CD3 –ї–Є–Љ—Д–Њ—Ж–Є—В—Л.
–Ь–∞—А—И II (–ї–Є–Љ—Д–Њ—Ж–Є—В–∞—А–љ—Л–є —Н–љ—В–µ—А–Є—В). –Я–Њ–Љ–Є–Љ–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є—П —З–Є—Б–ї–∞ –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤, –њ–Њ—П–≤–ї—П–µ—В—Б—П –≥–Є–њ–µ—А–њ–ї–∞–Ј–Є—П –Ї—А–Є–њ—В —Б —Г–і–ї–Є–љ–µ–љ–Є–µ–Љ –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –Љ–Є—В–Њ—В–Є—З–µ—Б–Ї–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є. –°–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ –≥–ї—Г–±–Є–љ—Л –Ї—А–Є–њ—В –Є –≤—Л—Б–Њ—В—Л –≤–Њ—А—Б–Є–љ–Њ–Ї —З–∞—Б—В–Њ —Б—В–∞–љ–Њ–≤–Є—В—Б—П —Г–Љ–µ–љ—М—И–µ–љ–љ—Л–Љ – –љ–Є–ґ–µ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П 1:3–5.
–Ь–∞—А—И III (–і–µ—Б—В—А—Г–Ї—Ж–Є—П) – –∞—В—А–Њ—Д–Є—П –≤–Њ—А—Б–Є–љ–Њ–Ї.
–Ь–∞—А—И IIIA (–њ–∞—А—Ж–Є–∞–ї—М–љ–∞—П –∞—В—А–Њ—Д–Є—П –≤–Њ—А—Б–Є–љ–Њ–Ї) –Њ–±–Њ–Ј–љ–∞—З–∞–µ—В —З–∞—Б—В–Є—З–љ—Г—О –∞—В—А–Њ—Д–Є—О –≤–Њ—А—Б–Є–љ–Њ–Ї, –Ї–Њ—В–Њ—А–∞—П —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ–Љ –≥–ї—Г–±–Є–љ—Л –Ї—А–Є–њ—В/–≤—Л—Б–Њ—В—Л –≤–Њ—А—Б–Є–љ–Њ–Ї –Љ–µ–љ—М—И–µ, —З–µ–Љ 1.
–Ь–∞—А—И IIIB (—Б—Г–±—В–Њ—В–∞–ї—М–љ–∞—П –∞—В—А–Њ—Д–Є—П –≤–Њ—А—Б–Є–љ–Њ–Ї) –Њ–±–Њ–Ј–љ–∞—З–∞–µ—В –∞—В—А–Њ—Д–Є—О –≤–Њ—А—Б–Є–љ–Њ–Ї, –Ї–Њ–≥–і–∞ –Њ—В–і–µ–ї—М–љ—Л–µ –Є–Ј –љ–Є—Е –µ—Й–µ —А–∞—Б–њ–Њ–Ј–љ–∞–≤–∞–µ–Љ—Л.
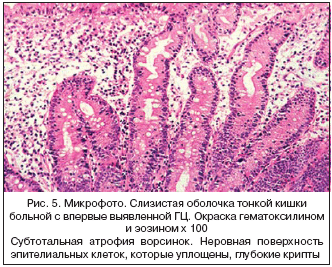
–Ь–∞—А—И IIIC (—В–Њ—В–∞–ї—М–љ–∞—П –∞—В—А–Њ—Д–Є—П –≤–Њ—А—Б–Є–љ–Њ–Ї) –Њ–±–Њ–Ј–љ–∞—З–∞–µ—В –њ–Њ–ї–љ—Г—О –∞—В—А–Њ—Д–Є—О –≤–Њ—А—Б–Є–љ–Њ–Ї –±–µ–Ј –њ–∞–ї—М—Ж–µ–≤–Є–і–љ—Л—Е –≤–Њ–Ј–≤—Л—И–µ–љ–Є–є, –љ–∞–њ–Њ–Љ–Є–љ–∞–µ—В —Б–ї–Є–Ј–Є—Б—В—Г—О –Њ–±–Њ–ї–Њ—З–Ї—Г —В–Њ–ї—Б—В–Њ–є –Ї–Є—И–Ї–Є (—А–Є—Б. 5).
–Ь–∞—А—И IV (–≥–Є–њ–Њ–њ–ї–∞—Б—В–Є—З–µ—Б–Ї–∞—П –∞—В—А–Њ—Д–Є—П) –Њ–±–Њ–Ј–љ–∞—З–∞–µ—В —А–µ–Ј–Ї–Њ–µ –Є—Б—В–Њ–љ—З–µ–љ–Є–µ –њ–ї–Њ—Б–Ї–Њ–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є, –Њ–±–Њ–Ј–љ–∞—З–∞—О—Й–µ–µ –љ–µ–Њ–±—А–∞—В–Є–Љ—Л–µ –∞—В—А–Њ—Д–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П, –≤—Л–Ј–≤–∞–љ–љ—Л–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ–Љ. –≠—В–∞ —А–µ–і–Ї–∞—П —Д–Њ—А–Љ–∞ –∞—В—А–Њ—Д–Є–Є —Б–≤—П–Ј–∞–љ–∞ —Б —А–µ—Д—А–∞–Ї—В–µ—А–љ–Њ–є —Ж–µ–ї–Є–∞–Ї–Є–µ–є –Є —А–∞–Ј–≤–Є—В–Є–µ–Љ —Н–љ—В–µ—А–Њ–њ–∞—В–Є–Є, —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б T––Ї–ї–µ—В–Њ—З–љ–Њ–є –ї–Є–Љ—Д–Њ–Љ–Њ–є. –•–∞—А–∞–Ї—В–µ—А–љ–∞ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ–∞—П –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є—П T––ї–Є–Љ—Д–Њ—Ж–Є—В–∞–Љ–Є –љ–µ–Њ–±—Л—З–љ–Њ–≥–Њ —Д–µ–љ–Њ—В–Є–њ–∞.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л—Е –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є (–Ь–∞—А—И I –Є II):
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є –љ–∞–±–ї—О–і–µ–љ–Є—П–Љ–Є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —Б—В–µ–њ–µ–љ—М –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є —П–≤–ї—П–µ—В—Б—П –Њ—В—А–∞–ґ–µ–љ–Є–µ–Љ —Б–њ–µ–Ї—В—А–∞ —В—П–ґ–µ—Б—В–Є –±–Њ–ї–µ–Ј–љ–Є. –Ґ—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ –і–Є–∞–≥–љ–Њ–Ј —Ж–µ–ї–Є–∞–Ї–Є–Є —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—О—В –њ—А–Є –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є, —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ—Л—Е –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П–Љ —В–Є–њ–∞ –Ь–∞—А—И III. –Ґ–µ–њ–µ—А—М —П—Б–љ–Њ, —З—В–Њ –Љ–љ–Њ–≥–Њ –ї—О–і–µ–є –Є–Љ–µ—О—В –≥–ї—О—В–µ–љ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ –±–µ–Ј –∞—В—А–Њ—Д–Є–Є –≤–Њ—А—Б–Є–љ–Њ–Ї. –≠—В–∞ –њ–∞—В–Њ–≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –≥—А–∞–љ–Є—Ж–∞ —Е–Њ—А–Њ—И–Њ –≤–Є–і–љ–∞ –њ–Њ—Б–ї–µ —Г–ї—Г—З—И–µ–љ–Є—П –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Р–У–Ф.
–Я–Њ–≤—В–Њ—А–љ—Л–µ –±–Є–Њ–њ—Б–Є–Є
–Т–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ —Б–ї–Є–Ј–Є—Б—В–Њ–є —П–≤–ї—П–µ—В—Б—П –і–ї–Є—В–µ–ї—М–љ—Л–Љ –њ—А–Њ—Ж–µ—Б—Б–Њ–Љ –Є —Г –љ–µ–Ї–Њ—В–Њ—А—Л—Е –±–Њ–ї—М–љ—Л—Е –Љ–Њ–ґ–µ—В –њ—А–Њ–і–Њ–ї–ґ–∞—В—М—Б—П –і–Њ –њ–Њ–ї—Г—В–Њ—А–∞ –ї–µ—В. –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –і–∞–ґ–µ –Њ–і–љ–Њ–≥–Њ –≥–Њ–і–∞ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ, —З—В–Њ–±—Л –Њ—Ж–µ–љ–Є—В—М –Ї–∞—З–µ—Б—В–≤–Њ —Б–Њ–±–ї—О–і–µ–љ–Є—П –і–Є–µ—В—Л. –Х—Б–ї–Є —Г—А–Њ–≤–љ–Є –∞–љ—В–Є—В–µ–ї –љ–µ —Г–Љ–µ–љ—М—И–∞—О—В—Б—П –≤ –њ—А–µ–і–µ–ї–∞—Е 12 –Љ–µ—Б—П—Ж–µ–≤, —Б–ї–µ–і—Г–µ—В —Г–±–µ–і–Є—В—М—Б—П –≤ —В—Й–∞—В–µ–ї—М–љ–Њ—Б—В–Є —Б–Њ–±–ї—О–і–µ–љ–Є—П –і–Є–µ—В—Л –±–Њ–ї—М–љ—Л–Љ, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –љ–∞–і–Њ –Є—Б–Ї–ї—О—З–Є—В—М –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –љ–µ–Њ—Б–Њ–Ј–љ–∞–љ–љ–Њ–≥–Њ –µ–µ –љ–∞—А—Г—И–µ–љ–Є—П –Ј–∞ —Б—З–µ—В —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –њ—А–Њ–і—Г–Ї—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В —Б–Њ–і–µ—А–ґ–∞—В—М –≥–ї—О—В–µ–љ. –Т —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ –љ–∞–і–Њ —Г–±–µ–і–Є—В—М –±–Њ–ї—М–љ–Њ–≥–Њ –≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –њ–Њ–≤—В–Њ—А–љ–Њ–є –±–Є–Њ–њ—Б–Є–Є —Б–њ—Г—Б—В—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Љ–µ—Б—П—Ж–µ–≤ –њ–Њ—Б–ї–µ –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Р–У–Ф.
–Ш–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є
–Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Р–У–Р –Є –Р–Ґ–Ґ–У –њ—А–Њ–≤–Њ–і—П—В —Б –њ–Њ–Љ–Њ—Й—М—О –Є–Љ–Љ—Г–љ–Њ—Д–µ—А–Љ–µ–љ—В–љ–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ (ELISA). –Т –љ–Њ—А–Љ–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Ш–У–Р –Р–У–Р –љ–µ –њ—А–µ–≤—Л—И–∞–µ—В 15 –Ь–Х/–Љ–ї.
–Ґ–µ—Б—В —Б –Р–Ґ–Ґ–У —Б—З–Є—В–∞–µ—В—Б—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ, –µ—Б–ї–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –∞–љ—В–Є—В–µ–ї –њ—А–µ–≤—Л—И–∞–µ—В 8 –Ь–Х/–Љ–ї. –†–µ–Ј—Г–ї—М—В–∞—В—Л —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є—П –љ–∞ –Р–≠–Р —Б—З–Є—В–∞—О—В –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–Љ–Є, –µ—Б–ї–Є —В–Є—В—А –∞–љ—В–Є—В–µ–ї –Љ–µ–љ—М—И–µ 1:5, –Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ–Є, –µ—Б–ї–Є –Њ–љ —А–∞–≤–µ–љ –Є–ї–Є –њ—А–µ–≤—Л—И–∞–µ—В 1:40.
–Т—Б–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ, —Г –Ї–Њ—В–Њ—А—Л—Е –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞—О—В –њ–Њ–≤—Л—И–µ–љ–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Р–У–Р –Є/–Є–ї–Є –Р–≠–Р –Є –Р–Ґ–Ґ–У, –њ–Њ–Ї–∞–Ј–∞–љ–Њ –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є–Ј—Г—З–µ–љ–Є–µ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –і–ї—П –Њ–Ї–Њ–љ—З–∞—В–µ–ї—М–љ–Њ–≥–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –і–Є–∞–≥–љ–Њ–Ј–∞. –Я—А–Є –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –њ–Њ–і–Њ–Ј—А–µ–љ–Є–Є –љ–∞ –љ–∞–ї–Є—З–Є–µ —Ж–µ–ї–Є–∞–Ї–Є–Є —Н–љ—В–µ—А–Њ–±–Є–Њ–њ—Б–Є—О —Б–ї–µ–і—Г–µ—В –њ—А–Њ–≤–Њ–і–Є—В—М –Є –≤ —Б–ї—Г—З–∞–µ –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е —В–Є—В—А–Њ–≤ –Р–У–Р –Є –Р–Ґ–Ґ–У.
–У–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–µ —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є–µ
–љ–∞ HLA–DQ2 –Є DQ8, –≥–µ–љ–Њ—В–Є–њ—Л
–¶–µ–ї–Є–∞–Ї–Є—П – –≤–∞–ґ–љ—Л–є –Ї–∞–љ–і–Є–і–∞—В –љ–∞ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–є —Б–Ї—А–Є–љ–Є–љ–≥, –Њ—Б–љ–Њ–≤–∞–љ–љ—Л–є –љ–∞ HLA–DQ –∞–ї–ї–µ–ї—П—Е. –Ґ–∞–Ї–Њ–є —В–µ—Б—В –њ–Њ–ї–µ–Ј–µ–љ –і–ї—П —А–∞–Ј–≤–Є—В–Є—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—П –≤ –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є–Є, —В.–Ї. –Њ–љ –і–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ–Њ–ї—Г—З–Є—В—М –і–∞–љ–љ—Л–µ –Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є —Ж–µ–ї–Є–∞–Ї–Є–Є. HLA––≥–∞–њ–ї–Њ—В–Є–њ—Л –Њ–њ—А–µ–і–µ–ї—П—О—В —Б –њ–Њ–Љ–Њ—Й—М—О –њ–Њ–ї–Є–Љ–µ—А–∞–Ј–љ–Њ–є —Ж–µ–њ–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є.
–Ф–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј
–Т –Њ—В–ї–Є—З–Є–µ –Њ—В –і—А—Г–≥–Є—Е –±–Њ–ї–µ–Ј–љ–µ–є, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О –њ–Є—Й–µ–≤—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ (–љ–∞–њ—А–Є–Љ–µ—А, –Љ–Њ–ї–Њ–Ї–∞ –Є–ї–Є –≥—А–Є–±–Њ–≤), –њ—А–Є –У–¶ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–∞—П —Б–≤—П–Ј—М –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ —Б —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ–Љ –≤ –њ–Є—Й—Г –њ—А–Њ–і—Г–Ї—В–Њ–≤, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –≥–ї—О—В–µ–љ. –Я–Њ—Н—В–Њ–Љ—Г –±–Њ–ї—М–љ—Л–µ –љ–Є–Ї–Њ–≥–і–∞ –љ–µ –Љ–Њ–≥—Г—В —Б–≤—П–Ј–∞—В—М —Б–≤–Њ—О –±–Њ–ї–µ–Ј–љ—М —Б –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О —Е–ї–µ–±–∞. –Я–Њ–≤—А–µ–ґ–і–∞—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –≥–ї—О—В–µ–љ–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М –≤—Л—П–≤–ї–µ–љ–Њ —В–Њ–ї—М–Ї–Њ –њ—А–Є –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –Є–Ј—Г—З–µ–љ–Є–Є –±–Є–Њ–њ—В–∞—В–Њ–≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є.
–£–≤–µ–ї–Є—З–µ–љ–Є–µ —З–Є—Б–ї–∞ –Ь–≠–Ы –Є –∞—В—А–Њ—Д–Є—П –≤–Њ—А—Б–Є–љ–Њ–Ї –љ–µ —П–≤–ї—П—О—В—Б—П –њ–∞—В–Њ–≥–љ–Њ–Љ–Њ–љ–Є—З–љ—Л–Љ–Є —В–Њ–ї—М–Ї–Њ –і–ї—П –У–¶. –°—Е–Њ–і–љ—Л–µ –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Љ–Њ–≥—Г—В —В–∞–Ї–ґ–µ –≤—Л–Ј—Л–≤–∞—В—М –Њ—Б—В—А—Л–µ –Ї–Є—И–µ—З–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є, –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–Є–µ —Б–ї–Є–Ј–Є—Б—В—Г—О –Њ–±–Њ–ї–Њ—З–Ї—Г —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є. –Э–µ–Ї–Њ—В–Њ—А—Л–µ –ї—О–і–Є –Љ–Њ–≥—Г—В –Є–Љ–µ—В—М –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є –і–µ—В–µ—А–Љ–Є–љ–Є—А–Њ–≤–∞–љ–љ—Г—О –њ–Њ–≤—Л—И–µ–љ–љ—Г—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –љ–µ –Ї –≥–ї—О—В–µ–љ—Г, –∞ –Ї –і—А—Г–≥–Є–Љ –±–µ–ї–Ї–∞–Љ, –љ–∞–њ—А–Є–Љ–µ—А, –Ї —Б–Њ–µ, –Љ—П—Б—Г –Є–љ–і–µ–є–Ї–Є –Є–ї–Є —В—Г–љ—Ж–∞. –Р—В—А–Њ—Д–Є—П –≤–Њ—А—Б–Є–љ–Њ–Ї –Є –≥–Є–њ–µ—А–њ–ї–∞–Ј–Є—П –Ї—А–Є–њ—В –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г –љ–µ–Ї–Њ—В–Њ—А—Л—Е –±–Њ–ї—М–љ—Л—Е —Б –і–µ—Д–Є—Ж–Є—В–Њ–Љ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤.
–Ф–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј –У–¶ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—М —Б–Њ –≤—Б–µ–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є, –њ—А–Њ—П–≤–ї—П—О—Й–Є–Љ–Є—Б—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –і–Є–∞—А–µ–µ–є –Є —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –Љ–∞–ї–∞–±—Б–Њ—А–±—Ж–Є–Є.
–Т –Њ—Б–љ–Њ–≤—Г –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ––і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є—Е –Ї—А–Є—В–µ—А–Є–µ–≤ –У–¶ –і–Њ–ї–ґ–µ–љ –±—Л—В—М –њ–Њ–ї–Њ–ґ–µ–љ –∞–љ–∞–ї–Є–Ј –±–Є–Њ–њ—В–∞—В–Њ–≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є. –Ю—Б–Њ–±–µ–љ–љ–Њ —В—А—Г–і–љ—Л–µ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–µ –Ј–∞–Ї–ї—О—З–µ–љ–Є—П –Ї–∞—Б–∞—О—В—Б—П —А–∞–љ–љ–Є—Е –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Ї—А–Є—В–µ—А–Є–µ–≤ – I –Є II —Б—В–∞–і–Є–є –њ–Њ –Ь–∞—А—И—Г. –Ъ—А–Є—В–µ—А–Є–Є –Ь–∞—А—И–∞ –Њ—Б–Њ–±–µ–љ–љ–Њ —Ж–µ–љ–љ—Л –њ—А–Є –Є–љ—В–µ—А–њ—А–µ—В–∞—Ж–Є–Є –±–Є–Њ–њ—Б–Є–Є —Г –±–Њ–ї—М–љ—Л—Е, –Ї–Њ–≥–і–∞ —А–µ–Ј—Г–ї—М—В–∞—В—Л —Б–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —В–µ—Б—В–Њ–≤ –љ–µ —Б–Њ–≤–њ–∞–і–∞—О—В —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є –љ–∞–±–ї—О–і–µ–љ–Є—П–Љ–Є.
–Ы–µ—З–µ–љ–Є–µ
–Р–≥–ї—О—В–µ–љ–Њ–≤–∞—П –і–Є–µ—В–∞. –Ю—Б–љ–Њ–≤–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –ї–µ—З–µ–љ–Є—П —Ж–µ–ї–Є–∞–Ї–Є–Є —П–≤–ї—П–µ—В—Б—П —Б—В—А–Њ–≥–Њ–µ –њ–Њ–ґ–Є–Ј–љ–µ–љ–љ–Њ–µ —Б–Њ–±–ї—О–і–µ–љ–Є–µ –Р–У–Ф. –Ш–Ј –њ–Є—Й–µ–≤–Њ–≥–Њ —А–∞—Ж–Є–Њ–љ–∞ –Є—Б–Ї–ї—О—З–∞—О—В –њ—И–µ–љ–Є—Ж—Г, —А–Њ–ґ—М, —П—З–Љ–µ–љ—М –Є –Њ–≤–µ—Б, —В.–µ. —Б–ї–µ–і—Г—О—Й–Є–µ –њ—А–Њ–і—Г–Ї—В—Л: —Е–ї–µ–±, –Љ–∞–Ї–∞—А–Њ–љ–љ—Л–µ –Є–Ј–і–µ–ї–Є—П, –Љ–∞–љ–љ—Г—О, –Њ–≤—Б—П–љ—Г—О –Є –њ—И–µ–љ–Є—З–љ—Г—О –Ї—А—Г–њ—Л. –†–∞–Ј—А–µ—И–∞—О—В –Ї–∞—И–Є –Є–Ј –≥—А–µ—З–љ–µ–≤–Њ–є, —А–Є—Б–Њ–≤–Њ–є, –Ї—Г–Ї—Г—А—Г–Ј–љ–Њ–є –Ї—А—Г–њ. –Э–∞–Ј–љ–∞—З–µ–љ–Є–µ –і–Є–µ—В—Л –Є–Љ–µ–µ—В –Є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ. –Х–µ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ —З–∞—Б—В–Њ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П —Г–ґ–µ –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤–Њ–≥–Њ –Љ–µ—Б—П—Ж–∞. –Ю–і–љ–∞–Ї–Њ —Г –љ–µ–Ї–Њ—В–Њ—А—Л—Е –±–Њ–ї—М–љ—Л—Е –Њ—В—З–µ—В–ї–Є–≤—Л–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –љ–∞—Б—В—Г–њ–∞–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ–Њ–Ј–ґ–µ.
–°–ї–µ–і—Г–µ—В –Њ–±—А–∞—В–Є—В—М –≤–љ–Є–Љ–∞–љ–Є–µ, —З—В–Њ –њ—А–Є —Ж–µ–ї–Є–∞–Ї–Є–Є –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–∞—П –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М –Љ–µ–ґ–і—Г —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ–Љ —Е–ї–µ–±–∞ –Є –Ј–ї–∞–Ї–Њ–≤ –Є —Е–∞—А–∞–Ї—В–µ—А–Њ–Љ —Б—В—Г–ї–∞. –Я–Њ—Н—В–Њ–Љ—Г –±–Њ–ї—М–љ—Л–µ –љ–Є–Ї–Њ–≥–і–∞ –љ–µ —Б–≤—П–Ј—Л–≤–∞—О—В —А–∞–Ј–≤–Є—В–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О —Е–ї–µ–±–∞. –Я–Њ–≤—А–µ–ґ–і–∞—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –≥–ї—О—В–µ–љ–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М –≤—Л—П–≤–ї–µ–љ–Њ —В–Њ–ї—М–Ї–Њ –њ–Њ —Б—В–µ–њ–µ–љ–Є –∞—В—А–Њ—Д–Є–Є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –Є –µ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–Є –њ—А–Є —В—Й–∞—В–µ–ї—М–љ–Њ–Љ —Б–Њ–±–ї—О–і–µ–љ–Є–Є –і–Є–µ—В—Л.
–С–µ–Ј–≥–ї—О—В–µ–љ–Њ–≤–Њ–µ –њ–Є—В–∞–љ–Є–µ – –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є —Б–њ–Њ—Б–Њ–± –ї–µ—З–µ–љ–Є—П —Ж–µ–ї–Є–∞–Ї–Є–Є. –Я–Њ—Н—В–Њ–Љ—Г –љ–µ–Њ–±—Е–Њ–і–Є–Љ —В—Й–∞—В–µ–ї—М–љ—Л–є –Ї–Њ–љ—В—А–Њ–ї—М –Ј–∞ –µ–≥–Њ –Ї–∞—З–µ—Б—В–≤–Њ–Љ. –Ґ—А—Г–і–љ–Њ—Б—В–Є —Б–Њ–±–ї—О–і–µ–љ–Є—П –Р–У–Ф –Њ–±—К—П—Б–љ—П—О—В—Б—П: 1) –љ–µ–Њ—Б–Њ–Ј–љ–∞–љ–љ—Л–Љ –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –і–Є–µ—В—Л –≤ —Б–≤—П–Ј–Є —Б –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ –Љ–∞—А–Ї–Є—А–Њ–≤–Ї–Є –±–µ–Ј–≥–ї—О—В–µ–љ–Њ–≤—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤, 2) –љ–µ–ґ–µ–ї–∞–љ–Є–µ–Љ –±–Њ–ї—М–љ—Л—Е, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤, —Б—В—А–Њ–≥–Њ –њ—А–Є–і–µ—А–ґ–Є–≤–∞—В—М—Б—П –і–Є–µ—В—Л.
–Ь–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–∞—П —В–µ—А–∞–њ–Є—П. –С–Њ–ї—М–љ—Л–Љ –У–≠–Я –њ—А–Є —В—П–ґ–µ–ї–Њ–є –±–µ–ї–Ї–Њ–≤–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Б —Ж–µ–ї—М—О –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –Ї–Њ–ї–ї–Њ–Є–і–љ–Њ––Њ—Б–Љ–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –њ–ї–∞–Ј–Љ—Л –Є –ї–Є–Ї–≤–Є–і–∞—Ж–Є–Є –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–Є–Љ–µ–љ—П—О—В –њ—А–µ–њ–∞—А–∞—В—Л, —Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –±–µ–ї–Њ–Ї (–Ї—А–Њ–≤—М, –њ–ї–∞–Ј–Љ–∞, –∞–ї—М–±—Г–Љ–Є–љ, –њ—А–Њ—В–µ–Є–љ).
–Ы–µ—З–µ–љ–Є–µ –і–Є–∞—А–µ–Є –і–Њ–ї–ґ–љ–Њ –±—Л—В—М –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л–Љ, –≤–Њ–Ј–і–µ–є—Б—В–≤—Г—О—Й–Є–Љ –љ–∞ –≤—Б–µ –Њ—Б–љ–Њ–≤–љ—Л–µ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –µ–µ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П.
–Э–∞–Ј–љ–∞—З–∞—О—В —Г–Љ–µ–љ—М—И–∞—О—Й–Є–µ –Ї–Є—И–µ—З–љ—Г—О –≥–Є–њ–µ—А—Б–µ–Ї—А–µ—Ж–Є—О –≤—П–ґ—Г—Й–Є–µ, –∞–љ—В–Є—Б–µ–њ—В–Є—З–µ—Б–Ї–Є–µ, –Њ–±–≤–Њ–ї–∞–Ї–Є–≤–∞—О—Й–Є–µ, –∞–і—Б–Њ—А–±–Є—А—Г—О—Й–Є–µ –Є –љ–µ–є—В—А–∞–ї–Є–Ј—Г—О—Й–Є–µ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–µ –Ї–Є—Б–ї–Њ—В—Л –њ—А–µ–њ–∞—А–∞—В—Л. –Ъ –љ–Є–Љ –Њ—В–љ–Њ—Б—П—В—Б—П –і–µ—А–Љ–∞—В–Њ–ї, –±–µ–ї–∞—П –≥–ї–Є–љ–∞, —Г–≥–ї–µ–Ї–Є—Б–ї—Л–є –Ї–∞–ї—М—Ж–Є–є, —Б–Љ–µ–Ї—В–∞. –Ф–ї—П —Г–ї—Г—З—И–µ–љ–Є—П –Ї–Є—И–µ—З–љ–Њ–≥–Њ –њ–Є—Й–µ–≤–∞—А–µ–љ–Є—П –љ–∞–Ј–љ–∞—З–∞—О—В —Д–µ—А–Љ–µ–љ—В–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л.
–•–Њ—А–Њ—И–Є–є —Н—Д—Д–µ–Ї—В –Њ–Ї–∞–Ј—Л–≤–∞—О—В –њ—А–Њ–±–Є–Њ—В–Є–Ї–Є. –Я—А–Њ–±–Є–Њ—В–Є–Ї–Є – –њ—А–µ–њ–∞—А–∞—В—Л, –≤ —Б–Њ—Б—В–∞–≤ –Ї–Њ—В–Њ—А—Л—Е –≤—Е–Њ–і—П—В –≤–µ—Й–µ—Б—В–≤–∞ –Љ–Є–Ї—А–Њ–±–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є–µ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –љ–∞ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –Є –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ —А–µ–∞–Ї—Ж–Є–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ —Е–Њ–Ј—П–Є–љ–∞ —З–µ—А–µ–Ј –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є—О –µ–≥–Њ –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞. –Э–Є–ґ–µ –њ–µ—А–µ—З–Є—Б–ї–µ–љ—Л —В—А–µ–±–Њ–≤–∞–љ–Є—П, –њ—А–µ–і—К—П–≤–ї—П–µ–Љ—Л–µ –Ї –њ—А–Њ–±–Є–Њ—В–Є–Ї–∞–Љ.
–≥ –Я–Њ–і–±–Њ—А –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е —И—В–∞–Љ–Љ–Њ–≤ –±–Є—Д–Є–і–Њ–±–∞–Ї—В–µ—А–Є–є.
–≥ –Ш–Ј—Г—З–µ–љ–Є–µ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –Є –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ —И—В–∞–Љ–Љ–Њ–≤ –≤ –њ—А–µ–і–µ–ї–∞—Е –Њ–і–љ–Њ–≥–Њ –≤–Є–і–∞.
–≥ –°–Њ–Ј–і–∞–љ–Є–µ –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б —Г—З–µ—В–Њ–Љ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –Є –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б–Њ—Б—В–∞–≤–∞ –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –Ї–Є—И–µ—З–љ–Є–Ї–∞.
–≥ –°–Њ–≤–µ—А—И–µ–љ—Б—В–≤–Њ–≤–∞–љ–Є–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Д–Њ—А–Љ –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ —Б —Ж–µ–ї—М—О —Г–ї—Г—З—И–µ–љ–Є—П –Њ—А–≥–∞–љ–Њ–ї–µ–њ—В–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤.
–≥ –°–Њ–Ј–і–∞–љ–Є–µ –≤—Л—Б–Њ–Ї–Њ–і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ –љ–∞ –Њ—Б–љ–Њ–≤–µ –ґ–Є–≤—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤, –Є—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ –Є –Є–љ—В–µ—А—Д–µ—А–Њ–љ–Њ–≤ —Б —Н—Д—Д–µ–Ї—В–Њ–Љ –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї—П—Ж–Є–Є.
–≥ –£—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї –і–µ–є—Б—В–≤–Є—О —Б–Њ–ї—П–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Є –ґ–µ–ї—З–Є.
–≥ –°–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Ї –∞–і–≥–µ–Ј–Є–Є (–њ—А–Є–ї–Є–њ–∞–љ–Є—О) –Ї —Б—В–µ–љ–Ї–µ –Ї–Є—И–Ї–Є.
–≥ –°–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Ї —А–∞–Ј–Љ–љ–Њ–ґ–µ–љ–Є—О –≤ –Ї–Є—И–µ—З–љ–Є–Ї–µ.
–≥ –°–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Ї –њ—А–Њ–і—Г–Ї—Ж–Є–Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л—Е —Б—Г–±—Б—В–∞–љ—Ж–Є–є.
–≥ –Р–љ—В–∞–≥–Њ–љ–Є–Ј–Љ –Ї –њ–∞—В–Њ–≥–µ–љ–љ—Л–Љ –±–∞–Ї—В–µ—А–Є—П–Љ.
–≥ –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ—Л–є —Н—Д—Д–µ–Ї—В.
–≠—В–Є–Љ —В—А–µ–±–Њ–≤–∞–љ–Є—П–Љ –Њ—В–≤–µ—З–∞–µ—В –Ы–Є–љ–µ–Ї—Б – –Њ–і–Є–љ –Є–Ј —И–Є—А–Њ–Ї–Њ –Є–Ј–≤–µ—Б—В–љ—Л—Е —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤. –Т —Б–Њ—Б—В–∞–≤ –Ы–Є–љ–µ–Ї—Б–∞ –≤–Ї–ї—О—З–µ–љ—Л –±–Є—Д–Є–і–Њ–±–∞–Ї—В–µ—А–Є–Є, –ї–∞–Ї—В–Њ–±–∞—Ж–Є–ї–ї—Л –Є —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї –Љ–Њ–ї–Њ—З–љ–Њ–Ї–Є—Б–ї–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П. –Я–Њ–Љ–Є–Љ–Њ –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л—Е –≤—Л—И–µ —Б–≤–Њ–є—Б—В–≤, –±–∞–Ї—В–µ—А–Є–Є, –≤—Е–Њ–і—П—Й–Є–µ –≤ —Б–Њ—Б—В–∞–≤ –Ы–Є–љ–µ–Ї—Б–∞, —Г—З–∞—Б—В–≤—Г—О—В –≤ —Б–Є–љ—В–µ–Ј–µ –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т, –†–†, –°, –Ъ, –Х, –Т12 –Є —Д–Њ–ї–Є–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –Ь–Њ–ї–Њ—З–љ–Њ–Ї–Є—Б–ї—Л–µ –±–∞–Ї—В–µ—А–Є–Є —Г—З–∞—Б—В–≤—Г—О—В –≤ –≥–Є–і—А–Њ–ї–Є–Ј–µ –Љ–Њ–ї–Њ—З–љ–Њ–≥–Њ —Б–∞—Е–∞—А–∞ –Є –і—А—Г–≥–Є—Е —Г–≥–ї–µ–≤–Њ–і–Њ–≤, –∞ —В–∞–Ї–ґ–µ –±–µ–ї–Ї–Њ–≤ –Є –ґ–Є—А–Њ–≤. –≠—В–Њ —Б–≤–Њ–є—Б—В–≤–Њ –Ы–Є–љ–µ–Ї—Б–∞ –Њ—Б–Њ–±–µ–љ–љ–Њ –њ–Њ–ї–µ–Ј–љ–Њ –і–ї—П –±–Њ–ї—М–љ—Л—Е —Ж–µ–ї–Є–∞–Ї–Є–µ–є, —В.–Ї. –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Г –љ–Є—Е –≤—Б–µ–≥–і–∞ –≤ —В–Њ–є –Є–ї–Є –Є–љ–Њ–є –Љ–µ—А–µ –љ–∞—А—Г—И–µ–љ–Њ –Ї–Є—И–µ—З–љ–Њ–µ (–Љ–µ–Љ–±—А–∞–љ–љ–Њ–µ) –њ–Є—Й–µ–≤–∞—А–µ–љ–Є–µ.
–≠–Ї—Б–њ–µ—А—В–Є–Ј–∞ —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є, –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –Њ–±–Њ—Б—В—А–µ–љ–Є–є, –њ—А–Њ–≥–љ–Њ–Ј. –Т—Б–µ –±–Њ–ї—М–љ—Л–µ –≤ –њ–µ—А–Є–Њ–і –Њ–±–Њ—Б—В—А–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Ї–Њ—В–Њ—А–Њ–µ –≤—Б–µ–≥–і–∞ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ–Љ —Б–Є–љ–і—А–Њ–Љ–∞ –љ–∞—А—Г—И–µ–љ–љ–Њ–≥–Њ –≤—Б–∞—Б—Л–≤–∞–љ–Є—П II –Є–ї–Є III —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є, —Г—В—А–∞—В–Њ–є —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є, –њ–Њ–і–ї–µ–ґ–∞—В –њ–µ—А–µ–≤–Њ–і—Г –љ–∞ II –≥—А—Г–њ–њ—Г –Є–љ–≤–∞–ї–Є–і–љ–Њ—Б—В–Є —Б—А–Њ–Ї–Њ–Љ –Њ—В 6 –Љ–µ—Б. –і–Њ 1 –≥–Њ–і–∞ –њ–Њ —В—П–ґ–µ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Т –њ–µ—А–Є–Њ–і—Л —Б—В–Њ–є–Ї–Њ–є —А–µ–Љ–Є—Б—Б–Є–Є –Њ–љ–Є –Љ–Њ–≥—Г—В –≤—Л–њ–Њ–ї–љ—П—В—М —А–∞–±–Њ—В—Г, –љ–µ —Б–≤—П–Ј–∞–љ–љ—Г—О —Б —Д–Є–Ј–Є—З–µ—Б–Ї–Є–Љ –љ–∞–њ—А—П–ґ–µ–љ–Є–µ–Љ, –љ–µ—А–≤–љ—Л–Љ–Є –љ–∞–≥—А—Г–Ј–Ї–∞–Љ–Є, –њ–µ—А–µ–≥—А–µ–≤–∞–љ–Є–µ–Љ –Є –њ–µ—А–µ–Њ—Е–ї–∞–ґ–і–µ–љ–Є–µ–Љ, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й—Г—О –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ–Њ—Б—В–Њ—П–љ–љ–Њ–≥–Њ —Б–Њ–±–ї—О–і–µ–љ–Є—П –∞–≥–ї—О—В–µ–љ–Њ–≤–Њ–є –і–Є–µ—В—Л.
–Ю—Б–љ–Њ–≤–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–µ—Ж–Є–і–Є–≤–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —П–≤–ї—П–µ—В—Б—П —Б—В—А–Њ–≥–Њ–µ, –њ–Њ–ґ–Є–Ј–љ–µ–љ–љ–Њ–µ —Б–Њ–±–ї—О–і–µ–љ–Є–µ –∞–≥–ї—О—В–µ–љ–Њ–≤–Њ–є –і–Є–µ—В—Л. –Ф–∞–ґ–µ —Б–ї—Г—З–∞–є–љ–Њ–µ –њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ (0,06–2 –≥/—Б—Г—В.) –≥–ї—О—В–µ–љ–∞ —Б–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П –љ–∞ –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–µ: –Ј–∞–Љ–µ—В–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –Њ–±—К–µ–Љ –Є –≥–ї—Г–±–Є–љ–∞ –Ї—А–Є–њ—В, —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П —З–Є—Б–ї–Њ –Ь–≠–Ы.
–Т—Б–µ –±–Њ–ї—М–љ—Л–µ –љ—Г–ґ–і–∞—О—В—Б—П –≤ –і–Є—Б–њ–∞–љ—Б–µ—А–Є–Ј–∞—Ж–Є–Є –Є –њ—А–Є –њ–Њ–Ї–∞–Ј–∞–љ–Є—П—Е –≤ –њ–Њ–≤—В–Њ—А–љ—Л—Е –Ї—Г—А—Б–∞—Е –њ—А–Њ—В–Є–≤–Њ—А–µ—Ж–Є–і–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П 1–2 —А–∞–Ј–∞ –≤ –≥–Њ–і – –≤ —Г—Б–ї–Њ–≤–Є—П—Е –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—В–і–µ–ї–µ–љ–Є—П. –Ь–љ–Њ–≥–Є–µ –љ—Г–ґ–і–∞—О—В—Б—П –≤ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–Љ –њ—А–Є–µ–Љ–µ –њ–Њ–ї–Є—Д–µ—А–Љ–µ–љ—В–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б —Ж–µ–ї—М—О –Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є –љ–∞—А—Г—И–µ–љ–љ–Њ–≥–Њ –њ–Є—Й–µ–≤–∞—А–µ–љ–Є—П –Є –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤.
–Я—А–Њ–≥–љ–Њ–Ј –њ—А–Є –У–¶ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є –њ—А–Є —Г—Б–ї–Њ–≤–Є–Є –њ–Њ–ґ–Є–Ј–љ–µ–љ–љ–Њ–≥–Њ —Б–Њ–±–ї—О–і–µ–љ–Є—П –∞–≥–ї—О—В–µ–љ–Њ–≤–Њ–є –і–Є–µ—В—Л. –Э–µ–њ–Њ–ї–љ–Њ–µ —Б–Њ–±–ї—О–і–µ–љ–Є–µ –і–Є–µ—В—Л –≤–µ–і–µ—В –Ї –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—О –±–Њ–ї–µ–Ј–љ–Є –Є —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —А–Є—Б–Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є —П–Ј–≤–µ–љ–љ–Њ–≥–Њ –µ—О–љ–Є—В–∞ –Є –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Њ–њ—Г—Е–Њ–ї–µ–є –Ї–Є—И–µ—З–љ–Є–Ї–∞.
–С–Њ–ї—М–љ—Л–µ –і–Њ–ї–ґ–љ—Л –љ–∞—Е–Њ–і–Є—В—М—Б—П –њ–Њ–і –і–Є—Б–њ–∞–љ—Б–µ—А–љ—Л–Љ –љ–∞–±–ї—О–і–µ–љ–Є–µ–Љ –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–∞.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Mazzarella G, Maglio M, Paparo F, et al. An immunodominant DQ8 restricted gliadin peptide activates small intestinal immune response in in vitro cultured mucosa from HLA–DQ8 positive but not HLA–DQ8 negative coeliac patients Gut 2003;52:57–62
2. –Я–∞—А—Д–µ–љ–Њ–≤ –Р.–Ш., –Ъ—А—Г–Љ—Б –Ы.–Ь., –°–∞–±–µ–ї—М–љ–Є–Ї–Њ–≤–∞ –Х.–Р. –°–Њ–≤—А–µ–Љ–µ–љ–љ–∞—П –Ї–Њ–љ—Ж–µ–њ—Ж–Є—П, –і–µ—Д–Є–љ–Є—Ж–Є—П –Є –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П —Ж–µ–ї–Є–∞–Ї–Є–Є. –Ь–∞—В–µ—А–Є–∞–ї—Л V —Б—К–Ј–і–∞ –љ–∞—Г—З–љ–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Њ–≤ –†–Њ—Б—Б–Є–Є. –Ь.: –Р–љ–∞—Е–∞—А—Б–Є—Б, 2005:473–475
3. Gomez J.C., Selvaggio G.S., Viola M. et al. Prevalence of celiac disease in Argentina: screening of an adult population in the La Plata area. Am. J. Gastroenterol. 2001; 96 (9): 2700–2704.
4. Cook H.B., Burt M.J., Collett J.A. et. al. Adult coeliac disease: prevalence and clinical significance. J. Gastroenterol. Hepatol. 2000; 15 (9): 1032–1036.
5. Meloni GF, Dessole S, Vargiu N, et al. The prevalence of coeliac disease in infertility. Hum Reprod 1999;14:2759–2761
6. McCann JP, Nicholls DP, Verzin JA.Adult coeliac disease presenting with infertility. Ulster Med J. 1988;57:88–89
7. Lindh E, Ljunghall S, Larsson K, et al. Screening for antibodies against gliadin in patients with osteoporosis J Intern Med 1992;231:403–406
8. Patterson R.N., Johnston S.D. Iron deficiency anemia: are the British Society of Gastroenterology guidelines being adhered to? Postgrad. Med. J.; 2003;79 (930):226–228
9. Alonso Cotoner C, Casellas Jorda F, Chicharro Serrano ML, Iron deficiency: not always blood losses An. Med. Interna.; 2003;20(5):227–231
10. Murray J.A.Celiac disease in patients with an affected member, type 1 diabetes, iron–deficiency, or osteoporosis? Gastroenterology, 2005;128 (4):147.
11. Marsh MN. Mucosal pathology in gluten sensitivity. In: Marsh MN, ed. Coeliac disease. Oxford: Blackwell Scientific, 1992:136–191












