Нарушение всасывания ЖК в тонкой кишке может быть первичным (врожденным) и вторичным (приобретенным). Врожденное нарушение всасывания ЖК встречается редко. Вторичные нарушения развиваются при болезни Крона и резекции подвздошной кишки. Избыточное поступление желчи в кишечник возможно при плохой сократительной функции желчного пузыря или после холецистэктомии.
При нарушении функции или отсутствии желчного пузыря всасывание ЖК не нарушено, но асинхронное с пищей поступление их в большом количестве в тонкую кишку в межпищеварительный период возбуждает пропульсивную деятельность и в слепую кишку поступает значительно большее, чем в норме, количество желчи. Детергентное влияние ЖК на слизистую оболочку ободочной кишки ведет к болям в илеоцекальной области и холагенной диарее (ХД) [3].
Таким образом, ХД наиболее выражена при нарушении всасывания ЖК и после резекции подвздошной кишки. Повышение скорости кишечного транзита чаще наблюдается у больных с отсутствием желчного пузыря, при гипокинезии желчного пузыря и гиперкинезии кишечника.
В настоящей работе мы поставили перед собой цель описать ХД как нозологическую форму, отличающуюся от других типов диарей особенностями этиологии, патогенеза, клинической картины и лечения.
Материал и методы
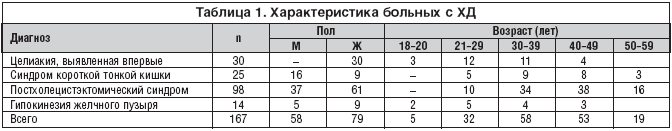
ХД мы наблюдали у 167 больных, перенесших резекцию тонкой кишки, холецистэктомию, а также у лиц с нарушениями сократительной функции желчного пузыря.
Синдром короткой тонкой кишки мы наблюдали у 25 больных. У 11 из них резекция ограничивалась подвздошной кишкой, у 14 – подвздошной и частично тощей кишкой. Причинами оперативных вмешательств явились болезнь Крона (9) и кишечная непроходимость (16).
У 98 больных диарее предшествовала холецистэктомия, выполненная в связи с желчно–каменной болезнью. У 44 больных диарее сопутствовала гипокинезия желчного пузыря. Причиной нарушения его функции у 30 больных являлась целиакия, у 14 – дискинезия желчевыводящих путей. В таблице 1 представлена характеристика больных.
Основным клиническим симптомом у всех больных являлась хроническая диарея. У больных с расширенной резекцией тонкой кишки диарея была особенно обильной и водянистой. После холецистэктомии и при дискинезии желчевыводящих путей преобладал частый жидкий, необильный стул. У больных целиакией стул был обильным, жидким или кашицеобразным. Большинство больных обращали внимание на ярко–желтую или зеленоватую окраску фекалий, характерную для холереи.
В дуоденальном содержимом больных определяли холевую кислоту. В качестве пищевого раздражителя применяли 40% раствор глюкозы или холецистокинин. Глюкозу вводили через дуоденальный зонд, а холецистокинин – в/в в количестве 1 ед/кг м.т.
Для выявления стеатореи измеряли суточный вес кала и содержание в нем жира по методу ван де Камера. В суточном количестве кала исследовали также содержание ионов К+ и Na+ для выяснения потерь их при диарее. Использовали методику плазменной фотометрии.
Контрольную группу составили 10 практически здоровых лиц в возрасте от 17 до 19 лет.
Результаты
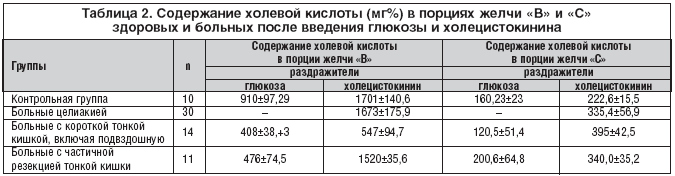
В таблице 2 показаны результаты исследования концентрации холевой кислоты в дуоденальном содержимом больных при использовании в качестве раздражителя 40% раствора глюкозы и холецистокинина. Из таблицы 2 видно, что при применении 40% раствора глюкозы у больных, перенесших резекцию тонкой кишки, содержание холевой кислоты в пузырной порции желчи отчетливо снижено по сравнению с нормой. Причем уровень снижения оказался пропорционален объему резекции тонкой кишки. Так, при норме 910±97,29 мг%, у больных с частичной резекцией кишки концентрация холевой кислоты в желчи составила в среднем 476,6±74,5 мг% (р<0,01), а у больных с обширной резекцией – 408,7±58,39 мг/% (р<0,001). В порции «С» желчи концентрация холевой кислоты у больных с обширной резекцией тонкой кишки была снижена по сравнению с показателями контрольной группы, а при частичной резекции оказалась более чем в 2 раза выше, нежели у больных с обширной резекцией, приближаясь к нормальным показателям. При исследовании дуоденального содержимого, полученного с применением вводимого в/в, установлено, что концентрация холевой кислоты в пузырной порции желчи даже при использовании максимального раздражителя возрастала незначительно, составляя в среднем 547,0±94,7 мг%. В порции «С» желчи после применения холецистокинина отмечено повышение холевой кислоты до нормальных величин (табл. 2). Удалось отметить зависимость между степенью снижения холевой кислоты и величиной полифекалии и стеатореи. При обширной резекции тонкой кишки суточный вес кала составлял в среднем 990 г, а потери жира с калом – 30 г/сут. При частичной резекции суточный вес кала не превышал нормы, а стеаторея составляла 9 г/сут. (норма ≤ 5 г/сут.).
Исследование дуоденального содержимого, проведенного с в/в введением холецистокинина, показало, что концентрация холевой кислоты в пузырной порции желчи даже при использовании максимального раздражителя возрастала незначительно, составляя в среднем 408±58,39мг% в ответ на глюкозу и 547,0±94,7мг% – после инъекции холецистокина. В порции «С» желчи в ответ на применение холецистокинина отмечено повышение холевой кислоты до нормы.
У больных целиакией применение раствора глюкозы не оказывало эффекта на моторную функцию желчного пузыря. В ответ на в/в введение холецистокинина появлялась густая желчь темного цвета с высоким содержанием холевой кислоты: в среднем 1673±175,9 мг/% (норма 1701±140,6 мг/%), составляя у отдельных больных 2600–3320 мг/%. Концентрация холевой кислоты в порции «С» была также повышена по сравнению с контрольной группой (335,4±56,9 и 222,6±15,5 мг% соответственно) при норме 160±23,3 мг% в ответ на глюкозу.
Таким образом, проведенные исследования показали существенное снижение концентрационной функции желчного пузыря и его сократительной способности у обследованных больных по сравнению с нормой.
Отсутствие существенной разницы между секрецией холевой кислоты в пузырной желчи в ответ на пищевой раздражитель и парентеральное введение холецистокинина у больных с обширной резекцией тонкой кишки может свидетельствовать об уменьшении пула ЖК за счет снижения их реабсорбции и повышенных потерь с калом. Косвенным подтверждением этого предположения являются результаты определения экскреции электролитов с калом.
На рисунке 1 показаны результаты исследования ионов К+ и Nа+ в суточном количестве кала у обследованных больных. При исследовании потерь натрия и калия с калом оказалось, что у больных целиакией потери натрия и калия с калом возрастали в равной степени, превышая норму в 3 раза. Натриево–калиевый коэффициент фекалий почти не отличался от такового в контрольной группе. При обширной резекции тонкой кишки (включая подвздошную) потери калия в суточном кале, как и при целиакии, превышали норму в 3 раза, а содержание натрия оказалось в 17 раз выше нормы и в 6 раза выше показателей у больных целиакией. Натриево–калиевый коэффициент увеличивался в 4,5 раза по сравнению с нормой.
Обильные водянистые поносы у больных с обширной резекцией тонкой кишки зависят от увеличения концентрации желчных кислот в толстой кишке, где они тормозят не только всасывание, но и усиливают секрецию воды, хлоридов и иона натрия [2,5].
С учетом установленных выше патогенетических механизмов ХД нами предложено ее комплексное лечение.
Больным назначали диету 4б с повышенным содержанием белка (135 г в сутки) и физиологической нормой жира (100–110 г в сутки). Уменьшение процессов брожения и гниения достигалось специальным подбором продуктов и методов их кулинарной обработки; исключением продуктов, богатых клетчаткой, термической обработкой, измельчением плодов и овощей, удалением соединительной ткани при обработке мяса и птицы и их измельчением. Лечебное питание оказывает отчетливое положительное действие на основные патогенетические механизмы диареи, способствуя снижению кишечной гиперсекреции. Это достигалось ограничением механических и химических стимуляторов кишечной секреции, резким ограничением, а иногда полным исключением из рациона молока, как продукта, богатого лактозой, облегчением процесса переваривания пищевых веществ за счет их термической и механической обработки. Диету 4б назначали до стойкой нормализации стула. При целиакии назначали аглютеновую диету.
С целью адсорбции ЖК в межпищеварительном периоде применяли энтеросорбенты, а также порошки, содержащие белую глину, углекислый кальций и дерматол. Эти вещества обладают также обволакивающим действием и защищают слизистую оболочку тонкой кишки от детергентного действия ЖК.
Для устранения асинхронного с пищей поступления желчи в тонкую кишку больным назначали желчегонные препараты, стимулирующие сократительную функцию желчного пузыря. После стихания диареи рекомендовали продолжать прием желчегонных средств в течение длительного времени (до 1 года).
Для подавления роста микроорганизмов в верхних отделах тонкой кишки и устранения дисбиоза толстой кишки назначали один из антибактериальных препаратов и пробиотики.
Пробиотики – препараты, в состав которых входят вещества микробного происхождения, оказывающие благоприятные эффекты на физиологические функции и биохимические реакции организма хозяина через оптимизацию его микробиологического статуса. Ниже перечислены требования, предъявляемые к пробиотикам:
– подбор перспективных штаммов бифидобактерий;
– изучение бактериальных и биохимических свойств штаммов в пределах одного вида;
– создание пробиотических препаратов с учетом особенностей количественного и качественного состава микрофлоры кишечника;
– совершенствование лекарственных форм пробиотиков с целью улучшения органолептических свойств;
– создание высокодифференцированных пробиотиков на основе живых микроорганизмов, их метаболитов и интерферонов с эффектом иммуномодуляции;
– устойчивость к действию соляной кислоты и желчи;
– способность к адгезии (прилипанию) к стенке кишки;
– способность к размножению в кишечнике
– способность к продукции антимикробных субстанций;
– антагонизм к патогенным бактериям;
– клинически подтвержденный эффект.
Этим требованиям отвечает Линекс – один из широко известных современных пробиотиков. В состав Линекса включены бифидобактерии, лактобациллы и энтерококк молочнокислого происхождения. Помимо перечисленных выше свойств, бактерии, входящие в состав Линекса, участвуют в синтезе витаминов группы В, РР, С, К, Е, В12 и фолиевой кислоты. Молочнокислые бактерии участвуют в гидролизе молочного сахара и других углеводов, а также белков и жиров. Это свойство Линекса особенно полезно для больных целиакией, т.к. известно, что у них всегда в той или иной мере нарушено кишечное (мембранное) пищеварение.
Учитывая особенности распределения микрофлоры на протяжении желудочно–кишечного тракта человека (преобладание лактобактерий и молочнокислого стрептококка в тонкой, а бифидобактерий – в толстой кишке), Линекс обеспечивает поступление «лечебной» микрофлоры в количественно и качественно сбалансированных соотношениях.
Антагонистические свойства Линекса связаны со способностью входящих в его состав микроорганизмов продуцировать молочную и, в меньшей степени, уксусную и пропионовую кислоты. Создаваемая кислая среда (рН внутрикишечного содержимого приближается к 4,0–5,8) является неблагоприятной для развития патогенных и условно–патогенных микроорганизмов.
Выращиванием на средах, содержащих антибиотики или химиотерапевтические средства, были отобраны резистентные штаммы, способные к дальнейшему размножению. Таким образом, Линекс содержит устойчивые к действию антибиотиков (пенициллинам, в т.ч. полусинтетическим, макролидам, цефалоспоринам, фторхинолонам и тетрациклинам) молочнокиcлые бактерии. Это обстоятельство позволяет применять Линекс при необходимости в комбинации с антибиотиками с целью профилактики дисбактериоза. Резистентность полученных штаммов сохраняется при повторной инокуляции в течение 30 поколений и также сохраняется in vivo.
Линекс назначают взрослым и детям старше 12 лет по 2 капсулы 3 раза в сутки, после еды в течение 2–3 месяцев, т.е. до полного прекращения кишечных симптомов.
В период выраженной диареи назначали лоперамид, обладающий свойством увеличивать время транзита кишечного содержимого. У больных с обширной резекцией тонкой кишки в случае диареи, резистентной к указанной выше терапии, назначали октреотид.
Применение такой комплексной терапии способствовало прекращению диареи у всех больных в течение 1–2 недель.
Обсуждение результатов
Полученные нами данные свидетельствуют, что при снижении сократительной функции желчного пузыря возникает ХД. Так, при целиакии сокращения желчного пузыря на пищевой раздражитель полностью отсутствовали. При парентеральном введении максимального раздражителя – холецистокинина выделялась пузырная желчь с высоким содержанием холевой кислоты, что свидетельствовало о выраженной гипокинезии желчного пузыря.
У больных, перенесших резекцию тонкой кишки, содержание всех компонентов желчи в пузырной порции желчи снижено (в большей степени – при обширной резекции тонкой кишки). Применение холецистокинина у больных с обширной резекцией тонкой кишки не приводило к заметному повышению холевой кислоты в пузырной желчи. Резкое снижение ее секреции у больных с обширной резекцией тонкой кишки сопровождалось значительной полифекалией, стеатореей и высокими фекальными потерями натрия, что свидетельствует о связи водной диареи с повышенным выделением ЖК с калом в результате нарушения их реабсорбции.
Наиболее известной причиной расстройства энтерогепатической циркуляции ЖК и развития холагенной диареи является резекция подвздошной кишки или заболевания, сопровождающиеся воспалительным процессом. Отсутствие активной транспортной системы для реабсорбции ЖК у больных, перенесших резекцию подвздошной кишки, влечет за собой значительную потерю их с калом. Присутствие ЖК в толстой кишке становится причиной гиперсекреции воды и электролитов, т.е. развития водной диареи. ХД обычно появляется уже после частичной резекции подвздошной кишки (менее 100 см), хотя у этих больных дефицит ЖК, необходимых для всасывания липидов, еще компенсируется усиленным синтезом их в печени. При более обширных (более 100 см) резекциях подвздошной кишки развивается абсолютная недостаточность ЖК вследствие прерванной энтерогепатической циркуляции, что является причиной стеатореи. В этих случаях возникает «жирнокислотная диарея».
Менее известна ХД, обусловленная патологией билиарной системы: гипомоторикой желчного пузыря, дискинезиями, связанными с анатомическими изменениями (перетяжка желчного пузыря, изогнутая форма и т.д ), холецистэктомией, гипокинезией желчного пузыря при целиакии. Патогенез диареи в этих случаях включает ряд факторов. При гипомоторной дискинезии, свойственной целиакии, анатомических изменениях желчного пузыря или его удалении возникает асинхронность поступления пищи и желчи в просвет тонкой кишки. Недостаточное поступление желчи в момент пищеварения в просвет двенадцатиперстной кишки способствует нарушению внешнесекреторной функции поджелудочной железы и, как следствие, возникновению диареи. Напротив, при попадании с пищей сильного возбудителя сокращения желчного пузыря, а при отсутствии его – гиперсекреции желчи, избыток ЖК, не успевающих реабсорбироваться в подвздошной кишке, вызывает диарею. Нередко в этих случаях возникают боли в правой подвздошной области, при колоноскопии можно видеть наличие желчи в слепой кишке [2].
В таблице 3 показаны причины избыточного поступления ЖК в толстую кишку и варианты нарушения их энтерогепатической циркуляции. Этими причинами могут быть нарушение всасывания ЖК в подвздошной кишке, асинхронное с пищей поступление их в кишку и ускоренный пассаж химуса по тонкой кишке.
Таким образом, описанная в настоящей работе холагенная диарея отличается от известных типов хронической диареи рядом особенностей. В ее этиологии и патогенезе ведущую роль играет повышенное поступление желчи в толстую кишку. Присутствие большого количества желчи в стуле сопряжено с появлением некоторых, свойственных только ей, симптомов. В лечении больных холагенной диареей следует отдавать предпочтение препаратам, связывающим избыток ЖК в толстой кишке.
Выводы
1. Холагенная диарея (ХД) развивается после обширной резекции тонкой кишки, включая подвздошную, у больных с воспалительными заболеваниями подвздошной кишки, дискинезиях желчевыводящих путей и после холецистэктомии.
2. Патогенетическим механизмом развития ХД является повышенное поступление желчи в толстую кишку, где она тормозит всасывание и усиливает секрецию воды и электролитов, вызывая гиперсекреторную диарею.
3. Основными клиническими симптомами ХД являются частый водянистый стул с ярко–желтой или зеленоватой окраской фекалий (холерея) и боли в правой подвздошной области при поступлении большого количества желчи в слепую кишку.
4. ХД, развивающуюся после холецистэктомии, можно рассматривать, как отдельный вариант постхолецистэктомического синдрома.
5. В лечении ХД наряду с кишечными антисептиками, пробиотиками и регуляторами моторики необходимо обязательно применять препараты, связывающие избыток ЖК в толстой кишке, и стимуляторы сократительной функции желчного пузыря.


Литература
1. Binder H. J. Causes of Chronic Diarrhea NEJM –2006;355:236–239
2. Крумс Л.М. Патогенетическая терапия хронических болезней тонкой кишки. Автореф. докт.дисс., Москва 1989 г, 51 с.
3. Парфенов. А.И. Болезни илеоцекальной области. Москва, 2005г., 271 c.
4. Парфенов А.И., Екисенина Н.И., Крумс Л.М.. Лечение хронических заболеваний тонкой кишки. Клин.мед. 1991:10:105–111.
5. Caprili R., Latella Q., Viscido F. Chronic diarrhea. In: Chronic gastrointestinal disorders. Milano, Italy 2000 P.295–303.
6. Gerok W. Pathophysiology of chronic diarrhea. Schweden Rundsch Med.Prax. 2000;12 (89):1635–41.












