Основным клиническим проявлением инертной толстой кишки (ИТК) является хронический запор (ХЗ). Распространенность ИТК среди населения находится, по данным разных авторов, в пределах от 4% до 20% [1, 2]. Причиной медленного транзита служат структурные, механические, метаболические и кортиковисцеральные влияния на толстую кишку. Особенно тяжелые нарушения транзита развиваются при болезни Паркинсона, псевдообструкции, обусловленной системной нейропатией и селективной нейропатией толстой кишки.
При ИТК наблюдается снижение как фоновой моторики, так и стимулированной — после пищевой нагрузки и других раздражителей. В зависимости от типа ответа толстой кишки на стимулирующие воздействия мы выделяем три степени нарушения моторики при этом заболевании.
Степени нарушения моторной функции при ИТК [3]
Длительный анамнез, отсутствие эффекта от использования пищевых добавок в адекватных количествах, слабительных средств и необходимость систематического очищения кишечника с помощью клизм дают все основания предполагать ИТК. Следует выяснить количество пищевых волокон и жидкости, потребляемых больными, а также режим питания. Клинические диагностические критерии ИТК сформулированы Римским консенсусом в 2006 г. [4].
Диагностические критерии ИТК в соответствии с Римским консенсусом 2006 г. [4]
Пациент должен соответствовать критериям диагностики функционального запора (Рим III, 2006 г.). Любые 2 из 6 пунктов:
1. Натуживание при дефекации.
2. «Овечий» или твердый стул.
3. Ощущение неполноценности дефекации.
4. Ощущение аноректальной обструкции (блокады).
5. Помощь при дефекации руками.
6. Менее 3 дефекаций в неделю.
Критерии 1, 2, 3, 4, 5 присутствуют не менее чем в 25% дефекаций, появились не ранее чем 6 мес. назад и проявляются последние 3 мес.
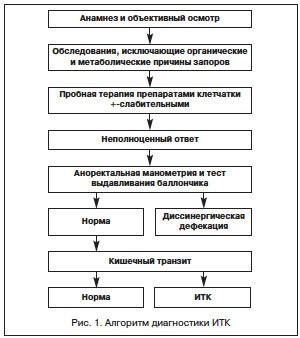
Алгоритм обследования должен включать функциональные исследования кишечника: аноректальную манометрию (АРМ), тест выдавливания баллончика и определение времени кишечного транзита с помощью рентгеноконтрастной
При сомнительном результате АРМ предлагается проведение дефекографии.
Основным функциональным методом, подтверждающим ИТК, является определение времени транзита. Исследование кишечного транзита проводится с помощью рентгеноконтрастной
Традиционно сложившийся взгляд на связь запоров с недостатком клетчатки [4] является непреложным условием увеличения потребления клетчатки в качестве начальной терапии хронических запоров любой этиологии. Нерастворимые волокна, такие как пшеничные отруби, как полагают, уменьшают время кишечного транзита, тем самым увеличивая частоту стула [5]. Растворимые волокна, например семена подорожника, растворяясь в воде, увеличивают объем и частоту стула [6]. Проведенные в последующие десятилетия многочисленные исследования,
Цель настоящей работы — установление частоты ИТК и эффективности пикосульфата натрия (Гуттасила) у больных первичными ХЗ.
Материал и методы
Проведено обследование 132 больных первичным ХЗ в возрасте от 18 до 89 лет, поступивших на лечение в МКНЦ. Критериями исключения являлись вторичные ХЗ и психические заболевания. Среди больных преобладали женщины — 121 (91,6%). Пациенты соответствовали критериям функционального запора (ФЗ) (Римские критерии III). Частота стула составляла у всех менее
Всем больным проводили проктологическое исследование, колонофиброскопию, эзофагогастродуоденоскопию (ЭГДС) и ультразвуковое исследование органов брюшной полости. Выполняли также тест выдавливания баллона. В прямую кишку вводили баллончик, который наполняли водой до объема 50 мл, после чего пациенту предлагалось вытолкнуть его в течение 5 мин. Также выполняли АРМ с помощью
Результаты и обсуждение
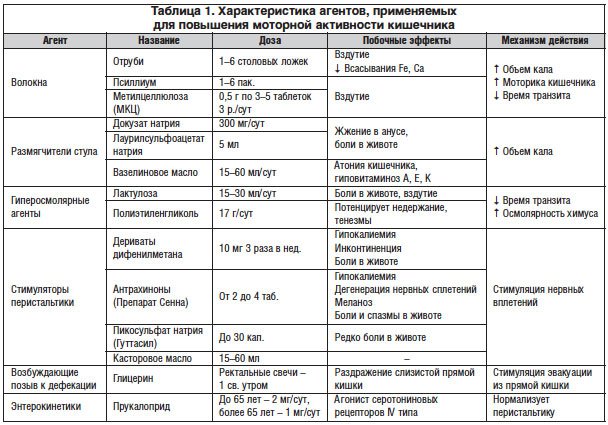
Результаты исследования показаны на рисунке 2. У 51 из 132 (39%) больных время транзита по толстой кишке и показатели АРМ не выходили за пределы нормы.
Поэтому в соответствии с Римскими критериями III (2006 г.) у них установлен первый тип ХЗ — функциональный запор, связанный с дискинезией кишечника. У 59 (45%) больных ХЗ выявлена ДД,
Всем пациентам с
Пациентам с выявленной ДД, помимо общих рекомендаций по лечению и профилактике запоров, предлагали курс
Для лечения 21 пациента с ИТК, помимо общих рекомендаций по диете, водной нагрузке и приему клетчатки, с целью стимуляции перистальтики к терапии назначали пикосульфат натрия (Гуттасил) в начальной дозе 15 кап./сут. В дальнейшем пациент мог менять дозу препарата на 2–5 кап./сут, добиваясь нормального стула. Максимальная доза составляла 27 капель.
Пикосульфат натрия (Гуттасил) стимулирует рецепторы слизистой оболочки кишечника, усиливает перистальтику. Активная форма препарата, образующаяся путем гидролиза под влиянием кишечных микроорганизмов, непосредственно возбуждает нервные структуры кишечной стенки, в результате ускоряется продвижение кишечного содержимого, уменьшается всасывание электролитов и воды. Слабительный эффект наступает через 6–12 ч после приема. При приеме внутрь не всасывается из ЖКТ и не подвергается
Для достижения ежедневного стула 5 пациентам потребовалось 20 капель (9–25 кап.), у 5 больных на максимальной дозе 27 кап. в сутки самостоятельный стул отмечался через каждые 2–3 дня. У 2 пациентов на фоне приема максимальной дозы 27 кап. частота стула сохранялась менее 3 раз в неделю, что послужило основанием для назначения прукалоприда в дозе 2 мг/сут.
Всем больным требовался систематический прием Гуттасила для сохранения нормального стула. В дальнейшем 4 пациентам удалось уменьшить дозу до 15 кап. в сутки.
Таким образом, применение Гуттасила у 14 пациентов с ИТК и отсутствием самостоятельного стула позволило добиться ежедневной дефекации, а у 5 пациентов — 1 раз в 2–3 дня. Приводим одно из клинических наблюдений.
Больная М., 67 лет, поступила в отделение заболеваний кишечника МКНЦ
Запорами страдает с 20 лет, последние 6 лет стул только с помощью слабительных препаратов и очистительных клизм. В январе 2014 г. госпитализирована в районную больницу в связи с болями в животе и отсутствием самостоятельного стула. При ирригоскопии патологии не выявлено, при ЭГДС — поверхностный гастрит. Проводилась терапия слабительными препаратами, на фоне которых запоры сохранялись. Рекомендовано дальнейшее обследование в МКНЦ.
Данные осмотра: общее состояние удовлетворительное. Телосложение нормальное. Рост 158 см. Вес 78 кг. ИМТ — 31,2 кг/м2, ожирение
Клинический и биохимический анализы крови без патологических значений. УЗИ органов брюшной полости: деформация желчного пузыря. Ректороманоскопия и колоноскопия с осмотром 15 см дистального отдела подвздошной кишки — без патологии.
По результатам АРМ, данных, свидетельствующих о ДД и других нарушениях дефекации, не получено. Для оценки моторики толстой кишки проведено исследование кишечного транзита с помощью рентгеноконтрастной
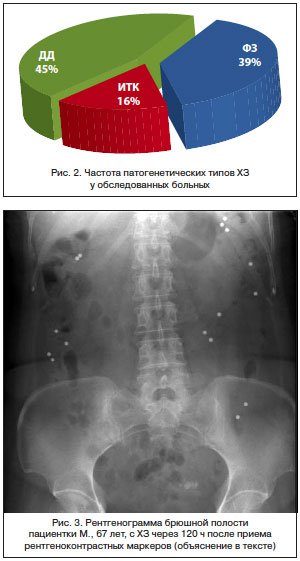
Пациентке назначен пикосульфат натрия (Гуттасил) в дозе 15 кап./сут. В процессе лечения она постепенно увеличила дозу до 25 кап./сут. На фоне поддерживающей терапии у нее сохраняется самостоятельный стул 2–3 раза в неделю, без дополнительного использования очистительных клизм.
Таким образом, для лечения пациентки М. с патогенетически обоснованной ИТК терапия пикосульфатом натрия (Гуттасил) оказалась достаточно эффективной.
Заключение
Диагноз ИТК должен устанавливаться в последовательности предлагаемого алгоритма с соблюдением Римских критериев. Ведущую роль в диагностике ИТК играют функциональные методы исследования — АРМ, тест выдавливания баллончика и определение времени транзита по толстой кишке с помощью рентгеноконтрастных маркеров. В лечении ИТК основное значение принадлежит энтерокинетикам, но определенную роль могут играть и слабительные, стимулирующие перистальтику (Гуттасил), а также гиперосмолярные агенты и пищевые волокна.












