–Р–ї–Ї–Њ–≥–Њ–ї—М–љ–∞—П –Є –љ–µ–∞–ї–Ї–Њ–≥–Њ–ї—М–љ–∞—П –ґ–Є—А–Њ–≤–∞—П –±–Њ–ї–µ–Ј–љ—М –њ–µ—З–µ–љ–Є (–Э–Р–Ц–С–Я) –Ј–∞–љ–Є–Љ–∞–µ—В –≤–∞–ґ–љ–Њ–µ –Љ–µ—Б—В–Њ –≤ —Б—В—А—Г–Ї—В—Г—А–µ –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –њ—А–Є—З–µ–Љ –љ–µ —В–Њ–ї—М–Ї–Њ –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є, –љ–Њ –Є –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є, –Є –Њ–±—Й–µ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –≤ —Ж–µ–ї–Њ–Љ. –Т–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –Э–Р–Ц–С–Я –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–Њ —Б —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ю—В–ї–Њ–ґ–µ–љ–Є–µ –ї–Є–њ–Є–і–Њ–≤ –≤ –њ–µ—З–µ–љ–Є —П–≤–ї—П–µ—В—Б—П –њ–µ—А–≤—Л–Љ —Н—В–∞–њ–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –±–Њ–ї–µ–Ј–љ–Є –Є –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї —Н—Д—Д–µ–Ї—В—Г –ї–Є–њ–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є, –Є–љ–Є—Ж–Є–∞—Ж–Є–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—О –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П [1].
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –±–Њ–ї—М—И–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ –њ—А–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –Э–Р–Ц–С–Я —Г–і–µ–ї—П–µ—В—Б—П —Б–≤—П–Ј–Є —Б –Є–Ј–±—Л—В–Њ—З–љ—Л–Љ –≤–µ—Б–Њ–Љ, –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є–µ–є, –Є–љ—Б—Г–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М—О, –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ, —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ (–°–Ф) 2-–≥–Њ —В–Є–њ–∞. –°—Е–Њ–ґ–Є–µ –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–µ—З–µ–љ–Є –Љ–Њ–≥—Г—В –љ–∞–±–ї—О–і–∞—В—М—Б—П –њ—А–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –≥–µ–њ–∞—В–Є—В–∞—Е, –Њ—Б—В—А—Л—Е –∞–ї–Ї–Њ–≥–Њ–ї—М–љ—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П—Е –њ–µ—З–µ–љ–Є, —Б–µ–њ—В–Є—З–µ—Б–Ї–Є—Е –Є —Н–љ—В–µ—А–Њ–≥–µ–љ–љ—Л—Е –≥–µ–њ–∞—В–Є—В–∞—Е.
–Т–µ–і—Г—Й–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Э–Р–Ц–С–Я —П–≤–ї—П—О—В—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –≤–Њ–Ј—А–∞—Б—В–∞, –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–є —Б–Є–љ–і—А–Њ–Љ –Є –µ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л, –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–µ –Њ–ґ–Є—А–µ–љ–Є–µ, –≥–Є–њ–µ—А—В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–µ–Љ–Є—П, –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П, –°–Ф, –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П. –Ъ—А–Њ–Љ–µ —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л—Е –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–є –Њ–± —Н—В–Є–Њ–ї–Њ–≥–Є–Є –Є –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –Э–Р–Ц–С–Я –њ–Њ—П–≤–Є–ї–Њ—Б—М –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ –љ–Њ–≤—Л—Е —Б–≤–µ–і–µ–љ–Є–є –Њ –Ј–≤–µ–љ—М—П—Е –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞, –≤–ї–Є—П—О—Й–Є—Е –љ–∞ —В–µ—З–µ–љ–Є–µ –Є –њ—А–Њ–≥–љ–Њ–Ј –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П [2].
–Ґ–µ—Б–љ–∞—П —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л –Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –њ–µ—З–µ–љ–Є –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ–Љ —А–∞–Ј–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ–Є, —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–µ –Њ–і–љ–Њ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Ї–Њ—В–Њ—А—Л—Е –њ—А–Є–≤–Њ–і–Є—В –Ї —Г—Е—Г–і—И–µ–љ–Є—О —В–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Њ–±–µ–Є—Е —Б–Є—Б—В–µ–Љ –Њ—А–≥–∞–љ–Њ–≤. –Я—А–Є –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –њ–Њ—А–∞–ґ–µ–љ–Є–µ –њ–µ—З–µ–љ–Є –Љ–Њ–ґ–µ—В –±—Л—В—М –Ї–∞–Ї –њ–µ—А–≤–Є—З–љ—Л–Љ (—А–∞–Ј–≤–Є–≤–∞—О—Й–Є–Љ—Б—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ), —В–∞–Ї –Є –≤—В–Њ—А–Є—З–љ—Л–Љ (–≤—Б–ї–µ–і—Б—В–≤–Є–µ —Г—Е—Г–і—И–µ–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –Њ—В—Б—Г—В—Б—В–≤–Є—П –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є–Є, –Њ–ґ–Є—А–µ–љ–Є—П, –°–Ф) [3, 4].
–Я—А–Є —А–∞—Б—Б–Љ–Њ—В—А–µ–љ–Є–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є —А—П–і –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є –Њ–±—А–∞—Й–∞—О—В –≤–љ–Є–Љ–∞–љ–Є–µ –љ–∞ —В–Њ, —З—В–Њ —Б—А–µ–і–Є –µ–≤—А–Њ–њ–µ–є—Ж–µ–≤ —Б —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є —З–∞—Й–µ –≤—Б—В—А–µ—З–∞—О—В—Б—П –љ–∞—А—Г—И–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Є –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–µ–є —Б–Є—Б—В–µ–Љ—Л –Є –њ—А–Є–Љ–µ—А–љ–Њ –≤ 1,5 —А–∞–Ј–∞ —З–∞—Й–µ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –ґ–µ–ї—З–љ–Њ–Ї–∞–Љ–µ–љ–љ–∞—П –±–Њ–ї–µ–Ј–љ—М (–Ц–Ъ–С). –Ґ–∞–Ї, —Б—А–µ–і–Є –µ–≤—А–Њ–њ–µ–є—Ж–µ–≤ —Б—В–∞—А—И–µ 70 –ї–µ—В —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Ц–Ъ–С —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ–Ї–Њ–ї–Њ 14%, —З—В–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ —Б—А–µ–і–љ–Є—Е –Ј–љ–∞—З–µ–љ–Є–є –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є. –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ—Б—В–∞–≤–ї—П—О—В –Љ—Г–ґ—З–Є–љ—Л —Б —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є (–°–°–Ч). –≠—В–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤—Л–Ј–≤–∞–љ—Л –≤—В–Њ—А–Є—З–љ–Њ–є –Э–Р–Ц–С–Я, –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ–Љ –ї–Є–њ–Є–і–Њ–≤ –≤ –њ–µ—З–µ–љ–Є –Є —Г—Е—Г–і—И–µ–љ–Є–µ–Љ –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б–Њ—Б—В–∞–≤–∞ —Б–Є–љ—В–µ–Ј–Є—А—Г–µ–Љ–Њ–є –ґ–µ–ї—З–Є. –Ш–Ј–±—Л—В–Њ—З–љ–Њ–µ –љ–∞—Б—Л—Й–µ–љ–Є–µ –ґ–µ–ї—З–Є —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–Њ–Љ (–•–°) –њ—А–Є–≤–Њ–і–Є—В –Ї –µ–µ –Ї—А–Є—Б—В–∞–ї–ї–Є–Ј–∞—Ж–Є–Є –Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –Ї–∞–Љ–љ–µ–є. –£—Б–Є–ї–µ–љ–Є–µ —Б–µ–Ї—А–µ—Ж–Є–Є –•–° –≤ –ґ–µ–ї—З—М —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ —Б–µ–Ї—А–µ—Ж–Є–Є –ґ–µ–ї—З–љ—Л—Е –Ї–Є—Б–ї–Њ—В –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, —А–∞–Ј–≤–Є—В–Є–µ–Љ –±–Є–ї–Є–∞—А–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Ф–∞–љ–љ—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—О –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ [5, 6].
–Ґ–µ—З–µ–љ–Є–µ –Э–Р–Ц–С–Я —Г –ґ–µ–љ—Й–Є–љ –Є–Љ–µ–µ—В —А—П–і –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Д–Њ–љ–∞. –Э–∞–ї–Є—З–Є–µ —Б—В–µ–∞—В–Њ–Ј–∞ –Є–ї–Є —Б—В–µ–∞—В–Њ–≥–µ–њ–∞—В–Є—В–∞ —Г –ґ–µ–љ—Й–Є–љ –≤ –Љ–µ–љ–Њ–њ–∞—Г–Ј–µ –Њ—Б–ї–Њ–ґ–љ—П–µ—В —В–µ—З–µ–љ–Є–µ –°–°–Ч, –≤ 3 —А–∞–Ј–∞ –њ–Њ–≤—Л—И–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Є —Г—Е—Г–і—И–∞–µ—В –њ—А–Њ–≥–љ–Њ–Ј. –Т –њ–µ—А–Є–Њ–і –Љ–µ–љ–Њ–њ–∞—Г–Ј—Л —А–∞–Ј–≤–Є—В–Є–µ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є –Є–љ—Б—Г–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –љ–∞ —Д–Њ–љ–µ —Б–љ–Є–ґ–µ–љ–љ–Њ–є –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ј–∞—З–∞—Б—В—Г—О –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј–≤–Є—В–Є—О —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ–ї–Є–Ї–Є—Б—В–Њ–Ј–љ—Л—Е —П–Є—З–љ–Є–Ї–Њ–≤. –≠—В–Њ –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—О –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є –і–∞–ї—М–љ–µ–є—И–µ–Љ—Г —Г—Е—Г–і—И–µ–љ–Є—О —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–µ—З–µ–љ–Є. –Я—А–Є–Љ–µ—А–љ–Њ —Г 2/3 —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–µ—В—Б—П –љ–µ–∞–ї–Ї–Њ–≥–Њ–ї—М–љ—Л–є —Б—В–µ–∞—В–Њ–≥–µ–њ–∞—В–Є—В. –†–∞–Ј–≤–Є—В–Є–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є —Б–µ—А–і—Ж–∞ –Є –∞–Њ—А—В—Л —Г –ґ–µ–љ—Й–Є–љ –≤ –Љ–µ–љ–Њ–њ–∞—Г–Ј–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ—А–Є–Љ–µ—А–љ–Њ –≤ 1,8 —А–∞–Ј–∞ —З–∞—Й–µ [Ramilli, 2009]. –†–∞–Ј–≤–Є—В–Є–µ –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Љ–Њ–ґ–µ—В –≤–Њ–Ј–і–µ–є—Б—В–≤–Њ–≤–∞—В—М –љ–∞ —Б—В—А—Г–Ї—В—Г—А—Г —В—А–Њ–Љ–±–∞, —З—В–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —З–∞—Б—В–Њ—В—Г —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є [Hickman, 2009]. –Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –Љ–µ–љ–Њ–њ–∞—Г–Ј–∞ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П –Ї–∞–Ї –љ–Њ–≤—Л–є –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–є –њ—А–µ–і–Є–Ї—В–Њ—А —А–∞–Ј–≤–Є—В–Є—П –°–°–Ч [7].
–Ъ—А–Њ–Љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ—Л—Е –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е —Б–≤—П–Ј–µ–є –Љ–µ–ґ–і—Г –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –њ–µ—З–µ–љ–Є –Є —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–ґ–љ–Њ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М –Ї–∞–Ї —Б–Њ—З–µ—В–∞–љ–љ—Г—О –њ–∞—В–Њ–ї–Њ–≥–Є—О, —Б—Г—Й–µ—Б—В–≤—Г–µ—В —Ж–µ–ї—Л–є —А—П–і —Д–Њ–љ–Њ–≤—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Ґ–∞–Ї, –љ–∞–ї–Є—З–Є–µ –∞–ї–Ї–Њ–≥–Њ–ї—М–љ–Њ–є –Є–ї–Є –љ–µ–∞–ї–Ї–Њ–≥–Њ–ї—М–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –њ–µ—З–µ–љ–Є –љ–µ –Є—Б–Ї–ї—О—З–∞–µ—В –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ —Г –њ–∞—Ж–Є–µ–љ—В–∞ –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–µ—З–µ–љ–Є, —З—В–Њ —З–∞—Б—В–Њ –Љ–Њ–ґ–љ–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞—В—М —Г –ґ–µ–љ—Й–Є–љ –Љ–Њ–ї–Њ–і–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞. –Я—А–Є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –њ–µ—З–µ–љ–Є —В–∞–Ї–ґ–µ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–ї–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П, –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –≤–Є—А—Г—Б–љ—Л—Е –≥–µ–њ–∞—В–Є—В–Њ–≤. –Э–∞ —Д–Њ–љ–µ –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Є–ї–Є –±–Њ–ї–µ–Ј–љ–µ–є —Б –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В—М—О, –љ–∞–њ—А–Є–Љ–µ—А, –≥–µ–Љ–Њ—Е—А–Њ–Љ–∞—В–Њ–Ј–Њ–≤, –љ–∞—А—Г—И–µ–љ–Є–є –њ–Є–≥–Љ–µ–љ—В–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞, –і–µ—Д–Є—Ж–Є—В–∞ —Д–µ—А–Љ–µ–љ—В–Њ–≤ –Є–ї–Є –±–Њ–ї–µ–Ј–љ–µ–є –љ–∞–Ї–Њ–њ–ї–µ–љ–Є—П, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ —А–∞–Ј–≤–Є—В–Є–µ –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –ґ–Є—А–Њ–≤–Њ–є –±–Њ–ї–µ–Ј–љ–Є –њ–µ—З–µ–љ–Є –Є–ї–Є —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П. –Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞—О—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –љ–∞–ї–Є—З–Є—П –ї–Є—И—М –Њ–і–љ–Њ–≥–Њ –Є–Ј –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –Є—Б–Ї–ї—О—З–∞—О—Й–Є—Е –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –і—А—Г–≥–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є.
–Ф–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј
–Ф–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–µ—З–µ–љ–Є –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Г—О —Б–ї–Њ–ґ–љ–Њ—Б—В—М, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –≤ —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ –љ–µ—В –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е –Є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є—Е –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–µ—З–µ–љ–Є, —В–∞–Ї–Є–µ –Ї–∞–Ї –∞–ї–Ї–Њ–≥–Њ–ї—М–љ–∞—П –Є –љ–µ–∞–ї–Ї–Њ–≥–Њ–ї—М–љ–∞—П –ґ–Є—А–Њ–≤–∞—П –±–Њ–ї–µ–Ј–љ—М –њ–µ—З–µ–љ–Є –Є–ї–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–є –≥–µ–њ–∞—В–Є—В. –Ч–∞—З–∞—Б—В—Г—О –≤—Л—А—Г—З–∞—О—В –Ї–ї—О—З–µ–≤—Л–µ –і–∞–љ–љ—Л–µ –∞–љ–∞–Љ–љ–µ–Ј–∞, –≤–∞–ґ–љ–Њ —Г—В–Њ—З–љ—П—В—М –њ—А–Є–≤—Л—З–Ї–Є —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –∞–ї–Ї–Њ–≥–Њ–ї—П –Є –µ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ, –њ—А–Є–µ–Љ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–≤ –њ–Њ –њ–Њ–≤–Њ–і—Г –≤—Б–µ—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–∞, —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –љ–∞—А–Ї–Њ—В–Є–Ї–Њ–≤, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є –њ—А–Є –µ–µ –љ–∞–ї–Є—З–Є–Є, —Б–≤—П–Ј—М —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є.
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –Њ–≥—А–Њ–Љ–љ–Њ–µ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–Є–µ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –Є –њ—А–Є—З–Є–љ, –њ—А–Є–≤–Њ–і—П—Й–Є—Е –Ї —А–∞–Ј–≤–Є—В–Є—О –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–µ—З–µ–љ–Є, –≤–∞–ґ–љ–Њ–є –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –Њ–±—Й–љ–Њ—Б—В—М –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –±–Њ–ї–µ–Ј–љ–µ–є –њ–µ—З–µ–љ–Є, –њ—А–Њ—В–µ–Ї–∞—О—Й–Є—Е –≤ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В–Є, –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–є –њ–µ—З–µ–љ–Њ—З–љ—Л–є –Ї–Њ–љ—В–Є–љ—Г—Г–Љ. –†–∞–Ј–ї–Є—З–љ—Л–Љ–Є —П–≤–ї—П—О—В—Б—П —В–Њ–ї—М–Ї–Њ –њ—Г—Б–Ї–Њ–≤—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –Є –њ—А–µ–Њ–±–ї–∞–і–∞—О—Й–Є–µ –Є—Б—Е–Њ–і—Л.
–Т—Б–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–µ—З–µ–љ–Є (–µ—Б–ї–Є —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –Ї–∞—А—В–Є–љ—Г –Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Б—В—А—Г–Ї—В—Г—А—Л –Њ—А–≥–∞–љ–∞) –њ—А–Њ—В–µ–Ї–∞—О—В –≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–є –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В–Є. –Ф–∞–љ–љ–∞—П —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В—М —Б—В–∞–і–Є–є –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–µ—З–µ–љ–Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В –њ–µ—З–µ–љ–Њ—З–љ—Л–є –Ї–Њ–љ—В–Є–љ—Г—Г–Љ, –Є–Љ–µ—О—Й–Є–є –≤ –Ї–∞—З–µ—Б—В–≤–µ –Є—Б—Е–Њ–і–Њ–≤ –њ–µ—З–µ–љ–Њ—З–љ—Г—О –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –Є–ї–Є –≥–µ–њ–∞—В–Њ—Ж–µ–ї–ї—О–ї—П—А–љ—Г—О –Ї–∞—А—Ж–Є–љ–Њ–Љ—Г (–њ–µ—А–≤–Є—З–љ—Л–є —А–∞–Ї –њ–µ—З–µ–љ–Є) [8].
–Ъ–ї–∞—Б—Б–Є—З–µ—Б–Ї–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ —Б—В—А–Њ–Є—В—Б—П –љ–∞ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Б—В—А—Г–Ї—В—Г—А—Л –њ–µ—З–µ–љ–Є –Є —Б—В–∞–і–Є–Є –њ—А–Њ—Ж–µ—Б—Б–∞, –∞ —В–∞–Ї–ґ–µ –≤—Л—П—Б–љ–µ–љ–Є–Є —Н—В–Є–Њ–ї–Њ–≥–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ф–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є 4-—Е –њ–µ—З–µ–љ–Њ—З–љ—Л—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤: —Ж–Є—В–Њ–ї–Є–Ј–∞, —Е–Њ–ї–µ—Б—В–∞–Ј–∞, –њ–µ—З–µ–љ–Њ—З–љ–Њ-–Ї–ї–µ—В–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П [8]. –Ю–і–љ–∞–Ї–Њ —Б –њ–Њ–Ј–Є—Ж–Є–є –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є —И–Ї–Њ–ї—Л –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –≤—Л–і–µ–ї–µ–љ–Є–µ –і—А—Г–≥–Є—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –Ї–∞—В–µ–≥–Њ—А–Є–є, —В–∞–Ї–Є—Е –Ї–∞–Ї –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ –Љ–µ–Љ–±—А–∞–љ (—Ж–Є—В–Њ–ї–Є–Ј), –≤–љ—Г—В—А–Є–њ–µ—З–µ–љ–Њ—З–љ—Л–є —Е–Њ–ї–µ—Б—В–∞–Ј, –њ–µ—А–µ–Ї–Є—Б–љ–Њ–µ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ –ї–Є–њ–Є–і–Њ–≤, —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ. –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л–µ –њ—А–Њ—В–Њ–Ї–Њ–ї—Л –Є —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ—А–µ–і–ї–∞–≥–∞—О—В –≤–∞—А–Є–∞–љ—В –њ—А–Њ–≤–µ–і–µ–љ–Є—П –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —Б–Є–љ–і—А–Њ–Љ–Њ–≤ —Ж–Є—В–Њ–ї–Є–Ј–∞ –Є —Е–Њ–ї–µ—Б—В–∞–Ј–∞, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–є –љ–∞ —А–Є—Б—Г–љ–Ї–µ 1 [9].
–Т—Л–±–Њ—А –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П,
–≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А—Л
–Ф–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Ј–∞—З–∞—Б—В—Г—О —В—А–µ–±—Г–µ—В –±–Њ–ї—М—И–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –≤—А–µ–Љ–µ–љ–Є, —В–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –≤ –і–∞–љ–љ—Л–є –њ–µ—А–Є–Њ–і –њ–∞—Ж–Є–µ–љ—В –і–Њ–ї–ґ–µ–љ –њ–Њ–ї—Г—З–∞—В—М –Ї–∞–Ї—Г—О-—В–Њ —В–µ—А–∞–њ–Є—О. –Ы–µ—З–µ–љ–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–µ—З–µ–љ–Є –і–Њ–ї–ґ–љ–Њ –±—Л—В—М –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л–Љ –Є –≤–Ї–ї—О—З–∞—В—М –≤ —Б–µ–±—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤. –°–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–µ –љ–∞ —Г–ї—Г—З—И–µ–љ–Є–µ —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є—П –њ–∞—Ж–Є–µ–љ—В–∞, –Њ–±—Л—З–љ–Њ –љ–µ —В—А–µ–±—Г–µ—В—Б—П –≤ —Б–≤—П–Ј–Є —Б–Њ —Б–Ї—Г–і–љ–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Њ–є. –≠—В–Є–Њ—В—А–Њ–њ–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –Љ–Њ–ґ–љ–Њ –љ–∞–Ј–љ–∞—З–∞—В—М —В–Њ–ї—М–Ї–Њ –њ—А–Є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–Љ –Њ–Ї–Њ–љ—З–∞—В–µ–ї—М–љ–Њ–Љ –і–Є–∞–≥–љ–Њ–Ј–µ, –∞ —Д–∞–Ї—В –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є—П —Ж–Є—В–Њ–ї–Є–Ј–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –љ–∞—З–∞—В—М –ї–µ—З–µ–љ–Є–µ —Б –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є [10].
–¶–µ–ї—П–Љ–Є –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —П–≤–ї—П—О—В—Б—П –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ –Љ–µ–Љ–±—А–∞–љ –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤ –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —Ж–Є—В–Њ–ї–Є–Ј–∞, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –њ–µ—З–µ–љ–Є, —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –°—В–∞–љ–і–∞—А—В—Л –ї–µ—З–µ–љ–Є—П –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О –њ–µ—З–µ–љ–Є (EASL) –Є –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–є –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є (AGA) –њ—А–µ–і—Г—Б–Љ–∞—В—А–Є–≤–∞—О—В –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Б —Н—В–Њ–є —Ж–µ–ї—М—О —Ж–Є—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–Њ–≤ (–≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–Њ–≤) [11, 12].
–†–Њ—Б—Б–Є–є—Б–Ї–Є–µ —Б—В–∞–љ–і–∞—А—В—Л –ї–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–µ—З–µ–љ–Є, —Г—В–≤–µ—А–ґ–і–µ–љ–љ—Л–µ –њ—А–Є–Ї–∞–Ј–∞–Љ–Є –Ь–Є–љ–Ј–і—А–∞–≤—Б–Њ—Ж—А–∞–Ј–≤–Є—В–Є—П, —В–∞–Ї–ґ–µ –њ—А–µ–і—Г—Б–Љ–∞—В—А–Є–≤–∞—О—В –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–Њ–≤, –Ї –Ї–Њ—В–Њ—А—Л–Љ –Њ—В–љ–Њ—Б—П—В—Б—П —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л–µ —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і—Л, —Г—А—Б–Њ–і–µ–Ј–Њ–Ї—Б–Є—Е–Њ–ї–µ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, –њ—А–µ–њ–∞—А–∞—В—Л —А–∞—Б—В–Њ—А–Њ–њ—И–Є (—Б–Є–ї–Є–±–Є–љ–Є–љ), –∞–і–µ–Љ–µ—В–Є–Њ–љ–Є–љ [13, 14]. –Ю–і–љ–∞–Ї–Њ –≤–Њ–њ—А–Њ—Б—Л –ї–µ—З–µ–љ–Є—П –і–Њ —Б–µ–≥–Њ–і–љ—П—И–љ–µ–≥–Њ –і–љ—П –Њ—Б—В–∞—О—В—Б—П –і–Є—Б–Ї—Г—Б—Б–Є–Њ–љ–љ—Л–Љ–Є.
–У–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А—Л (—Ж–Є—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А—Л) –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є —А–∞–Ј–љ–Њ—А–Њ–і–љ—Г—О –≥—А—Г–њ–њ—Г –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –≤ —В.—З. –Є –њ–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ –і–µ–є—Б—В–≤–Є—П. –°—Г—Й–µ—Б—В–≤—Г—О—В —Б—А–µ–і—Б—В–≤–∞ –Ї–∞–Ї —А–∞—Б—В–Є—В–µ–ї—М–љ–Њ–≥–Њ, —В–∞–Ї –Є –ґ–Є–≤–Њ—В–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П, –∞ —В–∞–Ї–ґ–µ —Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л.
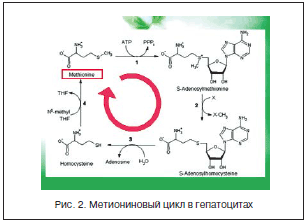
–Ш—Б—В–Њ—А–Є—П –ї–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–µ—З–µ–љ–Є –љ–∞—З–Є–љ–∞–ї–∞—Б—М —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Љ–µ—В–Є–Њ–љ–Є–љ–∞ –Є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ –Љ–µ—В–Є–Њ–љ–Є–љ–Њ–≤—Л–є —Ж–Є–Ї–ї –≤ –≥–µ–њ–∞—В–Њ—Ж–Є—В–∞—Е (—А–Є—Б. 2) [15, 16]. –Ю—Б–Њ–±–∞—П —А–Њ–ї—М –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ–Њ–є –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л –Љ–µ—В–Є–Њ–љ–Є–љ–∞ —Б–≤—П–Ј–∞–љ–∞ —Б –њ–Њ–і–≤–Є–ґ–љ–Њ–є –Љ–µ—В–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ–Њ–є. –° –µ–µ –њ–Њ–Љ–Њ—Й—М—О –Љ–µ—В–Є–Њ–љ–Є–љ —Г—З–∞—Б—В–≤—Г–µ—В –≤ –њ–µ—А–µ–Љ–µ—В–Є–ї–Є—А–Њ–≤–∞–љ–Є–Є, –і–µ–Ј–∞–Љ–Є–љ–Є—А–Њ–≤–∞–љ–Є–Є, –і–µ–Ї–∞—А–±–Њ–Ї—Б–Є–ї–Є—А–Њ–≤–∞–љ–Є–Є (—А–Є—Б. 3).
–° –њ–µ—А–µ–Љ–µ—В–Є–ї–Є—А–Њ–≤–∞–љ–Є–µ–Љ —Б–≤—П–Ј–∞–љ —Б–Є–љ—В–µ–Ј –Ї—А–µ–∞—В–Є–љ–∞, –∞–і—А–µ–љ–∞–ї–Є–љ–∞ –Є —Е–Њ–ї–Є–љ–∞, —П–≤–ї—П—О—Й–µ–≥–Њ—Б—П –њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї–Њ–Љ –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ–∞ –Є –≤–∞–ґ–љ–µ–є—И–Є–Љ –ї–Є–њ–Њ—В—А–Њ–њ–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ. –£–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П —Е–Њ–ї–Є–љ–∞ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—О —Б–Є–љ—В–µ–Ј–∞ —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤ –Є —Г–Љ–µ–љ—М—И–µ–љ–Є—О –Њ—В–ї–Њ–ґ–µ–љ–Є—П –ґ–Є—А–Њ–≤ –≤ –њ–µ—З–µ–љ–Є. –°–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –Љ–µ—В–Є–Њ–љ–Є–љ–∞ –Њ—В–і–∞–≤–∞—В—М –Љ–µ—В–Є–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –µ–≥–Њ –ї–Є–њ–Њ—В—А–Њ–њ–љ—Л–є —Н—Д—Д–µ–Ї—В. –Ґ–∞–Ї, –њ—А–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–µ –Љ–µ—В–Є–Њ–љ–Є–љ —Б–љ–Є–ґ–∞–µ—В –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –•–° –Є –њ–Њ–≤—Л—И–∞–µ—В –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤ –Ї—А–Њ–≤–Є. –Т–≤–µ–і–µ–љ–Є–µ –Љ–µ—В–Є–Њ–љ–Є–љ–∞ –≤—Л–Ј—Л–≤–∞–µ—В —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –≤ –Ї—А–Њ–≤–Є –•–° –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤.
–Ь–µ—В–Є–Њ–љ–Є–љ —Г—З–∞—Б—В–≤—Г–µ—В –≤ –Њ–±–Љ–µ–љ–µ —Б–µ—А–Њ—Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, –≤ —Б–Є–љ—В–µ–Ј–µ —Н–њ–Є–љ–µ—Д—А–Є–љ–∞, –Ї—А–µ–∞—В–Є–љ–Є–љ–∞, –≥–Њ—А–Љ–Њ–љ–Њ–≤, –љ–µ–є—А–Њ–Љ–µ–і–Є–∞—В–Њ—А–Њ–≤, –≤–Є—В–∞–Љ–Є–љ–Њ–≤. –Я—А–Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–Є –і–µ—Д–Є—Ж–Є—В–∞ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Љ–µ—В–Є–Њ–љ–Є–љ–∞ –љ–∞—А—Г—И–∞–µ—В—Б—П —Б–Є–љ—В–µ–Ј —Е–Њ–ї–Є–љ–∞, –ї–µ—Ж–Є—В–Є–љ–∞ –Є —Б—Д–Є–љ–≥–Њ–Љ–Є–µ–ї–Є–љ–∞, –Ї–Њ—В–Њ—А—Л–µ —П–≤–ї—П—О—В—Б—П –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞–Љ–Є –љ–µ—А–≤–љ–Њ–є —В–Ї–∞–љ–Є.
–Т–∞–ґ–љ—Л–є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є –∞—Б–њ–µ–Ї—В –≤–ї–Є—П–љ–Є—П –Љ–µ—В–Є–Њ–љ–Є–љ–∞ – –µ–≥–Њ —Г—З–∞—Б—В–Є–µ –≤ –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–Є –љ–∞ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–Љ —Г—А–Њ–≤–љ–µ –≥–ї—Г—В–∞—В–Є–Њ–љ–∞ – —Б–µ—А–Њ—Б–Њ–і–µ—А–ґ–∞—Й–µ–≥–Њ –њ–µ–њ—В–Є–і–∞, –Ј–∞—Й–Є—Й–∞—О—Й–µ–≥–Њ –≥–µ–њ–∞—В–Њ—Ж–Є—В—Л –Њ—В —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П —Б–≤–Њ–±–Њ–і–љ—Л–Љ–Є —А–∞–і–Є–Ї–∞–ї–∞–Љ–Є. –Э–∞–Ї–Њ–љ–µ—Ж, —Г—З–∞—Б—В–≤—Г—П –≤ —А–µ–∞–Ї—Ж–Є—П—Е —Б—Г–ї—М—Д–∞—В–Є—А–Њ–≤–∞–љ–Є—П, –Љ–µ—В–Є–Њ–љ–Є–љ –Є–≥—А–∞–µ—В –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ –і–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є —А—П–і–∞ –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤. –£–Ї–∞–Ј–∞–љ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Є–Љ–µ—О—В –њ—А—П–Љ–Њ–µ –Њ—В–љ–Њ—И–µ–љ–Є–µ –Ї –Ј–∞—Й–Є—В–µ –њ–µ—З–µ–љ–Є –Њ—В —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —Н—В–∞–љ–Њ–ї–∞ [8, 17].
–Ю–і–љ–Є–Љ –Є–Ј —Н—В–∞–њ–Њ–≤ —А–∞–Ј–≤–Є—В–Є—П –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б—В–∞–ї–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –∞–і–µ–Љ–µ—В–Є–Њ–љ–Є–љ–∞, —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є–Ј–љ–∞—З–∞–ї—М–љ–Њ –≤ –Ї–∞—З–µ—Б—В–≤–µ –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В–Њ–≤. –Ш—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –Њ—А–Є–µ–љ—В–Є—А–Њ–≤–∞–љ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–∞ –Љ–µ—В–Є–Њ–љ–Є–љ–Њ–≤—Л–є —Ж–Є–Ї–ї –Є –≤–љ—Г—В—А–Є–њ–µ—З–µ–љ–Њ—З–љ—Л–є —Е–Њ–ї–µ—Б—В–∞–Ј.
–Я—А–µ–њ–∞—А–∞—В—Л —Г—А—Б–Њ–і–µ–Ј–Њ–Ї—Б–Є—Е–Њ–ї–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Њ–±–ї–∞–і–∞—О—В –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –ґ–µ–ї—З–µ–≥–Њ–љ–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, –Њ–Ї–∞–Ј—Л–≤–∞—О—В —Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ –≥–µ–њ–∞—В–Њ—Ж–Є—В—Л –њ—А–Є –≤–љ—Г—В—А–Є–њ–µ—З–µ–љ–Њ—З–љ–Њ–Љ —Е–Њ–ї–µ—Б—В–∞–Ј–µ –Є –≤–Є—А—Г—Б–љ—Л—Е –≥–µ–њ–∞—В–Є—В–∞—Е.
–§–ї–∞–≤–Њ–љ–Њ–Є–і—Л —А–∞—Б—В–Њ—А–Њ–њ—И–Є –њ–µ—А–≤–Њ–љ–∞—З–∞–ї—М–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М –≤ –Є–љ—К–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е —Д–Њ—А–Љ–∞—Е –Ї–∞–Ї —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–є –∞–љ—В–Є–і–Њ—В –њ—А–Є –Њ—В—А–∞–≤–ї–µ–љ–Є–Є –±–ї–µ–і–љ–Њ–є –њ–Њ–≥–∞–љ–Ї–Њ–є. –Ш—Е –і–µ–є—Б—В–≤–Є–µ –Њ—Б–љ–Њ–≤–∞–љ–Њ –љ–∞ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –≤–љ—Г—В—А–Є–њ–µ—З–µ–љ–Њ—З–љ–Њ–≥–Њ —В—А–∞–љ—Б–њ–Њ—А—В–∞ –ґ–µ–ї—З–љ—Л—Е –Ї–Є—Б–ї–Њ—В, –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П—Е –≥–ї—Г—В–∞—В–Є–Њ–љ–∞ –Є –њ—А–Њ—Ж–µ—Б—Б–∞—Е –і–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є, —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–µ–љ–∞ —Б—В–Є–Љ—Г–ї—П—Ж–Є—П —Б–Є–љ—В–µ–Ј–∞ –±–µ–ї–Ї–∞ –љ–∞ —А–Є–±–Њ—Б–Њ–Љ–∞—Е, —З—В–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ –ї–µ—З–µ–љ–Є–Є —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е –Є –≤–Є—А—Г—Б–љ—Л—Е –≥–µ–њ–∞—В–Є—В–Њ–≤.
–Я—А–µ–њ–∞—А–∞—В—Л L-–Њ—А–љ–Є—В–Є–љ-L-–∞—Б–њ–∞—А—В–∞—В–∞ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –≤ –ї–µ—З–µ–љ–Є–Є –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –њ–µ—З–µ–љ–Њ—З–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є, –і–µ–є—Б—В–≤–Є–µ –Є—Е –Њ—Б–љ–Њ–≤–∞–љ–Њ –љ–∞ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–Є –љ–∞ –Њ—А–љ–Є—В–Є–љ–Њ–≤—Л–є —Ж–Є–Ї–ї, —Г—В–Є–ї–Є–Ј–∞—Ж–Є—О –∞–Ј–Њ—В–∞ –Є —Б–Є–љ—В–µ–Ј –≥–ї—Г—В–∞—В–Є–Њ–љ–∞ [18, 19].
–Т –ї–µ—З–µ–љ–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–µ—З–µ–љ–Є –љ–∞—Е–Њ–і—П—В –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В—Л, —Б–≤—П–Ј—Л–≤–∞—О—Й–Є–µ –њ—А–Њ–і—Г–Ї—В—Л –њ–µ—А–µ–Ї–Є—Б–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –ї–Є–њ–Є–і–Њ–≤. –Ю–і–љ–∞–Ї–Њ –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–µ –Є–Љ–µ–µ—В –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –±–∞–Ј—Л. –Я–µ–љ—В–Њ–Ї—Б–Є—Д–Є–ї–ї–Є–љ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –≤ –ї–µ—З–µ–љ–Є–Є –Э–Р–Ц–С–Я –≤ –Ї–∞—З–µ—Б—В–≤–µ –Є–љ–≥–Є–±–Є—В–Њ—А–∞ —Д–∞–Ї—В–Њ—А–∞ –љ–µ–Ї—А–Њ–Ј–∞ –Њ–њ—Г—Е–Њ–ї–Є. –Ґ–∞–Ї–ґ–µ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є —Б—В–µ–∞—В–Њ–≥–µ–њ–∞—В–Є—В–∞ –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –Љ–µ—В—Д–Њ—А–Љ–Є–љ, —А—П–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В –ї—Г—З—И–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —В–Є–∞–Ј–Њ–ї–Є–і–Њ–≤ [20–22].
–°—В–∞–љ–і–∞—А—В–Њ–Љ —В–µ—А–∞–њ–Є–Є –љ–∞ —Б–µ–≥–Њ–і–љ—П –Њ—Б—В–∞—О—В—Б—П —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л–µ —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і—Л – –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –і–ї—П —А–∞–Ј–≤–Є—В–Є—П –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П –Ї–ї–µ—В–Њ–Ї –њ–µ—З–µ–љ–Є. –Ю—Б–љ–Њ–≤–љ–∞—П —Д—А–∞–Ї—Ж–Є—П —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ —Д–Њ—Б—Д–∞—В–Є–і–Є–ї—Е–Њ–ї–Є–љ–Њ–Љ, —П–≤–ї—П—О—Й–Є–Љ—Б—П –Њ—Б–љ–Њ–≤–љ—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Љ–µ–Љ–±—А–∞–љ. –Я–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Њ—Б–љ–Њ–≤—Л —А–µ–∞–ї–Є–Ј–∞—Ж–Є–Є –і–∞–љ–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —Б–≤—П–Ј–∞–љ—Л —Б —А–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є –њ–µ—З–µ–љ–Є, –Ї–Њ—В–Њ—А—Л–µ –Њ–њ—А–µ–і–µ–ї—П—О—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В—М –љ–Њ–≤—Л–µ –Ї–ї–µ—В–Њ—З–љ—Л–µ –Љ–µ–Љ–±—А–∞–љ—Л, –љ–∞ 65% —Б–Њ—Б—В–Њ—П—Й–Є–µ –Є–Ј —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤. –Я–Њ–њ–∞–і–∞—П –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ, —Д–Њ—Б—Д–∞—В–Є–і–Є–ї—Е–Њ–ї–Є–љ –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В —Ж–µ–ї–Њ—Б—В–љ–Њ—Б—В—М –Љ–µ–Љ–±—А–∞–љ –њ–Њ—А–∞–ґ–µ–љ–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –њ–µ—З–µ–љ–Є –Є –∞–Ї—В–Є–≤–Є—А—Г–µ—В —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л–µ –≤ –Љ–µ–Љ–±—А–∞–љ–µ —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Ј–∞–≤–Є—Б–Є–Љ—Л–µ —Д–µ—А–Љ–µ–љ—В—Л, –љ–Њ—А–Љ–∞–ї–Є–Ј—Г—П —В–µ–Љ —Б–∞–Љ—Л–Љ –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М –Є —Г—Б–Є–ї–Є–≤–∞—П –і–µ–Ј–Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Њ–љ–љ—Л–є –Є —Н–Ї—Б–Ї—А–µ—В–Њ—А–љ—Л–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї –Ї–ї–µ—В–Њ–Ї –њ–µ—З–µ–љ–Є (—А–Є—Б. 4) [23].
–Ю—Б–љ–Њ–≤–љ—Л–Љ–Є –і–µ–є—Б—В–≤–Є—П–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ –≤—Л–њ–Њ–ї–љ—П–µ—В —Д–Њ—Б—Д–∞—В–Є–і–Є–ї—Е–Њ–ї–Є–љ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ, —П–≤–ї—П—О—В—Б—П –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ —Б—В—А—Г–Ї—В—Г—А—Л –Љ–µ–Љ–±—А–∞–љ –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤, –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ (–Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є–µ –њ–µ—А–µ–Ї–Є—Б–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –ї–Є–њ–Є–і–Њ–≤ –Є —Б–≤—П–Ј—Л–≤–∞–љ–Є–µ —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤), –∞–љ—В–Є—Д–Є–±—А–Њ–Ј–љ—Л–є —Н—Д—Д–µ–Ї—В (–њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є–µ –љ–∞–Ї–Њ–њ–ї–µ–љ–Є—П –Ї–Њ–ї–ї–∞–≥–µ–љ–∞ 1-–≥–Њ —В–Є–њ–∞, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ї–Њ–ї–ї–∞–≥–µ–љ–∞–Ј—Л).
–Ъ—А–Њ–Љ–µ –≤–ї–Є—П–љ–Є—П –љ–∞ –Ї–ї–µ—В–Њ—З–љ—Л–µ –Љ–µ–Љ–±—А–∞–љ—Л —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л–µ —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і—Л —Г–ї—Г—З—И–∞—О—В —Д—Г–љ–Ї—Ж–Є–Є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –≤ —В.—З. –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Л—Е; —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–љ–ї–Є–њ–∞–Ј—Л, –њ–Њ–≤—Л—И–∞—О—Й–µ–є —А–∞—Б—Й–µ–њ–ї–µ–љ–Є–µ —Е–Є–ї–Њ–Љ–Є–Ї—А–Њ–љ–Њ–≤ –Є –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤ –Њ—З–µ–љ—М –љ–Є–Ј–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є, –Є –ї–µ—Ж–Є—В–Є–љ-—Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞—Ж–Є–ї—В—А–∞–љ—Б—Д–µ—А–∞–Ј—Л, —Г—З–∞—Б—В–≤—Г—О—Й–µ–є –≤ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–Є –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤ –≤—Л—Б–Њ–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є. –°—В–Є–Љ—Г–ї—П—Ж–Є—П —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–ї–Є–њ–∞–Ј—Л –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ —Д–Њ—Б—Д–∞—В–Є–і–Є–ї—Е–Њ–ї–Є–љ–∞ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –≤—Л–і–µ–ї–µ–љ–Є—О –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В –≤ –Ї—А–Њ–≤–Њ—В–Њ–Ї –Є —Г–Љ–µ–љ—М—И–µ–љ–Є—О —Б—В–µ–∞—В–Њ–Ј–∞ –њ–µ—З–µ–љ–Є. –≠—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л–µ —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і—Л —Г–Љ–µ–љ—М—И–∞—О—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М —Б—В–µ–∞—В–Њ–Ј–∞ –њ–µ—З–µ–љ–Є –љ–µ —В–Њ–ї—М–Ї–Њ –њ—А–Є –љ–µ–∞–Ї–Њ–≥–Њ–ї—М–љ–Њ–Љ —Б—В–µ–∞—В–Њ–≥–µ–њ–∞—В–Є—В–µ, –љ–Њ –Є –њ—А–Є –∞–ї–Ї–Њ–≥–Њ–ї—М–љ—Л—Е, —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П—Е –њ–µ—З–µ–љ–Є [23].
–Ш—Б—В–Њ—А–Є—П –Є–Ј—Г—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤ –љ–∞—З–∞–ї–∞—Б—М —Б –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є F. Knüchel, –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ—Л—Е –≤ 1979 –≥. –Ю–љ –њ—А–Њ–≤–Њ–і–Є–ї —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –Є—Б–њ–Њ–ї—М–Ј—Г—П –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–µ –і–Њ–Ј—Л –∞–ї–Ї–Њ–≥–Њ–ї—П. –Ъ–Њ–љ—В—А–Њ–ї—М –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤ –њ—А–Њ–≤–Њ–і–Є–ї—Б—П —Б –њ–Њ–Љ–Њ—Й—М—О –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –і–∞–љ–љ—Л–µ –Њ –і–µ—Д–Њ—А–Љ–∞—Ж–Є–Є –Є —А–∞–Ј—А—Г—И–µ–љ–Є–Є –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –∞–ї–Ї–Њ–≥–Њ–ї—П. –Ю–њ—Л—В–љ–∞—П –≥—А—Г–њ–њ–∞ –њ–Њ–ї—Г—З–∞–ї–∞ –њ—А–µ–њ–∞—А–∞—В —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤, –Ї–Њ–љ—В—А–Њ–ї—М–љ–∞—П –≥—А—Г–њ–њ–∞ –љ–µ –њ–Њ–ї—Г—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є. –Я–Њ –Њ–Ї–Њ–љ—З–∞–љ–Є–Є –љ–∞–±–ї—О–і–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Ж–Є—В–Њ–ї–Є–Ј–∞ –≤ –≥—А—Г–њ–њ–µ –ї–µ—З–µ–љ–Є—П —Б–љ–Є–ґ–∞–ї–Є—Б—М, –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л —Г–±–µ–і–Є—В–µ–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ –Њ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–Є –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ [24].
–Э–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –њ—А–Њ–≤–µ–і–µ–љ–Њ –±–Њ–ї–µ–µ 250 –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤, –њ–Њ–Ї–∞–Ј–∞–≤—И–Є—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –њ–µ—З–µ–љ–Є. –£—В–≤–µ—А–ґ–і–µ–љ–Є—П –Њ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –±–∞–Ј–µ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤ –љ–µ –Љ–Њ–≥—Г—В —Б—З–Є—В–∞—В—М—Б—П –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ—Л–Љ–Є [25].
–Т —З–∞—Б—В–љ–Њ—Б—В–Є, —В–Њ–ї—М–Ї–Њ –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –њ–µ—З–µ–љ–Є, –≤ —В.—З. —Б —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є. –С—Л–ї–Њ –њ–Њ–ї—Г—З–µ–љ–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤ (—Б–љ–Є–ґ–µ–љ–Є–µ —Ж–Є—В–Њ–ї–Є–Ј–∞, —Г–ї—Г—З—И–µ–љ–Є–µ –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л) [26, 27].
–Ґ–∞–Ї–ґ–µ –±—Л–ї–Њ –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–Њ 4 –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б —Г—З–∞—Б—В–Є–µ–Љ —Б–≤—Л—И–µ 300 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–Р–Ц–С–Я, –Є–Љ–µ—О—Й–Є—Е –і–Є–∞–±–µ—В, –Њ–ґ–Є—А–µ–љ–Є–µ –Є–ї–Є –Њ–±–∞ —Д–∞–Ї—В–Њ—А–∞. –Т–Њ –≤—Б–µ—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ–Њ–Ї–∞–Ј–∞–љ–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є —Г –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л–µ —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і—Л –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–Њ–є, —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —В—А–∞–љ—Б–∞–Љ–Є–љ–∞–Ј –Є –ї–Є–њ–Є–і–Њ–≤ –≤ –Ї—А–Њ–≤–Є, –∞ —В–∞–Ї–ґ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ —Б—В–µ–∞—В–Њ–Ј–∞ –њ—А–Є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [28–30].
–Ґ–∞–Ї—В–Є–Ї–∞ –≤–µ–і–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б –∞–ї–Ї–Њ–≥–Њ–ї—М–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є –њ–µ—З–µ–љ–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤ –Є–Ј—Г—З–∞–ї–∞—Б—М –≤ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є –і–≤–Њ–є–љ—Л—Е —Б–ї–µ–њ—Л—Е –њ–ї–∞—Ж–µ–±–Њ-–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е. –Т—Б–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є —Г–ї—Г—З—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л–µ —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і—Л, –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–∞–Ї–Њ–≤–Њ–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л. –Я–Њ–Ї–∞–Ј–∞–љ–∞ —В–µ–љ–і–µ–љ—Ж–Є—П –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –і–Њ–ї–≥–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤ (3––ї–µ—В–љ—П—П –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М) [31, 32].
–Ш—Б—Е–Њ–і—П –Є–Ј –љ–∞–ї–Є—З–Є—П –Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є—Е –љ–∞–ї–Є—З–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –±–∞–Ј—Л —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤ —Б –њ–Њ–Ј–Є—Ж–Є–є –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л, –Љ–Њ–ґ–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞—В—М –і–µ–ї–∞—В—М –≤—Л–±–Њ—А –≤ –Є—Е –њ–Њ–ї—М–Ј—Г –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–∞–Љ–Є.
–Ч–∞—А—Г–±–µ–ґ–љ—Л–µ —Г—З–µ–±–љ—Л–µ –њ–Њ—Б–Њ–±–Є—П –Є —Б—В–∞–љ–і–∞—А—В—Л –≤–Ї–ї—О—З–∞—О—В —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—О —Д–Њ—Б—Д–∞—В–Є–і–Є–ї—Е–Њ–ї–Є–љ–∞ –њ—А–Є —Б–Є–љ–і—А–Њ–Љ–µ —Ж–Є—В–Њ–ї–Є–Ј–∞ –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є —Б —Ж–µ–ї—М—О –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П —Б—В—А—Г–Ї—В—Г—А—Л –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–µ —Б —Н—В–Є–Њ—В—А–Њ–њ–љ—Л–Љ –ї–µ—З–µ–љ–Є–µ–Љ [33].
–Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –≤—Б–µ —З–∞—Й–µ –≤—Б—В—А–µ—З–∞—О—В—Б—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤. –Ґ–∞–Ї, —Б—Г—Й–µ—Б—В–≤—Г—О—В –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –≤–Є—В–∞–Љ–Є–љ–∞–Љ–Є –≥—А—Г–њ–њ—Л –Т, —Б–Є–ї–Є–±–Є–љ–Є–љ–Њ–Љ, –≥–ї–Є—Ж–Є—А—А–Є–Ј–Є–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є –Є –і—А. –Я—А–Є —Н—В–Њ–Љ —З–∞—Б—В—М –њ–Њ–і–Њ–±–љ—Л—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є –Њ–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –Є–ї–Є –Є–Љ–µ–µ—В —А—П–і –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–є –≤ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є. –Э–∞–њ—А–Є–Љ–µ—А, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –і–ї–Є—В–µ–ї—М–љ—Л—Е –Ї—Г—А—Б–Њ–≤ —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤, –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л—Е —Б —Б–Є–ї–Є–±–Є–љ–Є–љ–Њ–Љ, –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–≥—А–∞–љ–Є—З–µ–љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ц–Ъ–С.
–Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є —Ж–Є—В–Њ–ї–Є–Ј–∞ –Є —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–Љ–µ–љ—П—В—М —А–∞–Ј–ї–Є—З–љ—Л–µ –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А—Л. –Я—А–Є —Г–Љ–µ—А–µ–љ–љ–Њ –≤—Л—Б–Њ–Ї–Њ–Љ –Є –≤—Л—Б–Њ–Ї–Њ–Љ —Ж–Є—В–Њ–ї–Є–Ј–µ –Є–ї–Є –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–Є –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –≤–љ—Г—В—А–Є–њ–µ—З–µ–љ–Њ—З–љ–Њ–≥–Њ —Е–Њ–ї–µ—Б—В–∞–Ј–∞ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –і–Њ–±–∞–≤–ї–µ–љ–Є–µ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Г—О —В–µ—А–∞–њ–Є—О –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –∞–і–µ–Љ–µ—В–Є–Њ–љ–Є–љ–∞ –Є —Г—А—Б–Њ–і–µ–Ј–Њ–Ї—Б–Є—Е–Њ–ї–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Є–љ—В–µ–љ—Б–Є–≤–љ—Л–Љ –Ї–Њ—А–Њ—В–Ї–Є–Љ –Ї—Г—А—Б–Њ–Љ. –Я—А–Є –≤—Л—Б–Њ–Ї–Њ–Љ —Ж–Є—В–Њ–ї–Є–Ј–µ –Є–ї–Є –Њ–±—Й–µ–Љ —В—П–ґ–µ–ї–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є –±–Њ–ї—М–љ–Њ–≥–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ –њ—Г–ї—М—Б-—В–µ—А–∞–њ–Є—П –њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–Њ–Љ —Б –љ–∞—З–∞–ї—М–љ–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–Њ–є 50 –Љ–≥ –Є –њ–Њ—Б—В–µ–њ–µ–љ–љ—Л–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –љ–∞ 5 –Љ–≥/–љ–µ–і. –Я–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –і–ї—П –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є —П–≤–ї—П–µ—В—Б—П —Г–Љ–µ—А–µ–љ–љ–Њ –≤—Л—Б–Њ–Ї–Є–є –Є –≤—Л—Б–Њ–Ї–Є–є —Ж–Є—В–Њ–ї–Є–Ј.
–Т—Л–±–Њ—А –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–Њ–≤
–£—З–Є—В—Л–≤–∞—П —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –љ–∞—А—Г—И–µ–љ–Є–є –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –њ–Њ—А–∞–ґ–µ–љ–Є–є –њ–µ—З–µ–љ–Є, —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–Њ–≤ —Б–Њ —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є [34–36]. –Т–µ—Б—М–Љ–∞ –≤–∞–ґ–µ–љ –і–∞–љ–љ—Л–є –∞—Б–њ–µ–Ї—В –≤ –ї–µ—З–µ–љ–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–µ—З–µ–љ–Є –њ—А–Є —Б–Њ—З–µ—В–∞–љ–љ–Њ–є —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –Ї–Њ–≥–і–∞ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –і–µ–є—Б—В–≤—Г—О—Й–Є—Е –≤–µ—Й–µ—Б—В–≤ —Б —А–∞–Ј–љ—Л–Љ–Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ–Є –і–µ–є—Б—В–≤–Є—П –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –±–Њ–ї–µ–µ –±—Л—Б—В—А—Л–є –Є –≤—Л—А–∞–ґ–µ–љ–љ—Л–є —Н—Д—Д–µ–Ї—В –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–µ–є.
–Ю–і–љ–Є–Љ –Є–Ј —В–∞–Ї–Є—Е –њ—А–Є–Љ–µ—А–Њ–≤ –Љ–Њ–ґ–µ—В —Б–ї—Г–ґ–Є—В—М –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤ 300 –Љ–≥ —Б –Љ–µ—В–Є–Њ–љ–Є–љ–Њ–Љ 100 –Љ–≥ (–≠—Б–ї–Є–і–Є–љ). –Я—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –њ—А–Є–µ–Љ–µ –Љ–µ—В–Є–Њ–љ–Є–љ –Є —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л–µ —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і—Л —Г—Б–Є–ї–Є–≤–∞—О—В –і–µ–є—Б—В–≤–Є–µ –і—А—Г–≥ –і—А—Г–≥–∞, —П–≤–ї—П—П—Б—М –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е –Є —Н–Ї–Ј–Њ–≥–µ–љ–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ.
–Я—А–µ–і—Б—В–∞–≤–ї—П—О—В—Б—П –Є–љ—В–µ—А–µ—Б–љ—Л–Љ–Є —А–µ–Ј—Г–ї—М—В–∞—В—Л –Њ–і–љ–Њ–≥–Њ –Є–Ј –Љ–љ–Њ–ґ–µ—Б—В–≤–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ —Б —Г—З–∞—Б—В–Є–µ–Љ 46 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–Р–Ц–С–Я, –Ї–Њ—В–Њ—А—Л–µ –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—О—В –≤—Л—Б–Њ–Ї–Є–є –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Љ–µ—В–Є–Њ–љ–Є–љ–Њ–Љ –Є —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л–Љ–Є —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–∞–Љ–Є (–≠—Б–ї–Є–і–Є–љ), –±–Њ–ї–µ–µ –±—Л—Б—В—А—Г—О –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є, —А–∞–љ–љ—О—О –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Ж–Є—В–Њ–ї–Є–Ј–∞ –Є –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –Ї—А–Њ–≤–Є, –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ —Б—В—А—Г–Ї—В—Г—А—Л –њ–µ—З–µ–љ–Є [4, 10, 37].
–Ґ–∞–Ї, –Є—Б—Е–Њ–і–љ–Њ –њ–Њ–≤—Л—И–µ–љ–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Њ–±—Й–µ–≥–Њ –•–° —Б–љ–Є–Ј–Є–ї—Б—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –ї–µ—З–µ–љ–Є—П –±–µ–Ј –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≥–Є–њ–Њ–ї–Є–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є (—А–Є—Б. 5). –Т –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ —Г—А–Њ–≤–µ–љ—М –•–° —Б–љ–Є–Ј–Є–ї—Б—П –і–Њ 7,2 –Љ–Љ–Њ–ї—М/–ї (–љ–∞ 11%), –≤ –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –≠—Б–ї–Є–і–Є–љ, – –і–Њ 5,6 –Љ–Љ–Њ–ї—М/–ї (–љ–∞ 28,7%). –°–љ–Є–ґ–µ–љ–Є–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є–ї–Њ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –Ј–∞ —Б—З–µ—В –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤ –љ–Є–Ј–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є, —Г—А–Њ–≤–µ–љ—М –Ї–Њ—В–Њ—А—Л—Е —Г–њ–∞–ї –љ–∞ 25,4%. –†–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –±—Л–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –≤–Ј–∞–Є–Љ–љ–Њ–Љ –њ–Њ—В–µ–љ—Ж–Є—А–Њ–≤–∞–љ–Є–Є –і–µ–є—Б—В–≤–Є—П –њ—А–Є —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤ –Є –Љ–µ—В–Є–Њ–љ–Є–љ–∞ [38].
–Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Љ–µ—В–Є–Њ–љ–Є–љ–Њ–Љ –Є —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л–Љ–Є —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–∞–Љ–Є (–≠—Б–ї–Є–і–Є–љ) –≤ –ї–µ—З–µ–љ–Є–Є —Б–Њ—З–µ—В–∞–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –њ–µ—З–µ–љ–Є —Б –њ—А–µ–Њ–±–ї–∞–і–∞—О—Й–Є–Љ–Є –њ—А–Њ—Ж–µ—Б—Б–∞–Љ–Є —Ж–Є—В–Њ–ї–Є–Ј–∞ –Є –њ–µ—А–µ–Ї–Є—Б–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П, –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞. –Э–∞ —Д–Њ–љ–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г—О—Й–Є–Љ–Є—Б—П –≤ —Б–Є—Б—В–µ–Љ–µ —Ж–Є—В–Њ—Е—А–Њ–Љ–Њ–≤ –њ–µ—З–µ–љ–Є, –≤–∞–ґ–љ—Л–Љ–Є –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В—Б—П –і–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Њ–љ–љ—Л–µ –Є –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –Љ–µ—В–Є–Њ–љ–Є–љ–∞ –Є —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤.
–Т—Л–≤–Њ–і—Л
–Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П —Б—В–∞–і–Є–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–µ—З–µ–љ–Є –њ—А–Є –≤—Л—П–≤–ї–µ–љ–Є–Є —Б–Є–љ–і—А–Њ–Љ–Њ–≤ —Ж–Є—В–Њ–ї–Є–Ј–∞ –Є —Е–Њ–ї–µ—Б—В–∞–Ј–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Э–µ–і–Њ–њ—Г—Б—В–Є–Љ–∞ –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–∞ –і–Є–∞–≥–љ–Њ–Ј–∞ –±–µ–Ј –Є—Б–Ї–ї—О—З–µ–љ–Є—П –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –њ—А–Є—З–Є–љ —Ж–Є—В–Њ–ї–Є–Ј–∞.
–Я—А–Є –≤—Л—П–≤–ї–µ–љ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–∞ —Б–Њ—З–µ—В–∞–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є —Б–ї–µ–і—Г–µ—В –љ–∞–Ј–љ–∞—З–∞—В—М —Н—В–Є–Њ—В—А–Њ–њ–љ—Г—О –Є –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї—Г—О —В–µ—А–∞–њ–Є—О —Б —Г—З–µ—В–Њ–Љ –њ—А–µ–Њ–±–ї–∞–і–∞—О—Й–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –њ—А–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –Є–ї–Є —В–µ–Ї—Г—Й–µ–≥–Њ —Б—В–∞—В—Г—Б–∞ –њ–∞—Ж–Є–µ–љ—В–∞.
–Ы–µ—З–µ–љ–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–µ—З–µ–љ–Є –і–Њ–ї–ґ–љ–Њ –±—Л—В—М –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л–Љ –Є –≤–Ї–ї—О—З–∞—В—М —Н—В–Є–Њ—В—А–Њ–њ–љ—Г—О (–њ–Њ—Б–ї–µ –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–Є –і–Є–∞–≥–љ–Њ–Ј–∞) –Є –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї—Г—О —В–µ—А–∞–њ–Є—О (—Б –Љ–Њ–Љ–µ–љ—В–∞ –≤—Л—П–≤–ї–µ–љ–Є—П —Ж–Є—В–Њ–ї–Є–Ј–∞ –Є–ї–Є —Е–Њ–ї–µ—Б—В–∞–Ј–∞).
–Я—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ—Л–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –≠—Б–ї–Є–і–Є–љ, —Б–Њ–і–µ—А–ґ–∞—Й–µ–≥–Њ —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л–µ —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і—Л –Є –Љ–µ—В–Є–Њ–љ–Є–љ, –њ—А–Є –≤—Л—П–≤–ї–µ–љ–Є–Є —Б–Є–љ–і—А–Њ–Љ–∞ —Ж–Є—В–Њ–ї–Є–Ј–∞ –≤ –Ї–∞—З–µ—Б—В–≤–µ –љ–µ–і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є.
![–†–Є—Б. 1. –†–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ —В–∞–Ї—В–Є–Ї–µ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —Ж–Є—В–Њ–ї–Є–Ј–∞ –Є —Е–Њ–ї–µ—Б—В–∞–Ј–∞ [Bloom S., Webster G., Marks D., 2012, —Б –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є]](/data/articles/Image/t21/n31/1621-1.gif)
![–†–Є—Б. 3. –≠—Д—Д–µ–Ї—В—Л –Љ–µ—В–Є–Њ–љ–Є–љ–∞ [–Т—П–ї–Њ–≤ –°.–°., 2011]](/data/articles/Image/t21/n31/1621-3.gif)
![–†–Є—Б. 4. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–ї–Є—П–љ–Є—П —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤ –љ–∞ –Љ–µ–Љ–±—А–∞–љ—Л –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤ [–Т—П–ї–Њ–≤ –°.–°., 2013]](/data/articles/Image/t21/n31/1621-4.gif)
![–†–Є—Б. 5. –Ф–Є–љ–∞–Љ–Є–Ї–∞ —Б–љ–Є–ґ–µ–љ–Є—П —Г—А–Њ–≤–љ–µ–є –ї–Є–њ–Є–і–Њ–≤ –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є —Нcc–µ–љ—Ж–Є–∞–ї—М–љ—Л–Љ–Є —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–∞–Љ–Є –Є –Љ–µ—В–Є–Њ–љ–Є–љ–Њ–Љ [–Т—П–ї–Њ–≤ –°.–°., 2011]](/data/articles/Image/t21/n31/1621-5.gif)
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Т—П–ї–Њ–≤ –°.–°. –Э–µ–∞–ї–Ї–Њ–≥–Њ–ї—М–љ–∞—П –ґ–Є—А–Њ–≤–∞—П –±–Њ–ї–µ–Ј–љ—М –њ–µ—З–µ–љ–Є –Ї–∞–Ї –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞: –ґ–Є—А–Њ–≤–∞—П –њ–µ—З–µ–љ—М –Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј // Consilium Medicum. –Ъ–∞—А–і–Є–Њ–ї–Њ–≥–Є—П. 2012. вДЦ 5. –Ґ. 14. –°. 41–45.
2. Mednez N., Sanchez N.C., Chevez J. Strong association between gallstones and cardiovascular disease // Am J Gastroenterol. 2007. Vol. 50 (3). –†. 183–187.
3. –°—В–Њ—А–Њ–ґ–∞–Ї–Њ–≤ –У.–Ш., –Ш–≤–Ї–Њ–≤–∞ –Р.–Э. –Я–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –∞—Б–њ–µ–Ї—В—Л —Д–Є–±—А–Њ–≥–µ–љ–µ–Ј–∞ –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –њ–µ—З–µ–љ–Є // –Ъ–ї–Є–љ. –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є–Є, –≥–µ–њ–∞—В–Њ–ї–Њ–≥–Є–Є. 2009. вДЦ 2. –°. 3–10.
4. –Т—П–ї–Њ–≤ –°.–°. –Ш–Ј–Љ–µ–љ–µ–љ–Є–µ —Б–њ–µ–Ї—В—А–∞ –Є–Љ–Љ—Г–љ–љ—Л—Е –Љ–∞—А–Ї–µ—А–Њ–≤ –Є –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –њ–µ—З–µ–љ–Є // –Ъ–∞—А–і–Є–Њ—Б–Њ–Љ–∞—В–Є–Ї–∞. 2011. –Ґ. 2. вДЦ 3. –°. 67–73.
5. Targher G., Bertolini L., Pandovani R. et al. Prevalence of non-alcoholic fatty liver disease and its association with cardiovascular disease among Type 2 diabetic patients // Diab Care. 2007. Vol. 30 (6). –†. 1212–1218.
6. –Т–Њ–≤–Ї –Х.–Ш. –Ы–µ—З–µ–љ–Є–µ –љ–µ–∞–ї–Ї–Њ–≥–Њ–ї—М–љ–Њ–є –ґ–Є—А–Њ–≤–Њ–є –±–Њ–ї–µ–Ј–љ–Є –њ–µ—З–µ–љ–Є –≤ –њ—А–∞–Ї—В–Є–Ї–µ —В–µ—А–∞–њ–µ–≤—В–∞: —З—В–Њ? –≥–і–µ? –Ї–Њ–≥–і–∞? // –†–Ь–Ц. 2011. –Ґ. 19. вДЦ 16 (409).
7. –Ф—А–∞–њ–Ї–Є–љ–∞ –Ю., –Ш–≤–∞—И–Ї–Є–љ –Т. –Э–∞—Б—В–Њ—П—Й–µ–µ –Є –±—Г–і—Г—Й–µ–µ —В–µ—А–∞–њ–Є–Є –љ–µ–∞–ї–Ї–Њ–≥–Њ–ї—М–љ–Њ–є –ґ–Є—А–Њ–≤–Њ–є –±–Њ–ї–µ–Ј–љ–Є –њ–µ—З–µ–љ–Є // –Т—А–∞—З. 2011. вДЦ 7.
8. –Т—П–ї–Њ–≤ –°.–°. –°–Є–љ–і—А–Њ–Љ —Ж–Є—В–Њ–ї–Є–Ј–∞ –≤ –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є–Є: —В–∞–Ї—В–Є–Ї–∞ –≤–µ–і–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –Њ–±—Й–µ–є –њ—А–∞–Ї—В–Є–Ї–µ // Consilium Medicum. –У–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—П. 2013. вДЦ 1. –°. 42–48.
9. –Т—П–ї–Њ–≤ –°.–°. –°–Є–љ–і—А–Њ–Љ —Е–Њ–ї–µ—Б—В–∞–Ј–∞: —В–∞–Ї—В–Є–Ї–∞ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –≤–µ–і–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ // –≠—Д—Д–µ–Ї—В–Є–≤–љ–∞—П —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П –≤ –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є–Є. 2012. вДЦ 6. –°. 10–15.
10. –Т—П–ї–Њ–≤ –°.–°. –Ъ–ї–Є–љ–Є–Ї–Њ-–њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –∞—Б–њ–µ–Ї—В—Л –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Г –ї–Є—Ж –Љ–Њ–ї–Њ–і–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ // –Ф–Њ–Ї—В–Њ—А.—А—Г. 2011. вДЦ 5 (64). –°. 42–48.
11. Ratziu V. et al. A proposal for current and future therapeutic strategies for NAFLD // EASL Special Conference «NAFLD/NASH and Related Metabolic Disease», Bologna, Italy, 2009.
12. Chalasani N., Younossi Z. The Diagnosis and Management of Non-alcoholic Fatty Liver Disease: Practice Guideline by AGA, AASLD, ACG // Gastroenterology. 2012. Vol. 142. –†. 1592–1609.
13. –°—В–∞–љ–і–∞—А—В –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й–Є –±–Њ–ї—М–љ—Л–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –∞–Ї—В–Є–≤–љ—Л–Љ –≥–µ–њ–∞—В–Є—В–Њ–Љ, –љ–µ–Ї–ї–∞—Б—Б–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–Љ –≤ –і—А—Г–≥–Є—Е —А—Г–±—А–Є–Ї–∞—Е. –Я—А–Є–Ї–∞–Ј –Ь–Є–љ–Ј–і—А–∞–≤—Б–Њ—Ж—А–∞–Ј–≤–Є—В–Є—П вДЦ 123, 2006.
14. –°—В–∞–љ–і–∞—А—В –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й–Є –±–Њ–ї—М–љ—Л–Љ —Ж–Є—А—А–Њ–Ј–Њ–Љ –њ–µ—З–µ–љ–Є, –љ–µ–Ї–ї–∞—Б—Б–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–Љ –≤ –і—А—Г–≥–Є—Е —А—Г–±—А–Є–Ї–∞—Е. –Я—А–Є–Ї–∞–Ј –Ь–Є–љ–Ј–і—А–∞–≤—Б–Њ—Ж—А–∞–Ј–≤–Є—В–Є—П вДЦ 122, 2006.
15. Wang H., Liu J. Descriptive study of possible link between cardioankle vascular index and homocysteine in vascular-related diseases // BMJ Open. 2013 Mar 25. Vol. 3 (3).
16. Unal E., Mungan S., Bilen S. The effects of lipoprotein(a) and homocysteine on prognosis and risk factors in acute ischemic stroke // Int J Neurosci. 2013 Mar 11.
17. Mouralidarane A., Lin C., Suleyman N. et al. Practical management of the increasing burden of non-alcoholic fatty liver disease // Frontline Gastroenterol. 2010. Vol. 1. –†. 149–155.
18. –Ъ—Г—З–µ—А—П–≤—Л–є –Ѓ.–Р., –Ь–Њ—А–Њ–Ј–Њ–≤ –°.–Т. –У–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А—Л: —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –∞—Б–њ–µ–Ї—В—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П. –Ь., 2012.
19. –Ь–Є–љ—Г—И–Ї–Є–љ –Ю.–Э. –£—А—Б–Њ–і–µ–Ј–Њ–Ї—Б–Є—Е–Њ–ї–µ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ –≤ –њ—А–∞–Ї—В–Є–Ї–µ —В–µ—А–∞–њ–µ–≤—В–∞. –Ь., 2012.
20. Zein C.O., Yerian L.M. Pentoxifylline improves nonalcoholic steatohepatitis: a randomized placebo-controlled trial // Hepatology. 2011 Nov. Vol. 54 (5). –†. 1610–1619.
21. McCullough A.J. Thiazolidinediones for nonalcoholic steatohepatitis-promising but not ready for prime time // N Engl J Med. 2006 Nov 30. Vol. 355 (22). –†. 2361–2363.
22. Lavine J.E., Schwimmer J.B., Van Natta M.L. Effect of vitamin E or metformin for treatment of nonalcoholic fatty liver disease in children and adolescents: the TONIC randomized controlled trial // JAMA. 2011 Apr 27. Vol. 305 (16). –†. 1659–1668.
23. Gundermann K.J., Kuenker A. –µt al. Activity of essential phospholipids (EPL) form soybean in liver disease // Pharmacological Report. 2011. Vol. 63. –†. 643–659.
24. Knuechel F. Double-blind study in patients with alcoholic toxic fatty liver. Effect of essential phospholipids on enzyme behavior and lipid composition of the serum // Med Welt. 1979. Vol. 30. –†. 411–416.
25. Guo S. Observation on treatment of fatty liver disease with polyene phosphatidylcholine // China Foreign Med J. 2007.
26. Du Q. Treatment of 52 cases with hepatic dysfunctional fatty liver with Essentiale // Chin J Gastro Hepa. 2004. Vol. 13.
27. Liang H. Discussion of treatment of fatty liver using polyene phosphatidylcholine capsules // Chinese med Fact Mine. 2006. Vol. 19.
28. Sun C., Zheng X., Tan Z., Cui F., Zhang R., Zhang H. Clinical observation on polyene phosphatidylcholine and metformin in the treatment of type-2 diabetes and non-alcoholic fatty liver disease // Clin Focus. 2008. Vol. 23.
29. Yin D., Kong L. Observation for curative effect of Essentiale in treatment of fatty liver caused by diabetes mellitus // Med J Q ilu. 2000. Vol. 15. –†. 277–278.
30. Arvind N., Savaikar P., Rajkumar J. Therapy for NAFLD. A comparative study of essential phospholipids vs ursodeoxycholic acid // Indian J Clin Pract. 2006. Vol. 16. –†. 21–24.
31. Xu B., Ren C., Long B. Clinical Observation of 24 Cases of Essentiale Treating Alcoholic Fatty Liver // Sichuan Medical Journal. 2007. Vol. 28. –†. 1116–1117.
32. Sas E., Grinevich V., Kravchuk U., Efimov O. Polyunsaturated phosphatidylcholine reduces insulin resistance and hepatic fibrosis in patients with alcoholic liver disease. Results of randomized blinded prospective clinical study // Journal of Hepatology. 2011. Vol. 54. –†. 207.
33. Kuntz E., Kuntz H.-D. Hepatologie. Springer Press, Heidelberg, 2008.
34. Ratziu V. et al. A proposal for current and future therapeutic strategies for NAFLD // EASL Special Conference «NAFLD/NASH and Related Metabolic Disease», Bologna, Italy, 2009. P. 29.
35. –С—Г–µ–≤–µ—А–Њ–≤ –Р.–Ю., –С–Њ–≥–Њ–Љ–Њ–ї–Њ–≤ –Я.–Ю. –Э–µ–∞–ї–Ї–Њ–≥–Њ–ї—М–љ–∞—П –ґ–Є—А–Њ–≤–∞—П –±–Њ–ї–µ–Ј–љ—М –њ–µ—З–µ–љ–Є: –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Є–µ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є // –Ъ–ї–Є–љ. –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї. 2009. вДЦ 1. –°. 3–9.
36. Ratzui V., Zelber-Sagi S. Pharmacologic therapy of non-alcoholic steatohepatitis // Clin. Liver Dis. 2009. Vol. 13. N 4. P. 667–688.
37. –Т—П–ї–Њ–≤ –°.–°. –Т–ї–Є—П–љ–Є–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–∞–Љ–Є –Є –Љ–µ—В–Є–Њ–љ–Є–љ–Њ–Љ –љ–∞ –ї–Є–њ–Є–і–љ—Л–є —Б–њ–µ–Ї—В—А –њ—А–Є —Б—В–µ–∞—В–Њ–≥–µ–њ–∞—В–Њ–Ј–µ // –†–Ц–У–У–Ъ. 2011. вДЦ 5. –°. 82.
38. –Т—П–ї–Њ–≤ –°.–°. –Ъ–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —В–µ—А–∞–њ–Є—П –Э–Р–Ц–С–Я: —Б—Г–Љ–Љ–∞—Ж–Є—П –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ // –†–Ц–У–У–Ъ. 2011. вДЦ 5. –°. 83.












