В настоящее время достаточно много внимания уделяют метаболическому синдрому. На фоне неуклонного роста числа лиц, страдающих сахарным диабетом, ожирением, злоупотребляющих алкоголем, а также с метаболическим синдромом, все большее значение приобретает проблема жировой болезни печени и холестерин-ассоциированных заболеваний гепатобилиарной системы. В последние годы особый интерес у клиницистов вызывает так называемая холестерин-ассоциированная патология билиарного тракта, основная причина формирования которой — перенасыщение желчи холестерином в результате дефицита желчных кислот.
Для коррекции липидного обмена применяют целый ряд препаратов, оказывающих гиполипидемический эффект, наиболее распространенными из которых являются статины и фибраты. В то же время известно, что гиполипидемический эффект этих препаратов сопровождается перенасыщением желчи холестерином с последующим формированием у части пациентов билиарного сладжа и желчных камней, прогрессированием холестероза желчного пузыря и нарушением функций печени. Эти данные являются существенным аргументом, ограничивающим их применение при холестерин-ассоциированных заболеваниях гепатобилиарной системы [3].
Неалкогольная жировая болезнь печени (НАЖБП) — это приобретенное метаболическое стресс-индуцированное заболевание печени, ассоциированное с инсулинорезистентностью и генетической предрасположенностью. НАЖБП представляет собой одну из важнейших проблем общественного здравоохранения во всем мире в ХХI в. и также становится все более актуальной проблемой в России. Распространенность НАЖБП, по данным разных исследователей, варьирует на фоне повышенного питания, при ИМТ более 28 кг/м2 составляет около 20%, при ожирении II–III степени — уже 55%. Основная цель терапии НАЖБП — профилактика и лечение метаболического синдрома. В соответствии с современными принципами лечения заболеваний печени программа комплексной терапии указанных заболеваний включает два основных направления. Первое — этиотропная терапия, направленная на подавление активности патологического агента-возбудителя, его элиминацию и санацию организма. Второе направление — патогенетическая терапия, которая представляет собой адекватное фармакологическое воздействие на звенья патогенеза заболевания.
До сих пор не утихают споры о роли гепатопротекторов в лечении НАЖБП и отсутствуют стандартные схемы терапии НАЖБП. Необходим анализ клинических исследований, посвященных изучению терапевтических эффектов различных групп лекарственных препаратов. В настоящее время гепатопротекторы могут использоваться в качестве дополнительной терапии в основном при следующих состояниях: у пациентов с подтвержденной биопсией, с выраженным повреждением печени и/или далеко зашедшим фиброзом: у пациентов, которым необходим прием препаратов, способных вызвать поражение печени, или же тех, у кого уровни сывороточных трансаминаз были повышены во время базисной терапии; а также пациентов с сопутствующей активной формой заболевания печени. Переносимость терапии оценивали на основании анализа возникших на фоне лечения нежелательных явлений.
Т. к. курс лечения НАЖБП длительный, то необходим поиск эффективных и доступных комбинированных препаратов, оказывающих гепатопротекторное действие.
На базе поликлиники для творческих работников было проведено открытое неконтролируемое клиническое исследование, цель которого состояла в изучении эффективности и переносимости препарата Эслидин в лечении больных НАЖБП с гиперлипидемией.
Цель исследования. Оценить эффективность и переносимость препарата Эслидин в лечении больных НАЖБП, а также эффективность и влияние Эслидина на липидограмму.
Материалы и методы
В исследование были включены 30 пациентов в возрасте от 26 до 65 лет с верифицированным диагнозом НАЖБП различной степени активности. Диагноз устанавливался на основании повышения активности АлАТ, АсАТ и (или) ферментов холестаза (гамма-глютамилтранспептидаза (ГГТП), щелочная фосфатаза (ЩФ), общий билирубин), показателей липидограммы в сыворотке крови, наличия признаков диффузных изменений — жировой дистрофии печени, выявляемых при ультразвуковом исследовании (УЗИ), а также исключения злоупотребления больными алкоголем (более 40 г этанола в день для мужчин и более 25 г этанола — для женщин), отрицательных результатов серологических реакций на маркеры вирусных гепатитов В и С, отсутствия указаний на употребление гепатотоксичных лекарственных препаратов.
Всем пациентам давали рекомендации по питанию (стол № 5 с ограничением легкоусвояемых углеводов и жиров) и назначали Эслидин по схеме: по 2 таблетки 3 р./сут. Обследование проводили в 1-й, 28-й и 84-й дни лечения. Для определения эффективности терапии оценивали следующие показатели: динамику клинических симптомов (астеновегетативный, диспепсический, тяжесть в правом подреберье по балльной системе), биохимических показателей функции печени (изменение маркеров цитолиза, холестаза), также оценивали показатели липидограммы. Для коррекции липидного обмена применяют целый ряд препаратов, оказывающих гиполипидемический эффект, наиболее распространенными из которых являются статины и фибраты. В то же время известно, что гиполипидемический эффект этих препаратов сопровождается перенасыщением желчи холестерином с последующим формированием у части пациентов билиарного сладжа и желчных камней, прогрессированием холестероза желчного пузыря и нарушением функций печени. Эти данные являются существенным аргументом, ограничивающим их применение при холестерин-ассоциированных заболеваниях гепатобилиарной системы [3]. Переносимость терапии оценивали на основании анализа возникших на фоне лечения нежелательных явлений.
Результаты исследования и обсуждение
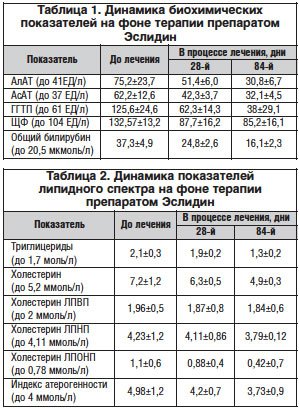
До назначения лечения у 51% пациентов наблюдались признаки астеновегетативного состояния (слабость, утомляемость), 70% больных жаловались на тяжесть в правом подреберье, симптомы диспепсии (тошнота, метеоризм) выявлены у 45% пациентов. На фоне лечения улучшение самочувствия отмечали 93,0% пациентов, особенно через 3 мес. после приема препарата и соблюдения рекомендаций по диетическому питанию. При динамическом наблюдении было установлено, что на 28-й день достоверно уменьшились слабость, утомляемость, симптомы диспепсии, симптом правого подреберья. На 84-й день терапии такие симптомы, как астеновегетативный и тошнота, были купированы полностью, у 6% (n=4) пациентов продолжали оставаться периодическая незначительная тяжесть в правом подреберье, симптомы диспепсии различного характера и степени выраженности, это было связано с имеющимся у них сопутствующим холецистолитиазом, невозможностью соблюдать диету и режим питания. В целом, соблюдая рекомендации относительно диетического питания, 51% пациентов в среднем похудели на 2,5–5 кг. При оценке изменений биохимических показателей на фоне проводимой терапии также отмечалась положительная динамика. Достоверно снизилась активность сывороточных ферментов: АлАТ, АсАТ, ГГТП (табл. 1) уже через 28 дней лечения, а также достоверно снизились показатели липидограммы.
До лечения показатель АлАТ был повышен у 30 больных в среднем до 75,2±23,7 ЕД/л, после 28-го и 84-го дней лечения активность АлАТ нормализовалась у всех исследуемых пациентов, по сравнению с исходными данными эти показатели снизились до 51,4±6,0 ЕД/л и 30,8±6,7 ЕД/л (через 28 и 84 дня соответственно).
До лечения значение АсАТ было повышено у 30 больных в среднем до 62,2±12,6 ЕД/л, после 28-и 84-х дней лечения активность АсАТ нормализовалась у всех пациентов, по сравнению с исходными данными эти показатели снизились до 42,3±3,7 ЕД/л и 32,1±4,5 ЕД/л (через 28 и 84 дня соответственно). Синдром холестаза встречался до лечения немного реже, чем симптом цитолиза: повышенный показатель ГГТП до 125,6±24,6 ЕД/л выявлен у всех пациентов, повышение ЩФ до 132,57 также отмечалось у большинства больных, общего билирубина — у всех пациентов. Через 28 дней после лечения ГГТП нормализовалась у 19 пациентов, а через 84 дня у всех больных этот показатель был в пределах нормы. После завершения лечения содержание билирубина и ЩФ у всех пациентов было нормальным.
Как видно из таблицы 2, произошло снижение всех показателей липидного спектра, что в комплексе дает возможность оценить эффективность препарата Эслидин не только как гепатопротективную, но и липидоснижающую.
По всем шкалам опросника SF-36 у пациентов было установлено снижение качества жизни как по физическим, так и психологическим составляющим. После проведенной препаратом Эслидин терапии на фоне улучшения общего состояния пациентов, а также нормализации показателей крови обнаружено достоверное (р>0,05) улучшение физического и психологического компонентов качества жизни.
Согласно результатам УЗИ печени, достоверно значимых изменений ее размеров выявлено не было в связи с непродолжительностью курса лечения (3 мес.). Побочных эффектов при проведении лечения не было отмечено ни в одном случае.
Выводы
Применение препарата Эслидин в терапии НАЖБП с повышенным липидным спектром приводит к улучшению самочувствия пациентов, нормализации биохимических показателей, нормализует липидограмму, предотвращает прогрессирование болезни, а все это улучшает качество жизни пациентов. Поэтому при отсутствии факторов риска развития сердечно-сосудистой патологии у больных с холестерин-ассоциированной патологией билиарного тракта, протекающей на фоне умеренно выраженной гиперхолестеринемии, лечение комбинированными гепатопротекторами позволяет добиться липидкорригирующего эффекта без применения статинов [5].













