По данным Росстата, в России по сравнению с соответствующими периодами 2010 и 2009 гг. (январь – август) эпидемиологическая обстановка характеризовалась ростом среди населения заболеваемости острым гепатитом В и С. Так, заболеваемость острым гепатитом В за январь – август 2011 гг. к 2010 г. составила 83,3%, за этот же период 2010 г. к 2009 г. – 77,7%. Аналогичные показатели заболеваемости острым гепатитом С составили 94,1 и 87,2% соответственно [1]. Следует отметить, что в 85% случаев острый вирусный гепатит приобретает хроническое течение.
Стабильно высокими сохраняются показатели заболеваемости хроническим гепатитом: за январь – август 2011 г. – 39,95 человека на 100 тыс. человек, за аналогичный период 2010 г. – 39,81 на 100 тыс. [2].
На фоне неуклонного роста числа лиц, страдающих сахарным диабетом (заболеваемость в 2010 г. составила 226,6 человека на 100 тыс. населения, в 2000 г. – 11,3 на 100 тыс.) [1], ожирением, метаболическим синдромом, злоупотребляющих алкоголем, все большее значение приобретает проблема жировой болезни печени (ЖБП).
В последние годы значение лекарственных поражений печени существенно возросло, что объясняется либерализацией доступа населения к лекарственным препаратам безрецептурного отпуска и часто агрессивной рекламой при отсутствии адекватной информации об их возможном побочном действии [3]. В связи с этим клиницистам нередко приходится сталкиваться с токсическими, в первую очередь лекарственно индуцированными поражениями печени, несмотря на изъятие препаратов, скомпрометировавших себя, или строгие ограничения их использования. Тем не менее существует более 1000 лекарственных субстанций, вызывающих гепатотоксические реакции. Побочные эффекты лекарственных препаратов служат причиной развития гепатита у 40% пациентов старше 40 лет [3].
В соответствии с современными принципами лечения заболеваний печени программа комплексной терапии указанных заболеваний включает два основных направления. Первое – этиотропная терапия, направленная на подавление активности патологического возбудителя (патологического агента), его элиминацию и санацию организма. Второе направление – патогенетическая терапия, которая представляет собой адекватное фармакологическое воздействие на различные звенья патогенеза заболевания.
В целом ассортимент лекарственных препаратов, применяемых в комплексной терапии заболеваний печени и желчевыводящих путей, насчитывает сотни наименований. Однако среди такого многообразия выделяют сравнительно небольшую группу лекарственных препаратов, оказывающих преимущественное воздействие на печень, – гепатопротекторы.
Более 40 лет назад были сформулированы ставшие классическими требования, которыми должен обладать идеальный гепатопротектор. Это препарат, полностью всасывающийся при приеме внутрь, имеющий эффект «первого прохождения» через печень, способный связывать токсины или предотвращать их образование, уменьшать воспаление и подавлять фиброгенез, стимулировать регенерацию клеток печени и улучшать их метаболизм, не являющийся собственно токсичным, обладающий экстенсивной (связанной с количественным, а не качественным изменением) энтерогепатической рециркуляцией [4].
В современной клинической гепатологии применяется множество препаратов, обладающих доказанными или предполагаемыми гепатопротективными свойствами, подразделяемых на 3 большие группы:
• препараты растительного происхождения (различные лекарственные формы расторопши пятнистой, чистотела, дымянки, артишока, цикория, тысячелистника, кассии и т.д.);
• препараты животного происхождения (гидролизаты экстракта печени крупного рогатого скота);
• препараты синтетического происхождения.
Некроз гепатоцитов, жировая инфильтрация гепатоцитов, интра– и экстралобулярный холестаз, фиброз являются теми патологическими процессами, при которых используются гепатопротекторы.
В последние годы в мире возродился интерес к группе гепатопротекторов животного происхождения, имеющих давнюю историю: первые публикации относятся к концу XIX – началу XX века [5].
Говоря о гепатопротекторах животного происхождения, можно отметить сравнительно новый для нашей страны немецкий препарат Прогепар® («Нордмарк Арцнаймиттель ГмбХ&Ко»), оказывающий комплексное воздействие на гепатоциты и применяемый в различных странах мира (в первую очередь, в Германии и Японии) для лечения цирроза печени, печеночной недостаточности, лекарственных и токсических гепатитов.
Прогепар® представляет собой гидролизат печени молодых бычков в возрасте до 6 мес., получающих однотипный рацион питания, тестируемых на наличие прионных заболеваний и проходящих обязательный ветеринарный контроль (поэтому опасения касательно потенциальной опасности заражения в первую очередь губчатым энцефалитом абсолютно беспочвенны), обогащенный цианокобаламином, холином, миоинозитолом и цистеином. Действующими компонентами препарата (для 1 таблетки) являются: 70,0 мг гидролизата печени молодых бычков, 21,5 мг цистеина гидрохлорида (что соответствует 16,57 мг L–цистеина), 100 мг холина гидротартрата, 25 мг миоинозитола и 1,5 мкг цианокобаламина.
Самым важным компонентом препарата Прогепар® признан гидролизат печени, в состав которого входят незаменимые аминокислоты, олигопептиды, нуклеозиды и эссенциальные микроэлементы. Холин и миоинозитол являются донаторами, а цианокобаламин – переносчиком метильных групп, необходимых для синтеза фосфолипидов, цистеин – донатором сульфгидрильных групп, необходимых для осуществления обезвреживающей функции и работы системы антиоксидантной защиты. Микроэлементы могут оказывать гепатопротекторное воздействие: к элементам, поддерживающим функцию печени, относятся Al, Cr, Fe, Mg, Se, Zn, Mn, V, Cu, Co; к элементам, способствующим восстановлению кроветворения, – Ni, Zn, Cu, Mn, Mo, Co, Fe; к элементам, поддерживающим обмен углеводов, – V, Mg, BR, Cr, Zn, Mn, Se. Особо следует отметить, что Прогепар® – источник хорошо усвояемого «органического» хрома, что позволяет покрывать более 50% суточной потребности в этом микроэлементе. В целом микроэлементный состав Прогепара® – важная составляющая терапевтического действия лекарственного препарата. Патогенетическим обоснованием для использования препарата является то обстоятельство, что Прогепар® состоит из натуральных эссенциальных фосфолипидов, поставляющих клеткам печени необходимые структурные элементы, помогающих гепатоцитам точно подстраивать фосфолипидный ресурс под текущие потребности клеток [6].
Экспериментальные исследования, проводившиеся в нашей стране и за рубежом, свидетельствуют о целесообразности применения данного препарата для лечения хронических диффузных заболеваний печени. Так, в работе Демидова В.И. и соавт. [7], выполненной на белых крысах линии Вистар при экспериментальном повреждении печени алкоголем и парацетамолом, было показано улучшение функционального и структурного состояния печени на фоне приема Прогепара®, причем гепатопротективный эффект был особенно заметен на алкогольной модели поражения печени. У экспериментальных животных, которым после приема гепатотоксических веществ (парацетамол, алкоголь) вводили Прогепар®, уровень патологического состояния гепатоцитов (дистрофия, некроз) оказался сравнительно ниже, а регенеративные изменения были более выраженными.
В работах Волкова А.Ю. и соавт., Тогузова Р.Т. и соавт. [8, 9] было доказано, что Прогепар® содержит крайне низкую концентрацию токсических элементов. Этот факт подтверждает высокую степень очистки лекарственного препарата. Установлено значительное содержание липоевой кислоты (кофактор энергетического метаболизма гепатоцитов и других клеток), тетрагидрофолата (регулятора деления клеток), подтверждена спецификация производителя о содержании цианокобаламина. Эти биологически активные компоненты вносят значительный вклад в компенсацию суточных потребностей данных микронутриентов и, более чем вероятно, в реализацию гепатопротекторного эффекта.
В более ранних экспериментальных работах зарубежных коллег [10–13], выполненных in vitro и на крысах линии Вистар, установлено, что применение Прогепара значимо нейтрализовало токсическое воздействие тетрахлорметана или алкоголя, улучшало синтез АТФ в гепатоцитах, белково–синтетическую функцию, снижало уровень свободного коллагена, уменьшало количество пораженных жировой инфильтрацией гепатоцитов, при этом возрастало кровоснабжение ткани печени. При экспериментальном воспроизведении инфекционного процесса с использованием пневмококков, паратифозных микроорганизмов при лечении гидролизатом печени повышалась выживаемость гепатоцитов. Препарат стимулировал фагоцитоз и образование антител.
Первые клинические исследования препарата на основе гидролизата печени для лечения ее хронических заболеваний стартовали в Японии в 1957 г. В ряде работ были доказаны положительная динамика клинико–биохимических показателей состояния печени, антифибротическое действие препарата, что способствовало началу широкого клинического применения данной группы лекарственных препаратов в качестве базисного средства лечения хронических заболеваний печени.
В более позднем двойном слепом плацебо–контролируемом исследовании японскими авторами [14] также была подтверждена высокая терапевтическая активность гидролизатов печени для лечения хронического гепатита. В общей сложности 556 пациентам с гистологически подтвержденным хроническим гепатитом провели трехмесячный курс лечения таблетированными препаратами гидролизата печени (монокомпонентным (Прогепарум S) или комбинированным (Прогепарум таблетки), или плацебо). Было показано, что при сравнении степени изменения биохимических показателей, отражающих состояние функции печени (АСТ, АЛТ, ГГТП, тимоловая проба, γ–глобулин), в группах приема комбинированного препарата и плацебо имели место достоверное улучшение в 1–й группе (р<0,001) и значительное улучшение функции печени на фоне терапии комбинированным препаратом по сравнению с приемом монокомпонентного (р<0,05). Частота развития побочных эффектов (ощущение дискомфорта в эпигастрии, тошнота, учащенное мочеиспускание, головная боль), которые не потребовали прекращения терапии, не превысила 4%. Авторы пришли к заключению, что эффективность пероральных препаратов гидролизата печени обусловлена восстановлением поврежденных гепатоцитов и, соответственно, уменьшением активности патологического процесса в печени.
Имеется целый комплекс работ немецких авторов, доказавших клиническую эффективность и безопасность Прогепара® [15–18] в лечении пациентов, страдавших хроническими диффузными заболеваниями печени.
В 2009 г. Прогепар® зарегистрирован в России в группе гепатопротекторных средств (код АТХ: А05ВА), появились первые сообщения отечественных авторов о его клинической эффективности [19].
В 2010 г. с целью изучения эффективности и безопасности Прогепара® при курсовом назначении в течение 2 мес., с общим сроком наблюдения 4 мес., в Ивановской государственной медицинской академии было проведено исследование эффективности препарата у пациентов, страдавших хроническим алкогольным гепатитом [20, 21]. Важно, что рандомизированный дизайн данного контролируемого исследования позволил разделить эффекты препарата и других терапевтических влияний, установить спектр клинического воздействия Прогепара® в группе пациентов с алкогольным гепатитом. Всего в исследовании приняли участие 60 пациентов в возрасте от 25 до 45 лет.
Было доказано, что в составе комплексной терапии на фоне приема Прогепара® отмечается улучшение клинического течения заболевания (снижение частоты расстройств со стороны органов пищеварения) и показателей функционального состояния печени (АСТ, АЛТ, билирубин, альбумин, тимоловая проба), причем положительная динамика отмечалась даже в случаях тяжелой прогрессирующей формы заболевания. По сравнению с группой контроля прием Прогепара® оказал статистически достоверное комплексное воздействие на организм пациента, помимо улучшения показателей функционального состояния печени отмечены уменьшение выраженности системного воспаления (улучшение показателей количества лейкоцитов и уровня интерлейкина–6), снижение клинических проявлений полигиповитаминоза (прежде всего гиповитаминозов В5, В6, РР и А), улучшение биохимических показателей функции почек. Авторы пришли к убеждению, что комплексный механизм воздействия препарата указывает на возможность его применения для гепатопротекции.
Многолетний опыт успешного применения Прогепара® для лечения хронических диффузных заболеваний печени в Японии и Германии, специфика потребления потенциально гепатотоксичных веществ в нашей стране, увеличение числа пациентов, страдающих сахарным диабетом, метаболическим синдромом, ожирением и, как следствие, ЖБП, подтверждает целесообразность введения данного препарата в широкую клиническую практику в России.
Учитывая вышеизложенное, нами было проведено простое открытое несравнительное исследование клинической эффективности и безопасности препарата Прогепар® при курсовом лечении ЖБП (стеатогепатита) в течение 3 мес. Исследование соответствовало этическим стандартам локального этического комитета поликлиники, разработанным на основе «Правил клинической практики в РФ» согласно Федеральному закону от 12.04.2010 № 61–ФЗ «Об обращении лекарственных средств». Все пациенты дали письменное информированное согласие на участие в исследовании, им была предоставлена подробная информация о проводимом исследовании, препарате Прогепар®.
Согласно разработанному дизайну исследования перед его началом (визит скрининга) и после завершения (через 12 нед. терапии, на 84–92–й день) каждый пациент прошел полное клиническое и лабораторно–инструментальное обследование. На 4–й (28–30–й день) и 8–й нед. (56–60–й день) приема препарата («промежуточные» визиты) проводились оценка физикального статуса и регистрация возможных побочных эффектов. Критериями включения служили наличие ЖБП (стеатогепатита), возраст от 18 до 70 лет, отсутствие признаков вирусного, аутоиммунного или лекарственного гепатита/цирроза печени, почечной недостаточности. Критериями исключения служили вирусный, аутоиммунный или лекарственный гепатит/цирроз печени, прием других гепатопротекторов, беременность и лактация, наличие онкологических заболеваний.
После включения больного в исследование Прогепар® назначался по 2 таблетке 3 раза ежедневно (пациент проглатывал таблетку целиком, не разжевывая, запивая достаточным количеством жидкости) в течение 12 нед.
В исследование было включено 36 больных (15 мужчин и 21 женщина, средний возраст – 57,2±6,8 года), страдавших ЖБП (стеатогепатитом). Диагноз заболевания основывался на тщательном анализе характера жалоб и данных анамнеза, результатах физикального обследования, лабораторных (общие анализы крови и мочи, биохимическое исследование крови: билирубин, глюкоза, белок, протромбин, холестерин, триглицериды, мочевина, креатинин, мочевая кислота, АсАТ, АлАТ, ЩФ, ГГТП) исследований и УЗИ печени и селезенки, допплерографии артерий и вен печени (рис. 1).
Анализ характера жалоб во время первого визита показал, что чувство тяжести, ощущение дискомфорта в правом подреберье беспокоили 28 (77,8%) больных, на боль в правом подреберье жаловались семеро (19,4%), жалобы на проявления диспепсии (тошнота, ощущение горечи во рту, снижение аппетита) и изжогу предъявляли 30 (83,3%) и 12 (33,3%) пациентов, у 19 (52,8%) отмечались признаки астенического синдрома (слабость, утомляемость, раздражительность, снижение работоспособности, настроения), в 4 случаях (11,1%) – кровоточивость десен.
Согласно анамнестическим данным длительность заболевания составила от 2 до 9 лет. У всех больных в последние 9–12 мес. до включения в исследование отмечалось стабильное повышение уровней АСТ, АЛТ и γ–ГТ в 1,5–2 раза. 12 пациентов полностью отрицали употребление алкогольных напитков, 13 курили по 10–20 сигарет в день.
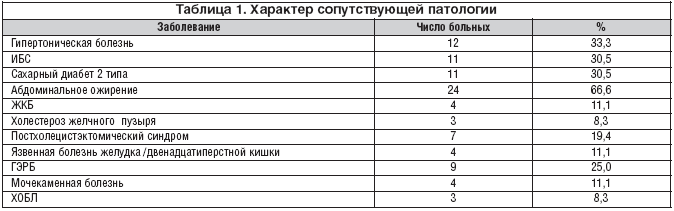
Из сопутствующих заболеваний (табл. 1) необходимо выделить гипертоническую болезнь (12 случаев), сахарный диабет и ИБС (по 11), ГЭРБ и ЖКБ (9 и 8 соответственно), по поводу которых проводилась базисная терапия.
При осмотре у 4 больных были выявлены телеангиоэктазии, у 7 перкуторно отмечалось увеличение размеров печени, у 16 – умеренная болезненность при пальпации правого подреберья, у шести – положительные «пузырные» симптомы. Абдоминальное ожирение диагностировано в 24 случаях (43,7%), при этом в качестве критериев использовали два антропометрических показателя: индекс массы тела (ИМТ≥30,0 кг/м2) и окружность талии (ОТ≥80 см у женщин и 94 см – у мужчин).
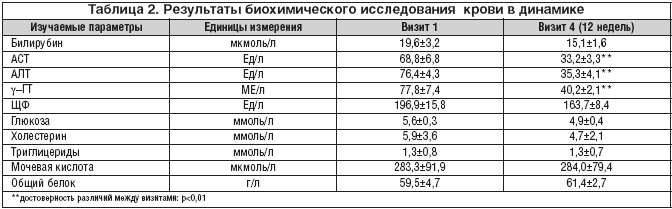
В общих анализах крови и мочи диагностически значимых изменений отмечено не было, в то время как при биохимическом исследовании крови зафиксировано повышение уровней билирубина, АСТ, АЛТ, ЩФ, γ–ГТ и холестерина (табл. 2).
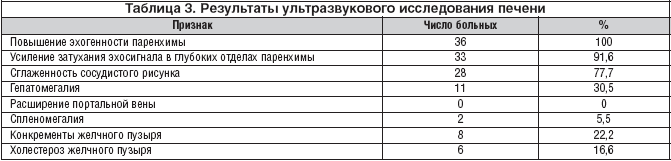
Во всех 36 случаях УЗИ выявило признаки стеатоза печени различной степени выраженности (табл. 3). Допплерографическое исследование портальной гемодинамики (диаметр, объемная скорость кровотока, индекс резистентности в общей печеночной и селезеночной артериях, воротной и селезеночной венах) не зафиксировало изменений, свидетельствовавших об остром гепатите или развитии цирроза печени. У 3 больных (8,3%) в процессе обследования диагностирован холестероз желчного пузыря (имели место множественные полипы), а у 4 (у троих впервые) – конкременты желчного пузыря (11,1).
Проведенная 32 больным ЭГДС не выявила признаков варикозного расширения вен пищевода. Всем пациентам перед началом терапии препаратом Прогепар® рекомендовано соблюдение режима питания (диета № 5).
Исследование завершили 34 пациента (двое были исключены из анализа, поскольку не явились на визит № 3). При контрольном визите (на 84–92–й день) физикальный осмотр не выявил значимых отклонений, как и клинический анализ крови и мочи. Соблюдение рациональной диеты привело к незначительной потере веса (на 2,5–3 кг) у 10 пациентов.
Контрольное УЗИ печени не выявило существенного изменения эхографической картины.
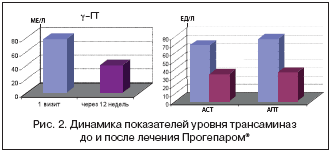
Положительная динамика была достигнута в биохимических показателях крови (рис. 2): зафиксировано статистически достоверное снижение средних уровней трансаминаз – АСТ (t=3,55, p<0,01), АЛТ (t=4,74, p<0,01) и γ–ГТ (t=5,60, p<0,01). Нормализация показателей имела место у подавляющего числа (χ²=4,43, p<0,05, d.f.=1) больных – 26 (72,2%). У оставшихся восьми (22,2%) отмечено их снижение, не достигшее, однако, референтных значений (в среднем на 22,1±2,7%).
Переносимость препарата была хорошей, из нежелательных побочных эффектов отмечались лишь тошнота у двоих больных, появление «печеночного» привкуса у 4 (11,1%), что не помешало им завершить курс лечения. Прием препарата не отразился на клинических проявлениях сопутствующих заболеваний.
Таким образом, терапия гепатопротектором Прогепар® нормализовала биохимические показатели, отражающие работу печени, и не сопровождалась развитием побочных эффектов, требующих коррекции проводимой терапии. В то же время представленные результаты свидетельствуют о необходимости проведения дальнейших исследований Прогепара®, основанных на современных требованиях доказательной медицины, с целью подтверждения полученных результатов для больных, страдающих как ЖБП (стеатогепатитом), так и другими хроническими диффузными заболеваниями печени.

Литература
1. Официальный сайт Росстата www.gks.ru.
2. Официальный сайт Роспотребнадзора www.rospotrebnadzor.ru.
3. Болезни печени и желчевыводящих путей: Рук–во для врачей / под ред. В.Т. Ивашкина. –2–е изд.– М.: ООО «Издат. дом «М–Вести», 2005. – 536 с.
4. Preisig F. Supplements to the editorial, Liver protection therapy // Schweiz Rundsch Med Prax 1970; 59 (45): 1559–1560.
5. Хортес Х. Медицинише клиник. – 1935. – № 11. – С. 1689.
6. Громова О.А., Торшин И.Ю., Юргель И.С. и соавт. Механизмы действия и клиническая эффективность комбинированного гепатопротекторного препарата Прогепар // Трудный пациент. – 2009. – № 12. – С. 78–82.
7. Демидов В.И., Назаренко О.А., Егорова Е.Ю. и соавт. Эффективность применения Прогепара при экспериментальном повреждении печени алкоголем и парацетамолом: биохимия и гистология // Фарматека. – 2011. – № 2. – С. 36–39.
8. Волков А.Ю., Тогузов Р.Т., Назаренко О.А. и соавт. Микроэлементный состав Прогепара // Клиническая фармакология и фармакоэкономика. – 2010. – № 6. – С. 2–5.
9. Тогузов Р.Т., Мамедов Э.С., Шачнев Е.Н. и соавт. Содержание фолатов и липоевой кислоты в гепатопротекторе Прогепар // Фарматека. – 2010. – № 11. – С. 57–59.
10. Hirayama S. et al. Nisshin Igaku. 1958; 45: 528.
11. Murato T. et al. Японское общество фармакологов. – 1969. – 89 с.
12. Баяши А.О., Акиома Х., Тацаки Х. Воздействие гидролизата печени на циркуляцию крови при хронических заболеваниях печени // Арцнаймиттель Форшунг. – 1972. – № 22. – С. 578–580.
13. Вахтер Х. Влияние гидролизата печени на течение основных инфекций // Арцнаймиттель Форшунг. – 1954. – № 4. – С. 201–208.
14. Fugisava K., Suzuki H., Yamamoto S., Hirayama C., Shikata T., Sanbe R. The therapeutic efficacy of liver hydrolysates in chronic hepatitis // Asian Med. J. – 1983. – Vol. 26. – № 8. – P. 497–526.
15. Беккре В. Лечение цирроза печени с помощью внутривенных инъекций печени // Медицинише Клиник. – 1956. – № 15. – С. 641–645.
16. Бауман В., Кюнкель Б. Терапия цирроза печени с помощью Прогепара // Германский медицинский журнал. – 1953. – № 8. – С. 257–260.
17. Йессбергер И. Динамика свободных сульфгидридных групп в крови после введения гидролизата печени // Актагепатологика. – 1956. – № 4. – С. 7–10.
18. Koizumi B., Sarcy L. Klinische Medizine und Forschung. – 1972. – Vol. 49. – № 1. – P. 261–269.
19. Грацианская А.Н. Гепатопротекторы в клинической практике: Прогепар // Фарматека. – 2010. – № 2. – С. 50–53.
20. Егорова Е.Ю., Философова М.С., Торшин И.Ю. и соавт. Сравнительная динамика персистирующей и прогрессирующей форм алкогольного гепатита в комплексной терапии препаратом Прогепар // РМЖ. – 2011. – № 5. – С. 309–313.
21. Егорова Е.Ю., Юргель И.С., Назаренко О.А. и соавт. Рандомизированное контролируемое исследование эффективности препарата Прогепар у пациентов с хроническим алкогольным гепатитом // РМЖ. – 2011. – № 10. – С. 1–10.












