Введение
Гепатопротекторы различаются по механизмам и спектру своего фармакологического воздействия. В 2008 году, в России в группе гепатопротекторных средств (КодАТХ: А05ВА) зарегистрирован препарат «Прогепар». В Германии и Японии этот препарат известен, как «Proheparum S.» От ранее известного препарата «Prohepar» отличается наличием особых синергидных компонентов (что и обозначает литера «S» в названии препарата).
Проведенные за последние 20 лет исследования по клинической, экспериментальной и молекулярной фармакологии указали на гепатопротекторные свойства цианокобаламина, цистеина, холина и миоинозитола [1]. Однако эти гепатопротекторные компоненты никогда ранее не использовались в составе единого препарата. В новом фармакологическом дизайне состав Прогепара представлен следующими действующими компонентами: в 1 таблетке находится 70 мг гидролизата печени молодых бычков, 21,5 мг цистеина гидрохлорида, что соответствует 16,57 мг L–цистеина, 100 мг холина гидротартрата, 25 мг мио–инозитола и 1,5 мкг цианокобаламина. Каждый из этих компонентов через специфические молекулярные механизмы способствует улучшению кровотока в печени, регенерации гепатоцитов и, соответственно, интенсификации репаративных способностей печеночной ткани и процессов I и II стадий детоксикации, что подтверждается в многоцентровых клинических исследованиях [2,3].
Имеющиеся данные по экспериментальной и клинической фармакологии препарата Прогепар и его компонентов указывают на несомненный гепатопротекторный эффект. В эксперименте с моделями острого парацетамолового и хронического алкогольного отравления, гистологическое изучение образцов тканей печени, почек, миокарда показало, что прием препарата приводил к уменьшению степени повреждения паренхиматозных элементов, регенерации паренхимы и улучшению кровообращения [4].
В нашей предыдущей работе [5] была установлена положительная динамика клинических и лабораторных параметров у пациентов с алкогольным гепатитом на фоне приема препарата Прогепар в составе комплексной терапии. И в подгруппе мужчин, и у женщин наблюдалась положительная динамика состояния печени, которая отчасти сохранялась и через 2 месяца после окончания курса. Как при персистирующей, так и при прогрессирующей форме заболевания наблюдалась положительная клинико–лабораторная динамика: снижение уровней маркеров воспаления, уровней билирубина, АСТ, АЛТ и др. Были установлены факторы, ассоциированные с тяжестью заболевания (т.е. с развитием прогрессирующей формы алкогольного гепатита): алкогольный стаж, ежедневное употреблением водки, возраст, повышенная кислотность желудка (p<0,03).
Без группы сравнения установленная положительная динамика не могла быть однозначно отнесена именно к приему препарата. В настоящей работе изложены результаты первого российского рандомизированного контролируемого исследования эффектов препарата Прогепар в группе пациентов с хроническим алкогольным гепатитом в сравнении с группой контроля. Рандомизированный дизайн настоящего исследования позволил разделить эффекты препарата Прогепар и других терапевтических воздействий и установить спектр клинического воздействия препарата в группе пациентов с алкогольным гепатитом.
Дизайн исследования
Настоящее исследование представляет собой рандомизированное контролируемое исследование препарата Прогепар у пациентов, страдающих алкогольным гепатитом (диагноз K70.1 по МКБ–10). Целью исследования являлась оценка эффективности и безопасности использования препарата при курсовом назначении в течение 2 месяцев, с общим сроком наблюдения 4 месяца (рис. 1). Обследование пациентов проводилось на день «0» (до начала приема препарата), день «60» (окончание курсового приема препарата) и день «120» (4 месяца от начала исследования).
Исследование соответствовало этическим стандартам комитетов по биомедицинской этике, разработанным в соответствии с Хельсинкской декларацией с поправками от 2000 года и «Правилами клинической практики в РФ» согласно Федеральному закону от 12.04.2010 N 61–ФЗ «Об обращении лекарственных средств» [6]. Все пациенты дали письменное информированное согласие на участие в исследовании. Все наблюдаемые были подробно информированы о проводимом исследовании, его целях, безопасности применения препарата Прогепар исходя из данных о его составе.
Всего в исследование включено 60 пациентов, мужчины и женщины от 25 до 45 лет. После подписания информированного согласия, проведения скрининга и проверки соответствия пациентов критериям включения/исключения из исследования, проведена рандомизация пациентов в 2 группы:
1. Пациенты первой группы (основная, n=30, 17 мужчин, 13 женщин) получали Прогепар в течение 60 дней по 2 таб. 3 раза в сутки и стандартную терапию. Стандартная терапия включала абстиненцию, нормализацию питания (качество и регулярность приема пищи), нормализацию питьевого режима.
2. Пациенты второй группы (сравнения, n=30, 18 мужчин, 12 женщин) получали стандартную терапию без гепатопротекторов.
Согласно этическим нормам, по окончании участия в исследовании (после 120–го дня) пациенты 2–й группы также получали препарат Прогепар (60 дней по 2 таб. 3 раза в сутки).
Исследуемый препарат Прогепар – таблетки, покрытые оболочкой, в дозах согласно листку–вкладышу: по 2 таб. 3 раза в сутки в течение 2 месяцев. На протяжении исследования пациентов регулярно наблюдали два врача–исследователя, оценивая клинические проявления нарушений функции печени, почек, параметров свертывания крови, активности воспаления и баллов дисвитаминозов. Во время исследования был исключен прием лекарственных средств и БАД, относящихся к группе гепатопротекторов, витаминов, аминокислот, препаратов на основе холина и его производных, а также лецитина.
Критерии включения пациентов:
1. Диагноз K70.1 «Алкогольный гепатит» по МКБ–10.
2. Мужчины и женщины в возрасте 25–45 лет, находящиеся на лечении в гепатологическом отделении стационара.
3. Письменное согласие пациента/пациентки на проведение обследования и лечения в рамках настоящего исследования.
4. Способность пациента к адекватному сотрудничеству в процессе исследования.
Критерии исключения пациентов:
1. Прием других гепатопротекторов.
2. Наличие патологии, требующей хирургического вмешательства.
3. Наличие эндокринных заболеваний (сахарный диабет, метаболический синдром).
4. Признаки тяжелых гематологических, иммунологических, дыхательных, урологических, желудочно–кишечных, печеночных, почечных, метаболических, обменных, психиатрических, дермато–венерологических заболеваний, нарушения питания, признаки коллагенозов, скелетно–мышечных, злокачественных и подобных заболеваний, о которых известно из анамнеза, физикального осмотра и/или лабораторных анализов, которые могут препятствовать участию пациентов в исследовании и оказать влияние на результаты.
5. Беременность
Обследование пациентов
1. Стандартный осмотр врача–терапевта – при скрининге и сразу после завершения приема препарата.
2. Оценка регулярности приема препарата.
3. Клиническая симптоматика пациентов, страдающих алкогольным гепатитом.
4. Клинический анализ крови с подсчетом следующих параметров (эритроциты, гемоглобин, цветной показатель, базофилы, нейтрофилы, эозинофилы, лимфоциты, моноциты, СОЭ) и учетом показателей свертываемости крови (протромбин, протеин С) и воспаления (фактор некроза опухоли, интерлейкин–6).
5. Оценка функции печени по лабораторным критериям биохимического анализа крови (альбумин, билирубин, креатинин, мочевина АЛТ, АСТ, щелочная фосфатаза, общий холестерин и липопротеин высокой плотности).
6. Общий анализ мочи с оценкой концентрирующей функции (удельный вес), а также оценкой оксалатов, уратов, креатинина, белка, а также лейкоцитов и эритроцитов.
7. Оценка гиповитаминозов В1, В2, В5, В6, фолатов, В12, А, Е, D, PP и С по верифицированной балльной шкале.
8. Оценка показателей безопасности использования препарата по клиническим параметрам, наличию аллергологических, диспептических и других осложнений.
Критерии эффективности
– Восстановление нормальных или улучшение показателей крови по биохимическому и общему анализу;
– восстановление нормальных или улучшение показателей свертывания крови;
– восстановление нормальных или улучшение показателей мочи;
– уменьшение выраженности болевого синдрома, отеков, диспептических жалоб, отеков, признаков интоксикации (оценка общего самочувствия, состояния кожи и слизистых, вес и т.д.);
– уменьшение выраженности симптомов алкогольного гепатита;
– нормализация уровня витаминов.
Оценка безопасности
Частота, характер, выраженность, длительность возникающих побочных эффектов и их связь с приемом препарата Прогепар.
Материалы и методы
В данном рандомизированном контролируемом исследовании изучались клинические эффекты препарата Прогепар у пациентов с хроническим алкогольным гепатитом. В ходе работы анализировалась выборка из 60 пациентов (35 мужчин, 25 женщин 25–45 лет) с хроническим алкогольным гепатитом, которая была рандомизирована на прием препарата Прогепар (n=30) или контроль (n=30).
У всех пациентов диагноз «вирусный гепатит» был исключен (сывороточные маркеры гепатита В, С и Д – отрицательные). При верификации диагноза алкогольного гепатита у всех пациентов была установлена отчетливая этиологическая связь заболевания печени с употреблением алкоголя с учетом данных опросника CAGE и анкетирования [7]. У всех пациентов имелось заключение психиатра–нарколога о наличии алкогольной зависимости.
Большинство пациентов (47 из 60) регулярно курили, стаж курения от 5 до 12 лет. При осмотре 60 пациентов на день «0» отмечались тремор конечностей, век и языка, бледность и одутловатость лица, темные круги вокруг глаз, землистый цвет лица. Телеангиоэктазии кожи лица наблюдались у 48 из 60 пациентов.
У 7 пациентов в выборке наблюдалась прогрессирующая форма алкогольного гепатита, у остальных – персистирующая. Персистирующая форма относительно стабильна; при ней сохраняется способность к обратимости воспалительного процесса при условии прекращения приема алкоголя. При продолжении употребления алкоголя персистирующая форма может перейти в прогрессирующую. Прогрессирующая форма алкогольного гепатита характеризуется мелкоочаговым некротическим поражением печени, исходом которого становится, как правило, цирроз печени [5,7].
Гинекомастия отмечалась у 4, гипогонадизм у 9 из 35 мужчин. Среди 60 пациентов, симптом «белые ногти» был найден у 6, асцит – 2, спленомегалия – 11, полинейропатия – 6, гипертрофия слюнных желез – 8, контрактура Дюпюитрена – у 5 пациентов. У всех пациентов отмечалась выраженная астенизация; у 20 пациентов были отмечены периодические перебои в области сердца.
Сбор и анализ данных
Для каждого из пациентов был собран значительный массив данных, включающий более 250 клинических и лабораторных параметров. Массив данных о пациенте включил демографические данные, опросники по потреблению алкоголя и по гастропатогенной диете, верифицированные вопросники по оценке гиповитаминозов [8], общий анализ крови, биохимический анализ крови, уровни фактора некроза опухоли (ФНО–α), интерлейкина–6 (ИЛ–6), анализ мочи и другие параметры, указанные в дизайне исследования. Исследованные функциональные показатели печени включили уровни билирубина, АЛТ, АСТ, уровень альбумина, тимоловую пробу. Сравнение параметров двух групп пациентов на день «0» представлено в таблице 1.
Собранные данные исследовались с использованием как общепринятых статистических технологий обработки данных, так и современных методов интеллектуального анализа данных. Основной статистический анализ данных проводился с помощью электронных таблиц MS Excel и пакета программ «STATISTICA 6.0». Статистическая значимость результатов оценивалась критериями хи–квадрат, парным и гетероскедастическим двусторонним тестом Стьюдента.
Правильность основного статистического анализа данных была исследована и подтверждена современными методами выявления скрытых закономерностей в эмпирических данных с использованием уникальных методов интеллектуального анализа данных, разрабатываемых более 30 лет в научной школе академика РАН, профессора Ю.И. Журавлева [9]. В качестве основного метода анализа данных был использован алгоритм вычисления оценок.
В алгоритмах вычисления оценок (АВО) отражены передовые концепции решения задач распознавания [10]. В модели АВО решение о классификации объекта (например, «есть эффект» – «нет эффекта») принимается с помощью анализа оценок близости объектов (в данном случае объектом является строка описания пациента, состоящая из 250 клинико–лабораторных параметров или «признаков») к классам (т.е. группам пациентов), а не только на основе какого–то фиксированного значения р (такого как р<0,05). Близость — схожесть описаний, малое расстояние между значениями признаков. При этом оценка близости объекта к классу тем выше, чем ближе он к эталонным объектам данного класса и дальше от эталонных объектов других классов. Близость распознаваемого объекта S к эталонному St определяется на основе расстояний pr(ar(S),ar(St)), r=1,2,...,n, и формализуется понятием функция близости. Существуют параметры функции близости (задающие «чувствуемую» степень похожести описаний объектов) ẽ=ẽ1(~Sm,~Sa), настройка которых в процессе анализа данных и позволяет распознавать характерные различия в состоянии пациентов основной и контрольной групп. Анализ полученных данных методом АВО и другими методами интеллектуального анализа данных – предмет отдельного исследования, которое проводится в настоящее время. В данной статье представлены результаты основного статистического анализа данных, подтвержденные анализом данных методов АВО.
Результаты и обсуждение
У пациентов обеих групп наблюдалось улучшение работы печени и почек, снижение показателей воспаления, улучшался аппетит и снижался как общий балл гиповитаминоза, так и баллы гиповитаминозов по отдельным витаминам (В12, В6, В2 и др.). Ко дню «60» у пациентов обеих групп улучшался внешний вид, уменьшался тремор языка, век и конечностей, снижалась отечность лица, улучшался тургор и цвет кожи, нормализовался цвет склер, снижалась патологическая симптоматика со стороны ЖКТ (отрыжка, изжога и др.). В течение всего курса ни у одного из пациентов не было отмечено каких–либо жалоб, связанных с применением препарата.
Следует отметить, что наблюдаемая положительная динамика может быть обусловлена как воздержанием от алкоголя, так и нормализацией диеты, и приемом препарата Прогепар. Рандомизированный дизайн настоящего исследования позволил разделить эффекты этих терапевтических воздействий и продемонстрировать позитивные эффекты собственно препарата Прогепар. Для установления статистической значимости этих изменений необходимо установление однородности групп на день «0» с последующим анализом значимости статистических различий в динамике исследования.
Оценка однородности групп
по исследуемым параметрам на день «0»
На день «0» были проведены сравнения обеих групп по всем 250 анамнестическим, клиническим и лабораторным параметрам, собранным в ходе настоящего исследования. Статистически значимыми являлись отличия только по 4 параметрам: возраст, цветовой показатель крови (ЦП), СОЭ и уровень ЩФ. В группе принимавших препарат, статистическая значимость отличия в среднем возрасте обусловлена присутствием в этой группе двух пациентов 45 лет. При исключении этих 2 пациентов статистически значимая разница в возрасте между группами исчезает (р=0,08).
В норме скорость оседания эритроцитов (СОЭ) у мужчин 0–15 мм/ч, у женщин 0–20 мм/ч. Показатели СОЭ в опытной группе были повышены и у 13 пациентов находились на верхней границе нормы или превышали ее. В контрольной группе СОЭ на верхней границе нормы установлена только у 2 пациентов (χ2 р=0,0022). Повышенное значение СОЭ может указывать на более активные процессы воспаления, интоксикацию, заболевания почек. Однако значимых отличий между группами в других биохимических маркерах воспаления (ИЛ–6, ФНО–α, протеин С, уровни моноцитов, лимфоцитов, базофилов) на день «0» не было.
В группе контроля отмечались более высокие уровни щелочной фосфатазы (ЩФ). В обеих группах наблюдались повышенные уровни ЩФ (норма для мужчин и женщин старше 20 лет – 40–150 Ед/л). Повышенные уровни ЩФ могут указывать не только на патологию костной ткани, но и на заболевания печени (гепатиты, цирроз, онкологические заболевания, паразитарные поражения), холестаз (холангиты, камни) и прием гепатотоксичных химических веществ (парацетамола, антибиотиков, алкоголя). Отметим, что различия в уровнях ЩФ сохранялись на день «60» (группа основная 194±106 ед./л, контрольная группа 2 241±130 ед./л, р=0,06) и на день «120» (группа основная 163±56 ед./л, группа контроля 192±78 ед./л, р=0,05). Значимых отличий в других маркерах функции печени (альбумин, билирубин, АЛТ, АСТ, тимоловая проба) не было выявлено, поэтому маловероятно, что более высокие уровни ЩФ в контрольной группе указывают на более значительное повреждение печени.
Таким образом, опытная и контрольная группы пациентов характеризовались высокой степенью однородности на момент начала исследования. Во время исследования пациенты обеих групп находились в одинаковых условиях стационара. Следовательно, все обсуждаемые далее статистически значимые отличия между группами, которые были выявлены на день «60» и на день «120», следует относить именно к приему препарата Прогепар.
Анализ данных настоящего рандомизированного исследования показал, что прием препарата Прогепар приводил к статистически достоверным изменениям многочисленных клинических и лабораторных параметров, однозначно соответствовавших положительной динамике лечения. К этим параметрам относятся отдельные клинические симптомы, изменения комплексных шкал, основанных на симптоматике гиповитаминозов (баллы гиповитаминоза), данные общего и биохимического анализа крови (в частности, изменения значений маркеров функции печени и маркеров воспаления). Эти изменения подробно рассматриваются в последующих разделах статьи.
Динамика клинической симптоматики
Прием Прогепара способствовал уменьшению числа пациентов с симптоматикой, вызванной хроническим алкогольным отравлением. Прием препарата способствовал снижению кровоточивости десен, глоссита и симптомов расстройства ЖКТ (отрыжка, изжога, повышенная кислотность и диарея, табл. 2). Наиболее достоверные отличия между основной группой терапии и контролем были отмечены на день «60», т.е. непосредственно после окончания приема препарата. Позитивная динамика состояния ЖКТ отчасти сохранялась и на день «120».
Динамика симптоматики гиповитаминозов
Симптоматика гиповитаминозов оценивалась по верифицированным шкалам–опросникам, калиброванным с использованием результатов реального исследования уровней витаминов в крови (средний коэффициент корреляции после калибровки опросников составил r=0,8) [8]. Использование именно верифицированных шкал является эффективным и довольно надежным методом оценки состояния витаминного депо пациентов на основе аккуратного анализа симптоматики гиповитаминозов.
Как известно, у алкоголиков часто наблюдаются симптомы полигиповитаминозов, как вследствие собственно употребления алкоголя (способствующего избыточному диурезу и потере микронутриентов), так и вследствие неадекватного питания [7]. Прием препарата Прогепар способствовал снижению дефицитов различных витаминов (табл. 3). На день «0», между группами не наблюдалось достоверных различий: суммарный балл гиповитаминоза был очень высок и составил 400±33 в основной группе и 399±32 в контрольной группе (р=0,49). По нашим данным, у здоровых россиян, балл гиповитаминоза не превышает 60±15. При других патологиях у пациентов той же возрастной группы (например, частые острые респираторные заболевания, артериальной гипертонии, миопией, бесплодием, ПМС и др.) суммарный балл гиповитаминоза не превышал 300.
На день «60», балл полигиповитаминоза в контрольной группе снизился до 365±30, в то время как в группе принимаших Прогепар снизился до 310±24 (р=1,4.10–10 для сравнения двух групп). На день «120» в группе контроля не наблюдалось дальнейшего снижения балла полигиповитаминоза (367±30), в отличие от основной группы (300±27, р=1,1.10–12, рис. 2).
Из исследованных витаминов в состав Прогепара входят только витамин В12 (цианокобаламин) и фолаты экстракта печени [11]. В то же время за исключением витамина D снижался балл всех исследованных гиповитаминозов. Положительная динамика клинической картины обеспеченности витаминами объясняется тем, что Прогепар способствовал восстановлению функций печени, которая, в частности, является центральным биосинтетическим депо большинства витаминов. Одним из возможных объяснений отсутствия положительной динамики по витамину D является то, что исследование проводилось в зимний период (ноябрь 2010 – март 2011 гг.), когда дефицит витамина D наиболее интенсивен вследствие низкой инсоляции [12,13].
Следует отметить, что баллы гиповитаминозов различались по характеру динамики. В группе принимавших Прогепар падение баллов большинства гиповитаминозов (В2, В5, В6, А, С, Е, РР) наблюдалось на день «60» и сохранялось ко дню «120». В случае витамина В1 и фолатов статистически значимая разница в баллах была достигнута ко дню «120». В случае витамина В12 (который, как известно, синтезируется и хранится практически исключительно в печени и является «классическим» витамином–гепатопротектором [12,14]) гиповитаминоз значимо уменьшался к концу курса приема препарата (день «60»), но различия между группами терялись к 120–му дню исследования. Известно, что обмен витамина В12 у пациентов с алкогольным гепатитом сильно подавлен и требует персонализированного восстановительного курса приема витамин В12–содержащих препаратов.
Динамика клинико–лабораторных показателей
В ходе исследования у пациентов проводился общий и биохимический анализ крови, общий анализ мочи, определялись уровни маркеров воспаления. В то время как на день «0» между группами наблюдались отличия в значениях всего лишь трех показателей (ЦП, СОЭ, ЩФ, см. выше), к концу курса терапии и через 2 месяца после окончания лечения статистически достоверные отличия были зарегистрированы более чем для 10 показателей. В таблице 4 суммированы данные только по статистически значимым отличиям в значениях исследованных клинико–лабораторных показателей. Биохимические показатели, являющися маркерами функции печени, рассмотрены в следующем разделе.
Изменения показателей, представленных в таблици, указывают на снижение воспаления и на положительную динамику состояния функции почек. Одним из главенствующих механизмов алкогольного повреждения печени является высокий уровень воспаления и усиление синтеза/секреции провоспалительных цитокинов (в частности, цитокинов ИЛ–6 и ФНО–α). На фоне абстиненции и применения Прогепара происходило снижение уровней маркеров воспаления (лимфоциты, СОЭ, ИЛ–6, ФНО–α).
Нами была отмечена положительная динамика во всех исследованных маркерах воспаления [5]. Например, в группе принимавших Прогепар уровни ИЛ–6 снижались от 5,6±1,2 пг/мл на день «0» до 4,9±0,6 пг/мл на день «60» (рис. 3); уровни ФНО–α снижались от 11,8±2,5 пг/мл на день «0» до 10,8±2,4 пг/мл на день «60» (р=0.057). Рандомизированный дизайн подтвердил статистическую значимость снижения уровней всех маркеров воспаления за исключением ФНО–α (табл. 4). Сравнение с группой контроля показало достоверное снижение СОЭ (несмотря на различия в день «0», см. ранее), лимфоцитов (р=0,04, день «120») и ИЛ–6 (р=0,006, день «60»).
Результаты коагуляционных тестов (протромбин, протеин С) также являются косвенным указателем на интенсивность воспалительных процессов – чем выше степень воспаления, тем, как правило, выше и свертываемость крови. Значение протромбинового теста (референсные значения 78–142%) было повышено в обеих группах на день «0» (что указывает на склонность к тромбозу и возможную гипогидратацию вследствие увеличения вязкости крови) и нормализовалось на фоне приема Прогепара (р= 3.10–5, день «60»). Протеин С – один из наиболее важных физиологических ингибиторов свертывания (норма для взрослых : 70–140%) и его уровни возрастали к концу курса приема препарата (р=0,005).
Как показали данные проведенного нами ранее экспериментального исследования препарата, Прогепар проявляет не только гепатопротекторные, но и нефропротекторные свойства. Сравнительный гистологический анализ тканей печени, почек и миокарда указал на отчетливую положительную динамику при употреблении Прогепара животными с хроническим алкогольным и острым химическим (парацетамол) поражениями печени [4]. В частности, гистологический анализ указал на то, что прием Прогепара способствует снижению воспаления и уменьшению апоптотических процессов в тканях почек. В настоящем клиническом исследовании у пациентов наблюдались согласованные изменения ряда биохимических маркеров, указывающие на улучшение работы почек (снижение оксалатов и белка в моче, снижение креатинина и мочевины плазмы, увеличение уровней альбумина).
Белок в моче – неспецифический симптом патологии почек. Когда клубочковая и канальцевая фильтрация в норме, содержание белка в моче должно быть равно 0. Небольшое количество белка в моче (физиологическая протеинурия) может быть и у здоровых людей, но выделение белка с мочой не превышает в норме 0,08 г/сут в покое и 0,25 г/сут при интенсивных физических нагрузках. Наличие белка в моче может указывать на нарушения абсорбции в почечных канальцах, инфекции мочевыводящих путей, нефротический синдром, гломерулонефрит. В настоящем исследовании число пациентов с ненулевыми уровнями белка в моче значимо уменьшалось на фоне приема препарата Прогепар (р=0,02..0,06, см. табл. 4) по сравнению с контрольной группой.
Кристаллы оксалата кальция являются одной из химических основ почечных камней. Наличие повышенных уровней оксалатов в моче может быть обусловлено употреблением в пищу продуктов, богатых щавелевой кислотой, пиелонефритом или вследствие отравления этиленгликолем (что возможно при употреблении низкокачественного алкоголя). Прием Прогепара способствовал снижению числа пациентов, имеющих оксалаты в осадке мочи, от 8 человек на день «0» до 2 человек на день «60» (р=0,04), чего не наблюдалось в контрольной группе.
В норме креатинин фильтруется в гломерулах почек и не подвергается реабсорбции или секреции в канальцах. Повышение уровня креатинина в крови обычно свидетельствует о снижении фильтрации в почечных клубочках и понижении выделительной функции почек и может быть обусловлено приемом нефротоксических веществ, возможно при увеличенной концентрации в крови таких эндогенных метаболитов, как глюкоза, фруктоза, мочевина, преобладанием мясной пищи в рационе и обезвоживанием. Референсные значения креатинина для взрослых составляют 53–97 мкмоль/л для женщин и 80–115 мкмоль/л для мужчин. Прием препарата Прогепар коррелировал со статистически значимым снижением средних уровней креатинина от 83±9 до 67±6 мкмоль/л (р=0,0005), при этом эффект был значим как в подгруппе мужчин, так и у женщин.
Осмотически активная мочевина играет важную роль в механизмах концентрирования мочи почками. В норме уровни мочевины в крови у взрослых должны составлять 2,5–6,4 мкмоль/л. Повышение уровня мочевины связано с ослабленной выделительной функцией почек вследствие гломерулонефрита, пиелонефрита, приема нефротоксичных веществ, дегидратацией. Понижение уровня мочевины ниже референсных значений может быть связано с нарушением функции печени (нарушается синтез мочевины). В настоящем исследовании на день «0» у пациентов обеих групп наблюдались более высокие уровни мочевины (5,2±1,1 мкмоль/л), хотя и находившиеся в пределах нормы. Прием Прогепара приводил к статистически значимому снижению уровней мочевины (до 3,6±0,4 мкмоль/л на день «60», р=3.10–6) по сравнению с контрольной группой.
Альбумин (норма для взрослых 18–60 лет: 35–52 г/л) – основной белок крови, поддерживает онкотическое давление плазмы, и, соответственно, объем циркулирующей крови. Снижение уровня альбумина связано с несбалансированной по аминокислотному составу диетой, гастроэнтеропатией (расстройства ЖКТ действительно наблюдались у пациентов, см. выше), дисфункцией печени и хронической почечной патологией. В исследовании уровни альбумина значимо возрастали ко дню «60» (от 42±7 г/л до 51±7 г/л, р=0,002) по сравнению с контролем.
Динамика маркеров функции печени
на фоне приема Прогепара
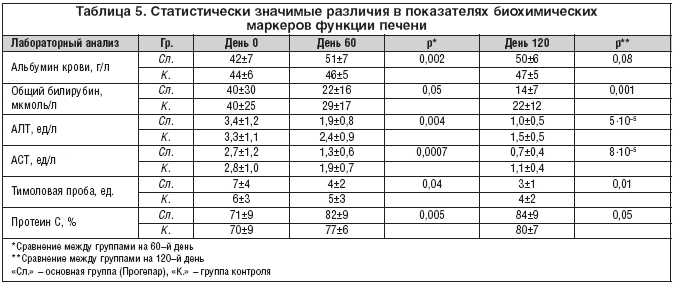
В экспериментальных [4] и клинических исследованиях [2,3,5], прием препарата Прогепар, содержащего короткоцепочечные пептиды экстракта печени и синергидные компоненты, приводил к достоверным улучшениям в функции печени. В настоящем рандомизированном исследовании сравнение с группой контроля показало достоверные эффекты препарата (табл. 5), приводящие к улучшению функциональных показателей печени (билирубин, АСТ, АЛТ) и, в частности, белково–синтетической функции печени (альбумин, тимоловая проба, протеин С).
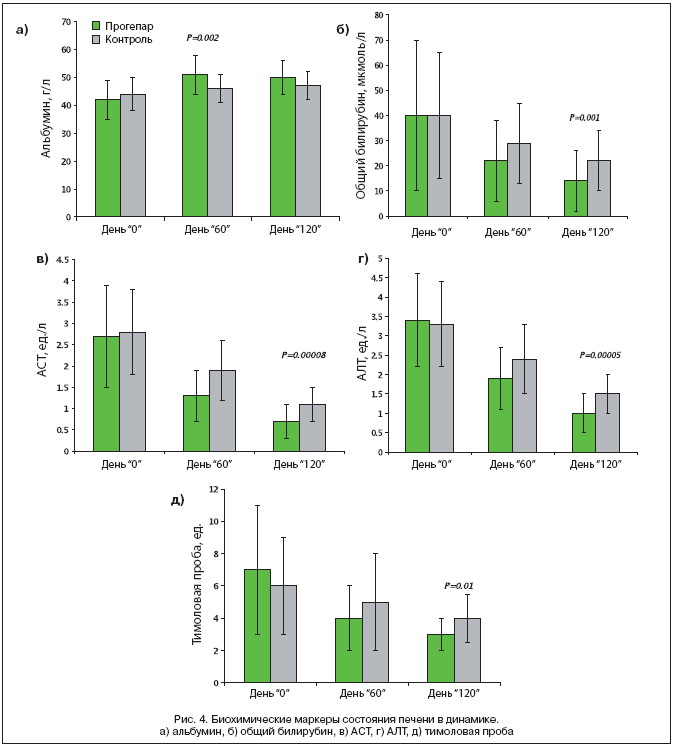
В исследованной выборке пациентов, получавших комплексную терапию, наблюдалась положительная динамика практически всех изученных клинико–лабораторных показателей функции печени (рис. 4). Уменьшались уровни билирубина, печеночных трансаминаз АЛТ и АСТ; увеличивались уровни альбумина и улучшались показатели тимоловой пробы.
Прием препарата Прогепар приводил к улучшению показателей биосинтетической функции печени – альбумина, протеина С и тимоловой пробы. Синтез альбумина происходит в печени. Альбумин выполняет транспортную функцию, связываясь с билирубином, желчными кислотами, ионами металлов и снижение уровня этого белка – также указывает на хронические заболевания печени (гепатиты, цирроз, атрофия, карцинома). Протеин С – синтезируемый в печени физиологический ингибитор свертывания крови и понижение уровня протеина С указывает на снижение синтетической функции. Повышенный уровень тимоловой пробы соответствует диспротеинемии – нарушению биосинтеза мелкодисперсных белков, так что снижение значений тимоловой пробы также указывает на восстановление белково–синтетической функции печени.
Выводы
Комплексная терапия хронического алкогольного гепатита требует использования эффективных многофункциональных гепатопротекторов, способствующих сохранению и восстановлению поврежденных алкоголем тканей печени. Терапевтическое воздействие препарата более эффективно, когда препарат сочетает гепатопротекторный, антифибротический и детоксикационный эффекты. Фармакологический дизайн препарата Прогепар (стандартизированный экстракт печени, цианокобаламин, миоинозитол, холин, цистеин) отвечает этим требованиям. Компоненты Прогепара оказывают комплексное воздействие на печеночный метаболизм, способствуя восстановлению гепатоцитов, уменьшению фиброза и, следовательно, улучшению белково–синтетической и детоксикационной функции печени.
Представленные в настоящей статье результаты рандомизированного, контролируемого исследования 60 пациентов с хроническим алкогольным гепатитом показали эффективность и безопасность применения препарата. В составе комплексной терапии прием Прогепара приводил к улучшению клинической картины и показателей функционального состояния печени пациента. Результаты исследования показывают, что по сравнению с группой контроля, прием Прогепара оказывал статистически достоверное комплексное воздействие на организм пациента. Особо следует отметить следующие эффекты препарата:
1) Улучшение показателей функционирования печени (АСТ, АЛТ, билирубина), в частности, белково–синтетической функции (альбумин, тимоловая проба);
2) Уменьшение системного воспаления (улучшение показателей уровней лейкоцитов и интерлейкина–6);
3) Снижение клинических проявлений практически всех гиповитаминозов, прежде всего гиповитаминозов В5, В6, РР и А;
4) Снижение частоты расстройств со стороны ЖКТ;
5) Снижение отечности, улучшение диуреза, сопровождающееся улучшением биохимических показателей функции почек (снижение белка и оксалатов в моче, креатинина и мочевины в крови; повышение уровней альбумина в крови).
Таким образом, использование препарата Прогепар в терапии хронического алкогольного гепатита показало комплексное положительное воздействие не только на симптоматику и функционирование печени, но и на другие системы организма (иммунную, мочевыделительную, обмен витаминов). Комплексный механизм воздействия препарата указывает на возможности его применения для гепатопротекции.







Литература
1. Громова О.А., Торшин И.Ю., Юргель И.С. с соавт. Механизмы действия и клиническая эффективность комбинированного гепатопротекторного препарата Прогепар. Трудный Пациент, 2009, №12.
2. Баяши А.О., Акиома Х., Тацаки Х. Воздействие гидролизата печени на циркуляцию крови при хронических заболеваниях печени //Арцнаймиттель Форшунг, – 1972, 22С.578–580.
3. Fujisawa K., Suzuki H., Yamamoto S., Hirayama C., Shikata T., Sanbe R. Therapeutic effects of liver hydrolyzate Prohepar in chronic hepatitis – A double–blind controlled study. Asian Med. J. 26(8):497–526
4. Демидов В.И., Назаренко О.А., Егорова Е.Ю. с соавт. Исследование эффективности Прогепара при экспериментальном повреждении печени алкоголем и парацетамолом: биохимия и гистология. Фарматека, 2011, № 2.
5. Егорова Е.Ю., Философова М.С., Торшин И.Ю. с соавт. Сравнительная динамика персистирующей и прогрессирующей форм алкогольного гепатита в курсе терапии препаратом Прогепар. Российский Медицинский Журнал, Российский Медицинский Журнал, Том 19, № 2, 2011.
6. Федеральный закон от 12.04.2010 N 61–ФЗ «Об обращении лекарственных средств» www.government.ru .
7. Ивашкин В.Т., Маевская М.В. Алкогольно–вирусные заболевания печени. – М.: Литтерра, 2007. – 160 с.
8. Громова О. А., Сатарина Т. Е., Калачева А. Г., Лиманова О. А. Структурированный вопросник по оценке дефицита витаминов. Рационализаторское предложение № 2461 от 17 ноября 2008 г.
9. Журавлев Ю. И. Избранные научные труды. – М.: Магистр, 1998. – 420 с.
10. Журавлев Ю.И. Об алгебраическом подходе к решению задач распознавания или классификации//Проблемы кибернетики: Вып.33.. – 1978. – с. 5–68.
11. Тогузов Р.Т., Шачнев Е.А., Назаренко О.А. с соавт. Содержание фолатов и липоевой кислоты в гепатопротекторе прогепар, Фарматека, 2011, 3
12. Ребров В.Г., Громова О.А. Витамины, макро– и микроэлементы. ГэотарМед, М., – 2008, 946 с.
13. Торшин И.Ю., Громова О.А. Физиологическая модель взаимосвязи витамина D3 с онкологическими заболеваниями и данные доказательной медицины, Трудный пациент, 2008, №11, С. 21–26
14. Isoda K, Kagaya N, Akamatsu S, Hayashi S, Tamesada M, Watanabe A, Kobayashi M, Tagawa Y, Kondoh M, Kawase M, Yagi K. Hepatoprotective effect of vitamin B12 on dimethylnitrosamine–induced liver injury. Biol Pharm Bull. 2008 Feb;31(2):309–11.












