–Ь–љ–Њ–≥–Є–µ –Ї—Б–µ–љ–Њ–±–Є–Њ—В–Є–Ї–Є —Б–њ–Њ—Б–Њ–±–љ—Л –≤—Л–Ј—Л–≤–∞—В—М –њ–Њ—А–∞–ґ–µ–љ–Є–µ –њ–µ—З–µ–љ–Є. –Ґ–∞–Ї, –≤ –°–®–Р —Г 2вАУ5% –±–Њ–ї—М–љ—Л—Е, –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–Њ –њ–Њ–≤–Њ–і—Г –ґ–µ–ї—В—Г—Е–Є, –≤–њ–Њ—Б–ї–µ–і—Б—В–≤–Є–Є –≤—Л—П–≤–ї—П–µ—В—Б—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –њ–µ—З–µ–љ–Є (–Ы–Я–Я), –∞ –Њ—В 15 –і–Њ 30% —Б–ї—Г—З–∞–µ–≤ —Д—Г–ї—М–Љ–Є–љ–∞–љ—В–љ–Њ–є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Є –Њ–Ї–Њ–ї–Њ 40% —Б–ї—Г—З–∞–µ–≤ –Њ—Б—В—А–Њ–≥–Њ –≥–µ–њ–∞—В–Є—В–∞ —Г –ї–Є—Ж —Б—В–∞—А—И–µ 50 –ї–µ—В —Б–≤—П–Ј–∞–љ—Л —Б –њ—А–Є–µ–Љ–Њ–Љ –Ы–° [2]. –†–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Ы–Я–Я –љ–µ–Њ–і–Є–љ–∞–Ї–Њ–≤–∞ –≤ —А–∞–Ј–љ—Л—Е —Б—В—А–∞–љ–∞—Е –Є –Ј–∞–≤–Є—Б–Є—В –Њ—В —Б—В—А—Г–Ї—В—Г—А—Л —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –ї–µ–Ї–∞—А—Б—В–≤. –Т –†–Њ—Б—Б–Є–Є –Њ—Б—В—А—Л–µ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ—Л–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–µ—З–µ–љ–Є –≤—Л—П–≤–ї—П—О—В—Б—П —Г 2,7% –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е, –Є –љ–∞ 1-–Љ –Љ–µ—Б—В–µ –љ–∞—Е–Њ–і—П—В—Б—П –њ—А–Њ—В–Є–≤–Њ—В—Г–±–µ—А–Ї—Г–ї–µ–Ј–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, –Ј–∞—В–µ–Љ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–µ, –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ, –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Л–µ, —Ж–Є—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Є–µ, –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–µ, –∞–љ—В–Є–∞—А–Є—В–Љ–Є—З–µ—Б–Ї–Є–µ —Б—А–µ–і—Б—В–≤–∞ [3]. –Э–∞ —А–Є—Б—Г–љ–Ї–µ 1 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –Њ—Б–љ–Њ–≤–љ—Л–µ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Д–∞–Ї—В–Њ—А—Л —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –Ы–Я–Я.
–°—А–µ–і–Є —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –љ–µ–ї—М–Ј—П –љ–µ–і–Њ–Њ—Ж–µ–љ–Є–≤–∞—В—М –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –Є—Е –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Ї–∞–Ї —А–µ–Ј—Г–ї—М—В–∞—В –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П –Є –≤–ї–Є—П–љ–Є—П –љ–∞ –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–Є—Б—В–µ–Љ—Л –Є–Ј–Њ—Д–µ—А–Љ–µ–љ—В–Њ–≤ –†450.
–Т—Б–µ –Ы–° –Љ–Њ–ґ–љ–Њ —А–∞–Ј–і–µ–ї–Є—В—М –љ–∞ 3 –≥—А—Г–њ–њ—Л –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї —Б–Є—Б—В–µ–Љ–µ —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450: —Б—Г–±—Б—В—А–∞—В—Л, –Є–љ–і—Г–Ї—В–Њ—А—Л –Є –Є–љ–≥–Є–±–Є—В–Њ—А—Л —Н—В–Њ–є —Б–Є—Б—В–µ–Љ—Л. –°—Г–±—Б—В—А–∞—В–∞–Љ–Є —П–≤–ї—П—О—В—Б—П –њ—А–µ–њ–∞—А–∞—В—Л, –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г—О—Й–Є–µ—Б—П –њ–Њ–і –Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ —Д–µ—А–Љ–µ–љ—В–Њ–≤ —Б–Є—Б—В–µ–Љ—Л —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –†450 вАУ —Н—В–Њ –њ—А–µ–њ–∞—А–∞—В—Л, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–і–∞–≤–ї—П—О—В –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –†450-—Б—Г–±—Б—В—А–∞—В–Њ–≤; –њ—А–Њ—Ж–µ—Б—Б –љ–Њ—Б–Є—В –Ї–Њ–љ–Ї—Г—А–µ–љ—В–љ—Л–є –Є –Њ–±—А–∞—В–Є–Љ—Л–є —Е–∞—А–∞–Ї—В–µ—А вАУ –Ї–∞–Ї —В–Њ–ї—М–Ї–Њ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Њ—В–Љ–µ–љ–∞ –Є–љ–≥–Є–±–Є—В–Њ—А–∞, –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –≤–Њ–Ј–≤—А–∞—Й–∞–µ—В—Б—П –Ї –љ–Њ—А–Љ–∞–ї—М–љ–Њ–Љ—Г. –Ш–љ–і—Г–Ї—В–Њ—А—Л –†450 вАУ —В–∞–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є–Ј–Њ—Д–µ—А–Љ–µ–љ—В–Њ–≤ –†450 in vivo. –≠—В–Њ—В –њ—А–Њ—Ж–µ—Б—Б —Б–≤—П–Ј–∞–љ —Б –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є —Б–Є–љ—В–µ–Ј–∞ —Д–µ—А–Љ–µ–љ—В–Њ–≤.
–¶–Є—В–Њ—Е—А–Њ–Љ –†450 3–Р4 —П–≤–ї—П–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ –Ј–љ–∞—З–Є–Љ—Л–Љ —Б—А–µ–і–Є —Ж–Є—В–Њ—Е—А–Њ–Љ–Њ–≤ –†450, —В. –Ї. –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В 225 —Б—Г–±—Б—В—А–∞—В–Њ–≤, –Є–Ј –Ї–Њ—В–Њ—А—Л—Е 191 –≤–µ—Й–µ—Б—В–≤–Њ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –Ы–°. –Я—А–Є —Г—З–∞—Б—В–Є–Є –†450 3–Р4 –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П –Њ–Ї–Њ–ї–Њ 60% –≤—Б–µ—Е –Є–Ј–≤–µ—Б—В–љ—Л—Е –Ы–°. –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Ы–°, –Ї–Њ—В–Њ—А—Л–µ —И–Є—А–Њ–Ї–Њ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –і–ї—П –ї–µ—З–µ–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П –Є–Љ–µ–љ–љ–Њ CYP3–Р4. –°—А–µ–і–Є –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В–Њ–≤ —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–∞–µ—В—Б—П –±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ CYP3–Р4. –Т —Б–ї—Г—З–∞–µ –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ы–°-—Б—Г–±—Б—В—А–∞—В–∞ –Є –Ы–°-–Є–љ–≥–Є–±–Є—В–Њ—А–∞ CYP3–Р4 –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ —Б—Г–±—Б—В—А–∞—В–∞ –Ј–∞–Љ–µ–і–ї—П–µ—В—Б—П, –Ы–°-—Б—Г–±—Б—В—А–∞—В –Љ–Њ–ґ–µ—В –љ–∞–Ї–∞–њ–ї–Є–≤–∞—В—М—Б—П –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ, –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ –њ–Њ–≤—Л—И–∞–µ—В—Б—П —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є, –≤ —В. —З. –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е [4]. –Ґ–∞–Ї–ґ–µ —Б—Г—Й–µ—Б—В–≤—Г–µ—В —А—П–і –Ы–°, –Ї–Њ—В–Њ—А—Л–µ –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —П–≤–ї—П—О—В—Б—П –Є —Б—Г–±—Б—В—А–∞—В–Њ–Љ, –Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ CYP3–Р4. –Я—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —В–∞–Ї–Є—Е –Ы–° –Є—Е –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –Ј–∞–Љ–µ–і–ї—П–µ—В—Б—П, –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є –њ–∞—Ж–Є–µ–љ—В–∞ –љ–∞—А–∞—Б—В–∞–µ—В –Є –Љ–Њ–ґ–µ—В –і–Њ—Б—В–Є–≥–∞—В—М —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ —Г—А–Њ–≤–љ—П.
–Т–∞–ґ–љ–µ–є—И–µ–є –Ј–∞–і–∞—З–µ–є —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л —П–≤–ї—П–µ—В—Б—П –њ–Њ–≤—Л—И–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –≠—В–∞ –Ј–∞–і–∞—З–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М —А–µ—И–µ–љ–∞ –њ—Г—В–µ–Љ –љ–µ —В–Њ–ї—М–Ї–Њ —Б–Њ–Ј–і–∞–љ–Є—П –љ–Њ–≤—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –≤–µ—Й–µ—Б—В–≤, –љ–Њ –Є –±–Њ–ї–µ–µ —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Г–ґ–µ —Б—Г—Й–µ—Б—В–≤—Г—О—Й–Є—Е –Ы–°, –∞ —В–∞–Ї–ґ–µ –њ–Њ–Є—Б–Ї–∞ –Є –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Є–љ–і—Г–Ї—В–Њ—А–Њ–≤ –Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –±–Є–Њ—В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –≤–µ—Й–µ—Б—В–≤ —Б —Ж–µ–ї—М—О –Є–Ј–Љ–µ–љ–µ–љ–Є—П –±–Є–Њ—В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–Є –Є —Г–Љ–µ–љ—М—И–µ–љ–Є—П —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ –њ–µ—З–µ–љ—М. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –∞–Ї—В–Є–≤–љ–Њ —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –Љ–µ—В–Њ–і—Л –∞–љ–∞–ї–Є–Ј–∞ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Д–µ—А–Љ–µ–љ—В–Њ–≤, –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г—О—Й–Є—Е –Ы–°, –Є —А–∞–Ј—А–∞–±–∞—В—Л–≤–∞—О—В—Б—П —Б–Є—Б—В–µ–Љ—Л, –Љ–Њ–і–µ–ї–Є—А—Г—О—Й–Є–µ (—Б–Є–Љ—Г–ї–Є—А—Г—О—Й–Є–µ) —В–∞–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М [5].
–°–Њ–±—Б—В–≤–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є–Ј—Г—З–µ–љ–Є—П –≤–ї–Є—П–љ–Є—П —В–∞—Г—А–Є–љ–∞ –љ–∞ –∞–Ї—В–Є–≤–љ–Њ—Б—В—М CY–†450 3–Р4
–Т–ї–Є—П–љ–Є–µ –љ–∞ –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–Ј–Њ—Д–µ—А–Љ–µ–љ—В–Њ–≤ —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450 –Љ–Њ–ґ–µ—В –ї–µ–ґ–∞—В—М –≤ –Њ—Б–љ–Њ–≤–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞ –Ј–∞—Й–Є—В–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Њ—В –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П. –Ю–і–љ–Є–Љ –Є–Ј –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є–Є —П–≤–ї—П–µ—В—Б—П –Є–Ј—Г—З–µ–љ–Є–µ –њ—Г—В–Є —Б–љ–Є–ґ–µ–љ–Є—П –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –љ–∞–Ј–љ–∞—З–∞–µ–Љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –∞–Ї—В–Є–≤–љ–Њ –≤–µ–і–µ—В—Б—П –њ–Њ–Є—Б–Ї –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –∞–Ї—В–Є–≤–љ—Л—Е –≤–µ—Й–µ—Б—В–≤, —Б–Њ—З–µ—В–∞–љ–љ—Л–є –њ—А–Є–µ–Љ –Ї–Њ—В–Њ—А—Л—Е –≤–Љ–µ—Б—В–µ —Б –Ы–° —Г–Љ–µ–љ—М—И–∞–µ—В –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –љ–∞–Љ–Є –њ—А–Њ–≤–µ–і–µ–љ–Њ –Є–Ј—Г—З–µ–љ–Є–µ –≤ —Н–ї–µ–Ї—В—А–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–Љ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–µ –≤–ї–Є—П–љ–Є—П —В–∞—Г—А–Є–љ–∞ –љ–∞ –Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Є–µ —Д—Г–љ–Ї—Ж–Є–Є —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450 3–Р4 –Ї–∞–Ї –љ–∞–Є–±–Њ–ї–µ–µ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ —Г—З–∞—Б—В–љ–Є–Ї–∞ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Ы–°.
–Ґ–∞—Г—А–Є–љ вАУ –Њ–і–Є–љ –Є–Ј –≤–∞–ґ–љ–µ–є—И–Є—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤, –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–µ –Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞, —Г—А–Њ–≤–µ–љ—М –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–є –Ј–∞—Й–Є—В—Л, –і–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Њ–љ–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. –Ґ–∞—Г—А–Є–љ (2-–∞–Љ–Є–љ–Њ—Н—В–∞–љ—Б—Г–ї—М—Д–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞) вАУ –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–∞—П —Б–≤–Њ–±–Њ–і–љ–∞—П –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–∞ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ —З–µ–ї–Њ–≤–µ–Ї–∞, –Є–≥—А–∞—О—Й–∞—П –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ —В–∞–Ї–Є—Е –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е, –Ї–∞–Ї –Ї–Њ–љ—К—О–≥–∞—Ж–Є—П –ґ–µ–ї—З–љ—Л—Е –Ї–Є—Б–ї–Њ—В, –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–µ –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј–∞ –Ї–∞–ї—М—Ж–Є—П, –Њ—Б–Љ–Њ—А–µ–≥—Г–ї—П—Ж–Є—П –Є —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є—П –Љ–µ–Љ–±—А–∞–љ. –£ –ї—О–і–µ–є —В–∞—Г—А–Є–љ –Њ–±—А–∞–Ј—Г–µ—В—Б—П –≤ –≥–µ–њ–∞—В–Њ—Ж–Є—В–∞—Е –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Њ–±–Љ–µ–љ–∞ –≤–µ—Й–µ—Б—В–≤ –Є–Ј –Љ–µ—В–Є–Њ–љ–Є–љ–∞ –Є —Ж–Є—Б—В–µ–Є–љ–∞ —З–µ—А–µ–Ј –≥–Є–њ–Њ—В–∞—Г—А–Є–љ. –Ґ–∞—Г—А–Є–љ –≤ –≤—Л—Б–Њ–Ї–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —Б–Њ–і–µ—А–ґ–Є—В—Б—П –≤ —Б–µ—А–і–µ—З–љ–Њ–є –Љ—Л—И—Ж–µ, —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ–µ, –ї–µ–є–Ї–Њ—Ж–Є—В–∞—Е, —Б–Ї–µ–ї–µ—В–љ–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А–µ. –Ф—А—Г–≥–Є–µ –Ї–ї–µ—В–Ї–Є (–љ–∞–њ—А–Є–Љ–µ—А, –љ–µ–є—В—А–Њ—Д–Є–ї—Л) —Б–Њ–і–µ—А–ґ–∞—В –Њ—З–µ–љ—М –≤—Л—Б–Њ–Ї–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —В–∞—Г—А–Є–љ–∞ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Ј–∞—Е–≤–∞—В–∞ –≤–µ—Й–µ—Б—В–≤–∞ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –Є–Ј –Ї—А–Њ–≤–Є, –Ї—Г–і–∞ —В–∞—Г—А–Є–љ –њ–Њ—Б—В—Г–њ–∞–µ—В –Ї–∞–Ї –Є–Ј —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е –Є—Б—В–Њ—З–љ–Є–Ї–Њ–≤, —В–∞–Ї –Є –Є–Ј –њ–Є—Й–Є. –С–Є–Њ—Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–µ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є —З–µ–ї–Њ–≤–µ–Ї–∞ –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В—М —В–∞—Г—А–Є–љ –Њ–≥—А–∞–љ–Є—З–µ–љ—Л —Г –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е, —Б–љ–Є–ґ–∞—О—В—Б—П —Б –≤–Њ–Ј—А–∞—Б—В–Њ–Љ –Є –њ—А–Є –љ–µ–Ї–Њ—В–Њ—А—Л—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е (—В—А–∞–≤–Љ—Л, —Б–µ–њ—Б–Є—Б). –Т —В–∞–Ї–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–µ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–µ —В–∞—Г—А–Є–љ–∞ –Є–Ј–≤–љ–µ —П–≤–ї—П–µ—В—Б—П –≤–∞–ґ–љ—Л–Љ –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ —Н—В–Њ–є –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л.
–Ґ–∞—Г—А–Є–љ –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ—В–љ–µ—Б–µ–љ –Ї –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–Љ –Њ—Б–Љ–Њ–ї–Є—В–∞–Љ, –Ї–Њ—В–Њ—А—Л–µ –Є–Љ–µ—О—В —Г–љ–Є–Ї–∞–ї—М–љ—Л–µ –±–Є–Њ—Д–Є–Ј–Є—З–µ—Б–Ї–Є–µ –Є –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞. –≠—В–Є –≤–µ—Й–µ—Б—В–≤–∞ –љ–∞–Ї–∞–њ–ї–Є–≤–∞—О—В—Б—П –≤ –Ї–ї–µ—В–Ї–µ –±–µ–Ј –Є–Ј–Љ–µ–љ–µ–љ–Є—П –µ–µ –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј–∞, —Б—В—А—Г–Ї—В—Г—А—Л –Є —Д—Г–љ–Ї—Ж–Є–Є –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В —Н–ї–µ–Ї—В—А–Њ–ї–Є—В–Њ–≤ –Є –Љ–Њ—З–µ–≤–Є–љ—Л, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –њ–Њ–≤—А–µ–ґ–і–∞—В—М –Ї–ї–µ—В–Ї—Г, –Ї–Њ–≥–і–∞ –љ–∞–Ї–∞–њ–ї–Є–≤–∞—О—В—Б—П –≤ –љ–µ–є –≤ –±–Њ–ї—М—И–Є—Е –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞—Е –Є–ї–Є –Ї–Њ–≥–і–∞ –≤–Њ–Ј–љ–Є–Ї–∞—О—В –≤—Л—А–∞–ґ–µ–љ–љ—Л–µ –Ї–Њ–ї–µ–±–∞–љ–Є—П –Є—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є.
–Э–∞–Љ–Є –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ–є —А–∞–±–Њ—В–µ –±—Л–ї–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Њ –≤–ї–Є—П–љ–Є–µ —В–∞—Г—А–Є–љ–∞ –љ–∞ –Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Є–µ —Д—Г–љ–Ї—Ж–Є–Є —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450 3–Р4 –Ї–∞–Ї –љ–∞–Є–±–Њ–ї–µ–µ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ —Г—З–∞—Б—В–љ–Є–Ї–∞ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Ы–°.
–≠–ї–µ–Ї—В—А–Њ–∞–љ–∞–ї–Є—В–Є—З–µ—Б–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є —А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О —Ж–Є–Ї–ї–Њ–≤–Њ–ї—М—В–∞–Љ–њ–µ—А–Њ–Љ–µ—В—А–Є–Є –Є –≤–Њ–ї—М—В–∞–Љ–њ–µ—А–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ (–Ї–≤–∞–і—А–∞—В–љ–Њ-–≤–Њ–ї–љ–Њ–≤–Њ–є –≤–Њ–ї—М—В–∞–Љ–њ–µ—А–Њ–Љ–µ—В—А–Є–Є) –њ–Њ –≤–Њ–ї—М—В–∞–Љ–њ–µ—А–љ—Л–Љ –њ–∞—А–∞–Љ–µ—В—А–∞–Љ —Н–ї–µ–Ї—В—А–Њ–і–Њ–≤ —Б –Є–Љ–Љ–Њ–±–Є–ї–Є–Ј–Њ–≤–∞–љ–љ—Л–Љ —Ж–Є—В–Њ—Е—А–Њ–Љ–Њ–Љ –†450 3–Р4 [6].
–Я—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є —Н–ї–µ–Ї—В—А–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ –±—Л–ї–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л —В—А–µ—Е–Ї–Њ–љ—В–∞–Ї—В–љ—Л–µ —Н–ї–µ–Ї—В—А–Њ–і—Л, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –Љ–µ—В–Њ–і–Њ–Љ —В—А–∞—Д–∞—А–µ—В–љ–Њ–є –њ–µ—З–∞—В–Є. –Я—А–Є –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –њ–µ—З–∞—В–љ—Л—Е –≥—А–∞—Д–Є—В–Њ–≤—Л—Е —Н–ї–µ–Ї—В—А–Њ–і–Њ–≤ 0,1 –Ь DDAB/Au –≤ —Е–ї–Њ—А–Њ—Д–Њ—А–Љ–µ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –≤–Ї–ї—О—З–µ–љ–Є–µ–Љ –≤ –Љ–µ–Љ–±—А–∞–љ–Њ–њ–Њ–і–Њ–±–љ—Г—О –Љ–∞—В—А–Є—Ж—Г —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450 3–Р4 –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А—П–Љ–Њ–є –±–µ–Ј–Љ–µ–і–Є–∞—В–Њ—А–љ—Л–є –њ–µ—А–µ–љ–Њ—Б —Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤ –Љ–µ–ґ–і—Г —Н–ї–µ–Ї—В—А–Њ–і–Њ–Љ –Є –≥–µ–Љ–Њ–Љ.
–Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Њ–є —Ж–Є—В–Њ—Е—А–Њ–Љ –†450-–Ј–∞–≤–Є—Б–Є–Љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є –≤ —Н–ї–µ–Ї—В—А–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б–Є—Б—В–µ–Љ–µ —А–µ–≥–Є—Б—В—А–Є—А—Г–µ—В—Б—П –Ї–∞—В–Њ–і–љ—Л–є —В–Њ–Ї, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–є –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–Љ—Г –њ–Њ—В–Њ–Ї—Г —Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤ –Ї –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–Љ—Г —Б—Г–±—Б—В—А–∞—В—Г (–Ы–°). –Ъ–∞—В–Њ–і–љ—Л–є —В–Њ–Ї (–Є–Љ–µ—О—Й–Є–є –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –∞–љ–Њ–і–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ —Б –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ –Ј–љ–∞—З–µ–љ–Є–µ–Љ —В–Њ–Ї–∞) —П–≤–ї—П–µ—В—Б—П –Љ–µ—А–Њ–є —Н–ї–µ–Ї—В—А–Њ–Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Д–µ—А–Љ–µ–љ—В–∞.
–Я—А–Њ–≤–µ–і–µ–љ –∞–љ–∞–ї–Є–Ј —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є—Е –Є –Ї–≤–∞–і—А–∞—В–љ–Њ-–≤–Њ–ї–љ–Њ–≤—Л—Е –≤–Њ–ї—М—В–∞–Љ–њ–µ—А–Њ–≥—А–∞–Љ–Љ DDAB/Au/P450 3–Р4 —Н–ї–µ–Ї—В—А–Њ–і–∞ –і–Њ –Є –њ–Њ—Б–ї–µ –њ—А–Є–±–∞–≤–ї–µ–љ–Є—П –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞ (100 –Љ–Ї–Ь). –Ъ–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Є–є —В–Њ–Ї (–Ї–∞—В–Њ–і–љ—Л–є –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–є), —А–µ–≥–Є—Б—В—А–Є—А—Г–µ–Љ—Л–є –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є —Н—В–Њ–≥–Њ –Ы–°, —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –њ—А–Њ—В–µ–Ї–∞–љ–Є–Є —Н–ї–µ–Ї—В—А–Њ–Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Њ–є —А–µ–∞–Ї—Ж–Є–Є: –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї –њ—А–Њ—П–≤–ї—П–µ—В —Б—Г–±—Б—В—А–∞—В–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї —Ж–Є—В–Њ—Е—А–Њ–Љ—Г –†450 3–Р4.
–Ш–љ–≥–Є–±–Є—В–Њ—А—Л —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450 –љ–µ –і–∞—О—В —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–∞—В–Њ–і–љ–Њ–≥–Њ —В–Њ–Ї–∞, —В. –Ї. –љ–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –њ–µ—А–µ–љ–Њ—Б–∞ —Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤ –≤ —Б–Є—Б—В–µ–Љ–µ. –Ш—В—А–∞–Ї–Њ–љ–∞–Ј–Њ–ї —П–≤–ї—П–µ—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –њ—А–Њ—В–Є–≤–Њ–≥—А–Є–±–Ї–Њ–≤—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ, –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л–Љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Њ–љ–Є—Е–Њ–Љ–Є–Ї–Њ–Ј–Њ–≤. –С—Л–ї–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Њ –≤–ї–Є—П–љ–Є–µ –Є—В—А–∞–Ї–Њ–љ–∞–Ј–Њ–ї–∞ –љ–∞ —Ж–Є—В–Њ—Е—А–Њ–Љ –†450 3–Р4. –Я—А–Є –њ—А–Є–±–∞–≤–ї–µ–љ–Є–Є –Ї DDAB/Au/P450 3–Р4 —Н–ї–µ–Ї—В—А–Њ–і—Г –Є—В—А–∞–Ї–Њ–љ–∞–Ј–Њ–ї–∞ –љ–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–∞—В–Њ–і–љ–Њ–≥–Њ –Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Њ–≥–Њ —В–Њ–Ї–∞, –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–µ –њ—А–Є–±–∞–≤–ї–µ–љ–Є–µ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞ —В–∞–Ї–ґ–µ –љ–µ –њ—А–Є–≤–Њ–і–Є—В –Ї —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є —Н–ї–µ–Ї—В—А–Њ–Ї–∞—В–∞–ї–Є–Ј–∞. –≠—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ –Є–љ–≥–Є–±–Є—А—Г—О—Й–Є—Е —Б–≤–Њ–є—Б—В–≤ –Є—В—А–∞–Ї–Њ–љ–∞–Ј–Њ–ї–∞ –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї —Ж–Є—В–Њ—Е—А–Њ–Љ—Г –†450 3–Р4.
–Ґ–∞—Г—А–Є–љ —П–≤–ї—П–µ—В—Б—П –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –∞–Ї—В–Є–≤–љ—Л–Љ —Б–Њ–µ–і–Є–љ–µ–љ–Є–µ–Љ —Б —Ж–µ–ї—Л–Љ —Б–њ–µ–Ї—В—А–Њ–Љ —Б–≤–Њ–є—Б—В–≤: –Њ–љ –њ—А–Є–љ–Є–Љ–∞–µ—В —Г—З–∞—Б—В–Є–µ –≤ —А–µ–≥—Г–ї—П—Ж–Є–Є –Њ—Б–Љ–Њ—Б–∞, —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ, –і–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є.
–≠–ї–µ–Ї—В—А–Њ—Е–Є–Љ–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450 3–Р4 —В–∞–Ї–ґ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О –∞–љ–∞–ї–Є–Ј–∞ –Њ—В–Ї–ї–Є–Ї–∞ —Д–µ—А–Љ–µ–љ—В–∞ –љ–∞ –≤–µ—Й–µ—Б—В–≤–Њ-–Љ–Њ–і—Г–ї—П—В–Њ—А. –Я—А–Є –њ—А–Є–±–∞–≤–ї–µ–љ–Є–Є —В–∞—Г—А–Є–љ–∞ (–Ї–Њ–љ–µ—З–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П 50 –Љ–Ї–Ь) –Ї DDAB/Au/P450 3–Р4 —Н–ї–µ–Ї—В—А–Њ–і—Г –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–∞—В–Њ–і–љ–Њ–≥–Њ —В–Њ–Ї–∞, —З—В–Њ –Њ–±—Л—З–љ–Њ —Е–∞—А–∞–Ї—В–µ—А–љ–Њ –і–ї—П —Б—Г–±—Б—В—А–∞—В–Њ–≤ —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ —В–∞—Г—А–Є–љ –љ–µ —П–≤–ї—П–µ—В—Б—П —Б—Г–±—Б—В—А–∞—В–Њ–Љ —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450 3–Р4. –Ф–ї—П –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞ –Њ—В—Б—Г—В—Б—В–≤–Є—П —Б–≤—П–Ј—Л–≤–∞–љ–Є—П —В–∞—Г—А–Є–љ–∞ —Б —Ж–Є—В–Њ—Е—А–Њ–Љ–Њ–Љ –†450 –њ–Њ —В–Є–њ—Г —Б—Г–±—Б—В—А–∞—В–Њ–≤ –±—Л–ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ—Л —А–∞–Ј–љ–Њ—Б—В–љ—Л–µ —Б–њ–µ–Ї—В—А—Л –њ–Њ–≥–ї–Њ—Й–µ–љ–Є—П —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450 –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞, –Є—В—А–∞–Ї–Њ–љ–∞–Ј–Њ–ї–∞ –Є —В–∞—Г—А–Є–љ–∞. –†–∞–Ј–љ–Њ—Б—В–љ—Л–є —Б–њ–µ–Ї—В—А —Б–≤—П–Ј—Л–≤–∞–љ–Є—П —Б –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–Њ–Љ –Є–Љ–µ–µ—В —Е–∞—А–∞–Ї—В–µ—А–љ—Г—О —Д–Њ—А–Љ—Г –і–ї—П —Б–≤—П–Ј—Л–≤–∞–љ–Є—П —Б—Г–±—Б—В—А–∞—В–Њ–≤ I —В–Є–њ–∞: —Б –Љ–∞–Ї—Б–Є–Љ—Г–Љ–Њ–Љ –њ—А–Є 380 –љ–Љ –Є –Љ–Є–љ–Є–Љ—Г–Љ–Њ–Љ –њ—А–Є 416 –љ–Љ –Є—В—А–∞–Ї–Њ–љ–∞–Ј–Њ–ї –і–∞–µ—В —А–∞–Ј–љ–Њ—Б—В–љ—Л–є —Б–њ–µ–Ї—В—А —Б–≤—П–Ј—Л–≤–∞–љ–Є—П II —В–Є–њ–∞, —Е–∞—А–∞–Ї—В–µ—А–љ—Л–є –і–ї—П —Б–Њ–µ–і–Є–љ–µ–љ–Є–є-–Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ —Б –Љ–∞–Ї—Б–Є–Љ—Г–Љ–Њ–Љ –њ—А–Є 420 –љ–Љ –Є –Љ–Є–љ–Є–Љ—Г–Љ–Њ–Љ –њ—А–Є 390 –љ–Љ. –Ґ–∞—Г—А–Є–љ –љ–µ –і–∞–µ—В —Е–∞—А–∞–Ї—В–µ—А–љ—Л—Е —А–∞–Ј–љ–Њ—Б—В–љ—Л—Е —Б–њ–µ–Ї—В—А–Њ–≤ —Б–≤—П–Ј—Л–≤–∞–љ–Є—П –љ–Є I, –љ–Є II —В–Є–њ–∞, —З—В–Њ –і–Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Б—Г–±—Б—В—А–∞—В–љ—Л—Е —Б–≤–Њ–є—Б—В–≤ —Г —В–∞—Г—А–Є–љ–∞ –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї —Ж–Є—В–Њ—Е—А–Њ–Љ—Г –†450 3–Р4 [7]. –°—А–µ–і–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –Ї–∞—В–Њ–і–љ–Њ–≥–Њ –Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Њ–≥–Њ —В–Њ–Ї–∞ –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є —Б—Г–±—Б—В—А–∞—В–Њ–≤ (–і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї), –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ (–Є—В—А–∞–Ї–Њ–љ–∞–Ј–Њ–ї) –Є –Љ–Њ–і—Г–ї—П—В–Њ—А–Њ–≤ (—В–∞—Г—А–Є–љ) CYP450 3–Р4 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 1.
–£–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Њ–≥–Њ —В–Њ–Ї–∞ –њ—А–Є –њ—А–Є–±–∞–≤–ї–µ–љ–Є–Є —В–∞—Г—А–Є–љ–∞ –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є —Н—В–Њ–≥–Њ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —Н–ї–µ–Ї—В—А–Њ–Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450 3–Р4 –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≥–µ–љ–µ—А–Є—А–Њ–≤–∞–љ–Є–µ –∞–Ї—В–Є–≤–љ—Л—Е —Д–Њ—А–Љ –Ї–Є—Б–ї–Њ—А–Њ–і–∞ (–Р–§–Ъ), —З—В–Њ –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї —З–∞—Б—В–Є—З–љ–Њ–є –Є–љ–∞–Ї—В–Є–≤–∞—Ж–Є–Є —Д–µ—А–Љ–µ–љ—В–∞. –Р–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ —В–∞—Г—А–Є–љ–∞ –њ—А–Њ—П–≤–ї—П—О—В—Б—П –≤ –љ–µ–є—В—А–∞–ї–Є–Ј–∞—Ж–Є–Є –Р–§–Ъ, —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є —Д–µ—А–Љ–µ–љ—В–∞ –Є —Г–≤–µ–ї–Є—З–µ–љ–Є—О –≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В–µ–ї—М–љ–Њ–≥–Њ –Ї–∞—В–Њ–і–љ–Њ–≥–Њ —В–Њ–Ї–∞. –Ш–љ–≥–Є–±–Є—А—Г—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –Є—В—А–∞–Ї–Њ–љ–∞–Ј–Њ–ї–∞ (–≤ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є 10 –Љ–Ї–Ь) –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є 50 –Љ–Ї–Ь —В–∞—Г—А–Є–љ–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б–љ–Є–ґ–∞–µ—В—Б—П. –Ю—Б–љ–Њ–≤–љ–Њ–є –≤—Л–≤–Њ–і, –Ї–Њ—В–Њ—А—Л–є –Љ–Њ–ґ–љ–Њ —Б–і–µ–ї–∞—В—М –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤, вАУ —В–∞—Г—А–Є–љ —Б–љ–Є–ґ–∞–µ—В –Є–љ–≥–Є–±–Є—А—Г—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –Є—В—А–∞–Ї–Њ–љ–∞–Ј–Њ–ї–∞ –љ–∞ —Ж–Є—В–Њ—Е—А–Њ–Љ –†450 3–Р4.
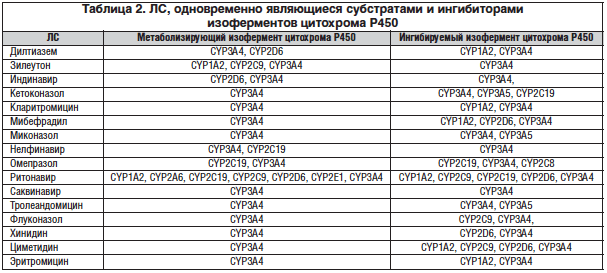
–¶–Є—В–Њ—Е—А–Њ–Љ—Л –†450 –Њ—В–љ–Њ—Б—П—В—Б—П –Ї —Б–∞–Љ–Њ–Є–љ–∞–Ї—В–Є–≤–Є—А—Г—О—Й–Є–Љ—Б—П –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Ї–∞—В–∞–ї–Є–Ј–∞ —Д–µ—А–Љ–µ–љ—В–∞–Љ. –Я—А–Њ—Ж–µ—Б—Б –і–µ—Б—В—А—Г–Ї—Ж–Є–Є —Б–≤—П–Ј–∞–љ —Б –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ–є –і–µ–≥—А–∞–і–∞—Ж–Є–µ–є –Є/–Є–ї–Є –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ–є –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–µ–є –Ј–∞ —Б—З–µ—В –Р–§–Ъ, –≥–µ–љ–µ—А–Є—А—Г—О—Й–Є—Е—Б—П –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –∞–Ї—В–Є–≤–∞—Ж–Є–Є –Ї–Є—Б–ї–Њ—А–Њ–і–∞, –≥–Є–і—А–Њ–Ї—Б–Є–ї–Є—А–Њ–≤–∞–љ–Є—П —Б—Г–±—Б—В—А–∞—В–Њ–≤ –Є –њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є. –Ґ–∞–Ї–∞—П –Є–љ–∞–Ї—В–Є–≤–∞—Ж–Є—П –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–∞—А—Г—И–µ–љ–Є—О —Д—Г–љ–Ї—Ж–Є–Є –Њ–Ї—Б–Є–≥–µ–љ–∞–Ј–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, –Ї –Є–Ј–Љ–µ–љ–µ–љ–Є—О —Б–Ї–Њ—А–Њ—Б—В–Є –Є –њ—Г—В–µ–є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Ы–° –Є –Ї—Б–µ–љ–Њ–±–Є–Њ—В–Є–Ї–Њ–≤, –∞ —В–∞–Ї–ґ–µ –Ї –љ–∞—А—Г—И–µ–љ–Є—О –Њ–±–Љ–µ–љ–∞ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞, —Б—В–µ—А–Њ–Є–і–љ—Л—Е –≥–Њ—А–Љ–Њ–љ–Њ–≤ –Є –і—А—Г–≥–Є—Е —Н–Ї–Ј–Њ–≥–µ–љ–љ—Л—Е —Б—Г–±—Б—В—А–∞—В–Њ–≤, —З—В–Њ –Љ–Њ–ґ–µ—В —П–≤–ї—П—В—М—Б—П –Њ–і–љ–Њ–є –Є–Ј –њ—А–Є—З–Є–љ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ —А–∞–Ј–ї–Є—З–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Р –і–ї—П –Ы–°, –Ї–Њ—В–Њ—А—Л–µ —П–≤–ї—П—О—В—Б—П –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є, –Є —Б—Г–±—Б—В—А–∞—В–∞–Љ–Є —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450 3–Р4, —Н—В–Њ –њ—А–Є–≤–Њ–і–Є—В –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є –і–Њ —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Є —А–∞–Ј–≤–Є—В–Є—О –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Ы–°, —П–≤–ї—П—О—Й–Є–µ—Б—П –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —Б—Г–±—Б—В—А–∞—В–∞–Љ–Є –Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –†450 3–Р4, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 2. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤—Б–µ –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л —Б—А–µ–і–Є –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Є–Љ–µ—О—В –љ–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є.
–£–≥–љ–µ—В–µ–љ–Є–µ —Д–µ—А–Љ–µ–љ—В–Њ–≤ –њ–µ—З–µ–љ–Є –Љ–Њ–≥—Г—В –≤—Л–Ј—Л–≤–∞—В—М 14-—З–ї–µ–љ–љ—Л–µ –Љ–∞–Ї—А–Њ–ї–Є–і—Л (—Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ, –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ), –њ—А–Њ—В–Є–≤–Њ–≥—А–Є–±–Ї–Њ–≤—Л–µ —Б—А–µ–і—Б—В–≤–∞ –Є –∞–љ—В–Є—А–µ—В—А–Њ–≤–Є—А—Г—Б–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –Є–Ј –≥—А—Г–њ–њ—Л –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –њ—А–Њ—В–µ–∞–Ј. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ –Љ–∞–Ї—А–Њ–ї–Є–і—Л –Љ–Њ–≥—Г—В –±—Л—В—М –Њ—В–љ–µ—Б–µ–љ—Л –Ї —З–Є—Б–ї—Г –±–µ–Ј–Њ–њ–∞—Б–љ—Л—Е –Ы–°, —В. –Ї. –Є—Е –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї, –њ—А–Њ—П–≤–ї—П—О—Й–Є–є—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Е–Њ–ї–µ—Б—В–∞—В–Є—З–µ—Б–Ї–Є–Љ –≥–µ–њ–∞—В–Є—В–Њ–Љ, —А–∞—Б—Ж–µ–љ–Є–≤–∞–µ—В—Б—П –≤ –њ—А–µ–і–µ–ї–∞—Е 3,6 —Б–ї—Г—З–∞—П –љ–∞ 100 —В—Л—Б. –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј–∞—Е –Є/–Є–ї–Є –і–ї–Є—В–µ–ї—М–љ—Л–є –њ—А–Є–µ–Љ –Љ–Њ–≥—Г—В —Г–≤–µ–ї–Є—З–Є—В—М —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є.
–Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Њ–≤–∞—В—М —Б CYP3A4 –≤—Б–µ –Љ–∞–Ї—А–Њ–ї–Є–і—Л –Љ–Њ–ґ–љ–Њ —А–∞–Ј–і–µ–ї–Є—В—М –љ–∞ 3 –Њ—Б–љ–Њ–≤–љ—Л–µ –≥—А—Г–њ–њ—Л: 1) —Б–Є–ї—М–љ—Л–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л —Н—В–Њ–≥–Њ –Є–Ј–Њ—Д–µ—А–Љ–µ–љ—В–∞ (—В—А–Њ–ї–µ–∞–љ–і–Њ–Љ–Є—Ж–Є–љ, —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ –Є –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ); 2) –њ—А–µ–њ–∞—А–∞—В—Л —Б –±–Њ–ї–µ–µ —Б–ї–∞–±—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –љ–∞ CYP3A4 (–Љ–Є–і–µ–Ї–∞–Љ–Є—Ж–Є–љ, –і–ґ–Њ–Ј–∞–Љ–Є—Ж–Є–љ –Є —А–Њ–Ї—Б–Є—В—А–Њ–Љ–Є—Ж–Є–љ) –Є 3) –њ—А–µ–њ–∞—А–∞—В—Л, –љ–µ –≤–ї–Є—П—О—Й–Є–µ –љ–∞ –∞–Ї—В–Є–≤–љ–Њ—Б—В—М CYP3A4 (–∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ, —Б–њ–Є—А–∞–Љ–Є—Ж–Є–љ –Є –і–Є—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ). –Я—А–µ–њ–∞—А–∞—В—Л 1-–є –≥—А—Г–њ–њ—Л –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г—О—В—Б—П —Б —Г—З–∞—Б—В–Є–µ–Љ CYP3A4 –Є –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ N-–і–µ–Љ–µ—В–Є–ї–Є—А–Њ–≤–∞–љ–Є—П –Њ–±—А–∞–Ј—Г—О—В —А–µ–∞–Ї—В–Є–≤–љ—Л–µ –љ–Є—В—А–Њ–Ј–Њ–∞–ї–Ї–∞–љ—Л, —Б–≤—П–Ј—Л–≤–∞—О—Й–Є–µ—Б—П —Б —Ж–Є—В–Њ—Е—А–Њ–Љ–Њ–Љ –†450. –Ю–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –Љ–µ–ґ–і—Г –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–Љ –Є –∞–Ї—В–Є–≤–љ—Л–Љ —Ж–µ–љ—В—А–Њ–Љ —Д–µ—А–Љ–µ–љ—В–∞ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ—Г—В–µ–Љ –Ї–Њ–≤–∞–ї–µ–љ—В–љ–Њ–є —Б–≤—П–Ј–Є, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–µ–Њ–±—А–∞—В–Є–Љ–Њ–Љ—Г —Г–≥–љ–µ—В–µ–љ–Є—О –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–Њ—Б–ї–µ–і–љ–µ–≥–Њ. –Я—А–µ–њ–∞—А–∞—В—Л 2-–є –≥—А—Г–њ–њ—Л –Њ–±—А–∞–Ј—Г—О—В –Ї–Њ–Љ–њ–ї–µ–Ї—Б—Л –≤ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є, 3-–є вАУ –≤–Њ–Њ–±—Й–µ –љ–µ –Њ–±—А–∞–Ј—Г—О—В –Ї–Њ–Љ–њ–ї–µ–Ї—Б—Л —Б —Ж–Є—В–Њ—Е—А–Њ–Љ–Њ–Љ. –°—З–Є—В–∞—О—В, —З—В–Њ —А–Є—Б–Ї –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –≤ —Б–≤—П–Ј–Є —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ —А–µ–∞–Ї—В–Є–≤–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ –Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–є –љ–∞–Є–±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї –і–ї—П —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –Є —В—А–Њ–ї–µ–∞–љ–і–Њ–Љ–Є—Ж–Є–љ–∞ (–Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Є/–Є–ї–Є –≤ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј–∞—Е) –Є –љ–Є—З—В–Њ–ґ–љ–Њ –Љ–∞–ї –і–ї—П –∞–Ј–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞, —Б–њ–Є—А–∞–Љ–Є—Ж–Є–љ–∞ –Є –і–Є—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞.
–Т —Ж–µ–ї–Њ–Љ —А–Є—Б–Ї –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –Њ—Ж–µ–љ–Є–≤–∞–µ—В—Б—П –Ї–∞–Ї –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—Б–Њ–Ї–Є–є. –Т —А—П–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —В—А–∞–љ—Б–∞–Љ–Є–љ–∞–Ј –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г 15% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ –±–Њ–ї–µ–µ 2 –љ–µ–і., –≥–µ–њ–∞—В–Є—В вАУ —Г 2%.
–Ф–∞–љ–љ—Л—Е –Њ –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–µ –Љ–µ–љ—М—И–µ, –Њ–і–љ–∞–Ї–Њ –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ–∞—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ –Њ–љ –Њ–±–ї–∞–і–∞–µ—В —Б—Е–Њ–і–љ—Л–Љ —Б —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–Њ–Љ –њ—А–Њ—Д–Є–ї–µ–Љ –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –Є, –њ–Њ-–≤–Є–і–Є–Љ–Њ–Љ—Г, —Б–Њ–њ—А—П–ґ–µ–љ —Б –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–Љ —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –Ы–Я–Я. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –≤ –±—А–Є—В–∞–љ—Б–Ї–Њ–Љ –њ–Њ–њ—Г–ї—П—Ж–Є–Њ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б–Ї–Њ—А—А–µ–Ї—В–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Њ—В–љ–Њ—И–µ–љ–Є–µ —И–∞–љ—Б–Њ–≤ –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –і–∞–ґ–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –њ—А–µ–≤—Л—И–∞–ї–Њ —В–∞–Ї–Њ–≤–Њ–µ –і–ї—П —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ (6,1 –њ—А–Њ—В–Є–≤ 5,3). –Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–ї—Г—З–µ–љ—Л –Є –∞–≤—Б—В—А–Є–є—Б–Ї–Є–Љ–Є —Н–Ї—Б–њ–µ—А—В–∞–Љ–Є –њ—А–Є —А–∞—Б—З–µ—В–µ —З–∞—Б—В–Њ—В—Л –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞ –љ–∞ 100 —В—Л—Б. –љ–∞–Ј–љ–∞—З–µ–љ–Є–є. –Ю–љ–∞ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 3,8 (–њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 3,6 –і–ї—П —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–∞). –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –њ—А–Є –њ—А–Є–µ–Љ–µ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –њ—А–µ–њ–∞—А–∞—В–∞ –Љ–Њ–ґ–µ—В —А–∞–Ј–≤–Є–≤–∞—В—М—Б—П –Њ–±—А–∞—В–Є–Љ—Л–є —Е–Њ–ї–µ—Б—В–∞—В–Є—З–µ—Б–Ї–Є–є –≥–µ–њ–∞—В–Є—В. –Ю–њ–Є—Б–∞–љ—Л –µ–і–Є–љ–Є—З–љ—Л–µ —Б–ї—Г—З–∞–Є —Д—Г–ї—М–Љ–Є–љ–∞–љ—В–љ–Њ–є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, –≤ —В. —З. —Б –ї–µ—В–∞–ї—М–љ—Л–Љ–Є –Є—Б—Е–Њ–і–∞–Љ–Є, –∞ —В–∞–Ї–ґ–µ –ї–µ—В–∞–ї—М–љ—Л–є –Є—Б—Е–Њ–і –≤—Б–ї–µ–і—Б—В–≤–Є–µ –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–µ—З–µ–љ–Є —Г 59-–ї–µ—В–љ–µ–є –ґ–µ–љ—Й–Є–љ—Л —Б —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О, –њ–Њ–ї—Г—З–Є–≤—И–µ–є –Ї–Њ—А–Њ—В–Ї–Є–є –Ї—Г—А—Б –ї–µ—З–µ–љ–Є—П –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–Њ–Љ (1 –≥/—Б—Г—В –≤ —В–µ—З–µ–љ–Є–µ 3 –і–љ–µ–є). –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ, –њ–Њ–і–Њ–±–љ–Њ —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ—Г, —П–≤–ї—П–µ—В—Б—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ CYP3A4, —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є –Љ–Њ–ґ–µ—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ–Њ–≤—Л—И–∞—В—М—Б—П –љ–∞ —Д–Њ–љ–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П —Б –і—А—Г–≥–Є–Љ–Є –Ы–°, –Є–љ–≥–Є–±–Є—А—Г—О—Й–Є–Љ–Є CYP3A4. –£—З–Є—В—Л–≤–∞—П –Љ–µ—Е–∞–љ–Є–Ј–Љ —А–∞–Ј–≤–Є—В–Є—П –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ 14-—З–ї–µ–љ–љ—Л—Е –Љ–∞–Ї—А–Њ–ї–Є–і–Њ–≤, –ї–Њ–≥–Є—З–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤–µ—Й–µ—Б—В–≤–∞, –Љ–Њ–і—Г–ї–Є—А—Г—О—Й–µ–≥–Њ (–Є–љ–і—Г—Ж–Є—А—Г—О—Й–µ–≥–Њ) –∞–Ї—В–Є–≤–љ–Њ—Б—В—М CYP3A4, –Љ–Њ–ґ–µ—В –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—А–Њ–≤–∞—В—М –і–∞–љ–љ—Л–є –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В, —З—В–Њ —В—А–µ–±—Г–µ—В –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є [8].
–Р–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В—Л, —Б–љ–Є–ґ–∞—П —Г—А–Њ–≤–µ–љ—М –Р–§–Ъ, –Љ–Њ–≥—Г—В –њ—А–Њ—П–≤–ї—П—В—М –Ј–∞—Й–Є—В–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї —Ж–Є—В–Њ—Е—А–Њ–Љ–∞–Љ –†450. –° –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В—Л –≤–ї–Є—П—О—В –љ–∞ —А–∞–Ј–Њ–±—Й–µ–љ–Є–µ –Љ–Њ–љ–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј–љ–Њ–≥–Њ —Ж–Є–Ї–ї–∞, —А–∞–Ј—А—Г—И–∞—П –њ–µ—А–Њ–Ї—Б–Є–і –≤–Њ–і–Њ—А–Њ–і–∞ –Є –±–ї–Њ–Ї–Є—А—Г—П –њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј–љ—Л–є –њ—Г—В—М –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є —Б—Г–±—Б—В—А–∞—В–Њ–≤, —З—В–Њ –Љ–Њ–ґ–µ—В –≤—Л—А–∞–ґ–∞—В—М—Б—П –≤ –≤—Л—А–∞–±–Њ—В–Ї–µ –Љ–µ–љ—М—И–Є—Е –Ї–Њ–ї–Є—З–µ—Б—В–≤ –њ—А–Њ–і—Г–Ї—В–Њ–≤ –Љ–Њ–љ–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є. –Р–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В—Л –Ї–∞–Ї –њ—А–Є—Б—Г—В—Б—В–≤—Г—О—В –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ, –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—П –Ј–∞—Й–Є—В–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є (–љ–∞–њ—А–Є–Љ–µ—А, –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–µ —Д–µ—А–Љ–µ–љ—В—Л –Ї–∞—В–∞–ї–∞–Ј–∞, —Б—Г–њ–µ—А–Њ–Ї—Б–Є–і–і–Є—Б–Љ—Г—В–∞–Ј–∞, –њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Л), —В–∞–Ї –Є –њ–Њ–њ–∞–і–∞—О—В –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ –Є–Ј–≤–љ–µ, —В. –Ї. —Б–Њ–і–µ—А–ґ–∞—В—Б—П –≤ –њ–Є—Й–µ –Є –Ы–°.
–Ш—Б–њ–Њ–ї—М–Ј—Г—П —Н–ї–µ–Ї—В—А–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–µ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450 3–Р4 –≤ –Ї–∞—З–µ—Б—В–≤–µ –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞ –і–ї—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Н–ї–µ–Ї—В—А–Њ–Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –≥–µ–Љ–Њ–њ—А–Њ—В–µ–Є–љ–∞ –Є –≤–ї–Є—П–љ–Є—П –љ–∞ —Н–ї–µ–Ї—В—А–Њ—Е–Є–Љ–Є—З–µ—Б–Ї—Г—О —Ж–Є—В–Њ—Е—А–Њ–Љ –†450-—Б–Њ–і–µ—А–ґ–∞—Й—Г—О —Б–Є—Б—В–µ–Љ—Г —А–∞–Ј–ї–Є—З–љ—Л—Е –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –∞–Ї—В–Є–≤–љ—Л—Е –≤–µ—Й–µ—Б—В–≤, –Љ–Њ–ґ–љ–Њ —Б–і–µ–ї–∞—В—М –≤—Л–≤–Њ–і: —В–∞—Г—А–Є–љ, —П–≤–ї—П—П—Б—М –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–Њ–Љ, –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –≤–ї–Є—П–µ—В –љ–∞ —Н–ї–µ–Ї—В—А–Њ–Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Њ–µ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450 3–Р4. –Я—А–Є —Н—В–Њ–Љ —В–∞—Г—А–Є–љ —Б–љ–Є–ґ–∞–µ—В –Є–љ–≥–Є–±–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В –Є—В—А–∞–Ї–Њ–љ–∞–Ј–Њ–ї–∞ [9].
–Ь–µ—Е–∞–љ–Є–Ј–Љ—Л –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П —В–∞—Г—А–Є–љ–∞
–У–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А—Л вАУ —А–∞–Ј–љ–Њ—А–Њ–і–љ–∞—П –≥—А—Г–њ–њ–∞ –Ы–°, –њ—А–µ–њ—П—В—Б—В–≤—Г—О—Й–Є—Е —А–∞–Ј—А—Г—И–µ–љ–Є—О –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ –Є —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є—Е —А–µ–≥–µ–љ–µ—А–∞—Ж–Є—О –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤. –Ъ –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–∞–Љ –Њ—В–љ–Њ—Б—П—В—Б—П –Ы–°, –Њ–±–ї–∞–і–∞—О—Й–Є–µ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –њ–Њ–≤—Л—И–∞—В—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤ –Ї –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—О —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–Є—Е –∞–≥–µ–љ—В–Њ–≤, —Г—Б–Є–ї–Є–≤–∞—О—Й–Є–µ –µ–µ –і–µ—В–Њ–Ї—Б–Є—Ж–Є—А—Г—О—Й—Г—О (–Њ–±–µ–Ј–≤—А–µ–ґ–Є–≤–∞—О—Й—Г—О) —Д—Г–љ–Ї—Ж–Є—О –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –њ–Њ–≤—Л—И–µ–љ–Є—П –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Д–µ—А–Љ–µ–љ—В–љ—Л—Е —Б–Є—Б—В–µ–Љ –Є/–Є–ї–Є –Љ–µ–Љ–±—А–∞–љ–Њ—Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г—О—Й–µ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –∞ —В–∞–Ї–ґ–µ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є–µ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—О —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤ –њ–Њ—Б–ї–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ –љ–Є—Е —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤.
–Ы–°, –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л–µ –і–ї—П –ї–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–µ—З–µ–љ–Є, –Њ–±–ї–∞–і–∞—О—В —А–∞–Ј–љ—Л–Љ–Є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ–Є –Ј–∞—Й–Є—В–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П. –У–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б–≤—П–Ј—Л–≤–∞—О—В —Б –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є–µ–Љ —Д–µ—А–Љ–µ–љ—В–∞—В–Є–≤–љ–Њ–≥–Њ –њ–µ—А–µ–Ї–Є—Б–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –ї–Є–њ–Є–і–Њ–≤, —Б –Є—Е —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –љ–µ–є—В—А–∞–ї–Є–Ј–Њ–≤–∞—В—М —А–∞–Ј–ї–Є—З–љ—Л–µ —Б–≤–Њ–±–Њ–і–љ—Л–µ —А–∞–і–Є–Ї–∞–ї—Л, –Њ–Ї–∞–Ј—Л–≤–∞—П –њ—А–Є —Н—В–Њ–Љ –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–є —Н—Д—Д–µ–Ї—В. –Ф—А—Г–≥–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л —П–≤–ї—П—О—В—Б—П —Б—В—А–Њ–Є—В–µ–ї—М–љ—Л–Љ –Љ–∞—В–µ—А–Є–∞–ї–Њ–Љ –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–ї–Њ—П –Ї–ї–µ—В–Њ–Ї –њ–µ—З–µ–љ–Є, –Њ–Ї–∞–Ј—Л–≤–∞—О—В –Љ–µ–Љ–±—А–∞–љ–Њ—Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В –Є –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—О—В —Б—В—А—Г–Ї—В—Г—А—Г –Љ–µ–Љ–±—А–∞–љ –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤. –Ґ—А–µ—В—М–Є –Є–љ–і—Г—Ж–Є—А—Г—О—В –Љ–Є–Ї—А–Њ—Б–Њ–Љ–∞–ї—М–љ—Л–µ —Д–µ—А–Љ–µ–љ—В—Л –њ–µ—З–µ–љ–Є, –њ–Њ–≤—Л—И–∞—О—В —Б–Ї–Њ—А–Њ—Б—В—М —Б–Є–љ—В–µ–Ј–∞ –Є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Н—В–Є—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤, —Г—Б–Є–ї–Є–≤–∞—О—В –±–Є–Њ—В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є—О –≤–µ—Й–µ—Б—В–≤, –∞–Ї—В–Є–≤–Є—А—Г—О—В –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—Ж–µ—Б—Б—Л, —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –±—Л—Б—В—А–Њ–Љ—Г –≤—Л–≤–µ–і–µ–љ–Є—О –Є–Ј –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ —З—Г–ґ–µ—А–Њ–і–љ—Л—Е —В–Њ–Ї—Б–Є—З–љ—Л—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є. –І–µ—В–≤–µ—А—В—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –Њ–±–ї–∞–і–∞—О—В —И–Є—А–Њ–Ї–Є–Љ —Б–њ–µ–Ї—В—А–Њ–Љ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, —Б–Њ–і–µ—А–ґ–∞—В –Ї–Њ–Љ–њ–ї–µ–Ї—Б –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –Є –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, –њ–Њ–≤—Л—И–∞—О—В —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Ї –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—О –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤, —Г–Љ–µ–љ—М—И–∞—О—В —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л, –≤ —В. —З. –њ–Њ—Б–ї–µ –њ—А–Є–љ—П—В–Є—П –∞–ї–Ї–Њ–≥–Њ–ї—П –Є –і—А. [10].
–С–Њ–ї—М—И–Њ–є –Є–љ—В–µ—А–µ—Б –і–ї—П –Ї–ї–Є–љ–Є—Ж–Є—Б—В–Њ–≤ –≤ –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —В–∞—Г—А–Є–љ, –Ї–Њ—В–Њ—А—Л–є —П–≤–ї—П–µ—В—Б—П –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л–Љ –њ—А–Њ–і—Г–Ї—В–Њ–Љ –Њ–±–Љ–µ–љ–∞ —Б–µ—А–Њ—Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В: —Ж–Є—Б—В–µ–Є–љ–∞, —Ж–Є—Б—В–µ–∞–Љ–Є–љ–∞, –Љ–µ—В–Є–Њ–љ–Є–љ–∞. –Ґ–∞—Г—А–Є–љ (—А–Є—Б. 2) вАУ –ґ–Є–Ј–љ–µ–љ–љ–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞—П —Б—Г–ї—М—Д–Њ–∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–∞, –Ї–Њ—В–Њ—А–∞—П –±—Л–ї–∞ –љ–∞–є–і–µ–љ–∞ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є —Г –≤—Б–µ—Е –≤–Є–і–Њ–≤ –ґ–Є–≤–Њ—В–љ—Л—Е. –Т —А–∞—Б—В–Є—В–µ–ї—М–љ–Њ–Љ –Љ–Є—А–µ —Н—В–Њ –≤–µ—Й–µ—Б—В–≤–Њ –љ–µ –≤—Б—В—А–µ—З–∞–µ—В—Б—П. –Ш—Б–Ї–ї—О—З–µ–љ–Є–µ —Б–Њ—Б—В–∞–≤–ї—П—О—В –Ї—А–∞—Б–љ—Л–µ –≤–Њ–і–Њ—А–Њ—Б–ї–Є. –Ґ–∞–Ї –Ї–∞–Ї —Б–Є–љ—В–µ–Ј —В–∞—Г—А–Є–љ–∞ —Г –ї—О–і–µ–є –Њ–≥—А–∞–љ–Є—З–µ–љ, —Б—Г—Й–µ—Б—В–≤—Г–µ—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –µ–≥–Њ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—П.
–Т–Њ 2-–є –њ–Њ–ї–Њ–≤–Є–љ–µ –•–• –≤. –±—Л–ї–Њ –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–Њ –±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —А–∞–±–Њ—В, –њ–Њ—Б–≤—П—Й–µ–љ–љ—Л—Е —Н—Д—Д–µ–Ї—В–∞–Љ —В–∞—Г—А–Є–љ–∞. –С–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –ї–µ—З–µ–±–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –±—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ –њ—А–Є –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е, –≥–ї–Є–Ї–Њ–Ј–Є–і–љ—Л—Е –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є—П—Е, –≥–Є–њ–µ—А—Е–Њ–ї–µ—Б—В–µ—А–Є–љ–µ–Љ–Є–Є, –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –њ–µ—З–µ–љ–Є, –≤ —В. —З. –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е, –∞–ї–Ї–Њ–≥–Њ–ї–Є–Ј–Љ–µ [11].
–†–µ–Ј—Г–ї—М—В–∞—В—Л —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –і–∞–љ–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —А–µ–њ–µ—А—Д—Г–Ј–Є–Њ–љ–љ–∞—П –Є—И–µ–Љ–Є—П –њ–µ—З–µ–љ–Є –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –љ–µ —В–Њ–ї—М–Ї–Њ —В—А–∞–≤–Љ–Њ–є –њ–µ—З–µ–љ–Є, –љ–Њ –Є —Н–љ–і–Њ–Ї—Б–µ–Љ–Є–µ–є, –Ї–Њ—В–Њ—А–∞—П —Г—Б—Г–≥—Г–±–ї—П–µ—В Hir-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ—Л–µ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –њ–µ—З–µ–љ–Є –Є –і–Є—Б—Д—Г–љ–Ї—Ж–Є—О –Є–ї–Є –і–∞–ґ–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–Є—З–Є–љ–Њ–є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —В–∞—Г—А–Є–љ–∞ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї –Ј–∞—Й–Є—В–µ –њ–µ—З–µ–љ–Є –Њ—В –Є—И–µ–Љ–Є–Є –Є —А–µ–њ–µ—А—Д—Г–Ј–Є–Є. –≠—В–Є –і–∞–љ–љ—Л–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —В–∞—Г—А–Є–љ–∞ –≤ –Ј–∞—Й–Є—В–µ –њ–µ—З–µ–љ–Є –Њ—В —Н–љ–і–Њ—В–Њ–Ї—Б–Є–љ–∞, –≤—Л–Ј–≤–∞–љ–љ–Њ–≥–Њ —В—А–∞–≤–Љ–Њ–є, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ–Њ—Б–ї–µ Hir-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –њ–µ—З–µ–љ–Є. –У–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ —В–∞—Г—А–Є–љ–∞, –њ–Њ–ї—Г—З–µ–љ–љ–Њ–µ –≤ —Н—В–Њ–є —Б–µ—А–Є–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤, –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М –µ–≥–Њ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ, –∞–љ—В–Є–Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ—Л–Љ –Є –∞–љ—В–Є–∞–њ–Њ–њ—В–Њ—В–Є—З–µ—Б–Ї–Є–Љ —Н—Д—Д–µ–Ї—В–∞–Љ–Є.
–Я—А–Њ–≤–µ–і–µ–љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–ї–Є—П–љ–Є—П –љ–Є–Ј–Ї–Њ–±–µ–ї–Ї–Њ–≤–Њ–є –і–Є–µ—В—Л –љ–∞ —Н–Ї—Б–њ—А–µ—Б—Б–Є—О –≥–µ–љ–Њ–≤ —Г –Љ—Л—И–µ–є. –Ю–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ —В–∞–Ї–∞—П –і–Є–µ—В–∞ –Ј–∞—В—А–∞–≥–Є–≤–∞–µ—В 2013 –≥–µ–љ–Њ–≤ –≤ –њ–µ—З–µ–љ–Є –Є 967 –≥–µ–љ–Њ–≤ —Б–Ї–µ–ї–µ—В–љ—Л—Е –Љ—Л—И—Ж. –†–µ–≥—Г–ї—П—Ж–Є—П —В–∞—Г—А–Є–љ–Њ–Љ –Ј–∞—В—А–∞–≥–Є–≤–∞–µ—В –≥–µ–љ—Л –≤ –њ–µ—З–µ–љ–Є, —А–µ–≥—Г–ї–Є—А—Г—О—Й–Є–µ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В, –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ–µ —Д–Њ—Б—Д–Њ—А–Є–ї–Є—А–Њ–≤–∞–љ–Є–µ –Є —Ж–Є–Ї–ї —В—А–Є–Ї–∞—А–±–Њ–љ–Њ–≤—Л—Е –Ї–Є—Б–ї–Њ—В –≤ —Б–Ї–µ–ї–µ—В–љ—Л—Е –Љ—Л—И—Ж–∞—Е. –Р–≤—В–Њ—А—Л –і–µ–ї–∞—О—В –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ, —З—В–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П –±–µ–ї–Ї–∞ –њ—А–Є –≥–µ—Б—В–∞—Ж–Є–Є –њ—А–Є–≤–Њ–і–Є—В –Ї –і–µ—Д–Є—Ж–Є—В—Г –Љ–∞—Б—Б—Л –њ—А–Є —А–Њ–ґ–і–µ–љ–Є–Є, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ–Љ –≥–µ–љ–љ–Њ–є —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є. –≠—В–Є —Н—Д—Д–µ–Ї—В—Л –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–∞—О—В—Б—П –њ—А–Є –і–Њ–±–∞–≤–ї–µ–љ–Є–Є –≤ —А–∞—Ж–Є–Њ–љ —В–∞—Г—А–Є–љ–∞. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —В–∞—Г—А–Є–љ —П–≤–ї—П–µ—В—Б—П –Ї–ї—О—З–µ–≤—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ –≤ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–Љ —Д–µ—В–∞–ї—М–љ–Њ–Љ –њ—А–Њ–≥—А–∞–Љ–Љ–Є—А–Њ–≤–∞–љ–Є–Є.
–Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —В–∞—Г—А–Є–љ –Ј–∞—Й–Є—Й–∞–µ—В –≥–µ–њ–∞—В–Њ—Ж–Є—В—Л –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П—Е: –њ—А–Є –і–Є–µ—В–µ —Б –≤—Л—Б–Њ–Ї–Є–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞, –Њ—В—А–∞–≤–ї–µ–љ–Є–Є —Н–љ–і–Њ—В–Њ–Ї—Б–Є–љ–Њ–Љ, —Н—В–∞–љ–Њ–ї–Њ–Љ, —З–µ—В—Л—А–µ—Е—Е–ї–Њ—А–Є—Б—В—Л–Љ —Г–≥–ї–µ—А–Њ–і–Њ–Љ, —Ж–Є–Ї–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–Љ. –Ґ–∞—Г—А–Є–љ —Г–Љ–µ–љ—М—И–∞–µ—В –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—О, –Њ–Ї—Б–Є–і–∞—В–Є–≤–љ—Л–є —Б—В—А–µ—Б—Б –Є —Д–Є–±—А–Њ–≥–µ–љ–µ–Ј.
–Э–∞–Ј–љ–∞—З–µ–љ–Є–µ —В–∞—Г—А–Є–љ–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ —Б–њ–Њ—Б–Њ–±–Њ–Љ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –љ–∞—А—Г—И–µ–љ–Є–є —Д—Г–љ–Ї—Ж–Є–є –њ–µ—З–µ–љ–Є –њ—А–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є –њ–µ—А–µ–і–Њ–Ј–Є—А–Њ–≤–Ї–µ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞. –Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ —В–∞—Г—А–Є–љ–∞ –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В —Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–Љ—Г –і–µ–є—Б—В–≤–Є—О –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –≤—Л–≤–µ–і–µ–љ–Є—О –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ –Є–Ј –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, —Б–Њ—Е—А–∞–љ–µ–љ–Є—О –њ—Г–ї–∞ –≥–ї—Г—В–∞—В–Є–Њ–љ–∞, –њ–Њ–і–і–µ—А–ґ–Є–≤–∞–µ—В —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є–µ —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е —Б–Є—Б—В–µ–Љ –і–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є. –Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —В–∞—Г—А–Є–љ –Њ–њ—В–Є–Љ–Є–Ј–Є—А—Г–µ—В –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –Њ–±—К–µ–Љ–∞ –Ј–∞ —Б—З–µ—В —А–µ–≥—Г–ї–Є—А–Њ–≤–∞–љ–Є—П —Г—А–Њ–≤–љ—П Ca2+ –≤ –≥–µ–њ–∞—В–Њ—Ж–Є—В–∞—Е, —Б–њ–Њ—Б–Њ–±–µ–љ –њ–Њ–і–∞–≤–ї—П—В—М –њ—А–Њ—Ж–µ—Б—Б—Л –њ–µ—А–µ–Ї–Є—Б–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –ї–Є–њ–Є–і–Њ–≤, —Б—В–∞–±–Є–ї–Є–Ј–Є—А–Њ–≤–∞—В—М –Љ–µ–Љ–±—А–∞–љ–љ—Г—О –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М –Є —В—А–∞–љ—Б–њ–Њ—А—В –Є–Њ–љ–Њ–≤. –Ґ–∞—Г—А–Є–љ, —Г—З–∞—Б—В–≤—Г—П –≤ —Д–Њ—Б—Д–Њ—А–Є–ї–Є—А–Њ–≤–∞–љ–Є–Є –љ–µ–Ї–Њ—В–Њ—А—Л—Е —А–µ–≥—Г–ї—П—В–Њ—А–љ—Л—Е –Є –Љ–µ–Љ–±—А–∞–љ–љ—Л—Е –±–µ–ї–Ї–Њ–≤, –Є–Ј–Љ–µ–љ—П–µ—В –Є—Е –Ї–Њ–љ—Д–Њ—А–Љ–∞—Ж–Є—О, –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, —Б—В—А—Г–Ї—В—Г—А–љ–Њ-—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ –Љ–µ–Љ–±—А–∞–љ –Ї–ї–µ—В–Њ–Ї. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–µ–Љ–±—А–∞–љ–Њ—Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г—О—Й–Є–µ, –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–µ –Є –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ –њ–Њ–Ј–≤–Њ–ї—П—О—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М —В–∞—Г—А–Є–љ –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б—А–µ–і—Б—В–≤–∞ –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П CYP2E1-–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є –њ–µ—З–µ–љ–Є, –≤ —В. —З. –њ—А–Є –њ–µ—А–µ–і–Њ–Ј–Є—А–Њ–≤–Ї–µ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ [12].
–Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–µ –і–∞–љ–љ—Л–µ –Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–Љ –≤–ї–Є—П–љ–Є–Є —В–∞—Г—А–Є–љ–∞ –љ–∞ —Д—Г–љ–Ї—Ж–Є—О –њ–µ—З–µ–љ–Є –њ–Њ—Б–ї—Г–ґ–Є–ї–Є –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П —Б–Њ–Ј–і–∞–љ–Є—П –Ы–°, –Њ–±–ї–∞–і–∞—О—Й–Є—Е –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ. –Ю–і–љ–Є–Љ –Є–Ј —В–∞–Ї–Є—Е –љ–Њ–≤—Л—Е –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞ –Њ—Б–љ–Њ–≤–µ —В–∞—Г—А–Є–љ–∞ —П–≤–ї—П–µ—В—Б—П –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –Ф–Є–±–Є–Ї–Њ—А. –Ф–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Ф–Є–±–Є–Ї–Њ—А –Њ–±–ї–∞–і–∞–µ—В –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є –њ—А–Є –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є—П—Е —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞; –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –њ–µ—З–µ–љ–Є, –њ—А–Њ—В–µ–Ї–∞—О—Й–Є—Е —Б –ґ–Є—А–Њ–≤–Њ–є –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є–µ–є –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤; —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є—П—Е –њ–µ—З–µ–љ–Є, –≤—Л–Ј–≤–∞–љ–љ—Л—Е CCl4, –≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ–Є –Є –і—А—Г–≥–Є–Љ–Є –ї–µ–Ї–∞—А—Б—В–≤–∞–Љ–Є (–Ы–Я–Я). –Ю–±–∞ —Н—В–Є –њ–Њ–Ї–∞–Ј–∞–љ–Є—П –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–∞–љ—Л, —В. –Ї. –њ—А–Є –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —Д—Г–љ–Ї—Ж–Є–Є –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤ –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—О—В—Б—П –Њ–±–Љ–µ–љ –ґ–Є—А–Њ–≤ –Є –ї–Є–њ–Є–і–љ—Л–є –њ—А–Њ—Д–Є–ї—М.
–Ю–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ф–Є–±–Є–Ї–Њ—А–∞ —Г –±–Њ–ї—М–љ—Л—Е —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –њ–µ—А—Б–Є—Б—В–Є—А—Г—О—Й–Є–Љ –≥–µ–њ–∞—В–Є—В–Њ–Љ –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –њ—А–µ–њ–∞—А–∞—В –≤ –і–Њ–Ј–µ 0,5 –≥ 2 —А./—Б—Г—В –њ—А–Є–≤–Њ–і–Є–ї –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О –њ–µ—З–µ–љ–Њ—З–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Є —Г–Љ–µ–љ—М—И–µ–љ–Є—О —Ж–Є—В–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ [13].
–Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л —Б–Њ—В—А—Г–і–љ–Є–Ї–∞–Љ–Є –Т–Њ–ї–≥–Њ–≥—А–∞–і—Б–Ї–Њ–≥–Њ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–≥–Њ —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–∞, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –њ–Њ—Б–ї–µ –Ї—Г—А—Б–∞ —В–µ—А–∞–њ–Є–Є –Ф–Є–±–Є–Ї–Њ—А–Њ–Љ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О 21 –і–µ–љ—М –≤ –і–Њ–Ј–µ 1 –≥/—Б—Г—В –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ —Г –±–Њ–ї—М–љ—Л—Е, —Б—В—А–∞–і–∞—О—Й–Є—Е —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –∞–Ї—В–Є–≤–љ—Л–Љ –≥–µ–њ–∞—В–Є—В–Њ–Љ. –Я—А–µ–і—И–µ—Б—В–≤—Г—О—Й–∞—П –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П (–њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ 40 –Љ–≥/—Б—Г—В) –Ї –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О –љ–µ –њ—А–Є–≤–µ–ї–∞: —Б–Њ—Е—А–∞–љ—П–ї–Є—Б—М –≤—Л—Б–Њ–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Д–µ—А–Љ–µ–љ—В–Њ–≤ –Є —Б–љ–Є–ґ–µ–љ–Є–µ –њ–µ—З–µ–љ–Њ—З–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ [14].
–Ф–∞–љ–љ—Л–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ф–Є–±–Є–Ї–Њ—А–∞ –≤ –Ї–ї–Є–љ–Є–Ї–µ –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В –љ–∞–ї–Є—З–Є–µ —Г —В–∞—Г—А–Є–љ–∞ –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Є —А–∞—Б—И–Є—А—П—О—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –µ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Ъ–∞–Ї –њ—А–∞–≤–Є–ї–Њ, —В–∞—Г—А–Є–љ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ —Б–Њ—Б—В–∞–≤–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є, —З—В–Њ –њ–Њ–і—А–∞–Ј—Г–Љ–µ–≤–∞–µ—В —Б–Њ—З–µ—В–∞–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Ы–°, —З–∞—Б—В–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г—О—Й–Є—Е—Б—П –Њ–і–љ–Є–Љ –Є —В–µ–Љ –ґ–µ –Є–Ј–Њ—Д–µ—А–Љ–µ–љ—В–Њ–Љ —Ж–Є—В–Њ—Е—А–Њ–Љ–∞, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О –≤–µ—А–Њ—П—В–љ–Њ—Б—В–Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П –Ы–° –љ–∞ —Г—А–Њ–≤–љ–µ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Є —А–Є—Б–Ї–∞ –њ—А–Њ—П–≤–ї–µ–љ–Є–є –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –ї–µ–Ї–∞—А—Б—В–≤. –Т —В–∞–Ї–Њ–Љ —Б–ї—Г—З–∞–µ –њ—А–Є—А–Њ–і–љ–Њ–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є–µ —В–∞—Г—А–Є–љ, –Њ–±–ї–∞–і–∞—О—Й–µ–µ –Љ–Њ–і—Г–ї–Є—А—Г—О—Й–Є–Љ (–Є–љ–і—Г—Ж–Є—А—Г—О—Й–Є–Љ) –і–µ–є—Б—В–≤–Є–µ–Љ –љ–∞ —Б–Є—Б—В–µ–Љ—Г CYP450 3A4 –Є –≥–µ–њ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, –Љ–Њ–ґ–µ—В –±—Л—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Њ –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ –і–ї—П –њ–Њ–≤—Л—И–µ–љ–Є—П –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є.










.gif)



