–ö–į–ļ —á–į—Ā—ā–ĺ –≤ –Ņ—Ä–į–ļ—ā–ł–ļ–Ķ –≤—Ä–į—á–į-—ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–į –ł –≥–į—Ā—ā—Ä–ĺ—ć–Ĺ—ā–Ķ—Ä–ĺ–Ľ–ĺ–≥–į –≤–ĺ–∑–Ĺ–ł–ļ–į–Ķ—ā –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–ĺ—Ā—ā—Ć –Ĺ–į–∑–Ĺ–į—á–į—ā—Ć –≥–Ķ–Ņ–į—ā–ĺ–Ņ—Ä–ĺ—ā–Ķ–ļ—ā–ĺ—Ä—č? –ö–į–ļ–ĺ–≤—č —ā–ĺ—á–ļ–ł –Ņ—Ä–ł–Ľ–ĺ–∂–Ķ–Ĺ–ł—Ź –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ —ć—ā–ĺ–Ļ –ļ–į—ā–Ķ–≥–ĺ—Ä–ł–ł? –Ď–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–ĺ –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č—Ö –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –ī–Ľ—Ź –•–ó–ü –ł–ľ–Ķ—é—ā, –ļ–į–ļ –Ņ—Ä–į–≤–ł–Ľ–ĺ, –Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ķ—ā–ł—á–Ķ—Ā–ļ—É—é –Ĺ–į–Ņ—Ä–į–≤–Ľ–Ķ–Ĺ–Ĺ–ĺ—Ā—ā—Ć –ī–Ķ–Ļ—Ā—ā–≤–ł—Ź –ł –≤ –†–ĺ—Ā—Ā–ł–ł —ā—Ä–į–ī–ł—Ü–ł–ĺ–Ĺ–Ĺ–ĺ –ĺ—ā–Ĺ–ĺ—Ā—Ź—ā—Ā—Ź –ļ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į–ľ –≥–Ķ–Ņ–į—ā–ĺ–Ņ—Ä–ĺ—ā–Ķ–ļ—ā–ĺ—Ä–Ĺ–ĺ–≥–ĺ –ī–Ķ–Ļ—Ā—ā–≤–ł—Ź (–ü–ď–ü–Ē). –ď–ĺ–≤–ĺ—Ä—Ź –ĺ —ā–ĺ—á–ļ–į—Ö –Ņ—Ä–ł–Ľ–ĺ–∂–Ķ–Ĺ–ł—Ź –ü–ď–ü–Ē, —Ā–Ľ–Ķ–ī—É–Ķ—ā –≤ –Ņ–Ķ—Ä–≤—É—é –ĺ—á–Ķ—Ä–Ķ–ī—Ć —É–Ņ–ĺ–ľ—Ź–Ĺ—É—ā—Ć –į–Ľ–ļ–ĺ–≥–ĺ–Ľ—Ć–Ĺ—č–Ķ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź –Ņ–Ķ—á–Ķ–Ĺ–ł (–ź–ü–ü). –ź–Ľ–ļ–ĺ–≥–ĺ–Ľ—Ć–Ĺ—č–Ļ –≥–Ķ–Ņ–į—ā–ł—ā, —Ä–į–∑–≤–ł–≤–į—é—Č–ł–Ļ—Ā—Ź –Ĺ–į —Ą–ĺ–Ĺ–Ķ —Ü–ł—Ä—Ä–ĺ–∑–į –Ņ–Ķ—á–Ķ–Ĺ–ł –į–Ľ–ļ–ĺ–≥–ĺ–Ľ—Ć–Ĺ–ĺ–Ļ —ć—ā–ł–ĺ–Ľ–ĺ–≥–ł–ł, —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –ĺ–ī–Ĺ–ĺ–Ļ –ł–∑ –≥–Ľ–į–≤–Ĺ—č—Ö –Ņ—Ä–ł—á–ł–Ĺ –≥–ĺ—Ā–Ņ–ł—ā–į–Ľ–ł–∑–į—Ü–ł–ł –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö —Ā –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź–ľ–ł –Ņ–Ķ—á–Ķ–Ĺ–ł [1]. –ü–ĺ –ī–į–Ĺ–Ĺ—č–ľ –í–ě–ó, 4% –≤—Ā–Ķ—Ö –Ī–ĺ–Ľ–Ķ–∑–Ĺ–Ķ–Ļ –ĺ–Ī—É—Ā–Ľ–ĺ–≤–Ľ–Ķ–Ĺ—č –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ–ľ –į–Ľ–ļ–ĺ–≥–ĺ–Ľ—Ź ‚Äď –ĺ–ī–Ĺ–ĺ–≥–ĺ –ł–∑ –≤–Ķ–ī—É—Č–ł—Ö —Ā—Ä–Ķ–ī–ł 26 –ł–∑—É—á–Ķ–Ĺ–Ĺ—č—Ö —Ą–į–ļ—ā–ĺ—Ä–ĺ–≤ —Ä–ł—Ā–ļ–į —Ā–ľ–Ķ—Ä—ā–Ĺ–ĺ—Ā—ā–ł –ł –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ķ–ľ–ĺ—Ā—ā–ł –≤–ĺ –≤—Ā–Ķ–ľ –ľ–ł—Ä–Ķ [2, 3]. –ď–ĺ–≤–ĺ—Ä—Ź –ĺ –Ņ—Ä–ł–Ĺ—Ü–ł–Ņ–į—Ö —ā–Ķ—Ä–į–Ņ–ł–ł –į–Ľ–ļ–ĺ–≥–ĺ–Ľ—Ć–Ĺ—č—Ö –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–Ļ –Ņ–Ķ—á–Ķ–Ĺ–ł, —Ā–Ľ–Ķ–ī—É–Ķ—ā —É–ļ–į–∑–į—ā—Ć, —á—ā–ĺ, –Ĺ–į—Ä—Ź–ī—É —Ā –Ņ–ĺ–Ľ–Ĺ—č–ľ –ł—Ā–ļ–Ľ—é—á–Ķ–Ĺ–ł–Ķ–ľ –į–Ľ–ļ–ĺ–≥–ĺ–Ľ—Ź, –į–ļ—ā–ł–≤–Ĺ–ĺ –ł–∑—É—á–į—é—ā—Ā—Ź –≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ—Ā—ā–ł –Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ķ—ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł, –≤ —ā. —á. —Ā –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ–ľ —Ä–į–∑–Ľ–ł—á–Ĺ—č—Ö –≥–Ķ–Ņ–į—ā–ĺ–Ņ—Ä–ĺ—ā–Ķ–ļ—ā–ĺ—Ä–ĺ–≤.
–Ē–ĺ—Ā—ā–į—ā–ĺ—á–Ĺ–ĺ —á–į—Ā—ā–ĺ –ĺ–Ī—Ā—É–∂–ī–į–Ķ—ā—Ā—Ź –≤ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ņ—Ä–į–ļ—ā–ł–ļ–Ķ –≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ—Ā—ā—Ć –ł –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–ĺ—Ā—ā—Ć –Ĺ–į–∑–Ĺ–į—á–Ķ–Ĺ–ł—Ź –≥–Ķ–Ņ–į—ā–ĺ–Ņ—Ä–ĺ—ā–Ķ–ļ—ā–ĺ—Ä–ĺ–≤ —É –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł–ľ–ł –≥–Ķ–Ņ–į—ā–ł—ā–į–ľ–ł –í (–•–ď–í) –ł –° (–•–ď–°). –ü—Ä–ĺ–Ī–Ľ–Ķ–ľ–į –•–ď–í –ł –•–ď–° ‚Äď –ĺ–ī–Ĺ–į –ł–∑ —Ā–į–ľ—č—Ö —Ā–Ķ—Ä—Ć–Ķ–∑–Ĺ—č—Ö –≤ –∑–ī—Ä–į–≤–ĺ–ĺ—Ö—Ä–į–Ĺ–Ķ–Ĺ–ł–ł –≤ —Ü–Ķ–Ľ–ĺ–ľ. –ü–ĺ –ī–į–Ĺ–Ĺ—č–ľ –í–ě–ó, –ĺ–ļ–ĺ–Ľ–ĺ 400 –ľ–Ľ–Ĺ —á–Ķ–Ľ–ĺ–≤–Ķ–ļ —Ā—ā—Ä–į–ī–į—é—ā –•–ď–í, —á–ł—Ā–Ľ–ĺ –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –•–ď–° –≤ –ľ–ł—Ä–Ķ —Ā–ĺ—Ā—ā–į–≤–Ľ—Ź–Ķ—ā –Ī–ĺ–Ľ–Ķ–Ķ 170 –ľ–Ľ–Ĺ [4, 5]. –ü—Ä–ł —ć—ā–ĺ–ľ –ī–ĺ–ļ–į–∑–į–Ĺ–ĺ, —á—ā–ĺ –≤–ł—Ä—É—Ā—č –≥–Ķ–Ņ–į—ā–ł—ā–ĺ–≤ –í –ł –° —Ź–≤–Ľ—Ź—é—ā—Ā—Ź –≤–į–∂–Ĺ–Ķ–Ļ—ą–ł–ľ–ł –Ņ—Ä–ł—á–ł–Ĺ–į–ľ–ł –Ĺ–Ķ —ā–ĺ–Ľ—Ć–ļ–ĺ —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł—Ö –≥–Ķ–Ņ–į—ā–ł—ā–ĺ–≤, –Ĺ–ĺ —Ü–ł—Ä—Ä–ĺ–∑–ĺ–≤ –Ņ–Ķ—á–Ķ–Ĺ–ł –ł –≥–Ķ–Ņ–į—ā–ĺ—Ü–Ķ–Ľ–Ľ—é–Ľ—Ź—Ä–Ĺ–ĺ–Ļ –ļ–į—Ä—Ü–ł–Ĺ–ĺ–ľ—č (–ď–¶–ö). –ź–Ī—Ā–ĺ–Ľ—é—ā–Ĺ–ĺ –Ī–Ķ—Ā—Ā–Ņ–ĺ—Ä–Ĺ–ĺ–Ļ –Ņ—Ä–ł–∑–Ĺ–į–Ĺ–į –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–ĺ—Ā—ā—Ć —ć—ā–ł–ĺ—ā—Ä–ĺ–Ņ–Ĺ–ĺ–Ļ –Ņ—Ä–ĺ—ā–ł–≤–ĺ–≤–ł—Ä—É—Ā–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł (–ü–í–Ę) –•–ď–í –ł –•–ď–° [4, 5].
–ü—Ä–ł —ć—ā–ĺ–ľ –ī–ĺ—Ā—ā–į—ā–ĺ—á–Ĺ–ĺ –ī–į–≤–Ĺ–ĺ –ī–Ľ—Ź –∑–į–ľ–Ķ–ī–Ľ–Ķ–Ĺ–ł—Ź –Ņ—Ä–ĺ–≥—Ä–Ķ—Ā—Ā–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –Ĺ–Ķ–ļ—Ä–ĺ–≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö –ł —Ą–ł–Ī—Ä–ĺ—ā–ł—á–Ķ—Ā–ļ–ł—Ö –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ļ –≤ –Ņ–Ķ—á–Ķ–Ĺ–ł –Ĺ–Ķ–ļ–ĺ—ā–ĺ—Ä—č–Ķ –į–≤—ā–ĺ—Ä—č —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī—É—é—ā –į–Ĺ—ā–ł–ĺ–ļ—Ā–ł–ī–į–Ĺ—ā—č, —Ü–ł—ā–ĺ–ļ–ł–Ĺ—č, –ī—Ä—É–≥–ł–Ķ –ü–ď–ü–Ē –ľ–ł–Ĺ—É—Ź –ü–í–Ę –Ņ—Ä–ł –Ĺ–Ķ–≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ—Ā—ā–ł –Ķ–Ķ –Ņ—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ–ł—Ź –Ņ–ĺ –ļ–į–ļ–ł–ľ-–Ľ–ł–Ī–ĺ –Ņ—Ä–ł—á–ł–Ĺ–į–ľ. –í –Ĺ–į—Ā—ā–ĺ—Ź—Č–Ķ–Ķ –≤—Ä–Ķ–ľ—Ź, –ĺ–ī–Ĺ–į–ļ–ĺ, —É–Ī–Ķ–ī–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ķ –ī–į–Ĺ–Ĺ—č–Ķ —Ā–≤–ł–ī–Ķ—ā–Ķ–Ľ—Ć—Ā—ā–≤—É—é—ā, —á—ā–ĺ, –Ĺ–Ķ –Ņ—Ä–ł–Ī–Ķ–≥–į—Ź –ļ –ü–í–Ę, –Ľ–ł—ą—Ć –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į–ľ–ł –≥–Ķ–Ņ–į—ā–ĺ—ā–ĺ–ļ—Ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ĺ–į–Ņ—Ä–į–≤–Ľ–Ķ–Ĺ–Ĺ–ĺ—Ā—ā–ł –Ĺ–Ķ –ĺ—Ā—ā–į–Ĺ–ĺ–≤–ł—ā—Ć –Ņ—Ä–ĺ–≥—Ä–Ķ—Ā—Ā–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź –Ņ–Ķ—á–Ķ–Ĺ–ł.
–ē—Č–Ķ –ĺ–ī–Ĺ–ĺ–Ļ —ā–ĺ—á–ļ–ĺ–Ļ –Ņ—Ä–ł–Ľ–ĺ–∂–Ķ–Ĺ–ł—Ź –ü–ď–ü–Ē —Ā—á–ł—ā–į—é—ā—Ā—Ź –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č–Ķ –ł —ā–ĺ–ļ—Ā–ł—á–Ķ—Ā–ļ–ł–Ķ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź –Ņ–Ķ—á–Ķ–Ĺ–ł (–õ–ü–ü). –†–į—Ā–Ņ—Ä–ĺ—Ā—ā—Ä–į–Ĺ–Ķ–Ĺ–Ĺ–ĺ—Ā—ā—Ć –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č—Ö –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–Ļ –Ņ–Ķ—á–Ķ–Ĺ–ł –≤ —Ä–į–∑–Ĺ—č—Ö —Ā—ā—Ä–į–Ĺ–į—Ö –Ĺ–Ķ–ĺ–ī–ł–Ĺ–į–ļ–ĺ–≤–į –ł –∑–į–≤–ł—Ā–ł—ā –ĺ—ā —Ā—ā—Ä—É–ļ—ā—É—Ä—č –Ņ—Ä–ł–ľ–Ķ–Ĺ—Ź—é—Č–ł—Ö—Ā—Ź –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤, –ī–ĺ–∑–ł—Ä–ĺ–≤–ĺ–ļ –ł –≤—Ä–Ķ–ľ–Ķ–Ĺ–ł –Ņ—Ä–ł–Ķ–ľ–į –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤. –í –†–ĺ—Ā—Ā–ł–ł –ĺ—Ā—ā—Ä—č–Ķ –ľ–Ķ–ī–ł–ļ–į–ľ–Ķ–Ĺ—ā–ĺ–∑–Ĺ—č–Ķ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź –Ņ–Ķ—á–Ķ–Ĺ–ł –≤—č—Ź–≤–Ľ—Ź—é—ā—Ā—Ź —É 2,7% –≥–ĺ—Ā–Ņ–ł—ā–į–Ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö [6, 7]. –ü—Ä–ł –õ–ü–ü —á–į—Č–Ķ –≤—Ā–Ķ–≥–ĺ —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī—É–Ķ—ā—Ā—Ź –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į—ā—Ć –≥–Ķ–Ņ–į—ā–ĺ–Ņ—Ä–ĺ—ā–Ķ–ļ—ā–ł–≤–Ĺ—É—é —ā–Ķ—Ä–į–Ņ–ł—é –ī–Ľ—Ź –Ņ—Ä–Ķ–ī–ĺ—Ö—Ä–į–Ĺ–Ķ–Ĺ–ł—Ź –Ņ–Ķ—á–Ķ–Ĺ–ĺ—á–Ĺ—č—Ö –ļ–Ľ–Ķ—ā–ĺ–ļ –ĺ—ā –Ņ–ĺ–≤—Ä–Ķ–∂–ī–į—é—Č–Ķ–≥–ĺ –≤–ĺ–∑–ī–Ķ–Ļ—Ā—ā–≤–ł—Ź —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–į –Ņ—Ä–ĺ–ī—É–ļ—ā–ĺ–≤ —Ä–į—Ā–Ņ–į–ī–į.
–Ě–į—É—á–Ĺ—č–Ķ –ł–∑—č—Ā–ļ–į–Ĺ–ł—Ź –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–ł—Ö –ī–Ķ—Ā—Ź—ā–ł–Ľ–Ķ—ā–ł–Ļ –Ņ–ĺ–ļ–į–∑–į–Ľ–ł, —á—ā–ĺ –Ĺ–Ķ–į–Ľ–ļ–ĺ–≥–ĺ–Ľ—Ć–Ĺ–į—Ź –∂–ł—Ä–ĺ–≤–į—Ź –Ī–ĺ–Ľ–Ķ–∑–Ĺ—Ć –Ņ–Ķ—á–Ķ–Ĺ–ł (–Ě–ź–Ė–Ď–ü) —Ā—ā–į–Ľ–į —Ā–Ķ—Ä—Ć–Ķ–∑–Ĺ–ĺ–Ļ –Ņ—Ä–ĺ–Ī–Ľ–Ķ–ľ–ĺ–Ļ –ł –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ—Ź–Ķ—ā —Ā–Ņ–Ķ–ļ—ā—Ä –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł—Ö –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ļ –Ņ–Ķ—á–Ķ–Ĺ–ł –ĺ—ā –Ņ—Ä–ĺ—Ā—ā–ĺ–≥–ĺ –ľ–į–ļ—Ä–ĺ–≤–Ķ–∑–ł–ļ—É–Ľ—Ź—Ä–Ĺ–ĺ–≥–ĺ —Ā—ā–Ķ–į—ā–ĺ–∑–į –ī–ĺ —Ü–ł—Ä—Ä–ĺ–∑–į –Ņ–Ķ—á–Ķ–Ĺ–ł –≤ –ł—Ā—Ö–ĺ–ī–Ķ –Ņ—Ä–ĺ–≥—Ä–Ķ—Ā—Ā–ł—Ä—É—é—Č–Ķ–≥–ĺ –Ĺ–Ķ–į–Ľ–ļ–ĺ–≥–ĺ–Ľ—Ć–Ĺ–ĺ–≥–ĺ —Ā—ā–Ķ–į—ā–ĺ–≥–Ķ–Ņ–į—ā–ł—ā–į (–Ě–ź–°–ď) –ł –ď–¶–ö. –°—Ä–Ķ–ī–ł –Ĺ–į—Ā–Ķ–Ľ–Ķ–Ĺ–ł—Ź –≤ —Ü–Ķ–Ľ–ĺ–ľ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ć —Ä–į—Ā–Ņ—Ä–ĺ—Ā—ā—Ä–į–Ĺ–Ķ–Ĺ–Ĺ–ĺ—Ā—ā–ł –Ě–ź–Ė–Ď–ü –ļ–ĺ–Ľ–Ķ–Ī–Ľ–Ķ—ā—Ā—Ź –ĺ—ā 3 –ī–ĺ 24%. –ě–ī–Ĺ–į–ļ–ĺ —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –ĺ–∂–ł—Ä–Ķ–Ĺ–ł–Ķ–ľ —á–į—Ā—ā–ĺ—ā–į –≤—Ā—ā—Ä–Ķ—á–į–Ķ–ľ–ĺ—Ā—ā–ł –Ě–ź–Ė–Ď–ü —É–≤–Ķ–Ľ–ł—á–ł–≤–į–Ķ—ā—Ā—Ź –ī–ĺ 84‚Äď96%, –≤ 25‚Äď55% –ł–∑ –ļ–ĺ—ā–ĺ—Ä—č—Ö –ł–ľ–Ķ—é—ā—Ā—Ź –Ņ—Ä–ł–∑–Ĺ–į–ļ–ł –Ě–ź–°–ď, –≤ 34‚Äď47% ‚Äď –Ņ—Ä–ł–∑–Ĺ–į–ļ–ł —Ą–ł–Ī—Ä–ĺ–∑–į, –į –≤ 3‚Äď12% ‚Äď –Ņ—Ä–ł–∑–Ĺ–į–ļ–ł —Ü–ł—Ä—Ä–ĺ–∑–į –Ņ–Ķ—á–Ķ–Ĺ–ł [8, 9]. –ü–į—Ü–ł–Ķ–Ĺ—ā—č —Ā —Ü–ł—Ä—Ä–ĺ–∑–ĺ–ľ –Ņ–Ķ—á–Ķ–Ĺ–ł –≤ –ł—Ā—Ö–ĺ–ī–Ķ –Ě–ź–Ė–Ď–ü –Ņ–ĺ–ī–≤–Ķ—Ä–≥–į—é—ā—Ā—Ź –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–ľ—É —Ä–ł—Ā–ļ—É —Ä–į–∑–≤–ł—ā–ł—Ź –ď–¶–ö (2,6% —Ā–Ľ—É—á–į–Ķ–≤ –≤ –≥–ĺ–ī) [10].
–ó–Ĺ–į–Ĺ–ł–Ķ –ľ–Ķ—Ö–į–Ĺ–ł–∑–ľ–ĺ–≤ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź, –ł—Ö —É–Ĺ–ł–≤–Ķ—Ä—Ā–į–Ľ—Ć–Ĺ–ĺ—Ā—ā—Ć –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ—Ź—é—ā —ā–Ķ–ĺ—Ä–Ķ—ā–ł—á–Ķ—Ā–ļ–ĺ–Ķ –ĺ–Ī–ĺ—Ā–Ĺ–ĺ–≤–į–Ĺ–ł–Ķ –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –ü–ď–ü–Ē ‚Äď —Ā–ĺ–Ķ–ī–ł–Ĺ–Ķ–Ĺ–ł–Ļ, –Ņ—Ä–Ķ–Ņ—Ź—ā—Ā—ā–≤—É—é—Č–ł—Ö —Ä–į–∑—Ä—É—ą–Ķ–Ĺ–ł—é –ļ–Ľ–Ķ—ā–ĺ—á–Ĺ—č—Ö –ľ–Ķ–ľ–Ī—Ä–į–Ĺ, –ĺ–ļ–į–∑—č–≤–į—é—Č–ł—Ö –≤–ĺ—Ā—Ā—ā–į–Ĺ–į–≤–Ľ–ł–≤–į—é—Č–Ķ–Ķ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ –Ĺ–į —Ā—ā—Ä—É–ļ—ā—É—Ä—É –ł —Ą—É–Ĺ–ļ—Ü–ł–ł –ľ–Ķ–ľ–Ī—Ä–į–Ĺ –≥–Ķ–Ņ–į—ā–ĺ—Ü–ł—ā–ĺ–≤, —Ā–Ņ–ĺ—Ā–ĺ–Ī–Ĺ—č—Ö –Ņ–ĺ–ī–į–≤–Ľ—Ź—ā—Ć –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā—č –Ņ–Ķ—Ä–Ķ–ļ–ł—Ā–Ĺ–ĺ–≥–ĺ –ĺ–ļ–ł—Ā–Ľ–Ķ–Ĺ–ł—Ź –Ľ–ł–Ņ–ł–ī–ĺ–≤, –Ĺ–ĺ—Ä–ľ–į–Ľ–ł–∑–ĺ–≤–į—ā—Ć –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā—č –≤–Ĺ—É—ā—Ä–ł–ļ–Ľ–Ķ—ā–ĺ—á–Ĺ–ĺ–≥–ĺ –ľ–Ķ—ā–į–Ī–ĺ–Ľ–ł–∑–ľ–į. –ü–ď–ü–Ē —Ā–ĺ—Ā—ā–į–≤–Ľ—Ź—é—ā —Ä–į–∑–Ĺ–ĺ—Ä–ĺ–ī–Ĺ—É—é –≥—Ä—É–Ņ–Ņ—É –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č—Ö –≤–Ķ—Č–Ķ—Ā—ā–≤ —Ā –ĺ–Ī—Č–ł–ľ —Ā–≤–ĺ–Ļ—Ā—ā–≤–ĺ–ľ –Ņ—Ä–Ķ–Ņ—Ź—ā—Ā—ā–≤–ĺ–≤–į—ā—Ć —Ä–į–∑—Ä—É—ą–Ķ–Ĺ–ł—é –ļ–Ľ–Ķ—ā–ĺ—á–Ĺ—č—Ö –ľ–Ķ–ľ–Ī—Ä–į–Ĺ –ł —Ā—ā–ł–ľ—É–Ľ–ł—Ä–ĺ–≤–į—ā—Ć —Ä–Ķ–≥–Ķ–Ĺ–Ķ—Ä–į—Ü–ł—é –≥–Ķ–Ņ–į—ā–ĺ—Ü–ł—ā–ĺ–≤ [11].
–Ě–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–ĺ –ĺ—ā–ľ–Ķ—ā–ł—ā—Ć, —á—ā–ĺ —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–į—Ü–ł–ł –Ī–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–į –ü–ď–ü–Ē –Ņ—Ä–ł –•–ó–ü —Ā—ā—Ä–ĺ—Ź—ā—Ā—Ź –Ĺ–į —ā–Ķ–ĺ—Ä–Ķ—ā–ł—á–Ķ—Ā–ļ–ĺ–ľ –ĺ–Ī–ĺ—Ā–Ĺ–ĺ–≤–į–Ĺ–ł–ł –ł—Ö —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –ł–Ľ–ł –Ĺ–į –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–ł —É—Ā—ā–į—Ä–Ķ–≤—ą–ł—Ö –ļ—Ä–ł—ā–Ķ—Ä–ł–Ķ–≤ –ī–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā–ł. –Ę–Ķ—Ä–ľ–ł–Ĺ ¬ę–ī–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ć–Ĺ–į—Ź –ľ–Ķ–ī–ł—Ü–ł–Ĺ–į¬Ľ –Ņ—Ä–Ķ–ī–Ņ–ĺ–Ľ–į–≥–į–Ķ—ā –Ņ–ĺ–ī—Ö–ĺ–ī –ļ –ľ–Ķ–ī–ł—Ü–ł–Ĺ—Ā–ļ–ĺ–Ļ –Ņ—Ä–į–ļ—ā–ł–ļ–Ķ, –Ņ—Ä–ł –ļ–ĺ—ā–ĺ—Ä–ĺ–ľ —Ä–Ķ—ą–Ķ–Ĺ–ł—Ź –ĺ –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–ł –ī–ł–į–≥–Ĺ–ĺ—Ā—ā–ł—á–Ķ—Ā–ļ–ł—Ö –ł –Ľ–Ķ—á–Ķ–Ī–Ĺ–ĺ-–Ņ—Ä–ĺ—Ą–ł–Ľ–į–ļ—ā–ł—á–Ķ—Ā–ļ–ł—Ö –ľ–Ķ—Ä–ĺ–Ņ—Ä–ł—Ź—ā–ł–Ļ –Ņ—Ä–ł–Ĺ–ł–ľ–į—é—ā—Ā—Ź –ł—Ā—Ö–ĺ–ī—Ź –ł–∑ –ł—Ö —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –ł –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł, –ī–ĺ–ļ–į–∑–į–Ĺ–Ĺ—č—Ö –≤ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł—Ö –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź—Ö.
–í –Ĺ–į—Ā—ā–ĺ—Ź—Č–Ķ–Ķ –≤—Ä–Ķ–ľ—Ź –ĺ–Ī—Č–Ķ–Ņ—Ä–ł–Ĺ—Ź—ā–ĺ–Ļ —Ā—Ö–Ķ–ľ—č –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –Ě–ź–Ė–Ď–ü –Ĺ–Ķ—ā. –ě—Ā–Ĺ–ĺ–≤–Ĺ–ĺ–Ķ –∑–Ĺ–į—á–Ķ–Ĺ–ł–Ķ –Ņ—Ä–ł–ī–į–Ķ—ā—Ā—Ź –ļ–ĺ—Ä—Ä–Ķ–ļ—Ü–ł–ł –ł–Ĺ—Ā—É–Ľ–ł–Ĺ–ĺ—Ä–Ķ–∑–ł—Ā—ā–Ķ–Ĺ—ā–Ĺ–ĺ—Ā—ā–ł, –ľ–Ķ—ā–į–Ī–ĺ–Ľ–ł–∑–ľ–į, –≤–ĺ—Ā–Ņ–į–Ľ–Ķ–Ĺ–ł—Ź, –į–Ņ–ĺ–Ņ—ā–ĺ–∑–į, —Ą–ł–Ī—Ä–ĺ–∑–į, –ļ–ł—ą–Ķ—á–Ĺ–ĺ–Ļ –ľ–ł–ļ—Ä–ĺ—Ą–Ľ–ĺ—Ä—č. –≠—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –ü–ď–ü–Ē —É –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –Ě–ź–Ė–Ď–ü –Ņ—Ä–ĺ–ī–ĺ–Ľ–∂–į–Ķ—ā –į–ļ—ā–ł–≤–Ĺ–ĺ –ł–∑—É—á–į—ā—Ć—Ā—Ź. –í–ľ–Ķ—Ā—ā–Ķ —Ā —ā–Ķ–ľ —Ā—É—Č–Ķ—Ā—ā–≤—É–Ķ—ā –ľ–Ĺ–Ķ–Ĺ–ł–Ķ, —á—ā–ĺ –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ —Ä–į–∑–Ľ–ł—á–Ĺ—č—Ö –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č—Ö —Ā—Ä–Ķ–ī—Ā—ā–≤, –≤ —ā. —á. –ü–ď–ü–Ē, –ĺ–≥—Ä–į–Ĺ–ł—á–Ķ–Ĺ–ĺ –Ņ–ĺ –Ņ—Ä–ł—á–ł–Ĺ–Ķ –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł—Ź –ī–į–Ĺ–Ĺ—č—Ö –ĺ–Ī –ł—Ö —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ņ—Ä–ł –Ě–ź–Ė–Ď–ü —Ā —É—á–Ķ—ā–ĺ–ľ –Ņ—Ä–ł–Ĺ—Ü–ł–Ņ–ĺ–≤ –ī–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ –ľ–Ķ–ī–ł—Ü–ł–Ĺ—č.
–ě–Ī—Č–Ķ–Ņ—Ä–ł–Ĺ—Ź—ā–ĺ–Ļ –ļ–Ľ–į—Ā—Ā–ł—Ą–ł–ļ–į—Ü–ł–ł –ü–ď–ü–Ē –Ĺ–Ķ —Ā—É—Č–Ķ—Ā—ā–≤—É–Ķ—ā. –í –Ņ—Ä–į–ļ—ā–ł–ļ–Ķ –ł—Ā–Ņ–ĺ–Ľ—Ć–∑—É—é—ā –ļ–Ľ–į—Ā—Ā–ł—Ą–ł–ļ–į—Ü–ł—é –Ņ–ĺ —Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ĺ–Ļ —Ā—ā—Ä—É–ļ—ā—É—Ä–Ķ, –Ņ—Ä–ĺ–ł—Ā—Ö–ĺ–∂–ī–Ķ–Ĺ–ł—é –ł –≤—č–ī–Ķ–Ľ—Ź—é—ā –Ĺ–Ķ—Ā–ļ–ĺ–Ľ—Ć–ļ–ĺ –≥—Ä—É–Ņ–Ņ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ —Ā —Ä–į–∑–Ĺ–ĺ–Ĺ–į–Ņ—Ä–į–≤–Ľ–Ķ–Ĺ–Ĺ—č–ľ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ–ľ –Ĺ–į –ľ–Ķ—ā–į–Ī–ĺ–Ľ–ł—á–Ķ—Ā–ļ–ł–Ķ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā—č. –Ě–į–ł–Ī–ĺ–Ľ–Ķ–Ķ –ł–∑—É—á–Ķ–Ĺ–Ĺ—č–ľ–ł —Ź–≤–Ľ—Ź—é—ā—Ā—Ź —Ą–Ľ–į–≤–ĺ–Ĺ–ĺ–ł–ī—č, –į–Ĺ—ā–ł–ĺ–ļ—Ā–ł–ī–į–Ĺ—ā—č, –Ņ—Ä–ĺ–ł–∑–≤–ĺ–ī–Ĺ—č–Ķ —É—Ä—Ā–ĺ–ī–Ķ–∑–ĺ–ļ—Ā–ł—Ö–ĺ–Ľ–Ķ–≤–ĺ–Ļ –ļ–ł—Ā–Ľ–ĺ—ā—č.
–í —Ā—ā—Ä—É–ļ—ā—É—Ä–Ķ –ü–ď–ü–Ē –≤—č–ī–Ķ–Ľ—Ź–Ķ—ā—Ā—Ź –≥—Ä—É–Ņ–Ņ–į –ī–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –Ņ—Ä–ł–ľ–Ķ–Ĺ—Ź–Ķ–ľ—č—Ö –≤ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ņ—Ä–į–ļ—ā–ł–ļ–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –į–Ĺ—ā–ł–ĺ–ļ—Ā–ł–ī–į–Ĺ—ā–Ĺ–ĺ–≥–ĺ –ī–Ķ–Ļ—Ā—ā–≤–ł—Ź, –ĺ–ī–ł–Ĺ –ł–∑ –ļ–ĺ—ā–ĺ—Ä—č—Ö ‚Äď –ľ–ĺ—Ä—Ą–ĺ–Ľ–ł–Ĺ–ł–Ļ-–ľ–Ķ—ā–ł–Ľ-—ā—Ä–ł–į–∑–ĺ–Ľ–ł–Ľ-—ā–ł–ĺ–į—Ü–Ķ—ā–į—ā (–Ę–ł–ĺ—ā—Ä–ł–į–∑–ĺ–Ľ–ł–Ĺ). –Ę–ł–ĺ—ā—Ä–ł–į–∑–ĺ–Ľ–ł–Ĺ —Ā–Ņ–ĺ—Ā–ĺ–Ī–Ķ–Ĺ –ł–Ĺ–≥–ł–Ī–ł—Ä–ĺ–≤–į—ā—Ć –į–ļ—ā–ł–≤–Ĺ—č–Ķ –ĺ–ļ–ł—Ā–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ-–≤–ĺ—Ā—Ā—ā–į–Ĺ–ĺ–≤–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ķ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā—č –≤ –ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–Ķ, –≤—č–∑—č–≤–į—é—Č–ł–Ķ –ĺ–ļ–ł—Ā–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ —Ā—ā—Ä–Ķ—Ā—Ā. –Ē–į–Ĺ–Ĺ–ĺ–Ķ —Ā–≤–ĺ–Ļ—Ā—ā–≤–ĺ –ĺ–Ī—É—Ā–Ľ–ĺ–≤–Ľ–Ķ–Ĺ–ĺ –Ĺ–į–Ľ–ł—á–ł–Ķ–ľ –≤ –Ķ–≥–ĺ –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ–Ķ —ā–ł–ĺ–Ľ—Ć–Ĺ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ—č, –ļ–ĺ—ā–ĺ—Ä–į—Ź –Ņ–ĺ –ĺ–ļ–ł—Ā–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ-–≤–ĺ—Ā—Ā—ā–į–Ĺ–ĺ–≤–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–ľ—É –Ņ–ĺ—ā–Ķ–Ĺ—Ü–ł–į–Ľ—É –Ī–Ľ–ł–∑–ļ–į –ļ —ā–ł–ĺ–Ľ—Ć–Ĺ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ–Ķ –≤ —Ü–ł—Ā—ā–Ķ–ł–Ĺ–ĺ–≤–ĺ–Ļ –ł —ā–ł–ĺ—ć—Ą–ł—Ä–Ĺ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ–ł—Ä–ĺ–≤–ļ–į—Ö, –≤—Ö–ĺ–ī—Ź—Č–ł—Ö –≤ —Ā–ĺ—Ā—ā–į–≤ –Ī–Ķ–Ľ–ļ–ĺ–≤—č—Ö –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ –ļ–Ľ–Ķ—ā–ĺ—á–Ĺ–ĺ–Ļ –ľ–Ķ–ľ–Ī—Ä–į–Ĺ—č, –ĺ—Ä–≥–į–Ĺ–Ķ–Ľ–Ľ –ł —Ź–ī—Ä–į. –í —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–Ķ —É–ľ–Ķ–Ĺ—Ć—ą–į–Ķ—ā—Ā—Ź –≤–Ľ–ł—Ź–Ĺ–ł–Ķ –Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ĺ—č—Ö –ĺ–ļ–ł—Ā–Ľ–ł—ā–Ķ–Ľ–Ķ–Ļ ‚Äď —Ā—É–Ņ–Ķ—Ä–ĺ–ļ—Ā–ł–ī–į –ł –Ņ–Ķ—Ä–ĺ–ļ—Ā–ł–Ĺ–ł—ā—Ä–ł—ā–į, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –≤—č–∑—č–≤–į—é—ā –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā—č –ī–Ķ—Ā—ā—Ä—É–ļ—Ü–ł–ł –Ī–Ķ–Ľ–ļ–ĺ–≤ –ļ–Ľ–Ķ—ā–ļ–ł (–ĺ–ļ–ł—Ā–Ľ–Ķ–Ĺ–ł–Ķ –ł –ī–Ķ–Ĺ–į—ā—É—Ä–į—Ü–ł—é). –ü–ĺ–ľ–ł–ľ–ĺ —ć—ā–ĺ–≥–ĺ, –Ę–ł–ĺ—ā—Ä–ł–į–∑–ĺ–Ľ–ł–Ĺ –ł–ľ–Ķ–Ķ—ā –≤ —Ā–≤–ĺ–Ķ–ľ —Ā–ĺ—Ā—ā–į–≤–Ķ —ā—Ä–Ķ—ā–ł—á–Ĺ—č–Ļ –į–∑–ĺ—ā, –Ņ—Ä–ł–ī–į—é—Č–ł–Ļ –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ–Ķ —Ā–Ņ–ĺ—Ā–ĺ–Ī–Ĺ–ĺ—Ā—ā—Ć —Ā–≤—Ź–∑—č–≤–į—ā—Ć –ł–∑–Ī—č—ā–ĺ–ļ –ł–ĺ–Ĺ–ĺ–≤ –≤–ĺ–ī–ĺ—Ä–ĺ–ī–į, —á—ā–ĺ –Ņ–ĺ–Ľ–ĺ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –≤–Ľ–ł—Ź–Ķ—ā –Ĺ–į –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā—č —ć–Ĺ–Ķ—Ä–≥–ĺ–ĺ–Ī—Ä–į–∑–ĺ–≤–į–Ĺ–ł—Ź –ł –Ņ—Ä–ĺ—ā–ł–≤–ĺ—Ā—ā–ĺ–ł—ā —Ä–į–∑–≤–ł—ā–ł—é –ļ–Ľ–Ķ—ā–ĺ—á–Ĺ–ĺ–≥–ĺ –į—Ü–ł–ī–ĺ–∑–į. –í —á–į—Ā—ā–Ĺ–ĺ—Ā—ā–ł, –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā —É—Ā–ł–Ľ–ł–≤–į–Ķ—ā –ļ–ĺ–ľ–Ņ–Ķ–Ĺ—Ā–į—ā–ĺ—Ä–Ĺ—É—é –į–ļ—ā–ł–≤–į—Ü–ł—é –į–Ĺ–į—ć—Ä–ĺ–Ī–Ĺ–ĺ–≥–ĺ –≥–Ľ–ł–ļ–ĺ–Ľ–ł–∑–į, —Ā–Ĺ–ł–∂–į–Ķ—ā —Ā—ā–Ķ–Ņ–Ķ–Ĺ—Ć —É–≥–Ĺ–Ķ—ā–Ķ–Ĺ–ł—Ź –ĺ–ļ–ł—Ā–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ –Ņ—Ä–ĺ–ī—É–ļ—Ü–ł–ł —ć–Ĺ–Ķ—Ä–≥–ł–ł –≤ —Ü–ł–ļ–Ľ–Ķ –ö—Ä–Ķ–Ī—Ā–į –ł –ī—č—Ö–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ —Ü–Ķ–Ņ–ł, —Ā–ĺ—Ö—Ä–į–Ĺ—Ź—Ź –Ņ—Ä–ł —ć—ā–ĺ–ľ –≤–Ĺ—É—ā—Ä–ł–ļ–Ľ–Ķ—ā–ĺ—á–Ĺ—č–Ļ —Ą–ĺ–Ĺ–ī –ź–Ę–§. –Ę–ł–ĺ—ā—Ä–ł–į–∑–ĺ–Ľ–ł–Ĺ –ĺ–Ī–Ľ–į–ī–į–Ķ—ā –≤–į–∂–Ĺ—č–ľ —Ā–≤–ĺ–Ļ—Ā—ā–≤–ĺ–ľ —Ā—ā–ł–ľ—É–Ľ–ł—Ä–ĺ–≤–į—ā—Ć –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā—č –į–ī–į–Ņ—ā–ł–≤–Ĺ–ĺ–≥–ĺ —Ā–ł–Ĺ—ā–Ķ–∑–į –Ī–Ķ–Ľ–ļ–ĺ–≤ –ł —Ä–ł–Ī–ĺ–Ĺ—É–ļ–Ľ–Ķ–ł–Ĺ–ĺ–≤–ĺ–Ļ –ļ–ł—Ā–Ľ–ĺ—ā—č, –į —ā–į–ļ–∂–Ķ –į–ļ—ā–ł–≤–ł—Ä–ĺ–≤–į—ā—Ć –į–Ĺ—ā–ł–ĺ–ļ—Ā–ł–ī–į–Ĺ—ā–Ĺ—É—é —Ā–ł—Ā—ā–Ķ–ľ—É —Ą–Ķ—Ä–ľ–Ķ–Ĺ—ā–ĺ–≤ –≤ —ā–ļ–į–Ĺ—Ź—Ö –Ņ–Ķ—á–Ķ–Ĺ–ł –ł —ā–ĺ—Ä–ľ–ĺ–∑–ł—ā—Ć –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā—č –Ņ–Ķ—Ä–Ķ–ļ–ł—Ā–Ĺ–ĺ–≥–ĺ –ĺ–ļ–ł—Ā–Ľ–Ķ–Ĺ–ł—Ź –Ľ–ł–Ņ–ł–ī–ĺ–≤. –Ď–Ľ–į–≥–ĺ–ī–į—Ä—Ź —É–ļ–į–∑–į–Ĺ–Ĺ—č–ľ –≤–Ľ–ł—Ź–Ĺ–ł—Ź–ľ –Ņ–ĺ–≤—č—ą–į–Ķ—ā—Ā—Ź –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –į–Ĺ—ā–ł–ĺ–ļ—Ā–ł–ī–į–Ĺ—ā–Ĺ—č—Ö —Ą–Ķ—Ä–ľ–Ķ–Ĺ—ā–ĺ–≤ –Ņ–Ķ—á–Ķ–Ĺ–ł (—Ā—É–Ņ–Ķ—Ä–ĺ–ļ—Ā–ł–ī–ī–ł—Ā–ľ—É—ā–į–∑—č, –ļ–į—ā–į–Ľ–į–∑—č, –≥–Ľ—É—ā–į—ā–ł–ĺ–Ĺ–Ņ–Ķ—Ä–ĺ–ļ—Ā–ł–ī–į–∑—č), –∑–į–ľ–Ķ–ī–Ľ—Ź—é—ā—Ā—Ź: —Ä–į—Ā—Ö–ĺ–ī —ć–Ĺ–ī–ĺ–≥–Ķ–Ĺ–Ĺ—č—Ö –į–Ĺ—ā–ł–ĺ–ļ—Ā–ł–ī–į–Ĺ—ā–ĺ–≤; –Ņ–Ķ—Ä–Ķ—Ö–ĺ–ī –ļ—Ā–į–Ĺ—ā–ł–Ĺ–ī–Ķ–≥–ł–ī—Ä–ĺ–≥–Ķ–Ĺ–į–∑—č –≤ –ļ—Ā–į–Ĺ—ā–ł–Ĺ–ĺ–ļ—Ā–ł–ī–į–∑—É; –ĺ—ā—ā–ĺ–ļ —ć–Ľ–Ķ–ļ—ā—Ä–ĺ–Ĺ–ĺ–≤ –≤ —ć–Ľ–Ķ–ļ—ā—Ä–ĺ–Ĺ–Ĺ–ĺ—ā—Ä–į–Ĺ—Ā–Ņ–ĺ—Ä—ā–Ĺ–ĺ–Ļ —Ü–Ķ–Ņ–ł –ľ–ł—ā–ĺ—Ö–ĺ–Ĺ–ī—Ä–ł–Ļ –ł —Ą–ĺ—Ä–ľ–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ —Ā—É–Ņ–Ķ—Ä–ĺ–ļ—Ā–ł–ī–Ĺ–ĺ–≥–ĺ –į–Ĺ–ł–ĺ–Ĺ–į. –ź–Ĺ—ā–ł–ĺ–ļ—Ā–ł–ī–į–Ĺ—ā–Ĺ–ĺ–Ķ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į –Ņ—Ä–ł–≤–ĺ–ī–ł—ā –ļ –ľ–Ķ–ľ–Ī—Ä–į–Ĺ–ĺ—Ā—ā–į–Ī–ł–Ľ–ł–∑–ł—Ä—É—é—Č–Ķ–ľ—É —ć—Ą—Ą–Ķ–ļ—ā—É, —ā. –Ķ. –ĺ—Ā—ā–į–Ĺ–į–≤–Ľ–ł–≤–į–Ķ—ā –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –ĺ—Ā–Ĺ–ĺ–≤–Ĺ—č—Ö —Ą–ł–∑–ł–ļ–ĺ-—Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ł—Ö —Ā–≤–ĺ–Ļ—Ā—ā–≤ –ļ–Ľ–Ķ—ā–ĺ—á–Ĺ—č—Ö –ľ–Ķ–ľ–Ī—Ä–į–Ĺ (–Ņ–Ľac—ā–ł—á–Ĺ–ĺ—Ā—ā—Ć, —ā–Ķ–ļ—É—á–Ķc—ā—Ć, –Ņ—Ä–ĺ–Ĺ–ł—Ü–į–Ķ–ľ–ĺc—ā—Ć, c–ĺ—Ö—Ä–į–Ĺ–Ķ–Ĺ–ł–Ķ —ā—Äa–Ĺc–ľ–Ķ–ľ–Ī—Ä–į–Ĺ–Ĺ–ĺ–≥–ĺ –Ņ–ĺ—ā–Ķ–Ĺ—Ü–ła–Ľa). –Ę–ł–ĺ—ā—Ä–ła–∑–ĺ–Ľ–ł–Ĺ –∑–į–Ņ—É—Ā–ļ–į–Ķ—ā –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā—č a–ļ—ā–ł–≤–į—Ü–ł–ł –Ľa–ļ—ā–į—ā–ī–Ķ–≥–ł–ī—Ä–ĺ–≥–Ķ–Ĺ–į–∑—č –ł –Ņ–ł—Ä—É–≤–į—ā–ļ–ł–Ĺa–∑—č –ł, –ļ–į–ļ —Ā–Ľ–Ķ–ī—Ā—ā–≤–ł–Ķ, a–Ĺ–į—ć—Ä–ĺ–Ī–Ĺ–ĺ–≥–ĺ –ł, –≤ –Īo–Ľ—Ć—ą–Ķ–Ļ c—ā–Ķ–Ņ–Ķ–Ĺ–ł, a—ć—Ä–ĺ–Ī–Ĺ–ĺ–≥–ĺ o–ļ–ł—Ā–Ľ–Ķ–Ĺ–ł—Ź –≥–Ľ—é–ļo–∑—č. –ü–ĺ—Ā–Ľ–Ķ–ī–Ĺ–Ķ–Ķ, –≤ —Ā–≤–ĺ—é –ĺ—á–Ķ—Ä–Ķ–ī—Ć, o–Ī—É—Ā–Ľ–ĺ–≤–Ľ–ł–≤–į–Ķ—ā –≤o—Ā—Ā—ā–į–Ĺ–ĺ–≤–Ľ–Ķ–Ĺ–ł–Ķ –Ņ—É–Ľa –ľa–ļ—Ä–ĺ—ć—Ä–≥–ĺ–≤ –īa–∂–Ķ –≤ —É—Ā–Ľo–≤–ł—Ź—Ö –≥–Ľ—É–Īo–ļ–ĺ–Ļ –≥–ł–Ņo–ļ—Ā–ł–ł –ł —Ā–Ĺ–ł–∂a–Ķ—ā —Ā—āe–Ņ–Ķ–Ĺ—Ć –Ľ–į–ļ—ā–į—ā–į—Ü–ł–ī–ĺ–∑–į –≤ –ļ–Ľe—ā–ļ–Ķ. –†e–∑—É–Ľ—Ć—ā–į—ā—č –Ĺ–Ķ–ļ–ĺ—ā–ĺ—Ä—č—Ö –ļ–Ľ–ł–Ĺ–ł—áe—Ā–ļ–ł—Ö –łcc–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ļ –Ņ–ĺ–ī—ā–≤e—Ä–ī–ł–Ľ–ł —ć—Ą—Ąe–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į –Ę–ł–ĺ—ā—Ä–ł–į–∑–ĺ–Ľ–ł–Ĺ –Ņ—Ä–ł –Ľ–Ķ—á–Ķ–Ĺ–ł–ł –•–ó–ü [12].
–í –ĺ—ā–ī–Ķ–Ľ–Ķ–Ĺ–ł–ł —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ –Ņ–Ķ—á–Ķ–Ĺ–ł –ú–ĺ—Ā–ļ–ĺ–≤—Ā–ļ–ĺ–≥–ĺ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –Ĺ–į—É—á–Ĺ–ĺ-–Ņ—Ä–į–ļ—ā–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —Ü–Ķ–Ĺ—ā—Ä–į –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ĺ—Ā—Ć –Ņ–ĺ—Ā—ā–ľ–į—Ä–ļ–Ķ—ā–ł–Ĺ–≥–ĺ–≤–ĺ–Ķ –ĺ—ā–ļ—Ä—č—ā–ĺ–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ ¬ę–ě—Ü–Ķ–Ĺ–ļ–į —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –ł –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į –Ę–ł–ĺ—ā—Ä–ł–į–∑–ĺ–Ľ–ł–Ĺ —É –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –Ĺ–Ķ–į–Ľ–ļ–ĺ–≥–ĺ–Ľ—Ć–Ĺ–ĺ–Ļ –∂–ł—Ä–ĺ–≤–ĺ–Ļ –Ī–ĺ–Ľ–Ķ–∑–Ĺ—Ć—é –Ņ–Ķ—á–Ķ–Ĺ–ł¬Ľ.
–¶–Ķ–Ľ—Ć –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź: –ĺ—Ü–Ķ–Ĺ–ļ–į —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –Ę–ł–ĺ—ā—Ä–ł–į–∑–ĺ–Ľ–ł–Ĺ–į —É –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –Ě–ź–Ė–Ď–ü.
–ú–į—ā–Ķ—Ä–ł–į–Ľ –ł –ľ–Ķ—ā–ĺ–ī—č
–í –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –ļ–Ľ—é—á–Ķ–Ĺ–ĺ 30 —á–Ķ–Ľ–ĺ–≤–Ķ–ļ: 18 (60%) –∂–Ķ–Ĺ—Č–ł–Ĺ –ł 12 –ľ—É–∂—á–ł–Ĺ (40%). –°—Ä–Ķ–ī–Ĺ–ł–Ļ –≤–ĺ–∑—Ä–į—Ā—ā –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –≤ –ĺ—Ā–Ĺ–ĺ–≤–Ĺ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ–Ķ —Ā–ĺ—Ā—ā–į–≤–ł–Ľ (56,2¬Ī7,7 –≥–ĺ–ī–į) (—Ä>0,05). –í—Ā–Ķ –Ī–ĺ–Ľ—Ć–Ĺ—č–Ķ –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ—č –Ņ–ĺ –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ–Ķ–Ĺ–Ĺ–ĺ–ľ—É –Ĺ–ł–∂–Ķ –į–Ľ–≥–ĺ—Ä–ł—ā–ľ—É.1. –õ–į–Ī–ĺ—Ä–į—ā–ĺ—Ä–Ĺ—č–Ķ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–ł.
1.1. –Ď–ł–ĺ—Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ł–Ļ –į–Ĺ–į–Ľ–ł–∑ –ļ—Ä–ĺ–≤–ł (–ľ–į—Ä–ļ–Ķ—Ä—č —Ü–ł—ā–ĺ–Ľ–ł—ā–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ, —Ö–ĺ–Ľ–Ķ—Ā—ā–į—ā–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–į, –≥–Ķ–Ņ–į—ā–ĺ–ī–Ķ–Ņ—Ä–Ķ—Ā—Ā–ł–ł, –ł–ľ–ľ—É–Ĺ–Ĺ–ĺ–≥–ĺ –≤–ĺ—Ā–Ņ–į–Ľ–Ķ–Ĺ–ł—Ź).
1.2. –ě—Ü–Ķ–Ĺ–ļ–į –Ľ–ł–Ņ–ł–ī–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ĺ—Ą–ł–Ľ—Ź.
2. –ė–Ĺ—Ā—ā—Ä—É–ľ–Ķ–Ĺ—ā–į–Ľ—Ć–Ĺ—č–Ķ –ľ–Ķ—ā–ĺ–ī—č.
2.1. –£–ó–ė –Ī—Ä—é—ą–Ĺ–ĺ–Ļ –Ņ–ĺ–Ľ–ĺ—Ā—ā–ł.
2.2. –§–ł–Ī—Ä–ĺ—ć–Ľ–į—Ā—ā–ĺ–ľ–Ķ—ā—Ä–ł—Ź –Ņ–Ķ—á–Ķ–Ĺ–ł.
3. –Ē–ł—Ą—Ą–Ķ—Ä–Ķ–Ĺ—Ü–ł–į–Ľ—Ć–Ĺ–į—Ź –ī–ł–į–≥–Ĺ–ĺ—Ā—ā–ł–ļ–į (–ł—Ā–ļ–Ľ—é—á–Ķ–Ĺ–ł–Ķ –į–Ľ–ļ–ĺ–≥–ĺ–Ľ—Ć–Ĺ–ĺ–Ļ –Ī–ĺ–Ľ–Ķ–∑–Ĺ–ł –Ņ–Ķ—á–Ķ–Ĺ–ł, –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ-–ł–Ĺ–ī—É—Ü–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö –≥–Ķ–Ņ–į—ā–ł—ā–ĺ–≤, –•–ď–°, –•–ď–í, –į—É—ā–ĺ–ł–ľ–ľ—É–Ĺ–Ĺ—č—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ, –≥–Ķ–ľ–ĺ—Ö—Ä–ĺ–ľ–į—ā–ĺ–∑–į, –Ī–ĺ–Ľ–Ķ–∑–Ĺ–ł –í–ł–Ľ—Ć—Ā–ĺ–Ĺ–į ‚Äď –ö–ĺ–Ĺ–ĺ–≤–į–Ľ–ĺ–≤–į).
–Ď–ł–ĺ—Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ł–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ł—Ā—Ć –Ĺ–į –į–≤—ā–ĺ–ľ–į—ā–ł—á–Ķ—Ā–ļ–ĺ–ľ –į–Ĺ–į–Ľ–ł–∑–į—ā–ĺ—Ä–Ķ ¬ęAU 400¬Ľ —Ą–ł—Ä–ľ—č Olimpus. –£ 10 –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –ī–ł–į–≥–Ĺ–ĺ–∑ –Ņ–ĺ–ī—ā–≤–Ķ—Ä–∂–ī–Ķ–Ĺ –ľ–ĺ—Ä—Ą–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł. –Ē–Ľ—Ź –ł—Ā–ļ–Ľ—é—á–Ķ–Ĺ–ł—Ź –Ĺ–į–Ľ–ł—á–ł—Ź –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ –Ņ–Ķ—á–Ķ–Ĺ–ł –ī—Ä—É–≥–ĺ–Ļ —ć—ā–ł–ĺ–Ľ–ĺ–≥–ł–ł –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ĺ—Ā—Ć –ł–ľ–ľ—É–Ĺ–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ĺ–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ —Ā–Ņ–Ķ—Ü–ł—Ą–ł—á–Ķ—Ā–ļ–ł—Ö –į–Ĺ—ā–ł–≥–Ķ–Ĺ–ĺ–≤ –ł –į–Ĺ—ā–ł—ā–Ķ–Ľ (HBsAg, aH–°V, –ź–ú–ź –ú2, ANA). –Ē–Ľ—Ź –ł—Ā–ļ–Ľ—é—á–Ķ–Ĺ–ł—Ź –į–Ľ–ļ–ĺ–≥–ĺ–Ľ—Ć–Ĺ—č—Ö –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–Ļ –Ņ–Ķ—á–Ķ–Ĺ–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ—Ź–Ľ–ł—Ā—Ć –ĺ–Ņ—Ä–ĺ—Ā–Ĺ–ł–ļ–ł –°–źGE –ł AUDIT-C. –Ē–Ľ—Ź –ł—Ā–ļ–Ľ—é—á–Ķ–Ĺ–ł—Ź –Ī–ĺ–Ľ–Ķ–∑–Ĺ–ł –í–ł–Ľ—Ć—Ā–ĺ–Ĺ–į ‚Äď –ö–ĺ–Ĺ–ĺ–≤–į–Ľ–ĺ–≤–į, –≥–Ķ–ľ–ĺ—Ö—Ä–ĺ–ľ–į—ā–ĺ–∑–į –≤—Ā–Ķ–ľ –Ī–ĺ–Ľ—Ć–Ĺ—č–ľ –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ł –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ —É—Ä–ĺ–≤–Ĺ—Ź —Ü–Ķ—Ä—É–Ľ–ĺ–Ņ–Ľ–į–∑–ľ–ł–Ĺ–į, —Ą–Ķ—Ä—Ä–ł—ā–ł–Ĺ–į, —Ā–ĺ–ī–Ķ—Ä–∂–į–Ĺ–ł—Ź –ľ–Ķ–ī–ł –≤ —Ā—É—ā–ĺ—á–Ĺ–ĺ–Ļ –ľ–ĺ—á–Ķ.
–ü—Ä–Ķ–Ņ–į—Ä–į—ā –Ę–ł–ĺ—ā—Ä–ł–į–∑–ĺ–Ľ–ł–Ĺ –Ĺ–į–∑–Ĺ–į—á–į–Ľ—Ā—Ź –≤ 2 —ć—ā–į–Ņ–į:
1) –≤/–≤ –ļ–į–Ņ–Ķ–Ľ—Ć–Ĺ–ĺ –≤ –ī–ĺ–∑–ł—Ä–ĺ–≤–ļ–Ķ 100 –ľ–≥ (4 –ľ–Ľ), –ļ—É—Ä—Ā 5 –ī–Ĺ–Ķ–Ļ;
2) –≤ —ā–į–Ī–Ľ–Ķ—ā–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–Ļ —Ą–ĺ—Ä–ľ–Ķ –≤–Ĺ—É—ā—Ä—Ć –Ņ–ĺ 2 —ā–į–Ī–Ľ–Ķ—ā–ļ–ł (0,1 –≥) 3 —Ä–į–∑–į –≤ –ī–Ķ–Ĺ—Ć, –ļ—É—Ä—Ā 14 –ī–Ĺ–Ķ–Ļ.
–°—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–į—Ź –ĺ–Ī—Ä–į–Ī–ĺ—ā–ļ–į –ī–į–Ĺ–Ĺ—č—Ö –≤—č–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ–į –Ĺ–į –ł–Ĺ–ī–ł–≤–ł–ī—É–į–Ľ—Ć–Ĺ–ĺ–ľ –ļ–ĺ–ľ–Ņ—Ć—é—ā–Ķ—Ä–Ķ —Ā –Ņ–ĺ–ľ–ĺ—Č—Ć—é —ć–Ľ–Ķ–ļ—ā—Ä–ĺ–Ĺ–Ĺ—č—Ö —ā–į–Ī–Ľ–ł—Ü Microsoft Excel –ł –Ņ–į–ļ–Ķ—ā–į –Ņ—Ä–ł–ļ–Ľ–į–ī–Ĺ—č—Ö –Ņ—Ä–ĺ–≥—Ä–į–ľ–ľ Statistica for Windows v. 7.0, StatSoft Inc. (–°–®–ź). –Ē–Ľ—Ź —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—Ź —á–ł—Ā–Ľ–ĺ–≤—č—Ö –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–Ķ–Ļ, –ł–∑–ľ–Ķ–Ĺ—Ź—é—Č–ł—Ö—Ā—Ź –≤ –ī–ł–Ĺ–į–ľ–ł–ļ–Ķ –ī–ĺ –ł –Ņ–ĺ—Ā–Ľ–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź, –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ľ–ł t-–ļ—Ä–ł—ā–Ķ—Ä–ł–Ļ –°—ā—Ć—é–ī–Ķ–Ĺ—ā–į –ī–Ľ—Ź –∑–į–≤–ł—Ā–ł–ľ—č—Ö –≤—č–Ī–ĺ—Ä–ĺ–ļ –ł –ļ—Ä–ł—ā–Ķ—Ä–ł–Ļ –£–ł–Ľ–ļ–ĺ–ļ—Ā–ĺ–Ĺ–į.
–†–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –ł –ł—Ö –ĺ–Ī—Ā—É–∂–ī–Ķ–Ĺ–ł–Ķ
–ě–Ī—Č–į—Ź —Ö–į—Ä–į–ļ—ā–Ķ—Ä–ł—Ā—ā–ł–ļ–į –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ–Ķ–Ĺ–į –≤ —ā–į–Ī–Ľ–ł—Ü–Ķ 1.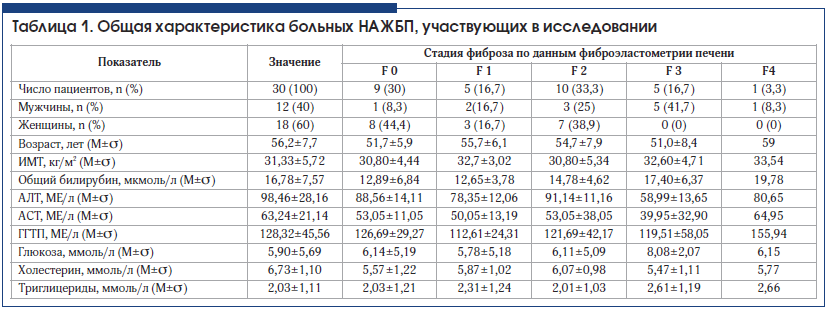
–í —ā–į–Ī–Ľ–ł—Ü–Ķ 2 –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ–Ķ–Ĺ–į –≤ –ī–ł–Ĺ–į–ľ–ł–ļ–Ķ –≤—č—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ—Ā—ā—Ć —Ā–ĺ–Ņ—É—ā—Ā—ā–≤—É—é—Č–ł—Ö —Ā–ĺ—Ā—ā–ĺ—Ź–Ĺ–ł–Ļ ‚Äď —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł—Ź –Ĺ–į—Ā—ā—Ä–ĺ–Ķ–Ĺ–ł—Ź, –į—Ā—ā–Ķ–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–į (–ĺ–Ī—Č–į—Ź —Ā–Ľ–į–Ī–ĺ—Ā—ā—Ć), –ī–ł—Ā–Ņ–Ķ–Ņ—Ā–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–į (—á—É–≤—Ā—ā–≤–ĺ —ā—Ź–∂–Ķ—Ā—ā–ł –≤ –Ņ—Ä–į–≤–ĺ–ľ –Ņ–ĺ–ī—Ä–Ķ–Ī–Ķ—Ä—Ć–Ķ, –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł–Ķ –į–Ņ–Ņ–Ķ—ā–ł—ā–į) –Ĺ–į —Ą–ĺ–Ĺ–Ķ —ā–Ķ—Ä–į–Ņ–ł–ł. –ü–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–ł –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–ł—Ā—Ć –≤ –Ī–į–Ľ–Ľ–į—Ö –Ņ–ĺ —Ā–Ľ–Ķ–ī—É—é—Č–Ķ–Ļ —ą–ļ–į–Ľ–Ķ: 0 –Ī–į–Ľ–Ľ–ĺ–≤ ‚Äď –∂–į–Ľ–ĺ–Ī—č –ĺ—ā—Ā—É—ā—Ā—ā–≤—É—é—ā; 1 –Ī–į–Ľ–Ľ ‚Äď –∂–į–Ľ–ĺ–Ī—č —Ā–Ľ–į–Ī–ĺ –≤—č—Ä–į–∂–Ķ–Ĺ—č; 2 –Ī–į–Ľ–Ľ–į ‚Äď —É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ–ĺ –≤—č—Ä–į–∂–Ķ–Ĺ—č; 3 –Ī–į–Ľ–Ľ–į ‚Äď —Ä–Ķ–∑–ļ–ĺ –≤—č—Ä–į–∂–Ķ–Ĺ—č.
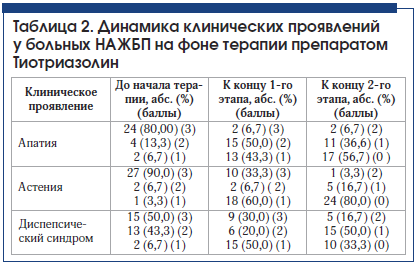
–ö –ĺ–ļ–ĺ–Ĺ—á–į–Ĺ–ł—é 1-–≥–ĺ —ć—ā–į–Ņ–į –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–ľ –Ę–ł–ĺ—ā—Ä–ł–į–∑–ĺ–Ľ–ł–Ĺ –ĺ—Ā–ĺ–Ī–Ķ–Ĺ–Ĺ–ĺ –ĺ—ā—á–Ķ—ā–Ľ–ł–≤–ĺ –Ņ—Ä–ĺ—Ā–Ľ–Ķ–∂–ł–≤–į–Ľ–ĺ—Ā—Ć —É–ľ–Ķ–Ĺ—Ć—ą–Ķ–Ĺ–ł–Ķ –Ņ—Ä–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł–Ļ –į—Ā—ā–Ķ–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–į, –ļ –ĺ–ļ–ĺ–Ĺ—á–į–Ĺ–ł—é 2-–≥–ĺ —ć—ā–į–Ņ–į –Ņ–ĺ—á—ā–ł –≤—Ā–Ķ –Ī–ĺ–Ľ—Ć–Ĺ—č–Ķ –ĺ—ā–ľ–Ķ—ā–ł–Ľ–ł —É–Ľ—É—á—ą–Ķ–Ĺ–ł–Ķ —Ā–į–ľ–ĺ—á—É–≤—Ā—ā–≤–ł—Ź ‚Äď –ł—Ā—á–Ķ–∑–Ĺ–ĺ–≤–Ķ–Ĺ–ł–Ķ –ł–Ľ–ł –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ —É–ľ–Ķ–Ĺ—Ć—ą–Ķ–Ĺ–ł–Ķ –į—Ā—ā–Ķ–Ĺ–ł–ł, —É–Ľ—É—á—ą–Ķ–Ĺ–ł–Ķ –Ĺ–į—Ā—ā—Ä–ĺ–Ķ–Ĺ–ł—Ź.
–í —ā–į–Ī–Ľ–ł—Ü–Ķ 3 –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ–Ķ–Ĺ–ĺ —Ä–į—Ā–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł–Ķ –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –Ě–ź–Ė–Ď–ü –≤ –∑–į–≤–ł—Ā–ł–ľ–ĺ—Ā—ā–ł –ĺ—ā –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł —Ü–ł—ā–ĺ–Ľ–ł–∑–į: –ľ–ł–Ĺ–ł–ľ–į–Ľ—Ć–Ĺ–į—Ź –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć ‚Äď –Ņ—Ä–ł –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –ź–õ–Ę –ī–ĺ 1,5 –Ĺ–ĺ—Ä–ľ—č; —É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ–į—Ź ‚Äď –ī–ĺ 3-—Ö –Ĺ–ĺ—Ä–ľ; –≤—č—Ā–ĺ–ļ–į—Ź ‚Äď 3‚Äď5 –Ĺ–ĺ—Ä–ľ.
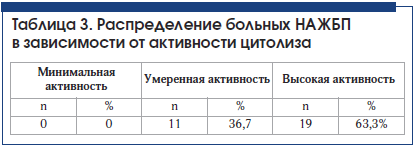
–í—Ā–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č –ł–ľ–Ķ–Ľ–ł –Ě–ź–Ė–Ď–ü –Ĺ–į —Ā—ā–į–ī–ł–ł —Ā—ā–Ķ–į—ā–ĺ–≥–Ķ–Ņ–į—ā–ł—ā–į, —É –Ī–ĺ–Ľ—Ć—ą–Ķ–Ļ —á–į—Ā—ā–ł –ł–∑ –Ĺ–ł—Ö –Ĺ–į–Ī–Ľ—é–ī–į–Ľ—Ā—Ź –Ě–ź–°–ď —Ā –≤—č—Ā–ĺ–ļ–ĺ–Ļ –Ī–ł–ĺ—Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć—é. –Ē–ł–Ĺ–į–ľ–ł–ļ–į —Ü–ł—ā–ĺ–Ľ–ł—ā–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–į –ł –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–Ķ–Ļ –Ľ–ł–Ņ–ł–ī–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ĺ—Ą–ł–Ľ—Ź —É –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –Ĺ–į —Ą–ĺ–Ĺ–Ķ —ā–Ķ—Ä–į–Ņ–ł–ł –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–ľ –Ę–ł–ĺ—ā—Ä–ł–į–∑–ĺ–Ľ–ł–Ĺ –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ–Ķ–Ĺ–į –≤ —ā–į–Ī–Ľ–ł—Ü–Ķ 4.
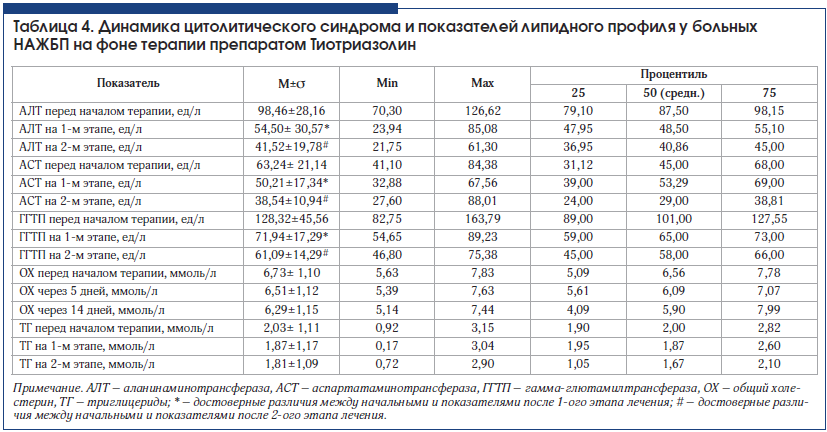
–Ě–į —Ą–ĺ–Ĺ–Ķ —ā–Ķ—Ä–į–Ņ–ł–ł –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–ľ –Ę–ł–ĺ—ā—Ä–ł–į–∑–ĺ–Ľ–ł–Ĺ –ĺ—ā–ľ–Ķ—á–į–Ķ—ā—Ā—Ź –∑–Ĺ–į—á–ł–ľ–ĺ–Ķ —É–Ľ—É—á—ą–Ķ–Ĺ–ł–Ķ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–Ķ–Ļ –Ņ–Ķ—á–Ķ–Ĺ–ĺ—á–Ĺ—č—Ö —Ą–Ķ—Ä–ľ–Ķ–Ĺ—ā–ĺ–≤ –ł —Ü–ł—ā–ĺ–Ľ–ł–∑–į –Ņ–ĺ—Ā–Ľ–Ķ 1-–≥–ĺ —ć—ā–į–Ņ–į –ł –Ņ–ĺ—á—ā–ł –Ņ–ĺ–Ľ–Ĺ–į—Ź –Ĺ–ĺ—Ä–ľ–į–Ľ–ł–∑–į—Ü–ł—Ź –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–Ķ–Ļ –ļ –ļ–ĺ–Ĺ—Ü—É 2-–≥–ĺ —ć—ā–į–Ņ–į. –õ–ł–Ņ–ł–ī–Ĺ—č–Ļ –Ņ—Ä–ĺ—Ą–ł–Ľ—Ć, –ļ–ĺ—ā–ĺ—Ä—č–Ļ –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ–Ķ–Ĺ –ě–• –ł –Ę–ď, –ł–ľ–Ķ–Ķ—ā —ā–Ķ–Ĺ–ī–Ķ–Ĺ—Ü–ł—é –ļ —É–Ľ—É—á—ą–Ķ–Ĺ–ł—é –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–Ķ–Ļ –ļ –ļ–ĺ–Ĺ—Ü—É —ā–Ķ—Ä–į–Ņ–ł–ł.












