Материалы и методы
Для выявления нарушений в регуляции ПЖ у больных ХП использовали стандартный завтрак как секреторный стимулятор и определяли изменения уровня нейромедиаторов до и после него.
Обследовано 65 больных ХП (40 мужчин, 25 женщин) в возрасте от 30 до 60 лет, из них 45 – больные алкогольным панкреатитом (АП) и 20 – билиарным панкреатитом (БП). Группу контроля составили 15 человек без заболеваний желудочно–кишечного тракта.
Для определения ацетилхолина (Ах), холинэстеразы (ХЭ) в сыворотке крови использовали химический метод определения ацетилхолина и других производных карбоксиловой кислоты, предложенный Sh. Hestrin в модификации Бассалык [5–7]. Определение содержания серотонина (5–НТ) в крови и ткани проводилось Ch. Sadovanqvivad [4]. ХЦК и секретин исследовали в крови с помощью стандартных наборов реактивов иммуноферментным методом. Для стимуляции секреции гастроинтестинальных гормонов и Ах, 5–НТ использовали стандартный завтрак, включающий не протертый вариант диеты 5п [8].
Результаты
Установлено, что в контрольной группе уровень 5–НТ был 0,19±0,02 мкг/мл, Ах – 0,8±0,09 ммоль/мл и ХЭ–активность – 0,9±0,09 ммоль/мл 30 мин.
В сыворотке крови больных АП выявлено повышение содержания 5–НТ – 0,40±0,07 мкг/мл (р<0,01) и Aх – 1,7±0,3 ммоль/мл (p<0,05), снижение ХЭ–активности – 0,15±0,01 ммоль/мл 30 мин. (р<0,01). При БП: 5–НТ – 0,28±0,04 мкг/мл (р<0,05) и Aх – 1,5±0,12 ммоль/мл (p<0,05), ХЭ–активность – 0,4 ммоль/мл 30 мин. (р<0,05).
В группе контроля наблюдалась тенденция к повышению 5–НТ с 0,19±0,02 до 0,23±0,019 мкг/мл (р>0,05) после завтрака. Достоверно возрастал уровень Ах с 0,8±0,06 до 1,0±0,05 ммоль/л (р<0,05). Данное увеличение Ах осуществлялось за счет снижения ХЭ–активности с 0,9±0,1 до 0,5±0,04 ммоль/л 30 мин. (p<0,01). У больных АП изменялась реакция биологически активных веществ на стандартный завтрак: концентрация 5–HT повышалась с 0,40±0,07 до 0,55±0,05 мкг/мл (p<0,05), а Ах снижался с 1,7±0,3 до 1,6±0,3 ммоль/л (р>0,05). ХЭ–активность низкая как до, так и после стандартного завтрака (0,15±0,01 и 0,2±0,01 ммоль/л 30 мин. соответственно). Исходный высокий уровень Ах при ХП не предполагает дополнительного повышения его после пищевой стимуляции. У больных БП на стандартный завтрак: концентрация 5–HT повышалась с 0,28±0,04 до 0,43±0,05 мкг/мл (p<0,05), Ах достоверно не менялся – 1,5±0,12 ммоль/мл и 1,45 ±0,21 ммоль/л (р>0,05). ХЭ–активность после стандартного завтрака снижалась с 0,4 ммоль/мл 30 мин. до 0,3±0,05 ммоль/мл 30 мин.
Таким образом, установлено, что у больных ХП повышено содержание ацетилхолина натощак, а после стимуляции он снижался. Основные изменения касались серотонина, у больных ХП он был повышен как натощак, так и после стандартного завтрака. У здоровых лиц после завтрака имеет место тенденция к увеличению 5–НТ в крови (р>0,05) и достоверное повышение Ах (р<0,05).
У больных ХП после завтрака наблюдается тенденция к снижению Ах (р>0,05) в сравнении с высоким исходным уровнем и достоверное повышение 5–НТ (р<0,05). Эти нарушения были более выраженными у больных, имеющих в анамнезе панкреонекроз и осложненное течение заболевания. Наличие ХП меняет «схему» регуляторных взаимоотношений. Можно предполагать, что в данном случае снижается роль парасимпатического отдела вегетативной нервной системы на внешнее воздействие – пищевую нагрузку.
Однофакторный корреляционный анализ показал, что внутри исследуемого ряда данных по 5–НТ и Ах существует сильная связь (R2=0,8802; R2=0,9143 – Ах до и после еды у здоровых; R2=0,860; R2=0,9301 – 5–НТ до и после еды у здоровых; R2=0,9091– серотонин до еды при панкреатите; R2=0,4692 – 5–НТ после еды при панкреатите; R2=0,9277 – Ах до еды при панкреатите; R2=0,6914 – Ах после еды при панкреатите; R2=0,9377 – до еды ХЭ у здоровых; R²=0,6764 – после еды, ХЭ у здоровых; R2=0,5705 – ХЭ до еды при панкреатите; R2=0,9573 – ХЭ после еды при панкреатите).
В группе больных панкреатитом уровень ХЭ–активности снижен до и после пищевой нагрузки. До пищевой нагрузки присутствует сильная связь внутри ряда данных, а после связь внутри исследуемого ряда ослабевает. Снижено разрушение Ах, и после пищевой нагрузки нет необходимости в его дополнительном выбросе. У больных формируются новые функционально–регуляторные механизмы (возможно, в результате постепенного увеличения соединительной ткани в ПЖ), которые достоверно проявляются после пищевой нагрузки. Здоровые и больные ХП реагируют высвобождением биологически активных веществ на пищевую нагрузку по–разному, создается новая, еще не устойчивая (R2=0,6822; R2=0,6914; R2=0,5705) схема регуляции секреторной активности ПЖ, но она уже существует.
Таким образом, в зависимости от тяжести деструктивных изменений в ПЖ у больных АП и БП выявлена различная степень экзокринной недостаточности, которая может быть обусловлена отсутствием повышения концентрации Ах в крови после приема пищи.
В контроле имеется незначительное повышение 5–НТ, которое обеспечивает секрецию пищеварительных ферментов, желудочного и панкреатического сока, вызывая «физиологическое» воспаление слизистой оболочки гастродуоденальной зоны. У больных ХП содержание 5–НТ возрастает вдвое, несмотря на то, что исходный уровень 5–НТ у больных высокий.
Источник такого значительного повышения 5–НТ не совсем ясен. Поэтому у больных ХП алкогольной этиологии в слизистой оболочке желудка и ДПК провели определение 5–НТ в ткани, учитывая, что 5–НТ синтезируется в клетках энтерохромаффин–серотониновой системы, являющейся частью APUD–системы, диффузной нейроэндокринной железы слизистой оболочки желудочно–кишечного тракта [1].
У больных ХП в слизистой оболочке ДПК было выявлено повышение содержания 5–НТ до 6,9±0,54 мкг/г ткани, контроль – 5,2±0,43мкг/г ткани (р<0,05). Таким образом, источником повышенного содержания в крови 5–НТ кроме высвобождения его из нервных окончаний является слизистая оболочка ДПК.
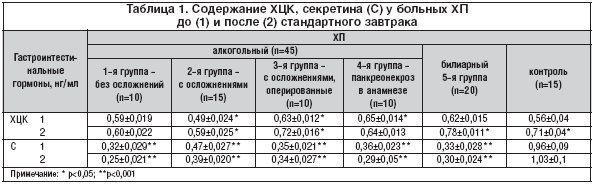
Данные содержания ХЦК и секретина у больных ХП приведены в таблице 1. ХЦК после стандартного завтрака достоверно повышался в группах больных АП с осложнениями и после хирургического лечения ХП при БП, т.е. в группах больных со сниженной внешнесекреторной функцией ПЖ (Е–1 кала ниже 100 мкг/г). В остальных группах только тенденция к его повышению, как и в контрольной группе. У больных АП и БП выявлена высокая корреляционная связь между содержанием 5–НТ и ХЦК – r=0,875439 и слабая отрицательная корреляционная связь с Ах – r=–0,2209
Секреция секретина у больных АП и БП была достоверно снижена (р<0,001). После стандартного завтрака у больных АП и БП уровень секретина снижался, в контроле он повышался (табл. 1). Секретин имел слабую корреляционную связь как с 5–НТ (r= –0,4839), так и с Ах (r=–0,33207). Снижение секреции секретина обусловливает снижение секреции бикарбонатов и слизи.
В нашем исследовании (табл. 1) уровень ХЦК натощак достоверно выше в группах 3 и 4 (113 и 161%) и ниже в группе 2 (88%) в сравнении с контрольной группой (р<0,05). Отмечена тенденция к повышению в группе 1 (105%). После стандартного завтрака содержание ХЦК в контрольной группе повышалось на 127% (р<0,05), группах 2 и 3 достоверно возрастало на 120 и 114% (р<0,05) в сравнении с уровнем ХЦК натощак. В группе 1 – возрастало на 102%, а в группе 4 снижалось до 98%. Во всех группах кроме 3–й (101%) стимулированный уровень ХЦК ниже уровня ХЦК в контрольной группе исследуемых (85, 83, 90% соответственно). Выявленные особенности содержания ХЦК в сыворотке крови до и после пищевой стимуляции косвенно указывают на нарушение в системе регуляции секреции и высвобождении ХЦК, что в свою очередь изменяет секрецию ферментов ПЖ.
Содержание секретина в крови натощак у больных ХП достоверно снижено (р<0,001, р<0,01). После стандартного завтрака у больных ХП уровень секретина снижается, а у здоровых лиц он повышается.
Таким образом, секреция гастроинтестинальных гормонов в группах больных ХП с тяжелой степенью панкреатической недостаточности была нарушена. Снижалась секреция секретина как натощак, так и после пищевой нагрузки. Секреция ХЦК натощак достоверно была повышена, но на пищевую нагрузку адекватный секреторный ответ отсутствует.
Обсуждение
Проведенное исследование позволило оценить содержание в крови нейромедиаторов и гормонов, выявить нарушения в системе регуляции и сопоставить их с секреторной активностью ПЖ. Изменение соотношения нейромедиаторов и гормонов при ХП носит адаптационный характер, направленный на сохранение секреторной активности ПЖ при значительных фиброзных изменениях ее ткани. Результатом выявленных изменений в системе регуляции является снижение качества составляющих панкреатического сока.
Проведенные исследования показали выраженные нарушения регуляторных механизмов гастроинтестинальных гормонов на фоне хронического панкреатита, и особенно – осложненного течения. Такие нарушения проявляются внешнесекреторной недостаточностью тяжелой степени. Не корригируемая в достаточном объеме панкреатическая недостаточность может приводить к формированию белково–энергетической недостаточности тяжелой степени. Особенно ярко эти проявления выражены у больных АП.
Панкреатическая недостаточность тяжелой степени ведет к полиорганному расстройству пищеварения и обмена веществ в организме. При сниженном потенциале внешнесекреторной активности ПЖ происходит перегрузка оставшихся секреторных элементов: чем ниже секреторный потенциал, тем с большим перенапряжением функционируют оставшиеся дуктулоциты и ациноциты, что усугубляет патологию органа [1]. Для избежания или замедления этого процесса применяется ферментозаместительная терапия.
Больным, страдающим тяжелыми нарушениями функции ПЖ, необходима пожизненная коррекция этих нарушений. В этих случаях применяются большие дозы полиферментных препаратов. Выбор дозы осуществляется с учетом ряда показателей. При этом оцениваются клинический эффект (устранение диареи и потери массы тела), индекс массы тела, объем принимаемой пищи, уровень стеатореи, нутритивный статус. В проведенном проспективном исследовании J.E. Domingues–Munoz et al. [9] было показано, что оптимальная доза ферментов – это доза, способная нормализовать коэффициент всасывания жиров (на основании дыхательного теста). Авторы показали, что начальная доза ферментов при тяжелой внешнесекреторной недостаточности составляла 40 000–50 000 ЕД FIP [9] на каждый прием пищи. В нашей стране имеется препарат с дозировкой 40 000 ЕД FIP – Креон.
При внешнесекреторной недостаточности имеет значение не только доза препарата, но и его форма. Применение мини–микросферических форм (препараты IV поколения), защищенных кислотоустойчивой пленкой, способствует более эффективному действию препарата. А помещение микросфер в дополнительную кислотоустойчивую капсулу обеспечивает двойную защиту. Креон полностью отвечает этим требованиям.
Внешнесекреторная недостаточность тяжелой степени требует назначения препаратов панкреатита до 200 тыс. ЕД FIP в сутки. Применение Креона с большим содержанием липазы (40 тыс. ЕД FIP) по 3–4 капсулы в сут. помогает купировать клинические проявления экзокринной недостаточности и улучшить качество жизни больных.
Литература
1. Коротько Г.Ф. Секреция поджелудочной железы – Краснодар: КГМУ, 2–е дополн. изд–е, 2005. – 311с.
2. Beger H.G., Matsuno S., Cameron J.L. Diseases of the Pancreas. Berlin.: Springer Heidlberg, New York, 2008. – 949 p.
3. Czako L., Hegyi H., Rakonczay J.Z. et al. Interactions between the endocrine and exocrine pancreas and their clinical relevanc // Pancreatol. 2009. Vol. 9(4). P. 351–359.
4. Бассалык Л.С. Гастрин и биогенные амины нейрогуморальной регуляции желудочной секреции в норме и патологии: Автореферат докт. дис. – М., 1975. – С.35.
5. Губергриц Н.Б., Христич Т.Н., Бондаренко О.А. Неалкогольная жировая болезнь поджелудочной железы. – Донецк: Лебедь, 2013. – 235с.
6. Камышин В.С. Способ определения холинэстеразной активности по Нestrin Sh. Клинико–биохимическая лабораторная диагностика. – Минск, 2003. – С. 52–57.
7. Трубицына И.Е., Дроздов В.Н., Руть М.В. Вариации и частота распределения количественного значения ацетилхолина холинестеразной активности в сыворотке и крови у здоровых лиц // Экспериментальная и клиническая гастроэнтерология. 2007. № 3. – С.78–81.
8. Барановский А.Ю. Диетология: Руководство / Под ред. А.Ю. Барановского, 4–е изд. – СПб., 2012. – 1024 с.
9. Domingues–Munoz Е. Хронический панкреатит и стойкая стеаторея: какую дозу ферментов считать оптимальной // Клин. гастроэнтерол. и гепатол. // Русское издание. – 2011. – Т. 4, № 4. – С. 231–237.












