По данным сравнительных исследований, при беременности не установлена необходимость в более продолжительных курсах лечения ВВК. Считается, что в случае острого течения заболевания достаточно применения антимикотиков местного действия с учетом срока беременности (в частности, имидазолов), служащих в течение многих лет в качестве средств выбора для лечения ВВК и эффективных при режиме многоразового дозирования с вполне приемлемой безопасностью [3,5].
В этом случае низкая комплаентность лечения является проблемой, так как только 1/3 женщин строго следует назначениям врача. Предприняты шаги к сокращению курса лечения антифунгальными препаратами при сохранении их клинической эффективности, что может быть решено за счет увеличения дозы одноразового интравагинального применения исходя из того, что общая доза в отличие от длительности терапии является более значимым фактором. Общим для ряда производных имидазола (изоконазола, оксиконазола, омоконазола и тиоконазола) является ограниченное системное всасывание при применении в больших дозах с усилением местных симптомов раздражения.
Впервые зарегистрированный в России сертаконазол в виде вагинальных суппозиториев с длительным высвобождением препарата, содержащих 300 мг активного вещества, произведенный Laboratoires Théramex (Монако) и маркетируемый на российском рынке по лицензии фирмы Ferrer Internacionale A.S. (Испания) венгерским фармацевтическим заводом EGIS под торговым названием Залаин (zalain), является производным имидазола и бензотиофена. Сертаконазол в терапевтических дозах наряду с фунгистатическим обладает выраженным фунгицидным действием и проявляет активность в отношении грибов рода Candida, включая штаммы с низкой чувствительностью и перекрестной резистентностью к другим производным имидазола [6]. В связи с отсутствием системной абсорбции после интравагинального применения сертаконазол не обнаруживается в плазме и моче, но присутствует в вагинальных секретах в течение не менее чем 96 ч [4]. Благодаря такому фармакокинетическому профилю использование сертаконазола не требует специальных мер предосторожности, и он наиболее безопасен во время беременности.
Целью исследования явилось проведение клинической оценки эффективности интравагинального применения нового противогрибкового препарата сертаконазола (Залаина) в сравнении с клотримазолом, одним из наиболее часто использующихся в клинической практике производных имидазола при местном лечении ВВК во время беременности.
Материал и методы исследования
Проведено одноцентровое амбулаторное клиническое рандомизированное исследование с активным контролем с использованием параллельных групп. Исследование выполнено на базе МУЗ «Перинатальный центр» г. Энгельса Саратовской области с мая 2006 г. по июнь 2007 г. Под наблюдением находились 62 беременные в возрасте от 18 до 37 лет (средний возраст 24±2,1 года) с диагнозом острый ВВК (менее чем три эпизода в течение предшествующего года), подтвержденным данными микроскопического и культурального исследований (выявление дрожжеподобных грибов рода Candida). Основные жалобы пациенток (обильные выделения, жжение и зуд во влагалище) и клинические симптомы ВВК (гиперемия, отечность слизистой оболочки, наличие характерных белей) оценивались по 3–балльной шкале: 0 баллов – отсутствие симптомов, 1 балл – легкая степень их выраженности, 2 балла – умеренные проявления и 3 балла – тяжелая степень заболевания. Присутствие дрожжеподобных грибов оценивалось полуколичественно: 0 баллов – отрицательное (отсутствие колоний), 1 балл – незначительное (≤10 колоний), 2 балла – умеренное (11–100 колоний) и 3 балла – выраженное (>100 колоний).
В критерии отбора пациенток входило отсутствие бактериального вагиноза, хронического рецидивирующего ВВК и инфекций, передаваемых половым путем (ИППП) в момент обследования, хотя перенесенные ИППП в анамнезе отмечались у 10 (16,1%) беременных.
Манифестация заболевания во время беременности у 47 (75,8%) женщин наступила впервые, у остальных 15 (24,2%) случаи ВВК наблюдались и до наступления беременности. В исследование не включали беременных с тяжелой экстрагенитальной патологией (эндокринные заболевания, состояние иммунодефицита), ведущей к развитию осложненного течения ВВК. Однако пациентки обеих групп имели различные осложнения и заболевания во время настоящей беременности.
Все пациентки для лечения ВВК были рандомизированно разделены на две группы. Пациентки 1–й группы (n=30) получали однократно 1 вагинальный суппозиторий (300 мг) сертаконазола (Залаин) глубоко в задний свод влагалища на ночь. Пациентки 2–й группы (n=32) получали интравагинально 1 таблетку (100 мг) клотримазола (торговое название и производитель на выбор женщины) на ночь в течение 7 дней. Всем женщинам рекомендовалось воздержаться от сексуальной близости до первого контрольного визита. Клинический мониторинг беременных осуществлялся через неделю (7±1 день) от момента начала лечения (ближайшее наблюдение) и через 4 нед (28±3 дня) после его завершения (отдаленное наблюдение). Все лабораторные исследования проводились перед началом лечения, через неделю от момента начала лечения и через 4 нед после его завершения. Таким образом, первое исследование служило базовым значением, результат второго исследования характеризовал клиническую эффективность применявшегося препарата, а третье – восстановление микробиоценоза гениталий. При отсутствии клинического и микологического излечения спустя одну неделю назначали повторную терапию. Таким образом, каждой пациентке проводилось 3–кратное контрольное исследование: через 7, 14 и 28 дней. При каждом визите проводился опрос больных с целью выявления возможных нежелательных эффектов. Информированное письменное согласие пациенток на участие в исследовании было обязательным.
Статистическая обработка полученных результатов проводилась с использованием методов параметрической и непараметрической статистики в программах Excel для Windows XP (Microsoft Co.) и Statistica (Stat Soft Inc.). Для оценки достоверности различий до и после лечения применяли t–критерий Стьюдента. Различия считались достоверными при p≤0,05.
Результаты исследования
и обсуждение
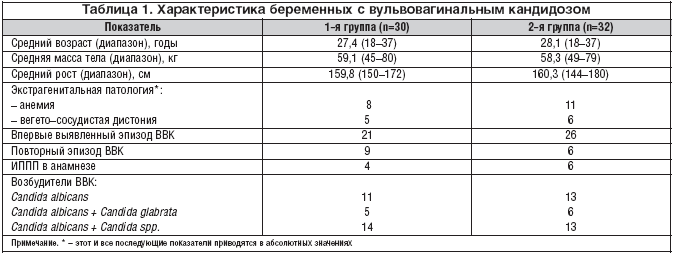
В исследование были отобраны больные со сходными характеристиками с целью воспроизводимости данных по эффективности и безопасности. Контрольная группа больных получала лечение стандартным препаратом клотримазолом, что обеспечивало достоверность при сопоставлении результатов. В таблице 1 отражены возрастные массо–ростовые показатели пациенток, данные анамнеза и возбудители ВВК у обследованных женщин. Однородность исследуемых групп подтверждена статистическим анализом, и несмотря на то, что в 1–ю группу входило больше пациенток, имевших в анамнезе заболевание ВВК, различие между группами не было статистически значимым.
Большинство больных – 44 пациентки (70,9%) – предъявляли жалобы на умеренные бели, которые оценивались двумя баллами, 18 (29,1%) пациенток отмечали выраженные выделения, соответствующие 3 баллам. Умеренный зуд во влагалище (2 балла) отмечали 60 (96,8%) женщин, сильный (3 балла) – 2 (3,2%) пациентки. Субъективные симптомы ВВК не всегда коррелировали с его клиническими проявлениями. При гинекологическом осмотре такие воспалительные изменения, как гиперемия, отечность слизистой оболочки влагалища и влагалищной части шейки матки умеренной степени (2 балла), отмечались у 52 (84,6%) пациенток, легкой степени (1 балл) – у 10 (15,4%) женщин.
Бактериологическое исследование у пациенток с ВВК показало, что у всех беременных до лечения были обнаружены грибы рода Candida в титре выше 5–6 lg КОЕ/мл. Наличие только Candida albicans установлено у 24 (38,7%) больных, наличие сочетания Candida albicans с Candida glabrata – у 11 (17,7%) и Candida albicans с Candida spp. – у 27 беременных (43,6%).
В нашем исследовании сертаконазол при однократном применении по эффективности не уступал семидневному курсу препарата сравнения клотримазола (ни при определении статистической достоверности различий, ни при простой оценке этих различий). При опросе пациенток с ВВК через неделю от начала лечения все женщины отмечали исчезновение жалоб и указывали на значительное улучшение самочувствия. Продолжительность лечения, при которой происходило улучшение самочувствия, была сходной для обеих исследуемых групп, при этом медиана времени, при котором наблюдалось облегчение выраженных симптомов заболевания, составила 3 дня, а полного улучшения самочувствия – 3–5 дней. Слабые клинические проявления ВВК (1 балл) через 7 дней при контрольном осмотре наблюдались у 2 (6,6%) женщин в 1–й и 3 женщин (9,4%) во 2–й группе. Умеренные клинические проявления заболевания (2 балла) беспокоили 6 женщин (18,7%) 2–й группы, что потребовало назначения повторного курса терапии. Таким образом, спустя 7 дней после лечения сертаконазолом клиническое выздоровление с полной микологической санацией наблюдалось у 28 (93,4%), а клотримазолом – у 23 (71,9%) беременных.
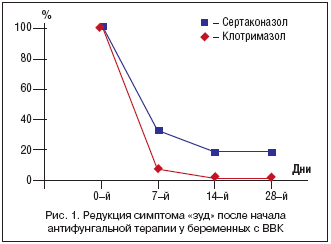
На рисунке 1 показана динамика изменения симптома «зуд», рассматриваемого в качестве основного при ВВК, до антифунгальной терапии, при ближайшем и отдаленном наблюдении после лечения. Повторное лечение двух (6,6%) пациенток с ВВК сертаконазолом и 9 (28,1%) пациенток – клотримазолом привело в первом случае у всех пациенток к исчезновению клинических и бактериологических признаков заболевания, а во втором – только у 4 (12,5%) женщин.
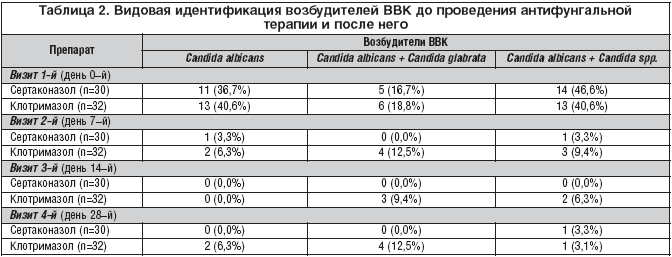
Из 62 беременных, включенных в исследование, у 8 (12,9%) при отдаленном наблюдении (28–й день) проявлялся микологический рецидив заболевания ВВК. Однако 3 (4,8%) пациентки оставались клинически здоровыми на протяжении всего периода наблюдения. В связи с этим была проведена видовая идентификация возбудителей ВВК до проведения антифунгальной терапии (табл. 2) и после него.
Установлено, что после лечения сертаконазолом одна (3,3%) из пациенток оставалась носителем Candida albicans + Candida spp. без проявлений клинической картины заболевания. В то же время в группе беременных, леченных клотримазолом, отсутствие микологической санации наблюдалось у 7 (21,9%) пациенток и только у 2 (6,3%) из них, являвшихся носителями Candida albicans, без клинических проявлений заболевания. Таким образом, показатели клинической эффективности при отдаленном наблюдении составили 100,0 и 84,4% случаев в группах однократного интравагинального применения сертаконазола (300 мг) и многократного интравагинального применения клотримазола (100 мг 1 раз/сут в течение 7 дней) соответственно. Микологическое выздоровление спустя 28 дней после лечения сертаконазолом обнаружено в 96,7%, а клотримазолом – в 78,1% случаев.
Ни одна пациентка не была исключена из исследования из–за непереносимости или побочных эффектов лечения сертаконазолом или клотримазолом. Важным достоинством сертаконазола по данным клинического и микологического обследования является длительное сохранение его эффекта. Число рецидивов после лечения препаратом было минимальным. При длительном наблюдении после лечения выявлялись достоверные различия между видами терапии по частоте возникновения рецидивов с преимуществом сертаконазола. При более коротких периодах наблюдения после окончания терапии такие различия трудно обнаружить. Эффективность сертаконазола проявлялась через несколько первых дней лечения значительным ослаблением клинических проявлений и симптомов заболевания, а также отрицательными результатами первого микробиологического тестирования. Быстрота развития эффекта сертаконазола благоприятствует его использованию больными, поскольку это важно для соблюдения ими режима лечения. Переносимость и безопасность сертаконазола определяют выполнение больными предписаний врача при лечении препаратом и хороший эффект терапии, снижающий в конечном счете ее стоимость.
Вывод
Высокая эффективность сертаконазола при однократном режиме лечения, его переносимость и удобство в применении позволяют считать этот препарат одним из перспективных в антифунгальной терапии острого ВВК у женщин во время беременности.
Статья опубликована в журнале
«Российский вестник акушера–гинеколога»,
2008, №3, с. 77–80
Литература
1. Михайлов А.В., Решетько О.В., Луцевич К.А. Рациональная фармакотерапия вульвовагинального кандидоза с позиций фармакоэпидемиологии и медицины доказательств. Клинмикробиол антимикроб химиотер 2007; 9: 1: 34–47.
2. Cotch M.F., Hillier S.L., Gibbs R.S., Eschenbach D.A. Epidemiology and outcomes associated with moderate to heavy Candida colonization during pregnancy. Am J Obstet Gynec 1998; 178:374–380.
3. Ernest J.M. Topical antifungal agents and pregnancy. Obstet Gynec Clin North Am 1999; 19: 587–607.
4. Guerin V., Delance V., Papalexious P. et al. Systemic absorption of 14C–radiolabelled sertaconazole administered in 300 mg prolongedliberation vaginal suppository form in four healthy postmenopausal women. J Mycol Med 1996; 6: 63–67.
5. King C.T., Rogers P.D., Cleary J.D., Chapman S.W. Antifungal therapy during pregnancy. Clin Infect Dis 1998; 27: 1151–1160.
6. Palacin C., Tarrago C., Ortiz J.A. Sertaconazole: pharmacology of a gynecological antifungal agent. Int J Gynec Obstet 2000; 71:Suppl.1: 37–46.
7. Xu J., Sobel J.D. Candida vulvovaginitis in pregnancy. Curr Infect Dis Rep 2004; 6: 445–449.












