–í–≤–Ķ–ī–Ķ–Ĺ–ł–Ķ
–ě–ī–Ĺ–ĺ–Ļ –ł–∑ –į–ļ—ā—É–į–Ľ—Ć–Ĺ—č—Ö –Ņ—Ä–ĺ–Ī–Ľ–Ķ–ľ —Ā–ĺ–≤—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ–ĺ–Ļ –ľ–Ķ–ī–ł—Ü–ł–Ĺ—č —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź —Ā—ā–į–Ī–ł–Ľ—Ć–Ĺ–ĺ –≤—č—Ā–ĺ–ļ–ł–Ļ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ć —á–ł—Ā–Ľ–į –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ĺ–Ĺ–Ĺ–ĺ-–≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ —É—Ä–ĺ–≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ —ā—Ä–į–ļ—ā–į, —á—ā–ĺ –Ņ—Ä–ł–≤–ĺ–ī–ł—ā –Ĺ–Ķ —ā–ĺ–Ľ—Ć–ļ–ĺ –ļ –ĺ–≥—Ä–ĺ–ľ–Ĺ—č–ľ –ľ–į—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ—č–ľ –∑–į—ā—Ä–į—ā–į–ľ, –Ĺ–ĺ –ł —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź —É–≥—Ä–ĺ–∑–ĺ–Ļ –ī–Ķ–ľ–ĺ–≥—Ä–į—Ą–ł—á–Ķ—Ā–ļ–ĺ–Ļ —Ā–ł—ā—É–į—Ü–ł–ł [1, 2].
–ü–ĺ—Ā–Ľ–Ķ–ī–Ĺ–ł–Ķ 10‚Äď15 –Ľ–Ķ—ā —Ā–Ņ–Ķ—Ü–ł–į–Ľ–ł—Ā—ā—č –ĺ—ā–ľ–Ķ—á–į—é—ā —á–Ķ—ā–ļ—É—é —ā–Ķ–Ĺ–ī–Ķ–Ĺ—Ü–ł—é –ļ –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—é —ć—ā–ł–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ĺ–Ļ —Ā—ā—Ä—É–ļ—ā—É—Ä—č –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ĺ–Ĺ–Ĺ—č—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ, –į –ł–ľ–Ķ–Ĺ–Ĺ–ĺ —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ —É–ī–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ –≤–Ķ—Ā–į –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–Ļ, –≤—č–∑—č–≤–į–Ķ–ľ—č—Ö –ĺ–Ī–Ľ–ł–≥–į—ā–Ĺ—č–ľ–ł –Ņ–į—ā–ĺ–≥–Ķ–Ĺ–į–ľ–ł, –ł –≤–ĺ–∑—Ä–į—Ā—ā–į—é—Č—É—é —Ä–ĺ–Ľ—Ć —É—Ā–Ľ–ĺ–≤–Ĺ–ĺ-–Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ĺ—č—Ö –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–ĺ–≤. –°–Ľ–Ķ–ī—É–Ķ—ā –ĺ—ā–ľ–Ķ—ā–ł—ā—Ć, —á—ā–ĺ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ĺ–Ĺ–Ĺ–ĺ-–≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ —É—Ä–ĺ–≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ —ā—Ä–į–ļ—ā–į, –į—Ā—Ā–ĺ—Ü–ł–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö —Ā –Ņ–į—ā–ĺ–Ī–ł–ĺ–Ĺ—ā–į–ľ–ł, —Ö–į—Ä–į–ļ—ā–Ķ—Ä–ł–∑—É–Ķ—ā—Ā—Ź —Ā—ā–Ķ—Ä—ā–ĺ–Ļ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ļ–į—Ä—ā–ł–Ĺ–ĺ–Ļ, –Ĺ–ĺ –Ņ—Ä–ł —ć—ā–ĺ–ľ —Ā–Ņ–ĺ—Ā–ĺ–Ī—Ā—ā–≤—É–Ķ—ā —Ą–ĺ—Ä–ľ–ł—Ä–ĺ–≤–į–Ĺ–ł—é –ļ–ĺ–ľ–Ņ–Ľ–Ķ–ļ—Ā–į –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł—Ö —Ā–ł–ľ–Ņ—ā–ĺ–ľ–ĺ–≤ –ł/–ł–Ľ–ł —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–ĺ–≤, —ā–į–ļ–ł—Ö –ļ–į–ļ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł—Ö –≤–į–≥–ł–Ĺ–į–Ľ—Ć–Ĺ—č—Ö –≤—č–ī–Ķ–Ľ–Ķ–Ĺ–ł–Ļ, —Ā–Ņ–į–Ķ—á–Ĺ—č–Ļ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā, –ĺ—Ā–Ľ–ĺ–∂–Ĺ–Ķ–Ĺ–ł—Ź —ā–Ķ—á–Ķ–Ĺ–ł—Ź –Ī–Ķ—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ–ĺ—Ā—ā–ł –ł —Ä–ĺ–ī–ĺ–≤, –ī–ł—Ā—Ą—É–Ĺ–ļ—Ü–ł—Ź –Ľ–ĺ–ļ–į–Ľ—Ć–Ĺ–ĺ–Ļ –Ņ—Ä–ĺ—ā–ł–≤–ĺ–ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–Ļ –∑–į—Č–ł—ā—č [3‚Äď5]. –í —Ā–Ľ—É—á–į–Ķ –ľ–ł–ļ—Ā—ā-–ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ł —ć—ā–ł–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ—É—é —Ä–ĺ–Ľ—Ć –ļ–į–∂–ī–ĺ–≥–ĺ –ł–∑ —É—á–į—Ā—ā–Ĺ–ł–ļ–ĺ–≤ –≤–ĺ—Ā–Ņ–į–Ľ–Ķ–Ĺ–ł—Ź –≤—č–ī–Ķ–Ľ–ł—ā—Ć –Ņ—Ä–į–ļ—ā–ł—á–Ķ—Ā–ļ–ł –Ĺ–Ķ–≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ, –Ĺ–ĺ –ļ–į–∂–ī—č–Ļ –ł–∑ –Ĺ–ł—Ö –Ņ—Ä–ł–≤–Ĺ–ĺ—Ā–ł—ā —Ā–≤–ĺ—é –Ľ–Ķ–Ņ—ā—É –≤ —Ä–į–∑–≤–ł—ā–ł–Ķ –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–į, –į –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–į—Ź –į–Ĺ—ā–ł–≥–Ķ–Ĺ–Ĺ–į—Ź –Ĺ–į–≥—Ä—É–∑–ļ–į —Ā–Ņ–ĺ—Ā–ĺ–Ī—Ā—ā–≤—É–Ķ—ā —É—Ā–ł–Ľ–Ķ–Ĺ–ł—é –≤–ł—Ä—É–Ľ–Ķ–Ĺ—ā–Ĺ–ĺ—Ā—ā–ł –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–ĺ–≤, —Ą–ĺ—Ä–ľ–ł—Ä–ĺ–≤–į–Ĺ–ł—é –į–Ĺ—ā–ł–Ī–į–ļ—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–ĺ–Ļ —Ä–Ķ–∑–ł—Ā—ā–Ķ–Ĺ—ā–Ĺ–ĺ—Ā—ā–ł, –Ņ—Ä–ł–≤–ĺ–ī—Ź –ļ –Ĺ–Ķ—ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł —ā–Ķ—Ä–į–Ņ–ł–ł –ł —Ä–į–∑–≤–ł—ā–ł—é –ĺ—Ā–Ľ–ĺ–∂–Ĺ–Ķ–Ĺ–ł–Ļ [6].
–í –ĺ—Ā–Ĺ–ĺ–≤–Ķ –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–į, –≤—č–∑–≤–į–Ĺ–Ĺ–ĺ–≥–ĺ —É—Ā–Ľ–ĺ–≤–Ĺ–ĺ-–Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ĺ—č–ľ–ł –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–į–ľ–ł, –Ľ–Ķ–∂–ł—ā —Ą–ĺ—Ä–ľ–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ –Ī–ł–ĺ–Ņ–Ľ–Ķ–Ĺ–ļ–ł, –≤ —Ā–ĺ—Ā—ā–į–≤–Ķ –ļ–ĺ—ā–ĺ—Ä–ĺ–Ļ –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ—č –∑–į—Č–ł—Č–Ķ–Ĺ—č –ĺ—ā —Ä–į–∑–Ĺ—č—Ö —Ā—ā—Ä–Ķ—Ā—Ā–ĺ–≤—č—Ö –≤–ĺ–∑–ī–Ķ–Ļ—Ā—ā–≤–ł–Ļ, –≤–ļ–Ľ—é—á–į—Ź –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā—č –ł –ł–ľ–ľ—É–Ĺ–Ĺ—É—é —Ā–ł—Ā—ā–Ķ–ľ—É —Ö–ĺ–∑—Ź–ł–Ĺ–į, –ł –Ī–Ľ–į–≥–ĺ–ī–į—Ä—Ź –ļ–ĺ—ā–ĺ—Ä–ĺ–Ļ –Ņ–ĺ–≤—č—ą–į–Ķ—ā—Ā—Ź —É—Ā—ā–ĺ–Ļ—á–ł–≤–ĺ—Ā—ā—Ć –ļ –į–Ĺ—ā–ł–Ī–ł–ĺ—ā–ł–ļ–į–ľ, –į–Ĺ—ā–ł—Ā–Ķ–Ņ—ā–ł–ļ–į–ľ, –ī–Ķ–∑–ł–Ĺ—Ą–Ķ–ļ—ā–į–Ĺ—ā–į–ľ –ł –∑–į—Č–ł—ā–Ĺ—č–ľ –ľ–Ķ—Ö–į–Ĺ–ł–∑–ľ–į–ľ –ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–į. –Ě–į —Ā–Ķ–≥–ĺ–ī–Ĺ—Ź –ī–ĺ–ļ–į–∑–į–Ĺ–ĺ, —á—ā–ĺ 99% –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–ĺ–≤ –Ĺ–į—Ö–ĺ–ī—Ź—ā—Ā—Ź –≤ —Ā–ĺ—Ā—ā–į–≤–Ķ –Ī–ł–ĺ–Ņ–Ľ–Ķ–Ĺ–ĺ–ļ. –ü—Ä–ł —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–ľ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–Ķ –ĺ—á–į–≥ –≤–ĺ—Ā–Ņ–į–Ľ–Ķ–Ĺ–ł—Ź —Ā–ĺ–ī–Ķ—Ä–∂–ł—ā –Ī–ł–ĺ–Ņ–Ľ–Ķ–Ĺ–ļ—É –≤ 60% —Ā–Ľ—É—á–į–Ķ–≤, –≤ —ā–ĺ –≤—Ä–Ķ–ľ—Ź –ļ–į–ļ –Ņ—Ä–ł –ĺ—Ā—ā—Ä–ĺ–ľ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–Ķ —ć—ā–ĺ—ā –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ć —Ā–ĺ—Ā—ā–į–≤–Ľ—Ź–Ķ—ā –Ľ–ł—ą—Ć 6% [7, 8]. –Ď–ł–ĺ–Ņ–Ľ–Ķ–Ĺ–ļ–ł —Ā—ā–ł–ľ—É–Ľ–ł—Ä—É—é—ā –≤–ĺ—Ā–Ņ–į–Ľ–Ķ–Ĺ–ł–Ķ, —É–≤–Ķ–Ľ–ł—á–ł–≤–į—Ź –Ņ—Ä–ĺ–Ĺ–ł—Ü–į–Ķ–ľ–ĺ—Ā—ā—Ć —Ā–ĺ—Ā—É–ī–ĺ–≤, –ĺ–Ī—Ä–į–∑–ĺ–≤–į–Ĺ–ł–Ķ —ć–ļ—Ā—Ā—É–ī–į—ā–į –ł —Ą–ĺ—Ä–ľ–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ —Ą–ł–Ī—Ä–ł–Ĺ–ĺ–≤–ĺ–≥–ĺ —Ā—ā—Ä—É–Ņ–į. –í –ļ–Ľ–Ķ—ā–ļ–į—Ö –Ī–ł–ĺ–Ņ–Ľ–Ķ–Ĺ–ļ–ł –ĺ–Ī—Ä–į–∑—É—é—ā—Ā—Ź —Ą–Ķ—Ä–ľ–Ķ–Ĺ—ā—č, –≤—č–∑—č–≤–į—é—Č–ł–Ķ –ī–Ķ–≥—Ä–į–ī–į—Ü–ł—é –ł–Ľ–ł –ľ–ĺ–ī–ł—Ą–ł–ļ–į—Ü–ł—é –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č—Ö –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤, –ĺ–Ī—É—Ā–Ľ–ĺ–≤–Ľ–ł–≤–į—Ź –Ĺ–Ķ—ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ—č–Ļ –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ –ĺ—ā–≤–Ķ—ā [7‚Äď9].
–ě—Ā–Ĺ–ĺ–≤–Ĺ—č–ľ–ł –ļ–ĺ–ľ–Ņ–ĺ–Ĺ–Ķ–Ĺ—ā–į–ľ–ł –Ī–ł–ĺ–Ņ–Ľ–Ķ–Ĺ–ĺ–ļ —É—Ä–ĺ–≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ —ā—Ä–į–ļ—ā–į —Ź–≤–Ľ—Ź—é—ā—Ā—Ź –ļ–ĺ–ľ–ľ–Ķ–Ĺ—Ā–į–Ľ—č, —ā–į–ļ–ł–Ķ –ļ–į–ļ Mycoplasma hominis, Ureaplasma urealyticum, Ureaplasma parvum, Gardnerella vaginalis, Atopobium vaginae, –ī–ł—Ą—ā–Ķ—Ä–ĺ–ł–ī—č, –į—ć—Ä–ĺ–Ī–Ĺ—č–Ķ –Ī–į–ļ—ā–Ķ—Ä–ł–ł. –ě–Ĺ–ł –į–ļ—ā–ł–≤–ł—Ä—É—é—ā—Ā—Ź –Ľ–ł—ą—Ć –Ņ—Ä–ł –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–Ĺ—č—Ö —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö, —Ā—ā–ł–ľ—É–Ľ–ł—Ä—É—Ź –ĺ–Ī—Ä–į–∑–ĺ–≤–į–Ĺ–ł–Ķ –ľ–Ķ–ī–ł–į—ā–ĺ—Ä–ĺ–≤ –≤–ĺ—Ā–Ņ–į–Ľ–Ķ–Ĺ–ł—Ź, –Ņ–ĺ–≤—Ä–Ķ–∂–ī–Ķ–Ĺ–ł–Ķ —ā–ļ–į–Ĺ–Ķ–Ļ, –≥–ł–Ņ–ĺ–ļ—Ā–ł—é, –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł–Ķ –ľ–ł–ļ—Ä–ĺ—Ü–ł—Ä–ļ—É–Ľ—Ź—Ü–ł–ł –ł —Ā–Ķ–Ĺ—Ā–ł–Ī–ł–Ľ–ł–∑–ł—Ä—É—Ź –ľ–į–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ –†–į–Ī–ĺ—ā—č —Ä–į–∑–Ĺ—č—Ö –į–≤—ā–ĺ—Ä–ĺ–≤ [4, 9‚Äď11] —Ā–≤–ł–ī–Ķ—ā–Ķ–Ľ—Ć—Ā—ā–≤—É—é—ā –ĺ —ā–ĺ–ľ, —á—ā–ĺ –Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ĺ–ĺ—Ā—ā—Ć G. vaginalis, Mobiluncus spp., M. hominis, U. urealyticum –ł –į–Ĺ–į—ć—Ä–ĺ–Ī–Ĺ—č—Ö –Ī–į–ļ—ā–Ķ—Ä–ł–Ļ —Ā–≤—Ź–∑–į–Ĺ–į —Ā –ľ–į—Ā—Ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć—é —Ä–į–∑–ľ–Ĺ–ĺ–∂–Ķ–Ĺ–ł—Ź –ľ–ł–ļ—Ä–ĺ–Ī–Ĺ–ĺ–≥–ĺ –į–≥–Ķ–Ĺ—ā–į –≤ –ĺ—á–į–≥–Ķ –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ł. –ė–ľ–Ķ–Ĺ–Ĺ–ĺ –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ —á–ł—Ā–Ľ–Ķ–Ĺ–Ĺ–ĺ—Ā—ā–ł —ā–ĺ–≥–ĺ –ł–Ľ–ł –ł–Ĺ–ĺ–≥–ĺ –≤–ł–ī–į –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–ĺ–≤ –ł–Ľ–ł –Ņ–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł–Ķ –Ī–į–ļ—ā–Ķ—Ä–ł–Ļ –≤ –Ĺ–Ķ—Ā–≤–ĺ–Ļ—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ–ľ –ī–Ľ—Ź –Ĺ–ł—Ö –ľ–Ķ—Ā—ā–Ķ –ĺ–Ī–ł—ā–į–Ĺ–ł—Ź —Ā–Ľ—É–∂–ł—ā —Ā–ł–≥–Ĺ–į–Ľ–ĺ–ľ –ī–Ľ—Ź –į–ī–į–Ņ—ā–ł–≤–Ĺ—č—Ö –ł–Ľ–ł –Ĺ–Ķ–ĺ–Ī—Ä–į—ā–ł–ľ—č—Ö –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ļ –≤ –Ī–ł–ĺ—Ü–Ķ–Ĺ–ĺ–∑–Ķ –≤–Ľ–į–≥–į–Ľ–ł—Č–į [6, 12‚Äď15].
–ü—Ä–ł –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł 1817 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–ļ —Ā –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–ľ–ł –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–į–ľ–ł —Ä–į–∑–Ľ–ł—á–Ĺ–ĺ–Ļ —ć—ā–ł–ĺ–Ľ–ĺ–≥–ł–ł –Ī—č–Ľ–ĺ —É—Ā—ā–į–Ĺ–ĺ–≤–Ľ–Ķ–Ĺ–ĺ, —á—ā–ĺ –≤ 432 —Ā–Ľ—É—á–į—Ź—Ö —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ļ –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā —Ź–≤–ł–Ľ—Ā—Ź —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–ĺ–ľ –≤–ĺ–∑–ī–Ķ–Ļ—Ā—ā–≤–ł—Ź —Ä–į–∑–Ľ–ł—á–Ĺ—č—Ö —É—Ā–Ľ–ĺ–≤–Ĺ–ĺ-–Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ĺ—č—Ö –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–ĺ–≤. –Ę–ĺ –Ķ—Ā—ā—Ć —Ä–Ķ—á—Ć –ł–ī–Ķ—ā –ĺ –ľ–ł–ļ—Ā—ā-–ł–Ĺ—Ą–Ķ–ļ—Ü–ł—Ź—Ö, –≤—č–∑–≤–į–Ĺ–Ĺ—č—Ö –ĺ–ī–Ĺ–ĺ–≤—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ–ĺ –Ĺ–Ķ—Ā–ļ–ĺ–Ľ—Ć–ļ–ł–ľ–ł –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–į–ľ–ł, —Ā–ĺ–≤–ľ–Ķ—Ā—ā–Ĺ–ĺ —É—á–į—Ā—ā–≤—É—é—Č–ł–ľ–ł –≤ –Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ķ–∑–Ķ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź [12]. –Ě–į–ł–Ī–ĺ–Ľ–Ķ–Ķ —á–į—Ā—ā–ĺ –≤—Ā—ā—Ä–Ķ—á–į–Ľ–ł—Ā—Ć —Ä–į–∑–Ľ–ł—á–Ĺ—č–Ķ —Ā–ĺ—á–Ķ—ā–į–Ĺ–ł—Ź U. urealyticum, U. parvum, M. hominis, –≥—Ä–ł–Ī–ĺ–≤ —Ä–ĺ–ī–į Candida, G. vaginalis, A. vaginae. –í —Ā–ĺ—Ā—ā–į–≤ –ľ–ł–ļ—Ä–ĺ–Ī–Ĺ–ĺ–Ļ –į—Ā—Ā–ĺ—Ü–ł–į—Ü–ł–ł –≤—Ö–ĺ–ī–ł–Ľ–ł —ā–į–ļ–ł–Ķ –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ—č, –ļ–į–ļ Streptococcus epidermidis, Streptococcus sapro—Äh—Éticus, Streptococcus spp., Corynebacterium xerosis, Escherichia coli, Enterococcus faecalis. –Ē–ĺ—Ā—ā–ĺ–≤–Ķ—Ä–Ĺ–ĺ —á–į—Č–Ķ –≤—č—Ź–≤–Ľ—Ź–Ľ—Ā—Ź S. –įureus, –ł –Ķ–≥–ĺ –Ņ—Ä–ł—Ā—É—ā—Ā—ā–≤–ł–Ķ –≤ –ī–ł–į–≥–Ĺ–ĺ—Ā—ā–ł—á–Ķ—Ā–ļ–ł –∑–Ĺ–į—á–ł–ľ–ĺ–ľ —ā–ł—ā—Ä–Ķ –≤–ĺ –ľ–Ĺ–ĺ–≥–ĺ–ľ –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ—Ź–Ľ–ĺ —Ö–į—Ä–į–ļ—ā–Ķ—Ä —ā–Ķ—á–Ķ–Ĺ–ł—Ź –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–į. –≠—ā–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ļ–ł —á–į—Č–Ķ –∂–į–Ľ–ĺ–≤–į–Ľ–ł—Ā—Ć –Ĺ–į —ā—Ź–Ĺ—É—Č–ł–Ķ –Ī–ĺ–Ľ–ł –≤–Ĺ–ł–∑—É –∂–ł–≤–ĺ—ā–į, –Ī–ĺ–Ľ–Ķ–∑–Ĺ–Ķ–Ĺ–Ĺ—č–Ķ –ľ–Ķ–Ĺ—Ā—ā—Ä—É–į—Ü–ł–ł, –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł –ĺ—ā–ľ–Ķ—á–į–Ľ–ł—Ā—Ć —Ā–Ľ–ł–∑–ł—Ā—ā–ĺ-–≥–Ĺ–ĺ–Ļ–Ĺ—č–Ķ –∂–Ķ–Ľ—ā–ĺ–≤–į—ā—č–Ķ –≤—č–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź [12].
–í —ć—ā–ĺ–ľ –∂–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł –Ī—č–Ľ–ĺ –Ņ–ĺ–ļ–į–∑–į–Ĺ–ĺ, —á—ā–ĺ –≤ —ć—ā–ł–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ĺ–ľ –į—Ā–Ņ–Ķ–ļ—ā–Ķ —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ļ –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā, –≤—č–∑–≤–į–Ĺ–Ĺ—č–Ļ U. urealyticum, U. parvum, M. hominis, C. albicans, —Ā–ĺ–Ņ—Ä–ĺ–≤–ĺ–∂–ī–į–Ķ—ā—Ā—Ź —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł–Ķ–ľ —Ā—Ä–Ķ–ī–Ĺ–Ķ–≥–ĺ —ā–ł—ā—Ä–į –≥—Ä–ł–Ī–ĺ–≤ —Ä–ĺ–ī–į Candida —Ā–≤—č—ą–Ķ 104 –ö–ě–ē/–ľ–Ľ, —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł–Ķ–ľ —Ā—Ä–Ķ–ī–Ĺ–Ķ–≥–ĺ —ā–ł—ā—Ä–į —Ā—ā–į—Ą–ł–Ľ–ĺ–ļ–ĺ–ļ–ļ–ĺ–≤ –ł —Ā—ā—Ä–Ķ–Ņ—ā–ĺ–ļ–ĺ–ļ–ļ–ĺ–≤, —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ–ľ —Ā—Ä–Ķ–ī–Ĺ–Ķ–≥–ĺ —ā–ł—ā—Ä–į –Ľ–į–ļ—ā–ĺ–Ī–į–ļ—ā–Ķ—Ä–ł–Ļ; –≤ —Ā–Ľ—É—á–į–Ķ –į—Ā—Ā–ĺ—Ü–ł–į—Ü–ł–ł U. urealyticum, U. parvum, M. hominis, G. vaginalis, A. vaginae —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ļ –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā —Ā–ĺ–Ņ—Ä–ĺ–≤–ĺ–∂–ī–į–Ķ—ā—Ā—Ź —Ä–Ķ–∑–ļ–ł–ľ —É–≥–Ĺ–Ķ—ā–Ķ–Ĺ–ł–Ķ–ľ –Ľ–į–ļ—ā–ĺ–Ī–ł—Ą–ł–ī–ĺ—Ą–Ľ–ĺ—Ä—č, —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł–Ķ–ľ —á–į—Ā—ā–ĺ—ā—č –≤—č—Ź–≤–Ľ–Ķ–Ĺ–ł—Ź –ł —Ā—Ä–Ķ–ī–Ĺ–Ķ–≥–ĺ —ā–ł—ā—Ä–į —ā–į–ļ–ł—Ö –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–ĺ–≤, –ļ–į–ļ Mobiluncus spp., Proteus spp, –ī–ł—Ą—ā–Ķ—Ä–ĺ–ł–ī—č. –•—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ļ –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā, –į—Ā—Ā–ĺ—Ü–ł–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–Ļ —Ā U. urealyticum, U. parvum,
M. hominis, —Ā–ĺ–Ņ—Ä–ĺ–≤–ĺ–∂–ī–į–Ķ—ā—Ā—Ź –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ —á–į—Ā—ā–ĺ—ā–ĺ–Ļ –≤—č—Ź–≤–Ľ–Ķ–Ĺ–ł—Ź E. coli –Ņ—Ä–ł —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł–ł —Ā—Ä–Ķ–ī–Ĺ–Ķ–≥–ĺ —ā–ł—ā—Ä–į –ī–ĺ 6,8¬Ī2,1 lg –ö–ě–ē/–ľ–Ľ, –į —ā–į–ļ–∂–Ķ –ī—Ä—É–≥–ł—Ö –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–ĺ–≤ –ļ–ł—ą–Ķ—á–Ĺ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ—č [12].
–ė–∑—É—á–Ķ–Ĺ–ł–Ķ –≤–∑–į–ł–ľ–ĺ–ī–Ķ–Ļ—Ā—ā–≤–ł—Ź –≥—Ä–ł–Ī–ĺ–≤ —Ä–ĺ–ī–į Candida –ł –ľ–į–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–į –Ņ–ĺ–ļ–į–∑–į–Ľ–ĺ, —á—ā–ĺ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź –Ĺ–ĺ—Ā—Ź—ā –ł—Ā–ļ–Ľ—é—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –ł–Ĺ–≤–į–∑–ł–≤–Ĺ—č–Ļ —Ö–į—Ä–į–ļ—ā–Ķ—Ä, —Ā–ĺ–Ņ—Ä–ĺ–≤–ĺ–∂–ī–į—é—ā—Ā—Ź –Ņ—Ä–ł—Ā—É—ā—Ā—ā–≤–ł–Ķ–ľ –≥–į—Ä–ī–Ĺ–Ķ—Ä–Ķ–Ľ–Ľ, –Ľ–į–ļ—ā–ĺ–Ī–į–ļ—ā–Ķ—Ä–ł–Ļ, –Ņ–ĺ–≤—Ä–Ķ–∂–ī–Ķ–Ĺ–ł–Ķ–ľ —É–Ľ—Ć—ā—Ä–į—Ā—ā—Ä—É–ļ—ā—É—Ä—č —ć–Ņ–ł—ā–Ķ–Ľ–ł–ĺ—Ü–ł—ā–ĺ–≤ –≤–Ľ–į–≥–į–Ľ–ł—Č–į –ł –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł–Ķ–ľ –ľ–Ķ—Ā—ā–Ĺ–ĺ–≥–ĺ –ł–ľ–ľ—É–Ĺ–Ĺ–ĺ–≥–ĺ –ĺ—ā–≤–Ķ—ā–į [15].
–ě—Ā–ĺ–Ī–ĺ–Ķ –∑–Ĺ–į—á–Ķ–Ĺ–ł–Ķ –≤ —Ä–į–∑–≤–ł—ā–ł–ł –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ĺ–Ĺ–Ĺ–ĺ-–≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ —É—Ä–ĺ–≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ —ā—Ä–į–ļ—ā–į –Ņ—Ä–ł–Ĺ–į–ī–Ľ–Ķ–∂–ł—ā –į–Ĺ–į—ć—Ä–ĺ–Ī–Ĺ–ĺ–Ļ –ľ–ł–ļ—Ä–ĺ—Ą–Ľ–ĺ—Ä–Ķ. –ß–į—Č–Ķ –≤—Ā–Ķ–≥–ĺ –Ņ–Ķ—Ä–≤–ł—á–Ĺ—č–ľ –ļ–ĺ–Ľ–ĺ–Ĺ–ł–∑–į—ā–ĺ—Ä–ĺ–ľ –≤–Ľ–į–≥–į–Ľ–ł—Č–į –≤—č—Ā—ā—É–Ņ–į—é—ā –ł–ľ–Ķ–Ĺ–Ĺ–ĺ –≥–į—Ä–ī–Ĺ–Ķ—Ä–Ķ–Ľ–Ľ—č, —Ā–ĺ–∑–ī–į–≤–į—Ź —É—Ā–Ľ–ĺ–≤–ł—Ź –ī–Ľ—Ź –Ņ–ĺ—Ā–Ľ–Ķ–ī—É—é—Č–Ķ–≥–ĺ —Ä–ĺ—Ā—ā–į –į–Ĺ–į—ć—Ä–ĺ–Ī–Ĺ—č—Ö –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–ĺ–≤ G. vaginalis –ĺ–Ī–Ľ–į–ī–į–Ķ—ā —É–Ĺ–ł–ļ–į–Ľ—Ć–Ĺ–ĺ–Ļ —Ā–Ņ–ĺ—Ā–ĺ–Ī–Ĺ–ĺ—Ā—ā—Ć—é –Ĺ–Ķ —ā–ĺ–Ľ—Ć–ļ–ĺ –į–ī–≥–Ķ–∑–ł—Ä–ĺ–≤–į—ā—Ć—Ā—Ź –Ĺ–į —ć–Ņ–ł—ā–Ķ–Ľ–ł–ĺ—Ü–ł—ā–į—Ö –≤–Ľ–į–≥–į–Ľ–ł—Č–į, –Ĺ–ĺ –ł –∑–į—Ā–Ķ–Ľ—Ź—ā—Ć –≤–Ķ—Ä—Ö–Ĺ–ł–Ķ –ĺ—ā–ī–Ķ–Ľ—č –≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ —ā—Ä–į–ļ—ā–į [4, 10, 11]. –ú–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ—č, –į—Ā—Ā–ĺ—Ü–ł–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–Ķ —Ā –Ī–į–ļ—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ—č–ľ –≤–į–≥–ł–Ĺ–ĺ–∑–ĺ–ľ, –Ņ—Ä–ĺ–ī—É—Ü–ł—Ä—É—é—ā —Ä–į–∑–Ľ–ł—á–Ĺ—č–Ķ –Ņ—Ä–ĺ—ā–Ķ–į–∑—č, –ľ—É—Ü–ł–Ĺ–į–∑—č, –≥–Ķ–ľ–ĺ–Ľ–ł–∑–ł–Ĺ, —Ź–Ĺ—ā–į—Ä–Ĺ—É—é –ļ–ł—Ā–Ľ–ĺ—ā—É, —á—ā–ĺ –Ņ—Ä–ł–≤–ĺ–ī–ł—ā –ļ —Ā—ā—Ä—É–ļ—ā—É—Ä–Ĺ—č–ľ –ł —Ą—É–Ĺ–ļ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ—č–ľ –Ņ–ĺ–≤—Ä–Ķ–∂–ī–Ķ–Ĺ–ł—Ź–ľ –Ľ–Ķ–Ļ–ļ–ĺ—Ü–ł—ā–ĺ–≤, –Ĺ–į—Ä—É—ą–į–Ķ—ā –ł—Ö –ľ–ł–≥—Ä–ł—Ä—É—é—Č—É—é –ł —Ą–į–≥–ĺ—Ü–ł—ā–į—Ä–Ĺ—É—é —Ā–Ņ–ĺ—Ā–ĺ–Ī–Ĺ–ĺ—Ā—ā—Ć –ö—Ä–ĺ–ľ–Ķ —ā–ĺ–≥–ĺ, —ā–į–ļ–ł–Ķ –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ—č, —Ā–Ĺ–ł–∂–į—Ź –ļ–į—ā–į–Ľ–į–∑–Ĺ—É—é –ł –Ņ–Ķ—Ä–ĺ–ļ—Ā–ł–ī–į–∑–Ĺ—É—é –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –≤–į–≥–ł–Ĺ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ĺ—ā–ī–Ķ–Ľ—Ź–Ķ–ľ–ĺ–≥–ĺ, –į —ā–Ķ–ľ —Ā–į–ľ—č–ľ –ł –Ņ—Ä–ĺ—ā–ł–≤–ĺ–ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ĺ–Ĺ–Ĺ—É—é –∑–į—Č–ł—ā—É —Ä–Ķ–Ņ—Ä–ĺ–ī—É–ļ—ā–ł–≤–Ĺ–ĺ–≥–ĺ —ā—Ä–į–ļ—ā–į, –Ņ–ĺ–≤—č—ą–į—é—ā —Ä–ł—Ā–ļ –ł–Ĺ—Ą–ł—Ü–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –ė–ü–ü–ü, –į–ļ—ā–ł–≤–į—Ü–ł–ł —Ā–ļ—Ä—č—ā–ĺ –Ņ—Ä–ĺ—ā–Ķ–ļ–į—é—Č–Ķ–Ļ –≤–ł—Ä—É—Ā–Ĺ–ĺ–Ļ –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ł –≤—Ā–Ľ–Ķ–ī—Ā—ā–≤–ł–Ķ –Ĺ–ł–∑–ļ–ĺ–≥–ĺ —Ä–Ķ–ī–ĺ–ļ—Ā-–Ņ–ĺ—ā–Ķ–Ĺ—Ü–ł–į–Ľ–į –ł –≥–ł–Ņ–ĺ–ļ—Ā–ł–ł —ā–ļ–į–Ĺ–Ķ–Ļ –≤–Ľ–į–≥–į–Ľ–ł—Č–į –Ņ—Ä–ł –≤—č—Ā–ĺ–ļ–ĺ–ľ –∑–Ĺ–į—á–Ķ–Ĺ–ł–ł pH [4, 10, 12]. –°–ĺ—Ö—Ä–į–Ĺ–Ķ–Ĺ–ł–Ķ –≤–ĺ–∑–Ī—É–ī–ł—ā–Ķ–Ľ—Ź –≤ –≥–Ľ—É–Ī–ĺ–ļ–ł—Ö —Ā–Ľ–ĺ—Ź—Ö —Ā–Ľ–ł–∑–ł—Ā—ā–ĺ–Ļ –≤–Ľ–į–≥–į–Ľ–ł—Č–į —Ā—ā–į–Ĺ–ĺ–≤–ł—ā—Ā—Ź –Ņ—Ä–ł—á–ł–Ĺ–ĺ–Ļ —É–Ņ–ĺ—Ä–Ĺ—č—Ö —Ä–Ķ—Ü–ł–ī–ł–≤–ĺ–≤ —ā–Ķ—Ö –ł–Ľ–ł –ł–Ĺ—č—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ, –≤ —á–į—Ā—ā–Ĺ–ĺ—Ā—ā–ł –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–Ļ –ľ–ĺ—á–Ķ–≤—č–≤–ĺ–ī—Ź—Č–ł—Ö –Ņ—É—ā–Ķ–Ļ –ł –Ī–į–ļ—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –≤–į–≥–ł–Ĺ–ĺ–∑–į –ė–ľ–Ķ–Ĺ–Ĺ–ĺ —ā–į–ļ–ĺ–Ķ —Ā–ĺ—á–Ķ—ā–į–Ĺ–ł–Ķ –Ĺ–į–Ī–Ľ—é–ī–į—é—ā —É 83% –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö —Ā —á–į—Ā—ā–ĺ —Ä–Ķ—Ü–ł–ī–ł–≤–ł—Ä—É—é—Č–Ķ–Ļ —Ą–ĺ—Ä–ľ–ĺ–Ļ –Ī–į–ļ—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –≤–į–≥–ł–Ĺ–ĺ–∑–į [10]. –ü—Ä–ł —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–ľ —ā–Ķ—á–Ķ–Ĺ–ł–ł –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź –Ĺ–į—Ä—Ź–ī—É —Ā —ć–ļ—Ā—Ā—É–ī–į—ā–ł–≤–Ĺ—č–ľ–ł –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź–ľ–ł –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ—Ź—é—ā—Ā—Ź –Ņ—Ä–ĺ–Ľ–ł—Ą–Ķ—Ä–į—ā–ł–≤–Ĺ—č–Ķ –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź: –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ķ –ł–Ĺ—Ą–ł–Ľ—Ć—ā—Ä–į—ā—č –≤ —Ā—É–Ī—ć–Ņ–ł—ā–Ķ–Ľ–ł–į–Ľ—Ć–Ĺ–ĺ–ľ —Ā–Ľ–ĺ–Ķ, —Ü–ł–Ľ–ł–Ĺ–ī—Ä–ł—á–Ķ—Ā–ļ–ł–Ļ —ć–Ņ–ł—ā–Ķ–Ľ–ł–Ļ –Ĺ–į –ĺ—ā–ī–Ķ–Ľ—Ć–Ĺ—č—Ö —É—á–į—Ā—ā–ļ–į—Ö —ā—Ä–į–Ĺ—Ā—Ą–ĺ—Ä–ľ–ł—Ä—É–Ķ—ā—Ā—Ź –≤ –ľ–Ĺ–ĺ–≥–ĺ—Ā–Ľ–ĺ–Ļ–Ĺ—č–Ļ –Ņ–Ľ–ĺ—Ā–ļ–ł–Ļ –ł, –Ĺ–Ķ—Ä–Ķ–ī–ļ–ĺ, –≤ –ĺ—Ä–ĺ–≥–ĺ–≤–Ķ–≤–į—é—Č–ł–Ļ, –ł—Ā—Ö–ĺ–ī–ĺ–ľ —á–Ķ–≥–ĺ –ľ–ĺ–∂–Ķ—ā —Ā—ā–į—ā—Ć —Ä—É–Ī—Ü–ĺ–≤–į—Ź –į—ā—Ä–ĺ—Ą–ł—Ź —ā–ļ–į–Ĺ–ł [4].
–Ě–į —Ā–Ķ–≥–ĺ–ī–Ĺ—Ź—ą–Ĺ–ł–Ļ –ī–Ķ–Ĺ—Ć —Ā—É—Č–Ķ—Ā—ā–≤—É–Ķ—ā –Ĺ–Ķ—Ā–ļ–ĺ–Ľ—Ć–ļ–ĺ –ĺ—Ā–Ĺ–ĺ–≤–ĺ–Ņ–ĺ–Ľ–į–≥–į—é—Č–ł—Ö –ī–ĺ–ļ—É–ľ–Ķ–Ĺ—ā–ĺ–≤, —Ä–Ķ–≥–Ľ–į–ľ–Ķ–Ĺ—ā–ł—Ä—É—é—Č–ł—Ö —ā–į–ļ—ā–ł–ļ—É –≤–Ķ–ī–Ķ–Ĺ–ł—Ź –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā —É—Ä–ĺ–≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ—č–ľ–ł –ł–Ĺ—Ą–Ķ–ļ—Ü–ł—Ź–ľ–ł: –Ņ—Ä–ł–ļ–į–∑—č –ú–ł–Ĺ-–∑–ī—Ä–į–≤–į –†–ĺ—Ā—Ā–ł–ł –ĺ—ā 1 –Ĺ–ĺ—Ź–Ī—Ä—Ź 2012 –≥. ¬ę–ě–Ī —É—ā–≤–Ķ—Ä–∂–ī–Ķ–Ĺ–ł–ł –ü–ĺ—Ä—Ź–ī–ļ–į –ĺ–ļ–į–∑–į–Ĺ–ł—Ź –ľ–Ķ–ī–ł—Ü–ł–Ĺ—Ā–ļ–ĺ–Ļ –Ņ–ĺ–ľ–ĺ—Č–ł –Ņ–ĺ –Ņ—Ä–ĺ—Ą–ł–Ľ—é ¬ę–į–ļ—É—ą–Ķ—Ä—Ā—ā–≤–ĺ –ł –≥–ł–Ĺ–Ķ–ļ–ĺ–Ľ–ĺ–≥–ł—Ź (–∑–į –ł—Ā–ļ–Ľ—é—á–Ķ–Ĺ–ł–Ķ–ľ –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł—Ź –≤—Ā–Ņ–ĺ–ľ–ĺ–≥–į—ā–Ķ–Ľ—Ć–Ĺ—č—Ö —Ä–Ķ–Ņ—Ä–ĺ–ī—É–ļ—ā–ł–≤–Ĺ—č—Ö —ā–Ķ—Ö–Ĺ–ĺ–Ľ–ĺ–≥–ł–Ļ) ¬Ľ (—Ā –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź–ľ–ł –Ĺ–į 21 —Ą–Ķ–≤—Ä–į–Ľ—Ź 2020 –≥.), –ĺ—ā 15 –Ĺ–ĺ—Ź–Ī—Ä—Ź 2012 –≥. ‚ĄĖ 924–Ĺ ¬ę–ě–Ī —É—ā–≤–Ķ—Ä–∂–ī–Ķ–Ĺ–ł–ł –ü–ĺ—Ä—Ź–ī–ļ–į –ĺ–ļ–į–∑–į–Ĺ–ł—Ź –ľ–Ķ–ī–ł—Ü–ł–Ĺ—Ā–ļ–ĺ–Ļ –Ņ–ĺ–ľ–ĺ—Č–ł –Ĺ–į—Ā–Ķ–Ľ–Ķ–Ĺ–ł—é –Ņ–ĺ –Ņ—Ä–ĺ—Ą–ł–Ľ—é ¬ę–ī–Ķ—Ä–ľ–į—ā–ĺ–≤–Ķ–Ĺ–Ķ—Ä–ĺ–Ľ–ĺ–≥–ł—Ź¬Ľ. –ö—Ä–ĺ–ľ–Ķ —ā–ĺ–≥–ĺ, —Ä–į–∑—Ä–į–Ī–ĺ—ā–į–Ĺ—č –ł –≤–Ĺ–Ķ–ī—Ä–Ķ–Ĺ—č –≤ –Ņ—Ä–į–ļ—ā–ł–ļ—É –ö–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ķ —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–į—Ü–ł–ł –Ņ–ĺ –≤–Ķ–ī–Ķ–Ĺ–ł—é –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –ė–ü–ü–ü –ł —É—Ä–ĺ–≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ—č–ľ–ł –ł–Ĺ—Ą–Ķ–ļ—Ü–ł—Ź–ľ–ł (2017). –í —ć—ā–ł—Ö –ī–ĺ–ļ—É–ľ–Ķ–Ĺ—ā–į—Ö –ĺ—ā—Ä–į–∂–Ķ–Ĺ–į —ā–į–ļ—ā–ł–ļ–į –ī–Ķ–Ļ—Ā—ā–≤–ł—Ź –≤—Ä–į—á–į –≤ —Ā–Ľ—É—á–į–Ķ —Ā—ā–į–Ĺ–ī–į—Ä—ā–Ĺ—č—Ö —Ā–ł—ā—É–į—Ü–ł–Ļ ‚ÄĒ –≤ –ĺ—Ā–Ĺ–ĺ–≤–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–Ļ, –≤—č–∑–≤–į–Ĺ–Ĺ—č—Ö –ĺ–Ī–Ľ–ł–≥–į—ā–Ĺ—č–ľ–ł –ł–Ľ–ł —É—Ā–Ľ–ĺ–≤–Ĺ–ĺ-–Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ĺ—č–ľ–ł –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–į–ľ–ł, –Ľ–Ķ–∂–ł—ā —ć—ā–ł–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–į—Ź —ā–Ķ—Ä–į–Ņ–ł—Ź. –ė–ľ–Ķ–Ĺ–Ĺ–ĺ –Ĺ–į–Ľ–ł—á–ł–Ķ –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–į —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –ĺ—Ā–Ĺ–ĺ–≤–į–Ĺ–ł–Ķ–ľ –ī–Ľ—Ź –Ĺ–į–∑–Ĺ–į—á–Ķ–Ĺ–ł—Ź –į–Ĺ—ā–ł–Ī–į–ļ—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł –Ņ—Ä–ł –≤—č—Ź–≤–Ľ–Ķ–Ĺ–ł–ł —É—Ā–Ľ–ĺ–≤–Ĺ–ĺ-–Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ĺ—č—Ö –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–ĺ–≤ [2, 16, 17].
–ě–ī–Ĺ–į–ļ–ĺ –Ī–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–ĺ –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č—Ö –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤, –Ņ—Ä–ł–ľ–Ķ–Ĺ—Ź–Ķ–ľ—č—Ö –≤ –Ľ–Ķ—á–Ķ–Ĺ–ł–ł —É—Ä–ĺ–≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ—č—Ö –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–Ļ, —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ—č –Ņ—Ä–ł –Ĺ–Ķ–ĺ—Ā–Ľ–ĺ–∂–Ĺ–Ķ–Ĺ–Ĺ—č—Ö –ł–Ľ–ł –ĺ—Ā—ā—Ä—č—Ö –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–į—Ö –í —Ā–Ľ—É—á–į–Ķ –∂–Ķ —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —Ä–Ķ—Ü–ł–ī–ł–≤–ł—Ä—É—é—Č–Ķ–≥–ĺ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–į –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ—č –ł–Ĺ—č–Ķ –Ņ–ĺ–ī—Ö–ĺ–ī—č, –≤ —á–į—Ā—ā–Ĺ–ĺ—Ā—ā–ł, –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ –Ľ–ĺ–ļ–į–Ľ—Ć–Ĺ–ĺ–Ļ –ł–ľ–ľ—É–Ĺ–ĺ–ļ–ĺ—Ä—Ä–Ķ–ļ—Ü–ł–ł —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –≤–Ķ—Ā—Ć–ľ–į –ĺ–Ī–Ĺ–į–ī–Ķ–∂–ł–≤–į—é—Č–ł–ľ –ľ–Ķ—ā–ĺ–ī–ĺ–ľ –Ņ—Ä–Ķ-–ĺ–ī–ĺ–Ľ–Ķ–Ĺ–ł—Ź —ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–ł—á–Ķ—Ā–ļ–ł—Ö –Ĺ–Ķ—É–ī–į—á [18‚Äď20]. –ė—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ –Ľ–ĺ–ļ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ł–ľ–ľ—É–Ĺ–ĺ—ā—Ä–ĺ–Ņ–Ĺ–ĺ–≥–ĺ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –ĺ–Ņ—ā–ł–ľ–į–Ľ—Ć–Ĺ—č–ľ, —ā–į–ļ –ļ–į–ļ –ĺ—Ā–Ĺ–ĺ–≤–Ĺ—č–Ķ —Ā–ĺ–Ī—č—ā–ł—Ź —Ä–į–∑–≤–ł–≤–į—é—ā—Ā—Ź –Ĺ–į —Ā–Ľ–ł–∑–ł—Ā—ā–ĺ–Ļ –ĺ–Ī–ĺ–Ľ–ĺ—á–ļ–Ķ –≤–Ľ–į–≥–į–Ľ–ł—Č–į [12, 18, 19]. –ü—Ä–Ķ–Ņ–į—Ä–į—ā –ü–ĺ–Ľ–ł–ĺ–ļ—Ā–ł–ī–ĺ–Ĺ–ł–Ļ¬ģ (–į–∑–ĺ–ļ—Ā–ł–ľ–Ķ—Ä–į –Ī—Ä–ĺ–ľ–ł–ī) (–ě–ě–ě –Ě–ü–ě ¬ę–ü–Ķ—ā—Ä–ĺ–≤–į–ļ—Ā –§–į—Ä–ľ¬Ľ) —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –ł–ľ–ľ—É–Ĺ–ĺ–ľ–ĺ–ī—É–Ľ–ł—Ä—É—é—Č–ł–ľ, –ī–Ķ—ā–ĺ–ļ—Ā–ł—Ü–ł—Ä—É—é—Č–ł–ľ, –į–Ĺ—ā–ł–ĺ–ļ—Ā–ł–ī–į–Ĺ—ā–Ĺ—č–ľ —Ā—Ä–Ķ–ī—Ā—ā–≤–ĺ–ľ. –ü—Ä–Ķ–Ņ–į—Ä–į—ā –≤—č–Ņ—É—Ā–ļ–į–Ķ—ā—Ā—Ź –≤ —Ą–ĺ—Ä–ľ–Ķ —ā–į–Ī–Ľ–Ķ—ā–ĺ–ļ (12 –ľ–≥ –į–∑–ĺ–ļ—Ā–ł–ľ–Ķ—Ä–į –Ī—Ä–ĺ–ľ–ł–ī), –Ľ–ł–ĺ—Ą–ł–Ľ–ł–∑–į—ā–į –ī–Ľ—Ź –Ņ—Ä–ł–≥–ĺ—ā–ĺ–≤–Ľ–Ķ–Ĺ–ł—Ź —Ä–į—Ā—ā–≤–ĺ—Ä–į –ī–Ľ—Ź –ł–Ĺ—ä–Ķ–ļ—Ü–ł–Ļ –ł –ľ–Ķ—Ā—ā–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź (1 –į–ľ–Ņ—É–Ľ–į –ł–Ľ–ł —Ą–Ľ–į–ļ–ĺ–Ĺ —Ā–ĺ–ī–Ķ—Ä–∂–ł—ā 3 –ľ–≥ –į–∑–ĺ–ļ—Ā–ł–ľ–Ķ—Ä–į –Ī—Ä–ĺ–ľ–ł–ī–į), —Ā—É–Ņ–Ņ–ĺ–∑–ł—ā–ĺ—Ä–ł–Ķ–≤ (–Ņ–ĺ 6 –ł 12 –ľ–≥ –į–∑–ĺ–ļ—Ā–ł–ľ–Ķ—Ä–į –Ī—Ä–ĺ–ľ–ł–ī–į). –ü–ĺ–ļ–į–∑–į–Ĺ–ł—Ź–ľ–ł –ļ –Ĺ–į–∑–Ĺ–į—á–Ķ–Ĺ–ł—é –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į —Ź–≤–Ľ—Ź—é—ā—Ā—Ź —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ķ —Ä–Ķ—Ü–ł–ī–ł–≤–ł—Ä—É—é—Č–ł–Ķ –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ķ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź –Ľ—é–Ī–ĺ–Ļ —ć—ā–ł–ĺ–Ľ–ĺ–≥–ł–ł, –Ĺ–Ķ –Ņ–ĺ–ī–ī–į—é—Č–ł–Ķ—Ā—Ź —Ā—ā–į–Ĺ–ī–į—Ä—ā–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł, –ĺ—Ā—ā—Ä—č–Ķ –ł —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ķ –Ī–į–ļ—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ—č–Ķ –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ł (–≤ —ā. —á. —É—Ä–Ķ—ā—Ä–ł—ā, —Ü–ł—Ā—ā–ł—ā, —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ļ —Ā–į–Ľ—Ć–Ņ–ł–Ĺ–≥–ĺ–ĺ—Ą–ĺ—Ä–ł—ā, —ć–Ĺ–ī–ĺ–ľ–Ķ—ā—Ä–ł—ā, –≤–į–≥–ł–Ĺ–ł—ā, –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź, –≤—č–∑–≤–į–Ĺ–Ĺ—č–Ķ –≤–ł—Ä—É—Ā–ĺ–ľ –Ņ–į–Ņ–ł–Ľ–Ľ–ĺ–ľ—č —á–Ķ–Ľ–ĺ–≤–Ķ–ļ–į). –ü–ĺ–Ľ–ł–ĺ–ļ—Ā–ł–ī–ĺ–Ĺ–ł–Ļ¬ģ –ł–ľ–Ķ–Ķ—ā –≤—č—Ā–ĺ–ļ—É—é (70%) –Ī–ł–ĺ–ī–ĺ—Ā—ā—É–Ņ–Ĺ–ĺ—Ā—ā—Ć, —É–≤–Ķ–Ľ–ł—á–ł–≤–į–Ķ—ā —Ä–Ķ–∑–ł—Ā—ā–Ķ–Ĺ—ā–Ĺ–ĺ—Ā—ā—Ć –ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–į –≤ –ĺ—ā–Ĺ–ĺ—ą–Ķ–Ĺ–ł–ł –Ī–į–ļ—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ—č—Ö, –≥—Ä–ł–Ī–ļ–ĺ–≤—č—Ö –ł –≤–ł—Ä—É—Ā–Ĺ—č—Ö –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–Ļ; –≤–ĺ—Ā—Ā—ā–į–Ĺ–į–≤–Ľ–ł–≤–į–Ķ—ā –ł–ľ–ľ—É–Ĺ–Ĺ—č–Ķ —Ä–Ķ–į–ļ—Ü–ł–ł –Ņ—Ä–ł –≤—ā–ĺ—Ä–ł—á–Ĺ—č—Ö –ł–ľ–ľ—É–Ĺ–ĺ–ī–Ķ—Ą–ł—Ü–ł—ā–Ĺ—č—Ö —Ā–ĺ—Ā—ā–ĺ—Ź–Ĺ–ł—Ź—Ö, –≤—č–∑–≤–į–Ĺ–Ĺ—č—Ö –ł–Ĺ—Ą–Ķ–ļ—Ü–ł—Ź–ľ–ł, –Ņ—Ä–ł —ć—ā–ĺ–ľ –ľ–Ķ—Ö–į–Ĺ–ł–∑–ľ –ł–ľ–ľ—É–Ĺ–ĺ–ľ–ĺ–ī—É–Ľ–ł—Ä—É—é—Č–Ķ–≥–ĺ –ī–Ķ–Ļ—Ā—ā–≤–ł—Ź –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į –∑–į–ļ–Ľ—é—á–į–Ķ—ā—Ā—Ź –≤ –Ņ—Ä—Ź–ľ–ĺ–ľ –≤–Ľ–ł—Ź–Ĺ–ł–ł –Ĺ–į —Ą–į–≥–ĺ—Ü–ł—ā–ł—Ä—É—é—Č–ł–Ķ –ļ–Ľ–Ķ—ā–ļ–ł –ł NK-–ļ–Ľ–Ķ—ā–ļ–ł, –į —ā–į–ļ–∂–Ķ —Ā—ā–ł–ľ—É–Ľ—Ź—Ü–ł–ł –į–Ĺ—ā–ł—ā–Ķ–Ľ–ĺ–ĺ–Ī—Ä–į–∑–ĺ–≤–į–Ĺ–ł—Ź –ü—Ä–Ķ–Ņ–į—Ä–į—ā –ĺ–Ī–Ľ–į–ī–į–Ķ—ā –≤—č—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ–Ļ –ī–Ķ—ā–ĺ–ļ—Ā–ł—Ü–ł—Ä—É—é—Č–Ķ–Ļ –ł –į–Ĺ—ā–ł–ĺ–ļ—Ā–ł–ī–į–Ĺ—ā–Ĺ–ĺ–Ļ –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć—é, –Ņ–ĺ–≤—č—ą–į–Ķ—ā —É—Ā—ā–ĺ–Ļ—á–ł–≤–ĺ—Ā—ā—Ć –ľ–Ķ–ľ–Ī—Ä–į–Ĺ –ļ–Ľ–Ķ—ā–ĺ–ļ –ļ —Ü–ł—ā–ĺ—ā–ĺ–ļ—Ā–ł—á–Ķ—Ā–ļ–ĺ–ľ—É –ī–Ķ–Ļ—Ā—ā–≤–ł—é –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č—Ö –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –ł —Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ł—Ö –≤–Ķ—Č–Ķ—Ā—ā–≤, —Ā–Ĺ–ł–∂–į–Ķ—ā –ł—Ö —ā–ĺ–ļ—Ā–ł—á–Ĺ–ĺ—Ā—ā—Ć. –ü—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ –Ņ–ĺ–Ľ–ł–ĺ–ļ—Ā–ł–ī–ĺ–Ĺ–ł—Ź¬ģ –≤ –ļ–ĺ–ľ–Ņ–Ľ–Ķ–ļ—Ā–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł –Ņ–ĺ–∑–≤–ĺ–Ľ—Ź–Ķ—ā –Ņ–ĺ–≤—č—Ā–ł—ā—Ć —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –ł —Ā–ĺ–ļ—Ä–į—ā–ł—ā—Ć –Ņ—Ä–ĺ–ī–ĺ–Ľ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā—Ć –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź, –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ —É–ľ–Ķ–Ĺ—Ć—ą–ł—ā—Ć –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ –į–Ĺ—ā–ł–Ī–į–ļ—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ—č—Ö –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –ł —É–ī–Ľ–ł–Ĺ–ł—ā—Ć —Ā—Ä–ĺ–ļ —Ä–Ķ–ľ–ł—Ā—Ā–ł–ł [21].
–ö–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ķ –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł–Ķ ‚ĄĖ 1
–ü–į—Ü–ł–Ķ–Ĺ—ā–ļ–į –ź, 25 –Ľ–Ķ—ā, –Ņ—Ä–Ķ–ī—ä—Ź–≤–Ľ—Ź–Ķ—ā –∂–į–Ľ–ĺ–Ī—č –Ĺ–į –Ņ–ĺ—Ā—ā–ĺ—Ź–Ĺ–Ĺ—č–Ķ –≤—č–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź –ł–∑ –≤–Ľ–į–≥–į–Ľ–ł—Č–į, –ī–ł—Ā–ļ–ĺ–ľ—Ą–ĺ—Ä—ā –Ņ—Ä–ł –Ņ–ĺ–Ľ–ĺ–≤—č—Ö –ļ–ĺ–Ĺ—ā–į–ļ—ā–į—Ö, –ĺ—Č—É—Č–Ķ–Ĺ–ł–Ķ —Ā—É—Ö–ĺ—Ā—ā–ł –≤–ĺ –≤–Ľ–į–≥–į–Ľ–ł—Č–Ķ. –Ď–ĺ–Ľ—Ć–Ĺ–į –Ī–ĺ–Ľ–Ķ–Ķ 2 –Ľ–Ķ—ā. –ó–į –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–ł–Ļ –≥–ĺ–ī –ĺ–Ņ–ł—Ā–į–Ĺ–Ĺ—č–Ķ —Ā–ł–ľ–Ņ—ā–ĺ–ľ—č —Ä–Ķ–∑–ļ–ĺ –≤–ĺ–∑–Ĺ–ł–ļ–į–Ľ–ł –Ĺ–Ķ –ľ–Ķ–Ĺ–Ķ–Ķ 4 —Ä–į–∑, –ł –Ņ—Ä–į–ļ—ā–ł—á–Ķ—Ā–ļ–ł –Ņ–ĺ—Ā—ā–ĺ—Ź–Ĺ–Ĺ–ĺ –ĺ—ā–ľ–Ķ—á–į–Ķ—ā—Ā—Ź –ī–ł—Ā–ļ–ĺ–ľ—Ą–ĺ—Ä—ā –≤–ĺ –≤–Ľ–į–≥–į–Ľ–ł—Č–Ķ, —á—ā–ĺ —Ā—É—Č–Ķ—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ –≤–Ľ–ł—Ź–Ķ—ā –Ĺ–į –ļ–į—á–Ķ—Ā—ā–≤–ĺ –∂–ł–∑–Ĺ–ł. –ü—Ä–ł –Ņ–Ķ—Ä–≤–ł—á–Ĺ–ĺ–ľ –ĺ–Ī—Ä–į—Č–Ķ–Ĺ–ł–ł –ļ –≤—Ä–į—á—É –Ī—č–Ľ –≤—č—Ā—ā–į–≤–Ľ–Ķ–Ĺ –ī–ł–į–≥–Ĺ–ĺ–∑: —Ü–Ķ—Ä–≤–ł—Ü–ł—ā, –į—Ā—Ā–ĺ—Ü–ł–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–Ļ —Ā —É—Ä–Ķ–į–Ņ–Ľ–į–∑–ľ–Ķ–Ĺ–Ĺ–ĺ–Ļ –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–Ķ–Ļ, –≤—É–Ľ—Ć–≤–ĺ–≤–į–≥–ł–Ĺ–į–Ľ—Ć–Ĺ—č–Ļ –ļ–į–Ĺ–ī–ł–ī–ĺ–∑. –Ď—č–Ľ –Ĺ–į–∑–Ĺ–į—á–Ķ–Ĺ –ī–∂–ĺ–∑–į–ľ–ł—Ü–ł–Ĺ –Ņ–ĺ 500 –ľ–≥ —ā—Ä–ł–∂–ī—č –≤ –ī–Ķ–Ĺ—Ć ‚ĄĖ 10, —Ą–Ľ—É–ļ–ĺ–Ĺ–į–∑–ĺ–Ľ 150 –ľ–≥ –ĺ–ī–Ĺ–ĺ–ļ—Ä–į—ā–Ĺ–ĺ. –ü–ĺ—Ā–Ľ–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –ĺ—ā–ľ–Ķ—ā–ł–Ľ–į –Ĺ–Ķ–∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ —É–Ľ—É—á—ą–Ķ–Ĺ–ł–Ķ. –ß–Ķ—Ä–Ķ–∑ –ľ–Ķ—Ā—Ź—Ü —Ā–ł–ľ–Ņ—ā–ĺ–ľ—č –≤–ĺ–∑–ĺ–Ī–Ĺ–ĺ–≤–ł–Ľ–ł—Ā—Ć –Ē–į–Ľ–Ķ–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ļ–į —Ā–į–ľ–ĺ—Ā—ā–ĺ—Ź—ā–Ķ–Ľ—Ć–Ĺ–ĺ –Ņ—Ä–ł–Ĺ–ł–ľ–į–Ľ–į –į–Ĺ—ā–ł–Ī–į–ļ—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ—č–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā—č, —ć—É–Ī–ł–ĺ—ā–ł–ļ–ł, –≤–į–≥–ł–Ĺ–į–Ľ—Ć–Ĺ—č–Ķ —Ā–≤–Ķ—á–ł —Ā –į–Ĺ—ā–ł–ľ–ł–ļ–ĺ—ā–ł–ļ–ĺ–ľ. –ó–į –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–ł–Ļ –≥–ĺ–ī –Ĺ–į–∑–Ĺ–į—á–į–Ľ–ł—Ā—Ć —ā—Ä–ł –ļ—É—Ä—Ā–į –į–Ĺ—ā–ł–Ī–į–ļ—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł, –Ľ–ĺ–ļ–į–Ľ—Ć–Ĺ–ĺ –į–Ĺ—ā–ł—Ā–Ķ–Ņ—ā–ł–ļ–ł, —ć—É–Ī–ł–ĺ—ā–ł–ļ–ł –Ņ–Ķ—Ä–ĺ—Ä–į–Ľ—Ć–Ĺ–ĺ –≠—Ą—Ą–Ķ–ļ—ā –ĺ—ā —ā–Ķ—Ä–į–Ņ–ł–ł —Ā–ĺ—Ö—Ä–į–Ĺ—Ź–Ľ—Ā—Ź –Ĺ–Ķ –Ī–ĺ–Ľ–Ķ–Ķ –ľ–Ķ—Ā—Ź—Ü–į. –ü–į—Ü–ł–Ķ–Ĺ—ā–ļ–į –ĺ—á–Ķ–Ĺ—Ć —ć–ľ–ĺ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ–ĺ –≤–ĺ—Ā–Ņ—Ä–ł–Ĺ–ł–ľ–į–Ķ—ā —Ā–≤–ĺ–Ķ —Ā–ĺ—Ā—ā–ĺ—Ź–Ĺ–ł–Ķ –ł —Ā—á–ł—ā–į–Ķ—ā, —á—ā–ĺ —Ā—ā—Ä–Ķ—Ā—Ā–ĺ–≤—č–Ķ —Ā–ł—ā—É–į—Ü–ł–ł –Ņ—Ä–ĺ–≤–ĺ—Ü–ł—Ä—É—é—ā –ĺ–Ī–ĺ—Ā—ā—Ä–Ķ–Ĺ–ł–Ķ.
–ė–∑ –į–Ĺ–į–ľ–Ĺ–Ķ–∑–į: –ī–Ķ—ā—Ā–ļ–ł–Ķ –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ł, —Ä–Ķ—Ü–ł–ī–ł–≤–ł—Ä—É—é—Č–ł–Ļ —Ü–ł—Ā—ā–ł—ā, —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ļ —ā–ĺ–Ĺ–∑–ł–Ľ–Ľ–ł—ā –ú–Ķ–Ĺ—Ā—ā—Ä—É–į—Ü–ł–ł —Ā 12 –Ľ–Ķ—ā, —Ä–Ķ–≥—É–Ľ—Ź—Ä–Ĺ—č–Ķ, –Ī–Ķ–∑–Ī–ĺ–Ľ–Ķ–∑–Ĺ–Ķ–Ĺ–Ĺ—č–Ķ, –ľ–Ķ–Ĺ—Ā—ā—Ä—É–į–Ľ—Ć–Ĺ—č–Ļ —Ü–ł–ļ–Ľ 26 –ī–Ĺ–Ķ–Ļ. –ü–ĺ–Ľ–ĺ–≤–į—Ź –∂–ł–∑–Ĺ—Ć —Ā 18 –Ľ–Ķ—ā, –≤ –Ī—Ä–į–ļ–Ķ.
–†–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź. –ü–ĺ –ī–į–Ĺ–Ĺ—č–ľ –ĺ—Ā–ľ–ĺ—ā—Ä–į, –Ĺ–į—Ä—É–∂–Ĺ—č–Ķ –Ņ–ĺ–Ľ–ĺ–≤—č–Ķ –ĺ—Ä–≥–į–Ĺ—č —Ā—Ą–ĺ—Ä–ľ–ł—Ä–ĺ–≤–į–Ĺ—č –Ņ—Ä–į–≤–ł–Ľ—Ć–Ĺ–ĺ, —Ä–ĺ—Ā—ā –≤–ĺ–Ľ–ĺ—Ā –Ņ–ĺ –∂–Ķ–Ĺ—Ā–ļ–ĺ–ľ—É —ā–ł–Ņ—É. –ě—ā–ľ–Ķ—á–į–Ķ—ā—Ā—Ź —É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ–į—Ź –≥–ł–Ņ–Ķ—Ä–Ķ–ľ–ł—Ź –≤—É–Ľ—Ć–≤—č. –ď—É–Ī–ļ–ł —É—Ä–Ķ—ā—Ä—č –Ĺ–Ķ—Ā–ļ–ĺ–Ľ—Ć–ļ–ĺ –ĺ—ā–Ķ—á–Ĺ—č, —Ā—ā–Ķ–Ĺ–ļ–į –ľ–ĺ—á–Ķ–ł—Ā–Ņ—É—Ā–ļ–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ļ–į–Ĺ–į–Ľ–į –Ņ–į—Ā—ā–ĺ–∑–Ĺ–į, –Ņ—Ä–ł –Ņ–į–Ľ—Ć–Ņ–į—Ü–ł–ł –≤—č–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź —Ā–Ľ–ł–∑–ł—Ā—ā—č–Ķ –≤ –Ĺ–Ķ–∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–ľ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–Ķ. –°–Ľ–ł–∑–ł—Ā—ā–į—Ź –ĺ–Ī–ĺ–Ľ–ĺ—á–ļ–į –≤–Ľ–į–≥–į–Ľ–ł—Č–į –∑–į—Ā—ā–ĺ–Ļ–Ĺ–ĺ-–ļ—Ä–į—Ā–Ĺ–ĺ–≥–ĺ —Ü–≤–Ķ—ā–į, –≤—č—Ä–į–∂–Ķ–Ĺ–į —Ā–ļ–Ľ–į–ī—á–į—ā–ĺ—Ā—ā—Ć, –Ĺ–į –Ņ–ĺ–≤–Ķ—Ä—Ö–Ĺ–ĺ—Ā—ā–ł –ļ—Ä–ĺ—ą–ļ–ĺ–≤–ł–ī–Ĺ—č–Ļ –Ī–Ķ–Ľ–Ķ—Ā–ĺ–≤–į—ā—č–Ļ –Ĺ–į–Ľ–Ķ—ā –≤ —É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ–ĺ–ľ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–Ķ –®–Ķ–Ļ–ļ–į –ľ–į—ā–ļ–ł –ļ–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ —Ą–ĺ—Ä–ľ—č, —Ā —ć–ļ—ā–ĺ–Ņ–ł–Ķ–Ļ —Ü–ł–Ľ–ł–Ĺ–ī—Ä–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —ć–Ņ–ł—ā–Ķ–Ľ–ł—Ź, –≤—č–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź –ł–∑ —Ü–Ķ—Ä–≤–ł–ļ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ļ–į–Ĺ–į–Ľ–į —Ā–Ľ–ł–∑–ł—Ā—ā—č–Ķ, —Ā–Ľ–Ķ–≥–ļ–į –∂–Ķ–Ľ—ā–ĺ–≤–į—ā—č–Ķ (—Ä–ł—Ā. 1–ź). –Ę–Ķ–Ľ–ĺ –ľ–į—ā–ļ–ł ‚ÄĒ –≤ anteflexio, –Ņ–ĺ–ī–≤–ł–∂–Ĺ–ĺ–Ķ, –Ī–Ķ–∑–Ī–ĺ–Ľ–Ķ–∑–Ĺ–Ķ–Ĺ–Ĺ–ĺ–Ķ –Ņ—Ä–ł –Ņ–į–Ľ—Ć–Ņ–į—Ü–ł–ł. –ü—Ä–ł–ī–į—ā–ļ–ł —Ā –ĺ–Ī–Ķ–ł—Ö —Ā—ā–ĺ—Ä–ĺ–Ĺ –Ĺ–Ķ —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ—č, –Ī–Ķ–∑–Ī–ĺ–Ľ–Ķ–∑–Ĺ–Ķ–Ĺ–Ĺ—č.
–ü—Ä–ł –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł —Ā –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ–ľ —ā–Ķ—Ā—ā-—Ā–ł—Ā—ā–Ķ–ľ—č ¬ę–§–Ķ–ľ–ĺ—Ą–Ľ–ĺ—Ä 16¬Ľ –≤—č—Ź–≤–Ľ–Ķ–Ĺ—č: U. urealyticum, C. albicans, E. coli, E. faecalis –≤ –ī–ł–į–≥–Ĺ–ĺ—Ā—ā–ł—á–Ķ—Ā–ļ–ł –∑–Ĺ–į—á–ł–ľ–ĺ–ľ —ā–ł—ā—Ä–Ķ 104 –ö–ě–ē/–ľ–Ľ. –õ–į–ļ—ā–ĺ–Ī–į–ļ—ā–Ķ—Ä–ł–ł –≤ —ā–ł—ā—Ä–Ķ 103 –ö–ě–ē/–ľ–Ľ. –ú–ł–ļ—Ä–ĺ—Ā–ļ–ĺ–Ņ–ł—Ź –ľ–į–∑–ļ–į –ł–∑ —É—Ä–ĺ–≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ —ā—Ä–į–ļ—ā–į –≤—č—Ź–≤–ł–Ľ–į 25 –Ņ–ĺ–Ľ–ł–ľ–ĺ—Ä—Ą–Ĺ–ĺ-—Ź–ī–Ķ—Ä–Ĺ—č—Ö –Ľ–Ķ–Ļ–ļ–ĺ—Ü–ł—ā–ĺ–≤ –≤ –Ņ–ĺ–Ľ–Ķ –∑—Ä–Ķ–Ĺ–ł—Ź, –Ņ–Ľ–į—Ā—ā—č —ć–Ņ–ł—ā–Ķ–Ľ–ł–į–Ľ—Ć–Ĺ—č—Ö –ļ–Ľ–Ķ—ā–ĺ–ļ –ü—Ä–ł —Ü–ł—ā–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ĺ–ľ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł–ł –Ĺ–Ķ –≤—č—Ź–≤–Ľ–Ķ–Ĺ–ĺ. –ü—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ–Ĺ—č–Ļ –≤ —Ä–į–ľ–ļ–į—Ö –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –į–Ĺ–į–Ľ–ł–∑ —Ą–į–ļ—ā–ĺ—Ä–ĺ–≤ –Ľ–ĺ–ļ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ł–ľ–ľ—É–Ĺ–ł—ā–Ķ—ā–į –Ņ–ĺ–ļ–į–∑–į–Ľ —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ĺ–Ķ–Ļ—ā—Ä–ĺ—Ą–ł–Ľ—Ć–Ĺ—č—Ö –≥—Ä–į–Ĺ—É–Ľ–ĺ—Ü–ł—ā–ĺ–≤, —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ —É—Ä–ĺ–≤–Ĺ—Ź –ī–ł—Ą–Ķ–Ĺ—Ā–ł–Ĺ–ĺ–≤, –Ľ–į–ļ—ā–ĺ—Ą–Ķ—Ä—Ä–ł–Ĺ–į, —Ā–Ķ–ļ—Ä–Ķ—ā–ĺ—Ä–Ĺ–ĺ–≥–ĺ –ł–ľ–ľ—É–Ĺ–ĺ–≥–Ľ–ĺ–Ī—É–Ľ–ł–Ĺ–į –ź, –ł–Ĺ—ā–Ķ—Ä—Ą–Ķ—Ä–ĺ–Ĺ–į ő≥, —á—ā–ĺ —Ā–≤–ł–ī–Ķ—ā–Ķ–Ľ—Ć—Ā—ā–≤—É–Ķ—ā –ĺ –≤—č—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ–Ļ –ī–ł—Ā—Ą—É–Ĺ–ļ—Ü–ł–ł –≤ —Ā–ł—Ā—ā–Ķ–ľ–Ķ –Ľ–ĺ–ļ–į–Ľ—Ć–Ĺ–ĺ–Ļ –Ņ—Ä–ĺ—ā–ł–≤–ĺ–ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–Ļ –∑–į—Č–ł—ā—č.
–Ē–ł–į–≥–Ĺ–ĺ–∑: N72.0 + –ź.63.8 –¶–Ķ—Ä–≤–ł—Ü–ł—ā, –≤—č–∑–≤–į–Ĺ–Ĺ—č–Ļ U. urealyticum. –í37.3 –ö–į–Ĺ–ī–ł–ī–ĺ–∑–Ĺ—č–Ļ –≤—É–Ľ—Ć–≤–ĺ–≤–į–≥–ł–Ĺ–ł—ā. –ź—ć—Ä–ĺ–Ī–Ĺ—č–Ļ –≤–į–≥–ł–Ĺ–ł—ā.
–ź—ć—Ä–ĺ–Ī–Ĺ—č–Ļ –≤–į–≥–ł–Ĺ–ł—ā ‚ÄĒ —Ā–ĺ—Ā—ā–ĺ—Ź–Ĺ–ł–Ķ, –ĺ–Ī—É—Ā–Ľ–ĺ–≤–Ľ–Ķ–Ĺ–Ĺ–ĺ–Ķ —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ–ľ –Ņ—É–Ľ–į –Ľ–į–ļ—ā–ĺ–Ī–į—Ü–ł–Ľ–Ľ –ł —Ä–į–∑–≤–ł—ā–ł–Ķ–ľ –≤–ĺ—Ā–Ņ–į–Ľ–Ķ–Ĺ–ł—Ź –Ņ—Ä–ł —É—á–į—Ā—ā–ł–ł –į—ć—Ä–ĺ–Ī–Ĺ—č—Ö —É—Ā–Ľ–ĺ–≤–Ĺ–ĺ-–Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ĺ—č—Ö –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–ĺ–≤:
E. coli, E. faecalis, S. viridans, S. epidermidis, S. agalactiae, S. –įureus, –Ķ–≥–ĺ —Ā–ł–ľ–Ņ—ā–ĺ–ľ—č –∑–į–≤–ł—Ā—Ź—ā –ĺ—ā —ā—Ź–∂–Ķ—Ā—ā–ł –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–į.
–õ–Ķ—á–Ķ–Ĺ–ł–Ķ –ü—Ä–ł–Ĺ–ł–ľ–į—Ź –≤–ĺ –≤–Ĺ–ł–ľ–į–Ĺ–ł–Ķ —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ķ —Ä–Ķ—Ü–ł–ī–ł–≤–ł—Ä—É—é—Č–Ķ–Ķ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–į, –Ĺ–į–Ľ–ł—á–ł–Ķ –ľ–ł–ļ—Ā—ā-–ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ł, –Ĺ–Ķ—ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć —Ä–į–Ĺ–Ķ–Ķ –Ņ—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ–Ĺ–ĺ–Ļ —ć—ā–ł–ĺ—ā—Ä–ĺ–Ņ–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł, –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ļ–Ķ –Ĺ–į–∑–Ĺ–į—á–ł–Ľ–ł —ā–Ķ—Ä–į–Ņ–ł—é –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–ľ –ü–ĺ–Ľ–ł–ĺ–ļ—Ā–ł–ī–ĺ–Ĺ–ł–Ļ¬ģ –≤ —Ā–≤–Ķ—á–į—Ö –≤ –ī–ĺ–∑–ł—Ä–ĺ–≤–ļ–Ķ 12 –ľ–≥ –Ņ–ĺ —Ā—Ö–Ķ–ľ–Ķ: 1 —Ā—É–Ņ–Ņ–ĺ–∑–ł—ā–ĺ—Ä–ł–Ļ –Ķ–∂–Ķ–ī–Ĺ–Ķ–≤–Ĺ–ĺ –ł–Ĺ—ā—Ä–į–≤–į–≥–ł–Ĺ–į–Ľ—Ć–Ĺ–ĺ –≤ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ 3 –ī–Ĺ–Ķ–Ļ, –∑–į—ā–Ķ–ľ 1 —Ā—É–Ņ–Ņ–ĺ–∑–ł—ā–ĺ—Ä–ł–Ļ —á–Ķ—Ä–Ķ–∑ –ī–Ķ–Ĺ—Ć –ĺ–Ī—Č–ł–ľ –ļ—É—Ä—Ā–ĺ–ľ 10 –≤–≤–Ķ–ī–Ķ–Ĺ–ł–Ļ, —Ą–Ľ—É–ļ–ĺ–Ĺ–į–∑–ĺ–Ľ 150 –ľ–≥ –≤ 1, 4, 7, 14-–Ļ –ī–Ĺ–ł —ā–Ķ—Ä–į–Ņ–ł–ł, –Ĺ–į—Ä—É–∂–Ĺ–ĺ —ć–Ņ–ł–≥–Ķ–Ĺ-–≥–Ķ–Ľ—Ć –ī–Ľ—Ź –ł–Ĺ—ā–ł–ľ–Ĺ–ĺ–Ļ –≥–ł–≥–ł–Ķ–Ĺ—č.
–Ě–į –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ć–Ĺ–ĺ–ľ –≤–ł–∑–ł—ā–Ķ —á–Ķ—Ä–Ķ–∑ –ľ–Ķ—Ā—Ź—Ü –Ņ—Ä–ł –ĺ–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ–ĺ–ľ –ĺ—Ā–ľ–ĺ—ā—Ä–Ķ: –Ĺ–į—Ä—É–∂–Ĺ—č–Ķ –Ņ–ĺ–Ľ–ĺ–≤—č–Ķ –ĺ—Ä–≥–į–Ĺ—č –ĺ–Ī—č—á–Ĺ–ĺ–Ļ –ĺ–ļ—Ä–į—Ā–ļ–ł –ď—É–Ī–ļ–ł —É—Ä–Ķ—ā—Ä—č –Ī–Ľ–Ķ–ī–Ĺ–ĺ-—Ä–ĺ–∑–ĺ–≤–ĺ–≥–ĺ —Ü–≤–Ķ—ā–į, –≤—č–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź –ĺ—ā—Ā—É—ā—Ā—ā–≤—É—é—ā. –°–Ľ–ł–∑–ł—Ā—ā–į—Ź –ĺ–Ī–ĺ–Ľ–ĺ—á–ļ–į –≤–Ľ–į–≥–į–Ľ–ł—Č–į —Ä–ĺ–∑–ĺ–≤–ĺ–≥–ĺ —Ü–≤–Ķ—ā–į, –≤—č–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź –≤ –∑–į–ī–Ĺ–Ķ–ľ —Ā–≤–ĺ–ī–Ķ –Ī–Ķ–Ľ–Ķ—Ā–ĺ–≤–į—ā—č–Ķ, –≤ –Ĺ–Ķ–∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–ľ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–Ķ, –Ī–Ķ–∑ –∑–į–Ņ–į—Ö–į. –®–Ķ–Ļ–ļ–į –ľ–į—ā–ļ–ł —Ā —ć–ļ—ā–ĺ–Ņ–ł–Ķ–Ļ —Ü–ł–Ľ–ł–Ĺ–ī—Ä–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —ć–Ņ–ł—ā–Ķ–Ľ–ł—Ź, –≤—č–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź –ł–∑ —Ü–Ķ—Ä–≤–ł–ļ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ļ–į–Ĺ–į–Ľ–į —Ā–Ľ–ł–∑–ł—Ā—ā—č–Ķ, —Ā–ļ—É–ī–Ĺ—č–Ķ (—Ä–ł—Ā. 1B). –ü—Ä–ł –ľ–ł–ļ—Ä–ĺ—Ā–ļ–ĺ–Ņ–ł–ł: –Ņ–ĺ–Ľ–ł–ľ–ĺ—Ä—Ą–Ĺ–ĺ—Ź–ī–Ķ—Ä–Ĺ—č–Ķ –Ľ–Ķ–Ļ–ļ–ĺ—Ü–ł—ā—č 12 –≤ –Ņ–ĺ–Ľ–Ķ –∑—Ä–Ķ–Ĺ–ł—Ź, —ć–Ņ–ł—ā–Ķ–Ľ–ł–į–Ľ—Ć–Ĺ—č–Ķ –ļ–Ľ–Ķ—ā–ļ–ł 3‚Äď5 –≤ –Ņ–ĺ–Ľ–Ķ –∑—Ä–Ķ–Ĺ–ł—Ź –ü—Ä–ł –ü–¶–†-–ī–ł–į–≥–Ĺ–ĺ—Ā—ā–ł–ļ–Ķ: Candida, E. coli, E. faecalis –Ĺ–Ķ –≤—č—Ź–≤–Ľ–Ķ–Ĺ—č, U. urealyticum ‚ÄĒ –≤ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–Ķ 102 –ď–≠–ē. –£—á–ł—ā—č–≤–į—Ź –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł–Ķ –∂–į–Ľ–ĺ–Ī, —Ä–į–∑—Ä–Ķ—ą–Ķ–Ĺ–ł–Ķ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ļ–į—Ä—ā–ł–Ĺ—č, –Ĺ–ĺ—Ä–ľ–į–Ľ–ł–∑–į—Ü–ł—é –ļ–Ľ–ł–Ĺ–ł–ļ–ĺ-–Ľ–į–Ī–ĺ—Ä–į—ā–ĺ—Ä–Ĺ—č—Ö –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–Ķ–Ļ, –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ļ–Ķ —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–ĺ–≤–į–Ľ–ł –ī–ł–Ĺ–į–ľ–ł—á–Ķ—Ā–ļ–ĺ–Ķ –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł–Ķ. –Ě–į –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ć–Ĺ–ĺ–ľ –≤–ł–∑–ł—ā–Ķ —á–Ķ—Ä–Ķ–∑ 6 –ľ–Ķ—Ā. –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ļ–į –∂–į–Ľ–ĺ–Ī –Ĺ–Ķ –Ņ—Ä–Ķ–ī—ä—Ź–≤–Ľ—Ź–Ľ–į, –ļ–Ľ–ł–Ĺ–ł–ļ–ĺ-–Ľ–į–Ī–ĺ—Ä–į—ā–ĺ—Ä–Ĺ—č–Ķ –Ņ—Ä–ł–∑–Ĺ–į–ļ–ł –≤–ĺ—Ā–Ņ–į–Ľ–Ķ–Ĺ–ł—Ź –ĺ—ā—Ā—É—ā—Ā—ā–≤–ĺ–≤–į–Ľ–ł, —á—ā–ĺ –Ī—č–Ľ–ĺ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–Ķ–ľ –ī–ĺ—Ā—ā–ł–∂–Ķ–Ĺ–ł—Ź —Ä–Ķ–ľ–ł—Ā—Ā–ł–ł.

–í –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ–Ķ–Ĺ–Ĺ–ĺ–ľ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–ľ –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ļ–į –ļ–į—ā–Ķ–≥–ĺ—Ä–ł—á–Ķ—Ā–ļ–ł –ĺ—ā–ļ–į–∑–į–Ľ–į—Ā—Ć –Ņ—Ä–ł–Ĺ–ł–ľ–į—ā—Ć –į–Ĺ—ā–ł–Ī–į–ļ—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ—č–Ļ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā, –Ĺ–į—Ā—ā–į–ł–≤–į—ā—Ć –Ĺ–į –Ķ–≥–ĺ –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–ł –Ī—č–Ľ–ĺ –Ĺ–Ķ—Ü–Ķ–Ľ–Ķ—Ā–ĺ–ĺ–Ī—Ä–į–∑–Ĺ–ĺ –£—á–ł—ā—č–≤–į—Ź, —á—ā–ĺ U. urealyticum —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź —É—Ā–Ľ–ĺ–≤–Ĺ–ĺ-–Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ĺ—č–ľ –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–ĺ–ľ, –į –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–į –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ—Ź–Ķ—ā—Ā—Ź –≤—č—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ—Ā—ā—Ć—é –ī–ł—Ā—Ą—É–Ĺ–ļ—Ü–ł–ł –≤ —Ā–ł—Ā—ā–Ķ–ľ–Ķ –Ņ—Ä–ĺ—ā–ł–≤–ĺ–ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–Ļ –∑–į—Č–ł—ā—č –≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ —ā—Ä–į–ļ—ā–į –ł –≥–Ľ—É–Ī–ł–Ĺ–ĺ–Ļ –ī–ł—Ā–Ī–ł–ĺ—ā–ł—á–Ķ—Ā–ļ–ł—Ö –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł–Ļ, –Ņ—Ä–Ķ–ī–Ņ–ĺ–Ľ–ĺ–∂–ł–Ľ–ł, —á—ā–ĺ –į–ļ—ā–ł–≤–į—Ü–ł—Ź –Ľ–ĺ–ļ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ł–ľ–ľ—É–Ĺ–Ĺ–ĺ–≥–ĺ –ĺ—ā–≤–Ķ—ā–į –ľ–ĺ–∂–Ķ—ā —É—Ā—ā—Ä–į–Ĺ–ł—ā—Ć —ć—ā–ł –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł—Ź –ł —Ā–Ņ–ĺ—Ā–ĺ–Ī—Ā—ā–≤–ĺ–≤–į—ā—Ć —Ā—ā–į–Ī–ł–Ľ–ł–∑–į—Ü–ł–ł –ľ–ł–ļ—Ä–ĺ–Ī–ł–ĺ—Ü–Ķ–Ĺ–ĺ–∑–į.
–° –Ĺ–į—ą–Ķ–Ļ —ā–ĺ—á–ļ–ł –∑—Ä–Ķ–Ĺ–ł—Ź, –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į –ü–ĺ–Ľ–ł–ĺ–ļ—Ā–ł–ī–ĺ–Ĺ–ł–Ļ¬ģ –Ņ—Ä–ł–≤–Ķ–Ľ–ĺ –ļ –į–ļ—ā–ł–≤–į—Ü–ł–ł —Ā–ł–Ĺ—ā–Ķ–∑–į –į–Ĺ—ā–ł–ľ–ł–ļ—Ä–ĺ–Ī–Ĺ—č—Ö –Ņ–Ķ–Ņ—ā–ł–ī–ĺ–≤ –Ĺ–Ķ–Ļ—ā—Ä–ĺ—Ą–ł–Ľ—Ć–Ĺ—č–ľ–ł –≥—Ä–į–Ĺ—É–Ľ–ĺ—Ü–ł—ā–į–ľ–ł, —á—ā–ĺ –≤ —Ā–≤–ĺ—é –ĺ—á–Ķ—Ä–Ķ–ī—Ć —Ā–Ņ–ĺ—Ā–ĺ–Ī—Ā—ā–≤–ĺ–≤–į–Ľ–ĺ —É—Ā–ł–Ľ–Ķ–Ĺ–ł—é —Ą–į–≥–ĺ—Ü–ł—ā–į—Ä–Ĺ–ĺ–Ļ –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –ł —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ–Ļ –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ —Ä–Ķ–į–ļ—Ü–ł–ł [12].
–ö–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ķ –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł–Ķ ‚ĄĖ 2
–ü–į—Ü–ł–Ķ–Ĺ—ā–ļ–į –ē., 32 –≥–ĺ–ī–į, –Ņ—Ä–Ķ–ī—ä—Ź–≤–Ľ—Ź–Ķ—ā –∂–į–Ľ–ĺ–Ī—č –Ĺ–į –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ –Ī–ĺ—Ä–ĺ–ī–į–≤–ĺ–ļ –≤ –ĺ–Ī–Ľ–į—Ā—ā–ł –Ņ–ĺ–Ľ–ĺ–≤—č—Ö –ĺ—Ä–≥–į–Ĺ–ĺ–≤, –Ņ–ĺ—Ā—ā–ĺ—Ź–Ĺ–Ĺ—č–Ķ –≤—č–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź –ł–∑ –≤–Ľ–į–≥–į–Ľ–ł—Č–į, –ī–ł—Ā–ļ–ĺ–ľ—Ą–ĺ—Ä—ā –Ņ—Ä–ł –Ņ–ĺ–Ľ–ĺ–≤—č—Ö –ļ–ĺ–Ĺ—ā–į–ļ—ā–į—Ö. –Ď–ĺ–Ľ—Ć–Ĺ–į –Ī–ĺ–Ľ–Ķ–Ķ –Ņ–ĺ–Ľ—É—ā–ĺ—Ä–į –Ľ–Ķ—ā, —Ā —ā–Ķ—Ö –Ņ–ĺ—Ä –ļ–į–ļ –Ĺ–į—á–į–Ľ–ł –Ņ–ĺ—Ź–≤–Ľ—Ź—ā—Ć—Ā—Ź –≤—č—Ā—č–Ņ–į–Ĺ–ł—Ź, –∑–į –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–ł–Ķ 3 –ľ–Ķ—Ā. –ł—Ö –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ —É–≤–Ķ–Ľ–ł—á–ł–Ľ–ĺ—Ā—Ć –≤ 2 —Ä–į–∑–į. –ü—Ä–ł –Ņ–ĺ–Ņ—č—ā–ļ–Ķ —É–ī–į–Ľ–Ķ–Ĺ–ł—Ź –ľ–Ķ—ā–ĺ–ī–ĺ–ľ —ć–Ľ–Ķ–ļ—ā—Ä–ĺ–ļ–ĺ–į–≥—É–Ľ—Ź—Ü–ł–ł –ĺ–ļ–ĺ–Ľ–ĺ 6 –ľ–Ķ—Ā. –Ĺ–į–∑–į–ī —É–Ņ–į–Ľ–į –≤ –ĺ–Ī–ľ–ĺ—Ä–ĺ–ļ –ł —Ā —ā–Ķ—Ö –Ņ–ĺ—Ä –ļ –≤—Ä–į—á—É –Ĺ–Ķ –ĺ–Ī—Ä–į—Č–į–Ľ–į—Ā—Ć.
–ė–∑ –į–Ĺ–į–ľ–Ĺ–Ķ–∑–į: –ī–Ķ—ā—Ā–ļ–ł–Ķ –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ł, —ć–Ņ–ł–Ľ–Ķ–Ņ—Ā–ł—Ź? (—Ā–ĺ —Ā–Ľ–ĺ–≤ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ļ–ł, –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤ –Ĺ–Ķ –Ņ—Ä–ł–Ĺ–ł–ľ–į–Ķ—ā –Ņ–ĺ —ć—ā–ĺ–ľ—É –Ņ–ĺ–≤–ĺ–ī—É), H–°V (–≤ –į–Ĺ–į–ľ–Ĺ–Ķ–∑–Ķ). –ú–Ķ–Ĺ—Ā—ā—Ä—É–į—Ü–ł–ł —Ā 13 –Ľ–Ķ—ā, —Ä–Ķ–≥—É–Ľ—Ź—Ä–Ĺ—č–Ķ, –Ī–Ķ–∑–Ī–ĺ–Ľ–Ķ–∑–Ĺ–Ķ–Ĺ–Ĺ—č–Ķ, –ľ–Ķ–Ĺ—Ā—ā—Ä—É–į–Ľ—Ć–Ĺ—č–Ļ —Ü–ł–ļ–Ľ 30 –ī–Ĺ–Ķ–Ļ. –ü–ĺ–Ľ–ĺ–≤–į—Ź –∂–ł–∑–Ĺ—Ć —Ā 16 –Ľ–Ķ—ā, –≤ –Ī—Ä–į–ļ–Ķ.
–†–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź. –ü–ĺ –ī–į–Ĺ–Ĺ—č–ľ –ĺ—Ā–ľ–ĺ—ā—Ä–į, –Ĺ–į—Ä—É–∂–Ĺ—č–Ķ –Ņ–ĺ–Ľ–ĺ–≤—č–Ķ –ĺ—Ä–≥–į–Ĺ—č —Ā—Ą–ĺ—Ä–ľ–ł—Ä–ĺ–≤–į–Ĺ—č –Ņ—Ä–į–≤–ł–Ľ—Ć–Ĺ–ĺ, —Ä–ĺ—Ā—ā –≤–ĺ–Ľ–ĺ—Ā –Ņ–ĺ –∂–Ķ–Ĺ—Ā–ļ–ĺ–ľ—É —ā–ł–Ņ—É. –í –į–Ĺ–ĺ–≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ–ĺ–Ļ –ĺ–Ī–Ľ–į—Ā—ā–ł –Ī–ĺ–Ľ—Ć—ą–ĺ–Ķ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ –Ī–ĺ—Ä–ĺ–ī–į–≤—á–į—ā—č—Ö –ĺ–Ī—Ä–į–∑–ĺ–≤–į–Ĺ–ł–Ļ —Ä–į–∑–ľ–Ķ—Ä–ĺ–ľ –ī–ĺ 0,3‚Äď0,4 —Ā–ľ, –ļ–ĺ—Ä–ł—á–Ĺ–Ķ–≤–ĺ–≥–ĺ —Ü–≤–Ķ—ā–į, —Ā –ī–ĺ–Ľ—Ć—á–į—ā–ĺ–Ļ —Ā—ā—Ä—É–ļ—ā—É—Ä–ĺ–Ļ, –Ī–Ķ–∑–Ī–ĺ–Ľ–Ķ–∑–Ĺ–Ķ–Ĺ–Ĺ—č—Ö –Ņ—Ä–ł –Ņ–į–Ľ—Ć–Ņ–į—Ü–ł–ł (—Ä–ł—Ā. 2A). –ě—ā–ľ–Ķ—á–į–Ķ—ā—Ā—Ź —É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ–į—Ź –≥–ł–Ņ–Ķ—Ä–Ķ–ľ–ł—Ź –≤—É–Ľ—Ć–≤—č. –ď—É–Ī–ļ–ł —É—Ä–Ķ—ā—Ä—č –Ī–Ķ–∑ –ĺ—Ā–ĺ–Ī–Ķ–Ĺ–Ĺ–ĺ—Ā—ā–Ķ–Ļ. –°–Ľ–ł–∑–ł—Ā—ā–į—Ź –ĺ–Ī–ĺ–Ľ–ĺ—á–ļ–į –≤–Ľ–į–≥–į–Ľ–ł—Č–į —É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ–ĺ –≥–ł–Ņ–Ķ—Ä–Ķ–ľ–ł—Ä–ĺ–≤–į–Ĺ–į, –≤—č–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź –≤ –∑–į–ī–Ĺ–Ķ–ľ —Ā–≤–ĺ–ī–Ķ –Ī–Ķ–Ľ–Ķ—Ā–ĺ–≤–į—ā—č–Ķ, —Ā–ĺ —Ā–Ľ–ł–∑—Ć—é, –Ī–Ķ–∑ –∑–į–Ņ–į—Ö–į –°–Ľ–ł–∑–ł—Ā—ā–į—Ź –ĺ–Ī–ĺ–Ľ–ĺ—á–ļ–į —ą–Ķ–Ļ–ļ–ł –ľ–į—ā–ļ–ł –≥–ł–Ņ–Ķ—Ä–Ķ–ľ–ł—Ä–ĺ–≤–į–Ĺ–į, –≤—č–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź –ł–∑ —Ü–Ķ—Ä–≤–ł–ļ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ļ–į–Ĺ–į–Ľ–į —Ā–Ľ–ł–∑–ł—Ā—ā—č–Ķ, —É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ—č–Ķ.
–Ę–Ķ–Ľ–ĺ –ľ–į—ā–ļ–ł ‚ÄĒ –≤ anteflexio, –Ņ–ĺ–ī–≤–ł–∂–Ĺ–ĺ–Ķ, –Ī–Ķ–∑–Ī–ĺ–Ľ–Ķ–∑–Ĺ–Ķ–Ĺ–Ĺ–ĺ–Ķ –Ņ—Ä–ł –Ņ–į–Ľ—Ć–Ņ–į—Ü–ł–ł. –ü—Ä–ł–ī–į—ā–ļ–ł —Ā –ĺ–Ī–Ķ–ł—Ö —Ā—ā–ĺ—Ä–ĺ–Ĺ –Ĺ–Ķ —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ—č, –Ī–Ķ–∑–Ī–ĺ–Ľ–Ķ–∑–Ĺ–Ķ–Ĺ–Ĺ—č.
–ü—Ä–ł –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł –ľ–Ķ—ā–ĺ–ī–ĺ–ľ –ü–¶–† –≤—č—Ź–≤–Ľ–Ķ–Ĺ—č: G. vaginalis, M. hominis, –í–ü–ß 6-–≥–ĺ –ł 11-–≥–ĺ —ā–ł–Ņ–į. –õ–į–ļ—ā–ĺ–Ī–į–ļ—ā–Ķ—Ä–ł–ł –≤ —ā–ł—ā—Ä–Ķ 102 –ö–ě–ē/–ľ–Ľ. –ú–ł–ļ—Ä–ĺ—Ā–ļ–ĺ–Ņ–ł—Ź –ľ–į–∑–ļ–į –ł–∑ —É—Ä–ĺ–≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ —ā—Ä–į–ļ—ā–į –≤—č—Ź–≤–ł–Ľ–į 12 –Ņ–ĺ–Ľ–ł–ľ–ĺ—Ä—Ą–Ĺ–ĺ-—Ź–ī–Ķ—Ä–Ĺ—č—Ö –Ľ–Ķ–Ļ–ļ–ĺ—Ü–ł—ā–ĺ–≤ –≤ –Ņ–ĺ–Ľ–Ķ –∑—Ä–Ķ–Ĺ–ł—Ź, ¬ę–ļ–Ľ—é—á–Ķ–≤—č–Ķ –ļ–Ľ–Ķ—ā–ļ–ł¬Ľ. –ü—Ä–ł —Ü–ł—ā–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ĺ–ľ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł–ł –Ĺ–Ķ –≤—č—Ź–≤–Ľ–Ķ–Ĺ–ĺ. –Ę–Ķ—Ā—ā –Ĺ–į HCV, HBV, –ė–§–ź –í–ė–ß, —Ā–ł—Ą–ł–Ľ–ł—Ā –ĺ—ā—Ä–ł—Ü–į—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ.
–Ē–ł–į–≥–Ĺ–ĺ–∑: –ź.63.0 –ź–Ĺ–ĺ–≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ—č–Ķ –Ī–ĺ—Ä–ĺ–ī–į–≤–ļ–ł, N89.0 –Ď–į–ļ—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ—č–Ļ –≤–į–≥–ł–Ĺ–ĺ–∑.
–£—á–ł—ā—č–≤–į—Ź –ī–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā—Ć –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź, –ĺ–Ī—ą–ł—Ä–Ĺ–ĺ—Ā—ā—Ć –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź, –Ņ—Ā–ł—Ö–ĺ—ć–ľ–ĺ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ—č–Ļ –Ĺ–į—Ā—ā—Ä–ĺ–Ļ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ļ–ł, –Ī—č–Ľ–ĺ –Ņ—Ä–ł–Ĺ—Ź—ā–ĺ —Ä–Ķ—ą–Ķ–Ĺ–ł–Ķ –Ņ—Ä–ĺ–≤–Ķ—Ā—ā–ł –Ņ—Ä–Ķ–ī–≤–į—Ä–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ —ā–Ķ—Ä–į–Ņ–ł—é –Ī–į–ļ—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –≤–į–≥–ł–Ĺ–ĺ–∑–į –ł —Ā–ļ–ĺ—Ä—Ä–Ķ–ļ—ā–ł—Ä–ĺ–≤–į—ā—Ć –ł–ľ–Ķ—é—Č–ł–Ķ—Ā—Ź –ł–ľ–ľ—É–Ĺ–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł–Ķ –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł—Ź. –° —ć—ā–ĺ–Ļ —Ü–Ķ–Ľ—Ć—é –Ī—č–Ľ –Ĺ–į–∑–Ĺ–į—á–Ķ–Ĺ –ļ–Ľ–ł–Ĺ–ī–į–ľ–ł—Ü–ł–Ĺ 2% –ļ—Ä–Ķ–ľ –ī–≤–į–∂–ī—č –≤ –ī–Ķ–Ĺ—Ć ‚ĄĖ 5, —Ā 6-–≥–ĺ –ī–Ĺ—Ź –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź ‚ÄĒ –ü–ĺ–Ľ–ł–ĺ–ļ—Ā–ł–ī–ĺ–Ĺ–ł–Ļ¬ģ –≤ —Ā–≤–Ķ—á–į—Ö 12 –ľ–≥ –Ņ–ĺ —Ā—Ö–Ķ–ľ–Ķ: 1 —Ā—É–Ņ–Ņ–ĺ–∑–ł—ā–ĺ—Ä–ł–Ļ –Ķ–∂–Ķ–ī–Ĺ–Ķ–≤–Ĺ–ĺ –ł–Ĺ—ā—Ä–į–≤–į–≥–ł–Ĺ–į–Ľ—Ć–Ĺ–ĺ –≤ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ 3 –ī–Ĺ–Ķ–Ļ, –∑–į—ā–Ķ–ľ –Ņ–ĺ 1 —Ā—É–Ņ–Ņ–ĺ–∑–ł—ā–ĺ—Ä–ł—é —á–Ķ—Ä–Ķ–∑ –ī–Ķ–Ĺ—Ć –ĺ–Ī—Č–ł–ľ –ļ—É—Ä—Ā–ĺ–ľ 10 –≤–≤–Ķ–ī–Ķ–Ĺ–ł–Ļ.
–ü—Ä–ł –ĺ—Ā–ľ–ĺ—ā—Ä–Ķ —á–Ķ—Ä–Ķ–∑ –ľ–Ķ—Ā—Ź—Ü –Ī—č–Ľ–ĺ –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ–ĺ —É–ľ–Ķ–Ĺ—Ć—ą–Ķ–Ĺ–ł–Ķ —Ä–į–∑–ľ–Ķ—Ä–ĺ–≤ –ł –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–į –į–Ĺ–ĺ–≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ—č—Ö –Ī–ĺ—Ä–ĺ–ī–į–≤–ĺ–ļ (—Ä–ł—Ā. 2B).
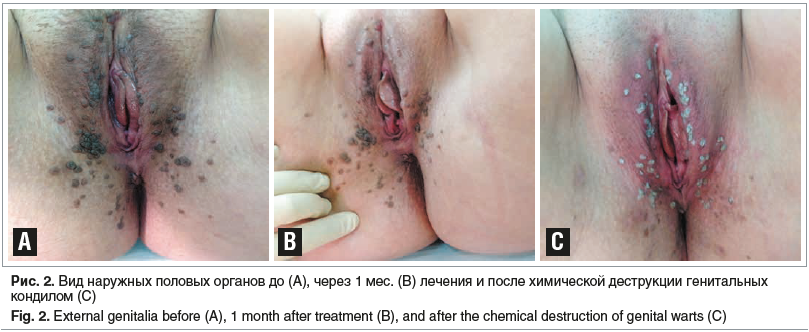
–õ–ĺ–ļ–į–Ľ—Ć–Ĺ–į—Ź –ł–ľ–ľ—É–Ĺ–ĺ–ļ–ĺ—Ä—Ä–ł–≥–ł—Ä—É—é—Č–į—Ź —ā–Ķ—Ä–į–Ņ–ł—Ź –Ņ–ĺ–∑–≤–ĺ–Ľ–ł–Ľ–į —É–ľ–Ķ–Ĺ—Ć—ą–ł—ā—Ć –≤—č—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ—Ā—ā—Ć –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł—Ö —Ā–ł–ľ–Ņ—ā–ĺ–ľ–ĺ–≤, —á—ā–ĺ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –ĺ–Ī–Ľ–Ķ–≥—á–ł–Ľ–ĺ –≤—č–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ–ł–Ķ —Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ī–Ķ—Ā—ā—Ä—É–ļ—Ü–ł–ł –į–Ĺ–ĺ–≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ—č—Ö –Ī–ĺ—Ä–ĺ–ī–į–≤–ĺ–ļ (—Ä–ł—Ā. 2C).
–ě–ļ–ĺ–Ľ–ĺ 90% —Ā–Ľ—É—á–į–Ķ–≤ –≥–Ķ–Ĺ–ł—ā–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ļ–ĺ–Ĺ–ī–ł–Ľ–ĺ–ľ–į—ā–ĺ–∑–į –≤—č–∑–≤–į–Ĺ–ĺ –í–ü–ß 6-–≥–ĺ –ł 11-–≥–ĺ —ā–ł–Ņ–į –ė–ľ–ľ—É–Ĺ–ł—ā–Ķ—ā –Ņ—Ä–ł –í–ü–ß-–ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ł —ā–ł–Ņ–ĺ—Ā–Ņ–Ķ—Ü–ł—Ą–ł—á–Ķ—Ā–ļ–ł–Ļ –ł –Ĺ–ł–∑–ļ–ł–Ļ. –ö–Ľ–Ķ—ā–ĺ—á–Ĺ—č–Ļ –ł–ľ–ľ—É–Ĺ–ł—ā–Ķ—ā –Ī–Ľ–ĺ–ļ–ł—Ä—É–Ķ—ā –Ņ–Ķ—Ä—Ā–ł—Ā—ā–Ķ–Ĺ—Ü–ł—é –≤–ł—Ä—É—Ā–į –ł –≤ —Ä—Ź–ī–Ķ —Ā–Ľ—É—á–į–Ķ–≤ —Ā–Ņ–ĺ—Ā–ĺ–Ī—Ā—ā–≤—É–Ķ—ā —Ā–Ņ–ĺ–Ĺ—ā–į–Ĺ–Ĺ–ĺ–ľ—É —Ä–Ķ–≥—Ä–Ķ—Ā—Ā—É –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–Ļ. –ß–į—Ā—ā–ĺ –Ņ—Ä–ł –í–ü–ß-–ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ł –Ĺ–į–Ī–Ľ—é–ī–į–Ķ—ā—Ā—Ź —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ –ļ–Ľ–Ķ—ā–ĺ—á–Ĺ–ĺ–≥–ĺ –ł–ľ–ľ—É–Ĺ–ł—ā–Ķ—ā–į, —Ü–ł—ā–ĺ–ļ–ł–Ĺ–ĺ–≤, –į —ā–į–ļ–∂–Ķ –ī–Ķ—Ą–ł—Ü–ł—ā őĪ-–ł–Ĺ—ā–Ķ—Ä—Ą–Ķ—Ä–ĺ–Ĺ–į –ł ő≥-–ł–Ĺ—ā–Ķ—Ä—Ą–Ķ—Ä–ĺ–Ĺ–į, —á—ā–ĺ –Ĺ–Ķ–ĺ–ī–Ĺ–ĺ–ļ—Ä–į—ā–Ĺ–ĺ –Ņ–ĺ–ī—ā–≤–Ķ—Ä–∂–ī–Ķ–Ĺ–ĺ –ľ–Ĺ–ĺ–≥–ł–ľ–ł –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź–ľ–ł [19, 22].
–° —É—á–Ķ—ā–ĺ–ľ —ā–ĺ–≥–ĺ, —á—ā–ĺ –í–ü–ß-–ł–Ĺ—Ą–Ķ–ļ—Ü–ł—Ź –Ņ–Ķ—Ä—Ā–ł—Ā—ā–ł—Ä—É–Ķ—ā –≤ –ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–Ķ —É –Ľ–ł—Ü —Ā –ł–ľ–ľ—É–Ĺ–ĺ–ī–Ķ—Ą–ł—Ü–ł—ā–Ĺ—č–ľ —Ā–ĺ—Ā—ā–ĺ—Ź–Ĺ–ł–Ķ–ľ, –į —ā–į–ļ–∂–Ķ –ł–ľ–Ķ–Ķ—ā—Ā—Ź –≤—č—Ā–ĺ–ļ–ł–Ļ —Ä–ł—Ā–ļ —Ä–Ķ—Ü–ł–ī–ł–≤–į –ļ–ĺ–Ĺ–ī–ł–Ľ–ĺ–ľ –Ņ–ĺ—Ā–Ľ–Ķ —Ö–ł—Ä—É—Ä–≥–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —É–ī–į–Ľ–Ķ–Ĺ–ł—Ź, –ī–į–Ĺ–Ĺ–ĺ–ľ—É –ļ–ĺ–Ĺ—ā–ł–Ĺ–≥–Ķ–Ĺ—ā—É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–ļ —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–ĺ–≤–į–Ĺ–į –ł–ľ–ľ—É–Ĺ–ĺ—ā–Ķ—Ä–į–Ņ–ł—Ź –Ē–Ľ—Ź –į–ļ—ā–ł–≤–į—Ü–ł–ł –Ņ—Ä–ĺ—ā–ł–≤–ĺ–ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–≥–ĺ –ł–ľ–ľ—É–Ĺ–ł—ā–Ķ—ā–į –Ĺ–į–ł–Ī–ĺ–Ľ–Ķ–Ķ —Ü–Ķ–Ľ–Ķ—Ā–ĺ–ĺ–Ī—Ä–į–∑–Ĺ–ĺ –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ –ł–ľ–ľ—É–Ĺ–ĺ–ľ–ĺ–ī—É–Ľ—Ź—ā–ĺ—Ä–ĺ–≤, –≤–ĺ–∑–ī–Ķ–Ļ—Ā—ā–≤—É—é—Č–ł—Ö –≤ –Ņ–Ķ—Ä–≤—É—é –ĺ—á–Ķ—Ä–Ķ–ī—Ć –Ĺ–į –ļ–Ľ–Ķ—ā–ĺ—á–Ĺ—č–Ļ –ł–ľ–ľ—É–Ĺ–ł—ā–Ķ—ā, –į —ā–į–ļ–∂–Ķ —Ā—ā–ł–ľ—É–Ľ–ł—Ä—É—é—Č–ł—Ö –≥—É–ľ–ĺ—Ä–į–Ľ—Ć–Ĺ–ĺ–Ķ –∑–≤–Ķ–Ĺ–ĺ –ł–ľ–ľ—É–Ĺ–ł—ā–Ķ—ā–į [19]. –í —Ā–≤—Ź–∑–ł —Ā —ć—ā–ł–ľ –ü–ĺ–Ľ–ł–ĺ–ļ—Ā–ł–ī–ĺ–Ĺ–ł–Ļ¬ģ –ľ–ĺ–∂–Ĺ–ĺ —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–ĺ–≤–į—ā—Ć –ļ–į–ļ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā –≤—č–Ī–ĺ—Ä–į –Ĺ–į –Ņ–Ķ—Ä–≤–ĺ–ľ —ć—ā–į–Ņ–Ķ —ā–Ķ—Ä–į–Ņ–ł–ł –Ņ—Ä–ł –Ľ–Ķ—á–Ķ–Ĺ–ł–ł –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–Ļ [12, 19]. –ü—Ä–Ķ–Ņ–į—Ä–į—ā –į–ļ—ā–ł–≤–ł—Ä—É–Ķ—ā –≤—Ā–Ķ —Ą–į–ļ—ā–ĺ—Ä—č –Ķ—Ā—ā–Ķ—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ–Ļ —Ä–Ķ–∑–ł—Ā—ā–Ķ–Ĺ—ā–Ĺ–ĺ—Ā—ā–ł: –ļ–Ľ–Ķ—ā–ļ–ł –ľ–ĺ–Ĺ–ĺ—Ü–ł—ā–į—Ä–Ĺ–ĺ-–ľ–į–ļ—Ä–ĺ—Ą–į–≥–į–Ľ—Ć–Ĺ–ĺ–Ļ —Ā–ł—Ā—ā–Ķ–ľ—č, –Ĺ–Ķ–Ļ—ā—Ä–ĺ—Ą–ł–Ľ—č –ł N–ö-–ļ–Ľ–Ķ—ā–ļ–ł, –≤—č–∑—č–≤–į—Ź –Ņ–ĺ–≤—č—ą–Ķ–Ĺ–ł–Ķ –ł—Ö —Ą—É–Ĺ–ļ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ–ĺ–Ļ –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ņ—Ä–ł –ł—Ā—Ö–ĺ–ī–Ĺ–ĺ —Ā–Ĺ–ł–∂–Ķ–Ĺ–Ĺ—č—Ö –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ź—Ö [12, 18, 19]. –ź–ļ—ā–ł–≤–į—Ü–ł—Ź –ľ–į–ļ—Ä–ĺ—Ą–į–≥–ĺ–≤ –≤–Ķ–ī–Ķ—ā –ļ —É—Ā–ł–Ľ–Ķ–Ĺ–ł—é —Ā–ł–Ĺ—ā–Ķ–∑–į –Ņ—Ä–į–ļ—ā–ł—á–Ķ—Ā–ļ–ł –≤—Ā–Ķ—Ö —Ü–ł—ā–ĺ–ļ–ł–Ĺ–ĺ–≤, –≤—č—Ä–į–Ī–į—ā—č–≤–į–Ķ–ľ—č—Ö —ć—ā–ł–ľ–ł –ļ–Ľ–Ķ—ā–ļ–į–ľ–ł, —Ā–Ľ–Ķ–ī—Ā—ā–≤–ł–Ķ–ľ —á–Ķ–≥–ĺ —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź —É—Ā–ł–Ľ–Ķ–Ĺ–ł–Ķ —Ą—É–Ĺ–ļ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ–ĺ–Ļ –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł —Ą–į–ļ—ā–ĺ—Ä–ĺ–≤ –ļ–į–ļ –ļ–Ľ–Ķ—ā–ĺ—á–Ĺ–ĺ–≥–ĺ, —ā–į–ļ –ł –≥—É–ľ–ĺ—Ä–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ł–ľ–ľ—É–Ĺ–ł—ā–Ķ—ā–į. –ė—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –Ņ–ĺ–ļ–į–∑–į–Ľ–ł, —á—ā–ĺ –ü–ĺ–Ľ–ł–ĺ–ļ—Ā–ł–ī–ĺ–Ĺ–ł–Ļ¬ģ –Ņ–ĺ–≤—č—ą–į–Ķ—ā –ł–ľ–ľ—É–Ĺ–Ĺ—É—é —Ä–Ķ–∑–ł—Ā—ā–Ķ–Ĺ—ā–Ĺ–ĺ—Ā—ā—Ć –ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–į –≤ –ĺ—ā–Ĺ–ĺ—ą–Ķ–Ĺ–ł–ł –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ –Ĺ–ł–∂–Ĺ–ł—Ö –ĺ—ā–ī–Ķ–Ľ–ĺ–≤ –Ņ–ĺ–Ľ–ĺ–≤—č—Ö –Ņ—É—ā–Ķ–Ļ, –≤—č–∑–≤–į–Ĺ–Ĺ—č—Ö —Ā–į–ľ—č–ľ–ł —Ä–į–∑–Ĺ—č–ľ–ł –Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ĺ—č–ľ–ł –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–į–ľ–ł [12, 18, 19].
–ó–į–ļ–Ľ—é—á–Ķ–Ĺ–ł–Ķ
–ú–ł–ļ—Ā—ā-–ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ł, –į—Ā—Ā–ĺ—Ü–ł–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–Ķ —Ā —É—Ā–Ľ–ĺ–≤–Ĺ–ĺ-–Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ĺ—č–ľ–ł –ľ–ł–ļ—Ä–ĺ–ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–į–ľ–ł, —Ā–≤–ł–ī–Ķ—ā–Ķ–Ľ—Ć—Ā—ā–≤—É—é—ā –ĺ –ī–ł—Ā–Ī–į–Ľ–į–Ĺ—Ā–Ķ –≤ –Ľ–ĺ–ļ–į–Ľ—Ć–Ĺ–ĺ–Ļ –Ņ—Ä–ĺ—ā–ł–≤–ĺ–ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–Ļ –∑–į—Č–ł—ā–Ķ —Ä–Ķ–Ņ—Ä–ĺ–ī—É–ļ—ā–ł–≤–Ĺ–ĺ–≥–ĺ —ā—Ä–į–ļ—ā–į. –Ę–Ķ—Ä–į–Ņ–ł—Ź —ā–į–ļ–ł—Ö —Ā–ĺ—Ā—ā–ĺ—Ź–Ĺ–ł–Ļ –Ī—É–ī–Ķ—ā –ĺ–Ņ—ā–ł–ľ–į–Ľ—Ć–Ĺ–į –Ņ—Ä–ł –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–ł –ł–ľ–ľ—É–Ĺ–ĺ—ā—Ä–ĺ–Ņ–Ĺ–ĺ–≥–ĺ –≤–ĺ–∑–ī–Ķ–Ļ—Ā—ā–≤–ł—Ź, –ł —ć—ā–ĺ —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –ĺ—Ā–Ĺ–ĺ–≤–į–Ĺ–ł–Ķ–ľ –ī–Ľ—Ź –Ĺ–į–∑–Ĺ–į—á–Ķ–Ĺ–ł—Ź –ł–ľ–ľ—É–Ĺ–ĺ—ā—Ä–ĺ–Ņ–Ĺ–ĺ–≥–ĺ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į –≤ —Ā–ĺ—Ā—ā–į–≤–Ķ –ļ–ĺ–ľ–Ņ–Ľ–Ķ–ļ—Ā–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł—Ö, —Ä–Ķ—Ü–ł–ī–ł–≤–ł—Ä—É—é—Č–ł—Ö –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ.
–ė–ľ–ľ—É–Ĺ–ĺ–ľ–ĺ–ī—É–Ľ—Ź—ā–ĺ—Ä (–ü–ĺ–Ľ–ł–ĺ–ļ—Ā–ł–ī–ĺ–Ĺ–ł–Ļ¬ģ) –ľ–ĺ–∂–Ķ—ā –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į—ā—Ć—Ā—Ź –ļ–į–ļ –≤ —Ā–ĺ—Ā—ā–į–≤–Ķ –ļ–ĺ–ľ–Ņ–Ľ–Ķ–ļ—Ā–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł, —ā–į–ļ –ł –≤ –≤–ł–ī–Ķ –ľ–ĺ–Ĺ–ĺ—ā–Ķ—Ä–į–Ņ–ł–ł, —á—ā–ĺ –Ņ–ĺ–∑–≤–ĺ–Ľ—Ź–Ķ—ā –ĺ–Ī–Ķ—Ā–Ņ–Ķ—á–ł—ā—Ć –Ņ–Ķ—Ä—Ā–ĺ–Ĺ–į–Ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–Ļ –Ņ–ĺ–ī—Ö–ĺ–ī –ļ –Ľ–Ķ—á–Ķ–Ĺ–ł—é –ł —Ā—É—Č–Ķ—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ –Ņ–ĺ–≤—č—Ā–ł—ā—Ć –ļ–į—á–Ķ—Ā—ā–≤–ĺ –ĺ–ļ–į–∑—č–≤–į–Ķ–ľ–ĺ–Ļ –ľ–Ķ–ī–ł—Ü–ł–Ĺ—Ā–ļ–ĺ–Ļ –Ņ–ĺ–ľ–ĺ—Č–ł.
–Ď–Ľ–į–≥–ĺ–ī–į—Ä–Ĺ–ĺ—Ā—ā—Ć
–†–Ķ–ī–į–ļ—Ü–ł—Ź –Ī–Ľ–į–≥–ĺ–ī–į—Ä–ł—ā –ě–ě–ě –Ě–ü–ě ¬ę–ü–Ķ—ā—Ä–ĺ–≤–į–ļ—Ā –§–į—Ä–ľ¬Ľ –∑–į –ĺ–ļ–į–∑–į–Ĺ–Ĺ—É—é –Ņ–ĺ–ľ–ĺ—Č—Ć –≤ —ā–Ķ—Ö–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ —Ä–Ķ–ī–į–ļ—ā—É—Ä–Ķ –Ĺ–į—Ā—ā–ĺ—Ź—Č–Ķ–Ļ –Ņ—É–Ī–Ľ–ł–ļ–į—Ü–ł–ł
Acknowledgment
Editorial Board is grateful to LLC ‚ÄúPetrovax Pharm‚ÄĚ for the assistance in technical edition of this publication.
–°–≤–Ķ–ī–Ķ–Ĺ–ł—Ź –ĺ–Ī –į–≤—ā–ĺ—Ä–į—Ö:
–õ–Ķ—ā—Ź–Ķ–≤–į –ě–Ľ—Ć–≥–į –ė–≤–į–Ĺ–ĺ–≤–Ĺ–į ‚ÄĒ –ī.–ľ.–Ĺ., –ī–ĺ—Ü–Ķ–Ĺ—ā, –Ņ—Ä–ĺ—Ą–Ķ—Ā—Ā–ĺ—Ä –ļ–į—Ą–Ķ–ī—Ä—č –ī–Ķ—Ä–ľ–į—ā–ĺ–≤–Ķ–Ĺ–Ķ—Ä–ĺ–Ľ–ĺ–≥–ł–ł –§–ď–Ď–ě–£ –í–ě –ģ–£–ď–ú–£ –ú–ł–Ĺ–∑–ī—Ä–į–≤–į –†–ĺ—Ā—Ā–ł–ł; 454092, –†–ĺ—Ā—Ā–ł—Ź, –≥. –ß–Ķ–Ľ—Ź–Ī–ł–Ĺ—Ā–ļ, —É–Ľ. –í–ĺ—Ä–ĺ–≤—Ā–ļ–ĺ–≥–ĺ, –ī. 64; ORCID iD 0000-0002-9085-6229.
–ó–ł–≥–į–Ĺ—ą–ł–Ĺ –ě–Ľ–Ķ–≥ –†–į–ł—Ā–ĺ–≤–ł—á ‚ÄĒ –ī.–ľ.–Ĺ, –Ņ—Ä–ĺ—Ą–Ķ—Ā—Ā–ĺ—Ä, –∑–į–≤–Ķ–ī—É—é—Č–ł–Ļ –ļ–į—Ą–Ķ–ī—Ä–ĺ–Ļ –ī–Ķ—Ä–ľ–į—ā–ĺ–≤–Ķ–Ĺ–Ķ—Ä–ĺ–Ľ–ĺ–≥–ł–ł –§–ď–Ď–ě–£ –í–ě –ģ–£–ď–ú–£ –ú–ł–Ĺ–∑–ī—Ä–į–≤–į –†–ĺ—Ā—Ā–ł–ł; 454092, –†–ĺ—Ā—Ā–ł—Ź, –≥. –ß–Ķ–Ľ—Ź–Ī–ł–Ĺ—Ā–ļ, —É–Ľ. –í–ĺ—Ä–ĺ–≤—Ā–ļ–ĺ–≥–ĺ, –ī. 64; ORCID iD 0000-0002-5857-0319.
–ö–ĺ–Ĺ—ā–į–ļ—ā–Ĺ–į—Ź –ł–Ĺ—Ą–ĺ—Ä–ľ–į—Ü–ł—Ź: –õ–Ķ—ā—Ź–Ķ–≤–į –ě–Ľ—Ć–≥–į –ė–≤–į–Ĺ–ĺ–≤–Ĺ–į, e-mail: olga-letyaeva@yandex.ru. –ü—Ä–ĺ–∑—Ä–į—á–Ĺ–ĺ—Ā—ā—Ć —Ą–ł–Ĺ–į–Ĺ—Ā–ĺ–≤–ĺ–Ļ –ī–Ķ—Ź—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā–ł: –Ĺ–ł–ļ—ā–ĺ –ł–∑ –į–≤—ā–ĺ—Ä–ĺ–≤ –Ĺ–Ķ –ł–ľ–Ķ–Ķ—ā —Ą–ł–Ĺ–į–Ĺ—Ā–ĺ–≤–ĺ–Ļ –∑–į–ł–Ĺ—ā–Ķ—Ä–Ķ—Ā–ĺ–≤–į–Ĺ–Ĺ–ĺ—Ā—ā–ł –≤ –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ–Ķ–Ĺ–Ĺ—č—Ö –ľ–į—ā–Ķ—Ä–ł–į–Ľ–į—Ö –ł–Ľ–ł –ľ–Ķ—ā–ĺ–ī–į—Ö. –ö–ĺ–Ĺ—Ą–Ľ–ł–ļ—ā –ł–Ĺ—ā–Ķ—Ä–Ķ—Ā–ĺ–≤ –ĺ—ā—Ā—É—ā—Ā—ā–≤—É–Ķ—ā –°—ā–į—ā—Ć—Ź –Ņ–ĺ—Ā—ā—É–Ņ–ł–Ľ–į 24.11.2020, –Ņ–ĺ—Ā—ā—É–Ņ–ł–Ľ–į –Ņ–ĺ—Ā–Ľ–Ķ —Ä–Ķ—Ü–Ķ–Ĺ–∑–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź 17.12.2020, –Ņ—Ä–ł–Ĺ—Ź—ā–į –≤ –Ņ–Ķ—á–į—ā—Ć 19.01.2021.
About the authors:
Olga I. Letyaeva ‚ÄĒ Doct. of Sci. (Med.), Associate Professor, professor of the Department of Dermatovenerology, South Ural State Medical University; 64, Vorovskiy str., Chelyabinsk, 454092, Russian Federation; ORCID iD 0000-0002-9085-6229.
Oleg R. Ziganshin ‚ÄĒ Doct. of Sci. (Med.), Professor, Head of the Department of Dermatovenerology, South Ural State Medical University; 64, Vorovskiy str., Chelyabinsk, 454092, Russian Federation; ORCID iD 0000-0002-5857-0319.
Contact information: Olga I. Letyaeva, e-mail: olga-letyaeva@yandex.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 24.11.2020, revised 17.12.2020, accepted 19.01.2021.












