Несмотря на то, что эндометриоз был описан еще в XIX в., полностью причины его появления и распространения не изучены. Также многие вопросы относительно методов лечения остаются далекими от решения. В связи с хроническим и часто рецидивирующим характером течения заболевания Комитет врачебной практики Американского общества репродуктивной медицины (ASRM) заключил следующее: «эндометриоз должен рассматриваться как хроническое заболевание, требующее пожизненного плана ведения, приоритетом которого является медикаментозное лечение и профилактика повторных хирургических процедур» [3].
План лечения должен быть индивидуальным в зависимости от симптомов эндометриоза, распространенности патологического процесса, желания иметь детей, возраста, опыта хирурга, побочных эффектов препаратов и хирургического лечения
- симптоматическое лечение нестероидными противовоспалительными препаратами (НПВП);
- гормональное лечение (комбинированные оральные контрацептивы (КОК) в циклическом или пролонгированном режиме, агонисты
гонадотропин-рилизинг-гормонов (ГнРГ), даназол, ингибиторы ароматазы); - хирургическое лечение, которое разделяют на консервативное (органосохраняющее),
т. е. с сохранением матки и ткани яичников, и радикальное: с удалением матки и, возможно, яичников; - комплексное лечение: сочетание медикаментозного лечения до и/или после хирургии.
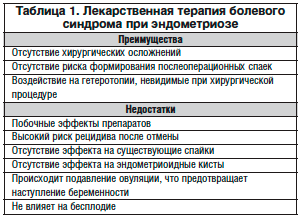
Лапароскопия, бесспорно, является «золотым стандартом» в диагностике и лечении эндометриоза, позволяет коагулировать или иссекать гетеротопии и спайки, и таким образом если не предотвратить, то, как минимум, значительно отсрочить рецидив болезни. Также полное удаление очагов позволяет снизить расходы и побочные реакции медикаментозной терапии. В то же время нередки интраоперационные осложнения, связанные с повреждением нижних отделов кишечника и мочеполового тракта, инфекционные осложнения и формирование послеоперационных спаек, иногда более выраженных, чем до операции. Преимущества и недостатки медикаментозной терапии приведены в таблице 1.
НПВП часто применяются женщинами для купирования болевого синдрома, однако клинические исследования крайне скудны. Главным сдерживающим фактором длительного использования НПВП являются побочные эффекты, такие как язва желудка и ановуляторный эффект при применении в середине менструального цикла [4, 5].
Наиболее часто в клинической практике для лечения эндометриоза используются агонисты ГнРГ, даназол и некоторые прогестины. Эти препараты и КОК имеют общее воздействие на эндометриоз. По сравнению с эутопическим эндометрием эндометрий в имплантатах синтезирует больше простагландинов, эстрогенов и провоспалительных цитокинов, это приводит к пролиферации и инфильтративному росту, обусловливая боль. Более того, повышенная активность ароматазы потенцирует синтез циклооксигеназы
КОК широко применяются для лечения симптомов эндометриоза, однако, судя по данным исследований, эффект незначительный. P. Verchellini et al. полагают, что действие препаратов заключается в подавлении имплантации гетеротопий, но имеется и протективный эффект против их некроза [6]. В состав большинства КОК входит этинилэстрадиол, значительно более активный, чем эстрадиол. В настоящее время высказываются опасения, что этинилэстрадиол может поддерживать локальную гиперэстрогению в гетеротопиях, таким образом «подстегивая» эндометрий. Хотя КОК не входят в протоколы лечения эндометриоза во многих странах, тем не менее, их используют долгое время при необходимости в контрацепции у таких больных. Главная проблема — прорывные кровотечения, которые могут прекратиться при отмене препарата, и через несколько дней можно возобновить лечение. Также КОК не имеют зарегистрированных показаний для лечения эндометриоза, хотя и указаны во многих национальных руководствах и стандартах лечения.
Возможно применение непероральных эстрогенпрогестероновых контрацептивов, однако этот вопрос изучен недостаточно.
Даназол — это андрогенный стероидный препарат, достаточно эффективный при лечении эндометриоза. По данным исследований, более 80% пациенток отмечают исчезновение или значительное ослабление боли [7–9], но его применение ограничено частыми побочными эффектами: влиянием на липидный профиль, прибавкой массы тела, отечностью, усилением секреции сальных желез и акне, сухостью во влагалище, приливами, гирсутизмом, гепатотоксичностью и атрофией молочных желез.
Пероральные, парентеральные, внутриматочные контрацептивы или прогестины в виде имплантатов используются в течение десятилетий с различной доказательной базой. Однако для достижения терапевтического эффекта зачастую необходимо переходить на более высокие дозировки по сравнению с другими показаниями для их применения, что, конечно, увеличивает частоту побочных реакций (прибавка массы тела, андрогенные эффекты и
Отдельного внимания заслуживает препарат диеногест (Визанна, Bayer, Германия), который рекомендован в качестве монотерапии эндометриоза в Европе, Японии и др. Он представляет собой синтетический пероральный прогестин с выраженным прогестагенным и умеренным антигонадотропным эффектами, но без андрогенной, глюкокортикоидной и минералокортикоидной активности. Механизм действия на эндометриоидные гетеротопии многофакторный. Диеногест снижает секрецию гонадотропинов, что приводит к значительному снижению синтеза эстрадиола. При продолжительном применении вызывает гипоэстрогению, повышение уровня прогестерона, что приводит к децидуализации, а затем атрофии эндометриальной ткани [11]. В эксперименте на животных также показано, что диеногест вызывает апоптоз гранулезных клеток яичников [12]. В исследованиях на животных показано следующее влияние диеногеста: подавление пролиферации, ангиогенеза и противовоспалительный эффект диеногеста [13, 14].
Рандомизированное клиническое исследование показало, что перорально принимаемый диеногест более эффективен по сравнению с плацебо, уменьшая боль при подтвержденном эндометриозе [15]. В исследованиях, сравнивающих прием диеногеста длительностью 16 и 24 нед. вместе с агонистами ГнРГ у пациентов с эндометриозом, и прием агонистов ГнРГ, получены сопоставимые результаты по уменьшению боли по баллам и по классификации эндометриоза rAFS при повторной лапароскопии [16]. Другое рандомизированное исследование, сравнивающее агонисты ГнРГ и диеногест, предлагают последний как сопоставимый по эффективности, но более безопасный и лучше переносимый, что связано с меньшей гипоэстрогенией, меньшими изменениями минеральной плотности костной ткани и маркеров костной резорбции [17].
Общеизвестно, что самые эффективные методы снижения продукции эстрогенов — это двухсторонняя овариоэктомия и применение агонистов ГнРГ. По понятным причинам удаление яичников в репродуктивном возрасте выполняется крайне редко. Однако частое и длительное применение агонистов ГнРГ ограничено в связи с высокой ценой и побочными эффектами, обусловленными гипоэстрогенией (аменорея, вазомоторные симптомы (80%), нарушение сна, приливы, урогенитальная атрофия (30%), головные боли (30%) и снижение минеральной плотности костной ткани (МПКТ); доказано, что применение ГнРГ увеличивает риск переломов спустя годы после приема препаратов. В
Для выяснения оптимального длительного режима
- Агонисты ГнРГ в дозе 3,75 мг
в/м каждые 4 нед. - Агонисты ГнРГ и прогестин (норэтиндрона ацетат 5 мг 1 р./сут).
- Агонисты ГнРГ и малые дозы конъюгированного эстрогена 0,625 мг и прогестин (норэтиндрона ацетат 5 мг 1 р./сут).
- Агонисты ГнРГ и конъюгированный эстроген в высокой дозе (1,25 мг 1 р./сут) и прогестин (норэтиндрона ацетат 5 мг 1 р./сут).
Всем пациенткам назначался кальций 1000 мг/сут на весь срок лечения [19]. В результате данного исследования выяснилось, что женщины без
Следует отметить, что на момент написания статьи препарат диеногест еще не зарегистрирован в США, что связано с правилами регистрации в стране. Первой линией терапии являются агонисты ГнРГ и прогестины (уровень доказательности IА). При непереносимости побочных эффектов применения высоких доз некоторых прогестинов предполагается использовать агонисты ГнРГ и низкие дозы эстрогенов и прогестина (уровень доказательности IIА).
Конечно, оптимальный режим
Необходимо признать, что в выборе терапии немаловажным фактором является стоимость,
Применение ингибиторов ароматазы — это новый многообещающий метод лечения эндометриоза. Эти препараты снижают локальный синтез эстрогенов в эндометриоидных гетеротопиях, к тому же ингибируют образование эстрогенов в яичниках, головном мозге и жировой ткани [23]. В эндометриоидных очагах простагландин E2 стимулирует гиперпродукцию ароматазы, что приводит к локальному синтезу эстрогенов из андрогенов. Эстрогены в свою очередь увеличивают синтез простагландина E2, обеспечивая положительную обратную связь. В нескольких описательных работах и одном рандомизированном исследовании ингибиторы ароматазы использовались для лечения тяжелых форм эндометриоза [24–31]. При систематическом обзоре этих исследований выяснилось, что ингибиторы ароматазы статистически значимо более выраженно снижают боль в сравнении с агонистами ГнРГ [32]. Важно знать, что ингибиторы ароматазы вызывают значительную потерю костной плотности при длительном применении и не могут назначаться в виде монотерапии у пременопаузальных женщин,
Еще одним перспективным направлением в лечении эндометриоза является попытка минимизировать воспалительный компонент в гетеротопиях. Важная роль в генезе симптомов эндометриоза отводится провоспалительным цитокинам и активации оксидативного стресса, при этом происходит активация внутриядерного воспалительного медиатора
В качестве заключения хочется отметить общую мысль, проходящую через многие обзорные статьи. В частности, в статье P. Vercellini из Миланского университета с символическим названием «В ожидании Годо» [35] авторы достаточно скептически и пессимистично относятся к современным фармакологическим методам лечения эндометриоза. Делается вывод о том, что многие женщины за свою жизнь, несмотря на применение современных и дорогостоящих препаратов, не избегут повторных операций, таким образом, «должны ли мы все еще ждать Годо»?












