–Т–≤–µ–і–µ–љ–Є–µ
–Ш–Ї—Б–Њ–і–Њ–≤—Л–є –Ї–ї–µ—Й–µ–≤–Њ–є –±–Њ—А—А–µ–ї–Є–Њ–Ј (–±–Њ—А—А–µ–ї–Є–Њ–Ј–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П, –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј) —П–≤–ї—П–µ—В—Б—П –њ—А–Є—А–Њ–і–љ–Њ–Њ—З–∞–≥–Њ–≤—Л–Љ —В—А–∞–љ—Б–Љ–Є—Б—Б–Є–≤–љ—Л–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ, –≤—Л–Ј—Л–≤–∞–µ–Љ—Л–Љ –≥—А–∞–Љ¬≠–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–Љ–Є –±–∞–Ї—В–µ—А–Є—П–Љ–Є Borrelia burgdorferi sensu lato, –њ–µ—А–µ–і–∞—О—Й–Є–Љ–Є—Б—П –Ї–ї–µ—Й–∞–Љ–Є —А–Њ–і–∞ Ixodes. –С–Њ—А—А–µ–ї–Є–Њ–Ј–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –њ–Њ–ї–Є–Љ–Њ—А—Д–Є–Ј–Љ–Њ–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є. –С–µ–Ј—Н—А–Є—В–µ–Љ–љ–∞—П —Д–Њ—А–Љ–∞ –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј–∞ –њ—А–Њ—В–µ–Ї–∞–µ—В –≤ –≤–Є–і–µ –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є –Њ—Б—В–∞–µ—В—Б—П —В—А—Г–і–љ–Њ–і–Є–∞–≥–љ–Њ—Б—В–Є—А—Г–µ–Љ–Њ–є, —В. –Ї. –≤ –Љ–µ—Б—В–µ –њ—А–Є—Б–∞—Б—Л–≤–∞–љ–Є—П –Ї–ї–µ—Й–∞ —Г –±–Њ–ї—М–љ—Л—Е –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В –њ–∞—В–Њ–≥–љ–Њ–Љ–Њ–љ–Є—З–љ—Л–є –Љ–∞—А–Ї–µ—А –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П вАФ –Љ–Є–≥—А–Є—А—Г—О—Й–∞—П —Н—А–Є—В–µ–Љ–∞ [1вАУ10]. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј–Њ–Љ –Њ–њ—А–µ–і–µ–ї—П—О—В—Б—П –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ–Є –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ –Љ–∞–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞ [1вАУ14]. –Ь–љ–Њ–ґ–µ—Б—В–≤–Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –љ–∞—Г—З–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –≤ —В. —З. –≤ –Њ–±–ї–∞—Б—В–Є –Є–Ј—Г—З–µ–љ–Є—П –±–Њ—А—А–µ–ї–Є–Њ–Ј–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є, –≤–Ї–ї—О—З–∞—О—В –Є–Ј—Г—З–µ–љ–Є–µ –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є –Є –Ї—А–Є—В–µ—А–Є–µ–≤ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–≥–Њ —В–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –∞ —В–∞–Ї–ґ–µ —Б–Є—Б—В–µ–Љ–љ—Л–є –∞–љ–∞–ї–Є–Ј –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є [12вАУ15]. –Ь–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ—Л–є –∞–љ–∞–ї–Є–Ј (–Љ–µ—В–Њ–і –≥–ї–∞–≤–љ—Л—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В) –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤—Л—П–≤–Є—В—М –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –Њ—В–і–µ–ї—М–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –љ–∞ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Є –Њ–њ—А–µ–і–µ–ї–Є—В—М —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є [15].
–¶–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –≤—Л—П–≤–ї–µ–љ–Є–µ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е, –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є, –≤—Л—А–∞–±–Њ—В–Ї–Є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є—В–µ–ї –Є —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ (–Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–Њ–≤ IL-17A, -23, -33, -35) —Г –±–Њ–ї—М–љ—Л—Е —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј–∞ —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Љ–µ—В–Њ–і–∞ –Љ–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–° 2012 –њ–Њ 2014 –≥. –њ—А–Њ–≤–µ–і–µ–љ–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≥–Њ—Б–њ–Є—В–∞-–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –≤ –Ъ–Ю–У–С–£–Ч ¬Ђ–Ш–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–∞—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї—М–љ–Є—Ж–∞¬ї 30 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј–∞ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 15 –і–Њ 75 –ї–µ—В (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –±–Њ–ї—М–љ—Л—Е вАФ 45,5¬±15,73 –≥–Њ–і–∞), –Є–Ј –љ–Є—Е –Љ—Г–ґ—З–Є–љ—Л —Б–Њ—Б—В–∞–≤–Є–ї–Є 53,3%. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –Њ–і–Њ–±—А–µ–љ–Њ –ї–Њ–Ї–∞–ї—М–љ—Л–Љ —Н—В–Є—З–µ—Б–Ї–Є–Љ –Ї–Њ–Љ–Є—В–µ—В–Њ–Љ –§–У–С–Ю–£ –Т–Ю –Ъ–Є—А–Њ–≤—Б–Ї–Є–є –У–Ь–£ –Ь–Є–љ¬≠–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є. –Ф–Є–∞–≥–љ–Њ–Ј –±–Њ—А—А–µ–ї–Є–Њ–Ј–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –±—Л–ї –њ–Њ—Б—В–∞–≤–ї–µ–љ –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –∞–љ–∞–Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Є—Е, –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –і–∞–љ–љ—Л—Е –Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є. –Ф–Є–∞–≥–љ–Њ–Ј —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј–∞ –±—Л–ї —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–µ–є E. Asbring (1988 –≥.) –Є –Э.–Э. –Т–Њ—А–Њ–±—М–µ–≤–Њ–є (2013 –≥.) [1вАУ4]. –°–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–∞—П —Б–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –±–Њ—А—А–µ–ї–Є–Њ–Ј–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤–Ї–ї—О—З–∞–ї–∞ –≤—Л—П–≤–ї–µ–љ–Є–µ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤ IgM –Є IgG –Ї –∞–љ—В–Є–≥–µ–љ–љ—Л–Љ —Б—В—А—Г–Ї—В—Г—А–∞–Љ Borrelia afzelii, Borrelia garinii –Љ–µ—В–Њ–і–Њ–Љ –Є–Љ–Љ—Г–љ–Њ—З–Є–њ–∞ –≤ –§–С–£–Э –¶–Э–Ш–Ш –≠–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є–Є –†–Њ—Б–њ–Њ—В—А–µ–±–љ–∞–і–Ј–Њ—А–∞. –Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Г—А–Њ–≤–љ–µ–є —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ (IL-17A, -23, -33, -35) —Б—Л–≤–Њ—А–Њ—В–Ї–Є –Ї—А–Њ–≤–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Њ–≤–µ–і–µ–љ–Њ –≤ –њ–µ—А–Є–Њ–і —А–∞–Ј–≥–∞—А–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —А–µ–Ї–Њ–љ–≤–∞–ї–µ—Б—Ж–µ–љ—Ж–Є–Є. –Т –Ї–Њ–љ—В—А–Њ–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л 30 –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–љ–Њ—А–Њ–≤, –њ–Њ –њ–Њ–ї—Г –Є –≤–Њ–Ј—А–∞—Б—В—Г —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–≤—И–Є–µ –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –У—А—Г–њ–њ–∞ –Ї–Њ–љ—В—А–Њ–ї—П —Б–Њ—Б—В–Њ—П–ї–∞ –Є–Ј –ї–Є—Ж –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 15 –і–Њ 75 –ї–µ—В (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В вАФ 45,6¬±12,27 –≥–Њ–і–∞), –Є–Ј –љ–Є—Е –Љ—Г–ґ—З–Є–љ вАФ 53,3%. –£—А–Њ–≤–љ–Є —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –ї–Є—Ж –Њ–њ—А–µ–і–µ–ї–µ–љ—Л –≤ –§–У–С–Ю–£ –Т–Ю –Ъ–Є—А–Њ–≤—Б–Ї–Є–є –У–Ь–£ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ —А–µ–∞–Ї—В–Є–≤–Њ–≤ –Тender Med Systems
(–Р–≤—Б—В—А–Є—П), Uscscn Life Science Ins. Wuhan (–Ъ–Є—В–∞–є).
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–∞—П –Њ–±—А–∞–±–Њ—В–Ї–∞ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ Statistica v 10.0 (StatSoft Inc., –°–®–Р). –Ъ–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ –≤–Є–і–µ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є (%). –†–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е –Њ—Ж–µ–љ–µ–љ–Њ –њ–Њ –њ–Њ—Б—В—А–Њ–µ–љ–љ—Л–Љ –≥–Є—Б—В–Њ–≥—А–∞–Љ–Љ–∞–Љ –Є –Ї—А–Є—В–µ—А–Є—О –®–∞–њ–Є—А–Њ вАФ –£–Є–ї–Ї–∞. –Я—А–Є –љ–Њ—А–Љ–∞–ї—М–љ–Њ–Љ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤—Л—З–Є—Б–ї—П–ї–Њ—Б—М —Б—А–µ–і–љ–µ–µ –∞—А–Є—Д–Љ–µ—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ —Б–Њ —Б—А–µ–і–љ–µ–Ї–≤–∞–і—А–∞—В–Є—З–љ—Л–Љ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є–µ–Љ (–Ь¬±ѕГ) –Є –њ—А–Њ–≤–µ–і–µ–љ–Њ —Б—А–∞–≤–љ–µ–љ–Є–µ –њ–Њ t-–Ї—А–Є—В–µ—А–Є—О –°—В—М—О–і–µ–љ—В–∞. –Ь–µ–і–Є–∞–љ–∞, –∞ —В–∞–Ї–ґ–µ –љ–Є–ґ–љ–Є–є –Є –≤–µ—А—Е–љ–Є–є –Ї–≤–∞—А—В–Є–ї–Є (Me (Q25; Q75)) –≤—Л—З–Є—Б–ї—П–ї–Є—Б—М –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Њ—В–ї–Є—З–љ–Њ–≥–Њ –Њ—В –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є. –Ъ—А–Є—В–µ—А–Є–є –Ь–∞–љ–љ–∞ вАФ –£–Є—В–љ–Є –≤—Л—З–Є—Б–ї—П–ї—Б—П –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –њ—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е –≤—Л–±–Њ—А–Њ–Ї; –Ї—А–Є—В–µ—А–Є–є –Т–Є–ї–Ї–Њ–Ї—Б–Њ–љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –њ—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є –Ј–∞–≤–Є—Б–Є–Љ—Л—Е –≤—Л–±–Њ—А–Њ–Ї. –Ъ–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В –°–њ–Є—А–Љ–µ–љ–∞ –Њ–њ—А–µ–і–µ–ї—П–ї—Б—П –њ—А–Є –Є–Ј—Г—З–µ–љ–Є–Є —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –і–≤—Г–Љ—П —А—П–і–∞–Љ–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е. –Ф–Њ—Б—В–Њ–≤–µ—А–љ–Њ—Б—В—М —А–∞–Ј–ї–Є—З–Є–є –Ј–љ–∞—З–µ–љ–Є–є –±—Л–ї–∞ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞ –њ—А–Є –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–Љ —Г—А–Њ–≤–љ–µ –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є –±–Њ–ї–µ–µ 95% (—А<0,05).
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–Ч–∞ –њ–µ—А–Є–Њ–і —Б 2000 –њ–Њ 2019 –≥. –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј–Њ–Љ –≤ –Ъ–Є—А–Њ–≤—Б–Ї–Њ–є –Њ–±–ї–∞—Б—В–Є –њ—А–µ–≤—Л—И–∞–ї–Є —Б—А–µ–і–љ–µ—А–Њ—Б—Б–Є–є—Б–Ї–Є–µ –≤ 2,6вАУ8,2 —А–∞–Ј–∞ [16]. –°—А–µ–і–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —З–∞—Й–µ –≤—Б—В—А–µ—З–∞–ї–Є—Б—М —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ—Л–µ –ї–Є—Ж–∞, —А–µ–ґ–µ вАФ –њ–µ–љ—Б–Є–Њ–љ–µ—А—Л (80,0% –Є 20,0%; —А<0,001). –Ю—В—А–Є—Ж–∞–ї–Є —Д–∞–Ї—В –њ—А–Є—Б–∞—Б—Л–≤–∞–љ–Є—П –Ї–ї–µ—Й–∞, –љ–Њ –љ–∞—Е–Њ–і–Є–ї–Є—Б—М –љ–∞ –њ—А–Є–≥–Њ—А–Њ–і–љ—Л—Е —В–µ—А—А–Є—В–Њ—А–Є—П—Е –≤ —Б—А–Њ–Ї–Є 1вАУ35 —Б—Г—В –і–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П 30,0% –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–∞ –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є—П B. garinii –Є B. afzelii (76,7%), –Љ–Њ–љ–Њ–Є–љ—Д–µ–Ї—Ж–Є—П B. garinii (20,0%), –Љ–Њ–љ–Њ–Є–љ—Д–µ–Ї—Ж–Є—П B. afzelii (3,3%). –£ 21 –±–Њ–ї—М–љ–Њ–≥–Њ –Є–љ–Ї—Г–±–∞—Ж–Є–Њ–љ–љ—Л–є –њ–µ—А–Є–Њ–і —Б–Њ—Б—В–∞–≤–Є–ї –Њ—В 2 –і–Њ 25 —Б—Г—В (–≤ —Б—А–µ–і–љ–µ–Љ 12,7¬±1,49 –і–љ—П), —Г –і—А—Г–≥–Є—Е 9 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (30,0%) –Є–љ–Ї—Г–±–∞—Ж–Є–Њ–љ–љ—Л–є –њ–µ—А–Є–Њ–і –љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ. –У–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є—П –њ—А–Њ–≤–µ–і–µ–љ–∞ —З–µ—А–µ–Ј 4,1¬±0,66 —Б—Г—В –Њ—В –Љ–∞–љ–Є—Д–µ—Б—В–∞—Ж–Є–Є –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ —Б –ї–Є—Е–Њ—А–∞–і–Њ—З–љ—Л–Љ–Є —А–µ–∞–Ї—Ж–Є—П–Љ–Є –Є –Њ–±—Й–µ–є —Б–ї–∞–±–Њ—Б—В—М—О —Г –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (100,0%). –Я–∞—Ж–Є–µ–љ—В—Л –ґ–∞–ї–Њ–≤–∞–ї–Є—Б—М –љ–∞ –≥–Њ–ї–Њ–≤–љ—Г—О –±–Њ–ї—М (83,3%), –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ (46,7%), –Њ–Ј–љ–Њ–±—Л (43,3%), –Љ–Є–∞–ї–≥–Є–Є (46,7%), –∞—А—В—А–∞–ї–≥–Є–Є (16,7%), —В–Њ—И–љ–Њ—В—Г (36,7%), –≤—П–ї–Њ—Б—В—М –Є –Ј–∞—В–Њ—А–Љ–Њ–ґ–µ–љ–љ–Њ—Б—В—М (43,3%). –Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –ї–Є—Е–Њ—А–∞–і–Ї–Є —Г –±–Њ–ї—М–љ—Л—Е —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ 8,3¬±1,27 —Б—Г—В. –£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–∞ —Б—А–µ–і–љ—П—П —Б—В–µ–њ–µ–љ—М —В—П–ґ–µ—Б—В–Є (90,0%). –Ґ—П–ґ–µ–ї–∞—П —Б—В–µ–њ–µ–љ—М —Б —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –Љ–µ–љ–Є–љ–≥–Є–Ј–Љ–∞ (—А–≤–Њ—В–∞, –≤—Л—А–∞–ґ–µ–љ–љ–∞—П –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М, –±–Њ–ї—М –≤ –≥–ї–∞–Ј–љ—Л—Е —П–±–ї–Њ–Ї–∞—Е, —А–Є–≥–Є–і–љ–Њ—Б—В—М –Љ—Л—И—Ж –Ј–∞—В—Л–ї–Ї–∞) –≤—Л—П–≤–ї–µ–љ–∞ —Г 10,0% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є–µ–є –Т. garinii, B. afzelii. –Э–∞—А—Г—И–µ–љ–Є–µ –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л (–±–µ—Б–њ–Њ–Ї–Њ–є—Б—В–≤–Њ, –±–µ—Б—Б–Њ–љ–љ–Є—Ж–∞, –њ—Б–Є—Е–Њ–Љ–Њ—В–Њ—А–љ–Њ–µ –≤–Њ–Ј–±—Г–ґ–і–µ–љ–Є–µ) –Њ—В–Љ–µ—З–µ–љ–Њ —Г 30,0% –±–Њ–ї—М–љ—Л—Е, –њ—А–Є —Н—В–Њ–Љ –Њ–њ—А–µ–і–µ–ї–µ–љ–∞ –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є—П B. garinii, B. afzelii —Г 26,6%, –Љ–Њ–љ–Њ–Є–љ—Д–µ–Ї—Ж–Є—П –Т. garinii вАФ —Г 3,3%. –Т–∞–≥–Њ-–Є–љ—Б—Г–ї—П—А–љ—Л–µ –Ї—А–Є–Ј—Л –±—Л–ї–Є –Њ–њ—А–µ–і–µ–ї–µ–љ—Л —Г 5 –±–Њ–ї—М–љ—Л—Е —Б –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є–µ–є B. garinii –Є B. afzelii (16,7%). –°–µ–љ—Б–Њ—А–љ–∞—П –љ–µ–є—А–Њ–њ–∞—В–Є—П –≤–µ—А—Е–љ–Є—Е –Є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є (–±–Њ–ї–Є, —Б—Г–і–Њ—А–Њ–≥–Є, –њ–Њ–Ї–∞–ї—Л–≤–∞–љ–Є–µ, –Њ–љ–µ–Љ–µ–љ–Є–µ) –≤—Л—П–≤–ї–µ–љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ 26,7% —Б–ї—Г—З–∞–µ–≤, —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є—П B. garinii, B. afzelii –Њ–њ—А–µ–і–µ–ї–µ–љ–∞ –≤ 16,7% —Б–ї—Г—З–∞–µ–≤, –Љ–Њ–љ–Њ–Є–љ—Д–µ–Ї—Ж–Є—П B. garinii вАФ –≤ 6,7%, –Љ–Њ–љ–Њ–Є–љ—Д–µ–Ї—Ж–Є—П B. afzelii вАФ –≤ 3,3%.
–£ –±–Њ–ї—М–љ—Л—Е –≤ 40,0% —Б–ї—Г—З–∞–µ–≤ –±—Л–ї–Є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ—Л –љ–∞—А—Г—И–µ–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ–≥–Њ —А–Є—В–Љ–∞ –Є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ 16,7% —Б–ї—Г—З–∞–µ–≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–∞ —Б–Є–љ—Г—Б–Њ–≤–∞—П –±—А–∞–і–Є–Ї–∞—А–і–Є—П (54,2¬±2,03 —Г–і–∞—А–∞ –≤ –Љ–Є–љ—Г—В—Г), –≤ 3,3% вАФ —Б–Є–љ—Г—Б–Њ–≤–∞—П —В–∞—Е–Є–Ї–∞—А–і–Є—П (98 —Г–і–∞—А–Њ–≤ –≤ –Љ–Є–љ—Г—В—Г). –Э–∞—А—Г—И–µ–љ–Є—П —А–µ–њ–Њ–ї—П—А–Є–Ј–∞—Ж–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ—Л –≤ 10,0% —Б–ї—Г—З–∞–µ–≤, –Ј–∞–Љ–µ–і–ї–µ–љ–Є–µ –≤–љ—Г—В—А–Є–ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤–Њ–є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є вАФ –≤ 6,7%, –љ–∞—А—Г—И–µ–љ–Є—П –∞—В—А–Є–Њ–≤–µ–љ—В—А–Є–Ї—Г–ї—П—А–љ–Њ–є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є вАФ –≤ 3,3%, —А–µ–і–Ї–Є–µ –∞—В—А–Є–Њ–≤–µ–љ—В—А–Є–Ї—Г–ї—П—А–љ—Л–µ —Н–Ї—Б—В—А–∞—Б–Є—Б—В–Њ–ї—Л вАФ –≤ 3,3%. –Ц–∞–ї–Њ–±—Л –љ–∞ –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В –≤ –Њ–±–ї–∞—Б—В–Є —Б–µ—А–і—Ж–∞ –Є –њ—А–Є–≥–ї—Г—И–µ–љ–љ–Њ—Б—В—М —Б–µ—А–і–µ—З–љ—Л—Е —В–Њ–љ–Њ–≤ –Њ–њ—А–µ–і–µ–ї–µ–љ—Л –≤ 6,7% —Б–ї—Г—З–∞–µ–≤. –£ –±–Њ–ї—М–љ—Л—Е —Б –њ–Њ—А–∞–ґ–µ–љ–Є—П–Љ–Є —Б–µ—А–і—Ж–∞ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞ –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є—П B. garinii, B. afzelii (36,7%) –Є –Љ–Њ–љ–Њ–Є–љ—Д–µ–Ї—Ж–Є—П B. garinii (3,3%).
–Т 26,7% —Б–ї—Г—З–∞–µ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–њ—А–µ–і–µ–ї–µ–љ –±–µ–Ј–ґ–µ–ї—В—Г—И–љ—Л–є –≥–µ–њ–∞—В–Є—В —Б –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —Г—А–Њ–≤–љ—П –∞–ї–∞–љ–Є–љ–∞–Љ–Є–љ–Њ—В—А–∞–љ—Б—Д–µ—А–∞–Ј—Л –≤ 1,1вАУ2,6 —А–∞–Ј–∞ (–≤ —Б—А–µ–і–љ–µ–Љ вАФ 66,5¬±7,51 –Х–і/–ї) –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є–µ–є B. garinii –Є B. afzelii.
–Т —Е–Њ–і–µ –Ї—Г—А—Б–Њ–≤–Њ–≥–Њ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е –±—Л–ї–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л —А–∞—Б—В–≤–Њ—А —Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ–∞ вАФ —Г 80,0%, —А–∞—Б—В–≤–Њ—А —Ж–µ—Д–Њ—В–∞–Ї—Б–Є–Љ–∞ вАФ —Г 16,7%, —А–∞—Б—В–≤–Њ—А –±–µ–љ–Ј–Є–ї–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ вАФ —Г 3,3%.
–Ґ–µ—З–µ–љ–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ —Б –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Њ–љ–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ —Г –±–Њ–ї—М–љ—Л—Е —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–ї–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –Њ–±—Й–µ–Љ –∞–љ–∞–ї–Є–Ј–µ –Ї—А–Њ–≤–Є –Є —Г—А–Њ–≤–љ–Є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е IgM, IgG –Ї –∞–љ—В–Є–≥–µ–љ–∞–Љ B. garinii –Є B. afzelii (—В–∞–±–ї. 1). –Т –њ—А–Њ—Ж–µ—Б—Б–µ –ї–µ—З–µ–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤—Л—П–≤–ї–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –њ–Њ–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ–µ–є –њ–∞–ї–Њ—З–Ї–Њ—П–і–µ—А–љ—Л—Е –Є —Б–µ–≥–Љ–µ–љ—В–Њ—П–і–µ—А–љ—Л—Е –љ–µ–є—В—А–Њ—Д–Є–ї–Њ–≤, –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –∞ —В–∞–Ї–ґ–µ —В–µ–љ–і–µ–љ—Ж–Є—П –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О —Б–Њ–і–µ—А–ґ–∞–љ–Є—П —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є—В–µ–ї –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –њ—А–Є –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є.

–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤ –Ъ–Є—А–Њ–≤—Б–Ї–Њ–є –Њ–±–ї–∞—Б—В–Є –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–∞—П —Д–Њ—А–Љ–∞ –±–Њ—А—А–µ–ї–Є–Њ–Ј–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є —З–∞—Б—В–Њ –≤—Б—В—А–µ—З–∞–µ—В—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ (80,0%), –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є—П B. garinii –Є B. afzelii (76,7%), –њ—А–Є –Ї–Њ—В–Њ—А–Њ–є –≤—Л—П–≤–ї—П—О—В—Б—П –≠–Ъ–У-–Є–Ј–Љ–µ–љ–µ–љ–Є—П (40,0%) –Є —Б–Є–љ–і—А–Њ–Љ —Ж–Є—В–Њ–ї–Є–Ј–∞ (26,7%). –£ –±–Њ–ї—М–љ—Л—Е —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є —Б–і–≤–Є–≥–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –Ї—А–Њ–≤–Є –Њ—В—А–∞–ґ–∞—О—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –≤ —А–∞–Ј–≥–∞—А –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≥–µ–Љ–Њ—Б—В–∞–Ј–∞, –њ–Њ–≤—Л—И–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –≥—Г–Љ–Њ—А–∞–ї—М–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ –Ї –њ–µ—А–Є–Њ–і—Г —А–µ–Ї–Њ–љ–≤–∞–ї–µ—Б—Ж–µ–љ—Ж–Є–Є.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г –±–Њ–ї—М–љ—Л—Е –Є–Ј—Г—З–∞–ї–Є—Б—М —Г—А–Њ–≤–љ–Є –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ IL-23, –Љ–∞—А–Ї–µ—А–∞ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –Ј–≤–µ–љ–∞ –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞. –Ъ–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є IL-23 –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ —А–∞–Ј–≥–∞—А –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (Me 1267,95 (Q25 399,18; Q75 1518,27) –њ–≥/–Љ–ї) –Є –≤ –њ–µ—А–Є–Њ–і —А–µ–Ї–Њ–љ–≤–∞–ї–µ—Б—Ж–µ–љ—Ж–Є–Є (Me 1137,88 (Q25 553,42; Q75 1508,26) –њ–≥/–Љ–ї) –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –њ—А–µ–≤—Л—И–∞–ї–Є –Ј–љ–∞—З–µ–љ–Є—П –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–љ–Њ—А–Њ–≤ (Me 24,89 (Q25 17,56; Q75 40,20) –њ–≥/–Љ–ї); —А1<0,001; —А2<0,001). –Я—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є IL-33 —П–≤–ї—П–µ—В—Б—П –Љ–∞—А–Ї–µ—А–Њ–Љ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –≥—Г–Љ–Њ—А–∞–ї—М–љ–Њ–≥–Њ –Ј–≤–µ–љ–∞ –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞, —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В —Б–µ–Ї—А–µ—Ж–Є—О –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–Њ–≤ –Ґ-–ї–Є–Љ—Д–Њ—Ж–Є—В–∞–Љ–Є —Е–µ–ї–њ–µ—А–∞–Љ–Є (Th) 2 —В–Є–њ–∞ [11]. –Ъ–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є IL-33 —Б—Л–≤–Њ—А–Њ—В–Ї–Є –Ї—А–Њ–≤–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ —А–∞–Ј–≥–∞—А–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (Me 84,68 (Q25 72,55; Q75 121,00) –њ–≥/–Љ–ї) –Є –≤ –њ–µ—А–Є–Њ–і —А–µ–Ї–Њ–љ–≤–∞–ї–µ—Б—Ж–µ–љ—Ж–Є–Є (Me 76,17 (Q25 57,97; Q75 99,22) –њ–≥/–Љ–ї) –±—Л–ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ –Ј–љ–∞—З–µ–љ–Є–є –≥—А—Г–њ–њ—Л –Ї–Њ–љ—В—А–Њ–ї—П (Me 6,79 (Q25 4,35; Q75 11,67) –њ–≥/–Љ–ї; —А1<0,001; —А2<0,001). –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, —Г –±–Њ–ї—М–љ—Л—Е —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј–∞ –њ–Њ–≤—Л—И–µ–љ–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е IL-23 –Є -33 –Њ–њ—А–µ–і–µ–ї—П–ї–Є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л—Е –і–ї—П —Н–ї–Є–Љ–Є–љ–∞—Ж–Є–Є –±–Њ—А—А–µ–ї–Є–є. –Ю–і–љ–∞–Ї–Њ –њ—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Ї–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ–Њ–є —Б–≤—П–Ј–Є –≤—Л—А–∞–±–Њ—В–Ї–Є IL-23 –Є -33 —Г –±–Њ–ї—М–љ—Л—Е –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М, —З—В–Њ –Љ–Њ–≥–ї–Њ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞—В—М –Њ—В–і–µ–ї—М–љ—Л–µ —Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–≤—И–Є–µ—Б—П –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—П —А–µ–∞–ї–Є–Ј–∞—Ж–Є–Є Th1- –Є Th2-—В–Є–њ–∞ –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г –±–Њ–ї—М–љ—Л—Е –њ—А–Њ–≤–µ–і–µ–љ –∞–љ–∞–ї–Є–Ј –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ IL-17A, –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ–≥–Њ –Ј–∞ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л—Е –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –≤ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є –Є –љ–µ—А–≤–љ–Њ–є —В–Ї–∞–љ–Є [11]. –£—А–Њ–≤–љ–Є IL-17–Р —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ —А–∞–Ј–≥–∞—А –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (Me 0,47 (Q25 0,26;
Q75 0,63) –њ–≥/–Љ–ї) –Є –≤ –њ–µ—А–Є–Њ–і —А–µ–Ї–Њ–љ–≤–∞–ї–µ—Б—Ж–µ–љ—Ж–Є–Є (Me 0,29 (Q25 0,17; Q75 0,63) –њ–≥/–Љ–ї) –±—Л–ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л (Me 0,10 (Q25 0,00; Q75 0,64) –њ–≥/–Љ–ї; —А1<0,01; —А2<0,05), —З—В–Њ –Љ–Њ–≥–ї–Њ —Г–Ї–∞–Ј—Л–≤–∞—В—М –љ–∞ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л—Е –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є. IL-35 –≤—Л—А–∞–±–∞—В—Л–≤–∞–µ—В—Б—П –Ґ-–ї–Є–Љ—Д–Њ—Ж–Є—В–∞–Љ–Є-—Б—Г–њ—А–µ—Б—Б–Њ—А–∞–Љ–Є –Є —П–≤–ї—П–µ—В—Б—П —Ж–Є—В–Њ–Ї–Є–љ–Њ–Љ, –њ–Њ–і–∞–≤–ї—П—О—Й–Є–Љ –њ—А–Њ–і—Г–Ї—Ж–Є—О –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ IL-17A [11]. –Ъ–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ IL-35 –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є —Г –±–Њ–ї—М–љ—Л—Е –≤ –њ–µ—А–Є–Њ–і —А–∞–Ј–≥–∞—А–∞ (Me 12,07 (Q25 2,03; Q7519,92) –њ–≥/–Љ–ї) –Є –њ–µ—А–Є–Њ–і —А–µ–Ї–Њ–љ–≤–∞–ї–µ—Б—Ж–µ–љ—Ж–Є–Є (Me 11,26 (Q25 2,03; Q75 20,65) –њ–≥/–Љ–ї) –±—Л–ї–Є –љ–Є–ґ–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≥—А—Г–њ–њ—Л –Ї–Њ–љ—В—А–Њ–ї—П (Me 21,24 (Q25 13,68; Q75 29,44) –њ–≥/–Љ–ї; —А1<0,01; —А2<0,01), —З—В–Њ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–ї–Њ –і–µ—Д–Є—Ж–Є—В –≤—Л—А–∞–±–Њ—В–Ї–Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Ж–Є—В–Њ–Ї–Є–љ–∞ IL-35. –Я—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –∞–љ–∞–ї–Є–Ј–∞ –≤—Л—А–∞–±–Њ—В–Ї–Є IL-17A –Є -35 —Г –±–Њ–ї—М–љ—Л—Е –Ї–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ–∞—П —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –љ–Є–Љ–Є –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї–∞, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Њ –Њ –і–Є—Б–±–∞–ї–∞–љ—Б–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є.
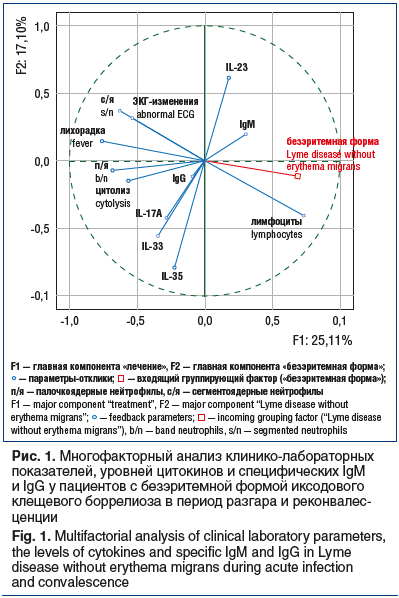
–Ф–ї—П –≤—Л—П–≤–ї–µ–љ–Є—П –љ–∞–Є–±–Њ–ї–µ–µ –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –Є–Љ–Љ—Г–љ–Њ–њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ—Л –Є–Ї—Б–Њ–і–Њ–≤–Њ–≥–Њ –Ї–ї–µ—Й–µ–≤–Њ–≥–Њ –±–Њ—А—А–µ–ї–Є–Њ–Ј–∞ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ –њ—А–Њ–≤–µ–і–µ–љ —Б–Є—Б—В–µ–Љ–љ—Л–є (–Љ–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ—Л–є) –∞–љ–∞–ї–Є–Ј –і–∞–љ–љ—Л—Е (—А–Є—Б. 1). –Я—А–Є —Н—В–Њ–Љ –Њ—Ж–µ–љ–Є–≤–∞–ї–Њ—Б—М –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ –≤—Б–µ—Е –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –Є –њ—А–Њ—Д–Є–ї—П IL-17A, -23, -33, -35 –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј–∞. –С—Л–ї–Є –≤—Л–і–µ–ї–µ–љ—Л –≥–ї–∞–≤–љ—Л–µ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л вАФ ¬Ђ—Д–Њ—А–Љ–∞¬ї –Є ¬Ђ–ї–µ—З–µ–љ–Є–µ¬ї, –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є–µ –Є–Ј–Љ–µ–љ—З–Є–≤–Њ—Б—В—М –≤—Б–µ–є —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є. –Т —Е–Њ–і–µ –Љ–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –±—Л–ї–Є –Њ–њ—А–µ–і–µ–ї–µ–љ—Л –љ–∞–Є–±–Њ–ї–µ–µ –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ—Л–µ –Є–Љ–Љ—Г–љ–Њ–њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Д–∞–Ї—В–Њ—А—Л: –ї–Є—Е–Њ—А–∞–і–Њ—З–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є, –≠–Ъ–У-–љ–∞—А—Г—И–µ–љ–Є—П, –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–µ—З–µ–љ–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є —Г—А–Њ–≤–љ–µ–є IL-23, -33, -35 –Є –љ–Є–Ј–Ї–Є–µ —Г—А–Њ–≤–љ–Є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є—В–µ–ї –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є. –Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ –њ–Њ–≤—Л—И–µ–љ–љ—Л—Е —Г—А–Њ–≤–љ–µ–є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –±–Њ—А—А–µ–ї–Є–Њ–Ј–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –љ–∞ —А–∞–љ–љ–Є—Е —Б—А–Њ–Ї–∞—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Љ–Њ–ґ–µ—В —Г–Ї–∞–Ј—Л–≤–∞—В—М –љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–µ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Њ—А–≥–∞–љ–љ—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є, –Ј–∞–Љ–µ–і–ї–µ–љ–љ—Л–є –∞–љ—В–Є—В–µ–ї–Њ–≥–µ–љ–µ–Ј.
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤
–Ъ–Є—А–Њ–≤—Б–Ї–∞—П –Њ–±–ї–∞—Б—В—М –µ–ґ–µ–≥–Њ–і–љ–Њ —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –ї–Є–і–µ—А–Њ–≤ –њ–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –Є–Ї—Б–Њ–і–Њ–≤—Л–Љ –Ї–ї–µ—Й–µ–≤—Л–Љ –±–Њ—А—А–µ–ї–Є–Њ–Ј–Њ–Љ –≤ –†–Њ—Б—Б–Є–Є (–Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –і–Њ—Б—В–Є–≥–∞–ї–Є 55,90 —Б–ї—Г—З–∞—П –љ–∞ 100 000 –љ–∞—Б–µ–ї–µ–љ–Є—П, –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л вАФ 15,03вАУ16,88 —Б–ї—Г—З–∞—П –љ–∞ 100 000 –љ–∞—Б–µ–ї–µ–љ–Є—П), —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –Ї–ї–Є–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є, –≥–µ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–Љ–Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ–Є (–Њ–±–ї–∞—Б—В—М —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–∞ –≤ –њ–Њ–і–Ј–Њ–љ–∞—Е —Б—А–µ–і–љ–µ–є –Є —О–ґ–љ–Њ–є —В–∞–є–≥–Є, –≤ —Г—Б–ї–Њ–≤–Є—П—Е —Г–Љ–µ—А–µ–љ–љ–Њ-–Ї–Њ–љ—В–Є–љ–µ–љ—В–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–Є–Љ–∞—В–∞). –Т—Л—Б–Њ–Ї–∞—П –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В—М –±–Њ—А—А–µ–ї–Є–Њ–Ј–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–µ–є —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–∞–µ—В—Б—П –љ–∞ —В–µ—А—А–Є—В–Њ—А–Є–Є –Т–Њ–ї–Њ–≥–Њ–і—Б–Ї–Њ–є –Њ–±–ї–∞—Б—В–Є (22,85вАУ23,04 —Б–ї—Г—З–∞—П –љ–∞ 100 000 –љ–∞—Б–µ–ї–µ–љ–Є—П), –Ъ–Њ—Б—В—А–Њ–Љ—Б–Ї–Њ–є –Њ–±–ї–∞—Б—В–Є (11,33вАУ17,39 —Б–ї—Г—З–∞—П –љ–∞ 100 000 –љ–∞—Б–µ–ї–µ–љ–Є—П), –†–µ—Б–њ—Г–±–ї–Є–Ї–Є –Ґ—Л–≤–∞ (23,51вАУ32,17 —Б–ї—Г—З–∞—П –љ–∞ 100 000 –љ–∞—Б–µ–ї–µ–љ–Є—П) [17]. –Ч–љ–∞—З–Є—В–µ–ї—М–љ—Г—О —З–∞—Б—В—М –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ—Б—В–∞–≤–ї—П–ї–Є –ї–Є—Ж–∞ —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, —З—В–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –≤ –і—А—Г–≥–Є—Е –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е (–≤ –Ь–Њ—Б–Ї–Њ–≤—Б–Ї–Њ–є –Њ–±–ї–∞—Б—В–Є вАФ 56%, –≤ –Я—А–Є–Љ–Њ—А—Б–Ї–Њ–Љ –Ї—А–∞–µ вАФ 79,6%) [18, 19]. –£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є—П B. garinii, B. afzelii (86,7%). –Э–∞ –≤—Л—Б–Њ–Ї—Г—О —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –±–Њ—А—А–µ–ї–Є–Њ–Ј–љ–Њ–є –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є–Є —Г–Ї–∞–Ј—Л–≤–∞—О—В —А–∞–±–Њ—В—Л —А–Њ—Б—Б–Є–є—Б–Ї–Є—Е –Є –Ј–∞—А—Г–±–µ–ґ–љ—Л—Е —Г—З–µ–љ—Л—Е [13, 18, 20, 22].
–°—А–µ–і–љ–Є–є –Є–љ–Ї—Г–±–∞—Ж–Є–Њ–љ–љ—Л–є –њ–µ—А–Є–Њ–і —Г –±–Њ–ї—М–љ—Л—Е —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј–∞ –≤ –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї 12,7 —Б—Г—В, –≤ –і—А—Г–≥–Є—Е –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е вАФ –Њ—В 11,6 –і–Њ 11,9 —Б—Г—В [18, 21]. –£ –±–Њ–ї—М–љ—Л—Е –Њ–њ—А–µ–і–µ–ї–µ–љ –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Њ–љ–љ—Л–є —Б–Є–љ–і—А–Њ–Љ (100,0%), –≠–Ъ–У-–Є–Ј–Љ–µ–љ–µ–љ–Є—П (40,0%), –±–µ–Ј–ґ–µ–ї—В—Г—И–љ—Л–є –≥–µ–њ–∞—В–Є—В (26,7%). –Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј–∞ —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–∞—О—В—Б—П –ї–Є—Е–Њ—А–∞–і–Ї–∞ (51,9вАУ100,0%), –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М (50,0вАУ85,2%) –Њ–±—Й–∞—П —Б–ї–∞–±–Њ—Б—В—М (52,9вАУ68,7%), –∞—А—В—А–∞–ї–≥–Є–Є (16,7вАУ50,0%), –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–µ—А–і—Ж–∞ (16,4вАУ84,4%) –Є –≥–µ–њ–∞—В–Є—В—Л (15вАУ31,1%) [18, 21, 23, 25].
–£ –±–Њ–ї—М–љ—Л—Е –≤ –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Њ–њ—А–µ–і–µ–ї–µ–љ—Л —Б–і–≤–Є–≥–Є –≤ –Њ–±—Й–µ–Љ –∞–љ–∞–ї–Є–Ј–µ –Ї—А–Њ–≤–Є, —З—В–Њ —П–≤–ї—П–ї–Њ—Б—М –Њ—В—А–∞–ґ–µ–љ–Є–µ–Љ –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ-–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –љ–∞—А—Г—И–µ–љ–Є–є —Б–Є—Б—В–µ–Љ—Л –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –≥–µ–љ–µ—А–∞–ї–Є–Ј–Њ–≤–∞–љ–љ–Њ–≥–Њ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞. –°—Е–Њ–і–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤—Л–і–µ–ї–µ–љ—Л —Г –±–Њ–ї—М–љ—Л—Е —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј–∞ –≤ –Я–µ—А–Љ—Б–Ї–Њ–Љ –Ї—А–∞–µ [3, 4]. –Ю–≥—А–∞–љ–Є—З–µ–љ–љ–∞—П —В–µ–љ–і–µ–љ—Ж–Є—П –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –≥—Г–Љ–Њ—А–∞–ї—М–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ —Г –±–Њ–ї—М–љ—Л—Е –Ј–∞–Ї–ї—О—З–∞–ї–∞—Б—М –≤ —Г–Љ–µ—А–µ–љ–љ–Њ–Љ –њ–Њ–≤—Л—И–µ–љ–Є–Є —Г—А–Њ–≤–љ–µ–є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є—В–µ–ї (IgM –Є IgG). –Р–љ—В–Є—В–µ–ї–Њ–≥–µ–љ–µ–Ј —Г –±–Њ–ї—М–љ—Л—Е –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј–Њ–Љ –Њ—В–Љ–µ—З–∞–µ—В—Б—П –љ–µ —А–∞–љ–µ–µ 2вАУ3 –љ–µ–і. –Њ—В –љ–∞—З–∞–ї–∞ –±–Њ–ї–µ–Ј–љ–Є, —З—В–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–≤—П–Ј–∞–љ–Њ —Б –Њ—В—Б—А–Њ—З–µ–љ–љ–Њ–є –Є —Б–ї–∞–±–Њ–≤—Л—А–∞–ґ–µ–љ–љ–Њ–є —Б–њ–Є—А–Њ—Е–µ—В–µ–Љ–Є–µ–є, –∞ —В–∞–Ї–ґ–µ —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е —Б—А–µ–і—Б—В–≤ –љ–∞ —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П [9, 24, 26]. –Т–∞–ґ–љ—Л–Љ –Ј–≤–µ–љ–Њ–Љ –Є–Љ–Љ—Г–љ–Њ–њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –±–Њ—А—А–µ–ї–Є–Њ–Ј–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є —П–≤–ї—П—О—В—Б—П –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤–Њ–Љ –њ—А–Њ—Д–Є–ї–µ —Б –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –±–∞–ї–∞–љ—Б–∞ –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–Њ–≤ [9, 10, 23вАУ25, 27]. –Ю—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –і–ї—П —Г—Б–њ–µ—И–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ –±–Њ—А—А–µ–ї–Є–Њ–Ј–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є —Б —Н–ї–Є–Љ–Є–љ–∞—Ж–Є–µ–є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ –±–∞–ї–∞–љ—Б —А–∞–љ–љ–µ–≥–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ Th1-—В–Є–њ–∞ –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ –Є –±–Њ–ї–µ–µ –њ–Њ–Ј–і–љ–µ–≥–Њ Th2-—В–Є–њ–∞ –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ—Е —А–µ–∞–Ї—Ж–Є–є [24, 28]. –Т –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–њ—А–µ–і–µ–ї–µ–љ –≤—Л—А–∞–ґ–µ–љ–љ—Л–є Th1-/Th2-–Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–є –Є–Љ–Љ—Г–љ–љ—Л–є –Њ—В–≤–µ—В (–њ–Њ–≤—Л—И–µ–љ–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е IL-23 –Є -33 –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є), –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–є –і–ї—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є —Н–ї–Є–Љ–Є–љ–∞—Ж–Є–Є –±–Њ—А—А–µ–ї–Є–є. –Ю–і–љ–∞–Ї–Њ –≤—Л—П–≤–ї–µ–љ–љ—Л–є –і–µ—Д–Є—Ж–Є—В –Є–Љ–Љ—Г–љ–Њ—Б—Г–њ—А–µ—Б—Б–Є–≤–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є (–њ–Њ–љ–Є–ґ–µ–љ–љ–∞—П –≤—Л—А–∞–±–Њ—В–Ї–∞ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ IL-35) –њ—А–Є –≤—Л—Б–Њ–Ї–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Љ–µ–і–Є–∞—В–Њ—А–∞ –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П IL-17A —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–Љ –і–ї–Є—В–µ–ї—М–љ–Њ–Љ —Б–Њ—Е—А–∞–љ–µ–љ–Є–Є –Є–Љ–Љ—Г–љ–Њ–њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤.
–Т—Л–≤–Њ–і—Л
–Т –Ъ–Є—А–Њ–≤—Б–Ї–Њ–є –Њ–±–ї–∞—Б—В–Є –Љ–љ–Њ–≥–Њ–ї–µ—В–љ—П—П –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В—М –±–Њ—А—А–µ–ї–Є–Њ–Ј–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–µ–є –њ—А–µ–≤—Л—И–∞–µ—В —Б—А–µ–і–љ–µ—А–Њ—Б—Б–Є–є—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≤ 2,6вАУ8,2 —А–∞–Ј–∞. –°—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј–∞ –њ—А–µ–Њ–±–ї–∞–і–∞–µ—В —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ–µ –љ–∞—Б–µ–ї–µ–љ–Є–µ (80,0%), –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є—П
B. garinii, B. afzelii (76,7%).
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –Ы–∞–є–Љ-–±–Њ—А—А–µ–ї–Є–Њ–Ј–∞ –≤ –њ–µ—А–Є–Њ–і —А–∞–Ј–≥–∞—А–∞ –Є –њ–µ—А–Є–Њ–і —А–µ–Ї–Њ–љ–≤–∞–ї–µ—Б—Ж–µ–љ—Ж–Є–Є –≤—Л—А–∞–ґ–µ–љ—Л –љ–∞—А—Г—И–µ–љ–Є—П –≤ —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤–Њ–Љ –њ—А–Њ—Д–Є–ї–µ: –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ IL-17A, -23 –Є -33 —Б –і–µ—Д–Є—Ж–Є—В–Њ–Љ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Є–Љ–Љ—Г–љ–Њ—Б—Г–њ—А–µ—Б—Б–Є–≤–љ–Њ–≥–Њ IL-35.
–Я—А–Є –Љ–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–µ–Ј—Н—А–Є—В–µ–Љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –±–Њ—А—А–µ–ї–Є–Њ–Ј–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Є–Љ–Љ—Г–љ–Њ–њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–і–≤–Є–≥–Њ–≤ —Б –ї–Є—Е–Њ—А–∞–і–Њ—З–љ—Л–Љ–Є —А–µ–∞–Ї—Ж–Є—П–Љ–Є, –њ–Њ—А–∞–ґ–µ–љ–Є—П–Љ–Є —Б–µ—А–і—Ж–∞ –Є –њ–µ—З–µ–љ–Є, –≤—Л—Б–Њ–Ї–Є–Љ–Є —Г—А–Њ–≤–љ—П–Љ–Є IL-23 –Є -33, –∞ —В–∞–Ї–ґ–µ —Б –і–µ—Д–Є—Ж–Є—В–Њ–Љ –≤—Л—А–∞–±–Њ—В–Ї–Є IL-35 –Є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є—В–µ–ї IgM, IgG.
–°–≤–µ–і–µ–љ–Є—П –Њ–± –∞–≤—В–Њ—А–∞—Е:
–°–∞–њ–Њ–ґ–љ–Є–Ї–Њ–≤–∞ –Т–µ—А–∞ –Т–Є–Ї—В–Њ—А–Њ–≤–љ–∞ вАФ –Ї.–Љ.–љ., –∞—Б—Б–Є—Б—В–µ–љ—В –Ї–∞—Д–µ–і—А—Л –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –±–Њ–ї–µ–Ј–љ–µ–є –§–У–С–Ю–£ –Т–Ю –Ъ–Є—А–Њ–≤—Б–Ї–Є–є –У–Ь–£ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є; 610027, –†–Њ—Б—Б–Є—П, –≥. –Ъ–Є—А–Њ–≤, —Г–ї. –Ъ. –Ь–∞—А–Ї—Б–∞, –і. 112; ORCID iD 0000-0002-3930-0460.
–С–Њ–љ–і–∞—А–µ–љ–Ї–Њ –Р–ї–ї–∞ –Ы—М–≤–Њ–≤–љ–∞ вАФ –і.–Љ.–љ., –њ—А–Њ—Д–µ—Б—Б–Њ—А, –Ј–∞–≤–µ–і—Г—О—Й–∞—П –Ї–∞—Д–µ–і—А–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –±–Њ–ї–µ–Ј–љ–µ–є –§–У–С–Ю–£ –Т–Ю –Ъ–Є—А–Њ–≤—Б–Ї–Є–є –У–Ь–£ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є; 610027, –†–Њ—Б—Б–Є—П, –≥. –Ъ–Є—А–Њ–≤, —Г–ї. –Ъ. –Ь–∞—А–Ї—Б–∞, –і. 112; ORCID iD 0000-0002-9151-604X.
–Ъ–Њ–љ—В–∞–Ї—В–љ–∞—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П: –°–∞–њ–Њ–ґ–љ–Є–Ї–Њ–≤–∞ –Т–µ—А–∞ –Т–Є–Ї—В–Њ—А–Њ–≤–љ–∞, e-mail: v_v_sapozhnikova@mail.ru. –Я—А–Њ–Ј—А–∞—З–љ–Њ—Б—В—М —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є: –љ–Є–Ї—В–Њ –Є–Ј –∞–≤—В–Њ—А–Њ–≤ –љ–µ –Є–Љ–µ–µ—В —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –Ј–∞–Є–љ—В–µ—А–µ—Б–Њ–≤–∞–љ–љ–Њ—Б—В–Є –≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –Љ–∞—В–µ—А–Є–∞–ї–∞—Е –Є–ї–Є –Љ–µ—В–Њ–і–∞—Е. –Ъ–Њ–љ—Д–ї–Є–Ї—В –Є–љ—В–µ—А–µ—Б–Њ–≤ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В. –°—В–∞—В—М—П –њ–Њ—Б—В—Г–њ–Є–ї–∞ 15.09.2019, –њ–Њ—Б—В—Г–њ–Є–ї–∞ –њ–Њ—Б–ї–µ —А–µ—Ж–µ–љ–Ј–Є—А–Њ–≤–∞–љ–Є—П 03.10.2019, –њ—А–Є–љ—П—В–∞ –≤ –њ–µ—З–∞—В—М 18.01.2020.
About the authors:
Vera V. Sapozhnikova вАФ Cand. of Sci. (Med.), assistant of the Department of Infectious Diseases, Kirov State Medical University, 112, Karl Marx str., Kirov, 610027, Russian Federation; ORCID iD 0000-0002-3930-0460.
Alla L. Bondarenko вАФ Doct. of Sci. (Med.), Professor, Head of the Department of Infectious Diseases, Kirov State Medical University, 112, Karl Marx str., Kirov, 610027, Russian Federation; ORCID iD 0000-0002-9151-604X.
Contact information: Vera V. Sapozhnikova, e-mail: v_v_sapozhnikova@mail.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 15.09.2019, revised 03.10.2019, accepted 18.01.2020.












