–Р–Љ–Є–Ї—Б–Є–љ (—В–Є–ї–Њ—А–Њ–љ) вАФ –љ–Є–Ј–Ї–Њ–Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–є —Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–є –Є–љ–і—Г–Ї—В–Њ—А —Б–Є–љ—В–µ–Ј–∞ –Є–љ—В–µ—А—Д–µ—А–Њ–љ–∞ (–Ш–§–Э), –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –Ї–ї–∞—Б—Б—Г —Д–ї—Г–Њ—А–µ–љ–Њ–љ–Њ–≤. –Х–≥–Њ
–°–µ–Љ–µ–є—Б—В–≤–Њ –Ш–§–Э —П–≤–ї—П–µ—В—Б—П –Ї–ї—О—З–µ–≤—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ –≤—А–Њ–ґ–і–µ–љ–љ–Њ–≥–Њ –Є –∞–і–∞–њ—В–Є–≤–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–µ–≥–Њ –њ–µ—А–≤—Г—О –ї–Є–љ–Є—О –Ј–∞—Й–Є—В—Л –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Њ—В —А–∞–Ј–ї–Є—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –∞–≥–µ–љ—В–Њ–≤ [5].
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ—Л 3 —В–Є–њ–∞ –Ш–§–Э:
1. –Ш–§–Э
2. –Ш–§–Э
3. –Э–µ–і–∞–≤–љ–Њ –Њ—В–Ї—А—Л—В—Л–є
–Т—Б–µ 3 —В–Є–њ–∞ –Ш–§–Э –≤—Л–њ–Њ–ї–љ—П—О—В —А–Њ–ї—М –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –Ј–∞—Й–Є—В—Л –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –љ–µ —В–Њ–ї—М–Ї–Њ –њ—А–Є –≤–Є—А—Г—Б–љ—Л—Е, –љ–Њ –Є –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –Є –њ–∞—А–∞–Ј–Є—В–∞—А–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е [15, 16]. –Т–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Ш–§–Э –њ—А–Њ–і—Г—Ж–Є—А—Г—О—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –њ—А–Є —А–∞–Ј–ї–Є—З–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –љ–Њ –Є –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ —А—П–і–∞ –≤—Л—Б–Њ–Ї–Њ- –Є –љ–Є–Ј–Ї–Њ–Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є вАФ –Є–љ–і—Г–Ї—В–Њ—А–Њ–≤ –Ш–§–Э [3, 4].
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Р–Љ–Є–Ї—Б–Є–љ —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В –≤—Л—А–∞–±–Њ—В–Ї—Г –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е –Ш–§–Э, –Ї–Њ—В–Њ—А—Л–µ –≤ —А–∞–љ–љ–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —В–µ—Б—В–Є—А–Њ–≤–∞–ї–Є—Б—М –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Љ–µ—В–Њ–і–Њ–Љ вАФ –њ–Њ –њ—А–Њ—В–Є–≤–Њ–≤–Є—А—Г—Б–љ–Њ–Љ—Г –і–µ–є—Б—В–≤–Є—О вАФ –Є –±—Л–ї–Є –Њ—В–љ–µ—Б–µ–љ—Л –Ї –Ш–§–Э -ќ±, -ќ≤ (
–Ф–ї—П –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–љ–і—Г–Ї—В–Њ—А–∞ –Ш–§–Э –Р–Љ–Є–Ї—Б–Є–љ–∞ –њ—А–µ–і—Б—В–∞–≤–ї—П–ї–Њ—Б—М —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –≤ —А–∞–Љ–Ї–∞—Е –і–Њ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤ —Б—В—А–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е, –Њ—Б–љ–Њ–≤–∞–љ–љ—Л—Е –љ–∞ –њ—А–Є–љ—Ж–Є–њ–∞—Е –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л, –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –Є –њ—А–Њ–≤–µ—Б—В–Є —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–µ –Є–Ј—Г—З–µ–љ–Є–µ –Є–љ–і—Г–Ї—Ж–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Р–Љ–Є–Ї—Б–Є–љ –Ш–§–Э -ќ± (
–¶–µ–ї—М –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П вАФ –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –љ–∞ –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–Љ —Г—А–Њ–≤–љ–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ –њ–Њ –Є–љ–і—Г–Ї—Ж–Є–Є –Ш–§–Э -ќ± –Є -ќ≤ (
–Ь–∞—В–µ—А–Є–∞–ї—Л –Є –Љ–µ—В–Њ–і—Л
–Ф–Є–Ј–∞–є–љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –≤ 2 —Н—В–∞–њ–∞. –Я–µ—А–≤—Л–є —Н—В–∞–њ вАФ –≤ –Ш–љ—Б—В–Є—В—Г—В–µ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ—В–µ–Ј–∞ –Ы–∞—В–≤–Є–Є (–≥. –†–Є–≥–∞), –≤–Ї–ї—О—З–∞–ї –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –і–Є–љ–∞–Љ–Є–Ї–Є –Є–љ–і—Г–Ї—Ж–Є–Є –Є –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Ш–§–Э -ќ±, -ќ≤, -ќ≥ –Є -ќї –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Р–Љ–Є–Ї—Б–Є–љ –≤ –і–Њ–Ј–∞—Е 40 –Є 400 –Љ–≥/–Ї–≥ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Љ—Л—И–µ–є –≤ —В–µ—З–µ–љ–Є–µ 120 —З.
–Т—В–Њ—А–Њ–є —Н—В–∞–њ вАФ –≤ –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –Є–љ–і—Г–Ї—В–Њ—А–Њ–≤ –Є–љ—В–µ—А—Д–µ—А–Њ–љ–∞ –§–У–С–£ ¬Ђ–§–Э–Ш–¶–≠–Ь –Є–Љ.
–Ц–Є–≤–Њ—В–љ—Л–µ
–Э–∞ –њ–µ—А–≤–Њ–Љ —Н—В–∞–њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М —Б–∞–Љ–Ї–Є 55 –Љ—Л—И–µ–є –ї–Є–љ–Є–Є –°–Т–Р/–°–∞–ЮlaHsd –≤–µ—Б–Њ–Љ 19вАУ30 –≥, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –Є–Ј –≤–Є–≤–∞—А–Є—П Harlan Laboratories, –Э–Є–і–µ—А–ї–∞–љ–і—Л.
–Э–∞ –≤—В–Њ—А–Њ–Љ —Н—В–∞–њ–µ вАФ —Б–∞–Љ–Ї–Є 85 –Љ—Л—И–µ–є –ї–Є–љ–Є–Є –°–Т–Р/CaOlaHsd –≤–µ—Б–Њ–Љ 18вАУ20 –≥, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –Є–Ј –њ–Є—В–Њ–Љ–љ–Є–Ї–∞ ¬Ђ–Р–љ–і—А–µ–µ–≤–Ї–∞¬ї (–§–У–С–£ ¬Ђ–Э–¶–С–Ь–Ґ¬ї –†–Р–Ь–Э).
–°–Њ–і–µ—А–ґ–∞–љ–Є–µ –ґ–Є–≤–Њ—В–љ—Л—Е
–°–Њ–і–µ—А–ґ–∞–љ–Є–µ, –њ–Є—В–∞–љ–Є–µ –Є —Г—Е–Њ–і –Ј–∞ –ґ–Є–≤–Њ—В–љ—Л–Љ–Є –≤ —Е–Њ–і–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–Є—Б—М –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б —В—А–µ–±–Њ–≤–∞–љ–Є—П–Љ–Є ¬Ђ–Я—А–∞–≤–Є–ї –њ—А–Њ–≤–µ–і–µ–љ–Є—П —А–∞–±–Њ—В —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –ґ–Є–≤–Њ—В–љ—Л—Е¬ї, –Я—А–Є–Ї–∞–Ј –Ь–Є–љ–Ј–і—А–∞–≤—Б–Њ—Ж—А–∞–Ј–≤–Є—В–Є—П –†–§ –Њ—В 23 –∞–≤–≥—Г—Б—В–∞ 2010 –≥. вДЦ 708–љ. –≠—В–Є—З–µ—Б–Ї–Є–µ –њ—А–Є–љ—Ж–Є–њ—Л –Њ–±—А–∞—Й–µ–љ–Є—П —Б –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–Љ–Є –ґ–Є–≤–Њ—В–љ—Л–Љ–Є —Б–Њ–±–ї—О–і–∞–ї–Є—Б—М –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б European Convention for the Protection of Vertebral Animals Used for Experimental and Other Scientific Purposes. CETS No.123. –Я–µ—А–µ–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ –ґ–Є–≤–Њ—В–љ—Л–µ –њ–Њ–і–≤–µ—А–≥–∞–ї–Є—Б—М
–Ш—Б—Б–ї–µ–і—Г–µ–Љ—Л–є –њ—А–µ–њ–∞—А–∞—В
–Р–Љ–Є–Ї—Б–Є–љ¬Ѓ (—В–Є–ї–Њ—А–Њ–љ) вАФ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–∞—П —Д–Њ—А–Љ–∞: —В–∞–±–ї–µ—В–Ї–Є, –њ–Њ–Ї—А—Л—В—Л–µ –њ–ї–µ–љ–Њ—З–љ–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Њ–є, 125 –Љ–≥,
–Я—А–Њ—Ж–µ–і—Г—А–∞ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞
–Ш—Б—Б–ї–µ–і—Г–µ–Љ—Л–є –њ—А–µ–њ–∞—А–∞—В —А–∞—Б—В–≤–Њ—А—П–ї–Є –≤ —Б—В–µ—А–Є–ї—М–љ–Њ–є –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і–µ –≤ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П—Е, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е –≤–≤–Њ–і–Є–Љ—Л–Љ –і–Њ–Ј–∞–Љ: 20, 40, 400 –Љ–≥/–Ї–≥. –≠–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –ґ–Є–≤–Њ—В–љ—Л–µ —А–∞—Б–њ—А–µ–і–µ–ї—П–ї–Є—Б—М –љ–∞ 2 –Є–ї–Є 3 –≥—А—Г–њ–њ—Л, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ —Н—В–∞–њ—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Є –і–Њ–Ј–∞–Љ –≤–≤–Њ–і–Є–Љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞. –Я–Њ–і–±–Њ—А –ґ–Є–≤–Њ—В–љ—Л—Е –≤ –≥—А—Г–њ–њ—Л –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї—Б—П –Љ–µ—В–Њ–і–Њ–Љ —Б–ї—Г—З–∞–є–љ–Њ–є –≤—Л–±–Њ—А–Ї–Є. –Ъ–∞–ґ–і–∞—П –і–Њ–Ј–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –Р–Љ–Є–Ї—Б–Є–љ –≤–≤–Њ–і–Є–ї–∞—Б—М –Љ—Л—И–∞–Љ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ (–≤–љ—Г—В—А–Є–ґ–µ–ї—Г–і–Њ—З–љ–Њ) –≤ –Њ–±—К–µ–Љ–µ 50 –Љ–Ї–ї —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л–Љ–Є –і–Њ–Ј–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є –Ј–Њ–љ–і–∞–Љ–Є —А–∞–Ј–Љ–µ—А–∞–Љ–Є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–Љ–Є —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –і–ї–Є–љ–µ –њ–Є—Й–µ–≤–Њ–і–∞ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Љ—Л—И–µ–є. –Э–∞ –Ї–∞–ґ–і—Л–є —Б—А–Њ–Ї –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М –њ–Њ 3 –Љ—Л—И–Є.
–Я–Њ–ї—Г—З–µ–љ–Є–µ –Њ–±—А–∞–Ј—Ж–Њ–≤ —Б—Л–≤–Њ—А–Њ—В–Ї–Є –Є —Б—Г—Б–њ–µ–љ–Ј–Є–Є –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є
–Ь—Л—И–µ–є –≤—Л–і–µ—А–ґ–Є–≤–∞–ї–Є –њ–Њ–і –ї–µ–≥–Ї–Є–Љ —Н—Д–Є—А–љ—Л–Љ –љ–∞—А–Ї–Њ–Ј–Њ–Љ –і–Њ –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є—П –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤. –Ч–∞–±–Њ—А –Ї—А–Њ–≤–Є –њ—А–Њ–≤–Њ–і–Є–ї–Є –Љ–µ—В–Њ–і–Њ–Љ –і–µ–Ї–∞–њ–Є—В–∞—Ж–Є–Є –≤ —Б—В–µ—А–Є–ї—М–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е. –Ю–±—А–∞–Ј—Ж—Л –Ї—А–Њ–≤–Є, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –≤ –Ї–∞–ґ–і—Л–є —Б—А–Њ–Ї –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —Б–Њ—Б—В–Њ—П–ї–Є –Є–Ј –њ—Г–ї–∞ (—Б–Љ–µ—Б–Є) –Ї—А–Њ–≤–Є –Њ—В 3 –Љ—Л—И–µ–є –≤ –Њ–±—К–µ–Љ–µ 3 –Љ–ї (–њ–Њ 1 –Љ–ї –Њ—В –Ї–∞–ґ–і–Њ–є –Њ—Б–Њ–±–Є), –Є–Ј –Ї–Њ—В–Њ—А–Њ–≥–Њ –њ–Њ—Б–ї–µ —Ж–µ–љ—В—А–Є—Д—Г–≥–Є—А–Њ–≤–∞–љ–Є—П –≤ —А–µ–ґ–Є–Љ–µ 5000 –Њ–±/–Љ–Є–љ 15 –Љ–Є–љ –Њ—В–±–Є—А–∞–ї–Є –љ–∞–і–Њ—Б–∞–і–Њ—З–љ—Г—О —Б—Л–≤–Њ—А–Њ—В–Ї—Г –≤ –Њ–±—К–µ–Љ–µ 1,0 –Љ–ї –≤ —Б—В–µ—А–Є–ї—М–љ—Л–µ –њ—А–Њ–±–Є—А–Ї–Є —В–Є–њ–∞ –≠–њ–њ–µ–љ–і–Њ—А—Д. –°—Л–≤–Њ—А–Њ—В–Ї–Є –Ї—А–Њ–≤–Є –Љ—Л—И–µ–є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–µ –Ї–∞–ґ–і–Њ–Љ—Г —Б—А–Њ–Ї—Г –Ј–∞–±–Њ—А–∞, —А–∞–Ј–і–µ–ї—П–ї–Є –љ–∞ –∞–ї–Є–Ї–≤–Њ—В—Л –њ–Њ 0,3 –Љ–ї –≤ 3 —Б—В–µ—А–Є–ї—М–љ—Л–µ –њ—А–Њ–±–Є—А–Ї–Є –≠–њ–њ–µ–љ–і–Њ—А—Д, –Ї–∞–ґ–і—Г—О –Є–Ј –Ї–Њ—В–Њ—А—Л—Е —Е—А–∞–љ–Є–ї–Є –њ—А–Є t -70¬∞C –і–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–≥–Њ –Є–Љ–Љ—Г–љ–Њ—Д–µ—А–Љ–µ–љ—В–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ (–Ш–§–Р). –Ф–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П —Б—Г—Б–њ–µ–љ–Ј–Є–Є –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Њ–±–µ—Б–Ї—А–Њ–≤–ї–µ–љ–љ—Л—Е –Љ—Л—И–µ–є —Д–Є–Ї—Б–Є—А–Њ–≤–∞–ї–Є –љ–∞ —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л—Е –њ–∞—А–∞—Д–Є–љ–Њ–≤—Л—Е –њ–Њ–і–ї–Њ–ґ–Ї–∞—Е, –≤ –∞—Б–µ–њ—В–Є—З–µ—Б–Ї–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е –≤—Б–Ї—А—Л–≤–∞–ї–∞—Б—М –≥—А—Г–і–љ–∞—П –Ї–ї–µ—В–Ї–∞, –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–ї–Є—Б—М –Є –Є–Ј–≤–ї–µ–Ї–∞–ї–Є—Б—М –ї–µ–≥–Ї–Є–µ (–њ—А–∞–≤–Њ–µ –Є –ї–µ–≤–Њ–µ), –Ї–Њ—В–Њ—А—Л–µ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ —В—А–µ—Е–Ї—А–∞—В–љ–Њ –њ—А–Њ–Љ—Л–≤–∞–ї–Є –≤ –±—Г—Д–µ—А–µ Hepes –Є –њ–Є—В–∞—В–µ–ї—М–љ–Њ–є —Б—А–µ–і–µ вДЦ 199, –≤–Ј–≤–µ—И–Є–≤–∞–ї–Є –Є —А–∞–Ј–Љ–µ–ї—М—З–∞–ї–Є —Б–љ–∞—З–∞–ї–∞ –≤ —Б—В—Г–њ–Ї–µ, –∞ –Ј–∞—В–µ–Љ –≤ —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ–Љ –≥–Њ–Љ–Њ–≥–µ–љ–Є–Ј–∞—В–Њ—А–µ. –Т—Б–µ –њ—А–Њ—Ж–µ–і—Г—А—Л –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –≤ –Ї—А–∞—В—З–∞–є—И–Є–µ —Б—А–Њ–Ї–Є –Є –љ–∞ —Е–Њ–ї–Њ–і–µ. –†–∞–Ј—А—Г—И–µ–љ–Є–µ –Ї–ї–µ—В–Њ–Ї —В–Ї–∞–љ–Є –ї–µ–≥–Ї–Њ–≥–Њ –і–Њ—Б—В–Є–≥–∞–ї–Њ—Б—М —В—А–µ—Е–Ї—А–∞—В–љ—Л–Љ –Ј–∞–Љ–Њ—А–∞–ґ–Є–≤–∞–љ–Є–µ–Љ –Є –Њ—В—В–∞–Є–≤–∞–љ–Є–µ–Љ. –У–Њ—В–Њ–≤–Є–ї–∞—Б—М 10% —Б—Г—Б–њ–µ–љ–Ј–Є—П –≥–Њ–Љ–Њ–≥–µ–љ–∞—В–∞ –≤ –њ–Є—В–∞—В–µ–ї—М–љ–Њ–є —Б—А–µ–і–µ вДЦ 199. –°—Г–њ–µ—А–љ–∞—В–∞–љ—В—Л —Б—Г—Б–њ–µ–љ–Ј–Є–Є –≥–Њ–Љ–Њ–≥–µ–љ–∞—В–∞ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –њ–Њ—Б–ї–µ –љ–Є–Ј–Ї–Њ—Б–Ї–Њ—А–Њ—Б—В–љ–Њ–≥–Њ —Ж–µ–љ—В—А–Є—Д—Г–≥–Є—А–Њ–≤–∞–љ–Є—П (–њ—А–Є 1600 g –≤ —В–µ—З–µ–љ–Є–µ 30 –Љ–Є–љ) –Њ—В–±–Є—А–∞–ї–Є –Є –Ј–∞–Љ–Њ—А–∞–ґ–Є–≤–∞–ї–Є –њ—А–Є -70¬∞–° –і–Њ –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Љ–µ—В–Њ–і–Њ–Љ –Ш–§–Р.
–Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Ш–§–Э –∞–ї—М—Д–∞, –±–µ—В–∞, –≥–∞–Љ–Љ–∞ –Є –ї—П–Љ–±–і–∞ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Є –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є
–°–Њ–і–µ—А–ґ–∞–љ–Є–µ –Ш–§–Э -ќ±, -ќ≤, -ќ≥ –Є -ќї2/3 –≤ –њ—А–Њ–±–∞—Е —Б—Л–≤–Њ—А–Њ—В–Њ–Ї –Є —Б—Г–њ–µ—А–љ–∞—В–∞–љ—В–Њ–≤ 10% —Б—Г—Б–њ–µ–љ–Ј–Є–Є –≥–Њ–Љ–Њ–≥–µ–љ–∞—В–Њ–≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –Њ–њ—А–µ–і–µ–ї—П–ї–Њ—Б—М –≤ 9 –≤—А–µ–Љ–µ–љ–љ—Л—Е —Б—А–Њ–Ї–∞—Е (0 —З, 4 —З, 8 —З, 12 —З, 24 —З, 48 —З, 72 —З, 96 —З, 120 —З вАФ 3 –Љ—Л—И–Є –≤ –Ї–∞–ґ–і—Л–є —Б—А–Њ–Ї) –њ–Њ—Б–ї–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ (–≤–љ—Г—В—А–Є–ґ–µ–ї—Г–і–Њ—З–љ–Њ–≥–Њ) –≤–≤–µ–і–µ–љ–Є—П –Р–Љ–Є–Ї—Б–Є–љ–∞ –≤ –і–Њ–Ј–∞—Е 20, 40, 400 –Љ–≥/–Ї–≥.
–Ъ–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Ш–§–Э -ќ±, -ќ≤, -ќ≥ –Є -ќї2/3 (
- Mouse Interferon Alpha ELISA Kit; R & D Systems; –°–®–Р.
- Mouse IFN-ќ≤ ELISA Kit; PBL Interferon Source; –°–®–Р.
- Mouse IFN-ќ≥ ELISA Kit; R&D Systems Europe LTD; –Т–µ–ї–Є–Ї–Њ–±—А–Є—В–∞–љ–Є—П.
- DuoSet¬Ѓ ELISA; Mouse IL-28A/B (IFN-ќї2/3) Kit; R&D Systems; C–®–Р.
–†–∞—Б—З–µ—В –Њ–њ—В–Є—З–µ—Б–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –њ—А–Њ–± –њ—А–Њ–≤–Њ–і–Є–ї–Є –љ–∞ —Б–њ–µ–Ї—В—А–Њ—Д–Њ—В–Њ–Љ–µ—В—А–µ вАФ —А–Є–і–µ—А–µ Anthos Labtec c –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –≤–Њ—И–µ—А–∞ –Є —И–µ–є–Ї–µ—А–∞ (Instruments GmbH, Austria) —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є –Њ–±—А–∞–±–Њ—В–Ї–Њ–є –Є –њ—А–µ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –і–∞–љ–љ—Л—Е –Њ–њ—В–Є—З–µ—Б–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є –≤ –њ–Є–Ї–Њ–≥—А–∞–Љ–Љ—Л –≤ –Љ–ї –Є –Љ–≥ (–њ–Ї–≥/–Љ–ї –Є –њ–Ї–≥/ –Љ–≥) –њ–Њ –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ–µ Software ADAP. –Т—Б–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї–Є –≤
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–∞—П –Њ–±—А–∞–±–Њ—В–Ї–∞
–†–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–і–≤–µ—А–≥–∞–ї–Є—Б—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Њ–±—А–∞–±–Њ—В–Ї–µ –њ—Г—В–µ–Љ —А–∞—Б—З–µ—В–∞ —Б—А–µ–і–љ–µ–≥–Њ –∞—А–Є—Д–Љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П (M) –Є —Б—В–∞–љ–і–∞—А—В–љ–Њ–є –Њ—И–Є–±–Ї–Є –Ї –љ–µ–Љ—Г (¬±ѕГ). –Ю—Ж–µ–љ–Ї–∞ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є —А–∞–Ј–ї–Є—З–Є–є –њ—А–Є –Љ–µ–ґ–≥—А—Г–њ–њ–Њ–≤—Л—Е —Б—А–∞–≤–љ–µ–љ–Є—П—Е –њ—А–Њ–Є–Ј–≤–Њ–і–Є–ї–∞—Б—М –њ–Њ –і–≤—Г—Б—В–Њ—А–Њ–љ–љ–µ–Љ—Г
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є
–Ш–љ–і—Г–Ї—Ж–Є—П –Є–љ—В–µ—А—Д–µ—А–Њ–љ–Њ–≤ –∞–ї—М—Д–∞, –±–µ—В–∞, –≥–∞–Љ–Љ–∞ –Є –ї—П–Љ–±–і–∞ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Љ—Л—И–µ–є –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Р–Љ–Є–Ї—Б–Є–љ
–Ю–і–љ–Њ–Ї—А–∞—В–љ–Њ–µ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –Р–Љ–Є–Ї—Б–Є–љ–∞ –≤ –і–Њ–Ј–∞—Е 40 –Є 400 –Љ–≥/–Ї–≥ –≤—Л–Ј—Л–≤–∞–ї–Њ –і–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ—Г—О –Є–љ–і—Г–Ї—Ж–Є—О –Є –њ—А–Њ–і—Г–Ї—Ж–Є—О –Ш–§–Э -ќ± –Є -ќї2/3 –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Љ—Л—И–µ–є, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Ї–Њ—В–Њ—А—Л—Е —З–µ—А–µ–Ј 24 —З –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –і–Њ–Ј–µ 40 –Љ–≥/–Ї–≥ —Б–Њ—Б—В–∞–≤–ї—П–ї–Њ 176¬±1,0 –Є 398¬±12,0 –њ–Ї–≥/–Љ–ї, –∞ –≤ –і–Њ–Ј–µ 400 –Љ–≥/–Ї–≥ вАФ 1337¬±93 –Є 2231¬±93 –њ–Ї–≥/–Љ–ї —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –£—А–Њ–≤–µ–љ—М –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Ш–§–Э-ќї2/3 –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Љ—Л—И–µ–є –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Р–Љ–Є–Ї—Б–Є–љ–∞ –≤ –і–Њ–Ј–µ 40 –Є 400 –Љ–≥/–Ї–≥ –≤ —Н—В–Њ—В —Б—А–Њ–Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ (–≤ 7,5 –Є 5,6 —А–∞–Ј–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ) –њ—А–µ–≤—Л—И–∞–ї —В–∞–Ї–Њ–≤–Њ–є –Ш–§–Э-ќ± (—А–Є—Б. 1).
–°–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М –≤ –Є–љ–і—Г–Ї—Ж–Є–Є –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Р–Љ–Є–Ї—Б–Є–љ–∞ –Є –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–Є –≤ –Ї—А–Њ–≤–Є –Ш–§–Э -ќ≤ –Є -ќ≥, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Ї–Њ—В–Њ—А—Л—Е –і–Њ—Б—В–Є–≥–∞–ї—Б—П —В–∞–Ї–ґ–µ —З–µ—А–µ–Ј 24 —З –њ–Њ—Б–ї–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞. –Ю–і–љ–∞–Ї–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Ш–§–Э -ќ≤ –Є -ќ≥ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –ґ–Є–≤–Њ—В–љ—Л—Е –љ–∞ –њ–Є–Ї–µ –њ—А–Њ–і—Г–Ї—Ж–Є–Є —В–µ—Б—В–Є—А–Њ–≤–∞–ї–Њ—Б—М –љ–∞ –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Њ–Љ —Г—А–Њ–≤–љ–µ, —З–µ–Љ —В–∞–Ї–Њ–≤–Њ–µ –Ш–§–Э-ќ± –Є -ќї2/3. –Я—А–Є –і–Њ–Ј–µ –Р–Љ–Є–Ї—Б–Є–љ–∞ 40 –Љ–≥/–Ї–≥ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М —Б–Є–љ—В–µ–Ј–∞ –Ш–§–Э-ќ≤, –Ї–∞–Ї –Є –Ш–§–Э-ќ≥, –≤ –Ї—А–Њ–≤–Є –Њ–њ—А–µ–і–µ–ї—П–ї—Б—П –љ–∞ —Г—А–Њ–≤–љ–µ —Д–Њ–љ–Њ–≤—Л—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –Ј–љ–∞—З–µ–љ–Є–є (8,1¬±4,3 –Є 4,4¬±1,2 –њ–Ї–≥/–Љ–ї —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ). –Я—А–Є –і–Њ–Ј–µ 400 –Љ–≥/–Ї–≥ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Ш–§–Э-ќ≤ –Є -ќ≥ —З–µ—А–µ–Ј 24 —З –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Є—Б—М –≤ —Б—А–µ–і–љ–µ–Љ –≤ 10 —А–∞–Ј –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –і–Њ–Ј—Л 40 –Љ–≥/–Ї–≥, –∞ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –Ї–Њ–љ—В—А–Њ–ї—П вАФ –≤ 110 –Є 46 —А–∞–Ј —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ (—А–Є—Б. 2).

–Я–Њ —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В–Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –љ–∞ —А–Є—Б—Г–љ–Ї–∞—Е 1 –Є 2, –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–µ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –Р–Љ–Є–Ї—Б–Є–љ–∞ –≤ –і–Њ–Ј–∞—Е 40 –Є 400 –Љ–≥/–Ї–≥ –≤—Л–Ј—Л–≤–∞–ї–Њ –Є–љ–і—Г–Ї—Ж–Є—О –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –ґ–Є–≤–Њ—В–љ—Л—Е –≤—Б–µ—Е —В–Є–њ–Њ–≤: -ќ±, -ќ≤, -ќ≥, -ќї, –љ–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Ш–§–Э -ќї –Є -ќ± –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є–ї–Њ —В–∞–Ї–Њ–≤–Њ–µ –Ш–§–Э-ќ≤ –Є -ќ≥ –≤ —Б—А–µ–і–љ–µ–Љ –≤ 10 —А–∞–Ј.
–Ш–љ–і—Г–Ї—Ж–Є—П –Є–љ—В–µ—А—Д–µ—А–Њ–љ–∞ –∞–ї—М—Д–∞ –Є –ї—П–Љ–±–і–∞ –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Р–Љ–Є–Ї—Б–Є–љ
–Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –њ–µ—А–≤–Њ–≥–Њ —Н—В–∞–њ–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –±—Л–ї–Є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ—Л –Є–љ–і—Г–Ї—Ж–Є—П –Р–Љ–Є–Ї—Б–Є–љ–Њ–Љ –≤—Б–µ—Е
–Ш–љ–Є—Ж–Є–∞—Ж–Є—П –Є–љ–і—Г–Ї—Ж–Є–Є –Ш–§–Э-ќ± –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –≤—Л—А–∞–ґ–∞–ї–∞—Б—М –≤ –і–≤—Г—Е–Ї—А–∞—В–љ–Њ–Љ –њ–Њ–≤—Л—И–µ–љ–Є–Є —З–µ—А–µ–Ј 24 —З –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П –Р–Љ–Є–Ї—Б–Є–љ–∞ –≤ –і–Њ–Ј–µ 400 –Љ–≥/–Ї–≥ —Б—А–µ–і–љ–µ—Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є—Е –Ј–љ–∞—З–µ–љ–Є–є –µ–≥–Њ –≤—Л—А–∞–±–Њ—В–Ї–Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ—Г–ї–µ–≤–Њ–є —В–Њ—З–Ї–Є, –∞ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ (1125 –њ–Ї–≥/–Љ–≥) —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–ї–Є—Б—М –Є –∞–Ї–Ї—Г–Љ—Г–ї–Є—А–Њ–≤–∞–ї–Є—Б—М —В–Њ–ї—М–Ї–Њ —З–µ—А–µ–Ј 48 —З –њ–Њ—Б–ї–µ –Є–љ–і—Г–Ї—Ж–Є–Є —В–Њ–є –ґ–µ –і–Њ–Ј–Њ–є –њ—А–µ–њ–∞—А–∞—В–∞ (—А–Є—Б. 3).

–Э–Є–Ј–Ї–∞—П –і–Њ–Ј–∞ –њ—А–µ–њ–∞—А–∞—В–∞ —В–∞–Ї–ґ–µ –≤—Л–Ј—Л–≤–∞–ї–∞ –і–≤—Г—Е–Ї—А–∞—В–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Ш–§–Э-ќ± –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї–µ–Љ —З–µ—А–µ–Ј 96 —З –њ–Њ—Б–ї–µ –µ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П. –£–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л –≤–≤–Њ–і–Є–Љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –і–Њ 40 –Љ–≥/–Ї–≥ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–Њ—Б—М —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ–Љ —Б—А–Њ–Ї–∞ –Є–љ–і—Г–Ї—Ж–Є–Є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л—Е –Ї–Њ–ї–Є—З–µ—Б—В–≤ –Ш–§–Э-ќ± –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –Ї 48 —З (595,0 –њ–Ї–≥/–Љ–≥), –њ—А–Є—З–µ–Љ –≤ —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і—Г—О—Й–Є—Е 24 —З —Б–Є–љ—В–µ–Ј –Ш–§–Э-ќ± —Б–Њ—Е—А–∞–љ—П–ї—Б—П –љ–∞ —Г—А–Њ–≤–љ–µ 335,0 –њ–Ї–≥/–Љ–≥.
–Т —Ж–µ–ї–Њ–Љ, –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е –і–Њ–Ј –Р–Љ–Є–Ї—Б–Є–љ–∞ –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М –і–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ–∞—П, –љ–Њ –±–Њ–ї–µ–µ –њ–Њ–Ј–і–љ—П—П, –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ —В–∞–Ї–Њ–≤–Њ–є –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є, –њ—А–Њ–і—Г–Ї—Ж–Є—П –Ш–§–Э-ќ± (—А–Є—Б. 3).
–Р–Љ–Є–Ї—Б–Є–љ –≤ –≤–Њ–Ј—А–∞—Б—В–∞—О—Й–Є—Е –Њ—В 20 –і–Њ 400 –Љ–≥/–Ї–≥ –і–Њ–Ј–∞—Е –≤—Л–Ј—Л–≤–∞–ї —В–∞–Ї–ґ–µ –Є–љ–і—Г–Ї—Ж–Є—О –њ—А–Њ–і—Г–Ї—Ж–Є–Є –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –Ш–§–Э-ќї, —Б—А–µ–і–љ–µ—Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Ї–Њ—В–Њ—А–Њ–≥–Њ –љ–∞ –њ–Є–Ї–µ –њ—А–Њ–і—Г–Ї—Ж–Є–Є —Б–Њ—Б—В–∞–≤–ї—П–ї–Є –Њ—В 675,0 –і–Њ 1547,5 –њ–Ї–≥/–Љ–≥ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ.
–Ш–Ј –і–∞–љ–љ—Л—Е, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –љ–∞ —А–Є—Б—Г–љ–Ї–µ 4, —Б–ї–µ–і—Г–µ—В, —З—В–Њ —З–µ—А–µ–Ј 48 —З –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П –Р–Љ–Є–Ї—Б–Є–љ–∞ –≤ –љ–Є–Ј–Ї–Њ–є –і–Њ–Ј–µ вАФ 20 –Љ–≥/–Ї–≥ вАФ –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –Њ–њ—А–µ–і–µ–ї—П–ї–Њ—Б—М —И–µ—Б—В–Є–Ї—А–∞—В–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Ш–§–Э-ќї2/3 –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –Ї–Њ–љ—В—А–Њ–ї—П –≤ –љ—Г–ї–µ–≤–Њ–є —В–Њ—З–Ї–µ. –£–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –і–Њ 40 –Љ–≥/–Ї–≥ –њ–Њ–≤—Л—И–∞–ї–Њ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –Ш–§–Э-ќї2/3 –і–Њ 1405,0 –њ–Ї–≥/–Љ–≥ –Є —Б–Њ–Ї—А–∞—Й–∞–ї–Њ —Б—А–Њ–Ї –Є–љ–і—Г–Ї—Ж–Є–Є –µ–≥–Њ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–Є –љ–∞ 24 —З –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–Є–Ј–Ї–Њ–є –і–Њ–Ј—Л. –Ш–љ—Л–Љ–Є —Б–ї–Њ–≤–∞–Љ–Є, –і–≤—Г—Е–Ї—А–∞—В–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ –≤–≤–Њ–і–Є–Љ–Њ–≥–Њ –Р–Љ–Є–Ї—Б–Є–љ–∞ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–Љ—Г –і–≤—Г—Е–Ї—А–∞—В–љ–Њ–Љ—Г –њ–Њ–≤—Л—И–µ–љ–Є—О –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Ш–§–Э-ќї2/3 –Є –Њ–±—А–∞—В–љ–Њ –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–Љ—Г –і–≤—Г—Е–Ї—А–∞—В–љ–Њ–Љ—Г —Б–Њ–Ї—А–∞—Й–µ–љ–Є—О —Б—А–Њ–Ї–∞ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –њ–Є–Ї–∞ –µ–≥–Њ –њ—А–Њ–і—Г–Ї—Ж–Є–Є. –Ь–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ –њ—А–µ–њ–∞—А–∞—В–∞ вАФ 400 –Љ–≥/–Ї–≥ вАФ —Б–Љ–µ—Й–∞–ї–∞ –њ–Є–Ї –Є–љ–і—Г–Ї—Ж–Є–Є –Ш–§–Э-ќї2/3 –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –Ї 12 —З, –∞ —Г—А–Њ–≤–µ–љ—М –µ–≥–Њ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –і–Њ—Б—В–Є–≥–∞–ї 1547,5 –њ–Ї–≥/–Љ–≥. –Я—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Р–Љ–Є–Ї—Б–Є–љ–∞ –≤ –і–Њ–Ј–∞—Е 20 –Є 40 –Љ–≥/–Ї–≥ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М —Б–Є–љ—В–µ–Ј–∞ –Ш–§–Э-ќї2/3 –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ—Г–ї–µ–≤–Њ–є —В–Њ—З–Ї–Є –Є –µ–≥–Њ –∞–Ї–Ї—Г–Љ—Г–ї—П—Ж–Є–Є –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –ґ–Є–≤–Њ—В–љ—Л—Е —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ 96 –Є 72 —З —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Ь–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ –њ—А–µ–њ–∞—А–∞—В–∞ вАФ 400 –Љ–≥/–Љ–≥ вАФ –≤—Л–Ј—Л–≤–∞–ї–∞ –±–Њ–ї–µ–µ –±—Л—Б—В—А—Л–є (12 —З) –Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є –њ–Њ–і—К–µ–Љ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Ш–§–Э-ќї2/3 (1547,5 –њ–Ї–≥/–Љ–≥), –Ї–Њ—В–Њ—А—Л–є —Б–Њ—Е—А–∞–љ—П–ї—Б—П –љ–∞ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–Љ —Г—А–Њ–≤–љ–µ (347,5 –њ–Ї–≥/–Љ–≥) –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –Ї–Њ–љ—В—А–Њ–ї—П –і–Њ 24 —З –≤–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –і–Є–љ–∞–Љ–Є–Ї–∞ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Ш–§–Э-ќї2/3 –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –њ–Њ–Ї–∞–Ј–∞–ї–∞, —З—В–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–є –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –Р–Љ–Є–Ї—Б–Є–љ —Б–Њ–Ї—А–∞—Й–∞–µ—В —Б—А–Њ–Ї –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –њ–Є–Ї–∞ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Ш–§–Э-ќї2/3. –Т –і–Њ–Ј–∞—Е 20, 40 –Є 400 –Љ–≥/–Ї–≥ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —Б–Є–љ—В–µ–Ј –Ш–§–Э-ќї2/3 –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є —В–µ—Б—В–Є—А—Г–µ—В—Б—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ —З–µ—А–µ–Ј 48, 24 –Є 12 —З –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞. –Я—А–Є—З–µ–Љ –і–≤—Г—Е–Ї—А–∞—В–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ –і–Њ–Ј—Л –Р–Љ–Є–Ї—Б–Є–љ–∞ —Б 20 –і–Њ 40 –Љ–≥/–Ї–≥ –≤—Л–Ј—Л–≤–∞–µ—В –±–Њ–ї–µ–µ —З–µ–Љ –і–≤—Г—Е–Ї—А–∞—В–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Ш–§–Э-ќї2/3 –љ–∞ –њ–Є–Ї–µ –µ–≥–Њ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–Є вАФ —Б 675,0¬±5,94 –і–Њ 1405,0¬±9,86 –њ–Ї–≥/–Љ–≥ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Я—А–Є –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–Љ

–°—А–∞–≤–љ–Є—В–µ–ї—М–љ–∞—П —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞ –і–Є–љ–∞–Љ–Є–Ї–Є –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Є–љ—В–µ—А—Д–µ—А–Њ–љ–Њ–≤ –∞–ї—М—Д–∞ –Є –ї—П–Љ–±–і–∞ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Є –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Р–Љ–Є–Ї—Б–Є–љ
–°—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є–љ–і—Г–Ї—Ж–Є–Є –Ш–§–Э-ќ± –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Є –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Р–Љ–Є–Ї—Б–Є–љ –≤ –і–Њ–Ј–µ 400 –Љ–≥/–Ї–≥ –њ–Њ–Ї–∞–Ј–∞–ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–µ –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ –µ–≥–Њ –њ—А–Њ–і—Г–Ї—Ж–Є–Є (–≤ 2,8 —А–∞–Ј–∞) –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ —В–∞–Ї–Њ–≤–Њ–є –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –ґ–Є–≤–Њ—В–љ—Л—Е. –Ю–і–љ–∞–Ї–Њ –њ–Є–Ї –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Ш–§–Э-ќ± –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Њ–њ—А–µ–і–µ–ї—П–ї—Б—П —З–µ—А–µ–Ј 24 —З –њ–Њ—Б–ї–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –њ—А–Њ–і—Г–Ї—Ж–Є—П –Ш–§–Э-ќ± –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є —В–µ—Б—В–Є—А–Њ–≤–∞–ї–∞—Б—М —В–Њ–ї—М–Ї–Њ —З–µ—А–µ–Ј 48 —З. –Ш–љ—Л–Љ–Є —Б–ї–Њ–≤–∞–Љ–Є, –њ—А–Њ–і—Г–Ї—Ж–Є—П –Ш–§–Э-ќ± –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Р–Љ–Є–Ї—Б–Є–љ–∞ –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ —Б–љ–∞—З–∞–ї–∞ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є (—З–µ—А–µ–Ј 24 —З –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П), –∞ –Ј–∞—В–µ–Љ –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є (—З–µ—А–µ–Ј 48 —З –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П), –љ–Њ –≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –±–Њ–ї—М—И–µ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ (—А–Є—Б. 5).
–Ь–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Ш–§–Э-ќї2/3 –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Р–Љ–Є–Ї—Б–Є–љ–∞ –≤ –і–Њ–Ј–µ 400 –Љ–≥/–Ї–≥ –і–Њ—Б—В–Є–≥–∞–ї—Б—П —З–µ—А–µ–Ј 12 —З –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –Є —Б–Њ—Б—В–∞–≤–ї—П–ї 1547,5¬±3,70 –њ–Ї–≥/–Љ–≥, –∞ –њ–Є–Ї –µ–≥–Њ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є —В–µ—Б—В–Є—А–Њ–≤–∞–ї—Б—П —З–µ—А–µ–Ј 24 —З –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –Є —Б–Њ—Б—В–∞–≤–ї—П–ї 2231¬±93 –њ–Ї–≥/–Љ–ї, —З—В–Њ –њ—А–µ–≤—Л—И–∞–ї–Њ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Ш–§–Э-ќї2/3 –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –љ–∞ –њ–Є–Ї–µ –µ–≥–Њ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –≤ 1,4 —А–∞–Ј–∞. –Ш–љ—Л–Љ–Є —Б–ї–Њ–≤–∞–Љ–Є, –њ—А–Њ–і—Г–Ї—Ж–Є—П –Ш–§–Э-ќї2/3 –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Њ–њ–µ—А–µ–ґ–∞–ї–∞ –њ–Њ —Б—А–Њ–Ї—Г –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–≥–Њ —Б–Є–љ—В–µ–Ј–∞ —В–∞–Ї–Њ–≤—Г—О –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Љ—Л—И–µ–є, –љ–Њ –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М –љ–∞ –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Њ–Љ —Г—А–Њ–≤–љ–µ (—А–Є—Б. 6).

–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Є–љ–і—Г–Ї—Ж–Є—П –Є –њ—А–Њ–і—Г–Ї—Ж–Є—П –Ш–§–Э-ќ± –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Њ–њ–µ—А–µ–ґ–∞–µ—В –≤–Њ –≤—А–µ–Љ–µ–љ–Є —В–∞–Ї–Њ–≤—Г—О –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –љ–∞ 24 —З, –љ–Њ –љ–∞ –њ–Є–Ї–µ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г—Б—В—Г–њ–∞–µ—В –њ–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–Љ—Г —Б–Њ–і–µ—А–ґ–∞–љ–Є—О (–≤ 2,8 —А–∞–Ј–∞). –Р –Є–љ–і—Г–Ї—Ж–Є—П –Є –њ—А–Њ–і—Г–Ї—Ж–Є—П –Ш–§–Э-ќї2/3 –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Њ–њ–µ—А–µ–ґ–∞–µ—В –њ–Њ –≤—А–µ–Љ–µ–љ–Є —В–∞–Ї–Њ–≤—Г—О –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Љ—Л—И–µ–є –љ–∞ 12 —З, –љ–Њ –љ–∞ –њ–Є–Ї–µ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ —В–µ—Б—В–Є—А—Г–µ—В—Б—П –љ–∞ –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Њ–Љ —Г—А–Њ–≤–љ–µ, —З–µ–Љ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Љ—Л—И–µ–є (–≤ 1,4 —А–∞–Ј–∞) (—А–Є—Б. 6).
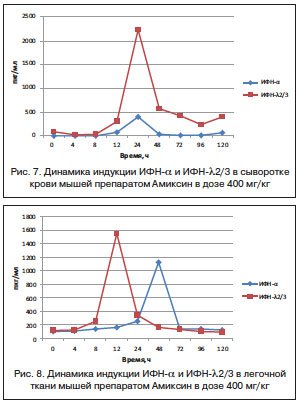
–°—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є–љ–і—Г–Ї—Ж–Є–Є –Ш–§–Э-ќ± –Є -ќї2/3 –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Љ—Л—И–µ–є –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–є –і–Њ–Ј—Л –Р–Љ–Є–Ї—Б–Є–љ–∞ 400 –Љ–≥/–Ї–≥ –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ —Б—А–Њ–Ї –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Є—Е –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–Є —Б–Њ–≤–њ–∞–і–∞–µ—В –Є –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —З–µ—А–µ–Ј 24 —З –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞. –Ю–і–љ–∞–Ї–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –≤ –Ї—А–Њ–≤–Є –Ш–§–Э-ќї2/3 –љ–∞ –њ–Є–Ї–µ –µ–≥–Њ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –≤ 5,6 —А–∞–Ј–∞ –њ—А–µ–≤—Л—И–∞–µ—В —В–∞–Ї–Њ–≤–Њ–µ –Ш–§–Э-ќ± (2231¬±93 –Є 398¬±12 –њ–Ї–≥/–Љ–ї —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ) (—А–Є—Б. 7).
–Т –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —Б–Є–љ—В–µ–Ј –Ш–§–Э-ќї2/3 –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Р–Љ–Є–Ї—Б–Є–љ–∞ –≤ —В–Њ–є –ґ–µ –і–Њ–Ј–µ –Њ–њ–µ—А–µ–ґ–∞–µ—В –њ–Њ –≤—А–µ–Љ–µ–љ–Є —Б–Є–љ—В–µ–Ј –Ш–§–Э-ќ± –љ–∞ 36 —З –Є –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В –µ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ –≤ 1,4 —А–∞–Ј–∞ (1547¬±3,0 –Є 1125,0¬±14,43 –њ–Ї–≥/–Љ–≥ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ) (—А–Є—Б. 8).
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є
–Я–Њ —Б—Г–Љ–Љ–∞—А–љ—Л–Љ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Є –Є—Е —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞, –њ—А–µ–њ–∞—А–∞—В –Р–Љ–Є–Ї—Б–Є–љ –≤ –і–Њ–Ј–µ 40 –Љ–≥/–Ї–≥ (—Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ–Њ–є —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ –і–ї—П —З–µ–ї–Њ–≤–µ–Ї–∞) –≤—Л–Ј—Л–≤–∞–µ—В –њ—А–Њ–ї–Њ–љ–≥–Є—А–Њ–≤–∞–љ–љ—Г—О —Б–Є—Б—В–µ–Љ–љ—Г—О –Є–љ–і—Г–Ї—Ж–Є—О –Є –њ—А–Њ–і—Г–Ї—Ж–Є—О –Ш–§–Э-ќ±, -ќ≤, -ќ≥ –Є -ќї –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Ї–Њ—В–Њ—А—Л—Е –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —Г–ґ–µ —З–µ—А–µ–Ј 24 —З –њ–Њ—Б–ї–µ –µ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П, –∞ —Д–Њ–љ–Њ–≤—Л–µ –Ј–љ–∞—З–µ–љ–Є—П —Б–Њ—Е—А–∞–љ—П—О—В—Б—П –і–Њ 120 —З (5 —Б—Г—В) –≤–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ. –Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –Р–Љ–Є–Ї—Б–Є–љ –≤ –і–Њ–Ј–µ 40 –Љ–≥/–Ї–≥ –Є–љ–і—Г—Ж–Є—А—Г–µ—В –њ—А–Њ–ї–Њ–љ–≥–Є—А–Њ–≤–∞–љ–љ—Г—О –ї–Њ–Ї–∞–ї—М–љ—Г—О –њ—А–Њ–і—Г–Ї—Ж–Є—О –Ш–§–Э -ќї –Є -ќ± –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –ґ–Є–≤–Њ—В–љ—Л—Е, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Ї–Њ—В–Њ—А—Л—Е —В–µ—Б—В–Є—А—Г–µ—В—Б—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ —З–µ—А–µ–Ј 24 –Є 48 —З –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –Є —В–∞–Ї–ґ–µ —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П –≤ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –Ј–љ–∞—З–µ–љ–Є—П—Е –і–Њ 96 –Є 120 —З –≤–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ.
–Ф–Є–љ–∞–Љ–Є–Ї–∞ –∞–Ї–Ї—Г–Љ—Г–ї—П—Ж–Є–Є –Ш–§–Э -ќ±, -ќ≤, -ќ≥ –Є -ќї –≤ –Ї—А–Њ–≤–Є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Р–Љ–Є–Ї—Б–Є–љ –≤ –і–Њ–Ј–µ 400 –Љ–≥/–Ї–≥ (—Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ–Њ–є –Ї—Г—А—Б–Њ–≤–Њ–є –і–ї—П –ї—О–і–µ–є) –њ–Њ–≤—В–Њ—А—П–µ—В —В–∞–Ї–Њ–≤—Г—О –≤ –і–Њ–Ј–µ 40 –Љ–≥/–Ї–≥, –љ–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Ш–§–Э-ќ± –Є -ќї, —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –љ–∞ –њ–Є–Ї–µ –њ—А–Њ–і—Г–Ї—Ж–Є–Є, —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В—Б—П –≤ —Б—А–µ–і–љ–µ–Љ –≤ 2 —А–∞–Ј–∞, –∞ –Ш–§–Э-ќ≤ –Є -ќ≥ вАФ –≤ 10 —А–∞–Ј –Є —Б–Њ—Е—А–∞–љ—П—О—В—Б—П –љ–∞ —Г—А–Њ–≤–љ–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –Ј–љ–∞—З–µ–љ–Є–є –≤ —В–µ—З–µ–љ–Є–µ 120 —З. –Ь–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –ї–Њ–Ї–∞–ї—М–љ–∞—П –њ—А–Њ–і—Г–Ї—Ж–Є—П –Ш–§–Э-ќ± –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Љ—Л—И–µ–є –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Р–Љ–Є–Ї—Б–Є–љ–∞ –≤ –і–Њ–Ј–µ 400 –Љ–≥/–Ї–≥ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —З–µ—А–µ–Ј 48 —З, –∞ —Б–Є–љ—В–µ–Ј –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л—Е –Ї–Њ–ї–Є—З–µ—Б—В–≤ –Ш–§–Э-ќї2/3 —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –Є —Г—Б–Ї–Њ—А—П–µ—В—Б—П –љ–∞ 36 —З, –Њ–њ–µ—А–µ–ґ–∞—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Г—О –њ—А–Њ–і—Г–Ї—Ж–Є—О –Ш–§–Э-ќ± –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –њ—А–Є –і–Њ–Ј–µ –њ—А–µ–њ–∞—А–∞—В–∞ 400 –Љ–≥/–Ї–≥. –Т –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–µ —Б—А–Њ–Ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П вАФ –і–Њ 120 —З –≤–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ, –≤ –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –ґ–Є–≤–Њ—В–љ—Л—Е –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –ї–Њ–Ї–∞–ї—М–љ–∞—П –њ—А–Њ–і—Г–Ї—Ж–Є—П —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –Ї–Њ–ї–Є—З–µ—Б—В–≤ –Ї–∞–Ї –Ш–§–Э-ќ±, —В–∞–Ї –Є –Ш–§–Э-ќї.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Њ–і–љ–Њ–Ї—А–∞—В–љ—Л–є –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –Р–Љ–Є–Ї—Б–Є–љ –≤ –і–Њ–Ј–µ, —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ–Њ–є —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ –і–ї—П —З–µ–ї–Њ–≤–µ–Ї–∞, –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е 24 —З –≤–Ї–ї—О—З–∞–µ—В —Б–Є–љ—В–µ–Ј –Ш–§–Э
–Ь–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ–Є –њ–Њ—Б–ї–µ–і–љ–Є—Е –ї–µ—В —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ —В–∞–Ї–ґ–µ, —З—В–Њ —А–∞–Ј–ї–Є—З–љ—Л–µ —И—В–∞–Љ–Љ—Л –≤–Є—А—Г—Б–∞ –≥—А–Є–њ–њ–∞, –Р,
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Т –љ–∞—Б—В–Њ—П—Й–µ–є —А–∞–±–Њ—В–µ, –≤–њ–µ—А–≤—Л–µ –≤ —Б—В—А–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е –њ—А–Є–љ—Ж–Є–њ–∞–Љ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л, –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ—Л –≤—Б–µ –Є–Ј–≤–µ—Б—В–љ—Л–µ 3 —В–Є–њ–∞ –Ш–§–Э, –Ї–Њ—В–Њ—А—Л–µ –Є–љ–і—Г—Ж–Є—А—Г—О—В—Б—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Р–Љ–Є–Ї—Б–Є–љ –≤ –Ї—А–Њ–≤–Є –Є –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є, –њ–Њ–і—А–Њ–±–љ–Њ –Є–Ј—Г—З–µ–љ–∞ –і–Є–љ–∞–Љ–Є–Ї–∞, –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В—М –Є –њ—А–Њ—Д–Є–ї—М –Є—Е —Б–Є—Б—В–µ–Љ–љ–Њ–є –Є –ї–Њ–Ї–∞–ї—М–љ–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–Є. –°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ—А–µ–њ–∞—А–∞—В –Р–Љ–Є–Ї—Б–Є–љ —П–≤–ї—П–µ—В—Б—П –±—Л—Б—В—А–Њ–і–µ–є—Б—В–≤—Г—О—Й–Є–Љ –≤ –њ–µ—А–≤—Л–µ 24 —З –њ—А–Њ—В–Є–≤–Њ–≤–Є—А—Г—Б–љ—Л–Љ —Б—А–µ–і—Б—В–≤–Њ–Љ —Н–љ–і–Њ–≥–µ–љ–љ–Њ–є –њ—А–Њ–ї–Њ–љ–≥–Є—А–Њ–≤–∞–љ–љ–Њ–є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –≤—Л—А–∞–±–Њ—В–Ї–Є –Ш–§–Э
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –њ—А–µ–њ–∞—А–∞—В –Р–Љ–Є–Ї—Б–Є–љ —П–≤–ї—П–µ—В—Б—П –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ —Б—А–µ–і–Є –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–љ—Л—Е –≤ –†–§ –Є–љ–і—Г–Ї—В–Њ—А–Њ–≤ –Ш–§–Э, –і–ї—П –Ї–Њ—В–Њ—А–Њ–≥–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –і–Њ–Ї–∞–Ј–∞–љ–Њ –і–µ–є—Б—В–≤–Є–µ –љ–∞ –≤—Л—А–∞–±–Њ—В–Ї—Г –≤—Б–µ—Е
–Ш–љ–і—Г–Ї—Ж–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Р–Љ–Є–Ї—Б–Є–љ —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е –Ш–§–Э












