Известные пути переноса Campylobacter включают фекально–оральный, также описан половой путь передачи. Наиболее частыми причинами являются употребление непастеризованного коровьего молока, домашней птицы, воды, зараженной фекалиями. По некоторым сообщениям, контакты с больными домашними животными (щенками) также ассоциированы с риском заражения Campylobacter. Передача Campylobacter человеку обычно происходит через инфицированных животных или пищу. Наиболее частое возникновение инфекции у человека ассоциировано с употреблением неправильно приготовленной пищи или уже зараженных продуктов питания. Описано, что около 50–70% цыплят являются носителями инфекции Campylobacter, известной у человека. Колонизированные виды животных также являются носителями подобной инфекции в течение длительного времени. Инфицирующей дозой является 1000–10000 бактерий. Инфекция Campylobacter может развиваться после употребления волонтером от 500 единиц инфекционных агентов; однако доза менее чем 10000 организмов не всегда является причиной заболения. Campylobacter является также чувствительной к соляной кислоте желудка.
Инкубационный период после заражения Сampylobacter длится около 1 нед. Бактерия повреждает тощую кишку, подвздошную кишку, толстую кишку. C. jejuni вторгается в эпителиальные клетки и разрушает их. Специальные жгутики помогают C. jejuni при помощи хемотаксиса прилипать ко слизистой кишки перед внедрением. Наличие липолисахаридов и других компонентов покрывающей мембраны помогает адгезии бактерий и колонизации в слизистой оболочке. Имеющися у бактерии поверхностный антиген PEB1 помогает проявлять высокие адгезивные и защитные свойства.
Некторые штамы C. jejuni продуцируют теплоустойчивый, холероподобный энтеротоксин, который играет важную роль в формировании симптомов водной диареи у инфицированных пациентов. При поражении слизистой оболочки кишки формируются диффузные морфологические изменения, характерные для отечного экссудативного энтероколита. Воспалительный инфильтрат состоит из нейтрофилов, мононуклеарных клеток и эозинофилов. В эпителиальных железах формируются абсцесы крипт и изъязвления эпителия слизистой оболочки кишки.
Имеются данные о продукции специального цитотоксина штаммами Campylobacter, полученные при анализе случаев диареи с примесью крови. Некоторые случаи инфекции могут быть ассоциированы с гемолитико–уремическим синдромом и тромботической тромбоцитопенической пурпорой, механизм возникновения которых полностью до сих пор не ясен. Повреждение эндотелиальных клеток опосредуется эндотоксинами или иммунными комплексами и ведет к интраваскулярной коагуляции и тромботической микроангиопатии в клубочках и гастроинтестинальной слизистой.
У пациентов с ВИЧ инфекция Campylobacter может быть широко распространена, является наиболее частой причиной длительной или периодической диареи и может быть наиболее часто ассоциированна с бактериемией и антибиотикорезистентностью.
При инвазии в слизистую желудка C. fetus покрывается поверхностным слоем S–протеина, который функционирует как капсула, что приводит к сывороточной и фагоцитарной резистентности. Инфекция C. jejuni наиболее распространена у детей и взрослых с недостаточностью иммуноглобулинов. После острой инфекции C. jejuni возможно формирование короткосрочного иммунитета. Пациенты вырабатывают специфические иммуноглобулины G (IgG), M (IgM) и A (IgA) в сыворотке, а IgA–антитела также формируются в кишечной стенке. Роль клеточно–опосредованного и гуморального иммунитета была показана при изучении инфекции C. jejuni у пациентов с ВИЧ и гипогаммаглобулинемией. Данные исследования показали роль данных видов иммунитета в предупреждении и прекращении инфекции. В США ежегодно регистрируется около 2 млн случаев энтерита, вызванного Campylobacter. Бактерия имеет огромный резервуар в животном мире, в 100% случаев инфекция обнаруживается у домашней птицы, включая курицу, индюшку, водоплавающих, имеющих асимптомную кишечную инфекцию. Наибольшим резервуаром для C. fetus является домашний скот и овцы. Однако частота инфекции Campylobacter в последние годы уменьшается, по данным Foodborne Diseases Active Surveillance Network (FoodNet).
Обычно инфекция Campylobacter имеет благоприятный исход и редко становится причиной смертельных исходов. Точных данных о смертности нет, однако, по некоторым сообщениям, случаи смерти, предписываемые Campylobacter, наблюдались в пожилом возрасте и у лиц с иммунодефицитом. Инфекция Campylobacter чаще встречается у мужчин, чем у женщин. Гомосексуальные мужчины имеют более высокий риск инфицирования атипичной инфекцией Campylobacter – Helicobacter cinaedi и Helicobacter fennelliae. Инфекция Campylobacter наблюдается у всех возрастных групп. Исследования показывают, что пик заболеваемости приходится на группу детей моложе 1 года и лиц 15–29 лет. Наибольшая заболевамость наблюдается в группе детей раннего возраста, а частота выявления инфекции в позитивных фекальных культурах – у взрослых и детей старшей возрастной группы. У взрослых иногда может наблюдаться асимптомное течение инфекции Сampylobacter. В развивающихся странах эта инфекция чаще встречается в первые 5 лет жизни и имеет асимптомное течение.
Инфекция Campylobacter может проявляться как асимптомным, так и тяжелым жизнеугрожающим колитом с развитием токсического мегаколона. Все случаи инфекции ассоциированы с кишечными синдромами и являются клинической манифестацией заболевания. В анамнезе заболевания превалируют случаи употребления неправильно приготовленной пищи, непастеризованного молока или некипяченой воды. Инкубационный период составляет около 1–7 дней и обычно связан с дозой поглощенных микроорганизмов. Продромальный период характеризуется лихорадкой, головной болью, миалгиями в первые 24 ч, после чего могут наблюдаться выраженная абдоминальная боль, лихорадка выше 40 °C и частая, более 10 раз/сут., водная диарея, иногда с примесью крови. Лихорадка, развивающаяся у более чем 90% пациентов, может длиться около недели. Пациенты с инфекцией C. jejuni, которые жалуются на рвоту, диарею с примесью крови, или те, кто имеет длительное течение заболевания, подлежат госпитализации. Боль в животе и тенезмы могут быть локализованными. Боль в правом нижнем квадранте может симулировать симптомы аппендицита (псевдоаппендицит). Тенезмы наблюдаются у более чем 25% пациентов. Среди прочих симптомов абдоминальная боль наблюдается чаще при инфекции Campylobacter, чем при инфекции, вызванной Salmonella или Shigella. По сранению с инфекцией C. jejuni C. fetus является причиной диареи реже. Однако C. fetus, которая вызывает диарею, приводит к клинической манифестации, очень схожей с клиническими проявлениями инфекций С. Jejuni. C. fetus является условно–патогенной инфекцией у ослабленных организмов, однако риск заражения здоровых организмов также имеется. При данной инфекции также может наблюдаться бактериемия, обычно у пациентов более старшего возраста и с воспалением подкожной жировой клетчатки (целлюлит), эндоваскулярными инфекциями или инфекциями, связанными с имплантируемыми устройствами. Также для этого вида инфекции характерны сосудистые осложнения – менингит, абсцессы. C. fetus может явиться причиной волнообразной диареи или неспецифической боли в животе. При объективном обследовании обращает внимание напряженность живота при пальпации, наличие зон более выраженной напряженности, как правило в правом или левом нижнем квадранте. Среди всех симптомов только абдоминальная боль является наиболее частым проявлением инфекции Campylobacter по сравнению с инфекциями, вызванными Salmonella и Shigella.
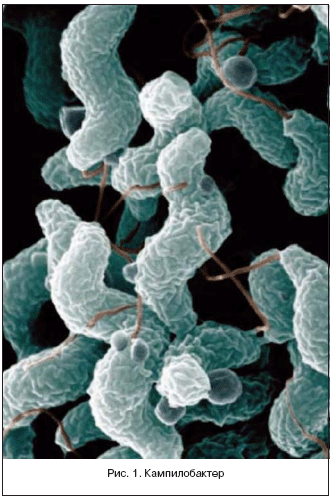
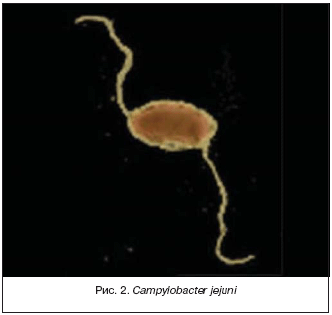
Campylobacter имеет форму завитка или спирали, является подвижным, неспорообразующим, грамотрицательным микроорганизмом. Подвижность обеспечивается одним или двумя жгутиками. Данный вид бактерий является оксидаза– и каталаза–позитивным и микроаэрофильным, требующим уменьшенного количества кислорода (5–10%) и повышенного уровня углекислого газа (3–10%) (рис. 2) [4].
Клиническая лабораторная диагностика кишечной инфекции Campylobacter основана на обнаружении микроорганизмов в фекалиях или на выделении организмов. Для выделения данного рода бактерий из фекалий применяются специальные техники. Они включают рост при 42 °C, использование специальных сред, фильтрацию через микроспоры с целью выделить бактерии больших диаметром из культуры. Образцы специальных сред должны содержать кровь, антибиотики. Для культивации C. jejuni могут быть использованы такие среды, как Mueller–Hinton и агар, которые создают прекрасные условия для роста C. jejuni. Оптимальная атмосфера для роста C. jejuni: 85% N2, 10% CO2, 5% O2. Исследование фекалий должно быть проведено в минимальные сроки.
При сигмоидоскопии в 80% случаев инфекции Campylobacter обнаруживаются признаки проктоколита. Однако признаки иногда могут быть такими же, как при псевдомембранозном колите или воспалительном заболении кишечника. Патология, выявляемая при сигмоидоскопии – от фокального отека слизитой и петехиальной гиперемией до диффузного или афтоидного изъязвления.
Главное звено лечения пациентов с Campylobacter infections – замещающая инфузионная терапия жидкостями и электролитами – регидратация оральными глюкозо–электролитными растворами. Недостаточный эффект от оральной гидратации может явиться показанием для назначения внутривенных вливаний [1]. Средством выбора при симптоматическом лечении интоксикационного синдрома инфекционной этиологии может служить препарат Энтеродез®. Его свойства, а также обзор проведенных исследований подробно представлены в статье, подготовленной сотрудниками компании «ЭР ЭНД ДИ ФАРМА» (Авдошенкова О.Г., Максвитис Р.Й., Иванив Р.В. «Применение препарата Энтеродез в терапии интоксикационного синдрома инфекционной этиологии»). Энтеродез является хорошо изученным препаратом. В основе его фармакологических свойств лежит дезинтоксикационное действие, заключающееся в способности к комплексообразованию. Механизм лечебного действия препарата заключается в способности активно связывать токсины и выводить их из организма через кишечник. Препарат нетоксичен, апробирован в эксперименте на животных, которые хорошо переносят его как в остром, так и в хроническом опыте. Многочисленной клинической практикой доказано, что Энтеродез не повреждает слизистую оболочку желудка и кишечника, не накапливается в организме, практически не имеет противопоказаний и побочных эффектов, то есть является вполне безопасным препаратом. В кровеносное русло препарат не поступает. Лечебный эффект проявляется через 15–30 мин после приема.
Некоторыми авторами была изучена возможность использования этого препарата с целью детоксикации. Энтеродез применяли у 104 больных с различной инфекционной патологией. Во всех этих наблюдениях имел место резкий эндотоксикоз, подтвержденный показателями формулы крови и токсичности крови, мочи и лимфы (по данным парамецийного теста). В 83 наблюдениях Энтеродез применяли в комплексе с другими методами детоксикации (гемосорбция, гемодиализ, дренирование грудного лимфатического протока).
У 21 больного при состоянии средней тяжести Энтеродез применяли изолированно, без использования других методов детоксикации. Препарат назначали по 5 г (растворяли в 100 мл воды с добавлением сахара) 3–4 раза/сут. Во всех наблюдениях при приеме препарата в течение 5–8 дней в дозе от 75 до 120 г на курс лечения у больных клинически отмечалась положительная динамика. Постепенно улучшались аппетит и сон, быстрее, чем при обычной терапии, нормализовалась функция кишечника (усиливалась перистальтика, отходили газы, нормализовалась дефекация), уменьшалась головная боль. При исследовании крови на токсичность в процессе лечения отмечали снижение токсичности исследуемой среды. Больные охотно принимали Энтеродез, осложнений не было выявлено. Изучено также влияние энтеродеза на состояние центральной гемодинамики с использованием тетраполярного реоплетизмографа, электрокардиограммы и фонокардиограммы. Через 30–60 мин после приема Энтеродеза у всех больных отмечено улучшение состояния кровообращения. Частота сердечных сокращений и артериальное давление практически не изменялись. Ударный объем увеличился на 10–35% по сравнению с исходным. Улучшение показателей центральной гемодинамики после применения Энтеродеза сопровождалось улучшением состояния больных и ускоренным их выздоровлением, что свидетельствовало о четко выраженном лечебном эффекте препарата.
Следует отметить, что Энтеродез более 20 лет широко использовался для лечения желудочно–кишечных интоксикаций – дизентерии, сальмонеллеза и др. Выявлено, что препарат снимает рвоту, тошноту, нормализует стул, температуру, пульс, позволяет исключить или уменьшить применение другой дезинтоксикационной терапии. Препарат оказался эффективным и при других видах интоксикации – ожоговой болезни, травматических поражениях, почечно–печеночной недостаточности и др. При таком частом осложнении тяжелой инфекционной интоксикации, как почечно–печеночная недостаточность, Энтеродез способствует снижению в 2–3 раза лейкоцитарного индекса интоксикации, нормализации числа лейкоцитов, снижению в 2–3 раза содержания билирубина, уменьшению в 2–4 раза токсичности крови по парамецийному тесту, повышению ударного и минутного объема сердца, нормализации функции печени. При данном патологическом состоянии применение Энтеродеза позволяет уменьшить объем вводимой в организм жидкости, что очень важно для ряда больных, особенно пожилого возраста.
Исследования, проведенные в Институте имени Н.В. Склифосовского, показали, что комплексное применение гемо– и лимфосорбции, гемодиализа и дезинтоксикационных препаратов для внутривенного (неогемодез) и перорального (Энтеродез) введения в терапии тяжелого интоксикационного синдрома дает хороший лечебный эффект. Также была исследована клиническая эффективность Энтеродеза у 85 больных в возрасте от 19 до 69 лет с острыми кишечными инфекционными болезнями (65 пациентов с пищевыми токсикоинфекциями и 20 – с острой дизентерией). Все больные поступали в остром периоде болезни, и препарат назначался при наличии интоксикации различной интенсивности. В частности выраженная интоксикация была у 42 больных с картиной быстро развивающейся слабости, заторможенности, потери аппетита, тошноты и рвоты от 1 до 4 раз/сут. У больных пищевой токсикоинфекцией стул был обычно жидкий, водянистый, от 5 до 10 раз/сут., в единичных случаях – до 20 раз, а при острой дизентерии – в среднем 5–6 раз/сут. с примесью слизи и крови. У всех этих больных были выражены боли в области, живота, часто интенсивные, но непродолжительные, отмечалась высокая лихорадка.
Препарат в дозе 5 г растворяли в 100 мл горячей воды и назначали перорально больным 1–4 раза/сут. в течение 1–3 дней в зависимости от степени интоксикации. Больные хорошо переносили препарат, хотя после растворения в воде он имел горьковатый вкус. При повышенном рвотном рефлексе к раствору добавляли одну столовую ложку сладкого сиропа.
Все больные с пищевыми токсикоинфекциями (85) были разделены на 2 группы. Первую составили 43 пациента, которые получали Энтеродез на фоне комплексного лечения: гидратационной терапии (внутривенного введения квартасоли, физиологического раствора) и симптоматических средств (спазмолитиков, витаминов, антигистаминных препаратов). Вторую группу (контрольную) составили 22 больных с пищевыми токсикоинфекциямй, которые получали гидратационную терапию и другие симптоматические средства без применения Энтеродеза; еще 20 больных острой дизентерией получали Энтеродез на фоне этиотропной терапии без приема симптоматических средств.
Основным критерием эффективности Энтеродеза было улучшение общего самочувствия больных, что связано прежде всего с уменьшением интоксикации. Положительный эффект имел место у всех леченных Энтеродезом больных. Достоверно раньше, чем в контрольной группе, при использовании Энтеродеза исчезали тошнота и рвота, уменьшались головная боль и слабость, снижалась повышенная температура, особенно у больных с пищевыми токсикоинфекциями; в 80% случаев нормализовался стул уже к концу 1–х и началу 2–х сут. после начала лечения. Измененные у некоторых больных функциональные пробы печени также быстро возвращались к норме (обычно на 2–е сут.). Средний срок пребывания больных в стационаре с пищевой токсикоинфекцией, леченных Энтеродезом, был достоверно ниже, чем в контрольной группе. Авторы отметили, что лечение Энтеродезом больных острой дизентерией почти полностью позволило исключить применение гидратационной терапии. Уже после 1–2 приемов этого препарата значительно уменьшались признаки интоксикации, исчезали болевой синдром и вздутие кишечника, появлялась тенденция к нормализации стула. У всех больных до и после лечения Энтеродезом существенных изменений в микрофлоре кишечника выявлено не было. Побочные явления также не отмечались. В ходе данного исследования было выявлено, что эффективность Энтеродеза зависит от срока начала его применения. Чем быстрее от начала болезни начато лечение, тем лучше эффект. Лечение Энтеродезом эффективно как на фоне другой комплексной (в том числе гидратационной) терапии, так и без нее. Применение Энтеродеза в ряде случаев позволяет исключить внутривенные капельные вливания жидкости даже при среднетяжелом и тяжелом течении болезни, особенно у больных острой дизентерией [2].
Использование антибиотиков для лечения инфекции Campylobacter является противоречивым. Исследования показали, что эритромицин быстро элиминирует Campylobacter из стула без воздействия на продолжительность заболевания. Исследования на детях с дизентерией, вызванной C. jejuni, показали пользу от раннего начала лечения эритромицином. Антибиотики могут быть назначены при следующих показаниях: лихорадка, диарея с примесью крови, диарея более 8 раз/сут., ухудшение симптомов, неэффективность проводимой терапии, длительность симптомов более 1 нед., беременность, ВИЧ–инфекция и другие состояния, связанные с иммунодефицитом.
Во время лечения необходимо воздерживаться от потребления препаратов, вызывающих антиперистальтику, в связи с тем, что их прием увеличивает продолжительность симптомов и увеличивают риск наступления неблагоприятных исходов. Пациенты с гипогаммаглобулинемией, имеющие волноообразную бактериемию, вызванную C. jejuni, могут потребовать назначения свежезамороженной плазмы и антибиотиков. Пациенты с тяжелой дизентерией или рецидивирующими сиптомами нуждаются в госпитализации. Пациенты с эндоваскулярной инфекцией C. fetus требуют не менее 4 нед. лечения, гентамицин может быть препаратом выбора, а терапия с ампициллином или 3–м поколением цефалоспоронов – альтернативой. Лечение инфекции центральной нервной системы C. fetus может продолжаться 2–3 нед. и проводиться 3–м поколением цефалоспоринов, ампициллина или хлорамфеникола. При подозрении на токсический мегаколон или аневризмы может быть проведено хирургическое вмешательство. При подозрении на токсический мегаколон или инфицированную аневризму консультация с хирургом обязательна. При подозрении на эндоваскулярную инфекцию C. fetus требуется консультация с инфекционистом. Во многих случаях системная инфекция Campylobacter диагносцируется ретроспективно, после успешного применения эмпирической антибиотикотерапии. В таких случаях рекомендуется повторный контроль роста культур в крови пациента. Оральное применение эритромицина может быть неэффективным при системной эндоваскулярной инфекции C. jejuni или C. fetus.
Установлено, что пастеризованное молоко и хлорированная вода разрушают Campylobacter. Не следует употреблять непастеризованное молоко или необработанную воду. Большое количество сообщений о возникновении Campylobacter связано с подобными случаями. Лечение антибиотиками может уменьшать экскрецию микроорганизмов с фекалиями. Сотрудники учреждений здравоохранения с инфекцией Campylobacter не должны иметь прямых контактов с пациентами, готовить пищу, когда у них имеется диарея.
При приготовлении пищи должна быть использована разная посуда для продуктов животного происхождения и других видов блюд. После приготовления пищи посуда должна быть тщательно вымыта при помощи специального средства и горячей воды. Курица должна быть тщательно приготовлена: сырая курица является превалирующим источником инфекции Campylobacter, замена данного вида курицы замороженной может снизить уроверь Campylobacter.
Наиболее частыми осложнениями инфекции Campylobacter являются токсический мегаколон, псевдомембранозный колит, геморрагический колит, гемолитико–уремический синдром, тромботическая тромбоцитопеническая пурпура, иммунопролиферативные заболевания тонкой кишки (известны случаи ассоцииации MALT лимфомы с инфекцией C. jejuni), реактивный артрит, бактериемия, эндокардит, холецистит, инфекция мочевых путей, выкидыши, септические аборты (C. fetus), синдром Guillain–Barr, инфицированная аорто–подвздошная аневризма.
Прогноз обычно благоприятный. В большинстве случаев пациенты выздоравливают самостоятельно или при помощи специфической терапии.
Многие виды инфекции Сampylobacter можно потенциально предупредить путем знания об основных механизмах передачи данного вида инфекции. Следует помнить, что перед употреблением мясо и домашняя птица должны быть хорошо приготовлены, руки надо хорошо вымыть до и после приготовления пищи. Родители должны быть информированы, что больные животные (щенки, котята) могут быть носителями тех же патогенов, что и человек, и что такие животные должны быть изолированы от детей. Необработанная вода и непастеризованное молоко не надо употреблять в пищу.
Таким образом, доказанная длительным использованием в клинической практике (более 20 лет) высокая детоксикационная эффективность Энтеродеза и возможность комбинирования его с другими лекарственными средствами позволяет рекомендовать данный препарат для лечения интоксикационного синдрома инфекционной этиологии как легкой и средней, так и тяжелой степени, особенно в ранние сроки от начала заболевания. Удобство использования, а также практически полное отсутствие побочных явлений позволяют рекомендовать применение Энтеродеза уже на догоспитальном этапе лечения, т. е. в поликлинических условиях [1].
Литература
1. Mahmud H Javid, MD, Chief, Section of Infectious Diseases, Shifa Hospital, Islamabad, Pakistan «Campylobacter Infections», 2009, http://emedicine.medscape.com/article/213720–followup
2. Авдошенкова О.Г. и соавт. «Применение препарата Энтеродез® в терапии интоксикационного синдрома инфекционной этиологии», http://www.rlsnet.ru/articles_469.htm
3. Scott Russell, Universidad de Georgia, Estados Unidos, Campilobacter, el siguiente desafio, 08.06.2009, http://www.wattagnet.com/IA/7863.html
4. Campylobacter blog: surveillance and analyses on campylobacter news and outbreaks, http://www.campylobacterblog.com/articles/campylobacter–watch












