–Р–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П (–Р–Ъ) –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≤ —В–µ—З–µ–љ–Є–µ –±–Њ–ї–µ–µ 40 –ї–µ—В. –Я–µ—А–≤—Л–є –Р–Ъ –≤–µ—А–∞–њ–∞–Љ–Є–ї –±—Л–ї —А–∞–Ј—А–µ—И–µ–љ –і–ї—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ –У–µ—А–Љ–∞–љ–Є–Є –≤ –Ї–∞—З–µ—Б—В–≤–µ –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ 1963 –≥. –Т –Ї–Њ–љ—Ж–µ 60–—Е – –љ–∞—З–∞–ї–µ 70–—Е –≥–Њ–і–Њ–≤ XX –≤–µ–Ї–∞ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –њ—А–∞–Ї—В–Є–Ї—Г –±—Л–ї–Є –≤–љ–µ–і—А–µ–љ—Л –і—А—Г–≥–Є–µ –Р–Ъ, —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е –љ–∞–Є–±–Њ–ї—М—И—Г—О –њ–Њ–њ—Г–ї—П—А–љ–Њ—Б—В—М –њ–Њ–ї—Г—З–Є–ї–Є –љ–Є—Д–µ–і–Є–њ–Є–љ –Є –і–Є–ї—В–Є–∞–Ј–µ–Љ. –Т –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–µ –≥–Њ–і—Л —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–љ—Л –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –і–µ—Б—П—В–Ї–Њ–≤ —Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є —Б–Њ —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є –Р–Ъ. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ–Њ–ї—Г—З–Є–ї–Є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –Р–Ъ L–—В–Є–њ–∞, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–µ –Њ—В–љ–Њ—Б—П—В—Б—П –Ї –Њ–і–љ–Њ–є –Є–Ј —В—А–µ—Е –≥—А—Г–њ–њ: 1) –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ —Д–µ–љ–Є–ї–∞–ї–Ї–Є–ї–∞–Љ–Є–љ–∞ (–≤–µ—А–∞–њ–∞–Љ–Є–ї –Є –і—А.); 2) –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ –±–µ–љ–Ј–Њ—В–Є–∞–Ј–µ–њ–Є–љ–∞ (–і–Є–ї—В–Є–∞–Ј–µ–Љ –Є –і—А.); 3) –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ 1,4––і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–∞ (–∞–Љ–ї–Њ–і–Є–њ–Є–љ, –љ–Є—Д–µ–і–Є–њ–Є–љ –Є –і—А.) [1–8].
–Т–µ—А–∞–њ–∞–Љ–Є–ї, –і–Є–ї—В–Є–∞–Ј–µ–Љ –Є –љ–Є—Д–µ–і–Є–њ–Є–љ – –њ–µ—А–≤—Л–µ –Є –љ–∞–Є–±–Њ–ї–µ–µ –Є–Ј–≤–µ—Б—В–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–Є —В—А–µ—Е –Њ—Б–љ–Њ–≤–љ—Л—Е –њ–Њ–і–≥—А—Г–њ–њ –Р–Ъ L–—В–Є–њ–∞. –Ш—Е —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –Њ—Б–Њ–±–µ–љ–љ–Њ —Е–Њ—А–Њ—И–Њ –Є–Ј—Г—З–µ–љ—Л, –њ–Њ—Н—В–Њ–Љ—Г —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї—Г –љ–Њ–≤—Л—Е –Р–Ъ –њ—А–Є–љ—П—В–Њ –і–∞–≤–∞—В—М –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –≤–µ—А–∞–њ–∞–Љ–Є–ї–Њ–Љ, –і–Є–ї—В–Є–∞–Ј–µ–Љ–Њ–Љ –Є –љ–Є—Д–µ–і–Є–њ–Є–љ–Њ–Љ, –Ї–Њ—В–Њ—А—Л–µ —Б—А–µ–і–Є –Р–Ъ L–—В–Є–њ–∞ —Б—З–Є—В–∞—О—В—Б—П –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є––њ—А–Њ—В–Њ—В–Є–њ–∞–Љ–Є. –Ф—А—Г–≥–Њ–µ –Њ–±—Й–µ–µ –љ–∞–Є–Љ–µ–љ–Њ–≤–∞–љ–Є–µ –≤–µ—А–∞–њ–∞–Љ–Є–ї–∞, –і–Є–ї—В–Є–∞–Ј–µ–Љ–∞ –Є –љ–Є—Д–µ–і–Є–њ–Є–љ–∞ – –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П 1––≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П.
–Т –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞ –≤—Л—Б–Њ–Ї–∞—П –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ–∞—П –Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Р–Ъ 1––≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –Њ–±–љ–∞—А—Г–ґ–µ–љ—Л —В–∞–Ї–Є–µ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–µ –Њ–±—Й–Є–µ –љ–µ–і–Њ—Б—В–∞—В–Ї–Є –≤–µ—А–∞–њ–∞–Љ–Є–ї–∞, –і–Є–ї—В–Є–∞–Ј–µ–Љ–∞ –Є –љ–Є—Д–µ–і–Є–њ–Є–љ–∞, –Ї–∞–Ї –љ–Є–Ј–Ї–∞—П –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М –Є–Ј––Ј–∞ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –њ—А–Є –њ–µ—А–≤–Њ–Љ –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є–Є —З–µ—А–µ–Ј –њ–µ—З–µ–љ—М, –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–∞—П —В–Ї–∞–љ–µ–≤–∞—П —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –Њ—Б–Њ–±–µ–љ–љ–Њ –±—Л—Б—В—А–∞—П —Н–ї–Є–Љ–Є–љ–∞—Ж–Є—П, –Ї–Њ—В–Њ—А–∞—П –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –љ–µ–њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ, –Є–Ј––Ј–∞ —З–µ–≥–Њ –њ—А–µ–њ–∞—А–∞—В—Л –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–љ–Є–Љ–∞—В—М 2–4 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є. –Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Р–Ъ 1––≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –љ–∞—Е–Њ–і–Є—В—Б—П –≤ –њ—А—П–Љ–Њ–є –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –њ–µ—А–Є–Њ–і–∞ –Є—Е –њ–Њ–ї—Г–ґ–Є–Ј–љ–Є –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є.
–Э–µ–њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Р–Ъ 1––≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –љ–µ —В–Њ–ї—М–Ї–Њ —П–≤–ї—П–µ—В—Б—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ –љ–µ—Г–і–Њ–±—Б—В–≤–Њ–Љ –і–ї—П –±–Њ–ї—М–љ–Њ–≥–Њ. –Т–µ–і—М –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –≤–µ—А–∞–њ–∞–Љ–Є–ї–∞, –і–Є–ї—В–Є–∞–Ј–µ–Љ–∞ –Є –љ–Є—Д–µ–і–Є–њ–Є–љ–∞, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –љ–µ —В–Њ–ї—М–Ї–Њ –љ–µ–њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ, –љ–Њ –Є –љ–∞—Б—В—Г–њ–∞–µ—В –±—Л—Б—В—А–Њ, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —З–∞—Б—В–Њ–Љ—Г —А–∞–Ј–≤–Є—В–Є—О –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є–µ–є, –Є –∞–Ї—В–Є–≤–∞—Ж–Є–Є —Б–Є–Љ–њ–∞—В–Є–Ї–Њ––∞–і—А–µ–љ–∞–ї–Њ–≤–Њ–є –Є —А–µ–љ–Є–љ––∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ. –Ю—Б–Њ–±–µ–љ–љ–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Г—О –љ–µ–є—А–Њ–≥—Г–Љ–Њ—А–∞–ї—М–љ—Г—О –∞–Ї—В–Є–≤–∞—Ж–Є—О –≤—Л–Ј—Л–≤–∞—О—В –љ–Є—Д–µ–і–Є–њ–Є–љ –Є –і—А—Г–≥–Є–µ –Ї–Њ—А–Њ—В–Ї–Њ–і–µ–є—Б—В–≤—Г—О—Й–Є–µ –Р–Ъ –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞, –Ї–Њ—В–Њ—А—Л–µ –≤—Л–Ј—Л–≤–∞—О—В –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Г—О –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є—О, —З–µ–Љ –≤–µ—А–∞–њ–∞–Љ–Є–ї –Є –і–Є–ї—В–Є–∞–Ј–µ–Љ.
–Э–µ–±–Њ–ї—М—И–∞—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –≤—Л—Б–Њ–Ї–∞—П —З–∞—Б—В–Њ—В–∞ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є–µ–є, –Є –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ–∞—П –∞–Ї—В–Є–≤–∞—Ж–Є—П —Б–Є–Љ–њ–∞—В–Є–Ї–Њ––∞–і—А–µ–љ–∞–ї–Њ–≤–Њ–є –Є —А–µ–љ–Є–љ––∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ –Њ–≥—А–∞–љ–Є—З–Є–≤–∞—О—В —И–Є—А–Њ–Ї–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Р–Ъ 1––≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –≤ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е 1,4––і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–∞. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, —З—А–µ–Ј–Љ–µ—А–љ–∞—П –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є—П –љ–∞ –Љ–∞–Ї—Б–Є–Љ—Г–Љ–µ –і–µ–є—Б—В–≤–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–µ–є—А–Њ––≥—Г–Љ–Њ—А–∞–ї—М–љ—Л—Е —Б–Є—Б—В–µ–Љ –і–µ–ї–∞—О—В –і–ї–Є—В–µ–ї—М–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Р–Ъ 1––≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –≤ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –љ–Є—Д–µ–і–Є–њ–Є–љ–∞, –љ–µ–±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ —Г –±–Њ–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є (–Р–У) –Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ—М—О —Б–µ—А–і—Ж–∞ (–Ш–С–°).
–Т–µ—А–∞–њ–∞–Љ–Є–ї, –і–Є–ї—В–Є–∞–Ј–µ–Љ, –љ–Є—Д–µ–і–Є–њ–Є–љ –Є –і—А—Г–≥–Є–µ –Р–Ъ —Б—А–∞–Ј—Г –њ–Њ–ї—Г—З–Є–ї–Є –њ—А–Є–Ј–љ–∞–љ–Є–µ, –Ї–∞–Ї —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–µ –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ—Л–µ (–∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ) —Б—А–µ–і—Б—В–≤–∞. –Ю–љ–Є —П–≤–ї—П—О—В—Б—П –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –≤—Л–±–Њ—А–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П –≤–∞–Ј–Њ—Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –Є —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –љ–∞–њ—А—П–ґ–µ–љ–Є—П. –Т —А—П–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ –Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤–µ—А–∞–њ–∞–Љ–Є–ї–∞ –Є –і–Є–ї—В–Є–∞–Ј–µ–Љ–∞ —Г –±–Њ–ї—М–љ—Л—Е, –њ–µ—А–µ–љ–µ—Б—И–Є—Е –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞. –Э–Є—Д–µ–і–Є–њ–Є–љ –Є –і—А—Г–≥–Є–µ –Р–Ъ –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞, –њ–Њ––≤–Є–і–Є–Љ–Њ–Љ—Г, –љ–µ –Њ–±–ї–∞–і–∞—О—В –Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, –∞ –Ї–Њ—А–Њ—В–Ї–Њ–і–µ–є—Б—В–≤—Г—О—Й–Є–µ —Д–Њ—А–Љ—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–∞–ґ–µ –Љ–Њ–≥—Г—В —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –Є –і–∞–ґ–µ —Б–Љ–µ—А—В–Є –Њ—В –љ–µ–≥–Њ.
–Ш–љ–Њ–µ –і–µ–ї–Њ –Р–У. –•–Њ—В—П –Р–Ъ, –љ–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ, —П–≤–ї—П—О—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –і–Њ –љ–µ–і–∞–≤–љ–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –љ–µ—П—Б–љ–Њ –±—Л–ї–Њ, —Б–њ–Њ—Б–Њ–±–љ—Л –ї–Є –Њ–љ–Є –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞—В—М —А–∞–Ј–≤–Є—В–Є–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е –Р–У. –Э–µ–і–∞–≤–љ–Њ –±—Л–ї–Њ –Ј–∞–≤–µ—А—И–µ–љ–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Ї—А—Г–њ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є (VHAS, NORDIL, INSIGHT, PREVENT, ALLHAT, INVEST, ACTION, CAMELOT, ELSA, ASCOT), –≤ –Ї–Њ—В–Њ—А—Л—Е –±—Л–ї–Њ —Г–±–µ–і–Є—В–µ–ї—М–љ–Њ –і–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Р–Ъ (–њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ, –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П) —Б—В–Њ–ї—М –ґ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—О—В —А–∞–Ј–≤–Є—В–Є–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е –Р–У, –Ї–∞–Ї –Є –і–Є—Г—А–µ—В–Є–Ї–Є –Є b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А—Л.
–£—З–Є—В—Л–≤–∞—П –≤—Б–µ —Н—В–Њ, —Б–Њ–Ј–і–∞—В–µ–ї–Є –љ–Њ–≤—Л—Е –Р–Ъ —Б—В—А–µ–Љ—П—В—Б—П –≤–љ–µ–і—А—П—В—М –Ї –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –њ—А–∞–Ї—В–Є–Ї—Г —В–Њ–ї—М–Ї–Њ —В–∞–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л, –Ї–Њ—В–Њ—А—Л–µ –њ—А–µ–≤–Њ—Б—Е–Њ–і—П—В –Р–Ъ 1––≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –µ—Б–ї–Є –љ–µ –њ–Њ —В–Ї–∞–љ–µ–≤–Њ–є —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є, —В–Њ, –њ–Њ –Љ–µ–љ—М—И–µ–є –Љ–µ—А–µ, –њ–Њ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –і–µ–є—Б—В–≤–Є—П. «–Ш–і–µ–∞–ї—М–љ—Л–є» –Р–Ъ –і–Њ–ї–ґ–µ–љ –Њ–Ї–∞–Ј—Л–≤–∞—В—М —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 24 —З–∞—Б–Њ–≤, —З—В–Њ–±—Л –њ—А–µ–њ–∞—А–∞—В –Љ–Њ–ґ–љ–Њ –±—Л–ї–Њ –њ—А–Є–љ–Є–Љ–∞—В—М –Њ–і–Є–љ —А–∞–Ј –≤ —Б—Г—В–Ї–Є. –Ы—Г—З—И–µ, –µ—Б–ї–Є –і–µ–є—Б—В–≤–Є–µ –Р–Ъ –њ—А–Њ–і–Њ–ї–ґ–∞–µ—В—Б—П –±–Њ–ї–µ–µ 24 —З–∞—Б–Њ–≤ – —В–Њ–≥–і–∞ –њ—А–µ–њ–∞—А–∞—В –±—Г–і–µ—В –Њ–Ї–∞–Ј—Л–≤–∞—В—М —Б–≤–Њ–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –≤ —В–µ—З–µ–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —З–∞—Б–Њ–≤ –≤ —Б–ї—Г—З–∞–µ –њ—А–Њ–њ—Г—Б–Ї–∞ –њ—А–Є–µ–Љ–∞ –Њ—З–µ—А–µ–і–љ–Њ–є –і–Њ–Ј—Л. –Ш–љ—Л–Љ–Є —Б–ї–Њ–≤–∞–Љ–Є, –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є—П —Д–µ–љ–Њ–Љ–µ–љ–∞ «—А–Є–Ї–Њ—И–µ—В–∞» (–Њ—В–Љ–µ–љ—Л) –љ–∞–Є–Љ–µ–љ—М—И–∞—П –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Р–Ъ —Б–Њ —Б–≤–µ—А—Е–і–ї–Є—В–µ–ї—М–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ.
–£–і–ї–Є–љ–µ–љ–Є—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –і–µ–є—Б—В–≤–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Љ–Њ–ґ–љ–Њ –і–Њ–±–Є—В—М—Б—П –і–≤—Г–Љ—П —Б–њ–Њ—Б–Њ–±–∞–Љ–Є: 1) –њ—Г—В–µ–Љ —Б–Њ–Ј–і–∞–љ–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Д–Њ—А–Љ —Б –Ј–∞–Љ–µ–і–ї–µ–љ–љ—Л–Љ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ–Љ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ –Є 2) –њ—Г—В–µ–Љ —Б–Є–љ—В–µ–Ј–∞ —Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є —Б –Љ–µ–і–ї–µ–љ–љ–Њ–є —Н–ї–Є–Љ–Є–љ–∞—Ж–Є–µ–є [1,4,7,9–11].
T. Toya–Oka –Є W. Nayler [11] –њ—А–µ–і–ї–Њ–ґ–Є–ї–Є —А–∞–Ј–і–µ–ї—П—В—М –Р–Ъ L–—В–Є–њ–∞ –љ–∞ —В—А–Є –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є —Б–ї–µ–і—Г—О—Й–Є—Е —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –Є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Ї—А–Є—В–µ—А–Є–µ–≤:
1) –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–µ–є—Б—В–≤–Є—П –Є–ї–Є —З–∞—Б—В–Њ—В–∞ –њ—А–Є–µ–Љ–∞ –і–Њ–Ј, –Ї–Њ—В–Њ—А—Л–µ –Њ–њ—А–µ–і–µ–ї—П—О—В—Б—П —Б–Ї–Њ—А–Њ—Б—В—М—О —Б–≤—П–Ј—Л–≤–∞–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ —Б —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є, –њ–µ—А–Є–Њ–і–Њ–Љ –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П –Є–Ј –њ–ї–∞–Ј–Љ—Л –Є –Њ–±—К–µ–Љ–Њ–Љ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П;
2) —З–∞—Б—В–Њ—В–∞ –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ —Б–≤—П–Ј–∞–љ—Л —Б –±—Л—Б—В—А–Њ–є –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є–µ–є –Є –Ј–∞–≤–Є—Б—П—В –Њ—В –≤—А–µ–Љ–µ–љ–Є, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ–≥–Њ –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є, —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П –Љ–µ–ґ–і—Г –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П–Љ–Є –Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є —Б–≤—П–Ј—Л–≤–∞–љ–Є—П —Б —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є;
3) –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–µ –Є–љ–Њ– –Є —Е—А–Њ–љ–Њ—В—А–Њ–њ–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Є –Ј–∞–Љ–µ–і–ї–µ–љ–Є–µ –∞—В—А–Є–Њ––≤–µ–љ—В—А–Є–Ї—Г–ї—П—А–љ–Њ–є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є, –Ї–Њ—В–Њ—А—Л–µ –Њ–њ—А–µ–і–µ–ї—П—О—В—Б—П —В–Ї–∞–љ–µ–≤–Њ–є —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –Љ–Њ–≥—Г—В —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –њ—А–µ–і—А–∞—Б–њ–Њ–ї–∞–≥–∞—В—М –Ї —А–∞–Ј–≤–Є—В–Є—О —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, —Б–Є–љ—Г—Б–Њ–≤–Њ–є –±—А–∞–і–Є–Ї–∞—А–і–Є–Є –Є –њ–Њ–њ–µ—А–µ—З–љ–Њ–є –±–ї–Њ–Ї–∞–і—Л —Б–µ—А–і—Ж–∞;
4) –њ—А–µ–і—Б–Ї–∞–Ј—Г–µ–Љ–Њ—Б—В—М —А–µ–∞–Ї—Ж–Є–Є –љ–∞ –њ—А–µ–њ–∞—А–∞—В, –Ї–Њ—В–Њ—А–∞—П –Ј–∞–≤–Є—Б–Є—В –Њ—В –µ–≥–Њ –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В–Є, –Њ–±—К–µ–Љ–∞ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –Є —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П –Љ–µ–ґ–і—Г –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П–Љ–Є –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є.
–С–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ–Є –і–ї—П –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б—З–Є—В–∞—О—В—Б—П –ї–Є—И—М –Р–Ъ 2 –Є 3 –њ–Њ–Ї–Њ–ї–µ–љ–Є–є.
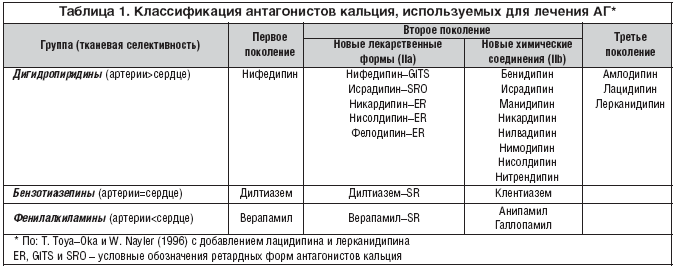
–Р–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П 2 –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Њ—В–ї–Є—З–∞—О—В—Б—П –Њ—В –њ—А–µ–њ–∞—А–∞—В–Њ–≤––њ—А–Њ—В–Њ—В–Є–њ–Њ–≤ —Г–ї—Г—З—И–µ–љ–љ—Л–Љ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ –њ—А–Њ—Д–Є–ї–µ–Љ –Є –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є –≤—Л—Б–Њ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О. T. Toya–Oka –Є W. Nayler [11] –њ–Њ–і—А–∞–Ј–і–µ–ї—П—О—В –Є—Е –љ–∞ –і–≤–µ –њ–Њ–і–≥—А—Г–њ–њ—Л — IIa –Є IIb. –Ъ –њ–µ—А–≤–Њ–є –њ–Њ–і–≥—А—Г–њ–њ–µ –Њ—В–љ–Њ—Б—П—В—Б—П —А–µ—В–∞—А–і–љ—Л–µ —Д–Њ—А–Љ—Л –Р–Ъ 1 –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –Ї–Њ –≤—В–Њ—А–Њ–є – –њ—А–µ–њ–∞—А–∞—В—Л —Б –Є–љ–Њ–є —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–Њ–є (—В–∞–±–ї. 1).
–Р–Ъ IIa –њ–Њ–і–Ї–ї–∞—Б—Б–∞ –Њ–Ї–∞–Ј—Л–≤–∞—О—В –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Ј–∞ —Б—З–µ—В —Б–Њ—З–µ—В–∞–љ–Є—П –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –і–Њ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Є –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П –Є–Ј –њ–ї–∞–Ј–Љ—Л –Ї—А–Њ–≤–Є. –Ъ–∞–Ї –њ—А–∞–≤–Є–ї–Њ, —А–µ—В–∞—А–і–љ—Л–µ —Д–Њ—А–Љ—Л –Р–Ъ –ї—Г—З—И–µ –њ–µ—А–µ–љ–Њ—Б—П—В—Б—П, —В–∞–Ї –Ї–∞–Ї —А–µ–ґ–µ –≤—Л–Ј—Л–≤–∞—О—В –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є–µ–є (–њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є 1 –њ–Њ–Ї–Њ–ї–µ–љ–Є—П) –±–ї–∞–≥–Њ–і–∞—А—П —Г–і–ї–Є–љ–µ–љ–Є—О –≤—А–µ–Љ–µ–љ–Є –і–Њ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є (—В.–µ. –±–Њ–ї–µ–µ –Љ–µ–і–ї–µ–љ–љ–Њ–Љ—Г –љ–∞—Б—В—Г–њ–ї–µ–љ–Є—О –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П).
–Р–Ъ IIb –њ–Њ–і–Ї–ї–∞—Б—Б–∞ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –Є –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є –≤–∞–Ј–Њ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О. –Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –Ї–∞–Ї –і–ї–Є—В–µ–ї—М–љ—Л–Љ –≤—А–µ–Љ–µ–љ–µ–Љ –і–Њ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є, —В–∞–Ї –Є –і–ї–Є—В–µ–ї—М–љ—Л–Љ –њ–µ—А–Є–Њ–і–Њ–Љ –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П.
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —Г–ї—Г—З—И–µ–љ–љ—Л–є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Д–Є–ї—М –Є –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї—Г—О —В–Ї–∞–љ–µ–≤—Г—О —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М, –Р–Ъ 2 –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –≤—Б–µ –ґ–µ –Њ—В–ї–Є—З–∞—О—В—Б—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є –њ—А–µ–і—Б–Ї–∞–Ј—Г–µ–Љ–Њ—Б—В—М—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤, —З—В–Њ –Њ–±—К—П—Б–љ—П–µ—В—Б—П –Є—Е –љ–Є–Ј–Ї–Њ–є –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М—О (–≤ –њ—А–µ–і–µ–ї–∞—Е –Њ—В 10 –і–Њ 40%), –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ–Є –Ї–Њ–ї–µ–±–∞–љ–Є—П–Љ–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є –≤ —В–µ—З–µ–љ–Є–µ «–Љ–µ–ґ–і–Њ–Ј–Њ–≤–Њ–≥–Њ» –Є–љ—В–µ—А–≤–∞–ї–∞ –Є –≤–љ–µ–Ј–∞–њ–љ—Л–Љ –њ—А–µ–Ї—А–∞—Й–µ–љ–Є–µ–Љ –і–µ–є—Б—В–≤–Є—П, –њ—А–Є–≤–Њ–і—П—Й–Є–Љ –Ї –±—Л—Б—В—А–Њ–Љ—Г –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є—О —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞. –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Р–Ъ 2 –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –љ–µ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—В —Б—В–∞–±–Є–ї—М–љ–Њ–≥–Њ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є —Б—Г—В–Њ–Ї, –њ–Њ—Н—В–Њ–Љ—Г –љ–µ–Ї–Њ—В–Њ—А—Л–Љ –±–Њ–ї—М–љ—Л–Љ –Є—Е –њ—А–Є—Е–Њ–і–Є—В—Б—П –љ–∞–Ј–љ–∞—З–∞—В—М 2 —А–∞–Ј–∞ –≤ –і–µ–љ—М.
–Т –Ї–∞—З–µ—Б—В–≤–µ –њ—А–Њ—В–Њ—В–Є–њ–∞ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П 3 –њ–Њ–Ї–Њ–ї–µ–љ–Є—П T. Toya–Oka –Є W. Nayler [11] —Г–Ї–∞–Ј–∞–ї–Є –љ–∞ –∞–Љ–ї–Њ–і–Є–њ–Є–љ, –Ї–Њ—В–Њ—А—Л–є –Њ—В–ї–Є—З–∞–µ—В—Б—П –≤–∞–ґ–љ—Л–Љ–Є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ–Є:
–∞) –±–Њ–ї–µ–µ –њ—А–µ–і—Б–Ї–∞–Ј—Г–µ–Љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –±–ї–∞–≥–Њ–і–∞—А—П –≤—Л—Б–Њ–Ї–Њ–є –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В–Є (60–80%) –Є –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ —А–∞–Ј–ї–Є—З–Є—П–Љ –Љ–µ–ґ–і—Г –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Ї—А–Њ–≤–Є –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є —Б—Г—В–Њ–Ї;
–±) –≤—Л—Б–Њ–Ї–∞—П —В–Ї–∞–љ–µ–≤–∞—П —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М, –±–ї–∞–≥–Њ–і–∞—А—П –Ї–Њ—В–Њ—А–Њ–є –Њ–љ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –≤–ї–Є—П–љ–Є—П –љ–∞ —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В—М –Љ–Є–Њ–Ї–∞—А–і–∞, —Д—Г–љ–Ї—Ж–Є—О —Б–Є–љ—Г—Б–Њ–≤–Њ–≥–Њ —Г–Ј–ї–∞ –Є –∞—В—А–Є–Њ––≤–µ–љ—В—А–Є–Ї—Г–ї—П—А–љ—Г—О –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В—М;
–≤) —Б–≤–µ—А—Е–і–ї–Є—В–µ–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ – –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –±–Њ–ї–µ–µ 24–36 —З–∞—Б–Њ–≤, —З—В–Њ –і–µ–ї–∞–µ—В –љ–µ–љ—Г–ґ–љ—Л–Љ —Б–Њ–Ј–і–∞–љ–Є–µ –µ–≥–Њ —А–µ—В–∞—А–і–љ—Л—Е —Д–Њ—А–Љ [11–14].
–Т 90––µ –≥–Њ–і—Л –њ—А–Њ—И–ї–Њ–≥–Њ –≤–µ–Ї–∞ –њ–Њ—П–≤–Є–ї–Є—Б—М –і–≤–∞ –і—А—Г–≥–Є—Е –њ—А–µ–њ–∞—А–∞—В–∞, –Ї–Њ—В–Њ—А—Л–µ –Њ–Ї–∞–Ј—Л–≤–∞—О—В —Б–≤–µ—А—Е–і–ї–Є—В–µ–ї—М–љ–Њ–µ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ—В–љ–µ—Б—В–Є –Є—Е –Ї –Р–Ъ 3 –њ–Њ–Ї–Њ–ї–µ–љ–Є—П. –≠—В–Њ – –ї–∞—Ж–Є–і–Є–њ–Є–љ –Є –ї–µ—А–Ї–∞–љ–Є–і–Є–њ–Є–љ [14–20].
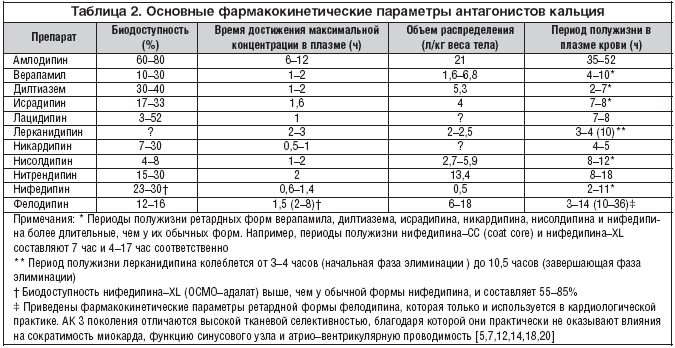
–°–≤–µ—А—Е–і–ї–Є—В–µ–ї—М–љ–Њ–µ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ —П–≤–ї—П–µ—В—Б—П –Њ—В–ї–Є—З–Є—В–µ–ї—М–љ–Њ–є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞, –ї–∞—Ж–Є–і–Є–њ–Є–љ–∞ –Є –ї–µ—А–Ї–∞–љ–Є–і–Є–њ–Є–љ–∞, –Њ–і–љ–∞–Ї–Њ —Д–Є–Ј–Є–Ї–Њ–—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ –Є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л —Н—В–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П —А–∞–Ј–ї–Є—З–љ—Л —Г —А–∞–Ј–љ—Л—Е –Р–Ъ 3 –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (—В–∞–±–ї. 2). [6,7,12–14,17–20].
–°—А–µ–і–Є –Р–Ъ 3 –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –љ–∞–Є–±–Њ–ї—М—И–µ–µ —З–Є—Б–ї–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ—Б–≤—П—Й–µ–љ–Њ –Є–Ј—Г—З–µ–љ–Є—О –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞, –Ї–Њ—В–Њ—А—Л–є –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –±–Њ–ї–µ–µ 20 –ї–µ—В.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—П
–∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞
–Я—А–Є –њ—А–Є–µ–Љ–µ –≤–љ—Г—В—А—М –∞–Љ–ї–Њ–і–Є–њ–Є–љ –њ–Њ–ї–љ–Њ—Б—В—М—О –≤—Б–∞—Б—Л–≤–∞–µ—В—Б—П –≤ —В–Њ–љ–Ї–Њ–Љ –Ї–Є—И–µ—З–љ–Є–Ї–µ. –Х–≥–Њ –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М –Ї–Њ–ї–µ–±–ї–µ—В—Б—П –Њ—В 60 –і–Њ 80%, —З—В–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –≤—Л—И–µ, —З–µ–Љ —Г –ї–∞—Ж–Є–і–Є–њ–Є–љ–∞ (–≤ —Б—А–µ–і–љ–µ–Љ 10%), –љ–Є—Д–µ–і–Є–њ–Є–љ–∞ (56%), —Д–µ–ї–Њ–і–Є–њ–Є–љ–∞ (15%) –Є –і—А—Г–≥–Є—Е –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П (—В–∞–±–ї. 2). –Э–Є –≤—Б–∞—Б—Л–≤–∞–µ–Љ–Њ—Б—В—М, –љ–Є –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –љ–µ –Є–Ј–Љ–µ–љ—П—О—В—Б—П –њ—А–Є –µ–≥–Њ —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–Љ –њ—А–Є–µ–Љ–µ —Б –њ–Є—Й–µ–є.
–Я–ї–∞–Ј–Љ–µ–љ–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –і–Њ—Б—В–Є–≥–∞—О—В –Љ–∞–Ї—Б–Є–Љ—Г–Љ–∞ –њ—А–Є–Љ–µ—А–љ–Њ —З–µ—А–µ–Ј 6 —З–∞—Б–Њ–≤ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –≤–љ—Г—В—А—М. –Я–Њ—Н—В–Њ–Љ—Г –∞–Љ–ї–Њ–і–Є–њ–Є–љ (–≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –љ–Є—Д–µ–і–Є–њ–Є–љ–∞) –љ–µ –њ–Њ–і—Е–Њ–і–Є—В –і–ї—П –±—Л—Б—В—А–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф.
–Р–Љ–ї–Њ–і–Є–њ–Є–љ —Ж–Є—А–Ї—Г–ї–Є—А—Г–µ—В –≤ –Ї—А–Њ–≤–Є –≤ –њ—А–Њ—З–љ–Њ–є —Б–≤—П–Ј–Є —Б –±–µ–ї–Ї–∞–Љ–Є –њ–ї–∞–Ј–Љ—Л –Ї—А–Њ–≤–Є (>95%). –£ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Њ—З–µ–љ—М –±–Њ–ї—М—И–Њ–є –Њ–±—К–µ–Љ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П (21 –ї/–Ї–≥ –≤–µ—Б–∞ —В–µ–ї–∞). –Э–∞–Є–±–Њ–ї—М—И–Є–µ –µ–≥–Њ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞—О—В—Б—П –≤ –њ–µ—З–µ–љ–Є, –ї–µ–≥–Ї–Є—Е, –њ–Њ—З–Ї–∞—Е –Є –љ–∞–і–њ–Њ—З–µ—З–љ–Є–Ї–∞—Е. –° –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, –Њ–љ –њ–ї–Њ—Е–Њ –њ—А–Њ–љ–Є–Ї–∞–µ—В —З–µ—А–µ–Ј –≥–µ–Љ–∞—В–Њ–—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Є–є –Є –њ–ї–∞—Ж–µ–љ—В–∞—А–љ—Л–є –±–∞—А—М–µ—А—Л, –∞ –Ј–љ–∞—З–Є—В, –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –≤–ї–Є—П–љ–Є—П –љ–∞ —Ж–µ–љ—В—А–∞–ї—М–љ—Г—О –љ–µ—А–≤–љ—Г—О —Б–Є—Б—В–µ–Љ—Г –Є —А–∞–Ј–≤–Є—В–Є–µ –њ–ї–Њ–і–∞ –≤–Њ –≤—А–µ–Љ—П –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є.
–Я–µ—А–Є–Њ–і –њ–Њ–ї—Г–ґ–Є–Ј–љ–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –±–Њ–ї—М—И–µ, —З–µ–Љ —Г –і—А—Г–≥–Є—Е –Р–Ъ, –Є –Ї–Њ–ї–µ–±–ї–µ—В—Б—П –Њ—В 35 –і–Њ 52 —З–∞—Б–Њ–≤, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –Љ–µ–і–ї–µ–љ–љ–Њ–є —Б–Ї–Њ—А–Њ—Б—В—М—О –µ–≥–Њ –±–Є–Њ—В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–Є –≤ –њ–µ—З–µ–љ–Є (—В–∞–±–ї. 2). –Я–µ—А–Є–Њ–і –њ–Њ–ї—Г–ґ–Є–Ј–љ–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ —Г–і–ї–Є–љ—П–µ—В—Б—П —Б –≤–Њ–Ј—А–∞—Б—В–Њ–Љ (—Б 35 –і–Њ 48 —З–∞—Б–Њ–≤) –Є –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Р–У (64 —З–∞—Б–∞). –Я–Њ—Н—В–Њ–Љ—Г –∞–Љ–ї–Њ–і–Є–њ–Є–љ –Љ–Њ–ґ–µ—В —Б—З–Є—В–∞—В—М—Б—П –Р–Ъ –њ–µ—А–≤–Њ–≥–Њ —А—П–і–∞ –і–ї—П –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –Р–У –Є–ї–Є —Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–µ–є –љ–∞–њ—А—П–ґ–µ–љ–Є—П.
–Х–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є –њ—Г—В—М —Н–ї–Є–Љ–Є–љ–∞—Ж–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є–Ј –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ – –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –≤ –њ–µ—З–µ–љ–Є —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ, –њ–Њ –Љ–µ–љ—М—И–µ–є –Љ–µ—А–µ, –і–µ—Б—П—В–Є –љ–µ–∞–Ї—В–Є–≤–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –≤—Л–≤–Њ–і—П—В—Б—П –њ–Њ—З–Ї–∞–Љ–Є.
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ–∞—А–∞–Љ–µ—В—А—Л —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Є–Ј–Љ–µ–љ—П—О—В—Б—П —Г –±–Њ–ї—М–љ—Л—Е —Б –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О. –≠—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –µ–≥–Њ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Г –±–Њ–ї—М–љ—Л—Е –њ–Њ–ґ–Є–ї–Њ–≥–Њ –Є —Б—В–∞—А—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, —Г –Ї–Њ—В–Њ—А—Л—Е —З–∞—Б—В–Њ –Є–Љ–µ–µ—В—Б—П —В–∞ –Є–ї–Є –Є–љ–∞—П —Б—В–µ–њ–µ–љ—М –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї. –Ю–і–љ–∞–Ї–Њ –њ–µ—А–Є–Њ–і –њ–Њ–ї—Г–ґ–Є–Ј–љ–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–і–ї–Є–љ—П–µ—В—Б—П –њ—А–Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б —Ж–Є—А—А–Њ–Ј–Њ–Љ –њ–µ—З–µ–љ–Є —В—А–µ–±—Г–µ—В –Њ—Б—В–Њ—А–Њ–ґ–љ–Њ—Б—В–Є.
–Ґ–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ
–∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞
–Ю—Б–љ–Њ–≤–љ–Њ–є –Њ–±–ї–∞—Б—В—М—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞, –Ї–∞–Ї –Є –і—А—Г–≥–Є—Е –Р–Ъ, —П–≤–ї—П–µ—В—Б—П –і–ї–Є—В–µ–ї—М–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ–Є –Є –і—А—Г–≥–Є—Е —Д–Њ—А–Љ –Р–У. –Я—А–Є –ї–µ—З–µ–љ–Є–Є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є –≤–∞–ґ–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ—О—В —В–∞–Ї–Є–µ –њ–Њ–ї–µ–Ј–љ—Л–µ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞, –Ї–∞–Ї –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ—Л–є (–∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–є), –≤–∞–Ј–Њ– –Є —А–µ–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–µ –Є, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –∞–љ—В–Є–∞—В–µ—А–Њ–≥–µ–љ–љ—Л–µ.
–Р—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П
–Р–Љ–ї–Њ–і–Є–њ–Є–љ –Њ–±–ї–∞–і–∞–µ—В –≤—Л—Б–Њ–Ї–Њ–є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О, —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –µ–≥–Њ –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ —Б–Њ—Б—Г–і–Њ—А–∞—Б—И–Є—А—П—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ. –Ю–љ –≤—Л–Ј—Л–≤–∞–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –Є —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Р–Ф –Ј–∞ —Б—З–µ—В —Г–Љ–µ–љ—М—И–µ–љ–Є—П –Њ–±—Й–µ–≥–Њ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П (–њ—А–Є —Н—В–Њ–Љ —З–∞—Б—В–Њ—В–∞ —Б–µ—А–і–µ—З–љ—Л—Е —Б–Њ–Ї—А–∞—Й–µ–љ–Є–є –Є —Г–і–∞—А–љ—Л–є –Њ–±—К–µ–Љ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –Є–Ј–Љ–µ–љ—П—О—В—Б—П). –Ю—В—Б—Г—В—Б—В–≤–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ –Ї–∞—А–і–Є–Њ–і–µ–њ—А–µ—Б—Б–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Њ—В–ї–Є—З–∞–µ—В –∞–Љ–ї–Њ–і–Є–њ–Є–љ –Њ—В –≤–µ—А–∞–њ–∞–Љ–Є–ї–∞ –Є –і–Є–ї—В–Є–∞–Ј–µ–Љ–∞, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–Њ—В–Њ—А—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ–Њ –њ—А–Є —Д—А–∞–Ї—Ж–Є–Є –≤—Л–±—А–Њ—Б–∞ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ –Љ–µ–љ–µ–µ 40%, –∞ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —А–µ—Д–ї–µ–Ї—В–Њ—А–љ–Њ–є —В–∞—Е–Є–Ї–∞—А–і–Є–Є – –Њ—В –љ–Є—Д–µ–і–Є–њ–Є–љ–∞, –Є—Б—А–∞–і–Є–њ–Є–љ–∞, –љ–Є–Ї–∞—А–і–Є–њ–Є–љ–∞, –љ–Є—В—А–µ–љ–і–Є–њ–Є–љ–∞ –Є —Д–µ–ї–Њ–і–Є–њ–Є–љ–∞.
–Р–Љ–ї–Њ–і–Є–њ–Є–љ –Њ—В–ї–Є—З–∞–µ—В—Б—П –Њ—В –њ–Њ–і–∞–≤–ї—П—О—Й–µ–≥–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –і—А—Г–≥–Є—Е –Р–Ъ –њ–Њ—Б—В–µ–њ–µ–љ–љ—Л–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П – —З–µ—А–µ–Ј –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –і–љ–µ–є –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є. –Ь–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –њ—А–µ–њ–∞—А–∞—В–∞ –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–µ—В—Б—П —З–µ—А–µ–Ј 4–8 –љ–µ–і–µ–ї—М, –њ–Њ—Н—В–Њ–Љ—Г –љ–∞—З–∞–ї—М–љ—Г—О –і–Њ–Ј—Г –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ (5 –Љ–≥ 1 —А–∞–Ј –≤ —Б—Г—В–Ї–Є) –љ–µ —Б–ї–µ–і—Г–µ—В —Г–і–≤–∞–Є–≤–∞—В—М —А–∞–љ–µ–µ, —З–µ–Љ —З–µ—А–µ–Ј 2–4 –љ–µ–і–µ–ї–Є –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є.
–Т –і–Њ–Ј–µ 5–10 –Љ–≥/—Б—Г—В. –∞–Љ–ї–Њ–і–Є–њ–Є–љ —Б–љ–Є–ґ–∞–µ—В —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –Р–Ф –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 15 –Љ–Љ —А—В.—Б—В. –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –Р–Ф –љ–∞ 10–15 –Љ–Љ —А—В.—Б—В. –Т –і–ї–Є—В–µ–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –∞–Љ–ї–Њ–і–Є–њ–Є–љ –≤—Л–Ј—Л–≤–∞–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф –Є–ї–Є –µ–≥–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—О –±–Њ–ї–µ–µ —З–µ–Љ —Г 70–90% –±–Њ–ї—М–љ—Л—Е —Б –Љ—П–≥–Ї–Њ–є –Є–ї–Є —Г–Љ–µ—А–µ–љ–љ–Њ–є —Д–Њ—А–Љ–∞–Љ–Є –Р–У. –Ъ–∞–Ї –Є –і—А—Г–≥–Є–µ –Р–Ъ –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞, –∞–Љ–ї–Њ–і–Є–њ–Є–љ –Њ—Б–Њ–±–µ–љ–љ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ —Г –њ–Њ–ґ–Є–ї—Л—Е –±–Њ–ї—М–љ—Л—Е —Б –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є.
–Т —В–µ—З–µ–љ–Є–µ 16 –љ–µ–і–µ–ї—М –Є–Ј—Г—З–∞–ї–∞—Б—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ (5–10 –Љ–≥/—Б—Г—В.). –Т —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е 4 –љ–µ–і–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Р–Ф —Б–љ–Є–Ј–Є–ї–Њ—Б—М –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 16,3/12,5 –Љ–Љ —А—В.—Б—В. –Ъ –Ї–Њ–љ—Ж—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Е–Њ—А–Њ—И–Є–є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ (—Б–љ–Є–ґ–µ–љ–Є–µ –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф –љ–Є–ґ–µ 90 –Љ–Љ —А—В.—Б—В. –Є–ї–Є –њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ –љ–∞ 10 –Љ–Љ —А—В. —Б—В.) –±—Л–ї –і–Њ—Б—В–Є–≥–љ—Г—В —Г 86% –±–Њ–ї—М–љ—Л—Е. –Р–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –±—Л–ї –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ —Г –ґ–µ–љ—Й–Є–љ, –∞ —В–∞–Ї–ґ–µ —Г –±–Њ–ї—М–љ—Л—Е —Б—В–∞—А—И–µ 65 –ї–µ—В [21]. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В —В–Є–∞–Ј–Є–і–љ—Л—Е –і–Є—Г—А–µ—В–Є–Ї–Њ–≤, b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ (–Р–Я–§) –њ—А–Є –Р–У –∞–Љ–ї–Њ–і–Є–њ–Є–љ, –Ї–∞–Ї –Є –і—А—Г–≥–Є–µ –Р–Ъ, –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ —Г –±–µ–ї—Л—Е –Є –љ–µ–≥—А–Њ–≤.
–Р–Љ–ї–Њ–і–Є–њ–Є–љ –њ—А–Є –њ—А–Є–µ–Љ–µ –Њ–і–Є–љ —А–∞–Ј –≤ —Б—Г—В–Ї–Є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –Є —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Р–Ф –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є —Б—Г—В–Њ–Ї. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –µ–≥–Њ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –њ—А–Њ–і–Њ–ї–ґ–∞–µ—В—Б—П –±–Њ–ї–µ–µ 24–48 —З–∞—Б–Њ–≤. –Я–Њ—Н—В–Њ–Љ—Г –∞–Љ–ї–Њ–і–Є–њ–Є–љ –Љ–Њ–ґ–µ—В —Б—З–Є—В–∞—В—М—Б—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ –і–ї—П –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є —Г –±–Њ–ї—М–љ—Л—Е, –Ї–Њ—В–Њ—А—Л–µ –љ–µ —Е–Њ—В—П—В –Є–ї–Є –Ј–∞–±—Л–≤–∞—О—В —А–µ–≥—Г–ї—П—А–љ–Њ –њ—А–Є–љ–Є–Љ–∞—В—М –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л.
–Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –і–ї—П –Њ–±—К–µ–Ї—В–Є–≤–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ—Б—В–Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –Њ—В–љ–Њ—И–µ–љ–Є–µ –Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ (–Ї–Њ–љ–µ—З–љ–Њ–≥–Њ) —Н—Д—Д–µ–Ї—В–∞ –Ї –љ–∞–Є–±–Њ–ї—М—И–µ–Љ—Г (–њ–Є–Ї–Њ–≤–Њ–Љ—Г) —Н—Д—Д–µ–Ї—В—Г. –°—З–Є—В–∞–µ—В—Б—П, —З—В–Њ –Њ—В–љ–Њ—И–µ–љ–Є–µ –Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Ї –љ–∞–Є–±–Њ–ї—М—И–µ–Љ—Г (–Ю–≠/–Э–≠) –і–ї—П –љ–Њ–≤—Л—Е –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–Њ–ї–ґ–љ–Њ –±—Л—В—М –љ–µ –Љ–µ–љ–µ–µ 50% (–Є–ї–Є 0,50). –Я–Њ –Љ–љ–µ–љ–Є—О P. Meredith (1998) [22], –≤ –Є–і–µ–∞–ї–µ –≤–µ–ї–Є—З–Є–љ–∞ –Њ—В–љ–Њ—И–µ–љ–Є—П –Ю–≠/–Э–≠ –і–Њ–ї–ґ–љ–∞ –њ—А–µ–≤—Л—И–∞—В—М 60%. –І–µ–Љ –±–ї–Є–ґ–µ –≤–µ–ї–Є—З–Є–љ–∞ –Њ—В–љ–Њ—И–µ–љ–Є—П –Ю–≠/–Э–≠ –Ї 100% (–Є–ї–Є 1,00), —В–µ–Љ —А–∞–≤–љ–Њ–Љ–µ—А–љ–µ–µ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ —В–µ—З–µ–љ–Є–µ —Б—Г—В–Њ–Ї.
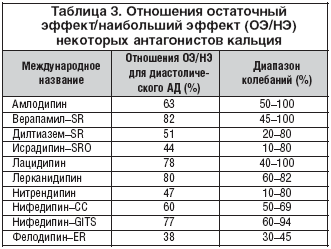
–≠—В–Є–Љ —В—А–µ–±–Њ–≤–∞–љ–Є—П–Љ –љ–µ —Г–і–Њ–≤–ї–µ—В–≤–Њ—А—П–µ—В –љ–Є –Њ–і–Є–љ –Є–Ј –Р–Ъ 1 –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –∞ —В–∞–Ї–ґ–µ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ 2 –њ–Њ–Ї–Њ–ї–µ–љ–Є—П. –£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –Р–Ъ 2 –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Њ—В–љ–Њ—И–µ–љ–Є–µ –Ю–≠/–Э–≠ –Ї–Њ–ї–µ–±–ї–µ—В—Б—П –≤ —И–Є—А–Њ–Ї–Є—Е –њ—А–µ–і–µ–ї–∞—Е. –Ь–Є–љ–Є–Љ–∞–ї—М–љ—Л–µ –Ј–љ–∞—З–µ–љ–Є–µ –Ю–≠/–Э–≠ —Б–Њ—Б—В–∞–≤–ї—П—О—В –љ–µ –Љ–µ–љ–µ–µ 50% –ї–Є—И—М —Г –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є —А–µ—В–∞—А–і–љ—Л—Е —Д–Њ—А–Љ –љ–Є—Д–µ–і–Є–њ–Є–љ–∞ –Є –љ–Є—Б–Њ–ї–і–Є–њ–Є–љ–∞ (—В–∞–±–ї. 3).
–Я–Њ –і–∞–љ–љ—Л–Љ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –≤ –і–Њ–Ј–∞—Е 5 –Є 10 –Љ–≥/—Б—Г—В. —Б—А–µ–і–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –µ–≥–Њ –Њ—В–љ–Њ—И–µ–љ–Є—П –Ю–≠/–Э–≠ –і–ї—П –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф –Ї–Њ–ї–µ–±–ї—О—В—Б—П –Њ—В 50 –і–Њ 100%, —Б–Њ—Б—В–∞–≤–ї—П—П –≤ —Б—А–µ–і–љ–µ–Љ 63% (—В–∞–±–ї. 3). –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –∞–Љ–ї–Њ–і–Є–њ–Є–љ – –Њ–і–Є–љ –Є–Ј –љ–µ–Љ–љ–Њ–≥–Є—Е –Р–Ъ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, —Г –Ї–Њ—В–Њ—А–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П –Њ—В–љ–Њ—И–µ–љ–Є—П –Ю–≠/–Э–≠ –њ—А–µ–≤—Л—И–∞—О—В 50% –Є –Љ–Њ–≥—Г—В –і–Њ—Б—В–Є–≥–∞—В—М 100%.
–Т—Л—Б–Њ–Ї–∞—П –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –±—Л–ї–∞ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е. –Ґ–∞–Ї, –≤ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є TOMHS [23] –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ, —З—В–Њ –њ—А–Є –Р–У –∞–Љ–ї–Њ–і–Є–њ–Є–љ –≤—Л–Ј—Л–≤–∞–ї –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф, —З–µ–Љ –∞—Ж–µ–±—Г—В–Њ–ї–Њ–ї, –і–Њ–Ї—Б–∞–Ј–Њ–Ј–Є–љ, —Е–ї–Њ—А—В–∞–ї–Є–і–Њ–љ –Є —Н–љ–∞–ї–∞–њ—А–Є–ї, –Є –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф, —З–µ–Љ –њ–ї–∞—Ж–µ–±–Њ. –Т –і—А—Г–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —В–∞–Ї–ґ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ–Њ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ —Б—А–∞–≤–љ–Є–Љ —Б –і–Є—Г—А–µ—В–Є–Ї–∞–Љ–Є (–≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і, —Е–ї–Њ—А—В–∞–ї–Є–і–Њ–љ), b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є (–∞—В–µ–љ–Њ–ї–Њ–ї), –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ (–Ї–∞–њ—В–Њ–њ—А–Є–ї, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї, —Н–љ–∞–ї–∞–њ—А–Є–ї) –Є –і—А—Г–≥–Є–Љ–Є –Р–Ъ (–≤–µ—А–∞–њ–∞–Љ–Є–љ, –ї–∞—Ж–Є–і–Є–њ–Є–љ, –љ–Є—В—А–µ–љ–і–Є–њ–Є–љ, –љ–Є—Д–µ–і–Є–њ–Є–љ–—А–µ—В–∞—А–і) –Є–ї–Є –і–∞–ґ–µ –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В –Є—Е [4,12,13 ].
–Я—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ –≤—Л–Ј—Л–≤–∞–µ—В –Њ–±—А–∞—В–љ–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞, –њ—А–Є—З–µ–Љ –њ–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –≤—Л–Ј—Л–≤–∞—В—М —А–µ–≥—А–µ—Б—Б–Є—О –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ –Њ–љ –љ–µ —Г—Б—В—Г–њ–∞–µ—В –љ–Є –і–Є—Г—А–µ—В–Є–Ї–∞–Љ, –љ–Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ –Р–Я–§. –Р–Љ–ї–Њ–і–Є–њ–Є–љ —Г–Љ–µ–љ—М—И–∞–µ—В —Н–Ї—Б–Ї—А–µ—Ж–Є—О –∞–ї—М–±—Г–Љ–Є–љ–Њ–≤ —Б –Љ–Њ—З–Њ–є —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 2 —В–Є–њ–∞. –Я–Њ –љ–µ–Ї–Њ—В–Њ—А—Л–Љ –љ–∞–±–ї—О–і–µ–љ–Є—П–Љ, —А–µ–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–µ–є —Б—В–Њ–ї—М –ґ–µ –≤—Л—А–∞–ґ–µ–љ–Њ, –Ї–∞–Ї –Є –і–µ–є—Б—В–≤–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§, –Ї–Њ—В–Њ—А—Л–µ —Б—З–Є—В–∞—О—В—Б—П –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –≤—Л–±–Њ—А–∞ –і–ї—П —В–∞–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е [13].
–Р–Љ–ї–Њ–і–Є–њ–Є–љ –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ –ї–Є–њ–Є–і–љ—Л–є —Б–Њ—Б—В–∞–≤ –Ї—А–Њ–≤–Є, –∞ —В–∞–Ї–ґ–µ –Њ—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –≥–ї—О–Ї–Њ–Ј—Л, —З—В–Њ –і–µ–ї–∞–µ—В –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Р–У —Г –±–Њ–ї—М–љ—Л—Е —Б –∞—В–µ—А–Њ–≥–µ–љ–љ–Њ–є –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є–µ–є –Є —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ.
–Т–∞–ґ–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В —В–Њ –Њ–±—Б—В–Њ—П—В–µ–ї—М—Б—В–≤–Њ, —З—В–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞, –Ї–∞–Ї, –≤–њ—А–Њ—З–µ–Љ, –Є –і—А—Г–≥–Є—Е –Р–Ъ –љ–µ –Ј–∞–≤–Є—Б–Є—В –Њ—В –њ–Њ–ї–∞, –≤–Њ–Ј—А–∞—Б—В–∞ –Є —А–∞—Б—Л –±–Њ–ї—М–љ—Л—Е, –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Є –њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –њ–Њ–≤–∞—А–µ–љ–љ–Њ–є —Б–Њ–ї–Є —Б –њ–Є—Й–µ–є. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, —Г –њ–Њ–ґ–Є–ї—Л—Е –ї–Є—Ж –∞–Љ–ї–Њ–і–Є–њ–Є–љ, –њ–Њ––≤–Є–і–Є–Љ–Њ–Љ—Г, –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ, —З–µ–Љ —Г –±–Њ–ї–µ–µ –Љ–Њ–ї–Њ–і—Л—Е –±–Њ–ї—М–љ—Л—Е.
–Э–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –љ–µ –Њ—Б–ї–∞–±–ї—П—О—В –∞–љ—В–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В —Н—Д—Д–µ–Ї—В–Њ–≤ —В–Є–∞–Ј–Є–і–љ—Л—Е –і–Є—Г—А–µ—В–Є–Ї–Њ–≤, b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§.
–Т —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є ALLHAT [24] —Г –±–Њ–ї—М–љ—Л—Е –Р–У –∞–Љ–ї–Њ–і–Є–њ–Є–љ –њ–Њ –≤–ї–Є—П–љ–Є—О –љ–∞ —З–∞—Б—В–Њ—В—Г –Њ—Б–љ–Њ–≤–љ—Л—Е –Є–Ј—Г—З–∞–≤—И–Є—Е—Б—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (—Б–Љ–µ—А—В—М –Њ—В –Ш–С–° + –љ–µ—Д–∞—В–∞–ї—М–љ—Л–є –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞) –љ–µ –Њ—В–ї–Є—З–∞–ї—Б—П –Њ—В —Е–ї–Њ—А—В–∞–ї–Є–і–Њ–љ–∞, –∞ –≤ –њ–ї–∞–љ–µ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є–љ—Б—Г–ї—М—В–∞ –±—Л–ї –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ. –£ –±–Њ–ї—М–љ—Л—Е, –ї–µ—З–µ–љ–љ—Л—Е –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ, —З–∞—Б—В–Њ—В–∞ –Є–љ—Б—Г–ї—М—В–∞ –±—Л–ї–∞ –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 7% –љ–Є–ґ–µ, —З–µ–Љ —Г –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Е–ї–Њ—А—В–∞–ї–Є–і–Њ–љ, –њ—А–Є—З–µ–Љ —Г –ґ–µ–љ—Й–Є–љ – –љ–∞ 16% –љ–Є–ґ–µ. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є ALLHAT —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В –њ—А–Є –ї–µ—З–µ–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ —А–∞–Ј–≤–Є–≤–∞–ї—Б—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —А–µ–ґ–µ, —З–µ–Љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Е–ї–Њ—А—В–∞–ї–Є–і–Њ–љ–Њ–Љ (9,8% –њ—А–Њ—В–Є–≤ 11,6%). –≠—В–Њ –Њ–Ј–љ–∞—З–∞–µ—В, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –і–ї—П –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Р–У –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–µ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –∞–Љ–ї–Њ–і–Є–њ–Є–љ, –∞ –љ–µ —Е–ї–Њ—А—В–∞–ї–Є–і–Њ–љ.
–Т –Ї—А—Г–њ–љ–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є ASCOT–BPLA [25] —Г 19257 –±–Њ–ї—М–љ—Л—Е –Р–У —Б—А–∞–≤–љ–Є–≤–∞–ї–Є –Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є, –Њ—Б–љ–Њ–≤–∞–љ–љ—Г—О –љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞, –Є —В–µ—А–∞–њ–Є–Є, –Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–є –љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –∞—В–µ–љ–Њ–ї–Њ–ї–∞. –Я—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Ї –∞–Љ–ї–Њ–і–Є–њ–Є–љ—Г —А–∞–Ј—А–µ—И–∞–ї–Њ—Б—М –і–Њ–±–∞–≤–ї–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї–∞, –∞ –Ї –∞—В–µ–љ–Њ–ї–Њ–ї—Г – —В–Є–∞–Ј–Є–і–љ–Њ–≥–Њ –і–Є—Г—А–µ—В–Є–Ї–∞ –±–µ–љ–і—А–Њ—Д–ї—О–Љ–µ—В–Є–∞–Ј–Є–і–∞. –Я–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Њ–є –±—Л–ї–Є —Б–ї—Г—З–∞–Є –љ–µ—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ (–≤–Ї–ї—О—З–∞—П –±–µ–Ј–±–Њ–ї–µ–≤—Л–µ) –Є —Д–∞—В–∞–ї—М–љ–Њ–є –Ш–С–°. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–і–Њ–ї–ґ–∞–ї–Њ—Б—М –≤ —Б—А–µ–і–љ–µ–Љ 5,5 –ї–µ—В.
–Р–Ф –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є —В–µ—А–∞–њ–Є—О, –Њ—Б–љ–Њ–≤–∞–љ–љ—Г—О –љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞, –±—Л–ї–Њ –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 2,7/1,9 –Љ–Љ —А—В.—Б—В. –љ–Є–ґ–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є —В–µ—А–∞–њ–Є—О, –Њ—Б–љ–Њ–≤–∞–љ–љ—Г—О –љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –∞—В–µ–љ–Њ–ї–Њ–ї–∞. –Я–µ—А–≤–Є—З–љ–∞—П –Ї–Њ–љ–µ—З–љ–∞—П —В–Њ—З–Ї–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ –і–Њ—Б—В–Є–≥–∞–ї–∞—Б—М –љ–∞ 10% —А–µ–ґ–µ, —З–µ–Љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –∞—В–µ–љ–Њ–ї–Њ–ї–Њ–Љ. –Т –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є —В–µ—А–∞–њ–Є—О, –Њ—Б–љ–Њ–≤–∞–љ–љ—Г—О –љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞, –Њ–±—Й–∞—П —Б–Љ–µ—А—В–љ–Њ—Б—В—М –±—Л–ї–∞ –љ–∞ 11% –љ–Є–ґ–µ (—А=0,0247), —Б–Љ–µ—А—В–љ–Њ—Б—В—М –Њ—В —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ—А–Є—З–Є–љ – –љ–∞ 24% –љ–Є–ґ–µ (—А=0,0010) –Є —З–∞—Б—В–Њ—В–∞ –Є–љ—Б—Г–ї—М—В–Њ–≤ – –љ–∞ 23% –љ–Є–ґ–µ (—А=0,0003), —З–µ–Љ —Г –±–Њ–ї—М–љ—Л—Е, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є —В–µ—А–∞–њ–Є—О, –Њ—Б–љ–Њ–≤–∞–љ–љ—Г—О –љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –∞—В–µ–љ–Њ–ї–Њ–ї–∞.
–С–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї—Г—О –Ї–∞—А–і–Є–Њ– –Є —Ж–µ—А–µ–±—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є, –Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–є –љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞, –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–µ—А–∞–њ–Є–µ–є, –Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–є –љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –∞—В–µ–љ–Њ–ї–Њ–ї–∞, –љ–µ–ї—М–Ј—П –њ–Њ–ї–љ–Њ—Б—В—М—О –Њ–±—К—П—Б–љ–Є—В—М —А–∞–Ј–ї–Є—З–Є—П–Љ–Є –≤ —Г—А–Њ–≤–љ—П—Е –і–Њ—Б—В–Є–≥–љ—Г—В–Њ–≥–Њ –Р–Ф, –Ї–Њ—В–Њ—А—Л–µ –±—Л–ї–Є –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ–Є.
–Э–∞–Є–±–Њ–ї–µ–µ –≤–µ—А–Њ—П—В–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є –≤—Л—Б–Њ–Ї–Њ–є –њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є ASCOT–BPLA —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ —Б–Є–љ–µ—А–≥–Є–Ј–Љ —Б –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ—В–Њ—А–Њ–≥–Њ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –њ–ї–∞—Ж–µ–±–Њ –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —Б–Њ —Б—А–∞–≤–љ–µ–љ–Є–µ–Љ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є –∞—В–µ–љ–Њ–ї–Њ–ї–∞.
–Ф–µ–ї–Њ –≤ —В–Њ–Љ, —З—В–Њ –≤ –њ—А–Њ–≤–Њ–і–Є–≤—И–µ–Љ—Б—П –≤ —А–∞–Љ–Ї–∞—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П ASCOT–BPLA, –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є ASCOT–LLA, –±–Њ–ї–µ–µ —З–µ–Љ —Г 10 —В—Л—Б—П—З –±–Њ–ї—М–љ—Л—Е —Б —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ—Л–Љ–Є —Г—А–Њ–≤–љ—П–Љ–Є –Њ–±—Й–µ–≥–Њ –•–° –Љ–µ–љ—М—И–µ 6,5 –Љ–Љ–Њ–ї—М/–ї (250 –Љ–≥/–і–ї) –Є–Ј—Г—З–∞–ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ (10 –Љ–≥/—Б—Г—В.). –Я–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞–ї –Њ–±—Й–µ–µ —З–Є—Б–ї–Њ —Б–ї—Г—З–∞–µ–≤ —Б–Љ–µ—А—В–Є –Њ—В –Ш–С–° –Є –љ–µ—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –Ш–Ь – –≤ –і–∞–љ–љ–Њ–Љ —Б–ї—Г—З–∞–µ –љ–∞ 36% (–Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї 0,64; 95%––є –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–≤–∞–ї –Њ—В 0,50 –і–Њ 0,87) [26].
–†–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л–є –∞–љ–∞–ї–Є–Ј –і–∞–љ–љ—Л—Е, –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е ASCOT–BPLA –Є ASCOT–LLA [27], –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ –њ—А–Њ—П–≤–ї—П–µ—В —Б–Є–љ–µ—А–≥–Є–Ј–Љ —Б –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ, –љ–Њ –љ–µ —Б –∞—В–µ–љ–Њ–ї–Њ–ї–Њ–Љ. –Ш–љ—Л–Љ–Є —Б–ї–Њ–≤–∞–Љ–Є, –Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ –Є –≤ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –µ–≥–Њ —Ж–µ—А–µ–±—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В —Г—Б–Є–ї–Є–≤–∞—О—В—Б—П –њ—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Б –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ, –љ–Њ –љ–µ —Б –∞—В–µ–љ–Њ–ї–Њ–ї–Њ–Љ (—В–∞–±–ї. 4).
–Э–∞–ї–Є—З–Є–µ —Б–Є–љ–µ—А–≥–Є–Ј–Љ–∞ –≤ –Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л—Е —Н—Д—Д–µ–Ї—В–∞—Е –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П —А–µ–Ј—Г–ї—М—В–∞—В–∞—В–∞–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П CAMELOT —Г –±–Њ–ї—М–љ—Л—Е –Ш–С–°, –љ–Њ —Б –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ –Р–Ф [28]. –Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –≤ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є CAMELOT —Б—А–∞–≤–љ–Є–≤–∞–ї–Є—Б—М –≤–ї–Є—П–љ–Є–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є —Н–љ–∞–ї–∞–њ—А–Є–ї–∞ –љ–∞ —А–∞–Ј–≤–Є—В–Є–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Я–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –њ—А–Є –ї–µ—З–µ–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ (–≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 31%), –љ–Њ –љ–µ –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Н–љ–∞–ї–∞–њ—А–Є–ї–Њ–Љ. –Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е –њ–Њ –њ–Њ–і–≥—А—Г–њ–њ–∞–Љ –∞–Љ–ї–Њ–і–Є–њ–Є–љ –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–ї —А–∞–Ј–≤–Є—В–Є–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –ї–Є—И—М —Г –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Б—В–∞—В–Є–љ—Л (—Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 34%). –£ –±–Њ–ї—М–љ—Л—Е, –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Б—В–∞—В–Є–љ—Л, –∞–Љ–ї–Њ–і–Є–њ–Є–љ –±—Л–ї –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ (—Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –≤—Б–µ–≥–Њ –љ–∞ 4%).
–°–Є–љ–µ—А–≥–Є–Ј–Љ –Ї–∞—А–і–Є–Њ––≤–∞–Ј–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Р–Ъ –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞ –Є —Б—В–∞—В–Є–љ–Њ–≤ –Љ–Њ–ґ–љ–Њ –±—Л–ї–Њ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞—В—М –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є ENCORE I –Є ENCORE II, –≤ –Ї–Њ—В–Њ—А—Л—Е –љ–Є—Д–µ–і–Є–њ–Є–љ –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б —Ж–µ—А–Є–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ. –Ю–і–љ–∞–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –љ–Є—Д–µ–і–Є–њ–Є–љ–∞ –Є —Ж–µ—А–Є–≤–∞—Б—В–∞—В–Є–љ–∞ –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ, —В–∞–Ї —В–∞–Ї —Ж–µ—А–Є–≤–∞—Б—В–∞—В–Є–љ –Є–Ј––Ј–∞ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –≤—Л—Б–Њ–Ї–Њ–є —З–∞—Б—В–Њ—В—Л –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –±—Л–ї –Њ—В–Њ–Ј–≤–∞–љ —Б —Д–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ —А—Л–љ–Ї–∞. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –Р–Ъ –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞ b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А—Л –Є –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§, —Б—Г–і—П –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П ASCOT –Є SCAT, –љ–µ –њ—А–Њ—П–≤–ї—П—О—В —Б–Є–љ–µ—А–≥–Є–Ј–Љ–∞ —Б–Њ —Б—В–∞—В–Є–љ–∞–Љ–Є.
–Ґ–∞–Ї –Є–ї–Є –Є–љ–∞—З–µ, –љ–Њ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ – –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–є –њ—А–µ–њ–∞—А–∞—В, —Б–Є–љ–µ—А–≥–Є–Ј–Љ –Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Є –∞–љ—В–Є–∞—В–µ—А–Њ–≥–µ–љ–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Ї–Њ—В–Њ—А–Њ–≥–Њ —Б–Њ —Б—В–∞—В–Є–љ–∞–Љ–Є –і–Њ–Ї–∞–Ј–∞–љ.
–Р–љ–∞–ї–Є–Ј –і–∞–љ–љ—Л—Е –ї–Є—В–µ—А–∞—В—Г—А—Л —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ —В–Њ–Љ, —З—В–Њ –µ—Б—В—М –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Ї–∞—В–µ–≥–Њ—А–Є–є –±–Њ–ї—М–љ—Л—Е –Р–У, —Г –Ї–Њ—В–Њ—А—Л—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ (–Є, –њ–Њ––≤–Є–і–Є–Љ–Њ–Љ—Г, –і—А—Г–≥–Є—Е –Р–Ъ –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞) –Љ–Њ–ґ–µ—В –±—Л—В—М –±–Њ–ї–µ–µ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ—Л–Љ, —З–µ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –і—А—Г–≥–Є—Е –Ї–ї–∞—Б—Б–Њ–≤ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –≤–Ї–ї—О—З–∞—П –љ–µ–Ї–Њ—В–Њ—А—Л–µ –і—А—Г–≥–Є–µ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П:
1. –Р–У —Г –±–Њ–ї—М–љ—Л—Е –Ш–С–°, —Г—З–Є—В—Л–≤–∞—П –љ–∞–ї–Є—З–Є–µ —Г –Р–Ъ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –Є –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ–Њ–≥–Њ (–∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ) —Н—Д—Д–µ–Ї—В–Њ–≤.
2. –Э–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В —Г—А–Њ–≤–љ—П –Р–Ф, –Є–Љ–µ–µ—В –Љ–µ—Б—В–Њ —Б–Є–љ–µ—А–≥–Є–Ј–Љ –≤ –Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л—Е —Н—Д—Д–µ–Ї—В–∞—Е –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ (–Є, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –і—А—Г–≥–Є—Е –Р–Ъ –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞) –Є —Б—В–∞—В–Є–љ–Њ–≤.
3. –Ш–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–∞—П —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П —Г –њ–Њ–ґ–Є–ї—Л—Е –ї–Є—Ж.
4. –Р–У —Г –±–Њ–ї—М–љ—Л—Е —Б–Њ —Б—В–µ–љ–Њ–Ј–Є—А—Г—О—Й–Є–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —Б–Њ–љ–љ—Л—Е –∞—А—В–µ—А–Є–є –Є–ї–Є —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞.
5. –Р–У —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –Є–ї–Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ.
6. –Р–У —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ (—Д—А–∞–Ї—Ж–Є—П –≤—Л–±—А–Њ—Б–∞ –Љ–µ–љ—М—И–µ 40%).
7. –Р–У —Г –±–Њ–ї—М–љ—Л—Е, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–љ–Є–Љ–∞—О—В –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞, –љ–∞–њ—А–Є–Љ–µ—А, –≤ —Б–≤—П–Ј–Є —Б –і–µ—Д–Њ—А–Љ–Є—А—Г—О—Й–Є–Љ –Њ—Б—В–µ–Њ–∞—А—В—А–Њ–Ј–Њ–Љ.
8. –†–µ–љ–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П.
9. –Р–У, –≤—Л–Ј–≤–∞–љ–љ–∞—П —Ж–Є–Ї–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–Љ.
10. –Ш–і–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–є –≥–Є–њ–µ—А–∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–Є–Ј–Љ (–і–≤—Г—Б—В–Њ—А–Њ–љ–љ—П—П –≥–Є–њ–µ—А–њ–ї–∞–Ј–Є—П –Ї–Њ—А—Л –љ–∞–і–њ–Њ—З–µ—З–љ–Є–Ї–Њ–≤).
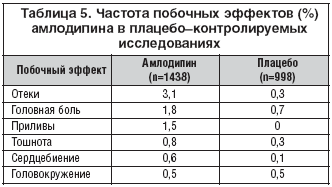
–Р–Љ–ї–Њ–і–Є–њ–Є–љ –Њ—В–ї–Є—З–∞–µ—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –≤—Л—Б–Њ–Ї–Њ–є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О, –љ–Њ –Є –њ—А–µ–≤–Њ—Б—Е–Њ–і–љ–Њ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О. –С–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –±–Њ–ї–µ–µ —З–µ–Љ —Г 2500 –±–Њ–ї—М–љ—Л—Е —Б –Р–У –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е. –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –±—Л–ї–Є –љ–µ–±–Њ–ї—М—И–Є–Љ–Є –Є–ї–Є —Г–Љ–µ—А–µ–љ–љ—Л–Љ–Є –њ–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Є –Ј–∞–≤–Є—Б–µ–ї–Є –Њ—В –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞. –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –≤—Б—В—А–µ—З–∞–ї–Є—Б—М: –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–µ –Њ—В–µ–Ї–Є, –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М –Є –њ—А–Є–ї–Є–≤—Л –Ї—А–Њ–≤–Є (—В–∞–±–ї. 5).
–Ю—В–Љ–µ–љ–∞ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–∞—Б—М –Љ–µ–љ–µ–µ —З–µ–Љ —Г 0,5% –±–Њ–ї—М–љ—Л—Е (—Б —В–∞–Ї–Њ–є –ґ–µ —З–∞—Б—В–Њ—В–Њ–є –њ—А–Є—Е–Њ–і–Є–ї–Њ—Б—М –Њ—В–Љ–µ–љ—П—В—М –њ–ї–∞—Ж–µ–±–Њ).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –∞–Љ–ї–Њ–і–Є–њ–Є–љ —П–≤–ї—П–µ—В—Б—П –≤—Л—Б–Њ–Ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –Ї–Њ—В–Њ—А—Л–є –Њ—В–ї–Є—З–∞–µ—В—Б—П –њ—А–µ–≤–Њ—Б—Е–Њ–і–љ–Њ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О –Є —Г–і–Њ–±–µ–љ –і–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П.
–Ш—И–µ–Љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–Ј–љ—М —Б–µ—А–і—Ж–∞
–Є –Ї–Њ—А–Њ–љ–∞—А–љ—Л–є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј
–Р–Љ–ї–Њ–і–Є–њ–Є–љ, –Ї–∞–Ї –Є –і—А—Г–≥–Є–µ –Р–Ъ, –Њ–±–ї–∞–і–∞–µ—В –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ—Л–Љ (–∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ) –і–µ–є—Б—В–≤–Є–µ–Љ –Є —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е —Д–Њ—А–Љ –Ш–С–° [4,12,13].
–Ъ–∞–Ї –Є –і—А—Г–≥–Є–µ –Р–Ъ, –∞–Љ–ї–Њ–і–Є–њ–Є–љ –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞–µ—В —А–∞–Ј–≤–Є—В–Є–µ –њ—А–Є—Б—В—Г–њ–Њ–≤ –≤–∞–Ј–Њ—Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є (—Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –Я—А–Є–љ—Ж–Љ–µ—В–∞–ї–∞). –Ю–і–љ–∞–Ї–Њ –µ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–µ–µ, –µ—Б–ї–Є —А–µ—З—М –Є–і–µ—В –Њ –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –≤–∞–Ј–Њ—Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–µ–є. –Т–µ–і—М –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ–Њ–µ (–∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–µ) –і–µ–є—Б—В–≤–Є–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –њ—А–Є –њ—А–Є–µ–Љ–µ 1 —А–∞–Ј –≤ —Б—Г—В–Ї–Є –њ—А–Њ–і–Њ–ї–ґ–∞–µ—В—Б—П –±–Њ–ї–µ–µ 24 —З–∞—Б–Њ–≤. –Ъ —В–Њ–Љ—Г –ґ–µ –Њ–љ –Њ—В–ї–Є—З–∞–µ—В—Б—П —Е–Њ—А–Њ—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є.
–Т —А—П–і–µ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ—Л–є (–∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–є) —Н—Д—Д–µ–Ї—В –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ, –∞—В–µ–љ–Њ–ї–Њ–ї–Њ–Љ, –і–Є–ї—В–Є–∞–Ј–µ–Љ–Њ–Љ –Є –і—А—Г–≥–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є [4,12,29]. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, —Г –±–Њ–ї—М–љ—Л—Е –Ш–С–° —Б–Њ —Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–µ–є –љ–∞–њ—А—П–ґ–µ–љ–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ (5–10 –Љ–≥/—Б—Г—В.) —Г–Љ–µ–љ—М—И–∞–µ—В —З–Є—Б–ї–Њ –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є, –њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ —В–∞–±–ї–µ—В–Њ–Ї –љ–Є—В—А–Њ–≥–ї–Є—Ж–µ—А–Є–љ–∞ (–≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 50%) –Є —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П —Д–Є–Ј–Є—З–µ—Б–Ї–Є—Е –љ–∞–≥—А—Г–Ј–Њ–Ї. –Я–Њ –і–∞–љ–љ—Л–Љ 4––љ–µ–і–µ–ї—М–љ–Њ–≥–Њ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –∞–Љ–ї–Њ–і–Є–њ–Є–љ (10 –Љ–≥/—Б—Г—В.) —З–µ—А–µ–Ј 24 —З–∞—Б–∞ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –≤–љ—Г—В—А—М —Г–≤–µ–ї–Є—З–Є–≤–∞–ї –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Є –љ–∞ —В—А–µ–і–Љ–Є–ї–µ (–≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 31%) –Є –≤—А–µ–Љ—П –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –љ–∞–≥—А—Г–Ј–Ї–Є –і–Њ –њ–Њ—П–≤–ї–µ–љ–Є—П –њ—А–Є—Б—В—Г–њ–∞ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є (–љ–∞ 48%). –Я–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ–ї–∞—Ж–µ–±–Њ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Є –љ–∞ —В—А–µ–і–Љ–Є–ї–µ –Є –≤—А–µ–Љ—П –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –љ–∞–≥—А—Г–Ј–Ї–Є –і–Њ –њ–Њ—П–≤–ї–µ–љ–Є—П –њ—А–Є—Б—В—Г–њ–∞ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є —Г–Љ–µ–љ—М—И–∞–ї–Є—Б—М (–љ–∞ 6 –Є 8% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ).
–Я–Њ –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ–Њ–є (–∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є) —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ –љ–µ —Г—Б—В—Г–њ–∞–µ—В b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ –Є –і—А—Г–≥–Є–Љ –Р–Ъ. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –≤–µ—А–∞–њ–∞–Љ–Є–ї–∞ –Є –і–Є–ї—В–Є–∞–Ј–µ–Љ–∞ –∞–Љ–ї–Њ–і–Є–њ–Є–љ –Љ–Њ–ґ–љ–Њ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞—В—М —Б b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г—Б–Є–ї–Є–≤–∞—О—В –µ–≥–Њ –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ–Њ–µ (–∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–µ) –і–µ–є—Б—В–≤–Є–µ.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є CASIS [30] –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б–Њ —Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–µ–є –љ–∞–њ—А—П–ґ–µ–љ–Є—П –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ—Л–µ (–∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ) —Н—Д—Д–µ–Ї—В—Л –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–∞ –∞—В–µ–љ–Њ–ї–Њ–ї–∞ –≤—Л—А–∞–ґ–µ–љ—Л –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ. –Я—А–∞–≤–і–∞, –∞–Љ–ї–Њ–і–Є–њ–Є–љ –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Г–≤–µ–ї–Є—З–Є–≤–∞–ї –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Є –љ–∞ —В—А–µ–і–Љ–Є–ї–µ –і–Њ –њ–Њ—П–≤–ї–µ–љ–Є—П —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є (–≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 29% –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 16% –љ–∞ –∞—В–µ–љ–Њ–ї–Њ–ї–µ). –Э–∞–њ—А–Њ—В–Є–≤, –∞—В–µ–љ–Њ–ї–Њ–ї –±—Л–ї –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –≤ –њ–Њ–і–∞–≤–ї–µ–љ–Є–Є —Н–њ–Є–Ј–Њ–і–Њ–≤ –Є—И–µ–Љ–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –≤–Њ –≤—А–µ–Љ—П —Б—Г—В–Њ—З–љ–Њ–≥–Њ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—П –≠–Ъ–У (—Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 57% –њ—А–Њ—В–Є–≤ 28% –љ–∞ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–µ). –Э–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –Њ–Ї–∞–Ј–∞–ї–∞—Б—М –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є –∞—В–µ–љ–Њ–ї–Њ–ї–∞, –Ї–Њ—В–Њ—А–∞—П —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–∞ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Є –љ–∞ —В—А–µ–і–Љ–Є–ї–µ –і–Њ –њ–Њ—П–≤–ї–µ–љ–Є—П —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 39% –Є —Г–Љ–µ–љ—М—И–∞–ї–∞ —З–Є—Б–ї–Њ —Н–њ–Є–Ј–Њ–і–Њ–≤ –Є—И–µ–Љ–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –≤–Њ –≤—А–µ–Љ—П —Б—Г—В–Њ—З–љ–Њ–≥–Њ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—П –≠–Ъ–У –љ–∞ 72%.
–Т –Ї—А—Г–њ–љ–Њ–Љ 10––љ–µ–і–µ–ї—М–љ–Њ–Љ –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є CAPE II (1994) [31] —Г 234 –±–Њ–ї—М–љ—Л—Е —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Ш–С–° —Б—А–∞–≤–љ–Є–≤–∞–ї–Є –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ—Г—О (–∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї—Г—О) —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є –і–Є–ї—В–Є–∞–Ј–µ–Љ–∞, –∞ —В–∞–Ї–ґ–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є –∞—В–µ–љ–Њ–ї–Њ–ї–∞ –Є –і–Є–ї—В–Є–∞–Ј–µ–Љ–∞ –Є –Є–Ј–Њ—Б–Њ—А–±–Є–і–∞–5––Љ–Њ–љ–Њ–љ–Є—В—А–∞—В–∞. –†–µ–Ј—Г–ї—М—В–∞—В—Л –Є–Ј—Г—З–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Њ–Ї–∞–Ј–∞–ї–Є—Б—М —Б—Е–Њ–і–љ—Л–Љ–Є. –Ф–Њ–±–∞–≤–ї–µ–љ–Є–µ –≤—В–Њ—А–Њ–≥–Њ –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї —Г—Б–Є–ї–µ–љ–Є—О –∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є –і–Є–ї—В–Є–∞–Ј–µ–Љ–∞, –њ—А–Є—З–µ–Љ –∞–Љ–ї–Њ–і–Є–њ–Є–љ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –∞—В–µ–љ–Њ–ї–Њ–ї–Њ–Љ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є–ї –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—О –і–Є–ї—В–Є–∞–Ј–µ–Љ–∞ –Є –љ–Є—В—А–∞—В–∞ (–љ–∞–њ—А–Є–Љ–µ—А, –њ—А–Є—А–Њ—Б—В –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –љ–∞–≥—А—Г–Ј–Ї–Є —Б–Њ—Б—В–∞–≤–Є–ї 70 –Є 47 —Б–µ–Ї. —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –∞–Љ–ї–Њ–і–Є–њ–Є–љ —П–≤–ї—П–µ—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ—Л–Љ (–∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ) —Б—А–µ–і—Б—В–≤–Њ–Љ, –Ї–Њ—В–Њ—А–Њ–µ –Љ–Њ–ґ–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Ї–∞–Ї –∞–љ–≥–Є–Њ—Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є, —В–∞–Ї –Є —Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –љ–∞–њ—А—П–ґ–µ–љ–Є—П. –Р–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –њ—А–Є –µ–≥–Њ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–Є–Є —Б b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є.
–Т –і–≤—Г—Е –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –Є–Ј—Г—З–∞–ї–∞—Б—М —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ —В–Њ—А–Љ–Њ–Ј–Є—В—М –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞. –≠—В–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П PREVENT –Є CAMELOT. –Т 3––ї–µ—В–љ–µ–Љ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є PREVENT –∞–Љ–ї–Њ–і–Є–њ–Є–љ (5–10 –Љ–≥/—Б—Г—В.) –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–ї –≤–ї–Є—П–љ–Є—П –љ–∞ —В–µ—З–µ–љ–Є–µ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞, –Њ–і–љ–∞–Ї–Њ —Г–Љ–µ–љ—М—И–∞–ї —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е —Б–Њ–±—Л—В–Є–є. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Њ–±—Й–∞—П —Б–Љ–µ—А—В–љ–Њ—Б—В—М —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 26%, —А–Є—Б–Ї –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ – –љ–∞ 6%, —А–Є—Б–Ї –Є–љ—Б—Г–ї—М—В–∞ – –љ–∞ 1% –Є –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞—Е –љ–∞ –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –∞—А—В–µ—А–Є—П—Е – –љ–∞ 43% [32]. –Я—А–∞–≤–і–∞, –њ—А–Є —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П PREVENT –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ, —З—В–Њ –∞–Љ–ї–Њ–і–Є–њ–Є–љ —Б–њ–Њ—Б–Њ–±–µ–љ –≤—Л–Ј—Л–≤–∞—В—М —А–µ–≥—А–µ—Б—Б–Є—О –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞, –µ—Б–ї–Є —Б—В–µ–љ–Њ–Ј –њ—А–µ–≤—Л—И–∞–µ—В 70% [33].
–Т —Г–ґ–µ —Г–њ–Њ–Љ—П–љ—Г—В–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є CAMELOT —Г –±–Њ–ї—М–љ—Л—Е –Ш–С–° –∞–Љ–ї–Њ–і–Є–њ–Є–љ —В–Њ—А–Љ–Њ–Ј–Є–ї –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –њ–ї–∞—Ж–µ–±–Њ –Є —Н–љ–∞–ї–∞–њ—А–Є–ї–∞ [28]. –†–∞–Ј–ї–Є—З–Є—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–∞—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є PREVENT –Є CAMELOT, –Ї–∞—Б–∞—О—Й–Є—Е—Б—П –≤–ї–Є—П–љ–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –љ–∞ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞, –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М —В–µ–Љ, —З—В–Њ –≤ –њ–µ—А–≤–Њ–Љ —Б—В–∞—В–Є–љ—Л –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –њ–Њ–ї—Г—З–∞–ї–Є 27% –±–Њ–ї—М–љ—Л—Е, –∞ –≤–Њ –≤—В–Њ—А–Њ–Љ – 83% –±–Њ–ї—М–љ—Л—Е.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –∞–Љ–ї–Њ–і–Є–њ–Є–љ —В–Њ—А–Љ–Њ–Ј–Є—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –≤ —В–Њ–Љ —Б–ї—Г—З–∞–µ, –µ—Б–ї–Є –љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б–Њ —Б—В–∞—В–Є–љ–∞–Љ–Є.
–Ф–∞–љ–љ—Л–µ, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є CAPARES, –њ–Њ—Б–ї—Г–ґ–Є–ї–Є –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ —Б —Ж–µ–ї—М—О —Г–ї—Г—З—И–µ–љ–Є—П –њ—А–Њ–≥–љ–Њ–Ј–∞ —Г –±–Њ–ї—М–љ—Л—Е –Ш–С–° –њ–Њ—Б–ї–µ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –∞–љ–≥–Є–Њ–њ–ї–∞—Б—В–Є–Ї–Є. –Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –≤ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є CAPARES [34] –і–≤–Њ–є–љ—Л–Љ —Б–ї–µ–њ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –Є–Ј—Г—З–∞–ї–Є –≤–ї–Є—П–љ–Є–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ (10 –Љ–≥/—Б—Г—В.) –љ–∞ —В–µ—З–µ–љ–Є–µ –Ш–С–° —Г 585 –±–Њ–ї—М–љ—Л—Е –њ–Њ—Б–ї–µ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –∞–љ–≥–Є–Њ–њ–ї–∞—Б—В–Є–Ї–Є. –Ы–µ—З–µ–љ–Є–µ –љ–∞—З–Є–љ–∞–ї–Є –Ј–∞ 2 –љ–µ–і–µ–ї–Є –і–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –Є –њ—А–Њ–і–Њ–ї–ґ–∞–ї–Є –≤ —В–µ—З–µ–љ–Є–µ 4 –Љ–µ—Б. –Ш–Ј–Љ–µ–љ–µ–љ–Є—П –і–Є–∞–Љ–µ—В—А–∞ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –∞—А—В–µ—А–Є–Є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –∞–Љ–ї–Њ–і–Є–њ–Є–љ –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ, –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–Є—Б—М. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є –≤ –њ–Њ–≤—В–Њ—А–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞—Е –љ–∞ –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –∞—А—В–µ—А–Є—П—Е (–љ–∞ 55%; —А=0,02), –∞ —В–∞–Ї–ґ–µ —Б—Г–Љ–Љ–∞—А–љ–Њ–≥–Њ —А–Є—Б–Ї–∞ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤, –≤–Ї–ї—О—З–∞—П —Б–Љ–µ—А—В—М, –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞, –∞–Њ—А—В–Њ––Ї–Њ—А–Њ–љ–∞—А–љ–Њ–µ —И—Г–љ—В–Є—А–Њ–≤–∞–љ–Є–µ –Є–ї–Є –∞–љ–≥–Є–Њ–њ–ї–∞—Б—В–Є–Ї—Г (–љ–∞ 35%; —А=0,049). –С–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –њ–Њ—Б–ї–µ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –∞–љ–≥–Є–Њ–њ–ї–∞—Б—В–Є–Ї–Є –Њ–±—К—П—Б–љ—П—О—В –µ–≥–Њ –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ—Л–Љ–Є –Є –∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –∞–Љ–ї–Њ–і–Є–њ–Є–љ —Г–ї—Г—З—И–∞–µ—В –њ—А–Њ–≥–љ–Њ–Ј —Г –±–Њ–ї—М–љ—Л—Е –Ш–С–° –њ–Њ—Б–ї–µ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –∞–љ–≥–Є–Њ–њ–ї–∞—Б—В–Є–Ї–Є, —Е–Њ—В—П –Є –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є–µ –љ–∞ —А–Є—Б–Ї —А–µ—Б—В–µ–љ–Њ–Ј–∞.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Ш—В–∞–Ї, –і–ї–Є—В–µ–ї—М–љ–Њ–і–µ–є—Б—В–≤—Г—О—Й–Є–є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В –Ї–∞–ї—М—Ж–Є—П –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞ –∞–Љ–ї–Њ–і–Є–њ–Є–љ —П–≤–ї—П–µ—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–Љ –Є –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ. –Я—А–Є –Р–У –Њ–љ —Б—А–∞–≤–љ–Є–Љ –њ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б –і—А—Г–≥–Є–Љ–Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Њ—Б–љ–Њ–≤–љ—Л—Е –Ї–ї–∞—Б—Б–Њ–≤; –Љ–Њ–ґ–µ—В –љ–∞–Ј–љ–∞—З–∞—В—М—Б—П –Ї–∞–Ї –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є, —В–∞–Ї –Є –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –і—А—Г–≥–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є. –Я—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е —Д–Њ—А–Љ–∞—Е –Ш–С–° –∞–Љ–ї–Њ–і–Є–њ–Є–љ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В—М –Ї —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–µ, —Г–Љ–µ–љ—М—И–∞–µ—В —З–Є—Б–ї–Њ –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –Є –њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –љ–Є—В—А–Њ–≥–ї–Є—Ж–µ—А–Є–љ–∞, –∞ —В–∞–Ї–ґ–µ —Г–Љ–µ–љ—М—И–∞–µ—В —З–Є—Б–ї–Њ –±–Њ–ї–µ–≤—Л—Е –Є –±–µ–Ј–±–Њ–ї–µ–≤—Л—Е —Н–њ–Є–Ј–Њ–і–Њ–≤ –Є—И–µ–Љ–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞. –Ю–љ —В–∞–Ї–ґ–µ —Г–ї—Г—З—И–∞–µ—В –њ—А–Њ–≥–љ–Њ–Ј —Г –±–Њ–ї—М–љ—Л—Е –Ш–С–° –њ–Њ—Б–ї–µ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –∞–љ–≥–Є–Њ–њ–ї–∞—Б—В–Є–Ї–Є. –Т –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б–Њ —Б—В–∞—В–Є–љ–∞–Љ–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ —Б–њ–Њ—Б–Њ–±–µ–љ —В–Њ—А–Љ–Њ–Ј–Є—В—М –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞.

–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Opie L.H. Clinical use of calcium channel antagonist drugs. 2th edition. – Boston, 1990.
2. –Я—А–µ–Њ–±—А–∞–ґ–µ–љ—Б–Ї–Є–є –Ф.–Т. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П. — –Ь., 1993.
3. –°–Є–і–Њ—А–µ–љ–Ї–Њ –С.–Р., –Я—А–µ–Њ–±—А–∞–ґ–µ–љ—Б–Ї–Є–є –Ф.–Т. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П –≤ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ. — –Ь., 1997.
4. –°–Є–і–Њ—А–µ–љ–Ї–Њ –С.–Р, –Я—А–µ–Њ–±—А–∞–ґ–µ–љ—Б–Ї–Є–є –Ф.–Т. –Р–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П. — –Ь., 1997.
5. Messerli F. (ed.) The ABC of antihypertensive therapy. — 2th edition. – Philadelphia, 2000.
6. Triggle D.J. Mechanisms of action of calcium channel antagonists. — In: Calcium antagonists in clinical medicine. Ed. by M.Epstein. – Philadelphia, 1998. – pp. 1–26.
7. Luscher Th.F., Cosebtino F. The classification of calcium antagonists and their selection in the treatment of hypertension. – Drugs, 1998; 55 (4): 309–317.
8. Opie L.H. Drugs for the heart. 4th edition. – Philadelphia, 1995.
9. Elliott H.L. Requirements for new calcium antagonists. – Research Clin. Forums, 1994; 16 (1): 9–16.
10. Hansson L Treatment of elderly hypertensive patients with calcium antagonists. –– Research Clin. Forums, 1994; 16 (1): 61–68.
11. Toyo–Oka T., Nayler W.G. Third generation calcium entry blockers. – Blood Pressure, 1996; 5: 206–208.
12. Nayler W.G. Amlodipine. – Berlin, 1995.— pp. 1–273.
13. –Я—А–µ–Њ–±—А–∞–ґ–µ–љ—Б–Ї–Є–є –Ф.–Т., –°–Є–і–Њ—А–µ–љ–Ї–Њ –С.–Р., –®–∞–±–∞–µ–≤–∞ –Х.–Э. –Р–Љ–ї–Њ–і–Є–њ–Є–љ – –∞–љ—В–∞–≥–Њ–љ–Є—Б—В –Ї–∞–ї—М—Ж–Є—П —В—А–µ—В—М–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П. – –Ъ–∞—А–і–Є–Њ–ї–Њ–≥–Є—П, 1998; вДЦ2. – —Б—В—А. 66–73.
14. Epstein M. Role of a third generation calcium antagonists in the management of hypertension. – Drugs, 1999; 57 (suppl. 1): 1–10.
15. McClellan K.J., Jarvis B. Lercanidipine. A review of its use in hypertension. – Drugs, 2000; 60 (5): 1123–1140.
16. Barchielli M., Dolfini E., Farina P. et al. Clinical pharmacokinetics of lercanidipine. — J. Cardiovascul. Pharmacol., 1997; 29 (supp;. 2): S1–S15.
17. Herbette L.G., Vecchiarelli M., Leonardi A. Lercanidipine: Short plasma half–life, long duration of action. — J. Cardiovascul. Pharmacol., 1997; 29 (supp;. 2): S19–S24.
18. Van Zweiten P.A., Pfaffendorf M. Similarities and differences between calcium antagonists: Pharmacological aspects. – J. Hypertension, 1993; 11 (suppl. 1): S3–S11.
19. Meredith P.A. Duration of action and through to peak rations of calcium antagonists. – Research Clin. Forums, 1994; 16 (1): 29–41.
20. Van Zweiten P.A., Pfaffendorf M. Pharmacology of dihydropyridine calcium antagonists; Relatiomship between lipophilicity and pharmacodynamic response — J. Hypertension, 1993; 11 (suppl. 6): S3—S11.
21. Kloner R., Sowers L., DiBona G. et al. Sex– and age–related Antihypertensive effects of amlodipine. The Amlodipine Cardiovascular Community Trial study group. – Amer. J. Cardiol., 1996; 77 (9): 713—722.
22. Meredith P.A. Role of through to peak efficacy in the evaluation of antihypertensive efficacy – J. Hypertension, 1998; 16 (suppl. 1): S59—S64.
23. Neaton J.D., Grimm R.H., Prineas R.J et al. Treatment of Mild Hypertension Study: final results – JAMA, 1993; 270: 713—724.
24. The ALLHAT officers and coordinators for the ALLHAT collaborative research group. Major cardiovascular events in hypertensive patients randomized to doxazosin vs chlorthalidone: The Antihypertensive and Lipid–Lowering treatment to prevent Heart Attack Trial (ALLHAT). – JAMA, 2000; 283: 1967—1975.
25. Dahlof B., Sever P. S., Poulter N. R. et al. Prevention of cardiovascular events with an Antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendrofluazide as required, in Anglo–Scandinavian Cardiac Outcomes Trial Blood Pressure Lowering Arm (ASCOT–BPLA): a multicentre randomized controlled trial. – Lancet, 2005; 366: 895—906.
26. Sever P. S., Dahlof B., Poultier N. R. et al. Prevention of coronary and stroke events with atorvastatin in hypertensive patients who have average or lower–than–average cholesterol concentrations, in Anglo–Scandinavian Cardiac Outcomes Trial–Lipid–Lowering Arm (ASCOT–LLA): multicentre randomised controlled trial. – Lancet, 2003; 361: 1149—1158.
27. Sever P. S., Dahlof B., Poultier N. R. et al. Potential synergy between lipid–lowering and blood–pressure–lowering in the Anglo–Scandinavian Cardiac Outcomes Trial. – Europ. Heart J., 2006; 27: 2982—2988.
28. Nissen S., Tuzcu E., Libby P. et al. Effects of antihypertensive drugs on cardiovascular events in patients with coronary heart disease and normal blood pressure. Randomized controlled CAMELOT study. – JAMA, 2004; 292 (18): 2217—2226.
29. Deanfield J., Detry J., Lichtlen P. et al. Amlodipine reduces transient myocardial ischemia in patients with coronary heart disease: Double–blind Circadian Anti–ischemia Program in Europe (CAPE trial). – JACC, 1994; 26 (4): 1460—1467.
30. Davis R. F., Habibi H., Klinke W. P. et al. Effect of amlodipine, atenolo and their combination on myocardial ischemia during treadmill exercise and ambulatory monitoring. – JACC, 1995; 25: 619—625.
31. Deanfield J., Detry J., Sellier P. et al. Medical treatment of myocardial ischemia in coronary heart disease: Effect of drug regimen and irregular dosing in CAPE II trial. – JACC, 2002; 40 (5): 917—925.
32. Pitt B., Byington R., Furberg C. et al. Effect of amlodipine on the progression of atherosclerosis and the occurrence of clinical events. – Circulation, 2000; 102: 1503—1510.
33. Mancini G. B. J., Miller M. E., Evans G. W. et al. Post hoc analysis of coronary findings from the Prospective Randomized Evaluation of the Vascular Effects of the Norvasc Trial (PREVENT). – Amer. J. Cardiol., 2002; 89 (12): 1414—1416.
34. Jorgensen B., Thaulow E. Effects of amlodipine on ischemia after percutaneuos transluminal coronary angioplasty: Secondary results of the Coronary Angioplasty Amlodipine Restenosis (CAPARES) study. – Amer. Heart J., 2003; 145: 1030—1035.












