АК представляют собой (как и большинство других классов лекарств, используемых в кардиологии) достаточно гетерогенную группу препаратов как по химическим свойствам, так и по фармакокинетике и фармакодинамике. По химической структуре АК разделяют на три группы: производные дигидропиридина, фенилалкиламина и бензодиазепина (табл. 1).
Механизм действия АК заключается в связывании с a1с субъединицей потенциалзависимых кальциевых каналов L–типа (медленно инактивируемых) и их неконкурентном блокировании [2]. Кальциевые каналы L–типа выделены из миокарда, гладкомышечных клеток сосудистой стенки (артериол и вен), гладкомышечных клеток внесосудистой локализации (бронхов, желудочно–кишечного и мочеполового трактов, матки), а также из несокращающихся тканей (поджелудочной железы, надпочечников, слюнных желез и др.) [1]. Блокируя эти каналы, АК обеспечивают вазодилатацию и уменьшение общего периферического сопротивления, а также негативный инотропный эффект, что, с одной стороны, обеспечивает их антигипертензивное и антиангинальное действие, а с другой – подчас нежелательное снижение сократительной способности миокарда.
Различие химической структуры дигидропиридиновых и недигидропиридиновых АК определяет неодинаковую их специфичность связывания с кальциевыми каналами L–типа. Дигидропиридины в основном связываются с кальциевыми каналами в гладкомышечных клетках сосудов, а недигидропиридиновые АК связываются с каналами не только в гладких миоцитах, но и в миокарде, клетках синоатриального и атриовентрикулярного (АВ) узлов. Вследствие этого дигидропиридиновые АК являются более сильными вазодилататорами, сравнительно слабо воздействующими на функцию миокарда, зачастую они приводят к развитию рефлекторной тахикардии. Недигидропиридиновые АК меньше дилатируют периферические артерии, но обладают значительными отрицательным и хронотропным и инотропным эффектами.
АК нередко разделяют на 3 поколения. I поколение препаратов характеризуется в основном коротким периодом полувыведения (3–12 ч.), что требует многократного (3–4 раза в сутки) приема. АК II поколения обладают большим периодом полувыведения, могут назначаться 1–2 раза в сутки, наиболее длительный период полувыведения свойственен препаратам III поколения (до 45 ч.), что позволяет получить стойкий эффект при однократном приеме в течение суток. Кроме того, для АК II и III поколений характерны менее выраженный отрицательный инотропный эффект, большая селективность в отношении коронарных и мозговых сосудов.
АК быстро всасываются при приеме внутрь, однако их биодоступность относительно невысока и зависит от интенсивности их метаболизма в кишечнике и печени [3]. Для АК характерен эффект первого прохождения, они метаболизируются в печени преимущественно системой цитохрома P–450 CYP3A4 [4–6]. Этот же изофермент цитохрома ответственен за метаболизм циклоспорина, теофиллина, симвастатина, хинидина и такролимуса. Поэтому возможно усиление токсичности теофиллина и увеличение риска развития рабдомиолиза на фоне приема симвастатина при их комбинации с АК, в частности с верапамилом. АК не должны применяться совместно с грейпфрутовым соком, который ингибируя изофермент цитохрома CYP3A4, может привести к повышению концентрации АК в крови и потенцированию нежелательных побочных эффектов.
Основные побочные действия и противопоказания к применению АК представлены в таблице 2.
В конце 80–х – начале 90–х годов прошлого века в США сложилась парадоксальная ситуация: АК стали самыми продаваемыми антигипертензивными препаратами, в то время как не было выполнено ни одного рандомизированного контролируемого испытания (РКИ) по применению АК при АГ. В 1995 г. K. Furberg на заседании Американской ассоциации сердца продемонстрировал пустой слайд под заголовком «РКИ с АК при артериальной гипертензии» [7]. Опубликованный им в том же году мета–анализ применения короткодействующего нифедипина при ИБС [8] бросил тень на всю группу АК и стимулировал дискуссию о месте этих препаратов в кардиологии, имевшую результатом существенное сокращение их использования. При этом данные, полученные в отношении применения короткодействующего нифедипина у больных, недавно перенесших инфаркт миокарда (ИМ), зачастую переносились на другие АК и распространялись на все сердечно–сосудистые заболевания, включая АГ. Однако в последующие годы было выполнено множество РКИ [9–29], оценивавших влияние АК на конечные точки у больных АГ.
SYST–EUR стало первым исследованием влияния АК на прогноз у больных АГ. Применение нитрендипина 10–40 мг/сут. в сравнении с плацебо у 4695 пожилых больных с изолированной систолической АГ (ИСАГ) обеспечило снижение числа инсультов на 42%, что позволило закончить исследование досрочно [9], причем в подгруппе больных сахарным диабетом (СД) также отмечалось снижение числа сердечно–сосудистых событий и даже общей смертности [10]. Последующее исследование Syst–China [11], хотя и не в полной мере отвечало современным западным стандартам РКИ, дало похожие результаты: нитрендипин обеспечил снижение числа инсультов и всех сердечно–сосудистых событий на 38% и 37% соответственно. В РКИ STOP–2 [12] новое лечение (фелодипин или исрадипин) не уступало традиционной терапии b–адреноблокатором (b–АБ) и диуретиком по способности снижать сердечно–сосудистую смертность и по влиянию на другие конечные точки. Влияние нифедипина в виде гастроинтестинальной терапевтической системы (ГИТС) в дозе 30–60 мг/сут. в сравнении с комбинированным диуретиком ко–амилоридом на основные сердечно–сосудистые события изучалось в испытании INSIGHT [13], включавшем 6321 больного АГ с сопутствующими факторами риска. Пролонгированный нифедипин оказался не только высокоэффективным в плане снижения АД (целевого АД достигли 70% пациентов), но и не уступал диуретику по снижению числа основных сердечно–сосудистых событий (нефатальный ИМ, внезапная смерть, фатальный и нефатальный инсульт, сердечная недостаточность), причем число новых случаев СД на фоне АК было меньшим на 23%. Однако было выявлено неблагоприятное влияение нифедипина ГИТС на риск фататльного ИМ (относительный риск (ОР=3,22; р=0,014). В исследовании NORDIL [14] с участием 10881 пациента с АГ дилтиазем не уступил b–АБ и/или диуретикам по снижению числа главных сердечно–сосудистых осложнений. Более того, число случаев фатального и нефатального инсульта на фоне приема дилтиазема было ниже, чем в группе b–АБ и/или диуретика (ОР=0,80; р=0,04). Аналогичные данные получены в испытании CONVINCE [15] при сравнении верапамила замедленного высвобождения с b–АБ и/или диуретиками у 16602 больных АГ с дополнительными факторами риска.
В крупнейшем испытании ALLHAT (33357 больных АГ), существенно повлиявшем на тактику антигипертензивной терапии в последние годы, АК амлодипин был так же эффективен по влиянию на конечные точки (фатальный и нефатальный ИМ, общая смертность), как диуретик хлорталидон и ингибитор ангиотензинпревращающего фермента (иАПФ) лизиноприл [16]. К сожалению, выводы из исследования ALLHAT о преимуществах терапии диуретиками по сути своей носили политический характер. Со строгой научной точки зрения результаты ALLHAT следует рассматривать с учетом высокого числа в популяции исследования лиц негроидной расы и латиноамериканцев, разницы в достижении целевого давления и высокой частоты новых случаев СД в группе диуретика. Так, ОР СД по сравнению с хлорталидоном в группе амлодипина составил 0,80, а в группе лизиноприла – 0,70. Очевидно, что с учетом этих данных, вывод из ALLHAT – одинаковая эффективности АК, иАПФ и диуретика. Сравнение эффективности АК с блокатором рецепторов ангиотензина II (БРА) валсартаном проводилось в многоцентровом рандомизированном испытании VALUE [17]. В это исследование включили 15245 больных АГ с высоким риском кардиальных осложнений, которых рандомизировали в группу амлодипина 5–10 мг/сут. или в группу валсартана 80–160 мг/сут. с последующим добавлением при необходимости гидрохлортиазида. К концу исследования между группами не было различий по частоте первичной комбинированной конечной точки, сердечной летальности, сердечной заболеваемости, новых случаев сердечной недостаточности. Вместе с тем в группе амлодипина было достоверно на 19% меньше новых случаев фатального и нефатального ИМ, а в группе валсартана достоверно на 23% меньше новых случаев СД.
В недавнем крупном РКИ ASCOT–BPLA, включавшем 19257 пациентов с АГ и минимум тремя факторами риска, сравнивались два режима терапии: амлодипином с добавлением при необходимости периндоприла и атенололом с добавлением при необходимости бендрофлуметиазида. Исследование было прекращено досрочно, так как было выявлено существенное преимущество терапии АК и иАПФ: в группе амлодипина частота инсульта была ниже на 23%, общая частота сердечно–сосудистых событий и вмешательств на 16%, а общая смертность – на 11%. Частота нефатального ИМ снизилась недостоверно (на 10%). В то же время в группе атенолола и диуретика частота возникновения новых случаев СД была достоверно выше (на 30%) [18].
Стратегия лечения больных АГ в сочетании с ИБС изучалась в исследовании INVEST [19]. 22576 пациентам назначали либо верапамил замедленного высвобождения в дозе 240 мг/сут. с присоединением иАПФ трандолаприла и диуретика гидрохлортиазида для достижения целевого АД, либо атенолол с присоединением гидрохлортиазида, а затем трандолаприла. В среднем через 2,7 лет наблюдения первичной конечной точки (общая смертность, нефатальный ИМ, нефатальный инсульт) достигли 9,93% пациентов в группе верапамила и 10,17% – в группе атенолола, различие было недостоверным. Таким образом, было показано, что в лечении больных АГ с ИБС АК (верапамил) не уступает b–АБ (атенололу).
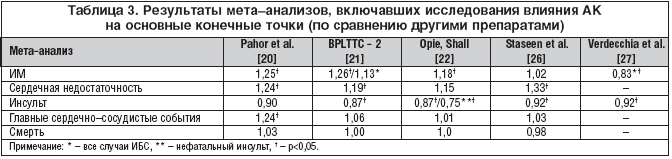
Результаты РКИ были обобщены в нескольких мета–анализах [20–26], позволивших четко определить место АК в лечении АГ (табл. 3).
Обобщая имеющиеся результаты отдельных РКИ и мета–анализов можно сделать следующие выводы: на сегодня не вызывает сомнений, что АК являются эффективными антигипертензивными лекарствами, не уступающими как «традиционным», так и «новым» препаратам по влиянию на общую смертность и частоту основных сердечно–сосудистых событий. При сравнении с плацебо эффективность и безопасность АК, а равно и их положительное влияние на прогноз при АГ, еще более очевидны.
Вместе с тем имеется ряд особенностей, присущих этому классу антигипертензивных препаратов. По–видимому, АК более эффективны в первичной профилактике инсульта у больных АГ, чем другие антигипертензивные средства. Недавно опубликован систематический обзор и мета–анализ [27] 28 исследований, включавших 179122 пациентов, целью которого было выяснение, насколько предотвращение ИБС и инсульта с помощью АК или иАПФ обусловлено именно специфическим действием данных групп препаратов, а не только снижением АД. Было отмечено, что хотя обе группы препаратов достоверно снижают риск инсульта по сравнению с плацебо, эффект АК (отношение шансов (ОШ) =0,65, р<0,001) значительно превосходит эффект иАПФ (ОШ=0,84, p<0,02), более того, эффективность иАПФ достоверно не отличалась от терапии диуретиками/ b–АБ, тогда как лечение АК было более эффективным (ОШ=0,92, р<0,04). Однако риск развития сердечной недостаточности на фоне терапии АК несколько выше, чем на фоне других антигипертензивных средств. В отношении частоты ИМ на сегодняшний день нет полной ясности, так как недавние исследования VALUE и ASCOT–BPLA показали снижение числа новых ИМ на фоне лечения амлодипином, в то время как ранее отмечалось отчетливое увеличение случаев ИМ на фоне лечения АК.
Интересно влияние АК на гипертрофию левого желудочка (ГЛЖ) – важного независимого предиктора внезапной смерти, ИМ и других сердечно–сосудистых осложнений у больных АГ. Как показали несколько мета–анализов [29–31], по способности вызывать регрессию ГЛЖ АК уступают только иАПФ, превосходя препараты других классов, а мета–анализ Schmeider [32] показал преимущества АК над другими классами препаратов. Вместе с тем данные отдельных исследований противоречивы, имеются методологические трудности проведения подобных испытаний, поэтому истинная роль различных классов или конкретных антигипертензивных препаратов в регрессии ГЛЖ недостаточно ясна.
Большим преимуществом АК является их метаболическая нейтральность, что позволяет их использовать при метаболическом синдроме и/или СД 2 типа. В новейшем мета–анализе [33] 22 РКИ, включавших 143153 пациента, оценивали способность различных классов антигипертензивных препаратов уменьшать число новых случаев СД у больных АГ. В мета–анализ вошли 9 исследований, в которых АК применялись как основные препараты или как препараты сравнения. В качестве референтного агента использовались диуретики, для которых ОШ было принято за 1,0. По влиянию на число новых случаев СД классы антигипертензивных препаратов и плацебо расположились в следующем порядке: БРА (ОШ=0,57, р<0,0001), иАПФ (ОШ=0,67, p<0,0001), АК (ОШ=0,75, р<0,002), плацебо (ОШ=0,77, р=0,009), b–АБ (ОШ=0,90, р=0,30). Таким образом, если сравнивать с плацебо, АК, уступая БРА и иАПФ, всё же достоверно снижают число новых случаев СД, тогда как диуретики и b–АБ – увеличивают.
По данным экспериментальных исследований, АК обладают антиатерогенными свойствами, то есть способны замедлить прогрессирование атеросклероза в коронарных и сонных артериях у больных АГ и/или ИБС. Первым РКИ по антиатерогенному действию АК было испытание INTACT [34] с нифедипином, в котором оценивалось влияние препарата на прогрессирование атеросклероза и формирование новых атеросклеротических бляшек в коронарных артериях у больных коронарным атеросклерозом. Через 3 года наблюдения в группе нифедипина число новых бляшек в пересчете на одного пациента было на 28% ниже, чем в группе плацебо (р=0,034). В исследовании ELSA [35] применение лацидипина у больных АГ независимо от снижения АД ассоциировалось с достоверным уменьшением толщины комплекса интима–медиа в области дистальных отделов общей сонной артерии и ее бифуркации, в то время как прием атенолола не оказывал подобного действия. Похожие данные были получены в исследовании VHAS для верапамила в сравнении с хлорталидоном [36]. Однако ни в одном из приведенных исследований зарегистрированное торможение процесса атерогенеза не сопровождалось улучшением отдаленного исхода заболевания по сравнению с другими препаратами.
В более позднем исследовании PREVENT применение амлодипина у больных ИБС обеспечило достоверное уменьшение скорости прогрессирования атеросклеротического поражения сонных артерий: толщина комплекса интима–медиа в группе амлодипина снизилась на 0,0126 мм, тогда как в группе плацебо возросла на 0,033 мм (р=0,007) [37]. В то же время не было выявлено влияния препарата на прогрессирование коронарного атеросклероза по данным коронарной ангиографии, но применение амлодипина обеспечило снижение частоты новых случаев нестабильной стенокардии на 33% и потребности в реваскуляризации миокарда на 43%. Интересны результаты плацебо–контролируемого исследования NICOLE [38], в котором дигидропиридиновый АК нисолдипин назначали пациентам, подвергнутым одно– или многососудистой ангиопластике. Несмотря на то, что между группами нисолдипина и плацебо не было выявлено достоверной разницы в частоте рестеноза, а также по величине минимального диаметра коронарной артерии или выраженности стенозов, отмечалось отчетливое снижение частоты неблагоприятных событий (смерть, инсульт, инфаркт миокарда, повторное чрескожное коронарное вмешательство (ЧКВ) или ЧКВ по поводу нового стеноза) в группе нисолдипина (44,6% против 52,6%, р=0,02).
Новые данные об антиатерогенном потенциале АК и связанном с этим эффектом влиянии на прогноз больных ИБС с нормальным АД или в сочетании с АГ получены в крупных РКИ ACTION и CAMELOT. В плацебо–контролируемом исследовании ACTION 7655 больным стенокардией в сочетании с АГ или без таковой, получавшим оптимальную терапию, назначали нифедипин ГИТС в дозе 60 мг/сут. Хотя через 5 лет наблюдения достоверных различий между группами по достижению первичной комбинированной конечной точки (смерть, ИМ, рефрактерная стенокардия, ХСН, инсульт) не было, терапия нифедипином ГИТС обеспечила достоверное снижение числа новых случаев ХСН, инсульта, а также потребность в проведении коронарного шунтирования [40]. Последующий анализ результатов исследования показал, что наибольшая эффективность пролонгированного нифедипина отмечалась в группе больных ИБС в сочетании с АГ, в которой лечение АК позволило достоверно снизить на 13% риск основных сердечно–сосудистых событий. В исследовании CAMELOT [41] 1991 пациенту с ИБС и нормальным АД в дополнение к оптимальной терапии назначали либо амлодипин 10 мг/сут., либо эналаприл 20 мг/сут., либо плацебо. Через 2 года наблюдения в группе амлодипина по сравнению с плацебо отмечено достоверное снижение на 31% частоты неблагоприятных сердечно–сосудистых событий (сердечно–сосудистой смерти, нефатального ИМ, коронарной реваскуляризации и др.), причем преимущественно за счет уменьшения частоты реваскуляризации. Внутрисосудистое ультразвуковое исследование коронарных артерий 274 больных показало отсутствие прогрессирования атеросклероза в группе амлодипина (p=0,31), тогда как в группе эналаприла отмечалась тенденция к его прогрессированию (p=0,08) и несомненное прогрессирование в группе плацебо (р<0,001).
Таким образом, наличие антиатерогенного действия у АК в целом не вызывает сомнений, и, возможно, именно этим эффектом объясняется выраженное снижение частоты инсультов у больных АГ на фоне терапии АК. В то же время имеющиеся данные исследований во многом противоречивы как в отношении влияния АК на разные сосудистые бассейны (сонные артерии, коронарные артерии), так и по влиянию отдельных препаратов на конечные точки. Последние в различных РКИ неодинаковы, не всегда жесткие и зачастую комбинированные. Вместе с тем использование данных эффектов АК представляется весьма перспективным.
Полученные в этих исследованиях данные об антиатерогенном действии АК позволили в Рекомендациях ЕОК/ЕОАГ 2003 г. по лечению АГ [39] в качестве одного из показаний к использованию АК указать атеросклероз сонных артерий. В отечественных Рекомендациях ВНОК 2004 г. [42] показаниями для дигидропиридиновых АК являются: пожилой возраст больного, ИСАГ, стенокардия, атеросклероз периферических или сонных артерий, беременность; для недигидропиридинов – стенокардия, атеросклероз сонных артерий, суправентрикулярная тахикардия.
Важно отметить, что АК наряду с диуретиками – препараты выбора для использования в комбинациях. В Рекомендациях ЕОК/ЕОАГ 2003 г. [39] АК, как и диуретики, предлагается комбинировать с любым из оставшихся пяти классов антигипертензивных препаратов. Успешно используются фиксированные комбинации АК и иАПФ (верапамил + трандолаприл), АК и b–АБ (фелодипин + метопролол), ожидается выпуск комбинации амлодипина и валсартана.
В 2007 году на фармацевтическом рынке России появляется новый представитель антогонистов кальция – леркарнидипин (Леркамен, «Берлин–Хеми/Менарини фарма ГмБх»).
Леркарнидипин – новый дигидропиридиновый антагонист кальция III поколения, синтезированный Recordati Research Laboratory. Леркарнидипину присуща необычная фармакокинетика, связанная с его высокой липофильностью. Препарат связывается с липидным бислоем клеточной мембраны рядом с рецептором кальциевого канала, откуда медленно высвобождается в течение последующего времени. Такое медленное высвобождение из клеточной мембраны обеспечивает фармакологическую и терапевтическую эффективность на протяжении 24 часов, несмотря на короткий период полувыведения (5 часов) [43].
Леркарнидипин зарегистрирован в качестве антигипертензивного средства в более чем 58 странах. На сегодняшний день выполнен ряд многоцентровых РКИ, где оценивалась антигипертензивная эффективность леркарнидипина в сравнении с плацебо, другими дигидропиридиновыми АК, а также антигипертензивными препаратами иных классов. Одним из первых и наиболее крупным РКИ с участием леркарнидипина было исследование ELYPSE [44], включавшее 9059 амбулаторных пациентов с АГ I–II ст. К 3 месяцу испытания 64% пациентов достигли целевого ДАД <90 мм рт.ст., целевого САД и ДАД – 32% (<130/85 мм рт.ст.). При этом была отмечена низкая частота побочных эффектов, частота отмены препарата составила <1%. В испытаниях у больных ИСАГ леркарнидипин оказался эффективенее чем лацидипин, обеспечивая устойчивое антигипертензивное действие в течение 24 часов с сохранением естественного суточного профиля АД. При этом не было отмечено изменений частоты сердечных сокращений и проводимости. Число побочных эффектов было низким для обоих препаратов, но леркарнидипин отменялся достоверно реже [45]. Cравнение в исследовании ELLE [46] эффективности трех дигидропиридиновых АК: леркарнидипина, лацидипина и нифедипина ГИТС – у пациентов с АГ старше 65 лет показало схожую антигипертензивную эффективность леркарнидипина и нифедипина ГИТС, несколько большую по сравнению с лацидипином. Частота побочных эффектов в группе леркарнидипина была достоверно ниже, чем в группе нифедипина ГИТС и лацидипина. При этом отеки на фоне лечения леркарнидипином встречались в 2,5 раза реже, чем при лечении лацидипином и более чем в 3 раза реже по сравнению с нифедипином ГИТС. В схожем по дизайну исследовании LEAD [47] у 250 пациентов среднего возраста, лечившихся леркарнидипином, фелодипином или нифедипином ГИТС, вновь была отмечена одинаковая антигипертензивная эффективность препаратов при явно меньшем числе неблагоприятных побочных реакций в группе леркарнидипина. Другие подобные исследования подтвердили эти данные [48], в том числе лучшую переносимость леркарнидипина по сравнению с амлодипином, рассматриваемым в последнее время в качестве эталонного АК [49].
Антигипертензивная эффективность леркарнидипина у пациентов с различным уровнем сердечно–сосудистого риска изучалась в открытом многоцентровом исследовании LAURA [50], включавшем 3175 больных АГ I–II ст. Пациенты получали леркарнидипин в дозе 10–20 мг/сут. в течение 6 мес. К концу исследования было отмечено достоверное снижение как систолического (с 159,5±11,7 мм рт.ст. до 136,0±9,7 мм рт.ст., р<0,001), так и диастолического АД (с 95,2±7,4 мм рт.ст. до 79,7±6,8 мм рт.ст., р<0,001). Препарат хорошо переносился, отмена из–за побочных эффектов потребовалась всего в 1,7% случаев, спектр побочных действий соответствовал обычным для дигидропиридиновых АК (головные боли в 3,3%, приливы в 2,5% и астения в 1% случаев). При этом как антигипертензивная эффективность, так и хорошая переносимость отмечались независимо от уровня сердечно–сосудистого риска.
Интересные данные получены в исследовании ZAFRA [51], в котором леркарнидипин назначался 175 пациентам с хронической почечной недостаточностью (ХПН) (клиренс креатинина <70 мл/мин.), у которых не было достигнуто целевое АД 130/85 мм рт.ст. несмотря на прием иАПФ или БРА. Добавление к терапии леркарнидипина обеспечило существенное снижение АД у 89,2% пациентов, а в 58,1% случаев были достигнуты его целевые значения. Хотя не было выявлено изменений плазменной концентрации креатинина, отмечалось достоверное увеличение его клиренса с 41,8±16,0 до 45,8±18,0 мл/мин (р=0,019), а также снижение концентрации холестерина в плазме с 221±46 до 211±35 мг/дл (р=0,001). При этом частота побочных эффектов была крайне низкой (1,48%), и ни у одного пациента не отмечено отеков.
Предложена фиксированная комбинация, содержащая 10 мг леркарнидипина и 10 мг эналаприла. В 12–недельном двойном слепом рандомизированном исследовании у больных АГ I–II ст. данная комбинация оказалась более эффективна, чем монотерапия леркарнидипином. При этом переносимость комбинации не отличалась от таковой для каждого препарата в отдельности: кашель отмечался менее чем в 5,2% случаев, а отеки голеней – менее чем в 1,5% случаев [52].
Таким образом, препарат демонстрирует высокую антигипертензивную эффективность при значительно меньшей чем у других АК частоте возникновения побочных эффектов, благоприятное влияние на функцию почек у больных ХПН, имеет потенциал для использования в комбинациях, не вызывает нежелательной гиперактивации симпатической нервной системы и тахикардии, сохраняет суточный профиль АД, поэтому может быть рекомендован для широкого использования в лечении больных АГ I–II ст.
Возможность применения леркарнидипина в дозе 10–20 мг/сут. у больных стабильной стенокардией напряжения изучалась в небольшом рандомизированном плацебо–контролируемом исследовании, показавшем достоверное увеличение времени до развития депрессии сегмента ST на 1 мм в ходе нагрузочной пробы для обеих дозировок препарата. При этом не было отмечено изменений ЧСС, вариабельности сердечного ритма и концентраций катехоламинов в крови, что позволило сделать вывод о потенциальной безопасности леркарнидипина для больных ИБС, поскольку именно с гиперактивацией симпатоадреналовой системы связывается неблагоприятное влияние короткодействующих АК у подобных пациентов [53]. Эти данные позволяют полагать, что леркарнидипин найдет свое место в лечении больных стабильной стенокардией при невозможности назначения b–АБ.


Литература
1. Abernathy DR, Schwartz JB. Calcium–antagonist Drugs. NEJM 1994;4:1447–1457
2. McDonald TF, Pelzer S, Tautwein W, Pelzer DJ. Regulation and modulation of calcium channels in cardiac,skeletal,and smooth muscle cells. Physiol Rev 1994;74:365–507.
3. Kolars JC, Schmiedlin–Ren P, Schuetz JD, Fang C, Watkins PB. Identification of ifampin–inducible P450IIIA4 (CYP3A4)in human small bowel enterocytes. J Clin Invest 1992;90:1871–8.
4. Koemer HK, Gautier J–C, Beaune P, Henderson C, Wolf CR, Eichelbaum M.Identification of P450 enzymes involved in metabolism of verapamil in humans.Naunyn Schmiedebergs Arch Pharmacol 1993;348:332–7.
5. Pichard L, Gillett G, Fabre I, et al.Identification of the rabbit and human cytochromes P–450IIIA as the major enzymes involved in the N–demethylation of diltiazem. Drug Metab Dispos 1990;18:711–9.
6. Guengerich FP, Brian WR, Iwasaki M, Sari M–A, Baarnhielm C, Berntsson P. Oxidation of dihydropy idine calcium channel blockers and analogues by human liver cytochrome P–450 IIIA4.J Med Chem 1991;34: 1838–44.
7. Trenkwalder P. Antihypertensive treatment with calcium channel blockers: pharmacological pornography or useful intervention? Nephrol Dial Transplant 2004;19:17 –20
8. Furberg K., Psaty B, Meyer J. Nifedipine. Dose–related increase in mortality in patients with coronary heart disease.Circulation 1995;92:1326–1331
9. Staessen JA,Fagard R,Thijs L et al.for the Systolic Hypertension in Europe (Syst–Eur)Trial Investigators. Randomised double–blind comparison of placebo and active treatment for older patients with isolated systolic hypertension. Lancet 1997;350:757 –764
10. Tuomilehto J,Rastenyte D,Birkenha.ger WH et al.Effect of calcium–channel blockade in older patients with diabetes and systolic hypertension.Systolic Hypertension in Europe Trial Investigators.N Engl J Med 1999;340:677 –684
11. Liu L, Wang JG, Gong L, Liu G, Staessen JA, for the Systolic Hypertension in China (Syst-China) Collaborative Group. Comparison of active treatment and placebo in older Chinese patients with isolated systolic hypertension. J Hypertens 1998;16:1823–9.
12. Hansson L, Lindholm LH, Ekbom R et al. Randomised trial of old and new antihypertensive drugs in elderly patients: cardiovascular mortality and morbidity the Swedish Trial in Old Patients with Hypertension–2 study. Lancet 1999;354: 1751 –1756
13. Brown MJ, Palmer CR, Castaigne A et al. Morbidity and mortality in patients randomised to double–blind treatment with a long–acting calcium–channel blocker or diuretic in the International Nifedipine GITS study:Intervention as a Goal in Hypertension Treatment (INSIGHT). Lancet 2000;356: 366 –372
14. Hansson L, Hedner T, Lund–Johansen R et al. Randomised trial of effects of calcium antagonists compared with diuretics and beta–blockers on cardiovascular morbidity and mortality in hypertension:the Nordic Diltiazem (NORDIL)study. Lancet 2000;356;359 –365
15. Black HR, Elliott WJ, Neaton JD, et al. Rationale and design for the Controlled ONset Verapamil INvestigation of Cardiovascular Endpoints (CONVINCE)trial. Control Clin Trials 1998;19: 370–90.
16. The ALLHAT Officers and Co–ordinators for the ALLHAT Collaborative Group.Major outcomes in high–risk hypertensive patients randomized to angiotensin converting enzyme inhibitor or calcium channel blocker vs diuretic. The Antihypertensive and Lipid–Lowering Treatment to Prevent Heart Attack Trial (ALLHAT).J Am Med Assoc 2002;288:1981 –1997
17. Julius S, Kjeldsen SE, Weber M, et al. Outcomes in hypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amlodipine: the VALUE randomised trial. Lancet 2004;363:2022–31
18. Dahl?f B, Sever PS, Poulter NR, et al. Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as rquired, in the Anglo–Scandinavian Cardiac Outcomes Trial – Blood Pressure Lowering Arm (ASCOT–BPLA): a multicentre randomised controlled trial. Lancet 2005;366:895–906
19. Pepine CJ, Handberg EM, Cooper–DeHoff RM, et al. A calcium antagonist vs a non–calcium antagonist hypertension treatment strategy for patients with coronary artery disease. JAMA 2003;290:2805–16
20. Pahor M, Psaty BM, Alderman MH,et al. Health outcomes associated with calcium antagonists compared with other first.line antihypertensive therapies: a meta.analysis of randomised controlled trials. Lancet 2000 Dec 9;356:1949–54.
21. Blood Pressure Lowering Treatment Trialists’ Collaboration. Effects of ACE inhibitors,calcium antagonists,and other blood–pressure–lowering drugs:results of prospectively designed overviews of randomised trials. Lancet 2000;356:1955–1964
22. Opie LH, Schall R. Evidence–Based Evaluation of Calcium Channel Blockers for Hypertension Equality of Mortality and Cardiovascular Risk Relative to Conventional Therapy. JACC 2002;39:315–322
23. Treatment of Uncomplicated Hypertension: Are ACE Inhibitors and Calcium Channel Blockers as Effective as Diuretics and ?–Blockers? Journal of the American Board of Family Practice 2003;16:156–164.
24. Blood Pressure Lowering Treatment Trialists’ Collaboration. Effects of different blood–pressure–lowering regimens on major cardiovascular events: results of prospectively designed overviews of randomised trials. Lancet. 2003;362:1527–1535.
25. Blood Pressure Lowering Treatment Trialists’ Collaboration. Effects of Different Blood Pressure–Lowering Regimens on Major Cardiovascular Events in Individuals With and Without Diabetes Mellitus: Results of Prospectively Designed Overviews of Randomized Trials. Arch Int Med 2005;165:1410–1419.
26. STAESSEN JA, LI Y, THIJS L, WANG JG. Blood Pressure Reduction and Cardiovascular Prevention: An Update Including the 2003–2004 Secondary Prevention Trials. Hypertens Res 2005;28(5):385–407
27. Verdecchia P, Reboldi G, Angeli F, et al. Angiotensin–Converting Enzyme Inhibitors and Calcium Channel Blockers for Coronary Heart Disease and Stroke Prevention. Hypertension 2005;46;386–392;
28. 2003 European Society of Hypertension –European Society of Cardiology guidelines for the management of arterial hypertension. Guidelines Committee. J Hypertens 2003;21(6):1011–53
33. WJ Elliott, PM Meyer. Incident diabetes in clinical trials of antihypertensive drugs: a network meta–analysis. Lancet 2007;369:201 –07
34. Lichtlen PR, Hugenholtz PG, Rafflenbeul W, Hecker H, Jost S, Deckers JW. Retardation of angiographic progression of coronary artery disease by nifedipine. Results of the International Nifedipine Trial on Antiatherosclerotic Therapy (INTACT). Lancet 1990;335:1109–13
35. Zanchetti A, Bond MG, Hennig M, et al. Calcium antagonist lacidipine slows down progression of asymptomatic carotid atherosclerosis. Circulation 2002;106:2422–7
36. Zanchetti A, Agabiti Rosei E, Dal Pal? C, et al. The Verapamil in Hypertension and Atherosclerosis Study (VHAS): results of long–term randomized treatment with either verapamil or chlorthalidone on carotid intima–media thickness. J Hypertens 1998;16:1667–76
37. Pitt B, Byington RP, Furberg CD, et al. Effect of amlodipine on the progression of atherosclerosis and the occurrence of clinical events. Circulation 2000;102:1503–10
38. Dens JA, Desmet WJ, Coussement P, et al. Long term effects of nisoldipine on the progression of coronary atherosclerosis and the occurrence of clinical events: the NICOLE study. Heart 2003;89:887–92
40. Poole–Wilson PA, Lubsen J, Kirwan B–A, et al. Effect of long–acting nifedipine on mortality and cardiovascular morbidity in patients with stable angina requiring treatment (ACTION trial): randomised controlled trial. Lancet 2004;364:849–57
42. Профилактика, диагностика и лечение артериальной гипертензии. Российские рекомендации (второй пересмотр). М., 2004. 20 стр.
43. Herbette LG, Vecchiarelli M, Leonardi A. Lercanidipine: short plasma half–life, long duration of action. A molecular model to rationalize its pharmacokinetic properties. J Cardiovasc Pharmacol 1997; 29 (Suppl 1): S19–S24.
44. Barrios V, Navarro A, Esteras A, et al. Antihypertensive efficacy and tolerability of lercanidipine in daily clinical practice. The ELYPSE study. Blood Press 2002;11:95–100
45. Millar–Craig M, Shaffu B, Greenough A, et al. Lercanidipine vs lacidipine in isolated systolic hypertension. J Hum Hypertens. 2003 Nov;17(11):799–806.
46. Cherubini A, Fabris F, Ferrari E, et al. Comparative effects of lercanidipine, lacidipine, and nifedipine gastrointestinal therapeutic system on blood pressure and heart rate in elderly hypertensive patients: the ELderly and LErcanidipine (ELLE) study. Arch Gerontol Geriatr. 2003 Nov–Dec;37(3):203–12.
47. Romito R, Pansini MI, Perticone F, et al. Comparative effect of lercanidipine, felodipine, and nifedipine GITS on blood pressure and heart rate in patients with mild to moderate arterial hypertension: the Lercanidipine in Adults (LEAD) Study. J Clin Hypertens (Greenwich). 2003 Jul–Aug;5(4):249–53.
48. Borghi C, Prandin MG, Dormi A, Ambrosioni E; Study Group of the Regional Unit of the Italian Society of Hypertension. Improved tolerability of the dihydropyridine calcium–channel antagonist lercanidipine: the lercanidipine challenge trial. Blood Press Suppl. 2003 May;1:14–21.
49. Zanchetti A. Emerging data on calcium–channel blockers: the COHORT study. Clin Cardiol. 2003 Feb;26(2 Suppl 2):II17–20.
50. V. BARRIOS, C. ESCOBAR, A. NAVARRO, et al. Lercanidipine is an effective and well tolerated antihypertensive drug regardless the cardiovascular risk profile: the LAURA Study. Int J Clin Pract, November 2006, 60, 11, 1364–1370
51. Robles NR, Ocon J, Gomez CF, et al. Lercanidipine in patients with chronic renal failure: the ZAFRA study. Ren Fail. 2005;27(1):73–80.
52. Hair PI, Scott LJ, Perry CM. Fixed–dose combination lercanidipine/enalapril. Drugs. 2007;67(1):95–106; discussion 107–8. Related Articles, Links
53. Acanfora D, Trojano L, Gheorghiade M, et al. A randomized, double–blind comparison of 10 and 20 mg lercanidipine in patients with stable effort angina: effects on myocardial ischemia and heart rate variability. Am J Ther. 2002 Sep–Oct;9(5):444–53.












