Артериальная гипертензия (АГ) и осложнения, к которым приводит это заболевание, являются одной из наиболее важных медицинских и социальных проблем не только в России, но и во всем мире. Так, по данным эпидемиологического исследования, проводившегося в нашей стране среди взрослого населения, повышенные цифры артериального давления (АД) выявляются у 39,2% мужчин и 41,1% женщин, то есть у 42,5 млн человек и, к сожалению, остаются стабильными на протяжении последних двух десятилетий [1]. В многочисленных исследованиях было продемонстрировано, что наличие АГ существенно ухудшает прогноз жизни [2], в первую очередь за счет увеличения риска инфаркта миокарда и мозгового инсульта. С другой стороны, на сегодняшний день совершенно очевидно, что адекватное лечение АГ способствует существенному снижению риска осложнений и увеличению продолжительности жизни больных [3].
По–прежнему АГ остается самым распространенным модифицируемым фактором риска сердечно–сосудистых заболеваний (ССЗ), принципиально определяющим величину сердечно–сосудистой смертности [4–6].
Данные современной доказательной медицины однозначно свидетельствуют о том, что главным условием успешного влияния на исходы АГ является достижение целевых уровней АД, которые составляют для всех больных АГ менее 140/90 мм рт. ст., а для отдельных категорий больных – и более низких цифр [4,7]. Вместе с тем на практике, к сожалению, значительная часть больных АГ либо не получает никакого лечения, либо получает неадекватную терапию и, соответственно, не достигает целевых уровней АД. До сих пор даже в Западной Европе и США не достигнут адекватный контроль за уровнем АД. В странах Запада АД должным образом контролируется менее чем у 30%. В России на начало прошлого десятилетия только 59% женщин и 37% мужчин знали о существовании у них АГ, лечились только 46% женщин и 21% мужчин, адекватную медикаментозную терапию АГ получало не более 7,5% мужчин и 17,5% женщин, страдающих этим заболеванием [1,8]. В США этот показатель в 2000 г. составил 34% [4]. Польза от снижения АД доказана не только в крупных многоцентровых исследованиях, о ней свидетельствует и реальное увеличение продолжительности жизни в Западной Европе и США.
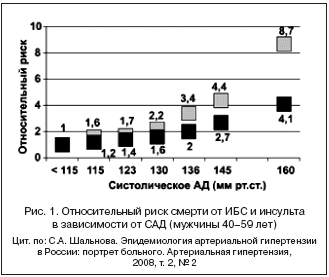
Взаимосвязь между уровнем АД и риском ССЗ непрерывна, постоянна и не зависит от других факторов риска. Иными словами, чем выше АД, тем выше риск развития сердечно–сосудистых осложнений. Так, данные проспективных исследований, проведенных в разные годы в Государственном научно–исследовательском центре профилактической медицины, показали, что если риск смерти у мужчин с уровнем систолического артериального давления (САД) менее 115 мм рт. ст. принять за единицу, то при уровне этого показателя более 160 мм рт. ст. риск смерти от ишемической болезни сердца (ИБС) увеличивается в 4 раза, а от инсульта – почти в 9 раз (рис. 1).
Согласно Рекомендации ВНОК четвертого пересмотра, при лечении больных АГ величина АД должна быть менее 140/90 мм рт.ст., что является ее целевым уровнем. При хорошей переносимости назначенной терапии целесообразно снижение АД до более низких значений. У пациентов с высоким и очень высоким риском сердечно–сосудистых осложнений (ССО) необходимо снизить АД до 140/90 мм рт.ст. и менее в течение 4 нед. В дальнейшем, при условии хорошей переносимости рекомендуется снижение АД до 130–139/80–89 мм рт. ст. [9].
При проведении антигипертензивной терапии следует иметь в виду, что бывает трудно достичь уровня систолического АД менее 140 мм рт. ст. у пациентов, больных сахарным диабетом, с поражением органов–мишеней, у пожилых больных и уже имеющих ССО. Достижение более низкого целевого уровня АД возможно только при хорошей переносимости и может занимать больше времени, чем его снижение до величины менее 140/90 мм рт. ст. При плохой переносимости снижения АД рекомендуется его снижение в несколько этапов. На каждой ступени АД снижается на 10–15% от исходного уровня за 2–4 нед. с последующим перерывом для адаптации пациента к более низким величинам АД.
При достижении целевого уровня АД необходимо учитывать нижнюю границу снижения систолического АД до 110–115 мм рт. ст. и диастолического АД до 70–75 мм рт. ст., а также следить за тем, чтобы в процессе лечения не происходило увеличения пульсового АД у пожилых пациентов, что возникает главным образом за счет снижения диастолического АД [9,10].
Польза от снижения АД до целевых значений подтверждается как результатами проспективных клинических испытаний, так и реальным увеличением продолжительности жизни взрослого населения США и Западной Европы по мере улучшения популяционного контроля АГ. Даже такому богатому государству, как США, согласно 7–му докладу Комитета экспертов по АГ США, потребовалось 20 лет, чтобы увеличить эффективность лечения АГ в популяции с 10 до 34%.
Мета–анализ 61 проспективного и обсервационного исследования (1 млн пациентов, 12,7 млн пациенто–лет) показал, что снижение систолического АД (САД) всего на 2 мм рт. ст. обеспечивает снижение риска смерти от ишемической болезни сердца (ИБС) на 7%, а смерти от мозгового инсульта – на 10%; снижение АД на 20/10 мм рт. ст. обеспечивает уменьшение сердечно–сосудистой смертности в 2 раза [11]. Несмотря на увеличение доли осведомленности (более 70%) и доли охваченных лечением пациентов с АГ (более 50%), эффективность антигипертензивной терапии, определяемая по достижению целевого уровня АД (АД менее 140/90 мм рт. ст.), составляет всего 21,5% [5].
Таким образом, при эффективном лечении АГ можно было бы теоретически сохранить примерно треть жизней мужчин и женщин. Анализ выживаемости в зависимости от уровня АД демонстрирует драматические потери продолжительности жизни у мужчин и женщин с высоким АД. По данным ГНИЦ профилактической медицины, мужчины и женщины, имеющие САД 180 мм рт. ст. и более, живут на 10 лет меньше по сравнению с теми, кто имеет САД менее 120 мм рт. ст. [12,13].
Гипертензия метаболически связана с дислипидемией, нарушенной толерантностью к глюкозе, абдоминальным ожирением, гиперинсулинемией и гипеурикемией. Приблизительно 63% случаев ИБС регистрируются у мужчин–гипертоников с сочетанием двух или более дополнительных факторов риска [14]. Влияние дополнительных факторов риска особенно важно при 1–й стадии гипертензии, когда средний риск повышенного АД еще очень мал, но многие пациенты должны лечиться, чтобы предупредить развитие ССЗ [13].
Современная антигипертензивная терапия должна воздействовать на различные системы, участвующие в регуляции АД в организме человека: симпато–адреналовую систему, ренин–ангиотензин–альдостероновую систему (РААС), обмен кальция, натрий–объем [15]. Влияние на любую из них позволяет добиться уменьшения АД. Это положение нашло свое отражение в Рекомендациях по АГ 2010 г., в которых все классы антигипертензивных препаратов, воздействующих на различные системы, разделили на основные и дополнительные. В Рекомендациях отмечается, что все основные классы антигипертензивных препаратов: ингибиторы АПФ (иАПФ), блокаторы ангиотензиновых рецепторов, диуретики, антагонисты кальция, β–блокаторы одинаково снижают АД. У каждого препарата есть доказанные эффекты и свои противопоказания в определенных клинических ситуациях [9].
Весьма важными для практикующих врачей при решении задач профилактики и лечения АГ, для организаторов здравоохранения при проведении экспертизы качества оказания медицинской помощи являются результаты фармакоэпидемиологического исследования АГ ПИФАГОР III [16]. Российские врачи указали, что из всех классов антигипертензивных препаратов (АГП) они наиболее часто назначают иАПФ (95,8% против 88,7% в 2002 г.). Частота назначения β–блокаторов, диуретиков и α–адреноблокаторов не претерпела существенных изменений. Отмечена тенденция к уменьшению частоты назначения АК (68,2% против 80,1% в 2002 г.) и препаратов с центральным механизмом действия (7,5% против 12,7% в 2002 г.) и, наоборот, значительный рост частоты назначения антагонистов рецепторов АТ II (30,2% против 17,9% в 2002 г.),
В настоящее время возможно использование двух стратегий терапии АГ для достижения целевого АД: монотерапии и комбинированного лечения. Количество назначаемых препаратов зависит от исходного уровня АД и сопутствующих заболеваний. Например, при АГ 1–й степени и отсутствии высокого риска осложнений возможно достижение целевого АД на фоне монотерапии примерно у 50% больных. При АГ 2–й и 3–й степени и наличии факторов высокого риска в большинстве случаев может потребоваться комбинация из двух или трех препаратов. Монотерапия на старте лечения может быть выбрана для пациентов с низким или средним риском. Комбинация двух препаратов в низких дозах должна быть предпочтительна у больных с высоким или очень высоким риском осложнений. Монотерапия базируется на поиске оптимального для больного препарата; переход на комбинированную терапию целесообразен только в случае отсутствия эффекта последней. Низкодозовая комбинированная терапия на старте лечения предусматривает подбор эффективной комбинации препаратов с различными механизмами действия [9].
Результаты множества проспективных клинических испытаний антигипертензивной терапии убедительно показывают, что в подавляющем большинстве случаев невозможно достичь целевых значений АД с помощью монотерапии, так как один препарат не может влиять на многокомпонентную систему регуляции АД. Каждый из этих подходов имеет свои достоинства и недостатки. При этом следует помнить, что при монотерапии удается достигнуть целевого АД в среднем только у 30–40% больных АГ.
В частности, в исследовании HOT на момент включения в исследование 59% пациентов получали монотерапию, тогда как через 3,2 года единственный АПГ принимали лишь 32% пациентов. При этом отмечалась четкая зависимость между величиной целевого ДАД и частотой комбинированной терапии. Для достижения ДАД<90 мм рт.ст. комбинированная терапия потребовалась в 63% случаев, ДАД<85 мм рт. ст. – в 68%, а для ДАД<80 мм рт. ст. – в 74 % (причем среднее ДАД в этой группе составило 81 мм рт. ст., т. е. цель так и не была достигнута) [17].
Частота назначения двух и более АПГ в других исследованиях также оказалась велика: в исследовании SHEP – 45,0%, MAPHY – 48,5%, ALLHAT – 62,0%, STOP–Hypertension – 66,0%, IPPPSH – 70,0%, INVEST – 84,0%, LIFE – 92,0%, COOPE – 93,0%, а в исследовании VA комбинация потребовалась всем пациентам [18].
Группой итальянских ученых изучались преимущества использования различных комбинаций антигипертензивных препаратов в повседневной клинической практике перед монотерапией в профилактике сердечно–сосудистых осложнений. В проведенное вложенное популяционное исследование типа случай–контроль (population–based, nested case–control study) были включены 209 650 пациентов из Ломбардии (Италия) в возрасте от 40 до 79 лет, впервые проходившие лечение по поводу АГ между 2000 и 2001 гг. У пациентов, получавших комбинацию двух препаратов с самого начала терапии, риск ССО был на 11% меньше, чем у больных, лечение которых было начато с монотерапии (95% CI: от 5% до 16%). По сравнению с пациентами, получавшими один АПГ в течение всего курса лечения, риск ССО у пациентов, получавших комбинированное лечение в течение всего периода наблюдения, был на 26% ниже (95% CI: от 15% до 35%). Таким образом, использование комбинации АПГ в повседневной практике ассоциировано с уменьшением риска развития ССО. Авторы исследования рекомендуют расширить перечень показаний для использования комбинации АПГ в клинической практике [19].
По данным отдела системных гипертензий НИИ кардиологии им. А.Л. Мясникова ФГУ РКНПК Росмедтехнологий, монотерапию удалось использовать лишь у 33% пациентов с АГ, у 22% для достижения целевого АД требовалось применение 2 препаратов, а у 25% – 3 лекарственных средств. В 10% случаев потребовалась терапия 4 препаратами, а 2% пациентов нуждались в 5–компонентной антигипертензивной терапии [20]. По данным исследования РОСА, в группе произвольного лечения монотерапию получали 34,1% пациентов; 2–компонентную терапию – 40,2%; 3–компонентную – 21,1% и 4–компонентную – 4,6% [21].
У большинства пациентов с АГ эффективный контроль АД может быть достигнут только при комбинированной терапии, а у 15–20% больных контроль АД не может быть достигнут 2–компонентной комбинацией; предпочтительны к назначению фиксированные комбинации АПГ.
В последнее время было показано, что некоторые комбинации препаратов не только имеют преимущества в осуществлении контроля за уровнем АД, но и улучшают прогноз у лиц с установленной АГ, которая сочетается с другими заболеваниями или нет. Поскольку у врача имеется огромный выбор различных антигипертензивных комбинаций, то основная проблема состоит в выборе наилучшей комбинации с наибольшими доказательствами для оптимального лечения больных АГ.
Комбинация двух препаратов в низких дозах должна быть предпочтительна у больных с высоким или очень высоким риском осложнений [10].
Преимущества комбинированной терапии АГ заключаются в следующем:
• значительное усиление антигипертензивного действия за счет взаимного потенцирования эффекта отдельных препаратов;
• снижение частоты нежелательных явлений за счет включения более низких доз препаратов и/или взаимной нейтрализации побочных действий отдельных компонентов препаратов;
• высокая эффективность, включая повышение частоты ответа на лечение и частоты достижения целевых уровней АД, рациональной низкодозовой терапии в результате воздействия на несколько механизмов поддержания повышенного АД;
• более эффективная защита органов–мишеней и, следовательно, более выраженное снижение риска осложнений;
• простота назначения и процесса титрования дозы, повышающая приверженность пациентов к лечению;
• уменьшение стоимости лечения за счет того, что цена комбинированного препарата меньше, чем стоимость компонентов, выписываемых врачом раздельно;
• исключение возможности использования нерациональных комбинаций.
Причинами недостижения целевого АД можно назвать:
• неправильный выбор препарата или дозы;
• отсутствие синергизма действия при использовании комбинации препаратов;
• проблемы, связанные с приверженностью к лечению.
В новых Российских рекомендациях по АГ 2010 г. подчеркивается, что в полной мере преимущества комбинированной терапии присущи только рациональным комбинациям АПГ: лидер – это комбинация ингибитора АПФ с диуретиком, при которой усиливаются преимущества и нивелируются недостатки обоих компонентов. Данная комбинация является наиболее популярной в терапии АГ благодаря высокой гипотензивной эффективности, защите органов–мишеней, хорошей безопасности и переносимости.
Далее следуют блокаторы ангиотензиновых рецепторов с диуретиками, ингибиторы АПФ с антагонистами кальция, блокаторы ангиотензиновых рецепторов с антагонистами кальция [9].
К возможным комбинациям АПГ относятся сочетание дигидропиридинового и недигидропиридинового АК, ингибиторов АПФ + β–блокаторов, БРА + β–блокаторов, ингибиторов АПФ + БРА, прямого ингибитора ренина или α–адреноблокатора со всеми основными классами АПГ. Применение этих комбинаций в виде двухкомпонентной антигипертензивной терапии в настоящее время не является абсолютно рекомендованным, но и не запрещено.
К комбинациям нерациональным, при использовании которых не происходит потенцирования антигипертензивного эффекта препаратов и/или усиливаются побочные эффекты при их совместном применении, относятся: сочетания разных лекарственных средств, относящихся к одному классу АПГ, β–блокаторы + недигидропиридиновый антагонист кальция, ингибитор АПФ + калийсберегающий диуретик, β–блокатор + препарат центрального действия
Отрадно, что в настоящее время российские врачи в подавляющем большинстве случаев (около 70%) предпочитают использовать комбинированную антигипертензивную терапию в лечении пациентов с АГ, в том числе терапию в виде свободных (69%), фиксированных (43%) и низкодозовых комбинаций (29%), и лишь 28% врачей остаются приверженными тактике монотерапии.
В связи с тем, что комбинированная терапия стала основным направлением при лечении больных АГ, все более широкое распространение получили фиксированные комбинации АПГ, то есть содержащие в одной таблетке два лекарственных средства. Такие лекарственные формы, обладая всеми преимуществами комбинированной терапии вообще (более выраженный антигипертензивный эффект, увеличение количества положительных ответов на лечение, меньшая частота побочных реакций, выраженное органопротективное действие), имеют ряд дополнительных преимуществ перед произвольными комбинациями.
Чаще всего при проведении комбинированной антигипертензивной терапии врачи назначают свободные комбинации АГП, реже – фиксированные комбинации, 29% предпочитают применение низкодозовых комбинаций. Эти данные согласуются с современными тенденциями повышения роли комбинированной терапии в лечении АГ, основанной на результатах последних крупных клинических исследований (ASCOT–BLA, ACCOMPLISH). Из современных фиксированных комбинированных препаратов 82% опрошенных врачей предпочитают использование сочетаний иАПФ с диуретиком, антагонистов рецепторов АТ II с диуретиком (49%), β–блокаторов с диуретиком (39%) и АК с другим препаратом (35%) [16]. 50% врачей назначают не содержащие диуретики комбинации (антагонисты кальция с ингибиторами АПФ или β–блокаторами).
В опубликованных рекомендациях Американского общества АГ (ASH) по комбинированной терапии АГ также приоритет отдается комбинации препаратов, блокирующих активность ренин–ангиотензиновой системы (блокаторы ангиотензиновых рецепторов или ингибиторы АПФ) с диуретиками или с антагонистами кальция [22].
На российском фармацевтическом рынке представлен широкий спектр комбинированных низкодозовых фиксированных АГП, в том числе содержащих иАПФ и диуретик.
К сведению, в США в топ–тройку всех назначаемых препаратов, наряду с симвастатином и L–тироксином, входит лизиноприл – 81,3 млн выписанных рецептов по итогам 2009 г. Во многом это происходит благодаря наличию дешевых генерических препаратов лизиноприла и специальных программ по закупке генериков по низким ценам. Лизиноприл – один из представителей большой группы ингибиторов АПФ.
По мнению российских врачей, среди класса иАПФ самыми популярными, а следовательно, и часто назначаемыми оказались 5 препаратов: эналаприл (21%), лизиноприл (19%), периндоприл (17%), фозиноприл (15%) и рамиприл (10%); их совокупная доля превысила 82%. Доля остальных представителей класса иАПФ составила менее 5%. В сравнении с результатами ПИФАГОР I отмечено увеличение доли лизиноприла (на 35%). Это объясняется тем, что лизиноприл, не являясь пролекарством, характеризуется гидрофильностью, большим периодом полувыведения, полной почечной экскрецией в активном виде [16]. Такие свойства обеспечивают лизиноприлу продолжительность действия 24 ч при однократном приеме в сутки, быстроту достижения гипотензивного и нефропротективного эффекта (уменьшение протеинурии) [23].
Третье место в структуре АГП, по результатам опроса врачей, занимает класс диуретиков, представленный на 2/3 индапамидом и на 1/3 гидрохлоротиазидом; доля фуросемида составила 6% [16].
Комбинация двух классов АГП иАПФ и диуретика является одной из наиболее логичных и привлекательных. Сегодня доказано, что иАПФ и диуретик действуют синергично и эффект от такой комбинации выше, чем у каждого из препаратов в отдельности. Лизиноприл – ингибитор АПФ. Механизм действия связан с ингибированием активности АПФ, что приводит к подавлению образования ангиотензина II из ангиотензина I и к прямому уменьшению выделения альдостерона. Уменьшает деградацию брадикинина и увеличивает синтез простагландинов. Снижает ОПСС, АД, преднагрузку, давление в легочных капиллярах, вызывает увеличение минутного объема крови и повышение толерантности к нагрузкам у больных хронической сердечной недостаточностью. Лизиноприл оказывает вазодилатирующее действие, при этом расширяет артерии в большей степени, чем вены. Некоторые эффекты объясняются воздействием на тканевые ренин–ангиотензиновые системы. Улучшает кровоснабжение ишемизированного миокарда. При длительном применении уменьшается гипертрофия миокарда и стенок артерий резистивного типа.
Лизиноприл был детально изучен в нескольких крупномасштабных клинических исследованиях. Лизиноприл продемонстрировал профилактическую и терапевтическую эффективность при сердечной недостаточности, в том числе после острого ИМ, и при сопутствующем сахарном диабете (исследования GISSI 3, ATLAS, CALM, IMPRESS). В самом крупном клиническом исследовании по лечению АГ различными классами препаратов ALLHAT среди принимавших лизиноприл достоверно снизилась заболеваемость СД 2–го типа [24].
Cуществует достаточно много исследований, в которых сравнивали антигипертензивную эффективность различных иАПФ. При этом в части из них проводилось сопоставление не совсем адекватных доз. Наиболее полное сравнение антигипертензивной эффективности различных иАПФ представлено результатами мета–анализа Cochrane Collaboration 2009 [25]. В этот анализ вошли результаты 92 исследований, в которых изучали эффективность монотерапии различными иАПФ. В целом в этих исследованиях принимали участие 12 954 пациента, средний возраст – 54,4 года, средний уровень АД – 157,1/101,2 мм рт. ст. Длительность лечения различными иАПФ в среднем составила 6,2 недели. Эффективность иАПФ сравнивалась с таковой плацебо, степень снижения АД при приеме препаратов рассчитывалась так: снижение АД на фоне иАПФ минус снижение АД на фоне плацебо. В среднем на фоне плацебо САД снизилось на 3,2 мм рт. ст., ДАД – на 3,7 мм рт. ст.
Для лизиноприла 10 мг оказались наименьшей стартовой дозой, которая позволяет избежать эффекта первой дозы, но при этом обеспечивает эффективное снижение АД, близкое к максимальному. Кроме того, необходимо учитывать, что для некоторых иАПФ степень снижения АД может возрастать при увеличении дозы (дозозависимый эффект), например, для лизиноприла – с 10 до 80 мг.
Лизиноприл в равной степени снижает САД и ДАД. При изучении и сравнении различных иАПФ в различных сопоставимых дозах – 1/8, 1/4, 1/2 от максимальной и в максимальной, оказалось, что в дозе 1/8 от максимальной наиболее эффективным был лизиноприл 10 мг, в дозе 1/4 от максимальной первенство лизиноприла сохранялось. Если оценить максимальное снижение АД, которое возможно достигнуть при использовании дозы ≥1/2 от максимальной, то наибольшую глубину гипотензии продемонстрировали лизиноприл и имидаприл. В максимальных дозах, рекомендуемых производителем, наиболее эффективными вновь были лизиноприл 80 мг, а также имидаприл 20 мг, периндоприл 8 мг.
В целом можно говорить, что антигипертензивная эффективность иАПФ одинакова и на первый план должна выходить не степень снижения АД, а такие показатели, как соотношение «пик/корыто», вариабельность АД, длительность антигипертензивного эффекта. Поэтому препараты с длительностью действия 24 ч и соотношением «пик/корыто» более 50%, безусловно, имеют преимущества, так как позволяют увеличить приверженность пациента к лечению и снизить вариабельность АД. Все перечисленное в полной мере относится к лизиноприлу.
С учетом сопутствующей патологии возможны некоторые предпочтения в назначении лизиноприла. Гидрофильный иАПФ лизиноприл возможно назначать при длительной терапии нестероидными противовоспалительными препаратами [26]. Существуют также доказательства, что у курильщиков лизиноприл реже вызывает кашель, чем другие иАПФ [27]. Согласно руководствам, лизиноприл также эффективен при наличии ретинопатии, мигрени, изолированной систолической гипертензии [24, 28].
Эксперты считают, что назначение фиксированной комбинации двух АПГ может быть первым этапом лечения пациентов с высоким сердечно–сосудистым риском или следовать сразу за монотерапией, а клинические исследования показали, что нелипофильный лизиноприл достоверно снижает смертность и риск госпитализаций при СН [29].
В рекомендациях Европейского общества кардиологов 2008–2010 гг. обязательной составляющей ведения пациентов с СН являются иАПФ, которые имеют наибольшую доказательную базу эффективности при СН: в их числе лизиноприл, эналаприл, каптоприл, рамиприл, трандолаприл [30]. Полученные в ходе исследований ATLAS, GISSI–3, EUCLID результаты дали основание утверждать, что длительная терапия лизиноприлом также эффективно влияет на выживаемость и заболеваемость пациентов на всех этапах развития сердечной недостаточности. При этом в исследовании ATLAS было показано, что при СН назначение лизиноприла в низких дозах сопровождалось достоверно большей вероятностью развития комбинированной конечной точки (смерть от всех причин + госпитализации от всех причин), чем при назначении высоких доз [31].
У пациентов с сахарным диабетом 1–го типа лизиноприл приводил к уменьшению прогрессирования ретинопатии низкой степени или предупреждал ее возникновение вне зависимости от наличия АГ [32,33]. Поэтому в показаниях к применению лизиноприла указан сахарный диабет 1–го типа. Уменьшение ретинопатии было также отмечено в исследовании UKPDS при более интенсивном контроле АД [34].
Нефропротективный эффект иАПФ, связанный с устранением неиммунных механизмов прогрессирования почечной патологии, остается максимальным в сравнении с другими лекарственными средствами на всех стадиях поражения почек. В исследовании BRILLIANT лизиноприл по сравнению с нифедипином продленного действия приводил к более выраженному уменьшению выделения белка с мочой. В исследовании CALM при почти одинаковом снижении АД лизиноприл в большей степени обеспечивал снижение уровня альбуминурии по сравнению с кандесартаном, а при их комбинации влияние на АД и регресс протеинурии усиливались.
Следует также отметить, что у пациентов с АГ (особенно высокого риска) назначение первых поколений иАПФ приводило к снижению частоты развития коронарных событий, прежде всего инфаркта миокарда. В исследование ALLHAT включались пациенты с АГ и одним из факторов риска развития ИБС. Оказалось, что лизиноприл был таким же эффективным в предупреждении первичной конечной точки (инфаркт миокарда или смертность от ИБС), как и амлодипин, и хлорталидон [24].
В исследование GISSI–3 было включено 19 394 пациента ОИМ, которые были рандомизированы получать лизиноприл или плацебо [35,36]. Смертность к 6–й нед. приема была ниже в группе лизиноприла. Разница сохранялась и на этапе 6 месяцев [37].
Лишь кратко напомним основные свойства «старого и доброго» гидрохлоротиазида. Это тиазидный диуретик, диуретический эффект которого связан с нарушением реабсорбции ионов натрия, хлора, калия, магния, воды в дистальном отделе нефрона; задерживает выведение ионов кальция, мочевой кислоты. Оказывает антигипертензивное действие за счет расширения артериол. Практически не оказывает влияния на нормальное АД. Диуретический эффект развивается через 1–2 ч, достигает максимума через 4 ч и продолжается 6–12 ч. Антигипертензивное действие проявляется через 3–4 дня, но для достижения оптимального терапевтического эффекта может потребоваться 3–4 нед.
Совместное использование иАПФ и диуретика позволяет взаимно нивелировать побочные эффекты обоих препаратов. Диуретики приводят к повышению экскреции калия, тогда как иАПФ способствуют задержке калия, соответственно, комбинация обеспечивает предотвращение как гипокалиемии, индуцированной мочегонным препаратом, так и гиперкалиемии, вызванной иАПФ. Предотвращение гипокалиемии может иметь существенное значение не только в плане повышения переносимости терапии. В исследовании SHEP у больных с гипокалиемией не отмечено снижения частоты неблагоприятных сердечно–сосудистых событий по сравнению с пациентами, имевшими нормокалиемию, несмотря на одинаковое снижение АД [38]. Известно, что тиазидные диуретики помимо гипокалиемии вызывают гиперурикемию, иАПФ же способствуют ее уменьшению, т. к. усиливают кровоток в кортикальном слое почек, что приводит к повышению экскреции мочевой кислоты [21].
В комбинации лизиноприл и гидрохлоротиазид оказывают аддитивное антигипертензивное действие.
Заключение
Основная цель лечения артериальной гипертензии – предупреждение развития сердечно–сосудистых осложнений и снижение сердечно–сосудистой смертности, достижение оптимального уровня АД, коррекция метаболических показателей и прочих факторов риска. Одним из важнейших условий обеспечения адекватного контроля АД и повышения приверженности пациентов к лечению является оптимальный выбор антигипертензивного средства. Комбинированная терапия наиболее эффективно предотвращает поражение органов–мишеней и приводит к уменьшению числа сердечно–сосудистых осложнений у пациентов с АГ. Преимущества комбинированной терапии, заключающиеся в потенцировании антигипертензивного эффекта и уменьшении числа побочных эффектов, присущи лишь так называемым рациональным комбинациям гипотензивных препаратов.
Литература
1. Шальнова С.А., Деев А.Д., Вихирева О.В. и др. Распространенность артериальной гипертонии в России. Информированность, лечение, контроль. Профилактика заболеваний и укрепление здоровья. – 2001. – № 2. – С. 3–7.
2. Stokes J., Kannel W., Wolf P. et al. Blood pressure as a risk factor fjr cardiovascular disease. The Framingham Study – 30 years of follow–up. Hypertension 1989; 1 3 (Suppl. I): 13–18.
3. Waeber B. Treatment strategy to control blood pressure optimally in hypertensive patients. Blood Pressure 2001; 10: 62–73.
4. Chobanian A.V., Bakris G.L., Black H.R. et al. Seventh report of the joint national committee on prevention, detection, evaluation, and treatment of high blood pressure. Hypertension 2003;42:1206–52.
5. Шальнова С.А., Баланова Ю.А., Константинов В.В. и др. Артериальная гипертония: распространенность, осведомленность, прием антигипертензивных препаратов и эффективность лечения среди населения Российской Федерации // Российский кардиологический журнал. – 2006. № 4. С. 45–50.
6. Ezzati M., Lopez A.D., Rodgers A. et al. Selected major risk factors and global and regional burden of disease. // Lancet 2002;360(9343):1347–60.
7. Guidelines Committee. 2003 European Society of Hypertension–European Society of Cardiology guidelines for the management of arterial hypertension. // J. Hypertension 2003; 21: 1011–1053.
8. Шальнова С.А., Марцевич С.Ю., Деев А.Д., Кутишенко Н.П., Оганов Р.Г.
Рабочая группа программы ПРОЛОГ. Артериальная гипертония в России: исследование ПРОЛОГ как способ доказательства возможностей современной терапии. // Рациональная фармакотерапия в кардиологии. – 2005. – № 1.
9. Российское медицинское общество по артериальной гипертонии (РМОАГ), Всероссийское научное общество кардиологов (ВНОК). Диагностика и лечение артериальной гипертензии. Российские рекомендации (четвертый пересмотр), 2010.
10. Карпов Ю.А. Новые рекомендации по артериальной гипертензии РМОАГ/ВНОК 2010 г.: вопросы комбинированной терапии. // РМЖ. Кардиология. – 2010. – Т. 18, № 22. – С. 1290–1298.
11. Lewington S., Clarke R., Qizilbash N. et al. Prospective Studies Collaboration. Age–specific relevance of usual blood pressure to vascular mortality: a meta–analysis of individual data for one million adults in 61 prospective studies. // Lancet 2002;360:1903–13.
12. Оганов Р.Г., Шальнова С.А., Деев А.Д. и др. Артериальная гипертония, смертность от сердечно–сосудистых заболеваний и вклад в продолжительность жизни населения // Профилактика заболеваний и укрепление здоровья. – 2001. – № 3. – С. 3–7.
13. Шальнова С.А. Эпидемиология артериальной гипертензии в России: портрет больного. // Артериальная гипертензия. – 2008. – Т. 2, № 2.
14. Kannel W.B. Risk stratification in hypеrtension: new insights from the Framingham Study // Am. J. Hypertens. – 2000. – 13(1). – 3–10.
15. 2007 Guidelines for management of arterial hypertension // J. Hypertens. – 2007. – 25. – 1105–1187.
16. Леонова М.В., Белоусов Д.Ю., Штейнберг Л.Л., Галицкий А.А., Белоусов Ю.Б. Результаты фармакоэпидемиологического исследования артериальной гипертонии ПИФАГОР III. // Consilium Medicum. Системные гипертензии. – 2010. – № 1.
17. Hansson L., Zanchetti A., Carruthers S.G. et al. Effects of intensive blood–pressure lowering and low–dose aspirin in patients with hypertension: principal results of the Hypertension Optimal Treatment (HOT) randomised trial. // Lancet 1998;351:1755–62.
18. Олейникова Г.Л. Комбинированная терапия артериальной гипертонии. // РМЖ. Кардиология. – 2008. – Т. 16, № 21. – С. 1470–1474.
19. Corrao G., Nicotra F., Parodi A., Zambon A., Heiman F., Merlino L., Fortino I., Cesana G., Mancia G. Профилактика сердечно–сосудистых осложнений в повседневной клинической практике с использованием комбинации антигипертензивных препаратов на начальных и последующих этапах лечения. // Hypertension. 2011 Oct;58(4):566–72. Epub 2011 Aug 8. http://www.ncbi.nlm.nih.gov/pubmed/21825231
20. Banegas J.R., Segura J., Ruilope L.M. et al. on behalf of the CLUE Study Group Investigators. Blood pressure control and physician management of hypertension in hospital hypertension units in Spain. // Hypertension 2004;43(6):1338–44.
21. Подзолков В.И., Осадчий К.К. Новый подход к терапии артериальной гипертензии: нефиксированные комбинации в одном блистере. // РМЖ. К конгрессу «Человек и лекарство». – 2008. – № 5 (159).
22. Gradman A.H., Basile J.N., Carter B.L. et al. Combination therapy in hypertension. // J Am Soc Hypertens 2010; 4: 42–50.
23. Еремина Ю.Н., Леонова М.В., Белоусов Ю.Б. и др. Влияние современных антигипертензивных препаратов на микропротеинурию. // Фарматека. – 2003. – № 12. С. 101–8.
24. The ALLHAT Officers and Coordinators for the ALLHAT Collaborative Research Group. Major outcomes in high–risk hypertensive patients randomized to angiotensin–converting enzyme inhibitor or calcium channel blocker vs. diuretic: the Antihypertensive and Lipid Lowering treatment to prevent Heart Attack Trial (ALLHAT). // JAMA, 2002; 288: 2981–97.
25. Heran B.S., Wong M.M., Heran I.K., Wright J.M. Blood pressure lowering efficacy of angiotensin converting enzyme (ACE) inhibitors for primary hypertension // The Cochrane Collaboration. Cochrane database of Systematic Reviews. – 2008. – Issue 4. Art.No.:CD003823.DOI:10.1002/ 14651858.CD003823.pub2.
26. Бобров В.А., Давыдова И.В., Медведенко О.И. Актуальные вопросы лекарственных взаимодействий в клинической практике. Как выбрать оптимальный ингибитор АПФ для больного, принимающего НПВС? // Укр. мед. часопис. – 2010. – № 1. – С. 43–48.
27. Сіренко Ю. Клінічні аспекти застосування лізиноприлу // Ліки України. – 2000. – № 9. – С. 51–54.
28. Balazsi I., Takacs J. The effect of lisinopril in hypertensive patients with diabetic nephropathy // Diabetologia Hungarica. – 1999. – Vol. 7. – P. 101–106.
29. The Task Force on ACE–inhibitors of the European Society of Cardiology. Expert consensus document on angiotensin converting enzyme inhibitors in cardiovascular disease // European Heart Journal. – 2004. – Vol. 25. – P. 1454–1470.
30. Task Force Members. The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2008 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association of the ESC (HFA) and endorsed by the European Society of Intensive Care Medicine (ESICM) // European Heart Journal. – 2008. – Vol. 29. – P. 2388–2442.
31. Packer M., Poole–Wilson P.A., Armstrong P.W. et al., on behalf of the ATLAS study group. Comparative effects of low and high doses of the angiotensin–converting enzyme inhibitor, lisinopril, on morbidity and mortality in chronic heart failure // Circulation. – 1999. – Vol. 100. – P. 2312–2318.
32. Chaturvedi N., Sjolie A.K., Stephenson J.M. et al. Effect of lisinopril on progression of retinopathy in normotensive people with type 1 diabetes. The EUCLID Study Group. EURODIAB Controlled Trial of Lisinopril in Insulin–Dependent Diabetes Mellitus // Lancet. – 1998. – Vol. 351. – P. 28–31.
33. The EUCLID Study Group Randomised placebo–controlled trial of lisinopril in normotensive patients with insulin–dependent diabetes and normoalbuminuria or microalbuminuria // Lancet. – 1997. – Vol. 349. – P. 1787–1792.
34. UK Prospective Diabetes Study Group. Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38 // Br. Med. J. – 1998. – Vol. 317. – P. 703–713.
35. Gottlieb S., Leor J., Shotan A., Harpaz D., Boyko V., Rott D. et al. Comparison of effectiveness of angiotensin–converting enzyme inhibitors after acute myocardial infarction in diabetic versus nondiabetic patients // Am. J. Cardiol. – 2003. – Vol. 92. – P. 1020–1025.
36. Pedrazzini G., Santoro E., Latini R. et al. GISSI–3 Investigators Causes of death in patients with acute myocardial infarction treated with angiotensin–converting enzyme inhibitors: findings from the Gruppo Italiano per lo Studio della Sopravvivenza nell’Infarto (GISSI)–3 trial // Am. Heart J. – 2008. – Vol. 155(2). – P. 388–394.
37. Радченко А.Д. «Старые» и «новые» ингибиторы АПФ: портит ли старый конь борозду? // Артериальная гипертензия. – 2011. – № 4(18).
38. Леонова М.В., Белоусов Д.Ю. Аналитическая группа исследования ПИФАГОР. Первое российское фармакоэпидемиологическое исследование артериальной гипертонии // Качественная клиническая практика. – 2002. – № 3. – C. 47–53.












