Материал и методы исследования
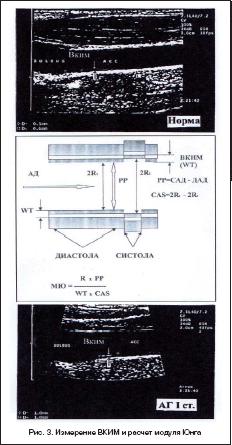
В исследование включены 100 пациентов: 80 больных АГ 1–2 степени, 1–3 риском (ВОЗ/МОГ 1999 г.), в возрасте от 45 до 65 лет (средний возраст – 51,41±6,3 лет), 47 мужчин и 33 женщины. Длительность заболевания АГ в среднем составила 6,4±2,1 лет. Практически у всех пациентов была сопутствующая ишемическая болезнь сердца. Контрольную группу составили 20 пациентов – нормотоники: средний возраст – 53,1±5,8 лет статистически не отличался от исследуемой группы (р>0,05); 11 мужчин, 9 женщин. В зависимости от уровня концентрации магния в эритроцитах больные АГ были распределены на две подгруппы: А – 32 пациента – АГ с дефицитом магния (40%); Б – 48 больных АГ без дефицита магния (рис. 2). Селективный ? 1 –блокатор – Бисогамма (бисопролол, Вёрваг Фарма) применялся в качестве монотерапии по нарастающей схеме в зависимости от клинического эффекта от 2,5 мг до 10,0 мг однократно в сутки в течение 6 месяцев у 48 пациентов АГ без клеточного дефицита магния. У 32 пациентов АГ с дефицитом магния к терапии селективным ? 1 –блокатором Бисогамма был добавлен Магнерот 1–2 г в сутки. У всех наблюдаемых пациентов с АГ до и после 4–недельной и 6–месячной терапии изучали агрегационную активность тромбоцитов (АТр), электрофоретическую подвижность эритроцитов (ЭФПЭ), исследовали клинические и биохимические показатели крови: Ht, липидный профиль, фибриноген, глюкозу. Нормативные показатели реологии крови были определены у нормотоников (20 пациентов), проходящих очередное рутинное диспансерное обследование. Тромбоцитарный гемостаз изучали путем записи агрегации тромбоцитов на лазерном агрегометре – Aggregation Analyser – Biola Ltd (Юнимед, Москва) по методу Born в модификации O'Brien. В качестве индуктора агрегации использовали АДФ (фирма «Serva», Франция) в конечной концентрации 0,1 мкм. Электрофоретическую подвижность эритроцитов (ЭФПЭ) определяли на цитофотометре «Opton» в режиме: I =5 мА, V =100 B , t =25 град. Передвижение эритроцитов регистрировали в фазово–контрастном микроскопе при увеличении в 800 раз. ЭФПЭ вычисляли по формуле: B = I / t . E, где I – путь эритроцитов в сетке окуляра – микроскопа в одну сторону (см), t – время прохождения (с), E – напряженность электрического поля (B/см). В каждом случае расчитывалась скорость миграции 20–30 эритроцитов. Нормальная величина ЭФПЭ – 1,128±0,018 мкм/cм/с –1 /B –1 . Уровень общего холестерина (ОХС), холестерина липопротеидов высокой плотности (ХС ЛПВП) и триглицеридов определяли энзиматическим методом на автоанализаторе FM–901 (Labsystems – Финляндия) с использованием реактивов фирмы Randox (Франция). Концентрацию холестерина липопротеидов очень низкой плотности (ХС ЛПОНП) и холестерина липопротеидов низкой плотности (ХС ЛПНП) последовательно рассчитывали по формуле Friedewald W.T. (1972):
ХС ЛПОНП = ТГ/2,2 ХС ЛПНП = ОХС – (ХС ЛПОНП + ХС ЛПВП)
Расчет индекса атерогенности (ИА) проводили по формуле А.И. Климова (1977):
ИА = (OXC – ХС ЛПВП) /ХС ЛПВП
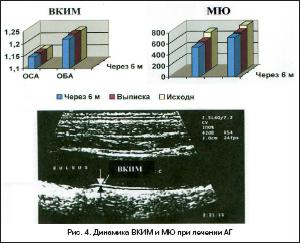
Концентрацию фибриногена в плазме крови определяли фотометрически с турбодиметрическим методом регистрации «Fibrintimer» (Германия), с помощью коммерческих наборов « Multifibrin Test – Kit » ( Behring AG ). Количественное определение магния в сыворотке выполнялось фотометрическим методом по цветной реакции с ксилидином синим. Исследование проводилось на анализаторе Master Screen с использованием реактивов «Human». Аналогичным образом определяли количество магния в эритроцитах после их лизиса в хлорной кислоте по Bonney. Референтные значения концентрации магния в эритроцитах – 1,65–2,65 ммоль/л, в сыворотке – 0,74–1,0 ммоль/л. Величину комплекса интим–медиа (ВКИМ) дистальных участков общей сонной и бедренной артерий оценивали доплер УЗ–исследованием в В–режиме по методике Pignolli (1986) на аппарате ELEGRA фирмы Simens линейным датчиком 5–10 мГц (рис. 3). Расчет модуля Юнга (МЮ) – отношение нагрузки (сила на единицу площади сосуда) к растяжению (относительное изменение линейного расстояния, определяемого вдоль вектора сила–воздействие) проводили по формуле:
где R – радиус артерии; ВКИМ – величина комплекса интим–медиа; ПД – пульсовое давление; ИДА – изменение диаметра артерии за один сердечный цикл. Все результаты исследования обработаны алгоритмами биометрии математической статистики №№ 1, 2, 14, 20 (Плохинский М.А., 1962).
Результаты исследования
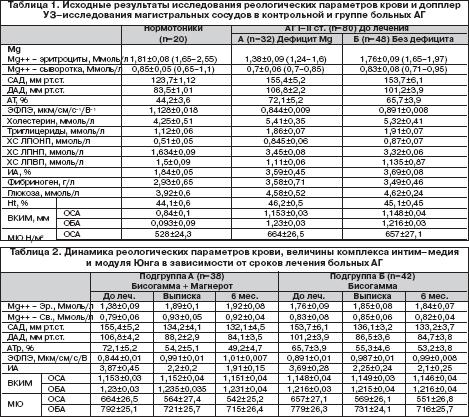
Суммарные результаты исходного исследования в контрольной группе и больных АГ в зависимости от концентрации магния в эритроцитах представлены в таблице 1. Обращает на себя внимание исходно повышенное агрегационное состояние тромбоцитов в группе пациентов с АГ по сравнению с нормотониками: у нормотоников АТ – 44,2±3,6%, суммарно у больных с АГ – 68,5±6,7%, т.е. на 55% больше (разница достоверна по третьему порогу вероятности безошибочного прогноза – p<0,001). Аналогично отмечено снижение ЭФПЭ в группе больных с АГ по сравнению с нормотониками на 42,3%: в группе нормотоников – 1,128±0,018 мкм/см/с –1 /В –1 , суммарно в исследуемой группе пациентов с АГ – 0,872±0,012 мкм/см/с –1 /В –1 (разница статистически достоверна по второму порогу вероятности безошибочного прогноза – р<0,01). В подгруппах А и Б больных АГ статистически достоверной разницы в функциональном состоянии форменных элементов крови не получено, однако в подгруппе А (дефицит магния ) имеет место тенденция к более выраженным изменениям ЭФПЭ и АТр. Суммарный показатель липидного профиля ИА также был повышен в группе больных с АГ по сравнению с контрольной группой почти вдвое (на 95%): 1,84±0,05, 3,59±0,09 соответственно (р<0,001). Показатели уровней фибриногена и глюкозы в сыворотку крови контрольной и исследуемой группах статистически не отличались друг от друга, хотя отмечена тенденция в сторону увеличения у больных с АГ. В таблице 2 представлена динамика реологических параметров крови и состояние резистивных сосудов в различные сроки лечения больных АГ с дефицитом магния и без дефицита магния. Как видно из таблицы, в подгруппе А, на фоне в/в Кормагнезина – 20 мл на 100 мл 5% глюкозы с 4 ЕД инсулина два раза в день в сутки в течение недели стационарного лечения, с последующим переходом на пероральный прием Магнерота (1–2 г в с утки), отмечена положительная динамика концентрации магния в эритроцитах и сыворотке крови: в эритроцитах концентрация магния последовательно увеличилась на 36,9% и к концу программы исследования – на 39,1% (разница статистически достоверна – р<0,001); в сыворотке соответственно – на 17,7% и на 16,5% (р<0,05). В подгруппе Б концентрация магния в эритроцитах и сыворотке крови оставалась на исходном уровне. В подгруппе А отмечено снижение САД, по сравнению с исходным уровнем последовательно на 13,6% и на 15% (р<0,01), ДАД уменьшилось на 17,4% и на 21,3% (р<0,01). В подгруппе Б больных АГ имела место менее выраженная динамика со стороны САД и ДАД: САД последовательно уменьшилось на 11,5% и на 13,3%, ДАД – на 14,5% и на 16,3% (р<0,05). Корреляционный анализ между динамикой концентрации магния в эритроцитах, систолическим и диастолическим давлением: rMgЭр – САД = –0,58, rMg Эр – ДАД = –0,64 (р<0,01) свидетельствует, что чем выше концентрация магния в эритроцитах, тем более эффективно снижается АД (особенно диастолическое) на фоне лечения ? –адреноблокаторами. Агрегационная активность тромбоцитов в подгруппе А снизилась на 24,8% и на 31,85; в подгруппе Б – соответственно на 15,8% и на 19% (р<0,05). Выявлена тесная прямая корреляционная связь между динамикой уровней АТр и АД: rАТр – САД = 0,67 и rАТр – ДАД = 0,72 (р<0,01). ЭФПЭ в подгруппа А после проведенного лечения последовательно увеличилась на 17,4% и на 19,7% (р,0,05); в подгруппе Б – на 10,8% и на 11,1% (р<0,05). Увеличение скорости ЭФПЭ находится в тесной обратной корреляционной связи с динамикой уровней АД: rЭФПЭ–САД = –0,56, rЭФПЭ–ДАД = –0,78 (р<0,01). Качество функционального состояния эритроцитов находится в тесной корреляционной связи с концентрацией в нем магния и ИА плазмы (суммарного показателя липидного спектра крови): rЭФПЭ – MgЭр = 0,74, rЭФПЭ – ИА = –0,74 (р<0,01). Зафиксировано снижение ИА последовательно на 43,2% и на 50,6%, за счет снижения концентрации триглицеридов на 12,4% и на15,1%, ХЛПНП – на 34,5%, 40,9% и увеличения ХЛПВП на 29,7%, на 30,6%. Существенной, статистически достоверной в сторону уменьшения концентрации фибриногена и глюкозы в сыворотке крови не получено. Отмечено статистически недостоверное снижение показателей Ht от 46,2±0,5% до 44,4±0,7% (р>0,05). ВКИМ в ОСА и ОБА на протяжении всего периода наблюдения не отличался от исходного уровня (р>0,05) независимо от программы лечения, что свидетельствует о профилактическом эффекте прогрессирования ремоделирования резистивных сосудов у больных АГ. МЮ – косвенный показатель дилатационного резерва сосудов – в ОСА и ОБА в обеих подгруппах претерпевал значительные изменения: в подгруппе А – МЮ в ОСА соответственно уменьшился на 15,1% и на 18,4%, в ОБА – на 9% и на 9,7%; в подгруппе Б МЮ в ОСА последовательно уменьшился на 13,4% и на 16,1%, в ОБА – на 6,2% и на 8,1% (р<0,05) (рис. 4).
Обсуждение результатов
Согласно существующей формуле: АД = МОС x ПСС, уровень АД линейно зависит не только от состояния насосной деятельности сердца, показателем которой является минутный объем, но и от периферического сосудистого сопротивления (ПСС). ПСС, в свою очередь, согласно упрощенной формуле Пуазейля зависит обратно пропорционально от тонуса сосудов, который определяет диаметр просвета сосудов, но и прямо пропорционально – от длины сосудистого русла и вязкостных параметров крови, т.е. от реологических свойств крови: ОПСС = L . ? / S , где S – площадь просвета сосудов, L – длина сосудистого русла, ? – реология крови. Реологические свойства крови включают в себя глюкозо–белково–липидный состав, количество (Ht) и функциональное состояние форменных элементов, коагуляционный потенциал. Общеизвестно, что применение селективных ? –адреноблокаторов, в частности, Бисогамма, в лечении АГ направлено на уменьшение МО за счет отрицательного хронотропного и инотропного эффектов (т.е. уменьшение УО и ЧСС, т.к. МО = УО x ЧСС). В настоящее время доказано, что повышенное агрегационное состояние тромбоцитов вносит определенный вклад в повышение АД – через секрецию тромбоксанов А 2 , мощного вазоконстриктора [1,2,3]. Тромбоцит – сложная по структуре и функции кровяная клетка, реализует свое функциональное состояние через адрено–рецепторы, аналогичные кардиомиоцитам и гладкомышечным клеткам сосудов. Поэтому использование ? –адреноблокаторов при лечении АГ оказывает эффект «успокоения» тромбоцитов, делая их нечувствительными к катехоламинам, что подтверждается результатами исследования ряда авторов и нашими наблюдениями. В наших наблюдениях после 4–недельного лечения Бисогаммой больных с АГ отмечено снижение агрегационной активности тромбоцитов суммарно по всей группе на 20,1%, косвенно свидетельствующее о наличии в тромбоцитарной мембране ? –адренорецепторов. Одновременно выявлена статистически достоверная корреляционная связь между уровнями САД, ДАД и агрегационным состояниемтромбоцитов. r АТр – ДАД = 0,72 (р<0,001), r АТр – САД = 0,67 (р<0,01). Увеличение ЭФПЭ суммарно по всей группе больных АГ на 14,6% на фоне лечения Бисогаммой, возможно, опосредовано через нормализацию липидного профиля в сторону антиатерогенности. Известно, что нарушения липидного состава эритроцитарных мембран являются одной из причин снижения способности эритроцитов к деформации, а следовательно, к нарушению их подвижности и в целом – текучести крови, что способствует повышению ПСС и АД. Нормализация липидного профиля у больных АГ на фоне лечения Бисогаммой в сочетании с Магнеротом подтверждается результатами наших наблюдений: ИА снизился на 43,1%% (р<0,001) преимущественно за счет увеличения ХЛПВП на 29,7%, (р<0,001). Аналогичная динамика получена в исследованиях других авторов [9,10], что указывает на преимущество Бисогаммы (метаболически нейтрален), действующим началом которого является бисопролол, перед другими ? –адреноблокаторами в лечении АГ, которые способствуют изменению липидного профиля в сторону атерогенности.