По–видимому, целесообразно отметить и тональность современных рекомендаций [1,2] в отношении применения БАБ при ХСН: препараты должны (!) применяться у всех больных, причем тяжесть декомпенсации, пол, возраст, уровни исходного АД и ЧСС не играют самостоятельной роли в определении противопоказаний к назначению БАБ. Основополагающими принципами применения БАБ при ХСН являются назначение препаратов стабильным больным, начало терапии с малых доз и медленное осторожное титрование в идеале до целевых (обозначенных в рекомендациях по данным рандомизированных клинических испытаний) или же терапевтических (оптимальных для конкретного пациента) доз препаратов. При этом обязательным условием является присутствие в терапии иАПФ (в случае противопоказаний к его применению – антагониста рецепторов к ангиотензину II), на фоне которого и должно осуществляться титрование суточной дозы БАБ.
Впрочем, с появлением результатов исследования CIBIS III (Third Cardiac Insufficiency BIsoprolol Study) [3] последнее условие уже не выглядит столь абсолютным. Так, в Национальных рекомендациях ВНОК и ОССН по диагностике и лечению ХСН (второй пересмотр) [2] впервые обозначена возможность начала терапии с b1–селективного БАБ бисопролола с последующим присоединением иАПФ. При этом было подчеркнуто, что конечной целью в любом случае является максимально быстрый перевод больных ХСН на комбинацию иАПФ плюс БАБ.
Насколько эффективна и безопасна стартовая терапия ХСН БАБ в случае, если в базисной терапии
отсутствуют иАПФ? Более того, насколько востребованным может оказаться начало лечения СН БАБ с последующим присоединением к терапии иАПФ? Обратимся к результатам инициированного исследователями многоцентрового проспективного, рандомизированного, открытого с ослепленными конечными точками, в двух параллельных группах исследования CIBIS III [3].
Как известно, гипотеза исследования CIBIS III состояла в том, что начало лечения больных ХСН b1–селективным БАБ бисопрололом (Конкор) (к которому впоследствии добавляется иАПФ эналаприл) будет так же эффективно и безопасно, как и режим начала терапии эналаприлом (к которому впоследствии добавляется бисопролол). Была поставлена цель продемонстрировать, что начальная монотерапия бисопрололом,
а затем комбинация препарата с эналаприлом сопоставима с обратной схемой (монотерапия эналаприлом,
а затем комбинация препарата с бисопрололом) по способности предупреждать смерть и госпитализации по всем причинам (первичная комбинированная конечная точка – время до наступления первого события).
В качестве вторичных конечных точек были обозначены: по завершении фазы монотерапии – смертность и госпитализации по всем причинам и раннее назначение второго препарата в силу плохого контроля течения ХСН;
а по завершении фазы монотерапии и всего исследования – отдельные компоненты первичной конечной точки, число случаев прекращения лечения и изменения функционального класса (ФК) ХСН. Дизайн исследования представлен на рисунке 1. Всего в исследование было включено 1010 пациентов с ХСН II–III ФК старше 65 лет (средний возраст 72,4 года), преимущественно ишемической этиологии (62,4%), ФВ ЛЖ менее 35% (в среднем 28,8%) со стабильным течением СН без признаков задержки жидкости, а также неизменными дозами диуретиков (в случае показаний к их применению) на протяжении 7 дней до рандомизации.
Динамика развития первичной конечной точки в исследуемых группах больных ХСН приведена на рисунке 2. При анализе, включившем данные всех 1010 пациентов с ХСН, рандомизированных в исследование, было установлено, что развитие первичной конечной точки имело место у 178 больных (35,2%) в группе стартовой терапии бисопрололом против 186 (36,8%) у пациентов, находящихся на стартовом лечении эналаприлом (отношение риска – ОР=0,94, 95% доверительный интервал – ДИ 0,77–1,16). При исключении из анализа больных
ХСН, которые не наблюдались до конца исследования и не принимали назначенных препаратов, первичная конечная точка имела место у 163 больных (32,4%)
в группе стартовой терапии бисопрололом против 165 (33,1%) в группе стартовой терапии эналаприлом (ОР=0,97, 95% ДИ 0,78–1,21). Иными словами, проведенный анализ показал сопоставимость двух режимов терапии ХСН: стартовая терапия БАБ бисопрололом,
а затем комбинация препарата с эналаприлом или стартовая терапия иАПФ эналаприлом, а затем комбинация препарата с бисопрололом по способности предупреждать смерть и госпитализации по всем причинам. Цель исследования CIBIS III была реализована, при этом были отмечены благоприятные тенденции (в пользу стартовой терапии бисопрололом) в отношении смертности пациентов с ХСН. Всего за весь период исследования
в группе стартовой терапии бисопрололом умерло 65 больных, а в группе стартовой терапии эналаприлом – 73 пациента (ОР=0,88, 95% ДИ 0,63–1,22, p=0,44). Примечательно, что в конце фазы монотерапии в группе стартовой терапии бисопрололом умерли только 23 больных, в то время как среди пациентов, начавших лечение эналаприлом – 32 пациента с ХСН (ОР=0,72, 95% ДИ 0,42–1,24, p=0,24), что соответствует 28%–му снижению смертности в пользу первого режима терапии (рис. 3). К концу первого года наблюдения среди больных с ХСН, начавших лечение бисопрололом, умерли 42 пациента, а в группе стартовой терапии эналаприлом – 60 больных (ОР=0,69, 95% ДИ 0,46–1,02, p=0,065), что указывает на 31%–е снижение риска смерти в пользу стартового режима терапии ХСН БАБ бисопрололом (рис. 4).
В качестве возможного объяснения преимущества стартовой терапии ХСН БАБ бисопрололом в отношении тенденции к снижению смертности больных авторы исследования указали на способность препарата снижать риск внезапной смерти, одной из важнейших составляющих смертельных исходов у пациентов с ХСН.
Действительно, риск внезапной смерти у больных
ХСН повышается в 6–9 раз по сравнению со значением показателя в общей популяции [4]. Хорошо известно, что на внезапную смерть приходится более
половины всех смертей при II и III ФК ХСН и больных
с ФВ ЛЖ > 21%, в то время как смерть от прогрессирования СН более характерна для IV ФК ХСН [5,6].
Следует подчеркнуть, что с учетом увеличения распространенности ХСН проблема профилактики внезапной смерти у данной категории пациентов приобретает все более важное значение. Примечательно, что по данным специального анализа [7], выполненного по результатам исследования CIBIS II [8], только у 20% больных с ХСН, умерших внезапно, за время наблюдения имело место обострение симптомов СН. В свою очередь, симптомы декомпенсации и связанные с этим госпитализации отмечались почти у 90% больных, умерших от прогрессирования СН [9]. Эти данные подчеркивают не только трудности в выявлении пациентов c ХСН и повышенным риском внезапной смерти, но и актуальность первичной профилактики данного осложнения.
Ранее, в ряде исследований было отмечено, что лечение b–блокаторами больных ХСН, уже находящихся на терапии иАПФ, ассоциируется со снижением риска внезапной смерти. Так, в двух основополагающих рандомизированных клинических испытаниях (РКИ) CIBIS II [8] и MERIT–HF [5] было показано, что терапия пациентов с ХСН бисопрололом и метопрололом CR/XL приводит к снижению риска внезапной смерти на 44 и 41% соответственно.
С другой стороны, в РКИ иАПФ при ХСН или у больных, перенесших инфаркт миокарда, было отмечено, что снижение смертности происходило прежде всего за счет уменьшения прогрессирования или предупреждения развития СН. При этом в таких РКИ, как CONSENSUS, SOLVD–treatment и SAVE [10–12] не удалось продемонстрировать достоверного снижения случаев внезапной смерти при терапии иАПФ эналаприлом. Впрочем, в РКИ AIRE [13] и TRACE [14], выполненных у больных, перенесших инфаркт миокарда и страдающих СН или дисфункцией ЛЖ, отмечено некоторое преимущество иАПФ рамиприла и трандолаприла в отношении внезапной смертности.
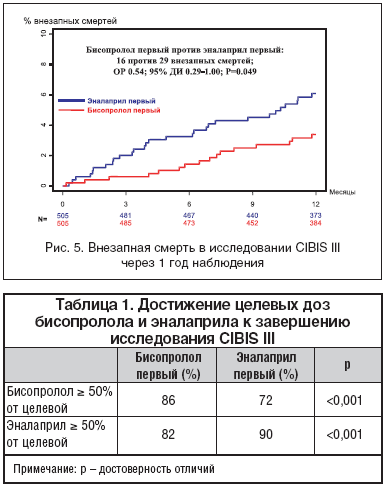
В свете выше изложенного представляет большой интерес специальный анализ, выполненный по данным исследования CIBIS III, в котором проведено сравнение эффектов стартовой терапии БАБ бисопрололом (к которой в последующем добавлялся эналаприл) и стартовой терапии иАПФ эналаприлом (к которой добавлялся бисопролол) в отношении внезапной смертности у больных ХСН. Было установлено, что к завершению фазы монотерапии в группе больных ХСН, принимавших первым бисопролол зафиксировано 8, а у пациентов, начавших лечение эналаприлом – 16 внезапных смертей (ОР=0,50, 95% ДИ 0,21–1,16, p=0,107). К концу первого года наблюдения (6 месяцев монотерапии БАБ бисопрололом или иАПФ эналаприлом и 6 месяцев комбинированной терапии препаратами) в группе больных ХСН, находящихся на стартовой терапии бисопрололом, отмечено 16 внезапных смертей, а у больных, находящихся на начальном лечении эналаприлом – 29
внезапных смертей (ОР=0,54; 95% ДИ 0,29–1,00, p=0,049). (рис. 5). В целом к завершению всего исследования зафиксировано 29 внезапных смертей в группе стартовой терапии бисопрололом и 34 случая внезапной смерти у больных ХСН, начавших лечение эналаприлом (ОР=0,84, 95% ДИ 0,51–1,38, p=0,487).
Полученные данные о преимуществе бисопролола над эналаприлом в отношении достоверного снижения риска внезапной смерти (к концу первого года наблюдения) становятся еще одним аргументом в пользу выбора БАБ в стартовой терапии ХСН. В качестве ограничения данного анализа авторы исследования CIBIS III указали на то, что первичной целью этого РКИ не было изучение влияния БАБ бисопролола на внезапную смертность. Соответственно, для решения этой задачи требуется большее количество наблюдений (хотя приоритет бисопролола выглядит достаточно убедительным).
С практической точки зрения представляется целесообразным обсуждение двух следующих позиций: продолжительности фазы монотерапии и достижение целевых доз БАБ бисопролола и иАПФ эналаприла
в двух сравниваемых режимах терапии.
Согласно дизайну исследования CIBIS III [3] продолжительность монотерапии составила 6 месяцев. Вместе с тем в условиях реальной клинической практики этот период времени может быть существенно сокращен. При этом нельзя не забывать тот факт, что частота госпитализаций, связанных с обострением ХСН в период монотерапии была на 2,7% выше в группе больных ХСН, начавших лечение с приема бисопролола. В Национальных рекомендациях ВНОК и ОССН по диагностике и лечению ХСН (второй пересмотр) [2] указано на необходимость максимально быстрого перевода больных ХСН на комбинацию иАПФ плюс БАБ. Если продолжительность фазы монотерапии БАБ бисопрололом напрямую зависит от того, как пациент с ХСН переносит возрастающие дозы препарата в процессе титрования, то очень важным становится вопрос о возможности достижения целевых дозах как иАПФ, так и БАБ. Действительно, согласно результатам исследования CIBIS III [3] с точки зрения достижения целевой дозы в лучших условиях оказывался тот препарат, с которого начиналось лечение (табл. 1).
По–видимому, свобода выбора стартовой терапии ХСН иАПФ или БАБ потребует от врача тщательного анализа клинической ситуации, что определит скорость титрования суточной дозы препаратов. Очевидно, особое внимание придется уделить больным с невысоким уровнем АД, пожилым больным, пациентам с ХСН ишемической этиологии, принимающим одновременно антиангинальные препараты (например, нитраты).
Следует подчеркнуть, что по завершении фазы монотерапии закономерное урежение ЧСС было обнаружено только у больных ХСН, начавших лечение с приема БАБ бисопролола (78,8±13,8 уд/мин. исходно и 67,9±13,7 уд/мин. через 6 месяцев, p<0,001). К концу же первого года наблюдения ЧСС в двух группах пациентов с ХСН (бисопролол + эналаприл и эналаприл + бисопролол) оказалась практически одинаковой:
66,7±11,8 уд/мин. и 67,5±12,7 уд/мин. соответственно.
В заключение необходимо отметить, что значение результатов исследования CIBIS III, в том числе и в отношении влияния на внезапную смертность, трудно переоценить. Результаты исследования CIBIS III поддерживают концепцию свободного выбора врачом стартовой терапии ХСН – эналаприл или бисопролол (Конкор), основанной на индивидуальном подходе к каждому пациенту. При этом выбор оптимальной стартовой терапии ХСН (иАПФ или БАБ с последующим максимально быстрым переводом больных на комбинацию препаратов) остается за врачом.


Литература
1. Guidelines for the diagnosis and treatment of Chronic Heart Failure: full text (update 2005): The Task Force for the Diagnosis and Treatment of CHF of the European Society of Cardiology. Eur. Heart J. 2005: doi: 10.1093/eurheartj/ehi205, pp1–45
2. Национальные рекомендации ВНОК и ОССН по диагностике и лечению ХСН (второй пересмотр). Журнал Сердечная Недостаточность. 2007; 8, №2: 35С.
3. Willenheimer R., van Veldhuisen D.J., Silke B. et al. Effect on survival and hospitalization of initiating for chronic heart failure with bisoprolol followed by enalapril, as compared with the opposite sequence. Results of the Randomized Cardiac Insufficiecy Bisoprolol Study (CIBIS III). Circulation 2005; 112: 2426–2435
4. American Heart Association. Heart disease and stroke statistics – 2005 update. http://americanheart.org/downloadable/heart/1105909181119HDStats2005Update.pdf (December 2005).
5. MERIT–HF Study Group. Effect of metoprolol CR/XL in chronic heart failure. Metoprolol CR/XL Randomised Intervention Trial in Congestive Heart Failure (MERIT–HF). Lancet 1999; 353: 2001–2007.
6. Cleland J.G.F., Chattopadhyaya S., Khand A. et al. Prevalence and incidence of arrhythmias and sudden death in heart failure. Heart Fail. Rev. 2002; 7: 229–242.
7. Vanoli E., Funck–Brentano C., Hansen S. t al. Effect of bisoprolol on nocturnal sudden death in chronic heart failure. Circulation. 1999; 99 (suppl.): I–783.
8. CIBIS–II Investigators and Committies. The cardiac insufficiency bisoprolol study II (CIBIS–II): a randomized trial. Lancet 1999; 353: 9–13.
9. Cohn J.N., Levine T.B., Olivari M.T. et al. Plasma norepinephrine as a guide to prognosis in patients with chronic congestive heart failure. N. Engl. J. Med. 1984; 311: 819–823.
10. CONSENSUS Trial Study Group. Effects of enalapril on mortality in severe congestive heart failure. Results of the Cooperative North Scandinavian Enalapril Survival Study (CONSENSUS). N. Engl. J. Med. 1987: 316: 1429–1435.
11. The SOLVD Investigators. Effect of enalapril on survival in patients with reduced left ventricular ejection fractions and congestive heart failure. N. Engl. J. Med. 1991; 325: 293–302.
12. Rutherford J.D., Pfeffer M.A., Moye L.A. et al. Effects of captopril on ischemic events after myocardial infarction. Results of the Survival and Ventricular Enlargement trial. SAVE investigators. Circulation. 1994; 90: 1731–1738.
13. Cleland J.G., Erhardt L., Murray G. et al. Effect of ramipril on morbidity and mode of death among survivors of acute myocardial infarction with clinical evidence of heart failure. A report from the AIRE Study Investigators. Eur. Heart J. 1997; 18: 41–51.
14. Torp_pedersen C., Kober L., Carlsen J. Angiotensin–converting enzyme inhibition after myocardial infarction: the Trandolapril Cardiac Evaluation Study. Am. Heart J. 1996; 132: 235–243.












