Поддержание нормального баланса калия и магния в организме – основа прочного здоровья, что актуализирует интерес к проблемам изучения биологической роли макро– и микроэлементов. Калий и магний – одни из наиболее распространенных катионов в организме, их недостаток играет ключевую роль в возникновении функциональных расстройств центральной нервной системы (ЦНС) и сердечно–сосудистой системы (ССС). Важность их оптимального баланса для нормальной жизнедеятельности организма в настоящее время сложно переоценить [2,3,8].
В последние годы пристальное внимание исследователей в различных областях клинической медицины привлечено к проблеме дефицита магния и калия – снижения их концентрации внутри клетки – и его роли при различных патологических состояниях органов и систем. Магний впервые был выделен английским химиком Гефри Дэви в 1808 г., является главным двухвалентным металлом (Mg++) второй группы периодической системы Менделеева, атомная единица массы 24,305; в ионизированной форме представляет собой положительный ион – катион с двойным положительным зарядом (Mg++); является одним из самых распространенных элементов на Земле. Особенно его много в воде Мирового океана (0,13%), которая по электролитному составу близка к электролитному составу сыворотки крови.
Магний (Mg++) по концентрации в организме занимает 4–е место среди других катионов (натрий, калий, кальций) – 0,6–1,1 ммоль/л в плазме крови, а в клетке – 2–е после калия (К+) – 1,6–2,2 ммоль/л (эритроцит). Магний и калий в совокупности с основными неорганическими химическими элементами: кальцием, натрием, хлором, фосфором, фтором, серой, углеродом, кислородом, водородом, азотом определяют 99% ионного состава человеческого организма. В настоящее время установлено наличие не менее 290 генов и белковых фрагментов в последовательности генома человека, которые способны привлекать Mg++ и К+ как кофакторы множества ферментов, участвующих в более чем 300 внутриклеточных биохимических реакциях.
Mагний – естественный физиологический антагонист кальция, универсальный регулятор биохимических и физиологических процессов в организме: контролирует гидролиз АТФ, уменьшая разобщение окисления и фосфолирования, регулирует гликолиз, уменьшает накопление лактата, способствует фиксации калия в клетках, обеспечивая поляризацию клеточных мембран. Mагний, контролируя спонтанную электрическую активность нервной ткани и проводящей системы сердца, обеспечивает нормальное функционирование всех субклеточных структур кардиомиоцита, что определяет его универсальность в кардиоцитопротекции (рис. 1). Магний участвует в энергетическом процессе (синтез АТФ), пластическом (синтез белка, липидов, нуклеиновых кислот, необходимых для синтеза ДНК), репаративном и процессах электролитного обмена, в синтезе соединительной ткани; принимает участие в расслаблении мышечного волокна, снижает агрегационную способность тромбоцитов, поддерживает нормальный трансмембранный потенциал в электровозбудимых тканях.
Дефицит магния при автономной кардиопатии проявляется синдромом удлинения QT–интервала с пароксизмами желудочковой тахикардии по типу torsades de pointes, синкопами и острой остановкой сердечной деятельности, сопровождается развитием синдрома дисплазии соединительной ткани. На ЭКГ дефицит магния манифестируется замедлением АВ–проводимости, уширением комплекса QRS, удлинением интервала QT, неспецифическим снижением ST–сегмента и формированием выраженной волны U [5].
Неврологические проявления при дефиците магния – раздражительность, депрессия, расстройства сна, снижение работоспособности, памяти, остроты слуха, появление шума в ушах, головокружение, мышечные судороги и т.д. Как свидетельствуют результаты крупного проспективного клинического исследования с участием более 41 тыс. женщин в возрасте от 38 до 63 лет, имеется обратная связь между потреблением магния и уровнем артериального давления [2,9].
В свою очередь калий также необходим для нормального функционирования разнообразных внутриклеточных ферментов: он поддерживает осмотический и кислотно–основной гомеостаз, принимает участие в синтезе белка, гликогена, медиаторов нервной системы (ацетилхолина) и т.д. От соотношения этого макроэлемента и других ионов зависят нервно–мышечная возбудимость, сократительная способность миокарда, секреция желез пищеварительного тракта. Сегодня известно, что ионы калия необходимы для регуляции секреции инсулина, особенно в условиях нарушенной толерантности к глюкозе или СД 2–го типа.
Чаще всего при гипокалиемии страдает ССС – возникает автономная кардионейропатия со сложными нарушениями ритма сердечной деятельности, вплоть до развития фибрилляции предсердий или внезапной сердечной смерти. На ЭКГ при дефиците калия регистрируются сглаженный зубец Т, патологическая волна U, политопные экстрасистолы [5]. Результаты многочисленных исследований подтверждают важную роль калия в профилактике и лечении артериальной гипертензии (АГ), а также снижении частоты развития мозгового инсульта.
Дефицит этого макроэлемента приводит к повышению артериального давления (АД) у пациентов с эссенциальной АГ [3,14]. Клиническая симптоматика со стороны ЦНС при дефиците калия – астения, депрессия, нервно–мышечные расстройства (мышечная слабость, судороги, парезы). Нарушения со стороны мочеполовой системы при низком уровне калия проявляются в виде атонии мочевого пузыря, полиурии, со стороны пищеварительной системы – в виде снижения перистальтики кишечника с постоянным запором, вплоть до паралитической кишечной непроходимости (рис. 2).
Таким образом, оптимальное соотношение калия и магния является основой нормального функционирования человеческого организма в целом.
Опосредованными признаками внутриклеточного дефицита калия и магния являются снижение их концентрации в сыворотке крови соответственно ниже 3,5 и 0,65 ммоль/л, специфические изменения стандартной ЭКГ с клиническими проявлениями эндотелиальной дисфункции, лежащей в основе ССЗ [2,9].
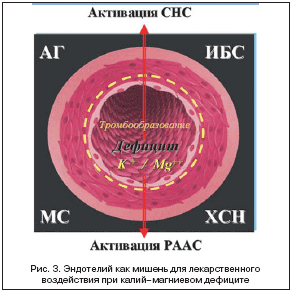
Эндотелий – монослой клеток, полуселективный барьер между кровью и сосудистой стенкой протяженностью 7 км, с общей площадью 400 м2 и весом около 2 кг, нормальная функция которого находится в прямой зависимости от внутриклеточного баланса электролитов (калий, магний), играет чрезвычайно важную роль в нормализации функционального состояния ССС. Дисфункция эндотелия – снижение способности эндотелиальных клеток секретировать эндотелийзависимый фактор релаксации (ЭЗФР) – NO, с относительным или абсолютным увеличением синтеза сосудосуживающих, агрегационных и пролиферативных факторов. Эндотелиальная дисфункция возникает в том числе и вследствие гиперактивации ренин–ангиотензин–альдостероновой системы (РААС) [7,8,11] (рис. 3).
Калий–магниевый дефицит в клинической практике довольно часто является причиной развития фибрилляции предсердий (ФП). ФП – самое частое осложнение из всех разновидностей наджелудочковой тахиаритмии, сопровождающееся тяжелыми гемодинамическими расстройствами. ФП встречается в общей популяции населения в 0,3–0,4% случаев, имеет тенденцию к учащению с возрастом и в подавляющем большинстве случаев является следствием нарушения внутриклеточного калий–магниевого баланса кардиомиоцитов. Пароксизмы ФП – причина более трети госпитализаций по поводу нарушений ритма сердечной деятельности. В настоящее время ФП наиболее часто ассоциируется с ИБС, ХСН. У 60% больных с ФП обнаруживается АГ, которая в большинстве случаев является сопутствующим заболеванием [1,4–6].
Клиническая картина ФП обусловлена выраженностью нарушений центральной гемодинамики и варьирует от бессимптомного течения до развития отека легкого, синкопальных состояний, приступов стенокардии, ишемических инсультов и т.д. Отсутствие систолы предсердия уменьшает диастолическое наполнение желудочков, предшествующее систоле желудочков, и при здоровом миокарде снижает МО сердца до 25%, а при заболеваниях миокарда левого желудочка – до 50% (в частности, гипертрофическая кардиомиопатия, ОКС).
Таким образом, восстановление синусового ритма при ФП необходимо для восстановления эффективной насосной деятельности сердца с целью предупреждения развития острой левожелудочковой недостаточности, ХСН и тромбоэмболических осложнений. В восстановлении синусового ритма немаловажное значение имеет состояние калий/магниевого баланса, обеспечивающего мембран–стабилизирующий эффект.
Другая разновидность наджелудочковых и желудочковых аритмий сердца, обусловленных недостатком калия и магния, – экстрасистолии. Экстрасистолическая аритмия (экстрасистолия) – нарушение сердечного ритма в связи с преждевременными сокращениями сердца, вызванными возбуждениями (по типу mikrо–re–entry), возникающими вне синусно–предсердного узла. Возникновение экстрасистолий зависит от состояния нервной системы: они часто наблюдаются при неврозах и эмоциональных стрессах (радость, гнев, испуг, страх и др.), сопровождающихся интенсивной потерей калия и магния. Серия экстрасистол может вызвать преходящие расстройства мозговой гемодинамики, клинически проявляющиеся общей слабостью, быстрой утомляемостью, раздражительностью, снижением внимания и памяти, потемнением в глазах или мельканием «мушек», головокружением, головной болью, нарушением сна [1–3,5].
Хроническая недостаточность магния и калия неблагоприятно сказывается на течении ИБС, что обусловлено нарушениями функции эндотелия, активацией перекисного окисления, прогрессированием атеросклероза [8,10,11]. При ИБС в механизмы развития защитного эффекта ишемического прекондиционирования вовлечено множество различных факторов. Согласно последним данным, в поддержании нормального внутриклеточного энергофосфатного баланса ведущую роль играют митохондриальные ионы Mg++, активизирующие К+–каналы, которые участвуют в электронно–транспортной цепи окислительного фосфорилирования в митохондриях. Фармакологическое открытие АТФ–зависимых К+–каналов с помощью внутривенного или перорального введения калий–магниевого состава полностью воспроизводит защитный эффект ишемического прекондиционирования – защиту кардиомицитов от ишемического повреждения [8].
У пациентов с АГ также имеет место снижение плазменных концентраций калия и магния с повышением уровнем натрия (более 140 ммоль/л). Одновременно активация РААС и эндотелиальная дисфункция при хроническом дефиците магния создают благоприятные условия для системной вазоконстрикции и развития сосудистых осложнений при АГ и ХСН.
Что же вызывает дефицит калия и магния в организме? Причиной может быть несбалансированное питание; кроме того, гипомагнезиемия и гипокалиемия нередко сопутствуют таким видам патологии, как заболевания ССС, СД 2–го типа, наследственные болезни почек, тяжелая форма диареи и рвоты. Дисбаланс калия и магния может развиться при избыточном употреблении продуктов, содержащих вытеснители калия и магния (NaCl): чипсы, сушеные кальмары и другие пересоленные продукты, так как соль способствует активному выведению калия и магния из организма и ингибирует их вхождение в клетку. К дефициту калия и магния может привести бесконтрольное применение некоторых лекарственных средств: диуретиков, не сберегающих калий, сердечных гликозидов, гентамицина и др.
Результаты многочисленных исследований, первое из которых было проведено еще в 1928 г., подтверждают роль магния и калия в профилактике и лечении АГ. В Роттердамском исследовании (Rotterdam Study, 1996) участвовало более 3200 человек в возрасте старше 55 лет, которые не принимали антигипертензивные препараты [9,13,14]. Результаты данного исследования подтверждают, что увеличение потребления калия и магния было сопряжено со снижением уровня систолического и диастолического АД. В 5–летнем рандомизированном плацебо–контролируемом исследовании SHEP (Systolic Hypertension in the Elderly Program) были проанализированы данные более 4 тыс. пациентов пожилого возраста с изолированной систолической АГ. Его целью было определить взаимосвязь гипокалиемии, которая имеет место при назначении низких доз диуретиков, и кардиоваскулярных событий. Полученные результаты свидетельствуют: существенное снижение риска развития сердечно–сосудистых осложнений, таких как инфаркт и инсульт, при лечении диуретиками имело место у больных с нормальными уровнями калия и магния в крови.
Не менее интересно другое исследование, целью которого было изучить, как влияет употребление калия, магния, кальция и клетчатки на риск развития инсульта. В испытание были включены более 43 тыс. мужчин в возрасте от 40 до 75 лет без диагностированных кардиоваскулярных заболеваний или СД. В течение последующих 8 лет было зафиксировано 328 геморрагических и ишемических инсультов. На основании анализа полученных результатов была выявлена обратная связь между уровнем потребления калия и магния и риском развития инсульта [6,9,13,14].
Восстановление запасов калия и магния способствует коррекции эндотелиальной дисфункции, являющейся инициатором становления и прогрессирования ССЗ. По данным различных исследователей, назначение пероральных препаратов магния и калия пациентам с ИБС сопровождалось достоверным увеличением эндотелийзависимой дилатации плечевой артерии на 15,5% (p<0,01) по сравнению с плацебо – на 4,4% (p>0,05), при этом выявлена линейная корреляционная связь между внутриклеточной концентрацией магния и степенью вазодилатации [9,11].
С учетом антиатерогенных эффектов препаратов магния коррекция его дефицита может способствовать замедлению прогрессирования ИБС [2,7–9]. В исследовании ARIC (The Atherosclerosis Risk In Communities) после 4–7 лет наблюдения за 13 922 пациентами анализ факторов риска показал наличие связи между развитием ИБС и гипомагниемии [9]. Наиболее выраженный дефицит магния имеет место у пациентов с повышенным содержанием атерогенных липидов [8]. Часто у пациентов с ССЗ выявляется СД 2–го типа, при котором усиливается дефицит магния, особенно в пожилом возрасте. Применение препаратов магния у таких пациентов способствует улучшению инсулинозависимой утилизации глюкозы [10].
Недостаток калия и магния у пациентов с ХСН ассоциирован с неблагоприятным качеством и прогнозом жизни. Назначение магний– и калийсодержащих препаратов особенно оправданно при длительном приеме сердечных гликозидов и диуретиков, которые провоцируют гипомагниемию/гипокалиемию и последующие нарушения ритма сердечной деятельности, связанные с дефицитом этих электролитов [3,9,12].
Антиаритмический эффект магния реализуется через воздействие на транспорт ионов натрия, калия и кальция, участвующих в формировании потенциала действия [2]. В качестве антиаритмика соли магния чаще всего используют при пируэт–желудочковых аритмиях (torsades de pointes) благодаря способности угнетать развитие следовых деполяризаций, укорачивая длительность интервала QT. Магний может быть применен как при врожденном синдроме удлиненного интервала QT, так и при ятрогенном его варианте, вызванном применением антиритмиков 1–го класса и других лекарственных средств [3,5]. Препараты магния применяются для профилактики аритмий, провоцируемых дигиталисной интоксиацией, когда нарушена функция калий–натриевой помпы [8].
Своевременное пополнение запасов калия и магния в организме необходимо пациентам с ССЗ. Эти внутриклеточные катионы улучшают метаболизм миокарда, принимают участие в молекулярных механизмах мышечного сокращения и необходимы для работы многих внутриклеточных ферментов.
Учитывая важную роль, которую играют микроэлементы калий и магний в нормальном функционировании организма, целесообразно применять комбинированные препараты, содержащие калий и магний. Сочетание ионов калия и магния в одном препарате обосновано тем, что дефицит калия в организме сопровождается или обусловлен дефицитом магния и требует одновременной коррекции содержания в организме обоих катионов. При одновременной коррекции уровней этих электролитов наблюдается аддитивный эффект; при этом калий и магний снижают токсичность гликозидных препаратов во время лечения ХСН, не оказывая отрицательного влияния на их положительный инотропный эффект.
К числу таких комбинированных препаратов относится безрецептурный препарат Панангин (компания «Гедеон Рихтер»), который за долгие годы присутствия на фармацевтическом рынке Российской Федерации успел завоевать доверие потребителей. Панангин можно смело рекомендовать не только пациентам с ССЗ, но и здоровым людям с целью восполнения дефицита этих важных катионов и своевременной профилактики широкого спектра патологических состояний. Входящий в состав Панангина эндогенный аспарагинат, характеризующийся большим сродством к клеткам, выступает в качестве проводника ионов внутрь клетки, т.е. способствует более быстрому и эффективному вхождению калия и магния в миоциты. Одновременно аспарагинат калия и магния оказывает положительное влияние на метаболизм миокарда.
Показаниями для применения Панангина с лечебной и профилактической целью являются: алиментарная гипокалиемия и гипомагниемия, а также заболевания ССС в комплексной терапии сердечной недостаточности, при перенесенном инфаркте миокарда и нарушениях сердечного ритма. Кроме того, Панангин необходимо назначать при лечении сердечными гликозидами (для повышения их эффективности и улучшения переносимости препаратов этой группы).
Учитывая высокую распространенность ССЗ в РФ, этот препарат по праву занимает важное место в лечебно–профилактических рекомендациях врачей первичного звена здравоохранения.
При лечении нарушений ритма сердечной деятельности Панангин назначают по 2–3 таблетки 3 р./сут., максимальная суточная доза – 3 таблетки 3 р./сут. В качестве поддерживающей или профилактической терапии (для предупреждения развития аритмий на фоне лечения диуретиками) препарат следует назначать по 1–2 таблетки 3 р./сут. после приема пищи, т.к. кислая среда содержимого желудка снижает эффективность его всасывания. Применение инфузионных растворов Панангина возможно как профилактика возникновения аритмий, а также в ряде случаев для их купирования, например у пациентов с ОКС, ХСН при приеме сердечных гликозидов [8].
Панангин – нетоксичный препарат, не обладает кумулятивным эффектом и имеет ограниченный перечень относительных противопоказаний для его применения: острая или хроническая почечная недостаточность (олигурия, анурия), на ЭКГ атриовентрикулярная блокада III степени, болезнь Аддисона, острый метаболический ацидоз, гиповолемия (обезвоживание), индивидуальная гиперчувствительность к компонентам препарата.
Таким образом, внутриклеточные концентрации ионов К+ и Mg++ обеспечивают нормальный метаболизм ЦНС и ССС и, как уже говорилось, являются основой нормального функционирования человеческого организма. Возникновение дефицита калия и магния – снижение внутриклеточной концентрации ниже референтных значений – сопровождается клиническими проявлениями нарушений функций со стороны ССС (ИБС, ОКС, ИМ, АГ, нарушения ритма сердечной деятельности) и ЦНС (синдром хронической усталости, циркуляторная энцефалопатия), является следствием нарушения баланса между их доставкой и темпом выведения. Компенсировать дефицит калия и магния следует с помощью комбинированных препаратов, одновременно содержащих калий и магний. Наиболее эффективным в профилактике и лечении осложнений ССЗ является препарат, содержащий аспарагинат калия и магния, – Панангин.


Литература
1. Аритмии сердца. Механизмы, диагностика, лечение. Т. 1. М.: Медицина, 1996. С. 346–379.
2. Громова О.А. Магний и пиридоксин: основы знаний. Новые технологии диагностики и коррекции дефицита магния. Обучающие программы ЮНЕСКО. М.: РСЦ Института микроэлементов, 2006. С 3–176.
3. Метелица В.И. Справочник по клинической фармакологии сердечно–сосудистых лекарственных средств. М., 2002. С. 509–513.
4. Нечаева Г.М., Яковлев В.М., Друк И.В., Тихонова О.В. Нарушения ритма сердца при недифференцированной дисплазии соединительной ткани // Лечащий врач. 2008. № 6. С. 2–7.
5. Томов Л., Томов И. Нарушения ритма сердца. Клиническая картина и лечение. София, 1976. С. 62–81.
6. Фонякин А.В., Машин В.В., Гераскина Л.А., Машин В.Вл. Кардиогенная энцефалопатия. Факторы риска и подходы к терапии // Consilium Medicum. 2012. Т. 14. |№ 2. С. 4–7.
7. Шевченко О.П., Праскурничий Е.А., Шевченко А.О. Артериальная гипертония и ожирение. М.: Реофарм, 2006.
8. Шилов А.М. Инфаркт миокарда. М.: Миклош, 2009. С. 7–163.
9. Шилов А.М., Мельник М.В., Осия А.О. Лечение сердечно–сосудистых заболеваний в практике врача первичного звена здравоохранения: место препаратов калия и магния (Панангин) // РМЖ. 2012. № 3. С. 102–107.
10. Barbato J.E., Zuckerbraun B.S., Overbaus M. and al. Nitric oxide modulates vascular inflammation and intimal hyperplasia in insulin resistance and metabolic syndrome // J. Physiol. Heart. Circ. 2005. Vol. 289. Р. 228–236.
11. Caballero A.E. Endothelial dysfunction in obesity and insulin resistance: a road to diabetes and heart disease // Obes. Res. 2003. Vol. 11. Р. 1278–1289.
12. Kannel W. Fifty years of Framingham Study contributions to understanding hypertension // J Hum Hypertens. 2000. Vol. 14 (2). Р. 83–90.
13. Jellinek H., Takacs E. Morphological aspects of the effects of orotic acid and magnesium // Arzneimittelforschung. 1995. Aug. Vol. 45 (8). Р. 836–842.
14. Seelig M.S. Metabolic Sindrom–X. A complex of common diseases – diabetes, hypertension, heart disease, dyslipidemia and obesity – marked by insulin resistance and low magnesium/high calcium // Mineral Res. Intern. Tech. Prod. Infor. 2003. Р. 1–11.












