Эпидемиология. В Российской Федерации распространенность ХСН I–IV функционального класса (ФК) составляет 7% (7,9 млн человек). Клинически выраженная ХСН (II–IV ФК) имеется у 4,5% населения (5,1 млн), распространенность терминальной ХСН (III–IV ФК) достигает 2,1% случаев (2,4 млн) [2].
Причины ХСН. В первую очередь это такие наиболее широко распространенные заболевания, как гипертоническая болезнь (ГБ) и другие состояния, сопровождающиеся артериальной гипертензией (АГ) (заболевания почек, надпочечников, гипофиза, щитовидной и паращитовидной желез), ишемическая болезнь сердца (ИБС), миокардиты, кардиомиопатии (КМП), пороки сердца, заболевания эндокарда и перикарда, аритмии, а также такие внесердечные болезни, как анемия, сепсис и др.
Следует особо подчеркнуть изменившуюся роль АГ в генезе возникновения ХСН. В настоящее время она вышла на первое место среди причин ХСН, составляя почти 1/2 случаев и опередив даже ИБС. Если еще несколько лет назад врач почти автоматически диагностировал ИБС при возникновении признаков ХСН у больного ГБ, то в настоящее время убедительно показана самостоятельная роль АГ в происхождении ХСН. Аналогичным образом при развитии различных форм фибрилляции предсердий (ФП) у больных с ХСН ставился диагноз ИБС. Современное понимание данных вопросов связано с тем положением, что ХСН и ФП могут возникать у больных с ГБ и без наличия ИБС. В этих случаях они являются проявлением так называемого «гипертонического сердца», критерии диагностики которого при ХСН изложены ниже. Диагноз ИБС следует ставить лишь в тех случаях, когда имеются убедительные признаки стенокардии, инфаркта или безболевой ишемии миокарда, что позволяет избежать в большинстве случаев ненужных диагностических (например, коронароангиографии) и лечебных мероприятий.
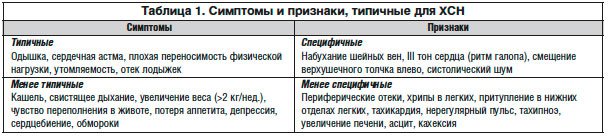
Диагностика ХСН. Верификации ХСН придается огромное значение. Это обусловлено, в первую очередь, выраженным сходством клинической симптоматики ХСН и других патологических состояний. Основные симптомы и признаки, типичные для ХСН, представлены в таблице 1.
Симптомы делят в настоящее время на типичные и менее типичные, а признаки – на специфические и менее специфические. Интересно отметить, что такие кардинальные признаки ХСН, как периферические отеки, хрипы в легких или крепитация, а также увеличение печени, отнесены к менее специфическим [1]. И, действительно, подобные признаки с не меньшей, а в некоторых случаях даже с большей частотой наблюдаются при заболеваниях почек, печени, щитовидной железы, венозной и лимфатических систем, а также других органов. Такой характерный и нередко первый симптом ХСН, как одышка, встречается при хронических заболеваниях легких, анемии, при различных экзогенных и эндогенных интоксикациях вследствие раздражения дыхательного центра продолговатого мозга, при органических поражениях центральной нервной системы, неврозах, гипервентиляционном синдроме, панических атаках и других патологических состояниях. Вследствие этого перед врачом стоит весьма непростая задача, связанная с дифференциальной диагностикой ХСН и других заболеваний.
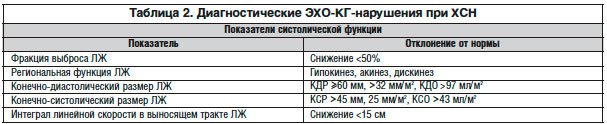
Большое значение в диагностике ХСН имеет тщательный сбор анамнеза. Она маловероятна при отсутствии АГ или перенесенного в прошлом инфаркта миокарда, или других признаков повреждения миокарда [3]. Регистрация ЭКГ является, как известно, обязательным исследованием у больных с подозрением на поражение сердца любого происхождения. На ЭКГ при ХСН могут быть признаки рубцовых поражений или гипертрофии миокарда, а также нередко регистрируются различные нарушения ритма и проводимости сердца. Однако подобные ЭКГ-признаки могут регистрироваться и без наличия ХСН, вследствие чего данный метод для подтверждения ХСН не является решающим. В то же время следует подчеркнуть, что нормальная ЭКГ практически в большинстве случаев позволяет исключить наличие клинически значимой ХСН [4]. Таким образом, в диагностике ХСН скорее имеет значение отрицательный результат, т. е. отсутствие существенных отклонений на ЭКГ, чем обнаружение каких-либо изменений. Кардинальное значение для установления ХСН имеют в настоящее время 2 метода: 1) ЭХО-КГ с допплерографией в состоянии покоя; 2) исследование уровня натрийуретических пептидов в плазме крови. Наиболее характерные ЭХО-КГ-показатели систолической дисфункции левого желудочка (ЛЖ) сердца при ХСН представлены в таблице 2.
Как видно из таблицы 2, наиболее важным показателем систолической дисфункции является снижение фракции выброса (ФВ) менее 50%. Особо следует подчеркнуть, что значение данного показателя в пределах 35–50% относится к «серой» или «переходной» зоне, и лишь снижение ФВ менее 35% является клинически значимым. Между тем до настоящего времени, согласно руководствам, изданным в последние десятилетия прошлого века, некоторые специалисты по ультразвуковой диагностике относили к снижению сократительной способности миокарда значение ФВ менее 55–60%. Оптимальным способом расчета ФВ является метод Симпсона [5]. Метод вычисления ФВ по Тейхольцу основан на измерении линейных размеров сердца и может давать неточные результаты, прежде всего у больных с нарушением локальной сократимости миокарда. Трехмерная ЭХО-КГ позволяет более точно определять объем и ФВ ЛЖ при условии получения изображения необходимого качества [6].
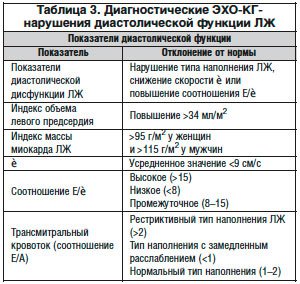
Более сложной является оценка диастолической функции ЛЖ с помощью ультразвуковых методов исследования. Важно помнить, что ни один из показателей не обладает достаточной диагностической точностью для оценки диастолической функции. Вследствие этого следует учитывать данные, полученные с использованием как допплеровского, так и двухмерного режимов. Особо важно подчеркнуть, что к настоящему времени накоплено достаточно данных, свидетельствующих о малой информативности характеристик трансмитрального потока, полученных с помощью импульсного допплеровского исследования. С целью оценки диастолической функции наиболее приемлемым является использование тканевого допплеровского исследования [7]. Максимальная скорость подъема основания ЛЖ в раннюю диастолу (скорость e), измеренная с помощью тканевого допплеровского исследования, позволяет оценить скорость расслабления миокарда. Соотношение Е/e тесно связано с давлением наполнения ЛЖ. В то же время невозможно представить значимую диастолическую дисфункцию ЛЖ без увеличения левого предсердия [8]. Подобным критерием в настоящее время, согласно рекомендациям, является повышение индекса объема левого предсердия более 34 мл/м2 (по прежним нормативам увеличение размера левого предсердия в продольной парастернальной позиции более 5,0 см). Основные признаки диастолической дисфункции ЛЖ представлены в таблице 3.
Важнейшими из них являются снижение скорости e (усредненная скорость менее 9 см/с) и/или повышение соотношения Е/e >15, увеличение индекса объема левого предсердия более 34 мл/м2. Отклонение от нормы по меньшей мере 2-х показателей и/или наличие фибрилляции предсердий повышают точность диагностики диастолической дисфункции.
Вторым методом, способным подтвердить или отвергнуть наличие ХСН, является определение в плазме крови концентрации натрийуретических гормонов (пептидов). Их секреция возрастает при органических поражениях сердца, а также при повышении гемодинамической нагрузки на сердце [3]. Нормальное содержание натрийуретических гормонов при отсутствии предшествующего лечения исключает значимое поражение сердца и наличие ХСН. В таких случаях целесообразно сосредоточиться на поиске внесердечных причин имеющейся у больного клинической симптоматики, сходной с ХСН. В настоящее время определены «пороговые значения» для данных пептидов. При остром начале сердечной недостаточности или резком нарастании ХСН диагностическое значение имеет повышение уровня мозгового натрийуретического пептида (BNP) более 100 пг/мл, а его N-концевого предшественника (NT-proBNP) – более 300 пг/мл. При постепенном начале симптоматики ХСН диагностическим значением BNP, подтверждающим диагноз, является уровень более 35 пг/мл, а NT-proBNP – более 125 пг/мл.
Другие методы исследования не столь важны для установления диагноза ХСН, но имеют значение для определения стадии процесса, выбора того или иного лекарственного препарата или возникновения нежелательных явлений в процессе лечения. В частности, рентгенография грудной клетки позволяет выявить венозный застой или отек легких. Исчезновение данных признаков на фоне лечения может служить объективным критерием его эффективности. Обнаружение величины кардиоторакального индекса более 50% свидетельствует о патологии сердца. В дополнение к стандартному биохимическому и гематологическому анализу крови большое значение имеет определение содержания тиреотропного гормона в крови, т. к. клинические проявления заболеваний щитовидной железы, и особенно гипотиреоза, могут быть схожими с ХСН. При лечении ингибиторами ангиотензинпревращающего фермента (иАПФ), блокаторами рецепторов ангиотензина (БРА), блокаторами минералокортикоидных рецепторов (БМКР), диуретиками следует особенно тщательно следить за содержанием в крови калия, натрия и креатинина.
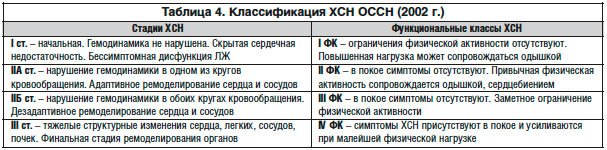
Классификация ХСН. Отечественная классификация ХСН, принятая в 2003 г. Российским съездом кардиологов, предусматривает объединение классификации ХСН по стадиям (классификация Стражеско – Василенко) и ФК (по NYHA). В систематизированном виде она представлена в таблице 4. Стадия ХСН определяет тяжесть поражения сердца, а ФК – субъективное самочувствие больного. Считается, что стадия ХСН не претерпевает обратного развития, а ФК – может.
Существенное значение для выбора тактики ведения пациента имеет установление преимущественно систолической, диастолической или смешанной дисфункции ЛЖ.
Для установления диагноза систолической дисфункции необходимо наличие 3-х компонентов. Это:
1. Симптомы, типичные для ХСН.
2. Типичные клинические признаки ХСН.
3. Низкая ФВ ЛЖ (менее 35–40%).
Для постановки диагноза диастолической дисфункции, или, как теперь ее принято называть, ХСН с сохранной ФВ ЛЖ, необходимо наличие 4-х компонентов. Это:
1. Симптомы, типичные для ХСН.
2. Клинические признаки, типичные для ХСН (на ранних стадиях ХСН могут отсутствовать).
3. Нормальная или слегка сниженная (не менее 40%) ФВ ЛЖ.
4. Соответствующие структурные изменения сердца (гипертрофия ЛЖ / расширение левого предсердия) и/или диастолическая дисфункция ЛЖ.
Впервые возникшая сердечная недостаточность может дебютировать остро (при остром инфаркте миокарда или остром миокардите, перикардите). Тогда следует констатировать острую сердечную недостаточность и классифицировать ее по Killip (I ФК – при остром заболевании признаки сердечной недостаточности отсутствуют; II ФК – имеются клинические и рентгенологические признаки застоя крови в легких; III ФК – сердечная астма или отек легких; IV ФК – кардиогенный шок).
ХСН нарастает постепенно, переходя от бессимптомной дисфункции сердца к клинически выраженной ХСН. В ходе лечения клинические проявления ХСН могут уменьшиться или вообще исчезнуть. В таких случаях констатируют достижение компенсации. Однако нередко на фоне стабильного состояния больного вследствие различных причин (прогрессирование заболевания, прекращение или уменьшение лечения, особенно приема диуретиков, интеркуррентные инфекции, операции, прием нестероидных противовоспалительных препаратов (НПВП) и др.) наступает ухудшение состояния. В этих случаях говорят об острой декомпенсации ХСН.
Помимо упомянутых выше терминов в медицинской литературе, особенно прежних лет, можно встретить такие определения, как «недостаточность кровообращения», «застойная сердечная недостаточность». Являясь по существу верной, подобная терминология все же не должна использоваться для единого понимания однотипных процессов.
Лечение ХСН. Задачи лечения ХСН очевидны и сводятся к предотвращению развития симптомной ХСН (на ранних стадиях), устранению ее признаков, замедлению прогрессирования болезни, улучшению качества жизни, уменьшению количества госпитализаций, улучшению прогноза.
Лечение следует всегда начинать с немедикаментозных мероприятий. Существенное значение имеет ограничение употребления соли. При I ФК не следует употреблять соленую пищу, при II ФК – нужно недосаливать пищу, при III и IV ФК – употреблять продукты с уменьшенным содержанием соли. Менее важно ограничение жидкости. Объем употребляемой жидкости не должен превышать 1,5–2,0 литра. Важнейшее значение имеет регулярный контроль веса больных с ХСН, который должен осуществляться не менее 3 р/нед. Увеличение веса более 2 кг за 1–3 дня свидетельствует о задержке жидкости в организме и риске развития декомпенсации ХСН [1]. Категорически запрещено употребление алкоголя при алкогольной кардиомиопатии. Больным с другим генезом ХСН разрешено употребление 20 мл этанола в сутки, но без больших объемов приема, например, пива. При стабильном состоянии пациента следует рекомендовать физическую активность при всех ФК заболевания. Большое значение имеет тренировка мышц вдоха и выдоха (раздувание шарика, использование дыхательного тренажера Фролова). При IV ФК рекомендуются упражнения для мелких групп мышц, при III ФК – также и для крупных мышц, ходьба, при II ФК – велотренажер, тредмил, при I – дополнительно легкий бег на месте, плавание.
Согласно современным рекомендациям, медикаментозные средства, применяемые для лечения ХСН, делятся на 3 основные группы:
1. Препараты, которые должны применяться в обязательном порядке у всех больных при отсутствии противопоказаний (доказательство эффективности IА).
2. Препараты, применяемые по определенным показаниям (доказательство эффективности IC–IIA).
3. Препараты, применяемые в особых клинических ситуациях (доказательство эффективности IIA–IIB). Препараты первых 2-х групп приводят к улучшению прогноза, снижению смертности и заболеваемости при ХСН, а 3-й группы – к улучшению качества жизни без влияния на прогноз заболевания.
Препараты, используемые при ХСН в обязательном порядке. К данной группе лекарств относятся иАПФ, b-адреноблокаторы (БАБ) и БМКР или спиронолактоны.
иАПФ относятся к первой линии лекарств, применяемых для лечения ХСН. Известное выражение патриарха современной кардиологии Браунвальда о том, что «иАПФ являются краеугольным камнем лечения сердечной недостаточности» сохраняет свою актуальность и по сей день. иАПФ показали свою эффективность как для профилактики развития ХСН, так и для лечения всех стадий и ФК заболевания. Все иАПФ, применяемые в нашей стране, имеют в качестве показания наличие ХСН. Однако наибольшую эффективность показали такие иАПФ, как каптоприл, эналаприл, фозиноприл, периндоприл и лизиноприл. Все эти иАПФ имеют свою «клиническую нишу» для применения. В частности, каптоприл и эналаприл целесообразно использовать на начальных этапах лечения, когда необходимы подбор и титрование дозы препарата. Однако необходимость использования данных средств 2–3 р./сут значительно снижает приверженность больных к их приему. Вследствие этого для многолетнего приема в амбулаторных условиях наиболее приемлемы препараты суточного действия. Липофильный иАПФ периндоприл, который показал способность влиять и на атеросклеротический процесс, особо показан для лечения больных ХСН ишемического генеза.
Гидрофильный препарат лизиноприл, который на 100% выводится почками, имеет преимущество у больных ХСН с поражением печени и желчевыводящих путей, ожирением, при необходимости одновременного приема НПВП. В то же время его использование должно быть ограничено при тяжелой ХСН, когда большинство больных имеют поражение почек.
В этих случаях следует использовать фозиноприл, который имеет 2 пути выведения из организма – через почки и через печень. Убедительно продемонстрирована способность фозиноприла увеличивать толерантность к физическим нагрузкам, замедлять прогрессирование ХСН и уменьшать число госпитализаций [3]. В рандомизированном сравнительном исследовании с эналаприлом показано преимущество фозиноприла (эффективность и безопасность) в предотвращении осложнений. Данное обстоятельство особенно важно при повышении уровня креатинина, которое наблюдается при ХСН в 5–15% случаев и нередко возникает в ходе лечения иАПФ вследствие снижения почечной фильтрации. Немаловажно, что типичный побочный эффект иАПФ – кашель при применении фозиноприла выражен в минимальной степени. Кроме кашля препятствием к назначению иАПФ является гипотония, которая может быть как исходной, так и возникать в ходе лечения ХСН. Минимальное систолическое АД, при котором возможно применение иАПФ, – 85 мм рт. ст. В этих случаях следует начинать лечение с малых доз (1/4 терапевтической дозы) иАПФ с очень медленным титрованием под контролем АД (увеличение дозы не чаще 1 р./нед.). Во избежание гипотонии первую дозу иАПФ следует назначать не менее чем через 24 ч после обильного диуреза. Если АД будет и далее снижаться, то лечение иАПФ приходится на некоторое время прекратить. Абсолютными противопоказаниями к назначению иАПФ, как, впрочем, и БРА, являются их непереносимость (ангионевротический отек), двусторонний стеноз почечных артерий, беременность, увеличение уровня калия крови более 5,5 ммоль/л.
В случаях непереносимости иАПФ (в большинстве случаев это развитие кашля и ангионевротического отека) они могут быть заменены на БРА (уровень доказанной эффективности IIА). Однако если все иАПФ так или иначе могут быть применены при ХСН, то из БРА только 3: лозартан, валсартан и кандесартан. Убедительно показано, что лозартан в дозе 150 мг/сут достоверно снижает риск смерти и госпитализаций больных с ХСН, а в дозе 100 мг/сут может предупреждать развитие ХСН, в т. ч. у пациентов с сахарным диабетом (СД) и нефропатией. Валсартан является эффективным средством профилактики ХСН у больных с острым коронарным синдромом. Он на 33% снижал риск смерти при декомпенсации ХСН. При лечении кандесартаном больных ХСН с низкой ФВ (<40%) снижение риска смерти составило 33% после первого года наблюдения, 20% – после второго и 12% – после третьего.
Обоснованием применения БАБ при ХСН (доказательство эффективности IA) является блокада симпатоадреналовой системы [1]. БАБ уменьшают дисфункцию и гибель кардиомиоцитов, улучшают показатели гемодинамики вследствие уменьшения числа зон гибернации, уменьшают гипертрофию миокарда, снижают ЧСС, частоту желудочковых аритмий и внезапной смерти. БАБ снижают смертность больных с декомпенсаций ХСН на 29%. Отрицательным свойством применения БАБ при ХСН является снижение сократительной способности миокарда. Поэтому необходимо строго соблюдать правила назначения БАБ больным с ХСН:
1. БАБ могут быть назначены лишь при стабилизации состояния у больных с декомпенсацией ХСН, т. е. при схождении отеков, исчезновении приступов сердечной астмы.
2. Перед назначением БАБ должны быть подобраны адекватные дозы иАПФ и диуретиков.
3. При ХСН разрешено применение только 4-х БАБ: метопролола сукцината (форма ЗОК), карведилола, бисопролола и небиволола.
4. Лечение БАБ должно начинаться осторожно, с 1/8 терапевтической дозы (для метопролола-ЗОК – 12,5 мг 1 р./сут, для карведилола – 3,125 мг 2 р./сут, для бисопролола и небиволола – 1,25 мг 1 р./сут).
5. Дозы БАБ следует увеличивать очень медленно (не чаще 1 раза в 2 недели, а при чрезмерном снижении АД – 1 р./мес.).
6. Дозы БАБ следует титровать до оптимальных, т. е. снижения ЧСС <70 уд./мин. На каждые 5 ударов снижения ЧСС достигается 18% снижения риска смерти больных c ХСН.
7. В первые 3–4 нед. использования БАБ может произойти усиление признаков ХСН из-за их отрицательного инотропного действия. Однако данное обстоятельство не должно служить основанием для отмены БАБ. В этих случаях следует вернуться к предыдущей дозе препарата и увеличить, при возможности, дозы иАПФ и диуретиков, а через несколько недель попытаться вновь увеличить дозу БАБ. Через 4–6 нед. применения БАБ при ХСН ФВ ЛЖ начинает повышаться вследствие снижения ЧСС и увеличения длительности диастолы, что ведет к восстановлению энергетических ресурсов миокарда. По способности снижать риск заболеваемости и смерти декомпенсированных больных с ХСН БАБ даже превосходят иАПФ [3].
При невозможности использования БАБ (бронхообструкция, атриовентрикулярная блокада выше I степени, тяжелое поражение периферических артерий, гипотония ниже 85 мм рт. ст.) может быть назначен при наличии синусового ритма и ЧСС >70 уд./мин ивабрадин [9]. Ивабрадин – селективный блокатор f-каналов синусового узла – урежает ЧСС без влияния на АД, нарушения ритма и проводимости, а также другие параметры. Ивабрадин снижает риск смерти или госпитализации больных на 29% при отсутствии серьезных побочных реакций. Он может быть использован совместно с БАБ. Ивабрадин неэффективен при наличии фибрилляции предсердий.
К препаратам 1-й группы, т. е. обязательно применяемым при ХСН, относятся также БМКР или спиронолактоны, имеющие уровень доказательности IA [10]. При декомпенсации тяжелой ХСН и необходимости применения петлевых и тиазидных диуретиков спиронолактон успешно применяется в дозе 100–300 мг/сут. При достижении компенсации ХСН доза спироналактона как дополнительного нейромодулятора и антифибротического средства снижается до 25–50 мг/сут. Длительное применение спироналактона чревато развитием гинекомастии или аменореи (до 10% случаев), гиперкалиемии (20%) и ухудшением функции почек.
Ситуация изменилась с появлением нового высокоселективного БМКР эплеренона, не оказывающего влияния на андрогеновые и прогестероновые рецепторы и реже провоцирующего ухудшение функции почек и гиперкалиемию в сравнении со спироналактоном. 30–дневное применение эплеренона в дозе 25–50 мг позволило снизить риск внезапной смерти у больных, перенесших инфаркт миокарда, на 21%, а риск общей смертности – на 15% [9]. Способность уменьшать выраженность фиброза миокарда при приеме эплеренона сопровождается ростом ФВ и снижением развития ФП при ХСН на 42%. Следует помнить, что при уровне креатинина >130 мкмоль/л и гиперкалиемии >5,2 ммоль/л сочетание спиронолактонов или БМКР с иАПФ/БРА требует необходимости контроля калия, креатинина, СКФ не менее 1–2 р./нед.
Препараты, применяемые по особым показаниям. К этой группе препаратов относятся БРА (сартаны), диуретики, гликозиды, ивабрадин и w-3-полиненасыщенные жирные кислоты. О применении БРА и ивабрадина при ХСН идет речь в предыдущем разделе. Существенным изменением позиции в отношении диуретиков, согласно последним рекомендациям, является их применение на более ранних стадиях ХСН. В частности, не с III ФК, а со II ФК (IIА стадии). Алгоритм назначения диуретиков представляется следующим [1]:
I ФК – не лечить диуретиками.
II ФК без клинических признаков застоя – малые дозы торасемида (2,5–5 мг 1 р./сут).
II ФК с признаками застоя – петлевые (тиазидные) диуретики + спиронолактон 100–150 мг.
III ФК (поддерживающее лечение) – торасемид + БМКР или спиронолактон (25–50 мг/сут) + ингибитор карбоангидразы (ИКАГ) диакарб (по 0,25 мг 3 р./сут в течение 3–4 дней 1 раз в 2 нед.).
III ФК (декомпенсация) – торасемид + тиазидные диуретики + спиронолактон 100–300 мг/сут + ИКАГ.
IV ФК – торасемид однократно или фуросемид 2 р./сут или в/в капельно в высоких дозах + тиазидные диуретики + БМКР или спиронолактоны + ИКАГ (диакарб по 0,25 мг 3 р./сут 3–4 дня 1 раз в 2 недели) + при необходимости механическое удаление жидкости.
Дегидрационная терапия при ХСН имеет 2 фазы: активную в период застоя и отеков и поддерживающую – при состоянии компенсации. В активной фазе превышение количества выделенной жидкости над принятой должно составлять 0,8–1 л/сут при снижении веса ежедневно ≈ на 1 кг. В поддерживающей фазе масса тела должна быть стабильной при ежедневном назначении мочегонных. Применение диуретиков всегда должно сочетаться с приемом иАПФ/БРА и БМКР.
Показанием для назначения гликозидов (дигоксина) является постоянная форма фибрилляции предсердий или наличие синусового ритма с ФВ <40%. Дигоксин должен всегда применяться в малых дозах – 0,125–0,25 мг/сут. При СКФ <60 мл/мин, особенно в пожилом возрасте, доза дигоксина должна быть снижена вдвое (1/4–1/2 таблетки). Предпочтительно сочетание приема дигоксина с БАБ. При этом лучше контролируется ЧСС и снижается риск опасных для жизни желудочковых нарушений ритма.
Применение w-3-полиненасыщенных жирных кислот является показанным при ХСН и перенесенном инфаркте миокарда, что снижает риск общей смерти на 41%, внезапной смерти – на 45% [10].
Препараты, применяемые в особых клинических ситуациях. К этой группе препаратов относятся антикоагулянты, дезагреганты, статины и триметазидин. Для предотвращения тромбозов и эмболий у больных с ХСН, находящихся на постельном режиме, эффективным является применение эноксапарина по 40 мг/сут в течение 2 нед. При наличии фибрилляции предсердий у больных с ХСН или наличии тромбов в полостях сердца у больных с синусовым ритмом применяются варфарин (международное нормализованное отношение в пределах 2–3) либо новые антикоагулянты. Дезагреганты и статины применяются в основном у больных с ИБС и собственно на ХСН существенного влияния не оказывают. Длительное использование триметазидина МВ (1,5–2 года) при ишемической этиологии ХСН позволяет снизить риск госпитализаций на 50%, а риск смерти и обострения ХСН – на 11,4% [11].
Профилактика ХСН. Нормализация АД позволяет на 50% снижать риск развития ХСН. Имеются неопровержимые данные о предотвращении ХСН при применении иАПФ. Статины рекомендуются в качестве профилактики ХСН у больных с ИБС. Наличие СД предрасполагает к развитию ХСН. иАПФ/БРА уменьшают, с одной стороны, риск развития СД, а с другой – вероятность развития ХСН у больных с СД [12]. При наличии клапанных пороков сердца лучшим средством профилактики и лечения ХСН является оперативное лечение.
Литература
1. Национальные рекомендации ОССН, РКО и РНМОТ по диагностике и лечению ХСН (четвертый пересмотр) // Сердечная недостаточность. 2013. Т. 81. № 7. С. 379–472.
2. Фомин И.В. Эпидемиология хронической сердечной недостаточности в Российской Федерации. В кн.: Хроническая сердечная недостаточность. М.: ГЭОТАР-Медиа, 2010. С. 7–77.
3. Беленков Ю.Н., Мареев В.Ю., Агеев Ф.Т. Хроническая сердечная недостаточность. М.: ГЭОТАР-Медиа, 2006. 532 с.
4. Madias J. Why recording of an ECG should be required in every inpatient and outpatient encounter of patients with heart failure // Pacing Clin. Electrophysiol. 2011. Vol. 34 (8). P. 963–967.
5. Fonseca C. Diagnosis of heart failure in primary care // Heart Fail. Rev. 2006. Vol. 11(2). P. 95–107.
6. Lang R., Badano L., Tsang W. et al. EAE/ASE Recommendations for Image Acquisition and Display Using Three-Dimensional Echocardiography // Eur. Heart J. Cardiovasc. Imaging. 2012. Vol. 13 (1). P. 1–46.
7. Paulus W., Tschope C., Sanderson J. et al. How to diagnose diastolic heart failure? // Eur. Heart J. 2007. Vol. 28 (20). P. 2539–2550.
8. Маслова А.П., Либис Р.А. Диастолическая дисфункция левого желудочка при сочетании хронической сердечной недостаточности и постоянной формы фибрилляции предсердий // Сердечная недостаточность. 2012. Т. 13, № 4. С. 205–208.
9. Swedberg K., Komajda M., Bohm М. et al. Ivabradine and outcomes in chronic heart failure (SHIFT) // Lancet. 2010. Vol. 376 (9744). P. 875–885.
10. Swedberg K., Zannad F., McMurray J.J. et al. Eplerenone and atrial fibrillation in mild systolic heart failure // J. Am. Coll. Cardiol. 2012. Vol. 59 (18). P. 1598–1603.
11. Fragasso G., Rosano G., Baek S.H. et al. Effect of partial fatty acid oxidation inhibition with trimetasidine on mortality and morbidity in heart failure // Int. J. Cardiol. 2013. Vol. 63 (3). P. 320–325.
12. Лапина Ю.В., Нарусов О.Ю., Мареев В.Ю. и др. Рациональная эффективная многокомпонентная терапия в борьбе с сахарным диабетом у больных ХСН // Сердечная недостаточность. 2007. Т. 8, № 4. С. 164–170.












