Ишемия миокарда, острая или хроническая, запускает целый ряд драматических событий в сердце, получивших в последнее время название сердечно-сосудистый континуум. Так, острая ишемия миокарда, если она не приводит к острой коронарной смерти, провоцирует появление обширной зоны асинергии миокарда, что наряду с активацией ренин-ангиотензин-альдостероновой и симпато-адреналовой систем вызывает ремоделирование левого желудочка (он становится более сферичным и тонкостенным), развитие сердечной недостаточности, инвалидизацию и смерть пациента. Хроническая ишемия миокарда, в свою очередь, вызывает развитие диффузного кардиосклероза, ремоделирование сердца с развитием ишемической кардиомиопатии, инвалидизацию и смерть пациента (аритмическую или от прогрессирования сердечной недостаточности.)
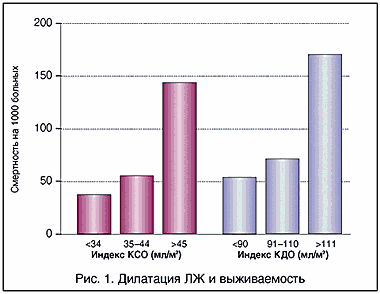
Рис. 1. Дилатация ЛЖ и выживаемость

Рис. 2. Выживаемость больных ХСН в подгруппах с КДР ЛЖ <= 5,5 см и > 5,5 см
Таким образом, формирование зоны асинергии миокарда и ее протяженность существенно влияют на течение заболевания и судьбу больного. Как показало исследование Hammermeister K.E. et al.,1979, смертность больных, перенесших инфаркт миокарда с развитием сердечной недостаточности, находится в тесной корреляции с индексом конечного систолического и конечного диастолического объемов левого желудочка (рис. 1). В отделе сердечной недостаточности института кардиологии имени А.Л. Мясникова на основании длительного (до двадцати лет) наблюдения показано, что шестилетняя выживаемость пациентов с диастолическим размером левого желудочка менее 5,5 см на 100% выше, чем у больных с дилатацией левого желудочка более 5,5 см (рис. 2). То же самое относится и к насосной функции левого желудочка. У пациентов с фракцией выброса левого желудочка более 50% риск смерти ниже на 28% по сравнению с больными, имеющими сниженную функцию желудочка (рис. 3).

Рис. 3. Выживаемость больных ХСН в подгруппах с сохраненной и со сниженной сократимостью ЛЖ
Что же происходит с миокардом при его ишемии? Достаточно упрощенно это представлено на рис. 4. Как видно, нарушение баланса между поступлением кислорода и потребности в нем миокарда приводит к некрозу примерно трети объема кардиомиоцитов. Примерно 45% кардиомиоцитов сохраняют свою жизнеспособность, однако находятся в состоянии компенсаторного гиперкинеза и гипертрофии. Кроме того, они электрически нестабильны. Наибольший интерес представляют 25% кардиомиоцитов, которые активно не сокращаются, но сохраняют минимальное потребление кислорода и основные компоненты клеточного метаболизма, то есть они «живы», но находятся как бы в резерве.
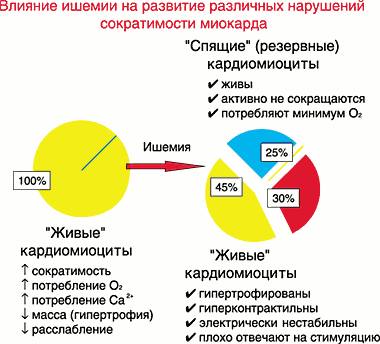
Рис. 4
Для обозначения подобных участков миокарда были предложены различные термины, в зависимости от степени и длительности ишемии и выраженности структурно-метаболических изменений. Наиболее распространенными являются:Оглушенный (Stunned) миокард (Braunvald Е. 1982). Браунвальд определил его, как запаздывание восстановления региональной дисфункции миокарда после острого периода ишемии, сопровождающегося последующей реперфузией. При этом повреждение миокарда зависит как от самого эпизода ишемии, так и от постишемической реперфузии. Длительная ишемия, по мнению Rahimtoola S.H.et al. 1985, приводит к появлению Спящего (Hibernating) миокарда – явления, скорее, компенсаторно-приспособительного к хронической нехватке кислорода даже в состоянии покоя. Но что наиболее важно, эти виды диссинергии миокарда, по данным Rozanski A.et al. 1981, носят обратимый характер как при восстановлении кровотока, так и при нормализации баланса поступление/потребление миокардом кислорода. Дальнейшие исследования позволили объединить оба эти состояния термином Жизнеспособный (Viable) миокард. При этом данные участки миокарда являются гипо- или акинетичными, но сохраняют определенный уровень метаболизма и резерв сократимости. Кроме того, как было сказано выше, их функция может быть восстановлена инструментально или медикаментозно.
Сразу воникает вопрос. Можем ли мы надежно выявлять жизнеспособный миокард у конкретного пациента? Ответ положительный, причем неинвазивно и с помощью аппаратуры, которая имеется во всех специализированных кардиологических стационарах. Наиболее часто для этого применяется введение синтетического b1–стимулятора - добутамина, который в небольших дозах способен повышать сократимость миокарда в этих регионах без существенного повышения частоты сердечных сокращений. Единый протокол введения препарата начинается с малых доз (5-10 мкг/кг/мин по 3 минуты каждая ступень). Доза увеличивается либо до появления признаков жизнеспособного миокарда, либо, при его отсутствии, до появления стандартных критериев прекращения любой пробы при ИБС (развитие приступа стенокардии, ишемическая динамика на ЭКГ, появление угрожающих нарушений ритма сердца, выходящее за критерии протокола повышение или снижение артериального давления и т.д.).
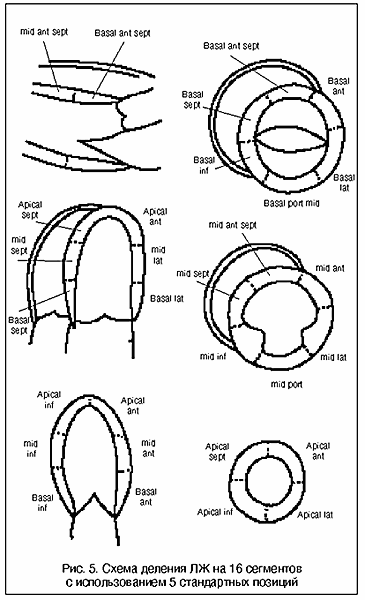
Рис. 5. Схема деления ЛЖ на 16 сегментов с использованием 5 стандартных позиций
При использовании в качестве метода контроля эхокардиографии оценка изменений локальной сократимости проводится по пятибальной шкале где: 1-нормокинезия; 2-гипокинезия; 3-акинезия; 4-дискинезия; 5-аневризматическое нарушение сократимости по данным стресс-эхокардиографии. Для унификации определения различных участков миокарда наиболее предпочтительна 16-ти сегментарная модель (рис. 5), рекомендованная Американским эхокардиографическим обществом. Используются шесть стандартных позиций: длинная, 3 коротких парастернальных - на уровне створок митрального клапана, папиллярных мышц и верхушки, 4-х камерная верхушечная и 5-ти камерная. Для каждого больного рассчитывается индекс асинергии (сумма баллов, разделенная на общее количество сегментов). Жизнеспособными считались сегменты с улучшением показателей более чем на 1 балл. Проба по выявлению жизнеспособного миокарда считалась отрицательной при отсутствии прироста или ухудшении сократимости.

Рис. 6. Выраженность нарушений перфузии миокарда у больных ИБС с недостаточностью кровообращения по данным сцинтиграфии миокарда с Tl201
4 - отсутствие включения Tl201; 3 - выраженный дефект перфузии; 2 - умеренный дефект перфузии; 1 - незначительный дефект перфузии; 0 - нормальное распределение Tl201
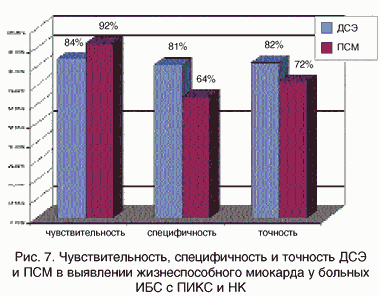
Рис. 7. Чувствительность, специфичность и точность ДСЭ и ПСМ в выявлении жизнеспособного миокарда у больных ИБС с ПИКС и НК

Рис. 8. Чувствительность, специфичность и точность комбинации ДСЭ и ПСМ в выявлении жизнеспособного миокарда у больных ИБС с ПИКС и НК
При использовании перфузионной сцинтиграфии с Tl201 (планарная в трех стандартных проекциях и однофотонная эмиссионная томография) протокол включает визуализацию миокарда через 5–10 минут после внутривенного введения 55 МБк Tl201 при проведении пробы с Дипиридамолом (0.56 мг/кг/4 мин), визуализацию отсроченных сцинтиграмм с оценкой перераспределения таллия в миокарде через 4 часа и через 10-20 минут после повторного введения 28 МБк Tl201. Оценка проводится по пятибальной шкале: 0 - нормальное распределение изотопа, 1 - незначительный дефект перфузии, 2 - умеренный дефект перфузии, 3 - выраженный дефект перфузии, 4 - отсутствие включения изотопа. Для каждого больного возможно вычисление индекса нарушения перфузии миокарда, как суммы баллов исследуемых сегментов, деленной на количество сегментов. Жизнеспособность миокарда определяется по увеличению накопления изотопа как на отсроченных изображениях, так и при повторном его введении. Исследования М.А. Саидовой с соавт., 1998, проведенные в нашем институте, показали, что у больных с жизнеспособным миокардом нормальное распределение изотопа повысилось через 4 часа с 0 до 38%, а при повторном введении до 51%. В группе больных без жизнеспособного миокарда показатели составили соответственно 8 и 11 % (рис. 6). Сопоставление данных вышеописанных методов с результатами, полученными после успешной реваскуляризации, показало высокую чувствительность, специфичность и точность в выявлении жизнеспособного миокарда как добутаминовой стресс-эхокардиографии (ДСЭ), так и перфузионной сцинтиграфии миокарда (ПСМ), причем первая имела большую специфичность и точность, вторая - чувствительность (рис. 7). Поэтому можно рекомендовать сочетанное применение этих двух методов (рис. 8), что существенно улучшает диагностические возможности, так как диагностика основана на различных признаках жизнеспособности: ДСЭ - на выявлении резерва сократимости; ПСМ - на диагностике состояния мембран кардиомиоцитов.В качестве методов контроля при добутаминовой пробе могут быть использованы и другие методы (МР-томография, электронно-лучевая томография). Но они либо очень дороги, а потому малодоступны, либо инвазивны, как, например, рентгеноконтрастная вентрикулография. Несомненные преимущества, с точки зрения диагностики, имеет позитронно-эмиссионная томография, которая позволяет непосредственно оценить потребление кислорода и метаболизм гипокинетичных кардиомиоцитов.Однако этот метод чрезвычайно дорогостоящий и требует наличия короткоживущих изотопов.

Рис. 9

Рис. 10. Изменение показателей внутрисердечной гемодинамики, ФК НК, ИА и ИНПМ у больных ИБС на фоне хирургической реваскуляризации и медикаментозной терапии
Знание закономерностей функционирования жизнеспособного миокарда и достаточно надежная неинвазивная его диагностика позволяют разрабатывать оптимальную тактику ведения пациентов, перенесших инфаркт миокарда и имеющих нарушение функции левого желудочка. В достаточно схематической форме это отражено на рисунке 9. Как видно, бесспорным преимуществом обладают методы прямой реваскуляризации (как хирургические, так и эндоваскулярные). Они позволяют вернуть к нормальному сокращению практически все жизнеспособные кардиомиоциты. Однако данные методы, к сожалению, достаточно дороги, требуют наличия высокотехнологического оборудования и подготовленного персонала. Поэтому большая часть пациентов получает то или иное медикаментозное лечение. На рисунке показано, что мы можем надеяться на успешное восстановление функции части резервных (жизнеспособных) кардиомиоцитов. Посмотрим, как это происходит в реальной практике (рис.10). Если разделить всех пациентов с ишемической дисфункцией левого желудочка на две большие группы: прошедшие аорто-коронарное шунтирование и получавшие только то или иное современное медикаментозное лечение, то повышение фракции выброса левого желудочка (ФВ), снижение объемов левого желудочка в диастолу и систолу (КДО, КСО), уменьшение функционального класса недостаточности кровообращения (ФКНК), а также индексов асинергии и нарушения перфузии миокарда (ИА, ИНПМ), в достоверно большей степени происходило у пациентов, прошедших хирургическую реваскуляризацию. Однако, как видно, и у пациентов, получавших только лекарственное лечение, также отмечалось улучшение показателей, но в значительно меньшей степени. Давайте рассмотрим, какими классами препаратов мы можем воздействовать на жизнеспособный миокард. Первое, что приходит в голову, - использовать позитивные инотропные средства, тем более, что диагностика жизнеспособного миокарда осуществляется с помощью одного из них (добутамин). На рисунке 11 представлен ответ на инотропную стимуляцию (в данном случае сердечными гликозидами) живых и жизнеспособных кардиомиоцитов. Как видно, немедленной реакцией является повышение сократимости, что проявляется в увеличении сердечного выброса, однако это происходит с увеличением потребления миокардом кислорода и некоторым ухудшением расслабления миокарда. То есть внешне реакция хоть и не самая выгодная, но положительная. При длительном же использовании позитивных инотропных средств, к сожалению, происходят крайне противоположные события. Часть живых кардиомиоцитов за счет снижения сократительного резерва переходит в разряд жизнеспособных, а часть живых и жизнеспособных кардиомиоцитов из-за полного исчерпания резервов метаболизма и сократимости подвергаются програмируемой гибели (апоптозу), что увеличивает объем безвозвратно утраченного миокарда, существенно ухудшает гемодинамику и прогноз пациентов.

Рис. 11

Рис. 12. Изменение показателей центральной гемодинамики, ФКНК, региональной сократимости и перфузии миокарда у больных ИБС с наличием (1 гр.) и отсутствием (2 гр.) жизнеспособного миокарда на фоне терапии карведилолом

Рис. 13. Изменение показателей центральной гемодинамики, ФКНК, региональной сократимости и перфузии миокарда у больных ИБС с наличием (1 гр.) и отсутствием (2 гр.) жизнеспособного миокарда на фоне терапии эналаприлом
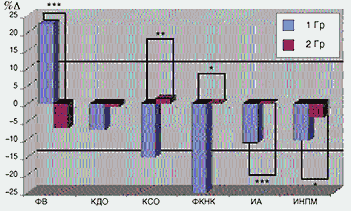
Рис. 14. Изменение показателей центральной гемодинамики, ФКНК, региональной сократимости и перфузии миокарда у больных ИБС с наличием (1 гр.) и отсутствием (2 гр.) жизнеспособного миокарда на фоне терапии комбинацией эналаприла с бисопрололом
Обратимся к другим классам препаратов. Как показали иследования, выполненные в нашем институте (М.А. Саидова, 1999), если разделить пациентов, получающих медикаментозное лечение, на группы с наличием и отсутствием жизнеспособного миокарда, использование препарата карведилол, обладающего b-блокирующими, в меньшей степени a-блокирующими свойствами, а также некоторой антиоксидантной активностью, позволяет существенно улучшить показатели функции левого желудочка и клиническое состояние больных, имеющих жизнеспособный миокард (рис. 12). Использование ингибиторов АПФ, в частности, эналаприла (рис. 13), также позволяет улучшить состояние больных, имеющих жизнеспособный миокард, однако в несколько меньшей степени, чем при использовании бета-блокаторов. Наиболее целесообразно использование комбинации ингибитор АПФ и b-блокатор (рис. 14). Как видно, прием эналаприла и бисопролола в наибольшей степени увеличивает фракцию выброса левого желудочка и улучшает функциональный класс недостаточности кровообращения. Это вполне объяснимо, так как суммируются положительные эффекты b-блокаторов (нормализация потребления миокардом кислорода за счет более экономной работы сердца, нейромодулирующее действие на САС) и ингибиторов АПФ (периферическое разгрузочное действие, нейромодулирующее действие на РААС).
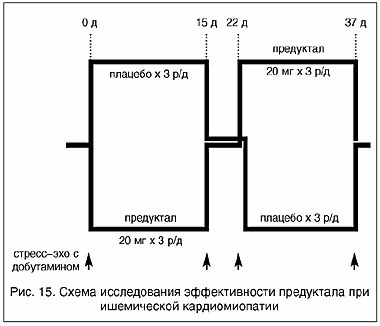
Рис. 15. Схема исследования эффективности предуктала при ишемической кардиомиопатии
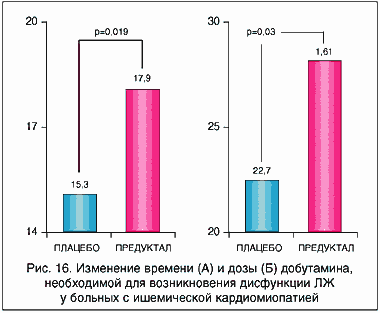
Рис. 16. Изменение времени (А) и дозы (Б) добутамина, необходимой для возникновения дисфункции ЛЖ у больных с ишемической кардиомиопатией

Рис. 17. Снижение индекса асинхронии сокращений ЛЖ у больных с ишемической кардиомиопатией
Еще один препарат достаточно интенсивно изучается, как эффективный компонент в комплексной терапии больных с жизнеспособным миокардом - это триметазидин (Предуктал). Он обладает комплексным антиангинальным, антигипоксическим и цитопротекторным действием. Активирует окислительное декарбоксилирование, нормализует потребление кислорода за счет усиления аэробного гликолиза и блокады окисления жирных кислот, уменьшает внутриклеточный ацидоз, обладает антиоксидантным действием. За последнее время проведено несколько клинических испытаний препарата. В одном из них, Shunzeng L.U. et.al 1997 (рис. 15), больные с ишемической кардиомиопатией в двойном слепом плацебоконтролируемом исследовании были разделены на две группы: одна в добавление к стандартной терапии получала 20 мг предуктала три раза в день, другая - плацебо. После 15 дней лечения был недельный перерыв на выведение препарата, затем производился кроссовер, то есть препарат и плацебо в группах менялись, и снова проводилось лечение в течение 15 дней. В начале и в конце каждого этапа проводилась стресс-эхо кардиография с добутамином. Было показано (рис. 16), что у больных, получавших предуктал, по сравнению с плацебо достоверно возрастали время нагрузки и доза добутамина, необходимые для возникновения дисфункции левого желудочка. У больных получавших предуктал также достоверно снижался индекс асинхронии сокращения левого желудочка как в покое, так и на высоте введения добутамина (рис. 17).

Рис. 18. Оптимальная тактика ведения больных с ИБС
Резюмируя вышесказанное, можно предложить следующий алгоритм обследования и ведения пациентов с ИБС, имеющих локальные нарушения сократимости миокарда, снижение фракции выброса левого желудочка, в том числе и с клиническими проявлениями ранних стадий сердечной недостаточности (рис. 18). Все они должны пройти процедуру диагностики наличия жизнеспособного миокарда с использованием методик, применяющихся в данном специализированном стационаре. В случае выявления жизнеспособного миокарда они должны пройти ту или иную процедуру реваскуляризации (АКШ, ангиопластика), либо, при невозможности радикального вмешательства, медикаментозное лечение (ингибиторами АПФ, бета-блокаторами, триметазидином). И в том и в другом случае могут быть обеспечены хороший клинический эффект и благоприятный прогноз на выживание. При этом положительное воздействие реваскуляризации или медикаментозного лечения может быть значительно шире, нежели просто усиление сократимости акинетичных ранее сегментов. Например, усиление кровотока в эпикардиальных слоях жизнеспособного миокарда при мелкоочаговом инфаркте миокарда не изменит и так сохранившуюся сократительную способность, но будет предотвращено возможное ремоделирование левого желудочка, обеспечена большая электрическая стабильность миокарда, то есть будут предотвращены жизненно опасные аритмии. Если у пациента не выявлено жизнеспособного миокарда, то проведение АКШ или ангиопластики тоже возможно – для уменьшения клинических проявлений заболевания, в частности, стенокардии напряжения, – это позволит даже несколько улучшить качество жизни больного, при этом врач должен четко представлять, что даже удачно проведенная операция не изменит неблагоприятного прогноза пациента. Это же касается и симптоматиче ского медикаментозного лечения, способного дать лишь кратковременное клиническое улучшение. Как помочь этой самой тяжелой категории больных? В настоящее время единственной реальной альтернативой пессимистическому прогнозу является трансплантация сердца. Промежуточным и, как показывают клинические наблюдения последних лет, достаточно длительным этапом может стать имплантация искусственного левого желудочка в обход имеющегося. В перспективе, и может быть, не столь отдаленной, это будет подсадка в сердце генетически измененных собственных стволовых клеток для обеспечения роста новых кардиомиоцитов, а также стимуляция неоангиогенеза как с использованием медикаментозных средств или нейрогуморальных медиаторов, так и физических воздействий, например, прерывистой ишемии (прекондиционирования).
Список литературы Вы можете найти на сайте http://www.rmj.ru
Триметазидин –
Предуктал (торговое название)
(Servier)
1. Саидова М.А., Беленков Ю.Н., Атьков О.Ю., и др. Исследование жизнеспособности миокарда у больных ишемической болезнью сердца с выраженной дисфункцией левого желудочка и хронической недостаточностью кровообращения. Кардиология № 6: 20–4, 1998.
2. Саидова М.А. Возможности медикаментозного и хирургического восстановления сократимости жизнеспособного миокарда у больных ИБС и ДКМП с хронической недостаточностью кровообращения.
Автореферат докторской диссертации, М., 1999.
3. Rozanski A., Berman DS, Gray R., et al. Use of thallium -201 redistribution scintigraphy in the preoperative differentiation of reversible and nonreversible asynergy/Circulation. 1981; 64: 936–44.
3. Braunvald E., Kloner RA., The stunned myokardium: Prolonged, postishemic ventricular disfunction. Circulation. 1982; 66: 1146–9.
4. Rahimtoola SH. A perspective on the three large multicenter randomized clinical trials of coronary bypass surgery for chronic stable angina. Circulation. 1985; 72 (V): 123–35.








.gif)



