–Р—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–Њ–љ–Є—П (–Р–У) —П–≤–ї—П–µ—В—Б—П —Б–∞–Љ—Л–Љ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ, –і–ї—П –ї–µ—З–µ–љ–Є—П –Ї–Њ—В–Њ—А–Њ–≥–Њ –Є–Љ–µ–µ—В—Б—П –±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤. –Ю—В—З–µ—В–ї–Є–≤–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Є–љ—Б—Г–ї—М—В–Њ–≤, –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –љ–µ—Б–Њ–Љ–љ–µ–љ–љ—Л—Е —Г—Б–њ–µ—Е–∞—Е —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є –Р–У. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ —Е–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–є –Ї–Њ–љ—В—А–Њ–ї—М –Р–У –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –Ї—А–∞–є–љ–µ —А–µ–і–Ї–Њ. –Ы—Г—З—И–Є–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –Р–Ф –њ—А–Є –Р–У –і–Њ—Б—В–Є–≥–љ—Г—В –≤ –°–®–Р –Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В –≤—Б–µ–≥–Њ 27% [1]. –Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ –і—А—Г–≥–Є—Е —А–µ–≥–Є–Њ–љ–Њ–≤ –Њ–љ –Ї–Њ–ї–µ–±–ї–µ—В—Б—П –≤ –њ—А–µ–і–µ–ї–∞—Е 5–10%. –Т 1989 –≥–Њ–і—Г –і–∞–љ–љ—Л–µ Glasgow Blood Pressure Clinic –њ–Њ–і—В–≤–µ—А–і–Є–ї–Є, —Б –Њ–і–љ–Њ–є —Б—В–Њ—А–Њ–љ—Л, –і–Њ–Љ–Є–љ–Є—А—Г—О—Й—Г—О —А–Њ–ї—М –і–Њ—Б—В–Є–≥–љ—Г—В–Њ–≥–Њ –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Г—А–Њ–≤–љ—П –Р–Ф –≤ –њ—А–Њ–≥–љ–Њ–Ј–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–У, —Б –і—А—Г–≥–Њ–є – —Б–Њ—Е—А–∞–љ–µ–љ–Є–µ –њ–Њ–≤—Л—И–µ–љ–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є –Є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –њ—А–Є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –µ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П. –Я–Њ–Ј–ґ–µ —Н—В–Є –њ–Њ–ї–Њ–ґ–µ–љ–Є—П –±—Л–ї–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ—Л –Є —А–∞–Ј–≤–Є—В—Л –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Э–Ю–Ґ [2]. –Ъ —З–Є—Б–ї—Г –≤—Л–і–∞—О—Й–Є—Е—Б—П —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ —Н—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ—В–љ–Њ—Б–Є—В—Б—П –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Ж–µ–ї–µ–≤–Њ–≥–Њ –Ф–Р–Ф < 90 –Љ–Љ —А—В.—Б—В. –±–Њ–ї–µ–µ —З–µ–Љ —Г 90% –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–Р–У –ї–Є–і–Є—А—Г–µ—В –љ–µ —В–Њ–ї—М–Ї–Њ –њ–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є, –љ–Њ –Є –њ–Њ –Ј–∞—В—А–∞—В–∞–Љ –љ–∞ –µ–µ –ї–µ—З–µ–љ–Є–µ. –Ъ –њ—А–Є–Љ–µ—А—Г, 20–40% –≤—Б–µ—Е –∞–Љ–±—Г–ї–∞—В–Њ—А–љ—Л—Е –≤–Є–Ј–Є—В–Њ–≤ –Ї –≤—А–∞—З–∞–Љ —Б–≤—П–Ј–∞–љ—Л —Б –Р–У [3]. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–є —Н—В–∞–њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В –∞–љ–∞–ї–Є–Ј —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є. –Э–µ–і–∞–≤–љ–Њ –Ј–∞–≤–µ—А—И–Є–≤—И–Є–µ—Б—П —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤—Л—П–≤–Є–ї–Є, —З—В–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–µ –Ј–∞—В—А–∞—В—Л –њ–Њ –ї–µ—З–µ–љ–Є—О –Р–У —Б–≤—П–Ј–∞–љ–љ—Л —Б –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Р–Ф, –љ–Є–Ј–Ї–Њ–є –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В—М—О –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї –ї–µ—З–µ–љ–Є—О –Є –Њ—Б–Њ–±–µ–љ–љ–Њ —Д–µ–љ–Њ–Љ–µ–љ–Њ–Љ «—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є —В—Г—А–±—Г–ї–µ–љ—В–љ–Њ—Б—В–Є –Є–ї–Є –љ–µ—А–∞–Ј–±–µ—А–Є—Е–Є», –Ї–Њ—В–Њ—А—Л–є –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ –њ—А–µ—А—Л–≤–∞–љ–Є–Є –Є —Б–Љ–µ–љ–µ —А–µ–ґ–Є–Љ–Њ–≤ –Є –і–Њ–Ј –ї–µ—З–µ–љ–Є—П [3,4]. –Я–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л–Љ –њ–Њ–і—Е–Њ–і–Њ–Љ –і–ї—П —Г–ї—Г—З—И–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є, –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Є –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —П–≤–ї—П–µ—В—Б—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –љ–Є–Ј–Ї–Њ–і–Њ–Ј–Њ–≤—Л—Е —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е —Б—А–µ–і—Б—В–≤.
–Ъ–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–є —А–µ–ґ–Є–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е —Б—А–µ–і—Б—В–≤ –≤—Б–µ–≥–і–∞ –њ—А–Є—Б—Г—В—Б—В–≤–Њ–≤–∞–ї –≤ –∞—А—Б–µ–љ–∞–ї–µ —Б—А–µ–і—Б—В–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П –Р–У. –Ю–і–љ–∞–Ї–Њ –≤–Ј–≥–ї—П–і—Л –љ–∞ –Љ–µ—Б—В–Њ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤ –ї–µ—З–µ–љ–Є–Є –Р–У –љ–µ–Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ –њ–µ—А–µ—Б–Љ–∞—В—А–Є–≤–∞–ї–Є—Б—М. –Я–µ—А–≤—Л–µ —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ–Њ—П–≤–Є–ї–Є—Б—М –≤ –љ–∞—З–∞–ї–µ 1960-—Е –≥–Њ–і–Њ–≤. –Ю–љ–Є –±—Л–ї–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л —Б–ї–µ–і—Г—О—Й–Є–Љ–Є —Б–Њ—Б—В–∞–≤–∞–Љ–Є: —А–µ–Ј–µ—А–њ–Є–љ + –≥–Є–і—А–∞–ї–∞–Ј–Є–љ + –≥–Є–і—А–Њ—Е–ї–Њ—А–Њ—В–Є–∞–Ј–Є–і; a––Љ–µ—В–Є–ї–і–Њ–њ–∞ + –≥–Є–і—А–Њ—Е–ї–Њ—А–Њ—В–Є–∞–Ј–Є–і; –≥–Є–і—А–Њ—Е–ї–Њ—А–Њ—В–Є–∞–Ј–Є–і + –Ї–∞–ї–Є–є—Б–±–µ—А–µ–≥–∞—О—Й–Є–µ –і–Є—Г—А–µ—В–Є–Ї–Є. –Т 70-–µ –Є 80-–µ –≥–Њ–і—Л –≤–µ–і—Г—Й–µ–µ –Љ–µ—Б—В–Њ –Ј–∞–љ—П–ї–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –і–Є—Г—А–µ—В–Є–Ї–∞, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –≤ –≤—Л—Б–Њ–Ї–Њ–є –і–Њ–Ј–µ, —Б b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є –Є–ї–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–≥–Њ —В–Є–њ–∞ –і–µ–є—Б—В–≤–Є—П. –° –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –љ–Њ–≤—Л—Е –Ї–ї–∞—Б—Б–Њ–≤ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ–Њ–њ—Г–ї—П—А–љ–Њ—Б—В—М –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М. –Т —Б–µ—А–µ–і–Є–љ–µ 80-—Е –≥–Њ–і–Њ–≤ –і–Њ–Љ–Є–љ–Є—А–Њ–≤–∞–ї–∞ —В–∞–Ї—В–Є–Ї–∞ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≤—Л–±–Њ—А–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є—Е –≤ —А–µ–ґ–Є–Љ–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є. –Ъ–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —В–µ—А–∞–њ–Є—П —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–ї–∞—Б—М –љ–∞ –њ–Њ–Ј–і–љ–Є—Е —Н—В–∞–њ–∞—Е –ї–µ—З–µ–љ–Є—П. –Ь–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –≤ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л—Е –і–Њ–Ј–∞—Е —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–Њ—Б—М, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –≤ —А–∞–Ј–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є –Ї–Њ–љ—В—А—А–µ–≥—Г–ї—П—В–Њ—А–љ—Л—Е –Є–ї–Є –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –і–Є—Г—А–µ—В–Є–Ї–Њ–≤, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј–∞—Е, –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї –∞–Ї—В–Є–≤–∞—Ж–Є–Є —Б–Є–Љ–њ–∞—В–Њ–∞–і—А–µ–љ–∞–ї–Њ–≤–Њ–є –Є —А–µ–љ–Є–љ––∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ —Б –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є –≤–∞–Ј–Њ–њ—А–µ—Б—Б–Є–љ–∞; –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—В–Њ—А–Њ–≤ –Ї –∞–Ї—В–Є–≤–∞—Ж–Є–Є —Б–Є–Љ–њ–∞—В–Њ–∞–і—А–µ–љ–∞–ї–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л –Є –Ј–∞–і–µ—А–ґ–Ї–µ –ґ–Є–і–Ї–Њ—Б—В–Є –Є —В.–і. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Љ–∞—П—В–љ–Є–Ї –≤–µ—А–љ—Г–ї—Б—П –≤ –Є—Б—Е–Њ–і–љ–Њ–µ –њ–Њ–ї–Њ–ґ–µ–љ–Є–µ, —З—В–Њ –Њ–Ј–љ–∞—З–∞–µ—В –Њ–±—Й–µ–µ –њ—А–Є–Ј–љ–∞–љ–Є–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–У.
–Э–Њ–≤—Л–є –≤–Є—В–Њ–Ї –≤ –Є—Б—В–Њ—А–Є–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Њ–Ј–љ–∞–Љ–µ–љ–Њ–≤–∞–љ –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є, –љ–µ —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –і–Є—Г—А–µ—В–Є–Ї–∞ (–∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П (–Р–Ъ) + –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ (–Є–Р–Я–§); –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–µ –Р–Ъ + b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А—Л). –£–ґ–µ –≤ 1997 –≥–Њ–і—Г –≤ —Б–њ–Є—Б–Ї–µ –њ—А–Є–ї–∞–≥–∞–µ–Љ—Л—Е –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –і–Њ–Ї–ї–∞–і–µ –Ю–Э–Ъ YI [1] –±—Л–ї–Њ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ 29 —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л—Е –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ю–і–љ–∞–Ї–Њ –ї–Є—И—М –і–µ—Б—П—В–Є–ї–µ—В–Є–µ —Б–њ—Г—Б—В—П, –њ–Њ—Б–ї–µ –њ–Њ—П–≤–ї–µ–љ–Є—П –≤–µ—Б–Ї–Є—Е –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤ –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є –≤ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–≥–Њ –Р–Ф —Г –∞–±—Б–Њ–ї—О—В–љ–Њ–≥–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–У, –і–∞–љ–љ—Л–є –њ–Њ–і—Е–Њ–і –≤–љ–Њ–≤—М –њ–µ—А–µ–Љ–µ—Б—В–Є–ї—Б—П –љ–∞ –ї–Є–і–Є—А—Г—О—Й–Є–µ –њ–Њ–Ј–Є—Ж–Є–Є. –У–ї–∞–≤–љ—Л–Љ –љ–Њ–≤—И–µ—Б—В–≤–Њ–Љ —П–≤–ї—П–µ—В—Б—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –љ–Є–Ј–Ї–Њ–і–Њ–Ј–Њ–≤—Л—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є –≤ –Ї–∞—З–µ—Б—В–≤–µ —В–∞–Ї—В–Є–Ї–Є –њ–µ—А–≤–Њ–≥–Њ –≤—Л–±–Њ—А–∞. –≠—В–Њ—В –њ—А–Є–љ—Ж–Є–њ –Ј–∞–Ї—А–µ–њ–ї–µ–љ –≤ –њ–Њ—Б–ї–µ–і–љ–Є—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е –њ–Њ –Р–У –Ю–Э–Ъ YI, 1997, –Т–Ю–Ч––Ь–Ю–Р–У, 1999; –Ф–Р–У–1, 2000, ANAES 2000 (1,5–7), –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Ї–Њ—В–Њ—А—Л–Љ–Є –љ–Є–Ј–Ї–Њ–і–Њ–Ј–Њ–≤–∞—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–∞—П —В–µ—А–∞–њ–Є—П –Љ–Њ–ґ–µ—В –±—Л—В—М –Љ–µ—А–Њ–є –њ–µ—А–≤–Њ–≥–Њ –≤—Л–±–Њ—А–∞, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤ –Є—Б—В–Њ—А–Є–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Љ–Њ–ґ–љ–Њ –≤—Л–і–µ–ї–Є—В—М —Б–ї–µ–і—Г—О—Й–Є–µ —Н—В–∞–њ—Л: I – –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ —А–∞—Г–≤–Њ–ї—М—Д–Є–Є –Є/–Є–ї–Є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л –≤ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј–∞—Е; II – –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —А–µ–ґ–Є–Љ–Њ–≤, –Њ—Б–љ–Њ–≤–∞–љ–љ—Л—Е –љ–∞ –і–Є—Г—А–µ—В–Є–Ї–∞—Е –≤ –≤—Л—Б–Њ–Ї–Є—Е –Є–ї–Є —Б—А–µ–і–љ–Є—Е –і–Њ–Ј–∞—Е, –і–Њ–њ–Њ–ї–љ—П–µ–Љ—Л—Е b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є, –Ї–∞–ї–Є–є—Б–±–µ—А–µ–≥–∞—О—Й–Є–Љ–Є –і–Є—Г—А–µ—В–Є–Ї–∞–Љ–Є, –Є–Р–Я–§; III – –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є –±–µ–Ј –і–Є—Г—А–µ—В–Є–Ї–Њ–≤ (b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А—Л + –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–µ –Р–Ъ; –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–µ –Р–Ъ+ –Є–Р–Я–§; –љ–µ–і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–µ –Р–Ъ + –Є–Р–Я–§); IV – –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л—Е –љ–Є–Ј–Ї–Њ–і–Њ–Ј–Њ–≤—Л—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ –і–Є—Г—А–µ—В–Є–Ї–Є –≤ –Њ—З–µ–љ—М –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј–∞—Е (–≥–Є–і—А–Њ—Е–ї–Њ—А–Њ—В–Є–∞–Ј–Є–і 6,25–12,5 –Љ–≥; –Є–љ–і–∞–њ–∞–Љ–Є–і 0,625 –Љ–≥) [8–10].
–Ъ–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–∞—П —В–µ—А–∞–њ–Є—П: –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Є–µ, –Њ–±—Й–Є–µ –њ—А–Є–љ—Ж–Є–њ—Л, —В–∞–Ї—В–Є–Ї–∞
–Т –њ–µ—А–µ–Ї—А–µ—Б—В–љ—Л—Е —Е–Њ—А–Њ—И–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–∞ –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–∞—П –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–∞—П –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —А–∞–Ј–љ—Л—Е –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ю–і–љ–∞–Ї–Њ –њ–Њ–Є—Б–Ї –љ–∞–і–µ–ґ–љ—Л—Е –Ї—А–Є—В–µ—А–Є–µ–≤ –і–ї—П –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–≥–Њ –≤—Л–±–Њ—А–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Њ–Ї–∞–Ј–∞–ї—Б—П –±–µ–Ј—Г—Б–њ–µ—И–љ—Л–Љ. –° –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, –≤–њ–µ—З–∞—В–ї—П–µ—В —Д–∞–Ї—В –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є –Љ–Њ—Й–љ–Њ—Б—В–Є –≤—Б–µ—Е –Ї–ї–∞—Б—Б–Њ–≤ –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Т —А–µ–ґ–Є–Љ–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Њ–љ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 40–50% –њ–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—О, –Њ—В–≤–µ—В–Є–≤—И–Є—Е –љ–∞ –ї–µ—З–µ–љ–Є–µ [8–13]. –≠—В–Є –і–∞–љ–љ—Л–µ –µ—Й–µ —А–∞–Ј –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В –≥–µ—В–µ—А–Њ–≥–µ–љ–љ–Њ—Б—В—М —Б–Є–љ–і—А–Њ–Љ–∞ –Р–У. –Т–Њ–Ј–≤—А–∞—В –Ї —А–µ–ґ–Є–Љ—Г –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ–∞ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ —Н—В–∞–њ–µ –Љ–љ–Њ–≥–Є–µ —Б–≤—П–Ј—Л–≤–∞—О—В —Б —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –Љ–µ–≥–∞–Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Э–Ю–Ґ [2]. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М—О –≤ –і–Њ—Б—В–Є–ґ–µ–љ–Є–Є –љ–µ –њ—А–Њ—Б—В–Њ —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф, –∞ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –µ–≥–Њ —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П –і–ї—П —А–µ–∞–ї—М–љ–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —А–Є—Б–Ї–∞. –Ф–ї—П —А–µ—И–µ–љ–Є—П —Н—В–Њ–є –Ј–∞–і–∞—З–Є —В—А–µ–±—Г–µ—В—Б—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–∞—П —В–µ—А–∞–њ–Є—П 2/3 –њ–∞—Ж–Є–µ–љ—В–∞–Љ. –Ю–і–љ–∞–Ї–Њ –њ—А–Є —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ —Ж–Є—В–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ –Р–У, –≤–Ї–ї—О—З–∞—П —В–∞–Ї–Њ–≤—Л–µ –њ–Њ –Ї–Њ–љ–µ—З–љ—Л–Љ —В–Њ—З–Ї–∞–Љ, –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ —З–∞—Б—В–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –І–µ–Љ –љ–Є–ґ–µ —В—А–µ–±—Г–µ–Љ—Л–є —Г—А–Њ–≤–µ–љ—М —Ж–µ–ї–µ–≤–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П (–≥—А—Г–њ–њ—Л —Б —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –Є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О), —В–µ–Љ –±–Њ–ї—М—И–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —В—А–µ–±—Г–µ—В—Б—П –і–ї—П —А–∞–Ј—А–µ—И–µ–љ–Є—П —Н—В–Њ–є –Ј–∞–і–∞—З–Є. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ –Ї —З–Є—Б–ї—Г –Њ–±–Њ—Б–љ–Њ–≤—Л–≤–∞—О—Й–Є—Е –∞–Ї—В—Г–∞–ї—М–љ–Њ—Б—В—М –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Д–∞–Ї—В–Њ—А–Њ–≤ –Љ–Њ–≥—Г—В –±—Л—В—М –Њ—В–љ–µ—Б–µ–љ—Л —Б–ї–µ–і—Г—О—Й–Є–µ: –≤–ї–Є—П–љ–Є–µ –љ–∞ —А–∞–Ј–љ—Л–µ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–Є—Б—В–µ–Љ—Л, –≤–Њ–≤–ї–µ—З–µ–љ–љ—Л–µ –≤ —А–µ–≥—Г–ї—П—Ж–Є—О –Р–Ф —Б –і–Њ–Ї–∞–Ј–∞–љ–љ—Л–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —З–Є—Б–ї–∞ –Њ—В–≤–µ—В–Є–≤—И–Є—Е –і–Њ 70–80% (–њ—А–Њ—В–Є–≤ 40–50% –њ—А–Є –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є); –љ–µ–є—В—А–∞–ї–Є–Ј–∞—Ж–Є—П –Ї–Њ–љ—В—А—А–µ–≥—Г–ї—П—В–Њ—А–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е –љ–∞ –њ–Њ–≤—Л—И–µ–љ–Є–µ –Р–Ф; —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —В—А–µ–±—Г–µ–Љ—Л—Е –≤–Є–Ј–Є—В–Њ–≤; –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –±–Њ–ї–µ–µ –±—Л—Б—В—А–Њ–є –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –Р–Ф –±–µ–Ј —Г–≤–µ–ї–Є—З–µ–љ–Є—П, –∞ –љ–µ—А–µ–і–Ї–Њ —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —З–∞—Б—В–Њ—В—Л –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є; —З–∞—Б—В–∞—П –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –≥—А—Г–њ–њ–∞—Е –≤—Л—Б–Њ–Ї–Њ–≥–Њ —А–Є—Б–Ї–∞ –±—Л—Б—В—А–Њ–≥–Њ, —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф –Є/–Є–ї–Є –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –і–Њ—Б—В–Є–ґ–µ–љ–Є–Є –љ–Є–Ј–Ї–Є—Е —Ж–µ–ї–µ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є –Р–Ф; —А–∞—Б—И–Є—А–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є–є –і–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П.
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–Љ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–Љ —А–µ–ґ–Є–Љ–µ —В—А–µ–±—Г–µ—В —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є—П —Ж–µ–ї–Њ–Љ—Г —А—П–і—Г –Њ–±—П–Ј–∞—В–µ–ї—М–љ—Л—Е —Г—Б–ї–Њ–≤–Є–є: –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤; –≤–Ї–ї–∞–і –Ї–∞–ґ–і–Њ–≥–Њ –Є–Ј –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –≤ –Њ–ґ–Є–і–∞–µ–Љ—Л–є —А–µ–Ј—Г–ї—М—В–∞—В; —А–∞–Ј–љ—Л–є, –љ–Њ –≤–Ј–∞–Є–Љ–Њ–і–Њ–њ–Њ–ї–љ—П—О—Й–Є–є –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤; –ї—Г—З—И–Є–є —А–µ–Ј—Г–ї—М—В–∞—В –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–∞–ґ–і—Л–Љ –Є–Ј –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤; —Б–±–∞–ї–∞–љ—Б–Є—А–Њ–≤–∞–љ–љ–Њ—Б—В—М –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –њ–Њ –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В–Є –Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –і–µ–є—Б—В–≤–Є—П; —Г—Б–Є–ї–µ–љ–Є–µ –Њ—А–≥–∞–љ–Њ––њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л—Е —Б–≤–Њ–є—Б—В–≤; –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ —Г–љ–Є–≤–µ—А—Б–∞–ї—М–љ—Л–µ (–љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–µ) –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –њ–Њ–≤—Л—И–µ–љ–Є—П –Р–Ф; —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є –Є —Г–ї—Г—З—И–µ–љ–Є–µ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є. –Т —В–∞–±–ї–Є—Ж–µ 1 –њ—А–Є–≤–µ–і–µ–љ—Л —В–Є–њ–Є—З–љ—Л–µ –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Њ—Б–љ–Њ–≤–љ—Л—Е –Ї–ї–∞—Б—Б–Њ–≤ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Є—Е –±–ї–Њ–Ї–∞–і—Л –і–Њ–±–∞–≤–ї–µ–љ–Є–µ–Љ –≤—В–Њ—А–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞.

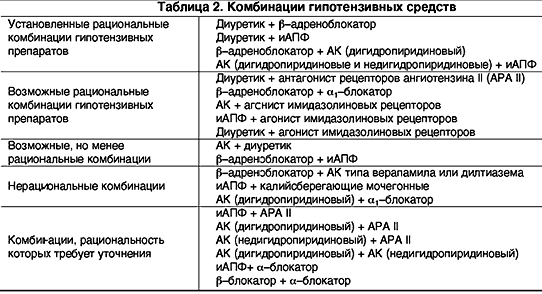
–Я–Њ—Б–ї–µ–і—Б—В–≤–Є—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–Є—П –і–≤—Г—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–є –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В–Є –Љ–Њ–≥—Г—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї —А–∞–Ј–ї–Є—З–љ—Л–Љ –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П–Љ c —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П: —Б–µ–љ—Б–Є—В–Є–Ј–∞—Ж–Є–Є (0+1=1,5); –∞–і–і–Є—В–Є–≤–љ–Њ–Љ—Г –і–µ–є—Б—В–≤–Є—О (1+1=1,75); —Б—Г–Љ–Љ–∞—Ж–Є–Є (1+1=2) –Є –њ–Њ—В–µ–љ—Ж–Є–Є—А–Њ–≤–∞–љ–Є—О (1+1=3). –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Г—Б–ї–Њ–≤–љ–Њ –Љ–Њ–ґ–љ–Њ –≤—Л–і–µ–ї–Є—В—М —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –Є –љ–µ—А–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (—В–∞–±–ї. 2).

–Т—Л—Б–Њ–Ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–µ–є, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–µ–є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –і–≤–∞ –Ї—А–∞–µ—Г–≥–Њ–ї—М–љ—Л—Е –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞ –Р–У (–љ–∞—В—А–Є–є––Њ–±—К–µ–Љ –Ј–∞–≤–Є—Б–Є–Љ—Л–є –Є –†–Р–°), —П–≤–ї—П–µ—В—Б—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –і–Є—Г—А–µ—В–Є–Ї–∞ –Є –Є–Р–Я–§. –С–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П –Њ–њ–Є—Б–∞–љ—Л –≤ –≥—А—Г–њ–њ–∞—Е –љ–Є–Ј–Ї–Њ-, –љ–Њ—А–Љ–Њ- –Є –≤—Л—Б–Њ–Ї–Њ—А–µ–љ–Є–љ–Њ–≤–Њ–є –Р–У, –≤–Ї–ї—О—З–∞—П –≥—А—Г–њ–њ—Л, –Є–Ј–≤–µ—Б—В–љ—Л–µ –Ї–∞–Ї –љ–Њ–љ–—А–µ—Б–њ–Њ–љ–і–µ—А—Л –љ–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б—А–µ–і—Б—В–≤ –±–ї–Њ–Ї–Є—А—Г—О—Й–Є—Е –†–Р–° (–љ–∞–њ—А–Є–Љ–µ—А, –ї–Є—Ж–∞ –љ–µ–≥—А–Њ–Є–і–љ–Њ–є —А–∞—Б—Л). –І–∞—Б—В–Њ—В–∞ –Ї–Њ–љ—В—А–Њ–ї—П –Р–У –њ–Њ–≤—Л—И–∞–µ—В—Б—П –і–Њ 80%. –С–ї–Њ–Ї–∞—В–Њ—А—Л –†–Р–° —Г—Б—В—А–∞–љ—П—О—В –≥–Є–њ–Њ–Ї–∞–ї–Є–µ–Љ–Є—О, –≥–Є–њ–Њ–Љ–∞–≥–љ–Є–µ–Љ–Є—О, –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є—О, –љ–∞—А—Г—И–µ–љ–Є—П —Г–≥–ї–µ–і–Њ–≤–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В —А–∞–Ј–≤–Є—В—М—Б—П –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –і–Є—Г—А–µ—В–Є–Ї–Њ–≤ –≤ —А–µ–ґ–Є–Љ–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є. –Ъ–Њ–Љ–±–Є–љ–∞—Ж–Є—П –≤–µ—Б—М–Љ–∞ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≥–Є–њ–µ—А—В—А–Њ—Д–Є–µ–є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ –Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–µ–є. –Ч–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ—Л –Є –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –Љ–љ–Њ–≥–Є–µ —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Н—В–Њ–≥–Њ —Б–Њ—Б—В–∞–≤–∞, –љ–Њ –Њ—Б–Њ–±–Њ–µ –Љ–µ—Б—В–Њ –≤ —Н—В–Њ–Љ —А—П–і—Г –Ј–∞–љ–Є–Љ–∞–µ—В –њ—А–µ–њ–∞—А–∞—В –Э–Њ–ї–Є–њ—А–µ–ї.
–Я—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Э–Њ–ї–Є–њ—А–µ–ї–∞
–Я—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ—Л–Љ –Њ—В–ї–Є—З–Є–µ–Љ –і–∞–љ–љ–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —П–≤–ї—П–µ—В—Б—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –≤ –і–Њ–Ј–∞—Е —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Љ–µ–љ—М—И–Є—Е –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л–Љ–Є –≤ —А–µ–ґ–Є–Љ–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є: –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї 2 –Љ–≥ –њ—А–Њ—В–Є–≤ 4–8 –Љ–≥ –Є –Є–љ–і–∞–њ–∞–Љ–Є–і 0,625 –Љ–≥ –њ—А–Њ—В–Є–≤ 2,5 –Љ–≥ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Ю—Б–љ–Њ–≤–љ—Л–µ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ–∞—А–∞–Љ–µ—В—А—Л –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є–≤–µ–і–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 4.

–С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ –і–ї—П –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –≤ –і–Њ–Ј–∞—Е 4/1,25 –Љ–≥. –§–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–∞—А–∞–Љ–µ—В—А—Л —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ–± –Њ—В—Б—Г—В—Б—В–≤–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –њ—А–Њ—Д–Є–ї–µ–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤, –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л—Е –≤ –≤–Є–і–µ —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —А–∞–Ј–і–µ–ї—М–љ—Л–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ.
–Я–Њ—П–≤–ї–µ–љ–Є—О —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –≤ –і–Њ–Ј–∞—Е 2 –Љ–≥/0,625 –Љ–≥ –њ—А–µ–і—И–µ—Б—В–≤–Њ–≤–∞–ї–Є –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л–µ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —Б—А–∞–≤–љ–Є–≤–∞—О—Й–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —А–∞–Ј–љ—Л—Е –і–Њ–Ј. –Т –Є—В–Њ–≥–µ –±—Л–ї–Њ –Є–Ј—Г—З–µ–љ–Њ 8 —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–Њ –і–Њ–Ј–Є—А–Њ–≤–Ї–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є (—А–Є—Б. 1) —Г 438 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ—П–≥–Ї–Њ–є/—Г–Љ–µ—А–µ–љ–љ–Њ–є –Р–У. –Ш–Ј—Г—З–µ–љ–љ—Л–є –і–Є–∞–њ–∞–Ј–Њ–љ –і–Њ–Ј –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ —Б–Њ—Б—В–∞–≤–Є–ї 2/0,625 –Љ–≥ – 8/2,5 –Љ–≥. –Т–Њ –≤—Б–µ—Е —Б–ї—Г—З–∞—П—Е, –≤–Ї–ї—О—З–∞—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—О 0/1,25 –Љ–≥, –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –±–Њ–ї—М—И–µ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Ф–Р–Ф –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ [14,15].

–†–Є—Б. 1. –°–љ–Є–ґ–µ–љ–Є–µ –Р–Ф –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –і–Њ–Ј –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї–∞/–Є–љ–і–∞–њ–∞–Љ–Є–і–∞
–Т –Њ–і–љ–Њ–Љ –Є–Ј –њ–µ—А–≤—Л—Е –Њ—В–Ї—А—Л—В—Л—Е –љ–µ—Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л—Е Forette B. –Є —Б–Њ–∞–≤. (1997) –±—Л–ї–∞ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞ –≤—Л—Б–Њ–Ї–∞—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–∞—П –Љ–Њ—Й–љ–Њ—Б—В—М —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ–Њ–є –љ–Є–Ј–Ї–Њ–і–Њ–Ј–Њ–≤–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї 2–Љ–≥/–Є–љ–і–∞–њ–∞–Љ–Є–і 0,625 –Љ–≥ [16]. –Ґ–∞–Ї, –≤ –≥—А—Г–њ–њ–µ –Є–Ј 50 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В–∞—А—И–µ 70 –ї–µ—В —Б–Њ —Б—А–µ–і–љ–Є–Љ –Є—Б—Е–Њ–і–љ—Л–Љ –Р–Ф 178/101 –Љ–Љ —А—В.—Б—В. —З–µ—А–µ–Ј 12 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П –Њ—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Р–Ф –љ–∞ 29,5/18,7 –Љ–Љ —А—В.—Б—В. –Ф–Њ–ї—П –Њ—В–≤–µ—В–Є–≤—И–Є—Е –љ–∞ –ї–µ—З–µ–љ–Є–µ –Є –љ–Њ—А–Љ–∞–ї–Є–Ј–Њ–≤–∞–≤—И–Є—Е –Р–Ф —Б–Њ—Б—В–∞–≤–Є–ї–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ 92% –Є 70%. –≠—В–Є –і–∞–љ–љ—Л–µ –±—Л–ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ—Л –≤ –і–≤–Њ–є–љ–Њ–Љ —Б–ї–µ–њ–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б –≤–Ї–ї—О—З–µ–љ–Є–µ–Љ 383 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В 72.4 –≥–Њ–і–∞) —Б –Љ—П–≥–Ї–Њ–є/—Г–Љ–µ—А–µ–љ–љ–Њ–є –Р–У [17]. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Э–Њ–ї–Є–њ—А–µ–ї–∞ –њ—А–Є–≤–µ–ї–Њ –Ї –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –Р–Ф —З–µ—А–µ–Ј 12 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П (22,5/13,2 –Љ–Љ —А—В.—Б—В. –њ—А–Њ—В–Є–≤ 12,3/7,3 –Љ–Љ —А—В.—Б—В. –љ–∞ –њ–ї–∞—Ж–µ–±–Њ). –Ф–Њ–ї—П –Њ—В–≤–µ—В–Є–≤—И–Є—Е —Б–Њ—Б—В–∞–≤–Є–ї–∞ 81,3% –Є 48,9% –≤ –њ–Њ–і–≥—А—Г–њ–њ–∞—Е —Б —Б–Є—Б—В–Њ–ї–Њ––і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –Є –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –Р–У —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. 253 –њ–∞—Ж–Є–µ–љ—В–∞ –њ—А–Њ–і–Њ–ї–ґ–Є–ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ [21]. –І–µ—А–µ–Ј –≥–Њ–і –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П –Ф–Р–Ф (< 90 –Љ–Љ —А—В.—Б—В.) –Њ—В–Љ–µ—З–µ–љ–∞ —Г 83,6% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–Є—Б—В–Њ–ї–Њ––і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –Р–У –Є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є (–°–Р–У) (< 160 –Љ–Љ —А—В.—Б—В.) – —Г 81,7% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –Р–У (—А–Є—Б. 2). –°—В–∞–±–Є–ї—М–љ–∞—П –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П –Р–Ф (–љ–Њ—А–Љ–∞–ї—М–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Р–Ф –љ–∞ –≤—Б–µ—Е –≤–Є–Ј–Є—В–∞—Е) –Њ—В–Љ–µ—З–µ–љ–∞ –≤ 79.8% —Б–ї—Г—З–∞–µ–≤. –Т –і–≤–Њ–є–љ–Њ–Љ —Б–ї–µ–њ–Њ–Љ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б –∞—В–µ–љ–Њ–ї–Њ–ї–Њ–Љ 50 –Љ–≥ –њ—А–Є —Г—З–∞—Б—В–Є–Є 446 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —З–µ—А–µ–Ј 12 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–Њ–µ –њ–Њ —Б—В–µ–њ–µ–љ–Є —Б–љ–Є–ґ–µ–љ–Є–µ –Р–Ф –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е. –Ю–і–љ–∞–Ї–Њ –≤ –њ–Њ–і–≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В–∞—А—И–µ 65 –ї–µ—В –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї—М—И–∞—П –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Э–Њ–ї–Є–њ—А–µ–ї–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –∞—В–µ–љ–Њ–ї–Њ–ї–Њ–Љ [18]. –Э–µ—Б–Њ–Љ–љ–µ–љ–љ—Л–є –Є–љ—В–µ—А–µ—Б –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —А–µ–Ј—Г–ї—М—В–∞—В—Л —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–≤–Њ–є–љ–Њ–≥–Њ —Б–ї–µ–њ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Э–Њ–ї–Є–њ—А–µ–ї–∞ —Б –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–Љ —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–∞ II –ї–Њ–Ј–∞—А—В–∞–љ–Њ–Љ [19]. 277 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–Є —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л –≤ –і–≤–µ –≥—А—Г–њ–њ—Л, –њ–Њ–ї—Г—З–∞–≤—И–Є–µ –ї–Є–±–Њ –Э–Њ–ї–Є–њ—А–µ–ї, –ї–Є–±–Њ –ї–Њ–Ј–∞—А—В–∞–љ 50 –Љ–≥ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 12 –љ–µ–і–µ–ї—М. –Ф–Њ–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–∞–Ї —Б—А–µ–і–Є –Њ—В–≤–µ—В–Є–≤—И–Є—Е –љ–∞ –ї–µ—З–µ–љ–Є—П, —В–∞–Ї –Є –љ–Њ—А–Љ–∞–ї–Є–Ј–Њ–≤–∞–≤—И–Є—Е –Р–Ф —З–µ—А–µ–Ј 12 –љ–µ–і–µ–ї—М –±—Л–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї—М—И–µ –≤ –≥—А—Г–њ–њ–µ –Э–Њ–ї–Є–њ—А–µ–ї–∞: 91,7% –њ—А–Њ—В–Є–≤ 81,8% (—А=0,025), 76% –њ—А–Њ—В–Є–≤ 60% (—А=0,009). –Ф–∞–љ–љ—Л–µ, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –њ—А–Є –°–Ь–Р–Ф, —В–∞–Ї–ґ–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –±–Њ–ї—М—И–µ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є –Љ–Њ—Й–љ–Њ—Б—В–Є –Э–Њ–ї–Є–њ—А–µ–ї–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –ї–Њ–Ј–∞—А—В–∞–љ–Њ–Љ 50 –Љ–≥ (—А–Є—Б. 3). –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–∞ II —Б—З–Є—В–∞—О—В—Б—П –Ї–ї–∞—Б—Б–Њ–Љ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б –љ–∞–Є–ї—Г—З—И–µ–є (—Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–Њ–є —Б –њ–ї–∞—Ж–µ–±–Њ), –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –Њ—Б–Њ–±—Л–є –Є–љ—В–µ—А–µ—Б –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Д–∞–Ї—В –Њ—В—Б—Г—В—Б—В–≤–Є—П –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –≤ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Э–Њ–ї–Є–њ—А–µ–ї–∞ –Є –ї–Њ–Ј–∞—А—В–∞–љ–∞ –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Њ–±—Б—Г–ґ–і–∞–µ–Љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П [19, 20].

–†–Є—Б. 2. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї 2 –Љ–≥/–Є–љ–і–∞–њ–∞–Љ–Є–і 0,625 –Љ–≥/—Б—Г—В–Ї–Є —Г –њ–Њ–ґ–Є–ї—Л—Е –±–Њ–ї—М–љ—Л—Е –Р–У

–†–Є—Б. 3. –Ф–Є–љ–∞–Љ–Є–Ї–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –°–Ь –Р–Ф –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї–Њ–Љ 2 –Љ–≥/–Є–љ–і–∞–њ–∞–Љ–Є–і–Њ–Љ 0,625 –Љ–≥ –Є –ї–Њ–Ј–∞—А—В–∞–љ–Њ–Љ 50 –Љ–≥/—Б—Г—В–Ї–Є
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М —А–∞–Ј–ї–Є—З–љ—Л—Е —А–µ–ґ–Є–Љ–Њ–≤ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –Є–Ј—Г—З–µ–љ–∞ —Г 26 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О [21]. –У–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –±—Л–ї–∞ –Њ—В—З–µ—В–ї–Є–≤–Њ–є –Ї–∞–Ї –њ—А–Є –µ–ґ–µ–і–љ–µ–≤–љ–Њ–Љ –њ—А–Є–µ–Љ–µ, —В–∞–Ї –Є –њ—А–Є–µ–Љ–µ —З–µ—А–µ–Ј –і–µ–љ—М. –І–µ—А–µ–Ј 12 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П –Њ—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –Р–Ф —Б–Њ 170,4/101,5 –Љ–Љ —А—В.—Б—В. –і–Њ 146,5/86,5 –Љ–Љ —А—В.—Б—В. –£—А–Њ–≤–µ–љ—М –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ —Б—Л–≤–Њ—А–Њ—В–Ї–Є –њ—А–Є —Н—В–Њ–Љ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ–Є–ї—Б—П.–Я—А–Њ—Д–Є–ї—М –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Э–Њ–ї–Є–њ—А–µ–ї–∞ –љ–µ –Њ—В–ї–Є—З–∞–ї—Б—П –Њ—В —В–∞–Ї–Њ–≤–Њ–≥–Њ –њ–ї–∞—Ж–µ–±–Њ. –Ф–∞–љ–љ–Њ–µ —Г—В–≤–µ—А–ґ–і–µ–љ–Є–µ —Б–њ—А–∞–≤–µ–і–ї–Є–≤–Њ –Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Ї–∞—И–ї—П, –Ї–Њ—В–Њ—А—Л–є —П–≤–ї—П–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ –њ–Њ–±–Њ—З–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ –і–ї—П –Є–Р–Я–§ [22]. –Ю—В–Љ–µ—З–µ–љ–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –≥–Є–њ–Њ–Ї–∞–ї–Є–µ–Љ–Є–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Є–љ–і–∞–њ–∞–Љ–Є–і–∞ –≤ —А–µ–ґ–Є–Љ–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –≤ 12––љ–µ–і–µ–ї—М–љ–Њ–Љ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [22] –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї–∞ 4 –Љ–≥/–Є–љ–і–∞–њ–∞–Љ–Є–і 1,25 –Љ–≥ –њ—А–Њ—В–Є–≤ –Є–љ–і–∞–њ–∞–Љ–Є–і–∞ 2,5 –Љ–≥ —Б —Г—З–∞—Б—В–Є–µ–Љ 1633 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —З–∞—Б—В–Њ—В–∞ –≥–Є–њ–Њ–Ї–∞–ї–Є–µ–Љ–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї–∞ 3,9 –њ—А–Њ—В–Є–≤ 8,0% (p < 0,01). –Т –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [22] –њ—А–Є 12-–Љ–µ—Б—П—З–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї–∞ 2 –Љ–≥/–Є–љ–і–∞–њ–∞–Љ–Є–і–∞ 1,25 –Љ–≥ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–∞—П —З–∞—Б—В–Њ—В–∞ —Г–Љ–µ—А–µ–љ–љ–Њ–є –≥–Є–њ–Њ–Ї–∞–ї–Є–µ–Љ–Є–Є –Њ—В–Љ–µ—З–µ–љ–∞ –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ: 1 —Б–ї—Г—З–∞–є –њ—А–Њ—В–Є–≤ 13. –Т —Н—В–Њ–Љ –ґ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Њ—В–Љ–µ—З–µ–љ–Њ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Љ–Њ—З–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –Ї—А–Њ–≤–Є –љ–∞ 20 –Љ–Љ–Њ–ї—М/–ї –≤ –≥—А—Г–њ–њ–µ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П. –Ю–і–љ–∞–Ї–Њ —А–∞–Ј–ї–Є—З–Є—П —Б –≥—А—Г–њ–њ–Њ–є –њ–ї–∞—Ж–µ–±–Њ, –≤ –Ї–Њ—В–Њ—А–Њ–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –њ–Њ–≤—Л—Б–Є–ї—Б—П –љ–∞ 15,2 –Љ–Љ–Њ–ї—М/–ї, –±—Л–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –љ–µ–і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Э–Њ–ї–Є–њ—А–µ–ї —П–≤–ї—П–µ—В—Б—П –Є—Б—В–Є–љ–љ–Њ –љ–Є–Ј–Ї–Њ–і–Њ–Ј–Њ–≤–Њ–є (1/2 –Є 1/4 –Њ—В –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ј –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤) –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–µ–є –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–µ–є —А–∞–Ј–љ—Л—Е –Ї–ї–∞—Б—Б–Њ–≤ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є–Р–Я–§ –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї–∞ –Є –љ–µ—В–Є–∞–Ј–Є–і–љ–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є –љ–µ–є—В—А–∞–ї—М–љ–Њ–≥–Њ –і–Є—Г—А–µ—В–Є–Ї–∞ –Є–љ–і–∞–њ–∞–Љ–Є–і–∞, –Њ–±–ї–∞–і–∞–µ—В –∞–і–і–Є—В–Є–≤–љ—Л–Љ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –Ї–Њ–љ—В—А–Њ–ї—М –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є —Б—Г—В–Њ–Ї –њ—А–Є –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–Љ –њ—А–Є–µ–Љ–µ, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –≤ –≥—А—Г–њ–њ–∞—Е —Б –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –Р–У, –њ–Њ–ґ–Є–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Њ–±–ї–∞–і–∞–µ—В —Е–Њ—А–Њ—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О –Є, —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –Њ—В–≤–µ—З–∞–µ—В –≤—Б–µ–Љ —В—А–µ–±–Њ–≤–∞–љ–Є—П–Љ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е —Б—В–∞–љ–і–∞—А—В–Њ–≤ –њ–Њ –Р–У –Ї –љ–Є–Ј–Ї–Њ–і–Њ–Ј–Њ–≤—Л–Љ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П–Љ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–Ь–µ—Б—В–Њ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –Р–У
–Я–µ—А–≤–Њ–љ–∞—З–∞–ї—М–љ—Л–є –≤—Л–±–Њ—А —В–∞–Ї—В–Є–Ї–Є –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Р–У –Є–≥—А–∞–µ—В —З–∞—Б—В–Њ –Ї—А–Є—В–Є—З–µ—Б–Ї—Г—О —А–Њ–ї—М –≤ –і–∞–ї—М–љ–µ–є—И–µ–є —Б—Г–і—М–±–µ –њ–∞—Ж–Є–µ–љ—В–∞. –£–і–∞—З–љ—Л–є –≤—Л–±–Њ—А —П–≤–ї—П–µ—В—Б—П –Ј–∞–ї–Њ–≥–Њ–Љ –і–ї—П –≤—Л—Б–Њ–Ї–Њ–є –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В–Є –Ї –ї–µ—З–µ–љ–Є—О, –љ–µ—Г–і–∞—З–љ—Л–є, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є–є—Б—П –љ–µ–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–є –Р–У –Є/–Є–ї–Є —Г—Е—Г–і—И–µ–љ–Є–µ–Љ —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є—П, –љ–µ—А–µ–і–Ї–Њ —Б–љ–Є–ґ–∞–µ—В —В–∞–Ї–Њ–≤—Г—О. –Т—Л–±–Њ—А –љ–∞—З–∞–ї—М–љ–Њ–≥–Њ —А–µ–ґ–Є–Љ–∞ –і–ї—П –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Р–У –Њ—Б—В–∞–µ—В—Б—П —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Є–Љ. –Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –љ–Є–Љ –ї–µ—З–µ–љ–Є–µ –і–Њ–ї–ґ–љ–Њ —Д–Њ—А–Љ–∞–ї—М–љ–Њ –љ–∞—З–Є–љ–∞—В—М—Б—П —Б –Њ–і–љ–Њ–≥–Њ –Є–Ј –Ї–ї–∞—Б—Б–Њ–≤ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є –і–Њ–Ј–µ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –і–Њ–Ј—Л –Є–ї–Є –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –≤—В–Њ—А–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞. –Ю–і–љ–∞–Ї–Њ —В–∞–Ї–Њ–є –њ–Њ–і—Е–Њ–і –љ–µ –Љ–Њ–ґ–µ—В —Б—З–Є—В–∞—В—М—Б—П –≤—Б–µ–≥–і–∞ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ—Л–Љ. –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, –њ—А–µ–і–љ–∞–Ј–љ–∞—З–µ–љ–љ—Л–µ –і–ї—П –±–∞–Ј–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є –Р–У, –њ–Њ–ї–љ–Њ—Б—В—М—О –њ—А–Њ—П–≤–ї—П—О—В —Б–≤–Њ–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї —З–µ—А–µ–Ј 4–6 –љ–µ–і–µ–ї—М –Є —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ –њ—А–Њ—Ж–µ—Б—Б –њ–Њ–і–±–Њ—А–∞ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Љ–Њ–ґ–µ—В —А–∞—Б—В—П–љ—Г—В—М—Б—П –љ–∞ –і–Њ–ї–≥–Є–µ –Љ–µ—Б—П—Ж—Л, —В—А–µ–±—Г—П –њ–Њ–≤—В–Њ—А–љ—Л—Е –≤–Є–Ј–Є—В–Њ–≤, –∞ –Є–љ–Њ–≥–і–∞ –Є –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–є. –Э–µ—А–µ–і–Ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П –і–ї—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (—В–∞–±–ї. 5) –љ–µ –њ–Њ–Ј–≤–Њ–ї—П—О—В —Б–Њ–Ї—А–∞—В–Є—В—М —Н—В–Њ—В –њ–µ—А–Є–Њ–і.


–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Љ—Л –Љ–Њ–ґ–µ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –і–≤–∞ –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ—Л—Е –њ–Њ–і—Е–Њ–і–∞ –њ—А–Є –Њ—Б—Г—Й–µ—Б—В–≤–ї–µ–љ–Є–Є –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Р–У: –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–∞—П –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –і–Њ –≤—Л–±–Њ—А–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Є —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ –Є–ї–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —В–µ—А–∞–њ–Є—П –≤ —А–µ–ґ–Є–Љ–µ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Є–ї–Є –њ–µ—А–≤–Њ–љ–∞—З–∞–ї—М–љ–Њ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є. –Ю–±–∞ –њ–Њ–і—Е–Њ–і–∞ –Є–Љ–µ—О—В —Б–≤–Њ–Є –і–Њ—Б—В–Њ–Є–љ—Б—В–≤–∞ –Є –љ–µ–і–Њ—Б—В–∞—В–Ї–Є. –°–Њ–≤—А–µ–Љ–µ–љ–љ–∞—П, —Е–Њ—А–Њ—И–Њ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–∞—П –Ї–Њ–љ—Ж–µ–њ—Ж–Є—П –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –Р–У –њ—А–Є–≤–ї–µ–Ї–ї–∞ –њ—А–Є—Б—В–∞–ї—М–љ–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ –Ї –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л—Е –љ–Є–Ј–Ї–Њ–і–Њ–Ј–Њ–≤—Л—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є. –Ъ–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–∞—П —В–µ—А–∞–њ–Є—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–≤–µ–ї–Є—З–Є—В—М –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Г—О –Љ–Њ—Й–љ–Њ—Б—В—М –ї–µ—З–µ–±–љ–Њ–≥–Њ —А–µ–ґ–Є–Љ–∞, —Г–Љ–µ–љ—М—И–Є—В—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є, –∞ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–є —Б–Њ–Ї—А–∞—В–Є—В—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ—А–Є–љ–Є–Љ–∞–µ–Љ—Л—Е —В–∞–±–ї–µ—В–Њ–Ї –Є –њ–Њ–≤—Л—Б–Є—В—М –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В—М –њ–∞—Ж–Є–µ–љ—В–∞ –Ї –ї–µ—З–µ–љ–Є—О –Є, —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –Њ–њ—В–Є–Љ–Є–Ј–Є—А–Њ–≤–∞—В—М —В–µ—А–∞–њ–Є—О —Г –±–Њ–ї—М—И–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –Њ—З–µ–≤–Є–і–љ—Л–µ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –њ—А–Є–љ—Ж–Є–њ—Л –Љ–µ–і–Є—Ж–Є–љ—Л, –Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–є –љ–∞ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞—Е, —В—А–µ–±—Г—О—В –і–∞–ї—М–љ–µ–є—И–Є—Е –Ї—А—Г–њ–љ–Њ–Љ–∞—Б—И—В–∞–±–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –Њ—В–≤–µ—В–Њ–≤ –љ–∞ –≤–Њ–њ—А–Њ—Б—Л –Њ –≤–ї–Є—П–љ–Є–Є —Н—В–Є—Е –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–Њ–≤—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞ –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ—Л–µ –њ—А–Њ–Љ–µ–ґ—Г—В–Њ—З–љ—Л–µ —Б—Г—А—А–Њ–≥–∞—В–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Є –Ї–Њ–љ–µ—З–љ—Л–µ —В–Њ—З–Ї–Є.
1. Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. The Sixth Report of the Joint National Commitee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. Arch Intern Med 1997; 157:2413–2446.
2. Hansson L, Zanchetti A, Carruthers SG, Dahlof B, Elmfeldt D, Julius S, et al. Effects of intensive blood pressure lowering and low–dose aspirin in patients with hypertension: principal results of the Hypertension Optimal Treatment (HOT) randomized trial. Lancet 1998, 351:1755–1762
3. Ambrosioni E Pharmacoeconomics of Hypertension Management The place of Combination Therapy Pharmacoeconomics 2001; 19 (4); 337– 347
4. Caro JJ, Sppecman Jl, Salas M, et al. Effect of initial drug choice on persistence with antihypertensive therapy: the importance of actual practice data. CMAJ 1999; 160; 41–6
5. World Health Organization–International Society of Hypertension. 1999 World Health Organization–International Society of Hypertension guidelines for the management of hypertension. Guidelines subcommittee. J Hypertens 1999; 17:151–18
6. –Я—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞, –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ –њ–µ—А–≤–Є—З–љ–Њ–є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–Є –≤ –†–Њ—Б—Б–Є–є—Б–Ї–Њ–є –§–µ–і–µ—А–∞—Ж–Є–Є (–Ф–Р–У 1) –Ъ–ї–Є–љ —Д–∞—А–Љ–∞–Ї –Є —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П 2000,3, 5–31
7. –РNAES Agence Nationale d’Accreditation et d’Evaluation en Sante Recommandations. 2000; 1–17
8. Opie L.H., Messerli F.H. Combination Drug Therapy for Hypertension 1997 Authors Publishing House New York 173 p
9. Kalpan NM. Low dose combinations in the treatment of hypertension: theory and practice. J Hym Hypertens 1999; 13: 707–10
10. Sica DA, Ripley E. Low–Dose Fixed–Combination Antihypertensive Therapy in Hypertension a companion to the Brenner and Rectors’ The Kidney (edited by) Oparil S, Weber M, 2000 Saunders Company p 497–504
11. Waeber B, Bruner HR. Combination antihypertensive therapy: does it have a role in rational therapy? Am J hypertens 1997; 101: 31S–137S
12. Weber MA. Strategies for improving blood pressure control. Am J Hypertens 1998; 11:897–9
13. Chalmers J. The importance of drug combinations for effective control of hypertension. Clin Exp Hypertens 1999; 21: 875–84
14. Myers M, Asmar R, Leenen F. Fixed low–dose combination therapy in hypertension: a dose response study of perindopril and indapamide. J Hypertens 2000; 18: 327–337
15. McClennan KH, Markham A. Perindopril 2 mg/Indapamide 0.625 mg Fixed Low–dose Combination. Drugs 1999; 58 (2); 297–302
16. Forette b, Feldmann L, Laurandin I, et al. Safety and efficacy of fixed–combination of perindopril and indapamide in 50 elderly hypertensive patients [abstract]. Am J Hypertens 1997 Apr; 10 (4 pt 2): 111A
17. Chalmers J, Castaigne A, Morgan T, et al. Long–term efficacy of a new, fixed, very–low–dose angiotesin–converting enzyme–inhibitor/diuretic combination as first–line therapy in elderly hypertensive patients. J Hypertens 2000; 18: 1–11
18. Mallion JM, Chastang C, Unger P. Efficacy and safety of a fixed low–dose perindopril /indapamide combination in essential hypertension; a randomised controlled study. Servier 1999. (Data on file)
19.Chanudet X, Phong Chau N, Champvallins M. Very–low–dose perindopril 2 mg/indapamide 0.625 mg combination gives higher response and normalization rates than losartan 50 mg in the treatment of essential hypertension [abstract no. P2.43]. J Hypertens 2000; 18 Suppl. 2:S100
20.Chanudet X, Champvallins M De Antihypertensive efficacy and tolerability of low–dose perindopril/indapamide combination compared with losatran in the treatment of essential hypertension Int J Clin Pract 2001; 55(4): 233–239.
21. Meyrier A, Dratwa M, Sennesael J. Fixed low–dose perindopril–indapamide combination in hypertensive patients with chronic renal failure. Am J Hypertens 1998 Sep; 11: 1087–92
22. Safar M, Salzman V, Brault Y, et al. Safety and efficacy of perindopril/indapamide fixed combination in mind–to–moderate hypertension [abstract]. J Hypertens 1996 Jun; 14 Suppl. 1: 225
–Я–µ—А–Є–љ–і–Њ–њ—А–Є–ї + –Є–љ–і–∞–њ–∞–Љ–Є–і –
–Э–Њ–ї–Є–њ—А–µ–ї (—В–Њ—А–≥–Њ–≤–Њ–µ –љ–∞–Ј–≤–∞–љ–Є–µ)
(Servier)












