Эволюция системы стратификации риска у больных мерцательной
аритмией
Первым рандомизированным исследованием, продемонстрировавшим преимущество Варфарина в отношении профилактики ТЭ у больных МА без поражения клапанов сердца, было AFASAK [3], результаты которого опубликованы в 1989 г. Последующие исследования SPAF, BAATAF и SPINAF подтвердили эффективность АВК в отношении первичной и вторичной профилактики инсульта у больных МА [2,5–6].
В исследовании SPINAF [6] впервые начались поиски возможности стратифицировать больных по степени риска ИИ. Авторы данного исследования выделили группу «низкого риска» – пациентов без артериальной гипертонии (АГ), сахарного диабета (СД), органических изменений сердца, признав АСК для них адекватной антитромботической терапией.
Поиск системы стратификации больных МА по степени риска тромбоэмболических осложнений был продолжен в исследовании SPAF II и SPAF III [7–9]. По результатам исследования SPAF II была выделена группа пациентов моложе 75 лет без предшествующих тромбоэмболических осложнений, АГ и хронической сердечной недостаточности (ХСН), частота ИИ у которых на фоне приема АСК составила 0,5% в год, что позволило им определить эту группу как пациентов «низкого риска» и не рекомендовать терапию АВК у данной категории больных.
В исследовании SPAF III в группу «низкого риска» включались больные с систолическим АД не выше 160/100 мм рт.ст., тем не менее анамнез артериальной гипертонии был у половины пациентов, включенных в эту группу. При отдельном анализе было выявлено, что пациенты с анамнезом АГ имели более высокую частоту первичных событий – 3,6% в год, в то время как нормотоники имели статистически достоверно более низкий риск – 1,1% в год. Частота ИИ, приведшего к инвалидизации, также была выше среди пациентов с АГ по сравнению с нормотониками. Таким образом, исследование SPAF III еще раз подтвердило, что даже наличие анамнеза АГ при адекватной в настоящее время уровне АД является фактором риска ИИ и системных эмболий у больных МА.
По данным мета–анализа исследований SPAF I–III [10], строгими предикторами инсульта у больных МА были: пожилой возраст, АГ, ИИ/ТИА в анамнезе, снижение функции левого желудочка. Возможными предикторами оказались: сахарный диабет, систолическое АД выше 160 мм рт.ст., женский пол (особенно женщины старше 75 лет), постменопаузальная гормонзаместительная терапия и ишемическая болезнь сердца.
Таким образом, к началу 90–х годов после получения результатов упомянутых исследований было определено, что пациенты низкого риска – это больные без органического поражения сердца, не переносившие ранее инсульт или системные эмболии и не имевшие АГ. При этом наличие АГ в анамнезе при адекватном уровне АД в настоящее время сохраняет значимость гипертонии как фактора риска высоких градаций.
В 2001 г. для выбора тактики антитромботической терапии Американской коллегией кардиологов, Американской ассоциацией сердца и Европейским обществом кардиологов была предложена стратификация по степени риска ИИ у больных МА [11]. К клиническим факторам, повышающим риск ИИ и СЭ у больных МА, были отнесены следующие: наличие в анамнезе ИИ или ТИА, АГ, хроническая сердечная недостаточность, пожилой возраст, СД и ишемическая болезнь сердца. При этом ИИ ТИА, АГ, ХСН, наличие митрального стеноза и протезов клапанов сердца были определены как факторы риска высоких градаций, а факторами риска средних градаций – ИБС и СД.
Выделены были также инструментальные факторы риска – дисфункция левого желудочка средней и тяжелой степени, выявляемая при ЭХО–КГ. А внедрение в рутинную клиническую практику ЧПЭХО–КГ позволило установить такие факторы риска тромбоэмболических осложнений, как тромбоз ушка или полости левого и правого предсердий и феномена спонтанного эхоконтрастирования в левом предсердии и его ушке, а также атероматоз грудного отдела аорты [8,9,11].
Стратификация риска инсульта
у больных МА по шкале CHADS2
В 2001 г. была предложена шкала CHADS2 (Cardiac Failure, Hypertension, Age, Diabetes, Stroke), позволяющая спрогнозировать риск инсульта у каждого конкретного больного [12]. В основу данной системы стратификации был положен анализ инсультов и системных эмболий, произошедших у больных, не принимавших АВК. CHADS2. Такие факторы, как ХСН, АГ, возраст ≥ 75 лет и сахарный диабет, оцениваются в 1 балл, а ИИ/ТИА или системные эмболии в анамнезе – в 2 балла. Частота инсультов увеличивается пропорционально возрастанию количества баллов по шкале CHADS2 и составляет 2,8% в год при наличии одного балла и 8,5% в год при наличии 4 баллов (рис. 1). Низким и средним риском тромбоэмболических осложнений обладают пациенты, имеющие 0 и 1 балл по шкале CHADS2 соответственно. Больным низкого риска показана терапия АСК, для больного среднего риска возможен выбор между Варфарином и АСК. Больные, имеющие 2 и более баллов по шкале CHADS2, имеют абсолютные показания к терапии Варфарином.
Обновленные рекомендации по лечению мерцательной аритмии, опубликованные в 2006 г. [13], оставили систему CHADS2 без изменений и определили группы низкого риска с вероятностью развития ИИ менее 2% в год, среднего – частота ИИ от 2 до 5% в год и группу высокого риска с частотой ИИ более 6% в год.
В вышедших в 2008 г. рекомендациях Американской коллегии торакальных врачей [14] данная шкала была оставлена как определяющая риск инсульта у больных МА (табл. 1).
Модификация факторов риска
тромбоэмболических осложнений
у больных МА
Шкала CHADS2 имеет два несомненных преимущества – простоту и удобство использования в реальной клинической практике. Однако накопление новых данных в течение последних лет позволил определить некоторые ее ограничения.
Риск ИИ и системных эмболий у больных МА неодинаков, и предложенные схемы стратифицируют больных на категории низкого, среднего и высокого риска. Хотя факторы риска, используемые в современной схеме, получены из крупных рандомизированных исследований, некоторые из определенных ранее остались за рамками шкалы CHADS2. Так, значимость женского пола как независимого фактора риска инсульта была показана в ряде исследований [10,15,16]. Такие же данные касаются такого параметра, как возраст старше 75 лет [5,10,16]. Однако несмотря на то что еще в исследовании BAATAF было продемонстрировано несомненное преимущество АВК перед АСК у больных старше 75 лет, врачи часто не назначают Варфарин данной категории больных по причине неоправданного риска потенциальных кровотечений.
В настоящих рекомендациях указано, что Варфарин показан больным высокого риска, АСК – больным низкого риска. В отношении группы среднего риска рекомендации оставляют врачу выбор в назначении одного из препаратов (или Варфарин, или АСК). Однако действительно ли низкий риск отражает реально низкий риск? И не служит ли трактовка формулировки «или Варфарин, или аспирин» в отношении больных среднего риска в реальной клинике поводом неназначения Варфарина в группе пациентов среднего риска?
Наблюдению за судьбой больных, имеющих низкий риск по шкале CHADS2, посвящено в последнее время много исследований, продемонстрировавших, что частота инсульта у больных низкого риска, не принимающих Варфарин, достаточно высока. Так, в корейском исследовании [18] было показано, что частота ИИ за 2 года наблюдения у больных МА, имеющих один балл по шкале CHADS2, на фоне терапии АСК составила 12,9 и 20,9% у больных, не получавших никакой антитромботической терапии. В исследовании Gorin et al. [19], включившем в себя когорту из 1012 больных МА, имевших один балл по шкале CHADS2, было показано, что частота ИИ и смерти у пациентов, не получавших терапию АВК, составила 17,9%. Данные исследования не были рандомизированными, однако ценность их заключается именно в отражении картины реальной клинической практики, отличающейся от условий современных многоцентровых исследований. Акцент, который сделан в последнее время на таких наблюдениях, обусловлен тем, что, возможно, категория больных, обозначаемых как пациенты низкого/среднего риска, нуждается в пересмотре. Не вызывает сомнений назначение АВК у больных, перенесших тромбоэмболические осложнения. Однако высокая частота инвалидизации и смерти, связанная с развитием ишемического инсульта, обусловливает высокую значимость именно первичной профилактики.
В 2009 г. группой исследователей из Бирмингема под руководством G.Y. Lip [17] была предложена новая система стратификации больных, названная ими CHA2DS2VASC. В основу было положено наблюдение в течение 1 года за когортой из 1577 больных с МА без поражения клапанов сердца, которые не получали АВК или гепарин. Средний возраст больных составил 66±14 лет, больных старше 75 лет было 28,5%. Большинство (67,3%) имели АГ, 23,5% – ХСН, 17,3% – СД, анамнез перенесенных ТЭ имели лишь 9,1% больных. Три четверти (74%) получали АСК. В результате анализа произошедших тромбоэмболических событий авторами была предложена балльная шкала (табл. 2). При этом низким риском обладают больные, не имеющие ни одного из перечисленных факторов (т.е. 0 баллов). При наличии 1 балла риск оценивается как средний и при наличии 2 и более баллов – как высокий.
По мнению авторов, данная обновленная система стратификации лучше идентифицирует риск инсульта у больных МА. Больным низкого риска не требуется назначение Варфарина, показано назначение АСК или никакой антитромботической терапии. Пациентам среднего риска, имеющим 1 балл, возможно назначение как АСК, так и Варфарина, при этом для этой категории больных в случае отсутствия противопоказаний следует отдавать предпочтение Варфарину. В случае если у больного имеется более 1 балла, показана терапия Варфарином с целевыми значениями МНО 2,0–3,0.
В качестве демонстрации различий в оценке риска в соответствии с обеими системами стратификации можно привести опыт наблюдения за больными МА, осуществляемый в ИКК им. А.Л. Мясникова на протяжении последних 10 лет. Данная когорта больных не является искусственной выборкой и представляет собой систему патронажного наблюдения за больными, принимающими АВК [20–22]. В настоящий анализ было включено 125 больных МА без поражения клапанов сердца, имевших показания для назначения АВК. Среди этих больных 23 пациента перенесли ИИ/ТИА или эпизод системных эмболий до назначения АВК. Нами был проведен анализ этой подгруппы пациентов. Средний возраст больного во время произошедшего эпизода тромбоэмболии был 58,3±0,9 года, при этом только 13% больных были на тот момент старше 65 лет, мужчин и женщин было примерно поровну. Ретроспективно был оценен риск по шкале CHADS2 и CHA2DS2VASC. Обращает на себя разница в рассчитанном риске. Так, средний балл по шкале CHADS2 до эпизода тромбоэмболий был 1,3, примерно две трети больных могли быть оценены как пациенты низкого риска (т.е. имевшие 1 балл) и не имевшие, таким образом, показаний для назначения Варфарина. В то же время при оценке по шкале CHA2DS2VASC только треть (34,8%) имели 1 балл, а две трети больных уже относились к категории высокого риска, имея 2 и более баллов, и у них были абсолютные показания для назначения Варфарина. Данный факт означает, что назначение этим больным тогда АВК, возможно, предотвратило бы развитие инсультов и эмболий. Обращает также на себя внимание, что при ретроспективной оценке этих больных не было, не имевших факторов риска вообще (рис. 2). Показательным также является тот факт, что среди этих 23 больных семеро перенесли повторные эпизоды тромбоэмболий до назначения АВК.
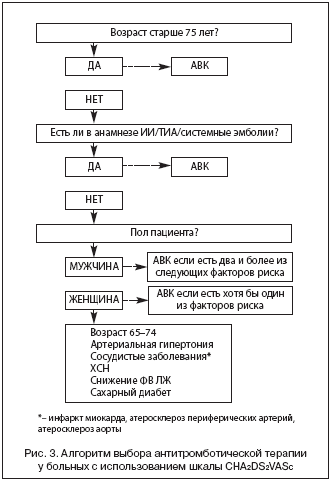
Пациенты, характеризующиеся низким риском, не являются однородной группой, и, возможно, именно в отношении этих больных необходима иная система стратификации. Шкала CHA2DS2VASC содержит большее число параметров, но для удобства использования авторы предлагают пользоваться схемой, показанной на рисунке 3.
Заключение
Варфарин является препаратом, предотвращающим фатальные и инвалидизирующие тромбоэмболические осложнения у больных мерцательной аритмией. Развитие стойкого неврологического дефицита после перенесенного инсульта не только нарушает жизнедеятельность больного, но приводит к его социальной и личностной дезадаптации. Врачами часто недооценивается риск инсульта и системных эмболий у больных мерцательной аритмией, в связи с чем многим пациентам не назначаются антагонисты витамина К при наличии абсолютных показаний. Изменение системы стратификации, расширяющее категорию больных среднего и высокого риска, позволит сделать больший акцент на проблеме первичной профилактики инсульта, что имеет как медицинское, так и социальное значение.




Литература
1. Hylek E.M., M.D., M.P.H., Yuchiao Chang, Ph.D., Nancy G. Jensvold, M.P.H. et al Effect of Intensity of Oral Anticoagulation on Stroke Severity and Mortality in Atrial Fibrillation. N Engl J Med, 2003; 349: 1019–1026.
2. Gullov A.L., Koefoed B.G., Petersen P. et al. Fixed minidose warfarin and aspirin alone and in combination versus adjusted–dose warfarin for stroke prevention in atrial fibrillation. Arch Intern Med, 1998; 158: 1513–1521.
3. Petersen P., Boysen G., Godtfredsen J. et al. Placebo–controlled, randomised trial of warfarin and aspirin for prevention of thromboembolic complications in chronic atrial fibrillation. The Copenhagen AFASAK study, Lancet, 1989; 1: 175–179.
4. EAFT (European Atrial Fibrillation Trial) Study Group. Secondary prevention in nonrheumatic atrial fibrillation and transient ischemic attack or minor stroke. Lancet 1993; 342: 1255–1262.
5. The Boston Area Anticoagulation Trial for Atrial Fibrillation Investigators. The effect of low–dose warfarin on the risk of stroke in patients with nonrheumatic atrial fibrillation. NEJM, 1990; 323: 1505–1511.
6. Ezekowitz M.D., Bridgers S.L., Javes K.E. et al. Warfarin in the prevention of stroke associated with nonrheumatic atrial fibrillation. NEJM 1992; 327: 1406–1413.
7. Patients with nonvalvular atrial fibrillation at low risk of stroke during treatment with aspirin: Stroke Prevention in Atrial Fibrillation III Study. The SPAF III Writing Committee for the Stroke Prevention in Atrial Fibrillation Investigators. JAMA; 1998: 279: 1273–7.
8. Asinger R.W., Koehler J., Pearce L.A., et al. J Pathophysiologic correlates of thromboembolism in nonvalvular atrial fibrillation: II. Dense spontaneous echocardiographic contrast (The Stroke Prevention in Atrial Fibrillation [SPAF–III] study). Am Soc Echocardiogr, 1999; 12: 1088–1096.
9. Goldman M.E., Pearce L.A., Hart R.G. Pathophysiologic correlates of thromboembolism in nonvalvular atrial fibrillation: I. Reduced flow velocity in the left atrial appendage (The Stroke Prevention in Atrial Fibrillation [SPAF–III]. study J Am Soc Echocardiogr, 1999; 12 (12): 1080–1087.
10. Hart R.G., Pearce L.A., McBride R., Rothbart R.M., Asinger R.W. Factors associated with ischemic stroke during aspirin therapy in atrial fibrillation: analysis of 2012 participants in the SPAF I–III clinical trials. The Stroke Prevention in Atrial Fibrillation (SPAF) Investigators. Stroke 1999; 30: 1223–1229.
11. Zabalgoitia M.; Halperin J.L.; Pearce L.A. et al. Transesophageal echocardiographic correlates of clinical risk of thromboembolism in nonvalvular atrial fibrillation. Stroke Prevention in Atrial Fibrillation III Investigators. J Am Coll Cardiol, 1998; 31: 1622–1626.
12. ACC/AHA/ESC guidelines for the management of patients with atrial fibrillation. European Heart J 2001;22:1852–1923.
13. ACC/AHA/ESC 2006 Guidelines for the Management of Patients With Atrial Fibrillation. A Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines and the European Society of Cardiology Committee for Practice Guidelines. JACC, 2006; 48: 149–246.
14. Singer D.E., Albers G.W., Dalen J.E. Americal Colledge of Chest Physicians. Antithrombotic therapy in Atrial Fibrillation: Americal Colledge of Chest Physicians evidence–based clinical practice guidelines (8th edition). Chest, 2008; 133: 546S–592S.
15. Lane D.A., Lip G.Y. Female gender is a risk factor for stroke and thromboembolism in atrial fibrillation patients. Thromb Haemost, 2009; 101: 802–805.
16. Stroke Risk in Atrial Fibrillation Working Group. Comparison of 12 risk stratification schemes to predict stroke in patients with non–valvular atrial fibrillation. Stroke, 2008; 39: 1901–1910.
17. Lip G.Y. H.MD, Nieuwlaat R., PhD, Pisters R, MD et al Refining Clinical Risk Stratification for Predicting Stroke and Thromboembolism in Atrial Fibrillation Using a Novel Risk Factor–Based Approach The Euro Heart Survey on Atrial Fibrillation. CHEST, 2010; 137: 263–272.
18. Lee B.H., Park J.H., et al. The effect and safety of the Antithrombotic therapies in patients with atrial fibrillation and CHADS2 score 1. J Cardiovasc Electrophysiol, 2010; in press.
19. Gorin I., Fauchier L., Nonin et al. Antithrombotic treatment and the risk of death and stroke in patients with atrial fibrillation and a CHADS2 score =1. Thromb Haemost, 2009; 103: 833–840.
20. Кропачева Е.С., Панченко Е.П., Атауллаханова Д.М. Сравнение эффективности и безопасности длительной терапии варфарином и аценокумаролом у больных мерцательной аритмией. Клиническая Медицина, 2004; № 6, стр 18–23.
21. Кропачева Е.С., Панченко Е.П., Добровольский А.Б. с соавт. Длительная терапия непрямыми антикоагулянтами у больных мерцательной аритмией без поражения клапанов сердца (проспективное наблюдение). Часть 1. Влияние 12–месячной терапии аценокумаролом на содержание Д–димера, частоту тромбоза и показатели гемодинамики ушка левого предсердия. Кардиология, 2004; №6 , с.24–30.
22. Панченко Е.П., Михеева Ю.А., Сычев Д.А. с соавт. Новый подход к повышению безопасности лечения вафарином (результаты фармакогенетического исследования). Кардиологический вестник, 2008, №2, с.38–44.












