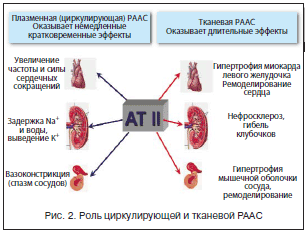
–Я–Њ–Ј–і–љ–µ–µ, –≤ –Ї–Њ–љ—Ж–µ –•–• –≤., –Њ—В–Ї—А—Л–ї–Є, —З—В–Њ –≤—Б–µ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л –†–Р–Р–° –∞–≤—В–Њ–љ–Њ–Љ–љ–Њ —Б–Є–љ—В–µ–Ј–Є—А—Г—О—В—Б—П –≤ –Њ—А–≥–∞–љ–∞—Е –Є —В–Ї–∞–љ—П—Е –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ —З–µ–ї–Њ–≤–µ–Ї–∞ (–Љ–Є–Њ–Ї–∞—А–і, —Н–љ–і–Њ—В–µ–ї–Є–є, –≥–ї–∞–і–Ї–Њ-–Љ—Л—И–µ—З–љ—Л–µ –Ї–ї–µ—В–Ї–Є —Б–Њ—Б—Г–і–Њ–≤, –њ–Њ—З–Ї–Є). –Ш–Љ–µ–љ–љ–Њ –∞–Ї—В–Є–≤–∞—Ж–Є—П —В–Ї–∞–љ–µ–≤—Л—Е –†–Р–Р–° –Є–≥—А–∞–µ—В –≥–ї–∞–≤–љ—Г—О —А–Њ–ї—М –≤ —А–∞–Ј–≤–Є—В–Є–Є –Њ—А–≥–∞–љ–љ—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є –њ—А–Є –Р–У, —Б–∞—Е–∞—А–љ–Њ–Љ –і–Є–∞–±–µ—В–µ (–°–Ф). –С—Л–ї–Њ —Б—Д–Њ—А–Љ—Г–ї–Є—А–Њ–≤–∞–љ–Њ –њ–Њ–ї–Њ–ґ–µ–љ–Є–µ –Њ –і–≤—Г—Е–Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–љ–Њ–є –†–Р–Р–° —Б –≤—Л–і–µ–ї–µ–љ–Є–µ–Љ —Ж–Є—А–Ї—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –Є –ї–Њ–Ї–∞–ї—М–љ–Њ–≥–Њ –Ј–≤–µ–љ—М–µ–≤, –Є–Љ–µ—О—Й–Є—Е –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П. –¶–Є—А–Ї—Г–ї–Є—А—Г—О—Й–µ–µ –Ј–≤–µ–љ–Њ –†–Р–Р–° –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –Њ—А–≥–∞–љ—Л-–Љ–Є—И–µ–љ–Є, –∞ –њ–Њ–≤—Л—И–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–Ї–∞–љ–µ–≤–Њ–≥–Њ –Ј–≤–µ–љ–∞ –Є–Љ–µ–µ—В —Г—Б—В–Њ–є—З–Є–≤—Л–є —Е–∞—А–∞–Ї—В–µ—А –Є –њ—А–Є–≤–Њ–і–Є—В –Ї —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –љ–µ —В–Њ–ї—М–Ї–Њ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е, –љ–Њ –Є —Б—В—А—Г–Ї—В—Г—А–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ –Њ—А–≥–∞–љ–∞—Е –Є —В–Ї–∞–љ—П—Е. –Х–≥–Њ –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ —В–Ї–∞–љ—П—Е –Њ—Б—В–∞–µ—В—Б—П –≤—Л—Б–Њ–Ї–Њ–є, –і–∞–ґ–µ –µ—Б–ї–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П —А–µ–љ–Є–љ–∞ –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є –љ–Њ—А–Љ–∞–ї–Є–Ј—Г–µ—В—Б—П (—А–Є—Б. 2). –Я—А–Є —Н—В–Њ–Љ —В–Ї–∞–љ–µ–≤–Њ–є A–Ґ II —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В —А–Њ—Б—В —Д–Є–±—А–Њ–±–ї–∞—Б—В–Њ–≤, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —А–∞–Ј–≤–Є—В–Є—О –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –Є –≥–Є–њ–µ—А–њ–ї–∞–Ј–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞, —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—О —Б–µ—А–і—Ж–∞ –Є —Б–Њ—Б—Г–і–Њ–≤, —Г—З–∞—Б—В–≤—Г–µ—В –≤ —А–µ–∞–Ї—Ж–Є—П—Е –Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –∞–њ–Њ–њ—В–Њ–Ј–∞.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–Њ–≤—Л—И–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –†–Р–Р–°, –Ї–∞–Ї —Ж–Є—А–Ї—Г–ї–Є—А—Г—О—Й–µ–є –≤ –Ї—А–Њ–≤–Є, —В–∞–Ї –Є —В–Ї–∞–љ–µ–≤–Њ–є, —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –≤–∞–ґ–љ–µ–є—И–Є—Е –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –Р–У, –њ–Њ—А–∞–ґ–µ–љ–Є—П –Њ—А–≥–∞–љ–Њ–≤-–Љ–Є—И–µ–љ–µ–є –њ—А–Є —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –Є –°–Ф, —А–∞–Ј–≤–Є—В–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (–•–°–Э).
–Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ (–Є–Р–Я–§) – —Н—В–Њ –≥—А—Г–њ–њ–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б–љ–Є–ґ–∞—О—Й–Є—Е –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –†–Р–Р–°. –Я–µ—А–≤—Л–є –Є–Р–Я–§ – —В–µ–њ—А–Њ—В–Є–і –±—Л–ї –њ–Њ–ї—Г—З–µ–љ –≤ 1971 –≥. –Є–Ј —П–і–∞ –±—А–∞–Ј–Є–ї—М—Б–Ї–Њ–є –Ј–Љ–µ–Є Jararaca (—А–Є—Б. 3). –Э–Њ –≤—Б–ї–µ–і—Б—В–≤–Є–µ –µ–≥–Њ —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —Н—В–Њ—В –њ—А–µ–њ–∞—А–∞—В –њ–Њ—З—В–Є –љ–µ –њ—А–Є–Љ–µ–љ—П–ї—Б—П. –Т 1975 –≥. D. Cushman –Є M. Ondetti (—А–Є—Б. 4) —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–ї–Є –њ–µ—А–≤—Л–є –њ–µ—А–Њ—А–∞–ї—М–љ—Л–є –Є–Р–Я–§ – –Ї–∞–њ—В–Њ–њ—А–Є–ї, –Ї–Њ—В–Њ—А—Л–є —Б—В–∞–ї —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ. –Э–∞—З–∞–ї–∞—Б—М —Н—А–∞ –Є–Р–Я–§.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Б—Г—Й–µ—Б—В–≤—Г–µ—В –±–Њ–ї–µ–µ 10 –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≥—А—Г–њ–њ—Л –Є–Р–Я–§, –Њ—В–ї–Є—З–∞—О—Й–Є—Е—Б—П –і—А—Г–≥ –Њ—В –і—А—Г–≥–∞ —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–Њ–є, —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ–∞—А–∞–Љ–µ—В—А–∞–Љ–Є. –°–Њ–≥–ї–∞—Б–љ–Њ –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є, –њ—А–µ–і–ї–Њ–ґ–µ–љ–љ–Њ–є –≤ 1994 –≥. L. Opie [5], –≤—Б–µ –Є–Р–Я–§ —А–∞–Ј–і–µ–ї—П—О—В—Б—П –љ–∞ 3 –Ї–ї–∞—Б—Б–∞ –Є –њ–Њ–і–≥—А—Г–њ–њ—Л (—В–∞–±–ї. 1).
–Ы–Є–њ–Њ—Д–Є–ї—М–љ—Л–µ (—Б–њ–Њ—Б–Њ–±–љ—Л–µ —А–∞—Б—В–≤–Њ—А—П—В—М—Б—П –≤ –ґ–Є—А–∞—Е) –Є–Р–Я–§ (I –Ї–ї–∞—Б—Б) –Њ–±—Л—З–љ–Њ —Б–≤—П–Ј—Л–≤–∞—О—В—Б—П —Б –±–µ–ї–Ї–∞–Љ–Є, –Њ–±–ї–∞–і–∞—О—В —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О, –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г—О—В—Б—П –≤ –њ–µ—З–µ–љ–Є —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –∞–Ї—В–Є–≤–љ—Л—Е –Є –љ–µ–∞–Ї—В–Є–≤–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –≤—Л–≤–Њ–і—П—В—Б—П –њ–Њ—З–Ї–∞–Љ–Є –Є –њ—А–Њ–љ–Є–Ї–∞—О—В —З–µ—А–µ–Ј –≥–µ–Љ–∞—В–Њ—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Є–є –±–∞—А—М–µ—А. II –Ї–ї–∞—Б—Б – —Н—В–Њ –њ—А–Њ–ї–µ–Ї–∞—А—Б—В–≤–∞, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ—Б–ї–µ –≥–Є–і—А–Њ–ї–Є–Ј–∞ –≤ –њ–µ—З–µ–љ–Є –њ–µ—А–µ—Е–Њ–і—П—В –≤ –∞–Ї—В–Є–≤–љ—Г—О —Д–Њ—А–Љ—Г. –Я—А–µ–њ–∞—А–∞—В—Л III –Ї–ї–∞—Б—Б–∞ –љ–µ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г—О—В—Б—П –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ, —Ж–Є—А–Ї—Г–ї–Є—А—Г—О—В –≤ –Ї—А–Њ–≤–Є –≤–љ–µ —Б–≤—П–Ј–Є —Б –±–µ–ї–Ї–∞–Љ–Є –њ–ї–∞–Ј–Љ—Л –Є –≤—Л–≤–Њ–і—П—В—Б—П –њ–Њ—З–Ї–∞–Љ–Є –≤ –љ–µ–Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–Љ –≤–Є–і–µ. –У–Є–і—А–Њ—Д–Є–ї—М–љ—Л–µ –Є–Р–Я–§ –Љ–∞–ї–Њ —Б–≤—П–Ј—Л–≤–∞—О—В—Б—П —Б –±–µ–ї–Ї–∞–Љ–Є, —З—В–Њ —Б–љ–Є–ґ–∞–µ—В –Є—Е –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М.
–Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є–Р–Я–§ –і–µ–ї—П—В—Б—П –њ–Њ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –і–µ–є—Б—В–≤–Є—П –љ–∞:
– –Є–Р–Я–§ –Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –Ї–Њ—В–Њ—А—Л–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –љ–∞–Ј–љ–∞—З–∞—В—М 2 –Є–ї–Є 3 —А./—Б—Г—В (–љ–∞–њ—А–Є–Љ–µ—А, –Ї–∞–њ—В–Њ–њ—А–Є–ї);
– –Є–Р–Я–§ —Б–Њ —Б—А–µ–і–љ–µ–є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –і–µ–є—Б—В–≤–Є—П, –Ї–Њ—В–Њ—А—Л–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–љ–Є–Љ–∞—В—М –љ–µ –Љ–µ–љ–µ–µ 2 —А./—Б—Г—В (–Ј–Њ—Д–µ–љ–Њ–њ—А–Є–ї –Є —Н–љ–∞–ї–∞–њ—А–Є–ї);
– –Є–Р–Я–§ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –Є—Е –њ—А–Є–љ–Є–Љ–∞—О—В 1 —А./—Б—Г—В (–Ї–≤–Є–љ–∞–њ—А–Є–ї, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї, –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї, —А–∞–Љ–Є–њ—А–Є–ї, —Б–њ–Є—А–∞–њ—А–Є–ї, —В—А–∞–љ–і–Њ–ї–∞–њ—А–Є–ї, —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї).
–Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л –≤—Л–і–µ–ї—П—О—В –Є–Р–Я–§, —Б–Њ–і–µ—А–ґ–∞—Й–Є–µ:
– —Б—Г–ї—М—Д–≥–Є–і—А–Є–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г (–Ї–∞–њ—В–Њ–њ—А–Є–ї, –Ј–Њ—Д–µ–љ–Њ–њ—А–Є–ї –Є –і—А.);
– –Ї–∞—А–±–Њ–Ї—Б–Є–∞–ї–Ї–Є–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г (—Н–љ–∞–ї–∞–њ—А–Є–ї, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї, –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї, —А–∞–Љ–Є–њ—А–Є–ї –Є –і—А.);
– —Д–Њ—Б—Д–Є–љ–Є–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г (—Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї).
–Я—А–Є —Н—В–Њ–Љ –љ–∞–ї–Є—З–Є–µ SH-–≥—А—Г–њ–њ—Л –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ —В–∞–Ї–Є—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –Ї–∞–Ї –≥–µ–Љ–∞—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М, –љ–∞—А—Г—И–µ–љ–Є–µ –≤–Ї—Г—Б–∞, –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М.
–Т –Ї–Њ–љ—Ж–µ –•–• –≤. –≥—А—Г–њ–њ–Њ–є –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є –њ–Њ–і —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ–Љ D. Cushman –±—Л–ї —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–љ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї, –Њ—В–ї–Є—З–∞—О—Й–Є–є—Б—П –њ–Њ —Б–≤–Њ–µ–є —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–µ –Њ—В –і—А—Г–≥–Є—Е –Є–Р–Я–§. –§–Њ–Ј–Є–љ–Њ–њ—А–Є–ї –Є –µ–≥–Њ –∞–Ї—В–Є–≤–љ—Л–є –Љ–µ—В–∞–±–Њ–ї–Є—В —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞—В —П–≤–ї—П—О—В—Б—П –њ—А–Њ–ї–Є–љ–Њ–≤—Л–Љ–Є –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–Љ–Є —Д–Њ—Б—Д–Є–љ–Є–ї—М–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –§–Њ—Б—Д–Є–љ–Є–ї—М–љ–∞—П –≥—А—Г–њ–њ–∞ —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П —Б –Є–Њ–љ–Њ–Љ —Ж–Є–љ–Ї–∞ –≤ –∞–Ї—В–Є–≤–љ–Њ–Љ —Ж–µ–љ—В—А–µ –Р–Я–§, –Є–љ–≥–Є–±–Є—А—Г—П –µ–≥–Њ –∞–Ї—В–Є–≤–љ–Њ—Б—В—М. –§–Њ–Ј–Є–љ–Њ–њ—А–Є–ї —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–ї–µ–Ї–∞—А—Б—В–≤–Њ–Љ –Є —В–Њ–ї—М–Ї–Њ –њ–Њ—Б–ї–µ –≤—Б–∞—Б—Л–≤–∞–љ–Є—П –≤ —В–Њ–љ–Ї–Њ–Љ –Ї–Є—И–µ—З–љ–Є–Ї–µ –Є –≥–Є–і—А–Њ–ї–Є–Ј–∞ –≤ –њ–µ—З–µ–љ–Є –њ–µ—А–µ—Е–Њ–і–Є—В –≤ –∞–Ї—В–Є–≤–љ—Л–є –Љ–µ—В–∞–±–Њ–ї–Є—В – —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞—В. –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —П–≤–ї—П–µ—В—Б—П —В–Њ, —З—В–Њ –µ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –≤ –њ–µ—З–µ–љ–Є, –љ–Њ –Є –≤ –і—А—Г–≥–Є—Е –Њ—А–≥–∞–љ–∞—Е (—Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–µ –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, –њ–Њ—З–Ї–∞—Е, —Б–Њ—Б—Г–і–∞—Е). –Я–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ—В 12 –і–Њ 15 —З, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –љ–∞–Ј–љ–∞—З–∞—В—М –µ–≥–Њ 1 —А./—Б—Г—В. –Я—А–Є —Г–Љ–µ—А–µ–љ–љ–Њ–Љ –љ–∞—А—Г—И–µ–љ–Є–Є —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї –њ–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –і–Њ 14–32 —З, –љ–Њ –Ј–љ–∞—З–Є–Љ–Њ–є –Ї—Г–Љ—Г–ї—П—Ж–Є–Є —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –љ–µ –Њ—В–Љ–µ—З–∞–µ—В—Б—П. –Т—Л—Б–Њ–Ї–∞—П –ї–Є–њ–Њ—Д–Є–ї—М–љ–Њ—Б—В—М —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –µ–≥–Њ —И–Є—А–Њ–Ї–Њ–µ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ, –∞ –Ј–љ–∞—З–Є—В, –Є –µ–≥–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Є–љ–≥–Є–±–Є—А–Њ–≤–∞—В—М –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–µ —В–Њ–ї—М–Ї–Њ —Ж–Є—А–Ї—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –≤ –Ї—А–Њ–≤–Є –Р–Я–§, –љ–Њ –Є —В–Ї–∞–љ–µ–≤–Њ–≥–Њ –Ј–≤–µ–љ–∞ –†–Р–Р–° (–≤ —Б–µ—А–і—Ж–µ, –ї–µ–≥–Ї–Є—Е, –њ–Њ—З–Ї–∞—Е, –≥–Њ–ї–Њ–≤–љ–Њ–Љ –Љ–Њ–Ј–≥–µ).
–Т —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–µ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї –њ–Њ–і–∞–≤–ї—П–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Р–Я–§ –≤ –Љ–Є–Њ–Ї–∞—А–і–µ –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є, —З–µ–Љ —Н–љ–∞–ї–∞–њ—А–Є–ї, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –Є —А–∞–Љ–Є–њ—А–Є–ї.
–Ю—Б–љ–Њ–≤–љ—Л–µ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–∞—А–∞–Љ–µ—В—А—Л —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–µ —А–∞–Ј–ї–Є—З–∞—О—В—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Љ–Њ–ї–Њ–і–Њ–≥–Њ –Є –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞. –Ґ–∞–Ї –Ї–∞–Ї –њ—А–µ–њ–∞—А–∞—В –Є–Љ–µ–µ—В 2 –Њ—Б–љ–Њ–≤–љ—Л—Е –њ—Г—В–Є –≤—Л–≤–µ–і–µ–љ–Є—П (—З–µ—А–µ–Ј –њ–Њ—З–Ї–Є –Є —Б –ґ–µ–ї—З—М—О), —В–Њ –њ—А–Є —Г–Љ–µ—А–µ–љ–љ–Њ–Љ –љ–∞—А—Г—И–µ–љ–Є–Є —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї/–њ–µ—З–µ–љ–Є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –і–Њ–Ј—Л –љ–µ —В—А–µ–±—Г–µ—В—Б—П [6–8]. –°—В–∞—А—В–Њ–≤–∞—П –і–Њ–Ј–∞ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ – 10 –Љ–≥/—Б—Г—В, –≤ —В.—З. —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –Є –њ—А–Є –љ–µ—В—П–ґ–µ–ї–Њ–Љ –љ–∞—А—Г—И–µ–љ–Є–Є —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї –Є –њ–µ—З–µ–љ–Є. –Я—А–Є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–Љ —Н—Д—Д–µ–Ї—В–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л –і–Њ 20–40 –Љ–≥/—Б—Г—В –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –Р–Ф [9].
–С–ї–∞–≥–Њ–і–∞—А—П —Б–≤–Њ–Є–Љ —Г–љ–Є–Ї–∞–ї—М–љ—Л–Љ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–Љ –Є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ –њ–∞—А–∞–Љ–µ—В—А–∞–Љ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –Р–У –Є –•–°–Э, –≤ —В.—З. —Б –њ–Њ—Б—В–Є–љ—Д–∞—А–Ї—В–љ—Л–Љ –Ї–∞—А–і–Є–Њ—Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ, –°–Ф –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –Љ–Є–Њ–Ї–∞—А–і–∞.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї –≤ –і–Њ–Ј–µ 10–40 –Љ–≥/—Б—Г—В —Б–љ–Є–ґ–∞–µ—В –Р–Ф –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 14–29/7–18 –Љ–Љ —А—В. —Б—В. –Я–Њ –і–∞–љ–љ—Л–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞ —Г –±–Њ–ї—М—И–µ–є —З–∞—Б—В–Є –±–Њ–ї—М–љ—Л—Е —Б –љ–µ—В—П–ґ–µ–ї–Њ–є –Р–У (–Њ—В 50 –і–Њ 92%) –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В —А–∞—Б—Л, –њ–Њ–ї–∞ –Є –њ—А–Є –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –Р–У —Г –њ–Њ–ґ–Є–ї—Л—Е [11]. –Я—А–Є –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–Љ –њ—А–Є–µ–Љ–µ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ —Б–љ–Є–ґ–∞–µ—В –Р–Ф –≤ —В–µ—З–µ–љ–Є–µ —Б—Г—В–Њ–Ї, –≤ —В.—З. –Є –≤ —А–∞–љ–љ–Є–µ —Г—В—А–µ–љ–љ–Є–µ —З–∞—Б—Л [12].
–Э–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–µ —П–≤–ї–µ–љ–Є—П –њ—А–Є –њ—А–Є–µ–Љ–µ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –≤—Б—В—А–µ—З–∞—О—В—Б—П —А–µ–і–Ї–Њ –Є, –њ–Њ –і–∞–љ–љ—Л–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л —Б —В–∞–Ї–Њ–≤—Л–Љ–Є –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ. –Я—А–Є –њ—А–Є–µ–Љ–µ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –љ–µ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П «–≥–Є–њ–Њ—В–Њ–љ–Є—П –њ–µ—А–≤–Њ–є –і–Њ–Ј—Л», —З—В–Њ –і–µ–ї–∞–µ—В –µ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э, –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –і–Є—Г—А–µ—В–Є–Ї–Є. –Я—А–µ–њ–∞—А–∞—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–µ –≤–ї–Є—П–µ—В –љ–∞ —Г—А–Њ–≤–µ–љ—М –∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–∞, –∞ —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –љ–∞ —Д–Њ–љ–µ –µ–≥–Њ –њ—А–Є–µ–Љ–∞ —А–µ–ґ–µ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≥–Є–њ–µ—А–Ї–∞–ї–Є–µ–Љ–Є—П. –Ъ–∞—И–µ–ї—М –њ—А–Є –њ—А–Є–µ–Љ–µ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –≤—Б—В—А–µ—З–∞–µ—В—Б—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —А–µ–ґ–µ, —З–µ–Љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –і—А—Г–≥–Є–Љ–Є –Є–Р–Я–§ (—А–Є—Б. 5) [10]. –Я—А–Є–µ–Љ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞, –Ї–∞–Ї –Є –≤—Б–µ—Е –Є–Р–Я–§, –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ –±–µ—А–µ–Љ–µ–љ–љ—Л–Љ, –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Б—В–µ–љ–Њ–Ј–∞ –Њ–±–µ–Є—Е –њ–Њ—З–µ—З–љ—Л—Е –∞—А—В–µ—А–Є–є –Є —А–µ–∞–Ї—Ж–Є–є –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є.
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —Г –±–Њ–ї—М–љ—Л—Е –Р–У –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞–µ—В —З–∞—Б—В–Њ—В—Г —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є –Є —Б–Љ–µ—А—В–Є –Њ—В –≤—Б–µ—Е –њ—А–Є—З–Є–љ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ (—А–Є—Б. 6).
–Э–∞ —Д–Њ–љ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ (–≤ —В–µ—З–µ–љ–Є–µ 12 –љ–µ–і.) –њ—А–Є–µ–Љ–∞ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ, –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є –њ–ї–∞—Ж–µ–±–Њ, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ (—А–Є—Б. 7). –Я—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –Ї–∞–њ—В–Њ–њ—А–Є–ї–Њ–Љ –Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –Є–љ–≥–Є–±–Є—А—Г–µ—В –Љ–Є–Њ–Ї–∞—А–і–Є–∞–ї—М–љ—Л–є –Р–Я–§, —З—В–Њ –≤–µ–і–µ—В –Ї –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О –Ї–∞–Ї —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є, —В–∞–Ї –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є —Д—Г–љ–Ї—Ж–Є–є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞, —Г–≤–µ–ї–Є—З–µ–љ–Є—О —Г–і–∞—А–љ–Њ–≥–Њ –Є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—К–µ–Љ–Њ–≤, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є —Б–Ї–Њ—А–Њ—Б—В–Є –Є–Ј–≥–љ–∞–љ–Є—П. –Э–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –њ—А–Є —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є –Р–Ф –љ–∞ —Ж–µ–ї–µ–≤–Њ–Љ —Г—А–Њ–≤–љ–µ –љ–µ —В–Њ–ї—М–Ї–Њ –љ–µ –Њ—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є—П –њ–Њ—З–µ—З–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Є –њ–Њ—З–µ—З–љ–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є – –љ–∞–њ—А–Њ—В–Є–≤, –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Н—В–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≤–Њ–Ј—А–∞—Б—В–∞—О—В. –Я—А–Є —Н—В–Њ–Љ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –њ—А–Њ—В–µ–Є–љ—Г—А–Є–Є. –Т–∞–ґ–љ–Њ, —З—В–Њ —Н—В–Є –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –љ–∞–±–ї—О–і–∞—О—В—Б—П –Є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ – –њ—А–Є —Б–Њ—З–µ—В–∞–љ–Є–Є –Р–У —Б –°–Ф. –§–Њ–Ј–Є–љ–Њ–њ—А–Є–ї, –Ї–∞–Ї –Є –і—А—Г–≥–Є–µ –Є–Р–Я–§, –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –љ–µ–≥–∞—В–Є–≤–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Г—А–Њ–≤–љ—П –≥–ї—О–Ї–Њ–Ј—Л –≤ –Ї—А–Њ–≤–Є [13, 14]. –Х—Б—В—М –і–∞–љ–љ—Л–µ –Њ —Б–љ–Є–ґ–µ–љ–Є–Є –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є Toll-—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е –Р–У —Б –љ–∞—А—Г—И–µ–љ–Є–µ–Љ —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї. –≠—В–Њ –Љ–Њ–ґ–µ—В —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞—В—М –Њ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–Љ –і–µ–є—Б—В–≤–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞, —З—В–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –Є –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ –љ–µ—Д—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ [15].
–Ъ–Њ–Љ–±–Є–љ–∞—Ж–Є—П —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —Б –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞–Љ–Є –Ї–∞–ї—М—Ж–Є—П (–∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ), –і–Є—Г—А–µ—В–Є–Ї–∞–Љ–Є (–≥–Є–і—А–Њ—Е–ї–Њ—А–Њ—В–Є–∞–Ј–Є–і–Њ–Љ, –Є–љ–і–∞–њ–∞–Љ–Є–і–Њ–Љ) –њ–Њ—В–µ–љ—Ж–Є—А—Г–µ—В –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –Є —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є [16, 17].
–£ –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –љ–∞–±–ї—О–і–∞—О—В—Б—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞, –њ–Њ–≤—Л—И–µ–љ–Є–µ —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В–Є –Ї —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–µ, —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є, —Г–ї—Г—З—И–∞—О—В—Б—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞. –Ю—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –±–Њ–ї—М–љ—Л—Е. –Я—А–Є —Н—В–Њ–Љ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –≤—Л—И–µ, —З–µ–Љ –і—А—Г–≥–Є–Љ–Є –Є–Р–Я–§, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є —Н–љ–∞–ї–∞–њ—А–Є–ї–Њ–Љ (—А–Є—Б. 8).
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –≤–µ–і–µ—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О –і–∞–≤–ї–µ–љ–Є—П –≤ –ї–µ–≥–Њ—З–љ–Њ–є –∞—А—В–µ—А–Є–Є. –Ґ–∞–Ї, –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є C. Martiniuc, A. Braniste, T. Braniste (2012) –љ–∞ —Д–Њ–љ–µ 2-–Љ–µ—Б—П—З–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ —Б—А–µ–і–љ–µ–≥–Њ –Є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –≤ –ї–µ–≥–Њ—З–љ–Њ–є –∞—А—В–µ—А–Є–Є [19].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Є–Р–Я–§ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї –≤—Б–ї–µ–і—Б—В–≤–Є–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л —Б–њ–Њ—Б–Њ–±–µ–љ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞—В—М –Ї–∞–Ї —Ж–Є—А–Ї—Г–ї–Є—А—Г—О—Й—Г—О, —В–∞–Ї –Є —В–Ї–∞–љ–µ–≤—Г—О –†–Р–Р–°. –§–Њ–Ј–Є–љ–Њ–њ—А–Є–ї –љ–µ —В–Њ–ї—М–Ї–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ —Б–љ–Є–ґ–∞–µ—В –Р–Ф, –љ–Њ –Є –Њ–±–ї–∞–і–∞–µ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ –Њ—А–≥–∞–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, —З—В–Њ –і–µ–ї–∞–µ—В –µ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–У –Є –°–Ф. –§–Њ–Ј–Є–љ–Њ–њ—А–Є–ї —Г–ї—Г—З—И–∞–µ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ —В–µ—З–µ–љ–Є–µ –•–°–Э –Є –њ–Њ–≤—Л—И–∞–µ—В –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ґ–µ—А–∞–њ–Є—П —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П. –Я—А–µ–њ–∞—А–∞—В –Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В–∞—А—И–Є—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ, –њ—А–Є –љ–µ—В—П–ґ–µ–ї–Њ–Љ –љ–∞—А—Г—И–µ–љ–Є–Є —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї –Є –њ–µ—З–µ–љ–Є.
![–†–Є—Б. 1. –†–Њ–ї—М –†–Р–Р–° –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (–°–Р–° вАУ —Б–Є–Љ–њ–∞—В–Њ–∞–і—А–µ–љ–∞–ї–Њ–≤–∞—П —Б–Є—Б—В–µ–Љ–∞) [–њ–Њ –У.–Т. –Ф–Ј—П–Ї, –Ы.–Ш. –Т–∞—Б–Є–ї—М–µ–≤–∞, –Р.–Р. –•–∞–љ—О–Ї–Њ–≤]](/data/articles/Image/t21/n36/1831-1.gif)

![–†–Є—Б. 5. –У–ї–∞–≤–љ—Л–µ –њ—А–Є—З–Є–љ—Л –Њ—В–Љ–µ–љ—Л –Є–Р–Я–§ —Г –±–Њ–ї—М–љ—Л—Е —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О (SPICE Registry) [Bart B.A. et al. Eur Heart J. 1999. Vol. 20. –†. 1182вАУ1190]](/data/articles/Image/t21/n36/1831-4.gif)
![–†–Є—Б. 6. –°—А–∞–≤–љ–µ–љ–Є–µ –≤–ї–Є—П–љ–Є—П —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –љ–∞ —Б–Љ–µ—А—В–љ–Њ—Б—В—М –Є —З–∞—Б—В–Њ—В—Г —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (–љ–∞ 100 –±–Њ–ї—М–љ—Л—Е –≤ –≥–Њ–і) [13]](/data/articles/Image/t21/n36/1831-5.gif)
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Ь–∞—А–µ–µ–≤ –Т.–Ѓ. –С–ї–Њ–Ї–∞–і–∞ —А–µ–љ–Є–љ-–∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ-–∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л –љ–∞ —А–∞–Ј–љ—Л—Е —Г—А–Њ–≤–љ—П—Е // –Я—А–∞–Ї—В–Є–Ї—Г—О—Й–Є–є –≤—А–∞—З. 2000. вДЦ 18. –°. 23–24.
2. Schrier R.W., Abraham W.T. Mechanisms of disease: Hormones and hemodynamics in heart failure // New Engl. J. Med. 1999. Vol. 341. вДЦ 8. P. 577–585.
3. –°–Є–і–Њ—А–µ–љ–Ї–Њ –С.–Р., –Я—А–µ–Њ–±—А–∞–ґ–µ–љ—Б–Ї–Є–є –Ф.–Т. –Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є. –І. 3. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –Є –±–ї–Њ–Ї–∞—В–Њ—А—Л –Р–Ґ1-–∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Ь.: –Я–µ—А—Б–Є–і, 2001. 164 —Б.
4. Dihn D.T., Frauman A.G., Jonston C.I., Fabiani C.I. Angiotensin receptors: distribution, signaling and function // Clinical Sci. 2001. Vol. 100. P. 481–492.
5. Opie L.H. Angiotensin converting enzyme inhibitors. 3th edition. N.Y.: Wiley-Liss, 1999.
6. –°–Є–і–Њ—А–µ–љ–Ї–Њ –С.–Р., –Я—А–µ–Њ–±—А–∞–ґ–µ–љ—Б–Ї–Є–є –Ф.–Т., –С–∞—В—Л—А–∞–ї–Є–µ–≤ –Ґ.–Р. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –Є –Р–Ґ1-–∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤—Л–µ –±–ї–Њ–Ї–∞—В–Њ—А—Л –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞. –І. 3. –Ь.: –Ч–Р–Ю «–Я—А–µ—Б–Є–і-–Р–ї—М—П–љ—Б», 2004.
7. Guthrie R. Fosinopril: an overview // Am J Cardiol. 1993. Vol. 72. –†. 22–24.
8. Grover G.J., Sleph P.G., Dzwonczyk S. et al. Effects of different angiotensin-converting enzyme (ACE) inhibitors on ischemic isolated rat hearts: relationship between cardiac ACE inhibition and cardioprotection // J Pharmacol Exp Ther. 1991. Vol. 257. –†. 919–929.
9. –§–µ–і–µ—А–∞–ї—М–љ–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –њ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤. –Ь., 2013.
10. Martin L.C., Velasco-Cornejro I.F., Franco R.J. Treatment of mild and moderate hypertension with fosinopril. Comparison of adverse effects with other antihypertensive agents // Arq Bras Cardiol. 1994. Vol. 62 (5). –†. 369–374.
11. Pool J.L. Antihypertensive effect of fosinopril, a new angiotensin-converting enzyme inhibitor: Findings on the Fosinopril Study Group II // Clin Ther. 1990. Vol. 12. –†. 520–527.
12. Anderson R.J., Duchin K.L., Gore R.D. et al. Once-daily fosinopril in the treatment of hypertension // Hypertension. 1991. Vol. 17. –†. 636–642.
13. Tatti P., Guarisco R. Pahor M. et al. Outcome results of the Fosinopril Versus Amlodipine Cardiovascular Events Randomized Trial (FACET) in patients with hypertension and NIDDM // Diabetes Care. 1998. Vol. 21 (4). –†. 597–603.
14. Cheung B.M., Lau C.P. Fosinopril reduces left ventricular mass in untreated hypertensive patients: a controlled trial // Br J Clin Pharmacol. 1999 Feb. Vol. 47 (2). –†. 179–187.
15. Tang T.F., Zhou Q.L., Zhu L.L., Tang R., Ao X. Effects of fosinopril and losartan on the expression of Toll-like receptor 4 in renal tubular epithelia cells // Zhong Nan Da, Xue Xue Bao, Yi Xue Ban. 2008 Oct. Vol. 33 (10). –†. 958–965.
16. Meng Y., Zhang Z., Liang X., Wu C., Qi G. Effects of combination therapy with amlodipine and fosinopril administered at different times on blood pressure and circadian blood pressure pattern in patients with essential hypertension // Acta Cardiol. 2010 Jun. Vol. 65 (3). –†. 309–314.
17. Zhang J.L., Qin Y.W., Zheng X., Qiu J.L., Zhao X.X., Zou D.J. Combination therapy with angiotensin-converting enzyme inhibitors and indapamide impairs glucose tolerance in Chinese hypertensive patients // Blood Press. 2010 Apr. Vol. 19 (2).110-8.
18. Blumenthal M. Treatment of congestive heart failure: experience with fosinopril // Am J Hypertens. 1997 Oct. Vol. 10 (10 Pt 2). –†. 289–298.
19. Martiniuc C., Braniste A., Braniste T. Angiotensin converting enzyme inhibitors and pulmonary hypertension // Rev Med Chir Soc Med Nat Iasi. 2012 Oct-Dec.Vol. 116 (4). –†. 1016–1020.












