Относительный риск ССЗ
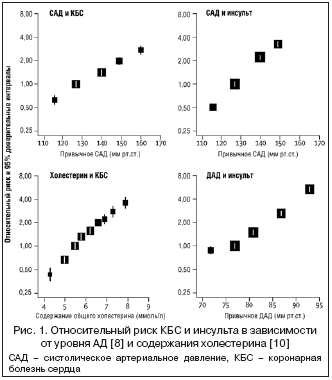
Мета–анализ индивидуальных данных больных, полученных в ходе проведения проспективных обсервационных исследований как в развитых, так и в развивающихся странах, выявил сходные корреляции между содержанием холестерина/АД и значениями показателей относительного риска ССЗ [4,7–9]. Как показано на рисунке 1, при специфических абсолютных изменениях АД в пределах от 110/70 мм рт.ст. до 170/105 мм рт.ст. относительный кардиоваскулярный риск постоянно меняется [2–4,7–10]. В этом широком диапазоне значений разница диастолического АД (ДАД) в 5 мм рт.ст. ассоциируется с относительным изменением коронарного риска на 20%, а риска инсульта – на 35% [3]. Разница уровня общего холестерина в 0,6 ммоль/л влечет за собой относительное изменение коронарного риска на 27% [3], причем это справедливо в границах содержания холестерина от 4,0 до 9,0 ммоль/л [7,10]. Между уровнем холестерина в крови и частотой встречаемости ишемического инсульта также существует положительная корреляция, в случае же геморрагического инсульта наличие такой взаимосвязи определить сложно [11]. И хотя результаты обсервационных исследований свидетельствуют о более выраженной ассоциации этих факторов с показателями кардиоваскулярного риска у молодых больных по сравнению с пожилыми, во всех возрастных группах относительные корреляции остаются постоянными [4,7,10].
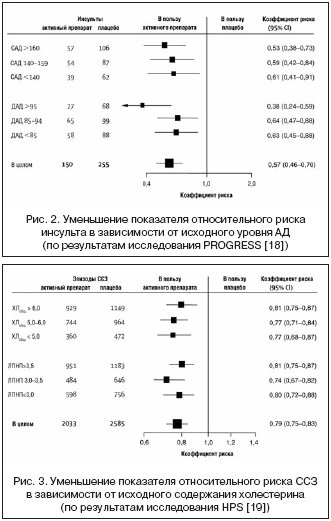
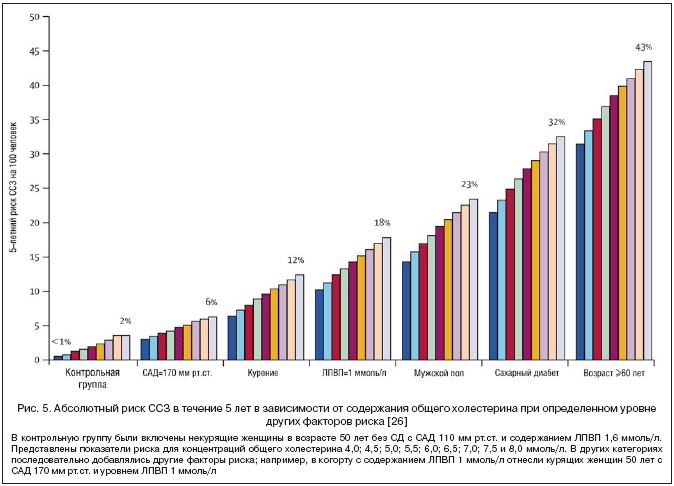
Данные, полученные в процессе рандомизированных испытаний гипотензивных и гипохолестеринемических препаратов, подтверждают исходы обсервационных исследований, приведенные выше. Эти испытания показали, что при фиксированном абсолютном снижении АД или уровня холестерина показатель риска ССЗ уменьшается на ту же самую величину, которая прогнозируется обсервационными исследованиями [3,12–15]. В большинстве случаев это происходит в течение 5 лет, что составляет типичный срок проведения испытаний. Сокращение относительного риска также коррелирует с величиной АД и содержанием холестерина до начала лечения. В ряде клинических испытаний не устанавливали никакого изначального порога АД [16,17], и показатели относительного риска снижались аналогичным образом вне зависимости от исходного АД. Так, на рисунке 2 представлена динамика постоянного снижения относительного риска инсульта в виде тертилей исходного АД, отмечаемая в проекте PROGRESS [17,18]; эти испытания гипотензивных препаратов проводили в когорте численностью более 6 тыс. человек с верифицированными диагнозами ССЗ. Аналогичные наблюдения были сделаны и при изучении гиполипидемических препаратов, например, в исследовании HPS (Исследование защиты сердца) [19], согласно дизайну которого более 20 тыс. пациентов группы высокого риска с содержанием общего холестерина свыше 3,5 ммоль/л были подвергнуты рандомизации для получения статинов или плацебо. Примерно в четверти случаев концентрация общего холестерина не превышала 5,0 ммоль/л, а ЛПВП – 3,0 ммоль/л, и по всем тертилям исходного содержания холестерина относительный кардиоваскулярный риск снижался одинаково (рис. 3).
Результаты обсервационных исследований свидетельствуют об ослаблении с возрастом относительной корреляции между уровнем холестерина или АД и риском [4,20,21], однако, по данным рандомизированных испытаний, явной ассоциации между эффективностью лечения и возрастом выявлено не было [16,19,22,23]. В любом случае, уменьшаются ли с возрастом показатели относительного риска с меньшей амплитудой на самом деле или же этот феномен является артефактом, не имеет особого значения, поскольку у пожилых больных показатели абсолютного риска до начала лечения обычно гораздо выше по сравнению с теми, кто моложе (а следовательно, у них можно добиться более ощутимой терапевтической выгоды) [16,17,19,22].
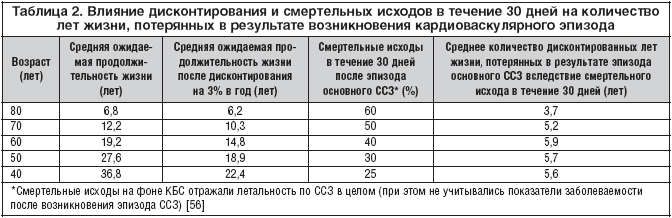
Абсолютный риск ССЗ
Абсолютный риск ССЗ (т.е. вероятность того, что в течение определенного времени у пациента возникнет эпизод ССЗ) определяется совокупным влиянием всех факторов кардиоваскулярного риска [24], причем у лиц с одинаковой концентрацией холестерина или АД абсолютная разница между значениями этих показателей может варьировать более чем в 20 раз [10]. Наиболее значимыми критериями прогноза риска ССЗ являются возраст, симптоматика ССЗ в анамнезе и патофизиологические изменения (гипертрофия левого желудочка, нарушение функции почек), хотя абсолютный риск также детерминируется и взаимодействием других факторов, таких как повышение АД и уровня липидов, курение, мужской пол и т.д. [25]. В отсутствие других факторов риска каждый из них в отдельности не оказывает ощутимого влияния на абсолютный риск ССЗ у конкретного пациента, но при наличии нескольких оно заметно нарастает. Так, на рисунке 4 отражено влияние последовательно суммируемых факторов риска на абсолютный кардиоваскулярный риск у испытуемых с различными значениями ДАД, а на рисунке 5 – последствия суммирования факторов риска у лиц с различным содержанием холестерина в крови. У некурящей женщины 50 лет без сахарного диабета (СД) с уровнем общего холестерина 4,0 ммоль/л, ЛПВП 1,6 ммоль/л и САД 130 мм рт.ст. показатель 5–летнего кардиоваскулярного риска равен 1%. При повышении содержания общего холестерина до 7 ммоль/л и снижении уровня ЛПВП до 1 ммоль/л в сочетании с курением 5–летний риск у той же самой женщины будет составлять уже 10%, а при сопутствующем СД – 20%, даже несмотря на то же самое АД. Аналогичные изменения значений показателей прогнозируемого абсолютного риска ССЗ будут наблюдаться и в случае стабильного содержания общего холестерина и ЛПВП, но сдвигов профиля других критериев. В результате такой синергии абсолютный кардиоваскулярный риск у больных с низким АД или холестерином может оказаться гораздо больше по сравнению с теми, у кого высокий уровень только одного из этих факторов риска. Описанные наблюдения лишний раз подтверждают ограниченную с клинической точки зрения значимость таких понятий, как гипертензия или гиперхолестеринемия.
Продемонстрированное в ходе клинических испытаний уменьшение абсолютного кардиоваскулярного риска, равно как и относительные изменения показателей риска, коррелирует с абсолютными преимуществами, прогнозируемыми по результатам проспективных обсервационных исследований. Если говорить о специфическом снижении АД или уровня холестерина, то данные, полученные в рандомизированных клинических испытаниях, свидетельствуют о том, что абсолютный выигрыш от лечения прямо пропорционален значению показателя абсолютного риска до начала проведения терапии (рис. 6 и 7) [22,27–29]. Эти рисунки также иллюстрируют одинаковое относительное уменьшение риска вне зависимости от включения в исследование больных с инсультами или сосудистыми заболеваниями в анамнезе. Напротив, у лиц с ССЗ в анамнезе абсолютная разница в терапевтической выгоде в 2–3 раза превышают таковую по сравнению с испытуемыми без анамнеза ССЗ.
Оценка абсолютного
кардиоваскулярного риска
Учитывая широкий диапазон значений показателя гипотетического абсолютного кардиоваскулярного риска у больных с одинаковым АД и уровнем холестерина, тщательный анализ этого критерия имеет решающее значение для эффективного устранения риска в клинической практике. Результаты исследования, проведенного в Северной Америке с целью проверки у врачей–клиницистов навыков количественной оценки кардиоваскулярного риска и терапевтической выгоды, наглядно демонстрируют, что компетентность врачей общей практики и узких специалистов в этом вопросе недостаточна [30]. Для клиницистов характерна завышенная оценка кардиоваскулярного риска и терапевтической выгоды. У гипотетического больного с повышенным холестерином семейные врачи и терапевты переоценивают 5–летний риск инфаркта миокарда более чем в 3 раза, абсолютную терапевтическую выгоду – еще больше; узкие специалисты переоценивают риск инфаркта миокарда в 2 раза, а терапевтическую выгоду – в 3 раза.
В настоящее время разработаны многочисленные шкалы (в том числе электронные) для прогнозирования кардиоваскулярного риска (табл. 1). И хотя уровень их интерпретации порой вызывает сомнения, появляется все больше данных в пользу того, что такие шкалы прогнозирования риска могут стать для современной клинической практики весьма полезным инструментом [39,40], позволяющим сократить риск ССЗ [41,42]. Многие шкалы были заимствованы из Фрамингемского исследования. Эти когортные испытания проводились в выборке объемом около 5 тыс. человек (белые американцы) на протяжении более чем 50 лет, а численность изучаемой группы поддерживалась за счет включения в нее пациентов из исходной когорты [43]. Шкалы также разрабатывали с учетом итогов исследования PROCAM (Проспективное кардиоваскулярное Мюнстерское исследование), стартовавшего в 1974 г., в которое вошло примерно 20 тыс. человек трудоспособного возраста с севера Германии [44], и Проспективного исследования по диабету, проводившегося в Великобритании с учетом 5 тыс. больных СД [35]. Обнародовано и еще несколько шкал оценки показателя смертности на фоне ССЗ. Одна из них базируется на данных, которые были получены у 47088 взрослых пациентов с повышенным АД, участвовавших в 8 европейских и североамериканских испытаниях [37], а другая – на ранжировании в ходе европейского проекта SCORE географических зон с высокими и низкими показателями риска в 12 когортах (2,7 млн. человеко–лет наблюдения) [38].
В большинстве случаев шкалы создавали с использованием регрессионных моделей, хотя специалистам, привлеченным к исследованию PROCAM, удалось разработать шкалу на основании нейрональных сетей, которая, как они полагают, повысит точность прогноза [36]. Их модель нейрональных сетей позволяет спрогнозировать по подгруппе высокого риска (в которую входит лишь 7,9% всех испытуемых) около 75% эпизодов ССЗ в изучаемой когорте на протяжении 10 лет, в то время как регрессионная модель позволяет спрогнозировать по 8,4% больных лишь 46% таких событий. Однако эффективность использования этих моделей еще нужно подтвердить в независимой популяции, а кроме того, обычно модели нейрональных сетей воспроизвести сложнее, чем регрессионные модели.
Несколько раз анализировали значимость шкал прогнозирования риска Фрамингемского исследования, но результаты оказались противоречивыми. По данным ученых, привлеченных к Фрамингемскому исследованию, предложенные ими шкалы достаточно легко воспроизвести в популяции лиц с частотой встречаемостью коронарной патологии, аналогичной таковой в Северной Америке, а применительно к другим группам населения эти шкалы можно перекалибровать [45]. Другие сообщают о менее благоприятных исходах в отношении дискриминационной способности и воспроизводимости прогностических функций Фрамингемского исследования [46,47]. В большинстве случаев анализ носил сравнительный характер, например, сопоставляли показатели относительного риска или площади под характеристическими кривыми. Но такой подход не позволяет проанализировать абсолютную прогностическую значимость (что более важно с клинической точки зрения), в частности, долю событий, спрогнозированных в небольшой по объему определимой группе высокого риска, поддающейся лечению. Модели, включающие более широкий спектр факторов риска [35,36], обладают большей прогностической способностью, чем те, в которые введено меньше факторов [26]; следовательно, есть определенный потенциал для дальнейшего совершенствования этих моделей, а значимость таких прогностических факторов, как С–реактивный белок [48], еще предстоит оценить.
При разработке шкал прогнозирования риска следует учитывать минимальное требование – использовать данные по популяции с достаточно однородными профилями риска и частотой встречаемости соответствующих эпизодов ССЗ, в ином случае потребуется калибровка в рамках изучаемой популяции [45]. Также необходимо определить долю лиц, которых можно классифицировать в зависимости от значения показателя абсолютного риска с тем, чтобы установить практически целесообразные и экономически рациональные пороги лечения. В идеале модели прогнозирования следует генерировать локально или же, по меньшей мере, анализировать их значимость в выборке местных жителей [49]. Учитывая все более активное внедрение электронных историй болезни, теоретически возможно связать профили факторов риска с эпизодами ССЗ в большой популяции [50,51]. Достижения в сфере информационных технологий дают возможность быстро сформировать шкалу прогнозирования кардиоваскулярного риска для конкретной группы лиц и применять ее в качестве одного из рутинных инструментов врачебной практики.
Неразрешенные проблемы
Предполагаемое увеличение продолжительности жизни вследствие профилактики эпизода ССЗ.
Явное замешательство вызывает наличие взаимосвязи между краткосрочным абсолютным риском (например, 5–летним риском эпизода ССЗ) и долгосрочной абсолютной терапевтической выгодой (например, предполагаемым увеличением продолжительности жизни, как результатом профилактики кардиоваскулярного явления). С возрастом значение показателя краткосрочного абсолютного риска, а следовательно, и краткосрочная абсолютная терапевтическая выгода нарастают по экспоненте (чем старше больной, тем эффективнее лечение, однако у лиц более молодого возраста преимущества от проведения превентивной терапии заметнее из–за большей предполагаемой продолжительности жизни) [52]. Хотя в результате развития эпизода ССЗ более молодые пациенты потенциально потеряют больше лет жизни по сравнению с пожилыми людьми, после внесения поправок на дисконтирование продолжительности жизни и смертельные исходы эти различия минимизируются [53]. Описание дано ниже и представлено в таблице 2.
Во–первых, большинство людей ценят в первую очередь не отдаленное, а ближайшее будущее [54]. Следовательно, чтобы обоснованно сравнивать потенциально потерянные годы жизни из–за возникновения эпизода ССЗ в том или ином возрасте, необходимо провести дисконтирование. Это позволяет придавать меньше значения годам жизни, потенциально потерянным в отдаленном будущем. С учетом стандартной частоты дисконтирования – 3%, рекомендованной Американской группой экспертов по изучению экономической эффективности [55] (т.е. каждый последующий год жизни оценивается на 3% ниже, чем предыдущий), средняя предполагаемая продолжительность жизни 40–летнего мужчины снизится с фактических 37 лет до дисконтированных 22 лет, а 70–летнего мужчины – с 12 фактических лет до 10 дисконтированных лет. Во–вторых, в пожилом возрасте вероятность смертельного исхода на фоне эпизода ССЗ гораздо выше, чем у более молодых лиц. Так, в возрастной группе 65 лет – 74 года показатель 30–дневной смертности в результате развития острых коронарных явлений составляет более 50%, а среди больных моложе 50 лет – 25% [56]. Таким образом, если у пациента старше 65 лет возник один из основных кардиоваскулярных эпизодов, то предполагаемая оставшаяся продолжительность жизни уменьшится более чем в половину (вплоть до смертельного исхода в первые 30 суток), а у больного менее 50 лет – только на четверть.
Из–за двукратной разницы в предполагаемой продолжительности жизни у 40– и 70–летних пациентов, возникающей после дисконтирования, и удвоения числа смертельных исходов в возрасте 70 лет (по сравнению с 40 годами) количество дисконтированных лет жизни, потерянных в обеих возрастных группах после развития эпизода ССЗ, становится одинаковым (табл. 2). Поэтому не исключено, что мероприятия, направленные на профилактику таких явлений, в действительности приносят меньше дополнительных долгосрочных преимуществ у лиц в возрасте 40 лет по сравнению с 70–летними больными, чем можно было бы предполагать. При проведении этих расчетов не принимались во внимание показатели заболеваемости или инвалидности вследствие возникновения эпизода ССЗ или сопутствующих заболеваний, а ведь более молодые люди, у которых возник эпизод ССЗ без смертельного исхода, могут потерять больше лет трудоспособной жизни, чем пожилые пациенты. На фоне эпизода ССЗ без смертельного исхода пожилые чаще становятся физически нетрудоспособными, они также более предрасположены к инвалидизации из–за других проблем со здоровьем. Однако психологическая травма, возникающая после эпизода ССЗ, оказывается у лиц этого возраста менее тяжелой. Таким образом, в различных возрастных группах сложно однозначно оценить последствия инвалидизации на фоне эпизода ССЗ, которая имеет как физические, так и психологические аспекты.
Данные, представленные в таблице 2, заставляют предположить, что в результате возникновения эпизода ССЗ больные старше 80 лет потенциально теряют меньше дисконтированных лет ожидаемой жизни, в первую очередь из–за того, что предполагаемая продолжительность жизни в этой возрастной группе в целом ниже. Тогда при разработке шкалы прогнозируемого риска на основании его абсолютного показателя было бы целесообразно вносить некоторую поправку, если предполагаемая продолжительность жизни невелика. В будущем можно будет пересмотреть удельный вес случаев инвалидности в зависимости от возраста.
Цели лечения
В ходе нескольких исследований с изучением кардиоваскулярных исходов испытуемых рандомизировали для назначения стандартной или более интенсивной схемы гипотензивной терапии. Полученные данные демонстрируют более заметное сокращение частоты возникновения эпизодов ССЗ на фоне интенсивного лечения: так, разница показателей риска инсульта составила 20% (95% ДИ 2–35), коронарного риска – 19% (2–33), а основных ССЗ – 15% (4–24) [14,59]. Активное использование гиполипидемических препаратов обеспечивает протективное действие в отношении ССЗ, превышающее аналогичный эффект стандартных подходов к лечению статинами [58], а в процессе гипохолестеринемической терапии прослеживается дозозависимая корреляция с исходами ССЗ [3,59]. Таким образом, наибольшей терапевтической выгоды удается добиться, если снижать уровень холестерина и АД как можно больше. Поскольку побочные эффекты лекарственных средств обычно являются дозозависимыми, а факторы риска ССЗ обладают синергичным влиянием, наиболее эффективной стратегией уменьшения кардиоваскулярного риска будет та, которая направлена на умеренное снижение уровня нескольких факторов риска, а не интенсивное воздействие на единственный критерий (хотя экспериментов, в процессе которых осуществляли бы такое сравнение, пока не было). Одним из препятствий на пути широкого внедрения этой стратегии является ее высокая стоимость и сложность реализации; существенную помощь может оказать т.н. политаблетка, в состав которой входят различные лекарственные соединения в небольшой дозировке [59]. Назначение такого препарата, включающего комбинацию низких доз активных компонентов, особенно актуально для пациентов группы высокого риска, у которых уровень различных факторов риска повышен лишь незначительно. Такой подход к лечению также согласуется с принципами стратегии абсолютного риска, в соответствии с которыми ни один фактор риска сам по себе не имеет решающего значения при выборе схемы терапии или определении ее задач.
Приоритетная задача лечения – не стараться достичь наиболее оптимального уровня факторов риска у конкретного индивидуума, а попытаться сохранить принимаемый им набор лекарственных препаратов. В повседневной практике амплитуду ответа пациента на терапию сложно определить точно, даже если анализировать один фактор риска неоднократно. Так, используя отклонения в содержании холестерина на индивидуальном и популяционном уровне, Irwig и соавт. [60] попытались оценить, сколько раз необходимо повторить обследование, чтобы с максимально возможной точностью вычислить концентрацию холестерина у конкретного больного и амплитуду ответа на лечение. Установлено, что даже при повторных измерениях границы доверительного интервала вокруг этой величины остаются широкими (то же самое справедливо и в отношении уровня АД) [61]. По этим причинам следует уделять меньше внимания решению задач лечения, касающихся специфических факторов риска, направляя больше усилий на выявление лиц с высоким риском и устранение его множественных факторов. В клинической медицине существует т.н. принцип «выстрелил–забыл» [62], в соответствии с которым целой группе лиц назначают статины в небольшой стандартной дозе, не учитывая при этом содержание холестерина в крови. Возможно, следует модифицировать этот подход и привести его к формуле «прицелился (в когорту высокого риска) – выстрелил (политаблеткой, содержащей низкие дозы лекарственных компонентов) – забыл (про индивидуальные факторы риска, но не строгое соблюдение плана лечения)».
Терапевтическая выгода,
ожидаемая пациентом
Вопросы, касающиеся терапевтической выгоды, ожидаемой пациентом на фоне проведения профилактических мероприятий, освещены мало, но не исключено, что сами больные (равно как и врачи) гипертрофируют кардиоваскулярный риск и терапевтическую выгоду [30]. Исследователи проанализировали пороговое значение терапевтической выгоды от применения гипотетического гипохолестеринемического препарата, ниже которого испытуемые не будут готовы принимать его [63]. Для этого исследования были отобраны 307 человек – выписавшиеся из отделения кардиореанимации; получавшие кардиопротекторы, но не имевшие в анамнезе инфаркта миокарда; не использовавшие никаких лекарственных средств и не имевшие в анамнезе инфаркта миокарда. В первых двух группах медиана пороговых значений абсолютной терапевтической выгоды в течение 5 лет составила 20%, а в третьей группе – 30%. Это значительно больше, чем выгода, ожидаемая на фоне большинства стандартных схем лечения (она редко превышает 10–15% в абсолютном выражении). Учитывая явное несоответствие реальных преимуществ от проводимой терапии ожиданиям пациента, следует отдавать основной приоритет оценке представлений больного о риске и возможной терапевтической выгоде. Именно это и обусловливает недопонимание целесообразности многих профилактических мероприятий.
Заключение
Индивидуализированное снижение уровня кардиоваскулярного риска должно определяться в первую очередь масштабом ожидаемой абсолютной терапевтической выгоды. О значимости этой выгоды плохо информированы и врачи, и больные. Следует уделять больше внимания не уровню АД и содержанию холестерина у конкретного пациента, а показателям абсолютного кардиоваскулярного риска и его детерминантам. Большинство факторов риска ССЗ нельзя отнести в категорию присутствующих или отсутствующих, а если учесть еще и синергию влияния этих факторов, то становится понятно, что величину показателя риска рассчитать не так просто. Количественная оценка кардиоваскулярного риска и терапевтической выгоды у лиц среднего и пожилого возраста должна стать общепринятой процедурой в качественной клинической практике. Пришло время изъять из словаря клинициста такие понятия, как гипертензия и гиперхолестеринемия с тем, чтобы врачи следующих поколений рассматривали в качестве объекта терапевтического приложения не факторы риска, а риск в целом.
Реферат подготовлен Е.Б. Третьяк
по материалам статьи
R. Jackson, K.M.M. Lawes, D.A. Bennet,
R.J. Milne, A. Rodgers
“Treatment with drugs to lower blood pressure
and blood cholesterol
based on an individual’s absolute cardiovascular risk”
Lancet 2005, 365: 434–441


Литература
1. Rose G. Sick individuals and sick populations. Int J Epidemiol 2001; 30: 427–32.
2. Rodgers A. Quantifying selected major risks to health. In: Murray CJL, Lopez AD, eds. The world health report 2002: reducing risks, promoting healthy life. Geneva: World Health Organization, 2002: 47–92.
3. Law MR, Wald NJ. Risk factor thresholds: their existence under scrutiny. BMJ 2002; 324: 1570–76.
4. Lewington S, Clarke R, Qizilbash N, Peto R, Collins R, for the Prospective Studies Collaboration. Age-specific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies. Lancet 2002; 360: 1903–13.
5. Alderman MH. Blood pressure management: individualised treatment based on absolute risk and the potential for benefit. Ann Intern Med 1993; 119: 329–35.
6. Jackson R, Barham P, Maling T, et al. The management of raised blood pressure in New Zealand. BMJ 1993; 307: 107–10.
7. Asia Pacific Cohort Studies Collaboration. Cholesterol, coronary heart disease and stroke in the Asia Pacific Region. Int J Epidemiol 2003; 32: 563–72.
8. Asia Pacific Cohort Studies Collaboration. Blood pressure and cardiovascular disease in the Asia Pacific Region. J Hypertens 2003; 21: 707–16.
9. Eastern Stroke and Coronary Heart Disease Collaborative Research Group. Blood pressure, cholesterol, and stroke in eastern Asia. Lancet 1998; 352: 1801–07.
10. Neaton JD, Wentworth D, for the Multiple Risk Factor Intervention Trial Research Group. Serum cholesterol, blood pressure, cigarette smoking, and death from coronary heart disease. Overall findings and differences by age for 316,099 white men. Arch Intern Med 1992; 152: 56–64.
11. Prospective Studies Collaboration. Cholesterol, diastolic blood pressure, and stroke:13,000 strokes in 450,000 people in 45 prospective cohorts. Lancet 1995; 346: 1647–53.
12. Lawes C, Bennett D, Lewington S, Rodgers A. Blood pressure and coronary heart disease: a review of the evidence. Seminars Vasc Med 2002; 2:355–68.
13. MacMahon S, Peto R, Cutler J, et al. Blood pressure, stroke and coronary heart disease. Part 1, prolonged differences in blood
pressure: prospective observational studies corrected for regression dilution bias. Lancet 1990; 335: 765–74.
14. Turnbull F, for the Blood Pressure Lowering Treatment Trialists’ Collaboration. Effects of different blood-pressure-lowering regimens on major cardiovascular events: results of prospectivelydesigned overviews of randomised trials. Lancet 2003; 362: 1527–35.
15. Lawes CMM, Bennett DA, Feigin VL, Rodgers A. Blood pressure and stroke: an overview of published reviews. Stroke 2004; 35: 776–85.
16. The Heart Outcomes Prevention Evaluation Study Investigators. Effects of an angiotensin-converting-enzyme inhibitor, Ramipril, on cardiovascular events in high-risk patients. N Engl J Med 2000; 342: 145–53.
17. Progress Collaborative Group. Randomised trial of a perindoprilbased blood-pressure-lowering regimen among 6,105 individuals with previous stroke or transient ischaemic attack. Lancet 2001; 358: 1033–41.
18. Cruikshank J. The lowering of blood pressure after stroke (authors’ reply). Lancet 2001; 358: 1994–95.
19. Heart Protection Study Collaborative Group. MRC/BHF Heart Protection Study of cholesterol lowering with simvastatin in 20,536 high-risk individuals: a randomised placebo-controlled trial. Lancet 2002; 360: 7–22.
20. Stamler J, Wentworth D, Neaton JD. Is relationship between serum cholesterol and risk of premature death from coronary heart disease continuous and graded? JAMA 1986; 256: 2823–28.
21. Law MR, Wald NJ, Thompson SG. By how much and how quickly does reduction in serum cholesterol concentration lower risk of ischaemic heart disease? BMJ 1994; 308: 367–62.
22. Mulrow CD, Cornell JA, Herrera CR, Kadri A, Farnett L, Aguilar C. Hypertension in the elderly. Implications and generalizability of randomised trials. JAMA 1994; 272: 1932–38.
23. LaRosa JC, He J, Vupputuri S. Effect of statins on risk of coronary disease. Meta-analysis of randomized controlled trials. JAMA 1999; 282: 2340–46.
24. Kannel WB. Some lessons in cardiovascular epidemiology from Framingham. Am J Cardiol 1976; 37: 269–82.
25. D’Agostino RB, Russell MW, Huse DM, et al. Primary and subsequent coronary risk appraisal: new results from the Framingham study. Am Heart J 2000; 139: 272–81. Series www.thelancet.com Vol 365 January 29, 2005 441.
26. Anderson KV, Odell PM, Wilson PWF, Kannel WB. Cardiovascular disease risk profiles. Am Heart J 1991; 121: 293–98.
27. West of Scotland Coronary Prevention Group. West of Scotland Coronary Prevention Study: identification of high-risk groups and comparison with other cardiovascular intervention trials. Lancet 1996; 348: 1339–42.
28. Rodgers A, Neal B, MacMahon S. The effects of blood pressure lowering in cerebrovascular disease. Neurol Rev Int 1997; 2: 12–15.
29. Law MR, Wald NJ, Rudnicka AR. Quantifying effects of statins on low density lipoprotein cholestrol, ischaemic heart disease and stroke: systematic review and meta-analysis. BMJ 2003; 326: 1423.
30. Friedmann PD, Brett AS, Mayo-Smith MF. Differences in generalists’ and cardiologists’ perceptions of cardiovascular risk and the outcomes of preventive therapy in cardiovascular disease. Ann Intern Med 1996; 124: 414–21.
31. Jackson R. Updated New Zealand cardiovascular disease riskbenefit prediction guide. BMJ 2000; 320: 709–10.
32. New Zealand Guideline Group. Management of mildly raised blood pressure in New Zealand: http://www.nzgg.org.nz/guidelines/dsp_guideline_popup.cfm?&guidelineID=35.
33. Wallis EJ, Ramsay LE, Haq IU, et al. Coronary and cardiovascular risk estimation for primary prevention: validation of a new Sheffield table in the 1995 Scottish Health Survey population. BMJ 2000; 320: 671–76.
34. Wood D. Joint British recommendations on prevention of coronary heart disease in clinical practice: summary. BMJ 2000; 320: 705–08.
35. Stevens RJ, Kothari V, Adler AI, Stratton IR, Holman RR. The UKPDS risk engine: a model for the risk of coronary heart disease in Type II diabetes (UKPDS 56). Clin Sci 2001; 101: 671–79.
36. Voss R, Cullen P, Schulte H, Assmann G. Prediction of risk of coronary events in middle-aged men in the Prospective Cardiovascular Munster Study (PROCAM) using neural networks. Int J Epidemiol 2002; 31: 1253–62.
37. Pocock SJ, McCormack V, Gueyffier F, Boutitie F, Fagard RH, Boissel JP. A score for predicting risk of death from cardiovascular disease in adults with raised blood pressure, based on individual patient data from randomised controlled trials. BMJ 2001; 323: 75–81.
38. Conroy RM, Pyorala K, Fitzgerald AP, et al. Estimation of ten-year risk of fatal cardiovascular disease in Europe: the SCORE project. Eur Heart J 2003; 24: 987–1003.
39. Montgomery AA, Fahey T, Peters TJ, MacIntosh C, Sharp DJ. Evaluation of computer based clinical decision support system and risk chart for management of hypertension in primary care: randomised controlled trial. BMJ 2000; 320: 686–89.
40. Isles CG, Ritchie LD, Murchie P, Norrie J. Risk assessment in primary prevention of coronary heart disease: randomised comparison of three scoring methods. BMJ 2000; 320: 690–91.
41. Lowensteyn I, Joseph L, Levinton C, Abrahamowicz M, Steinert Y, Grover S. Can computerized risk profiles help patients improve their coronary risk? The results of the Coronary Health Assessment Study (CHAS). Prev Med 1998; 27: 730–37.
42. Hall LML, Jung RT, Leese GP. Controlled trial of effect of documented cardiovascular risk scores on prescribing. BMJ 2003; 326: 251–52.
43. Kannel WB. The Framingham study: its 50-year legacy and future promise. J Atheroscler Thromb 2000; 6: 60–66.
44. Assmann G, Cullen P, Schulte H. Simple scoring scheme for calculating the risk of acute coronary events based on the 10-year follow-up of the prospective cardiovascular Munster (PROCAM) study. Circulation 2002; 105: 310–15.
45. D’Agostino RB Sr, Grundy S, Sullivan LM, Wilson P. Validation of the Framingham coronary heart disease prediction scores: results of a multiple ethnic groups investigation. JAMA 2001; 286: 180–87.
46. Diverse Populations Collaborative Group. Prediction of mortality from coronary heart disease among diverse populations: is there a common predictive function? Heart 2002; 88: 222–28.
47. Brindle P, Emberson J, Lampe F, et al. Predictive accuracy of the Framingham coronary risk score in British men: prospective cohort study. BMJ 2003; 327: 1267.
48. Pearson TA, Mensah GA, Alexander RW, et al. Markers of inflammation and cardiovascular disease: application to clinical and public health practice: a statement for healthcare professionals from the Centers for Disease Control and Prevention and the
American Heart Association. Circulation 2003; 107: 499–511.
49. Milne R, Gamble G, Whitlock G, Jackson R. Framingham Heart study risk equation predicts first cardiovascular event rates in New Zealanders at the population level. NZ Med J 2003; 116: U662.
50. Black N. Using clinical databases in practice. BMJ 2003; 326: 2–3.
51. Lundin J, Lundin M, Isola J, Joensuu H. A web-based system for individualised survival estimation in breast cancer. BMJ 2003; 326: 29.
52. Ulrich S, Hingorani AD, Martin J, Vallance P. What is the optimal age for starting lipid lowering treatment? A mathematical model. BMJ 2000; 320: 1134–40.
53. Marshall T. Optimal age for starting lipid lowering treatment. It is more efficient to screen and treat elderly people. BMJ 2000; 321: 637.
54. Gold M, Siegel J, Russell L, Weinstein M. Cost effectiveness in health and medicine. Oxford: Oxford University Press, 1996.
55. Weinstein MC, Seigel JE, Gold MR, Kamlet MS, Russel LB. Recommendations of the panel on cost-effectiveness in health and medicine. JAMA 1996; 276: 1253–58.
56. Norris RM. Fatality outside hospital from acute coronary events in three British health districts, 1994–5. United Kingdom Heart Attack Study Collaborative Group. BMJ 1998; 316: 1065–70.
57. Neal B, MacMahon S, Chapman N. Effects of ACE inhibitors, calcium antagonists, and other blood-pressure-lowering drugs: results of prospectively designed overviews of randomised trials. Blood Pressure Lowering Treatment Trialists’ Collaboration. Lancet 2000; 356: 1955–64.
58. Cannon CP, Braunwald E, McCabe CH, et al. Intensive versus moderate lipid lowering with statins after acute coronary syndromes. N Engl J Med 2004; 350: 1495–504.
59. Wald NJ, Law MR. A strategy to reduce cardiovascular disease by more than 80%. BMJ 2003; 326: 1419.
60. Irwig L, Glasziou P, Wilson A, Macaskill P. Estimating an individual’s true cholesterol level and response to intervention. JAMA 1991; 266: 1678–85.
61. Jones DW, Appel LJ, Sheps SG, Roccella EJ, Lenfant C. Measuring blood pressure accurately: new and persistent challenges. JAMA 2003; 289: 1027–30.
62. Shepherd J. Resource management in prevention of coronary heart disease: optimising prescription of lipid-lowering drugs. Lancet 2002; 359: 2271–73.
63. Trewby PN, Reddy AV, Trewby CS, Ashton VJ, Brennan G, Inglis J. Are preventive drugs preventive enough? A study of patients’ expectation of benefit from preventive drugs. Clin Med 2002; 2: 527–33.












