–Я–Њ –і–∞–љ–љ—Л–Љ Diabetes Atlas 2000, –≤ 2000 –≥–Њ–і—Г –≤ –Љ–Є—А–µ –±—Л–ї –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ 151 –Љ–ї–љ. –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞. –Я–Њ –і–∞–љ–љ—Л–Љ 2006 –≥–Њ–і–∞, —Н—В–Њ —Г–ґ–µ 246 –Љ–ї–љ. —З–µ–ї–Њ–≤–µ–Ї, –Є–Ј –љ–Є—Е 50% – –љ–∞–Є–±–Њ–ї–µ–µ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ (40–59 –ї–µ—В). –Я–Њ –њ—А–Њ–≥–љ–Њ–Ј–∞–Љ –Т—Б–µ–Љ–Є—А–љ–Њ–є –Ю—А–≥–∞–љ–Є–Ј–∞—Ж–Є–Є –Ч–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П, –Ї 2025 –≥–Њ–і—Г —З–Є—Б–ї–Њ –±–Њ–ї—М–љ—Л—Е –°–Ф –Љ–Њ–ґ–µ—В —Г–≤–µ–ї–Є—З–Є—В—М—Б—П –≤ 2–3 —А–∞–Ј–∞ –Є —Б–Њ—Б—В–∞–≤–Є—В—М –±–Њ–ї–µ–µ 380 –Љ–ї–љ. (!) —З–µ–ї–Њ–≤–µ–Ї (–≤ 2000 –≥–Њ–і—Г —Н—В–Њ—В –њ—А–Њ–≥–љ–Њ–Ј —Б–Њ—Б—В–∞–≤–ї—П–ї 300 –Љ–ї–љ.).
–Т –†–Њ—Б—Б–Є–Є –љ–∞ –љ–∞—З–∞–ї–Њ 2000 –≥–Њ–і–∞ 8 –Љ–ї–љ. —З–µ–ї–Њ–≤–µ–Ї —Б—В—А–∞–і–∞–ї–Є –°–Ф, —В.–µ. –Њ–Ї–Њ–ї–Њ 5,5% –љ–∞—Б–µ–ї–µ–љ–Є—П –†–Њ—Б—Б–Є–Є (–њ–Њ —Б—В–∞—В–Є—Б—В–Є–Ї–µ – –≤—Б–µ–≥–Њ 2 –Љ–ї–љ., –љ–∞ 01.01.08 –Њ—Д–Є—Ж–Є–∞–ї—М–љ–Њ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ 2,83 –Љ–ї–љ.). –Ъ 2025 –≥., –њ–Њ –њ—А–Њ–≥–љ–Њ–Ј–∞–Љ –Т–Ю–Ч, —Н—В–Њ —З–Є—Б–ї–Њ —Г–≤–µ–ї–Є—З–Є—В—Б—П –і–Њ 13,2 –Љ–ї–љ. —З–µ–ї–Њ–≤–µ–Ї. –Ю–і–љ–∞ –Є–Ј –њ—А–Є—З–Є–љ —В–∞–Ї–Њ–≥–Њ —А–∞—Б—Е–Њ–ґ–і–µ–љ–Є—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є—Е –Є —А–µ–∞–ї—М–љ—Л—Е –і–∞–љ–љ—Л—Е –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ —В–Њ–Љ, —З—В–Њ –љ–µ—А–µ–і–Ї–Њ –°–Ф 2 —В–Є–њ–∞ –і–Є–∞–≥–љ–Њ—Б—В–Є—А—Г–µ—В—Б—П —Б–њ—Г—Б—В—П –љ–µ–Ї–Њ—В–Њ—А–Њ–µ –≤—А–µ–Љ—П (–Є–љ–Њ–≥–і–∞ —Б–њ—Г—Б—В—П –±–Њ–ї–µ–µ —З–µ–Љ 5 –ї–µ—В) –њ–Њ—Б–ї–µ –Є—Б—В–Є–љ–Њ–є –Љ–∞–љ–Є—Д–µ—Б—В–∞—Ж–Є–Є —Н—В–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ–Є –µ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П.
–°–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П —П–≤–ї—П—О—В—Б—П –Њ—Б–љ–Њ–≤–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є –Є–љ–≤–∞–ї–Є–і–Є–Ј–∞—Ж–Є–Є –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞. –Ю—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї —Б–Љ–µ—А—В–Є —Г –ї–Є—Ж —Б –љ–∞—А—Г—И–µ–љ–љ–Њ–є —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В—М—О –Ї –≥–ї—О–Ї–Њ–Ј–µ –њ–Њ–≤—Л—И–µ–љ –љ–∞ 30%, —Г –ї–Є—Ж —Б –љ–µ–і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ–љ—Л–Љ –°–Ф – –љ–∞ 80% –Є —Г –ї—О–і–µ–є, –Ї–Њ—В–Њ—А—Л–Љ –њ–Њ—Б—В–∞–≤–ї–µ–љ –і–Є–∞–≥–љ–Њ–Ј –°–Ф, –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї —Б–Љ–µ—А—В–Є —Г–≤–µ–ї–Є—З–µ–љ –≤ 2,8 —А–∞–Ј–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–µ–Љ–Є, —Г –Ї–Њ–≥–Њ –љ–µ—В –°–Ф.
–†–Є—Б–Ї –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –≤ 5 —А–∞–Ј –њ—А–Є —Б–Њ—З–µ—В–∞–љ–Є–Є –°–Ф 2 —В–Є–њ–∞ –Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є (–Р–У). –Я—А–Є —Н—В–Њ–Љ —Б–Љ–µ—А—В–љ–Њ—Б—В—М –њ–Њ—Б–ї–µ –њ–µ—А–µ–љ–µ—Б–µ–љ–љ–Њ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –њ—А–Є —В–Њ–Љ –ґ–µ —Б–Њ—З–µ—В–∞–љ–Є–Є —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –≤ 6 —А–∞–Ј. –Р —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ю–Э–Ь–Ъ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –≤ 8 —А–∞–Ј –њ—А–Є —Б–Њ—З–µ—В–∞–љ–Є–Є –°–Ф 2 —В–Є–њ–∞ –Є –Р–У.
–°–ї–µ–і—Г–µ—В –Њ–±—А–∞—В–Є—В—М –≤–љ–Є–Љ–∞–љ–Є–µ –љ–∞ —В–Њ, —З—В–Њ 75% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б—В—А–∞–і–∞—О—Й–Є—Е –°–Ф 2 —В–Є–њ–∞, –Є–Љ–µ—О—В –њ–Њ–≤—Л—И–µ–љ–љ—Л–µ —Ж–Є—Д—А—Л –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П (–Р–Ф).
–§–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Ш–С–°
–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞
–Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –Є–Ј—Г—З–∞–µ–Љ—Л–µ —Д–∞–Ї—В–Њ—А—Л —Г—Б–ї–Њ–≤–љ–Њ –Љ–Њ–ґ–љ–Њ —А–∞–Ј–і–µ–ї–Є—В—М –љ–∞ —Б–ї–µ–і—Г—О—Й–Є–µ –≥—А—Г–њ–њ—Л:
– –љ–µ–Ї–Њ—А—А–Є–≥–Є—А—Г–µ–Љ—Л–µ (–≤–Њ–Ј—А–∞—Б—В, –њ–Њ–ї, –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ—Б—В—М);
– –Ї–Њ—А—А–Є–≥–Є—А—Г–µ–Љ—Л–µ (–њ–Њ–≤—Л—И–µ–љ–љ—Л–µ —Ж–Є—Д—А—Л –Р–Ф, –Ї—Г—А–µ–љ–Є–µ, –љ–µ—Б–±–∞–ї–∞–љ—Б–Є—А–Њ–≤–∞–љ–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ, –Њ–ґ–Є—А–µ–љ–Є–µ –Є –≥–Є–њ–Њ–і–Є–љ–∞–Љ–Є—П);
– —З–∞—Б—В–Є—З–љ–Њ –Ї–Њ—А—А–Є–≥–Є—А—Г–µ–Љ—Л–µ (–і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є—П: —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Ы–Я–Т–Я –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ы–Я–Э–Я; –°–Ф (–≥–Є–њ–µ—А–Є–љ—Б—Г–ї–Є–љ–µ–Љ–Є—П –Є –Є–љ—Б—Г–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М); –њ—Б–Є—Е–Њ—Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ –љ–∞–њ—А—П–ґ–µ–љ–Є–µ).
–Т—Б–µ —Н—В–Є —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Ш–С–° –љ–µ–Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ –Є–Ј—Г—З–∞–ї–Є—Б—М –≤ –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е. –Я–Њ–і—А–Њ–±–љ–µ–µ –Њ—Б—В–∞–љ–Њ–≤–Є–Љ—Б—П –љ–∞ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Є–Ј –љ–Є—Е.
–Я–Њ–ї. –Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –і–Њ –љ–∞—Б—В—Г–њ–ї–µ–љ–Є—П –Љ–µ–љ–Њ–њ–∞—Г–Ј—Л –ґ–µ–љ—Й–Є–љ—Л –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —А–µ–ґ–µ —Б—В—А–∞–і–∞—О—В –Ш–С–° – –Є—Е –Ј–∞—Й–Є—Й–∞–µ—В —Н—Б—В—А–∞–і–Є–Њ–ї. –Ю–і–љ–∞–Ї–Њ –њ–Њ—Б–ї–µ —В–Њ–≥–Њ, –Ї–∞–Ї –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —Г–≥–∞—Б–∞–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є —П–Є—З–љ–Є–Ї–∞, —З–∞—Б—В–Њ—В–∞ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –Ш–С–° —Г –Љ—Г–ґ—З–Є–љ –Є —Г –ґ–µ–љ—Й–Є–љ –≤—Л—А–∞–≤–љ–Є–≤–∞–µ—В—Б—П. –Т –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —Н—Б—В—А–Њ–≥–µ–љ–Њ–≤ –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О —Г—А–Њ–≤–љ—П –Ы–Я–Э–Я, –Њ–±—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞, —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –Є —Б–љ–Є–ґ–µ–љ–Є—О —Г—А–Њ–≤–љ—П –Ы–Я–Т–Я, —З—В–Њ –і–µ–ї–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–µ.
–Ч–і–µ—Б—М —Б—В–Њ–Є—В –Њ–±—А–∞—В–Є—В—М –≤–љ–Є–Љ–∞–љ–Є–µ, —З—В–Њ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –°–Ф –Ї–∞–Ї —Г –Љ—Г–ґ—З–Є–љ, —В–∞–Ї –Є —Г –ґ–µ–љ—Й–Є–љ, –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В —Б–Њ—Е—А–∞–љ–љ–Њ—Б—В–Є —Д—Г–љ–Ї—Ж–Є–Є —П–Є—З–љ–Є–Ї–∞, –Ш–С–° –Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј –≤—Б—В—А–µ—З–∞—О—В—Б—П —Б –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є —З–∞—Б—В–Њ—В–Њ–є.
–Ф–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є—П. –•–Њ—В—П —Г—А–Њ–≤–µ–љ—М –Ы–Я–Э–Я –Њ–±—Л—З–љ–Њ –љ–Њ—А–Љ–∞–ї—М–љ—Л–є, —Б–Ї–Њ—А–Њ—Б—В–Є —Б–Є–љ—В–µ–Ј–∞ –Є —Г–і–∞–ї–µ–љ–Є—П –Ы–Я–Э–Я —Г–≤–µ–ї–Є—З–µ–љ—Л. –†–∞–Ј–Љ–µ—А –њ–ї–Њ—В–љ–Њ—Б—В–Є —З–∞—Б—В–Є—Ж –Ы–Я–Э–Я —Г –ї—О–і–µ–є, —Б—В—А–∞–і–∞—О—Й–Є—Е –°–Ф 2 —В–Є–њ–∞, –≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –Ј–∞–≤–Є—Б—П—В –Њ—В —Г—А–Њ–≤–љ—П —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤. –Я—А–Є –≥–Є–њ–µ—А—В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–µ–Љ–Є–Є –њ–Њ–≤—Л—И–∞–µ—В—Б—П —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Љ–µ–ї–Ї–Є—Е, –±–Њ–ї–µ–µ –њ–ї–Њ—В–љ—Л—Е —Д—А–∞–Ї—Ж–Є–є –Ы–Я–Э–Я. –У–ї–Є–Ї–Њ–Ј–Є–ї–Є—А–Њ–≤–∞–љ–љ—Л–µ –Ы–Я–Э–Я –±–Њ–ї–µ–µ —Б–Ї–ї–Њ–љ–љ—Л –Ї –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ–є –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є.
–Я—А–Є —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –ї—О–і–µ–є, —Б—В—А–∞–і–∞—О—Й–Є—Е –°–Ф 2 —В–Є–њ–∞, —З–∞—Б—В–Њ –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞—О—В –≥–Є–њ–µ—А—Е–Њ–ї–µ—Б—В–µ—А–Є–љ–µ–Љ–Є—О, —Б–≤—П–Ј–∞–љ–љ—Г—О —Б –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –Ы–Я–Э–Я. –Я–Њ –і–∞–љ–љ—Л–Љ —А—П–і–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ–Њ–≤—Л—И–µ–љ–Є–µ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –њ–ї–∞–Ј–Љ—Л –≤—Л—П–≤–ї—П–µ—В—Б—П —Г 54–77% –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ю–і–љ–∞–Ї–Њ —З–∞—Б—В–Њ—В–∞ –≥–Є–њ–µ—А—Е–Њ–ї–µ—Б—В–µ—А–Є–љ–µ–Љ–Є–Є –њ—А–Є –°–Ф 2 —В–Є–њ–∞ —Г –ї—О–і–µ–є, –љ–µ –Є–Љ–µ—О—Й–Є—Е –і–∞–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –њ—А–Є–Љ–µ—А–љ–Њ –Њ–і–Є–љ–∞–Ї–Њ–≤–∞. –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є —Б—З–Є—В–∞—О—В, —З—В–Њ –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ы–Я–Э–Я —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є.
–£–Љ–µ–љ—М—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –Њ—В–Љ–µ—З–∞–µ—В—Б—П –њ—А–Є —В–µ—А–∞–њ–Є–Є –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –Є–ї–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ (–У–ї—О–Ї–Њ—Д–∞–ґ), –∞ —В–∞–Ї–ґ–µ –њ—А–Є —Б–љ–Є–ґ–µ–љ–Є–Є –≤–µ—Б–∞ —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞ —Б –Њ–ґ–Є—А–µ–љ–Є–µ–Љ. –Ю–і–љ–∞–Ї–Њ —З–∞—Б—В–Њ —Г—А–Њ–≤–µ–љ—М —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –Њ—Б—В–∞–µ—В—Б—П –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ —Г —В–∞–Ї–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—О —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–µ–Љ–Є–Є. –Я—А–Є —Н—В–Њ–Љ —З–µ–Љ –≤—Л—И–µ —Г—А–Њ–≤–µ–љ—М –Њ–±—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞, —В–µ–Љ –≤—Л—И–µ —А–Є—Б–Ї —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–љ–Њ–є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є —Г –і–∞–љ–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –њ—А–Є –Њ–і–љ–Њ–Љ –Є —В–Њ–Љ –ґ–µ —Г—А–Њ–≤–љ–µ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ —Б–Љ–µ—А—В–љ–Њ—Б—В—М –±–Њ–ї—М–љ—Л—Е –≤ —Б–≤—П–Ј–Є —Б –љ–∞–ї–Є—З–Є–µ–Љ –Ш–С–° –≤—Л—И–µ –≤ 3–4 —А–∞–Ј–∞ –њ—А–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–Љ –°–Ф 2 —В–Є–њ–∞ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б —Б–Є—В—Г–∞—Ж–Є–µ–є, –Ї–Њ–≥–і–∞ —Н—В–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В.
–°—А–µ–і–Є –њ—А–Є—З–Є–љ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –≤—Л–і–µ–ї—П—О—В –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л–µ –Є –Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤ –Ї—А–Њ–≤–Є. –Ш–Ј –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –љ–∞–Є–±–Њ–ї–µ–µ —Е–∞—А–∞–Ї—В–µ—А–љ—Л –≥–Є–њ–µ—А—В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–µ–Љ–Є—П –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –Ы–Я–Т–Я, –Ї–Њ—В–Њ—А—Л–µ –≤—Б—В—А–µ—З–∞—О—В—Б—П –њ—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ —Г 20% –±–Њ–ї—М–љ—Л—Е. –£–Љ–µ–љ—М—И–µ–љ–Є–µ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –Ы–Я–Т–Я –≤—Л—П–≤–ї—П–µ—В—Б—П –Ї–∞–Ї –њ—А–Є –≤–њ–µ—А–≤—Л–µ –≤—Л—П–≤–ї–µ–љ–љ–Њ–Љ –°–Ф 2 —В–Є–њ–∞, —В–∞–Ї –Є —Г –±–Њ–ї—М–љ—Л—Е —Б —А–∞–љ–µ–µ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ–љ—Л–Љ –°–Ф 2 —В–Є–њ–∞ –Є –љ–∞—Е–Њ–і—П—Й–µ–Љ—Б—П –љ–∞ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –≤–Ї–ї—О—З–∞—О—Й–µ–є –≤ —Б–µ–±—П –Ї–∞–Ї –і–Є–µ—В—Г, —В–∞–Ї –Є –њ–µ—А–Њ—А–∞–ї—М–љ—Л–µ —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л –Є/–Є–ї–Є –Є–љ—Б—Г–ї–Є–љ. –Ш–Ј –Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є – –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Љ–∞–ї–µ–љ—М–Ї–Є—Е –њ–ї–Њ—В–љ—Л—Е —З–∞—Б—В–Є—Ж –Ы–Я–Э–Я. –У–Є–њ–µ—А—Е–Њ–ї–µ—Б—В–µ—А–Є–љ–µ–Љ–Є—О, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Г—О –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ –•–° –Ы–Я–Э–Я, –њ—А–Є –°–Ф 2 —В–Є–њ–∞ –љ–∞—Е–Њ–і—П—В —Б —В–∞–Ї–Њ–є –ґ–µ —З–∞—Б—В–Њ—В–Њ–є, –Ї–∞–Ї –Є —Г –ї–Є—Ж –±–µ–Ј –°–Ф.
–Т—Л—П–≤–ї–µ–љ–∞ —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г —Г—А–Њ–≤–љ–µ–Љ —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –Є —А–Є—Б–Ї–Њ–Љ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Ш–С–° –Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞. –Я–Њ –і–∞–љ–љ—Л–Љ 11––ї–µ—В–љ–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (Paris Prospective Study), —Г—А–Њ–≤–µ–љ—М —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ —Б–≤—П–Ј–∞–љ —Б —А–Є—Б–Ї–Њ–Љ —Б–Љ–µ—А—В–Є –Њ—В –Ш–С–° –Є –µ–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –њ—А–Є —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –°–Ф 2 —В–Є–њ–∞. –£—А–Њ–≤–µ–љ—М —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –Љ–Њ–ґ–µ—В –Є–Љ–µ—В—М –±o–ї—М—И—Г—О –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї—Г—О —Ж–µ–љ–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —А–∞–Ј–≤–Є—В–Є—П –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞, —З–µ–Љ –і—А—Г–≥–Є–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞.
–Я–Њ –Љ–љ–µ–љ–Є—О M. Laakso –Є —Б–Њ–∞–≤—В., –≤–∞–ґ–љ–Њ–µ –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –Њ—В –Ш–С–° –Є –µ–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Є–Љ–µ–µ—В —Б–љ–Є–ґ–µ–љ–Є–µ –Ы–Я–Т–Я, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ї–Њ—В–Њ—А—Л—Е <0,9 –Љ–Љ–Њ–ї—М/–ї —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —З–µ—В—Л—А–µ—Е–Ї—А–∞—В–љ—Л–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —А–Є—Б–Ї–∞ —Б–Љ–µ—А—В–Є –Њ—В —Б–µ—А–і–µ—З–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є. –Т –§–Є–љ–ї—П–љ–і–Є–Є –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Є —Г—З–∞—Б—В–Є–Є 1059 —З–µ–ї–Њ–≤–µ–Ї, —Б—В—А–∞–і–∞—О—Й–Є—Е –°–Ф 2 —В–Є–њ–∞ —Б—А–µ–і–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –≥–і–µ –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ–Њ–≤—Л—И–µ–љ–Є–µ —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ >2,3 –Љ–Њ–ї—М/–ї –Є —Б–љ–Є–ґ–µ–љ–Є–µ –Ы–Я–Т–Я<1,0 –Љ–Љ–Њ–ї—М/–ї —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –і–≤—Г–Ї—А–∞—В–љ—Л–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –≤ —Б–≤—П–Ј–Є —Б –Ш–С–° –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –і—А—Г–≥–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞.
–У–Є–њ–µ—А–Є–љ—Б—Г–ї–Є–љ–µ–Љ–Є—П (–У–Ш) –Є –Є–љ—Б—Г–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М (–Ш–†) –≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –љ–∞—А—Г—И–µ–љ–Є–є –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ —П–≤–ї—П—О—В—Б—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Ш–С–°. –Т—Л—П–≤–ї–µ–љ–∞ —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –Ш–† –Є –љ–Є–Ј–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ –Ы–Я–Т–Я. –Ъ–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ы–Я–Т–Я —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –њ—А–Є —В–µ—А–∞–њ–Є–Є –°–Ф 2 —В–Є–њ–∞ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –Є —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –≤–µ—Б–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –У–Ш —П–≤–ї—П–µ—В—Б—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ –њ—А–µ–і–Є–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –Є —Б–Љ–µ—А—В–Є –Њ—В –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Ш–С–° –≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≤–Њ–Ј—А–∞—Б—В–∞, –Є–љ–і–µ–Ї—Б–∞ –Љ–∞—Б—Б—Л —В–µ–ї–∞ (–Ш–Ь–Ґ), –Р–Ф –Є —Г—А–Њ–≤–љ—П —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞, –Ї—Г—А–µ–љ–Є—П –Є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є. –Я—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л–µ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –У–Ш —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ–Њ–≥–Њ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –Є –Ї–Њ—А—А–µ–ї–Є—А—Г–µ—В —Б –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є —Б–Љ–µ—А—В–љ–Њ—Б—В—М—О –Њ—В –љ–µ–≥–Њ. –Ю–і–љ–Њ–Љ–Њ–Љ–µ–љ—В–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ (Atherosklerosis Risk in Communities Study) –њ–Њ–і—В–≤–µ—А–і–Є–ї–Њ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Љ–µ–ґ–і—Г —Г—А–Њ–≤–љ–µ–Љ –Є–љ—Б—Г–ї–Є–љ–∞ –љ–∞—В–Њ—Й–∞–Ї –Є —Б—В–µ–њ–µ–љ—М—О –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б—В–µ–љ–Њ–Ї –∞—А—В–µ—А–Є–є.
–Ш–Љ–µ—О—Й–Є–µ—Б—П –і–∞–љ–љ—Л–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ —В–Њ–Љ, —З—В–Њ –Ш–† –≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є, —З–µ–Љ –У–Ш, –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ, —В—А–Њ–Љ–±–Њ–≥–µ–љ–µ–Ј–Њ–Љ, –≥–Є–њ–µ—А—В–Њ–љ–Є–µ–є, –Њ–ґ–Є—А–µ–љ–Є–µ–Љ –Є –°–Ф. –Я—А–Є –Њ–ґ–Є—А–µ–љ–Є–Є –±–∞–Ј–∞–ї—М–љ–∞—П –Є —Б—Г—В–Њ—З–љ–∞—П —Б–µ–Ї—А–µ—Ж–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞ –≤ 3–4 —А–∞–Ј–∞ –≤—Л—И–µ, —З–µ–Љ —Г –ї–Є—Ж —Б –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –Љ–∞—Б—Б–Њ–є —В–µ–ї–∞.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —П–њ–Њ–љ—Б–Ї–Є—Е —Г—З–µ–љ—Л—Е —Г –±–Њ–ї—М–љ—Л—Е —Б –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ—Л–Љ –Ї–Њ—А–Њ–љ–∞—А–љ—Л–Љ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ –≤—Л—П–≤–Є–ї–Њ —Б—Г—Й–µ—Б—В–≤–Њ–≤–∞–љ–Є–µ —В–µ—Б–љ–Њ–є –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г —Б—В–µ–њ–µ–љ—М—О —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї –Є–љ—Б—Г–ї–Є–љ—Г –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М—О –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞.
–Ч–і–µ—Б—М —В–∞–Ї–ґ–µ –Є–≥—А–∞–µ—В —А–Њ–ї—М –Є –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ—Б—В—М, –Ї–∞–Ї –≤ —А–∞–Ј–≤–Є—В–Є–Є –°–Ф, —В–∞–Ї –Є –≤ —А–∞–Ј–≤–Є—В–Є–Є –Ш–С–° –Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞. –Э–µ —Б—В–Њ–Є—В —Г–њ—Г—Б–Ї–∞—В—М –Є–Ј –≤–Є–і—Г –Є –љ–∞–ї–Є—З–Є–µ –≤ —Б–µ–Љ—М—П—Е –љ–∞—А—Г—И–µ–љ–Є–є –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞, —Б–≤–µ—А—В—Л–≤–∞–µ–Љ–Њ—Б—В–Є –Ї—А–Њ–≤–Є, –Р–Ф, —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –Є, —А–∞–Ј—Г–Љ–µ–µ—В—Б—П, –°–Ф. –†–Њ–ї—М –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –љ–∞–ї–Є—З–Є–µ–Љ –≥–µ–љ–Њ–≤, –Љ—Г—В–∞—Ж–Є–Є –Ї–Њ—В–Њ—А—Л—Е –Љ–Њ–≥—Г—В –≤—Л–Ј–≤–∞—В—М –≥–Є–њ–µ—А—Е–Њ–ї–µ—Б—В–µ—А–Є–љ–µ–Љ–Є—О –Є —А–∞–љ–љ–Є–є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј.
–Ъ–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –У–Ш (—Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ —А–∞–Ј–≤–Є—В–Є–µ–Љ –Ш–†) —Б—В—А–∞–і–∞—О—В –ї–Є—Ж–∞ —Б –Є–Ј–±—Л—В–Њ—З–љ–Њ–є –Љ–∞—Б—Б–Њ–є —В–µ–ї–∞ –Є –Њ–ґ–Є—А–µ–љ–Є–µ–Љ. –Я—А–Є—З–µ–Љ –љ–∞–Є–±–Њ–ї–µ–µ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–є —П–≤–ї—П–µ—В—Б—П –Ї–∞—В–µ–≥–Њ—А–Є—П –ї–Є—Ж –Є–Љ–µ–љ–љ–Њ —Б –Є–Ј–±—Л—В–Њ—З–љ–Њ–є –Љ–∞—Б—Б–Њ–є —В–µ–ї–∞, —В.–µ. –Ш–Ь–Ґ –Њ—В 25 –і–Њ 29 –Ї–≥/–Љ2. –Я–Њ –і–∞–љ–љ—Л–Љ –§—А–∞–Љ–Є–љ–≥–µ–Љ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —Б–Љ–µ—А—В–љ–Њ—Б—В—М –Љ—Г–ґ—З–Є–љ —Б –Љ–∞—Б—Б–Њ–є —В–µ–ї–∞, –њ—А–µ–≤—Л—И–∞—О—Й–µ–є –Є–і–µ–∞–ї—М–љ—Г—О –љ–∞ 10–20%, –≤–і–≤–Њ–µ –≤—Л—И–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –ї–Є—Ж–∞–Љ–Є —Б –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –Љ–∞—Б—Б–Њ–є —В–µ–ї–∞ (–Ш–Ь–Ґ –Њ—В 18 –і–Њ 25 –Ї–≥/–Љ2). –Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П —З–µ—В–Ї–Њ –і–Њ–Ї–∞–Ј–∞–љ–∞ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ—Б—В—М –≤ –њ–ї–∞–љ–µ –њ—А–Њ–≥–љ–Њ–Ј–∞ –Њ–ґ–Є—А–µ–љ–Є—П –њ–Њ —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–Љ—Г —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–Љ—Г —В–Є–њ—Г, —В.–µ. —Б–Њ —Б–Ї–Њ–њ–ї–µ–љ–Є–µ–Љ –ґ–Є—А–Њ–≤—Л—Е –Њ—В–ї–Њ–ґ–µ–љ–Є–є –љ–∞ –њ–µ—А–µ–і–љ–µ–є –±—А—О—И–љ–Њ–є —Б—В–µ–љ–Ї–µ –Є, —З—В–Њ —Б–∞–Љ–Њ–µ –љ–µ–њ—А–Є—П—В–љ–Њ–µ, –≤–Њ–Ї—А—Г–≥ –≤–љ—Г—В—А–µ–љ–љ–Є—Е –Њ—А–≥–∞–љ–Њ–≤. –≠—В–Њ—В —В–Є–њ–∞ –Њ–ґ–Є—А–µ–љ–Є—П –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –≤–ї–Є—П–љ–Є–µ –љ–∞ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ —Б–Њ—Б—Г–і–Њ–≤. –Я—А–Є —Н—В–Њ–Љ —Б–ї–µ–і—Г–µ—В –њ–Њ–Љ–љ–Є—В—М, —З—В–Њ 80% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ —Б—В—А–∞–і–∞—О—В –Њ–ґ–Є—А–µ–љ–Є–µ–Љ —В–Њ–є –Є–ї–Є –Є–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є.
–Ґ–∞–Ї–ґ–µ —Е–Њ—З–µ—В—Б—П –Њ—В–і–µ–ї—М–љ–Њ –Њ—Б—В–∞–љ–Њ–≤–Є—В—М—Б—П –µ—Й–µ –љ–∞ –Њ–і–љ–Њ–Љ —Д–∞–Ї—В–Њ—А–µ —А–∞–Ј–≤–Є—В–Є—П –Ш–С–° –Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞, –∞ –Є–Љ–µ–љ–љ–Њ – –љ–∞ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є —Н–њ–Є—В–µ–ї–Є—П –Є –Ї—Г—А–µ–љ–Є–Є. –Ю—Б–љ–Њ–≤–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –Ї—Г—А–µ–љ–Є—П –љ–∞ –њ–∞—В–Њ–≥–µ–љ–µ–Ј –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ —Б–≤—П–Ј—Л–≤–∞—О—В —Б –µ–≥–Њ —Б–Є—Б—В–µ–Љ–љ—Л–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –љ–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є: —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Г–і–∞—А–љ–Њ–≥–Њ –Њ–±—К–µ–Љ–∞, —Г—З–∞—Й–µ–љ–Є–µ –І–°–°, –њ–Њ–≤—Л—И–µ–љ–Є–µ –Љ–Є–љ—Г—В–љ–Њ–≥–Њ –Њ–±—К–µ–Љ–∞, –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –ї–Є–њ–Є–і–љ—Л–є –Є —Г–≥–ї–µ–≤–Њ–і–љ—Л–є –Њ–±–Љ–µ–љ, –Њ–±–Љ–µ–љ –Ї–∞—В–µ—Е–Њ–ї–∞–Љ–Є–љ–Њ–≤, —Б–≤–µ—А—В—Л–≤–∞–µ–Љ–Њ—Б—В—М –Ї—А–Њ–≤–Є. –°—Г—Й–µ—Б—В–≤—Г–µ—В —З–µ—В–Ї–∞—П –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М —Б—В–µ–њ–µ–љ–Є —Б—В–µ–љ–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П —Б–Њ—Б—Г–і–Њ–≤ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є–Љ–Є –±–ї—П—И–Ї–∞–Љ–Є –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –њ–Њ—В—А–µ–±–ї—П–µ–Љ–Њ–≥–Њ –љ–Є–Ї–Њ—В–Є–љ–∞. –Ф–Њ–Ї–∞–Ј–∞–љ–∞ —А–µ–∞–Ї—Ж–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л –≤ –≤–Є–і–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ —Б–њ–∞–Ј–Љ–∞ –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –∞—А—В–µ—А–Є–є –Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –љ–Є–Ї–Њ—В–Є–љ–∞ (–Ј–і–µ—Б—М —Б–ї–µ–і—Г–µ—В –Њ–±—А–∞—В–Є—В—М –≤–љ–Є–Љ–∞–љ–Є–µ –љ–∞ —В–Њ—В —Д–∞–Ї—В, —З—В–Њ «–ї–µ–≥–Ї–Є–µ» —Б–Є–≥–∞—А–µ—В—Л –≤–ї–Є—П—О—В –љ–∞ —Б–Њ—Б—Г–і–Є—Б—В—Г—О —Б—В–µ–љ–Ї—Г –љ–µ –Љ–µ–љ—М—И–µ, —З–µ–Љ –Њ–±—Л—З–љ—Л–µ —Б–Є–≥–∞—А–µ—В—Л).
–Я—А–Є—З–Є–љ–∞ —В–∞–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –ї–µ–ґ–Є—В –≤ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є —Н–љ–і–Њ—В–µ–ї–Є—П, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–µ–≥–Њ –њ–Њ–і –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –љ–Є–Ї–Њ—В–Є–љ–∞. –Ф–Є—Б—Д—Г–љ–Ї—Ж–Є–Є —Н–њ–Є—В–µ–ї–Є—П –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Г–і–µ–ї—П–µ—В—Б—П –Њ—З–µ–љ—М –±–Њ–ї—М—И–Њ–µ –Є –њ—А–Є—Б—В–∞–ї—М–љ–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ. –≠–љ–і–Њ—В–µ–ї–Є–є – –Љ–Њ–љ–Њ—Б–ї–Њ–є –Ї–ї–µ—В–Њ–Ї –≤—Л—В—П–љ—Г—В–Њ–є —Д–Њ—А–Љ—Л, –≥–µ—В–µ—А–Њ–≥–µ–љ–љ—Л—Е –њ–Њ —А–∞–Ј–Љ–µ—А—Г, —В–µ—Б–љ–Њ —Б–≤—П–Ј–∞–љ–љ—Л—Е –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є. –≠–љ–і–Њ—В–µ–ї–Є–є —Б–µ–Ї—А–µ—В–Є—А—Г–µ—В –Љ–Њ—Й–љ—Л–µ –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ—Л–µ –≤–µ—Й–µ—Б—В–≤–∞: –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—В–Њ—А—Л (–Њ–Ї—Б–Є–і –∞–Ј–Њ—В–∞ NO, —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л–є –≥–Є–њ–µ—А–њ–Њ–ї—П—А–Є–Ј—Г—О—Й–Є–є —Д–∞–Ї—В–Њ—А, –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ) –Є –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В–Є—А–Є–Ї—В–Њ—А—Л (–∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ II, —Н–љ–і–Њ—В–µ–ї–Є–љ, —Б–≤–Њ–±–Њ–і–љ—Л–µ —А–∞–і–Є–Ї–∞–ї—Л –љ–µ–і–Њ–Њ–Ї–Є—Б–ї–µ–љ–љ—Л—Е –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В, –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ F2a, —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ –Р2). –Э–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л–Љ –Є –Ј–љ–∞—З–Є–Љ—Л–Љ –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—В–Њ—А–Њ–Љ —Б—З–Є—В–∞–µ—В—Б—П –Њ–Ї—Б–Є–і –∞–Ј–Њ—В–∞ NO. –Ю–љ –≤—Л–Ј—Л–≤–∞–µ—В —А–∞—Б—Б–ї–∞–±–ї–µ–љ–Є–µ –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї —Б–Њ—Б—Г–і–Њ–≤, –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞–µ—В —Б—В—А—Г–Ї—В—Г—А–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Н–љ–і–Њ—В–µ–ї–Є—П, –Є–љ–≥–Є–±–Є—А—Г—П —А–Њ—Б—В –Є –Љ–Є–≥—А–∞—Ж–Є—О –≥–ї–∞–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї. NO –њ—А–Є—Б—Г—В—Б—В–≤—Г–µ—В –≤–Њ –≤—Б–µ—Е —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е, –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В —А–∞–Ј–Љ–µ—А–∞ –Є —Д—Г–љ–Ї—Ж–Є–Є —Б–Њ—Б—Г–і–Њ–≤. –Т –њ–Њ–Ї–Њ–µ —Н–љ–і–Њ—В–µ–ї–Є–є –њ–Њ—Б—В–Њ—П–љ–љ–Њ —Б–µ–Ї—А–µ—В–Є—А—Г–µ—В NO, –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—П –љ–Њ—А–Љ–∞–ї—М–љ—Л–є —В–Њ–љ—Г—Б –∞—А—В–µ—А–Є–є. –Ф–Є—Б—Д—Г–љ–Ї—Ж–Є—П —Н–љ–і–Њ—В–µ–ї–Є—П –њ—А–Њ—В–µ–Ї–∞–µ—В —Б –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ–Љ –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—В–Њ—А–љ—Л—Е —Б—Г–±—Б—В–∞–љ—Ж–Є–є, —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤, —Д–∞–Ї—В–Њ—А–Њ–≤, —Г–≥–љ–µ—В–∞—О—Й–Є—Е —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л–є —Д–Є–±—А–Є–љ–Њ–ї–Є–Ј –Є —Г—Б–Є–ї–Є–≤–∞—О—Й–Є—Е –∞–≥—А–µ–≥–∞—Ж–Є—О —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ—Г—О –Є –Љ–Є–≥—А–∞—Ж–Є–Њ–љ–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤ (–Љ–∞–Ї—А–Њ—Д–∞–≥–Њ–≤) –Є –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї —Б–Њ—Б—Г–і–Њ–≤, —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —В—А–Њ–Љ–±–Њ–Ј—Г –Є —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–є –±–ї—П—И–Ї–Є. –Ч–і–µ—Б—М —Б–ї–µ–і—Г–µ—В –Њ–±—А–∞—В–Є—В—М –≤–љ–Є–Љ–∞–љ–Є–µ –љ–∞ —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –њ—А–Є –°–Ф –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П —Б–∞–Љ–∞ –њ–Њ —Б–µ–±–µ —П–≤–ї—П–µ—В—Б—П –Љ–Њ—Й–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ, –Є–љ–Є—Ж–Є–Є—А—Г—О—Й–Є–Љ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤ —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –њ—Г—В—П–Љ–Є (–∞—Г—В–Њ–Њ–Ї–Є—Б–ї–µ–љ–Є–µ –≥–ї—О–Ї–Њ–Ј—Л, –њ–Њ–ї–Є–Њ–ї–Њ–≤—Л–є —И—Г–љ—В –Є –і—А—Г–≥–Є–µ). –Я–Њ–Љ–Є–Љ–Њ —Н—В–Њ–≥–Њ, —Б—В–Њ–є–Ї–∞—П –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П —Б–љ–Є–ґ–∞–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Д–∞–Ї—В–Њ—А–Њ–≤ –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–є –Ј–∞—Й–Є—В—Л – —Б—Г–њ–µ—А–Њ–Ї—Б–Є–і–і–Є—Б–Љ—Г—В–∞–Ј—Л, –≤–Є—В–∞–Љ–Є–љ–∞ –° (–∞—Б–Ї–Њ—А–±–Є–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л) –Є –Х (a–—В–Њ–Ї–Њ—Д–µ—А–Њ–ї–∞) –Є –њ—А–Њ—З–Є—Е. –Т—Л—Б–Њ–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –њ—А–Є –°–Ф –љ–∞–њ—А—П–Љ—Г—О –Ї–Њ—А—А–µ–ї–Є—А—Г–µ—В —Б –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М—О —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.
–£—З–Є—В—Л–≤–∞—П, –Ї –Ї–∞–Ї–Є–Љ —Б–µ—А—М–µ–Ј–љ—Л–Љ –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П–Љ –њ—А–Є–≤–Њ–і–Є—В –≥–Є–њ–µ—А–Є–љ—Б—Г–ї–Є–љ–µ–Љ–Є—П –Є –Є–љ—Б—Г–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М, –ї–µ—З–µ–љ–Є–µ –°–Ф 2 —В–Є–њ–∞ –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Н—В–Є—Е –і–≤—Г—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ —Б–ї–µ–і—Г–µ—В –љ–∞–њ—А–∞–≤–ї—П—В—М –љ–µ —В–Њ–ї—М–Ї–Њ –љ–∞ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—О —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–µ–Љ–Є–Є, –љ–Њ –Є –љ–∞ —Г—Б—В—А–∞–љ–µ–љ–Є–µ –У–Ш –Є –Ш–†.
–Я—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ –≤ –і–∞–љ–љ–Њ–Љ —Б–ї—Г—З–∞–µ —П–≤–ї—П—О—В—Б—П –±–Є–≥—Г–∞–љ–Є–і—Л [2,4,5,9]. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ —Н—В–Њ–є –≥—А—Г–њ–њ—Л, —А–∞–Ј—А–µ—И–µ–љ–љ—Л–Љ –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О, —П–≤–ї—П–µ—В—Б—П –Љ–µ—В—Д–Њ—А–Љ–Є–љ. –Ю—А–Є–≥–Є–љ–∞–ї—М–љ—Л–Љ –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ —П–≤–ї—П–µ—В—Б—П –У–ї—О–Ї–Њ—Д–∞–ґ. –Ш—Б—В–Њ—А–Є—П –У–ї—О–Ї–Њ—Д–∞–ґ–∞ –љ–∞—З–∞–ї–∞—Б—М –≤ 1957–1959 –≥–Њ–і–∞—Е, –Ї–Њ–≥–і–∞ –±—Л–ї–Є –њ—А–Њ–≤–µ–і–µ–љ—Л –µ–≥–Њ –њ–µ—А–≤—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б–њ—Л—В–∞–љ–Є—П –≤ –і–Њ–Ј–µ 500 –Љ–≥. –Т 1960 –≥–Њ–і—Г –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ—Л –њ–µ—А–≤—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л, —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—Й–Є–µ –Њ —В–Њ–Љ, —З—В–Њ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ —Н—В–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —Г–ї—Г—З—И–∞–µ—В—Б—П –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –≥–ї—О–Ї–Њ–Ј—Л –≤ –Ї–ї–µ—В–Ї–Є, –Є, —З—В–Њ –љ–µ –Љ–µ–љ–µ–µ –≤–∞–ґ–љ–Њ – —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П –Є–љ—Б—Г–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М. –Т 1977–1982 –≥–Њ–і–∞—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≥—А—Г–њ–њ—Л –±–Є–≥—Г–∞–љ–Є–і–Њ–≤ –±—Л–ї–Њ —З–∞—Б—В–Є—З–љ–Њ –Ј–∞–њ—А–µ—Й–µ–љ–Њ –≤ —Б–≤—П–Ј–Є —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ –љ–∞ —Д–Њ–љ–µ —Д–µ–љ—Д–Њ—А–Љ–Є–љ–∞ –ї–∞–Ї—В–Њ–∞—Ж–Є–і–Њ–Ј–Њ–≤.
–Т 1977 –≥–Њ–і—Г –љ–∞—З–∞–ї–Њ—Б—М –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–µ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ UKPDS (UK Prospective Diabetes Study), –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–µ –≤ 23 –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Ж–µ–љ—В—А–∞—Е –Т–µ–ї–Є–Ї–Њ–±—А–Є—В–∞–љ–Є–Є. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г—З–∞—Б—В–≤–Њ–≤–∞–ї–Њ 5102 –њ–∞—Ж–Є–µ–љ—В–∞ —Б –≤–њ–µ—А–≤—Л–µ –≤—Л—П–≤–ї–µ–љ–љ—Л–Љ –°–Ф 2 —В–Є–њ–∞. –Х—Б—В–µ—Б—В–≤–µ–љ–љ–Њ, –њ–µ—А–≤—Л–Љ –њ—Г–љ–Ї—В–Њ–Љ –≤ –њ—А–Њ–≥—А–∞–Љ–Љ–µ –ї–µ—З–µ–љ–Є–Є —Б—В–Њ—П–ї–∞ –і–Є–µ—В–Њ—В–µ—А–∞–њ–Є—П. –Ш–љ—В–µ–љ—Б–Є–≤–љ—Л–є –Ї–Њ–љ—В—А–Њ–ї—М –≥–ї–Є–Ї–µ–Љ–Є–Є –і–Њ—Б—В–Є–≥–∞–ї—Б—П –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є, —В–µ—А–∞–њ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є —Б—Г–ї—М—Д–∞–љ–Є–ї–Љ–Њ—З–µ–≤–Є–љ—Л –Є–ї–Є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ (—В–Њ–ї—М–Ї–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є–Ј–±—Л—В–Њ—З–љ–Њ–є –Љ–∞—Б—Б–Њ–є —В–µ–ї–∞). –Т—Б–µ –≥—А—Г–њ–њ—Л –њ–Њ–Ї–∞–Ј–∞–ї–Є —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П:
– –ї—О–±–Њ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Е–Њ–і–∞, —Б–≤—П–Ј–∞–љ–љ–Њ–≥–Њ —Б –љ–∞–ї–Є—З–Є–µ–Љ –°–Ф –љ–∞ 12%;
– –Љ–Є–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є–є –љ–∞ 25%;
– —З–∞—Б—В–Њ—В—Г —Д–Њ—В–Њ–Ї–Њ–∞–≥—Г–ї—П—Ж–Є–Є —Б–µ—В—З–∞—В–Ї–Є –љ–∞ 29%.
–Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–є –Ї–Њ–љ—В—А–Њ–ї—М —Г—А–Њ–≤–љ—П –Р–Ф —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—Б–Њ–Ї–Є–Љ–Є —Ж–Є—Д—А–∞–Љ–Є –Р–Ф —Б–љ–Є–ґ–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П:
– –ї—О–±–Њ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Е–Њ–і–∞, —Б–≤—П–Ј–∞–љ–љ–Њ–≥–Њ —Б –љ–∞–ї–Є—З–Є–µ–Љ –°–Ф –љ–∞ 24%;
– —Б–Љ–µ—А—В–Є –Њ—В –і–ї–Є—В–µ–ї—М–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –°–Ф –љ–∞ 32%;
– –Њ—Б—В—А–Њ–≥–Њ –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –љ–∞ 44%;
– –Љ–Є–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є–є –љ–∞ 37%.
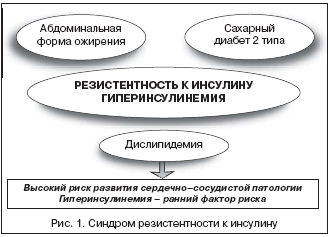
–Т –≥—А—Г–њ–њ—Г, –њ–Њ–ї—Г—З–∞—О—Й—Г—О –Љ–µ—В—Д–Њ—А–Љ–Є–љ (–њ—А–Є–Љ–µ–љ—П–ї—Б—П –У–ї—О–Ї–Њ—Д–∞–ґ), –≤—Е–Њ–і–Є–ї–Њ 342 –њ–∞—Ж–Є–µ–љ—В–∞. –£—З–Є—В—Л–≤–∞—П, —З—В–Њ —Г –њ–Њ–і–∞–≤–ї—П—О—Й–µ–≥–Њ —З–Є—Б–ї–∞ –ї—О–і–µ–є, —Б—В—А–∞–і–∞—О—Й–Є—Е –°–Ф 2 —В–Є–њ–∞, –Є–Љ–µ–µ—В—Б—П –Є–Ј–±—Л—В–Њ—З–љ–∞—П –Љ–∞—Б—Б–∞ —В–µ–ї–∞ (–±–Њ–ї–µ–µ 80%), –Љ–µ—В—Д–Њ—А–Љ–Є–љ —П–≤–ї—П–µ—В—Б—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П —Н—В–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –±–Њ–ї—М–љ—Л—Е —Б —Ж–µ–ї—М—О –Є—Б–Ї–ї—О—З–µ–љ–Є—П –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Љ–∞—Б—Б—Л —В–µ–ї–∞. –Ч–∞ —Б—З–µ—В —З–µ–≥–Њ —Н—В–Њ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В? –У–ї—О–Ї–Њ—Д–∞–ґ —Г–Љ–µ–љ—М—И–∞–µ—В –Ш–† –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, –У–Ш. –Ш–љ—Б—Г–ї–Є–љ – –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є –≥–Њ—А–Љ–Њ–љ, –≤—Л–Ј—Л–≤–∞—О—Й–Є–є —З—Г–≤—Б—В–≤–Њ –≥–Њ–ї–Њ–і–∞. –Я–Њ—Н—В–Њ–Љ—Г –ї—О–і–Є —Б –Є—Б—Е–Њ–і–љ–Њ –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ –µ–≥–Њ —Г—А–Њ–≤–љ–µ–Љ –њ–Њ—Б—В–Њ—П–љ–љ–Њ —Е–Њ—В—П—В –µ—Б—В—М. –Я—А–Є —Н—В–Њ–Љ –Є–љ—Б—Г–ї–Є–љ —В—А–µ–±—Г–µ—В –Є–Љ–µ–љ–љ–Њ —Г–≥–ї–µ–≤–Њ–і–љ–Њ–є –њ–Є—Й–Є. –Ъ–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ – –њ–µ—А–µ–µ–і–∞–љ–Є–µ, –Њ–ґ–Є—А–µ–љ–Є–µ. –≠—В–Њ –≤–µ–і–µ—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є: —В—П–ґ–µ–ї–Њ –≤—Б—В–∞—В—М –љ–∞ –±–µ–≥–Њ–≤—Г—О –і–Њ—А–Њ–ґ–Ї—Г –Є–ї–Є –њ–Њ–і–љ—П—В—М—Б—П –њ–µ—И–Ї–Њ–Љ –љ–∞ 3–4 —Н—В–∞–ґ–∞, –Ї–Њ–≥–і–∞ –і–Є–∞—Д—А–∞–≥–Љ–∞ «–њ–Њ–і–њ–Є—А–∞–µ—В—Б—П» –ґ–µ–ї—Г–і–Ї–Њ–Љ. –Ш –Ј–∞–Љ—Л–Ї–∞–µ—В—Б—П –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –Ї—А—Г–≥. –Р–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–µ –Њ–ґ–Є—А–µ–љ–Є–µ –≤–ї–µ—З–µ—В –Ј–∞ —Б–Њ–±–Њ–є —Г—Б–Є–ї–µ–љ–Є–µ –Ш–†, —Н—В–Њ, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В –µ—Й–µ –±–Њ–ї—М—И–Є–є –≤—Л–±—А–Њ—Б –Є–љ—Б—Г–ї–Є–љ–∞ –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –∞–њ–њ–µ—В–Є—В–∞. –Ъ—А—Г–≥ –Ј–∞–Љ–Ї–љ—Г–ї—Б—П. –Ґ–Њ–ї—М–Ї–Њ –љ–µ —Б–ї–µ–і—Г–µ—В –Ј–∞–±—Л–≤–∞—В—М, —З—В–Њ —Н—В–Њ –≤–µ–і–µ—В –љ–µ —В–Њ–ї—М–Ї–Њ –Ї –Ї–Њ—Б–Љ–µ—В–Є—З–µ—Б–Ї–Є–Љ –њ—А–Њ–±–ї–µ–Љ–∞–Љ, –љ–Њ –Є –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є (—А–Є—Б. 1).
–Я–Њ–Љ–Є–Љ–Њ —Б–љ–Є–ґ–µ–љ–Є—П —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–µ–Љ–Є–Є (–њ—А–Є –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ —Г—А–Њ–≤–µ–љ—М HbA1c —Б–љ–Є–ґ–∞–µ—В—Б—П –љ–∞ 0,9–1,5%), –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –Є –і—А—Г–≥–Є–µ –Є–љ—В–µ—А–µ—Б–љ—Л–µ –і–∞–љ–љ—Л–µ. –Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ UKPDS, –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О:
– –Њ–±—Й–µ–є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –љ–∞ 36%;
– —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –Њ—В –°–Ф –љ–∞ 42%;
– —З–∞—Б—В–Њ—В—Л —А–∞–Ј–≤–Є—В–Є—П –ї—О–±—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –љ–∞ 32%;
– —З–∞—Б—В–Њ—В—Л –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –љ–∞ 39%;
– —З–∞—Б—В–Њ—В—Л –Њ—Б—В—А–Њ–≥–Њ –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –љ–∞ 41%.
–†–µ–Ј—Г–ї—М—В–∞—В—Л UKPDS –Є –і—А—Г–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л, –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –Љ–µ—В—Д–Њ—А–Љ–Є–љ –Њ–±–ї–∞–і–∞–µ—В –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ–Љ —А–∞–Ј–љ–Њ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е –і–µ–є—Б—В–≤–Є–є. –Ю–і–љ–Њ –Є–Ј –µ–≥–Њ —Б–≤–Њ–є—Б—В–≤ – —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Б–љ–Є–ґ–∞—В—М –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –ї–Є–њ–Є–і–Њ–≤ –≤ –њ–ї–∞–Ј–Љ–µ –Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –∞–Ї—В–Є–≤–∞—В–Њ—А–∞ —В–Ї–∞–љ–µ–≤–Њ–≥–Њ –њ–ї–∞–Ј–Љ–Є–љ–Њ–≥–µ–љ–∞–1 (–Ш–Р–Я–1), —З—В–Њ –њ–Њ–≤—Л—И–∞–µ—В —Д–Є–±—А–Є–љ–Њ–ї–Є—В–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї—А–Њ–≤–Є. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ —Б–љ–Є–ґ–∞–µ—В—Б—П —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –Є –µ–≥–Њ –њ–Њ—Б–ї–µ–і—Б—В–≤–Є–є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б–њ–µ–Ї—В—А –і–µ–є—Б—В–≤–Є—П –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —Б–≤–Њ–і–Є—В—Б—П –Ї —Б–ї–µ–і—Г—О—Й–Є–Љ –њ—Г–љ–Ї—В–∞–Љ:
• —Б–љ–Є–ґ–∞–µ—В —Г—А–Њ–≤–µ–љ—М –≥–ї–Є–Ї–µ–Љ–Є–Є (HbA1c) –љ–∞ —Д–Њ–љ–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –і–∞–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ;
• —В–Њ—А–Љ–Њ–Ј–Є—В –≤—Б–∞—Б—Л–≤–∞–љ–Є–µ –≥–ї—О–Ї–Њ–Ј—Л –≤ –Ї–Є—И–µ—З–љ–Є–Ї–µ;
• —Б–љ–Є–ґ–∞–µ—В –Љ–∞—Б—Б—Г —В–µ–ї–∞ –Ј–∞ —Б—З–µ—В —Г–Љ–µ–љ—М—И–µ–љ–Є—П –Є–љ—Б—Г–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є;
• —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —В–Ї–∞–љ–µ–є –Ї –Є–љ—Б—Г–ї–Є–љ—Г;
• –њ–Њ–≤—Л—И–∞–µ—В —Д–Є–±—А–Є–љ–Њ–ї–Є—В–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –њ–ї–∞–Ј–Љ—Л, —З—В–Њ –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В —В—А–Њ–Љ–±–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О;
• –њ–Њ–≤—Л—И–∞–µ—В —Г—А–Њ–≤–µ–љ—М –∞–љ—В–Є–∞—В–µ—А–Њ–≥–µ–љ–љ–Њ–є —Д—А–∞–Ї—Ж–Є–Є –Ы–Я–Т–Я;
• —Б–љ–Є–ґ–∞–µ—В —Г—А–Њ–≤–µ–љ—М –Њ–±—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞, –Ы–Я–Э–Я, —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤;
• —Г–Љ–µ–љ—М—И–∞–µ—В –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Ї–Њ–љ–µ—З–љ—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ –≥–ї–Є–Ї–Њ–Ј–Є–ї–Є—А–Њ–≤–∞–љ–Є—П;
• —Г–Љ–µ–љ—М—И–∞–µ—В –Њ–Ї—Б–Є–ї–Є—В–µ–ї—М–љ—Л–є —Б—В—А–µ—Б—Б.
–Т—Б–µ –≤—Л—И–µ–њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л –≤–µ–і—Г—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —А–Є—Б–Ї–∞.
–Я—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –Ї –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —П–≤–ї—П—О—В—Б—П:
– –≥–Є–њ–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П –ї—О–±–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞ (—И–Њ–Ї, —Б–µ–њ—Б–Є—Б, –Ї—А–Њ–≤–Њ–њ–Њ—В–µ—А—П, –Њ—Б—В—А–∞—П –Є–ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –∞–љ–µ–Љ–Є—П, –≤—Л—А–∞–ґ–µ–љ–љ–∞—П –і—Л—Е–∞—В–µ–ї—М–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М II–III —Б—В., —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М II–III —Б—В.);
– –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –њ–µ—З–µ–љ–Њ—З–љ—Л—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤ (–±–Њ–ї–µ–µ 2 –љ–Њ—А–Љ);
– –љ–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї (—Г—А–Њ–≤–µ–љ—М –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ –±–Њ–ї–µ–µ 150 –Љ–Ї–Љ–Њ–ї—М/–ї, —А–∞—Б—З–µ—В–љ–∞—П –°–Ъ–§ –Љ–µ–љ–µ–µ 60 –Љ–≥/–Љ–Є–љ/1, 73 –Ї–≤.–Љ);
– –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–Њ–љ—В—А–∞—Б—В–љ—Л—Е –≤–µ—Й–µ—Б—В–≤;
– —Б–µ—А—М–µ–Ј–љ—Л–µ –Њ–њ–µ—А–∞—В–Є–≤–љ—Л–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞;
– –ї–∞–Ї—В–Њ—Ж–Є–і–Њ–Ј –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ;
– —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –∞–ї–Ї–Њ–≥–Њ–ї–Є–Ј–Љ;
– —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–њ–µ–љ–Є—П, –ї–µ–є–Ї–Њ–њ–µ–љ–Є—П.
–Э–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 500 –Љ–≥ –≤ –њ–Њ—Б–ї–µ–і–љ–Є–є –њ—А–Є–µ–Љ –њ–Є—Й–Є. –Я—А–µ–њ–∞—А–∞—В –њ—А–Є–љ–Є–Љ–∞–µ—В—Б—П –≤–Њ –≤—А–µ–Љ—П –Є–ї–Є –њ–Њ—Б–ї–µ –µ–і—Л. –Я—А–Є –љ–µ—Б–Њ–±–ї—О–і–µ–љ–Є–Є —Н—В–Њ–є —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –Љ–Њ–ґ–µ—В –њ–Њ—П–≤–Є—В—М—Б—П –Љ–µ—В–∞–ї–ї–Є—З–µ—Б–Ї–Є–є –њ—А–Є–≤–Ї—Г—Б –≤–Њ —А—В—Г –Є –±–Њ–ї–µ–µ –≤–µ—А–Њ—П—В–љ—Л –і–Є—Б–њ–µ–њ—Б–Є—З–µ—Б–Ї–Є–µ —П–≤–ї–µ–љ–Є—П. –Т –і–∞–ї—М–љ–µ–є—И–µ–Љ –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –і–Њ–Ј–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ —Г–≤–µ–ї–Є—З–µ–љ–∞ –і–Њ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є – 2000 –Љ–≥/—Б—Г—В. (–Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П —Б—Г—В–Њ—З–љ–∞—П –і–Њ–Ј–∞ – 3000 –Љ–≥/—Б—Г—В.). –Ґ–Є—В—А–∞—Ж–Є—П –і–Њ–Ј—Л –њ—А–Њ–≤–Њ–і–Є—В—Б—П –Ї–∞–ґ–і—Л–µ 7–14 –і–љ–µ–є.
–Ш–Ј –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –≤—Б—В—А–µ—З–∞–µ–Љ—Л–Љ–Є —П–≤–ї—П—О—В—Б—П —А–µ–∞–Ї—Ж–Є—П —Б–Њ —Б—В–Њ—А–Њ–љ—Л –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–µ —А–µ–∞–Ї—Ж–Є–Є –Є –ї–∞–Ї—В–∞—В––∞—Ж–Є–і–Њ–Ј –њ—А–Є –љ–µ—Б–Њ–±–ї—О–і–µ–љ–Є–Є –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–є –Ї –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –њ—А–µ–њ–∞—А–∞—В–∞.
–Ф–ї—П –Є—Б–Ї–ї—О—З–µ–љ–Є—П –љ–µ–≥–∞—В–Є–≤–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ –њ–µ—З–µ–љ—М –Є –њ–Њ—З–Ї–Є —З–µ—А–µ–Ј 3 –Љ–µ—Б—П—Ж–∞ –њ—А–Њ–≤–Њ–і–Є—В—Б—П –Ї–Њ–љ—В—А–Њ–ї—М —Г—А–Њ–≤–љ—П –њ–µ—З–µ–љ–Њ—З–љ—Л—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤ (–Р–°–Ґ, –Р–Ы–Ґ) –Є –Ї—А–µ–∞—В–Є–љ–Є–љ–∞. –Т –і–∞–ї—М–љ–µ–є—И–µ–Љ –Ї–Њ–љ—В—А–Њ–ї—М –њ—А–Њ–≤–Њ–і–Є—В—Б—П 1 —А–∞–Ј –≤ 6–12 –Љ–µ—Б. –Ґ–∞–Ї–ґ–µ –Њ—В—Б–ї–µ–ґ–Є–≤–∞–µ—В—Б—П –і–Є–љ–∞–Љ–Є–Ї–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞.
–° 2000 –≥–Њ–і–∞ –У–ї—О–Ї–Њ—Д–∞–ґ –Њ—Д–Є—Ж–Є–∞–ї—М–љ–Њ —А–∞–Ј—А–µ—И–µ–љ –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –≤ –њ–µ–і–Є–∞—В—А–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ (–≤ –†–Њ—Б—Б–Є–Є – —Б 2008 –≥.). –≠—В–Њ –Ї—А–∞–є–љ–µ –≤–∞–ґ–љ–Њ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –њ—А–Њ–±–ї–µ–Љ–∞ –Њ–ґ–Є—А–µ–љ–Є—П —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Б—В–Њ–Є—В –Њ—З–µ–љ—М –Њ—Б—В—А–Њ.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–µ—В—Д–Њ—А–Љ–Є–љ —П–≤–ї—П–µ—В—Б—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б—В—А–∞–і–∞—О—Й–Є—Е –°–Ф 2 —В–Є–њ–∞ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є–µ–є –љ–∞ —Д–Њ–љ–µ –Њ–ґ–Є—А–µ–љ–Є—П —Б –≤—Л—Б–Њ–Ї–Є–Љ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ —А–Є—Б–Ї–Њ–Љ. –Э–µ—Б–Њ–Љ–љ–µ–љ–љ—Л–Љ–Є –њ–ї—О—Б–∞–Љ–Є —П–≤–ї—П—О—В—Б—П:
– –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–є –Ї–Њ–љ—В—А–Њ–ї—М –≥–ї–Є–Ї–µ–Љ–Є–Є;
– –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є;
– –µ–≥–Њ –Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ;
– –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –°–Ф 2 —В–Є–њ–∞ (–Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ DPP, 2002 –≥.);
– –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Г –і–µ—В–µ–є.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –С–∞–ї–∞–±–Њ–ї–Ї–Є–љ –Ь.–Ш. –≠–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є—П. –Ь.: «–£–љ–Є–≤–µ—А—Б—Г–Љ –Я–∞–±–ї–Є—И–Є–љ–≥», 1998. C. 367–470.
2. –С–∞–ї–∞–±–Њ–ї–Ї–Є–љ –Ь.–Ш., –Ъ–ї–µ–±–∞–љ–Њ–≤–∞ –Х.–Ь., –Ъ—А–µ–Љ–Є–љ—Б–Ї–∞—П –Т.–Ь. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ 2 —В–Є–њ–∞ –љ–∞ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ —Н—В–∞–њ–µ // –†—Г—Б—Б–Ї–Є–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. – –Ґ.10. – вДЦ11. – 2002. – –°.496–502.
3. –С—Г—В—А–Њ–≤–∞ –°.–Р. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –У–ї—О–Ї–Њ—Д–∞–ґ–∞ –≤ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ 2 —В–Є–њ–∞ // –†—Г—Б—Б–Ї–Є–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. – –Ґ.11. – вДЦ27. – 2003. – –°.1494–1498.
4. –Ф–µ–і–Њ–≤ –Ш.–Ш., –®–µ—Б—В–∞–Ї–Њ–≤–∞ –Ь.–Т. –°–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В. –†—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є. – –Ь., 2003. – –°. 151–175, 282–292.
5. –Ф–µ–і–Њ–≤ –Ш.–Ш., –®–µ—Б—В–∞–Ї–Њ–≤–∞ –Ь.–Т., –Ь–∞–Ї—Б–Є–Љ–Њ–≤–∞ –Ь.–Р. –§–µ–і–µ—А–∞–ї—М–љ–∞—П —Ж–µ–ї–µ–≤–∞—П –њ—А–Њ–≥—А–∞–Љ–Љ–∞ —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В. –Ь., 2002.
6. –Ф—А–µ–≤–∞–ї—М –Р.–Т., –Ь–Є—Б–љ–Є–Ї–Њ–≤–∞ –Ш.–Т. –†–Њ–ї—М —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–Є—Е —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –ї–µ—З–µ–љ–Є–Є —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ 2 —В–Є–њ–∞ // –†–Њ—Б—Б–Є–є—Б–Ї–Є–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. – –Ґ.13. – вДЦ6. – 2005. – –°. 332–334.
7. –°–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В –Ф–Њ–Ї–ї–∞–і –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М—Б–Ї–Њ–є –≥—А—Г–њ–њ—Л –Т–Ю–Ч –°–µ—А–Є—П —В–µ—Е–љ–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ї–ї–∞–і–Њ–≤ 947 –њ–µ—А —Б –∞–љ–≥–ї. – –Ь., 1999.
8. –°–Љ–Є—А–љ–Њ–≤–∞ –Ю.–Ь. –Т–њ–µ—А–≤—Л–µ –≤—Л—П–≤–ї–µ–љ–љ—Л–є —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В 2 —В–Є–њ–∞. –Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞, —В–∞–Ї—В–Є–Ї–∞ –ї–µ—З–µ–љ–Є–Є. –Ь–µ—В–Њ–і–Є—З–µ—Б–Ї–Њ–µ –њ–Њ—Б–Њ–±–Є–µ.
9. –Ю–ґ–Є—А–µ–љ–Є–µ. –Ь–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–є —Б–Є–љ–і—А–Њ–Љ. –°–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В 2 —В–Є–њ–∞. / –Я–Њ–і —А–µ–і. –∞–Ї–∞–і. –†–Р–Ь–Э. –Ш.–Ш. –Ф–µ–і–Њ–≤–∞. –Ь., 2000. – –°.111.
10. –І—Г–≥—Г–љ–Њ–≤–∞ –Ы.–Р., –®–∞–Љ—Е–∞–ї–Њ–≤–∞ –Ь.–®., –®–µ—Б—В–∞–Ї–Њ–≤–∞ –Ь.–Т. –Ы–µ—З–µ–±–љ–∞—П —В–∞–Ї—В–Є–Ї–∞ –њ—А–Є —Б–∞—Е–∞—А–љ–Њ–Љ –і–Є–∞–±–µ—В–µ 2 —В–Є–њ–∞ —Б –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є–µ–є (–њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Ї—А—Г–њ–љ—Л—Е –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є), –Є–љ—Д. —Б–Є—Б—В.
11. Diabetes Prevention Program Research Group. N EnglJ Med 2002; 346: 393–403.
12. Howard B.V. Pathogenesis of diabetic dyslipidaemia. Diabetes Rev 1995; 3: 423–432.
13. Laakso M. Epidemiology of Diabetic Dyslipidemia. Diabetes Rev 1995; 3: 408–422.
14. Koyama K., Chen G., Lee Y., Unger R.H. Tissue triglycerides, insulin resistance, and insulin production: implications for hyperinsulinemia of obesity // Am. J. Physiol. – 1997. – Vol. 273. – P. 708–713.
15. Manzato E., Zambon A., Lapolla A. et al. Lipoprotein Abnormalities in well–treated type II diabetic patients. Diabetes Care 1993; 16: 469–475.
16. Stamler J., Vaccaro O., Neaton J.D. et al. for the Multiple Risk Factor Intervention Trial Research Group: Diabetes, other risk factors, and 12–yr cardiovascular mortality for men screened in the Multiple Risk Factor Intervention Trial. Diabetes Care 1993; 16: 434–444.
17. Sacks F.M., Pfeffer M.A., Moye L.A. et al. for the Cholesterol and Recurrent Events Trial Investigators. The effect of pravastatin on coronary events after myocardial infarction in patients with average cholesterol levels. N Engl J Med 1996; 335: 1001–1009.
18. United Kingdom Prospective Diabetes Study Group: Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38. BMJ 317:703–713, 1998.












