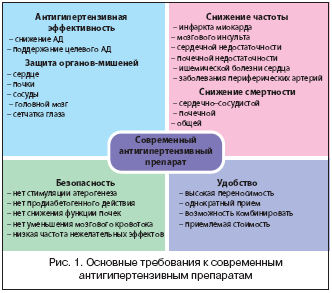
–Ь–љ–Њ–≥–Є–µ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –≤ —В–Њ–є –Є–ї–Є –Є–љ–Њ–є —Б—В–µ–њ–µ–љ–Є —Г–і–Њ–≤–ї–µ—В–≤–Њ—А—П—О—В –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–Љ —В—А–µ–±–Њ–≤–∞–љ–Є—П–Љ. –Ю–і–љ–∞–Ї–Њ, –≤ –љ–∞–Є–±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Н—В–Њ –Љ–Њ–ґ–љ–Њ —Б–Ї–∞–Ј–∞—В—М –Њ–± –Є–Р–Я–§. –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ —П–≤–ї—П–µ—В—Б—П –Є—Е —Г–љ–Є–Ї–∞–ї—М–љ–∞—П «–њ–Њ–ї–Є–њ–Њ—В–µ–љ—В–љ–Њ—Б—В—М». –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –Є–Љ–µ—О—В –љ–∞ —Б–µ–≥–Њ–і–љ—П –љ–∞–Є–±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Є–є —Б–њ–Є—Б–Њ–Ї –њ–Њ–Ї–∞–Ј–∞–љ–Є–є –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О, –≤–Ї–ї—О—З–∞—О—Й–Є–є –Р–У, –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞, —Б—В–∞–±–Є–ї—М–љ—Г—О –Ш–С–°, —Е—А–Њ–љ–Є—З–µ—Б–Ї—Г—О —Б–µ—А–і–µ—З–љ—Г—О –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М (–•–°–Э), –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є—О –Є –њ—А–Њ—В–µ–Є–љ—Г—А–Є—О, –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї—Г—О –Є –љ–µ–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї—Г—О –љ–µ—Д—А–Њ–њ–∞—В–Є—О, –њ–µ—А–µ–љ–µ—Б–µ–љ–љ—Л–є –Ь–Ш. –Я—А–Є—З–µ–Љ –њ–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤—Г –њ–Њ–Ї–∞–Ј–∞–љ–Є–є –і–ї—П –Є–Р–Я–§ –Є–Љ–µ–µ—В—Б—П –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–∞—П –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–∞—П –±–∞–Ј–∞ –Є –≤—Л—Б—И–Є–є —Г—А–Њ–≤–µ–љ—М —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є (—В–∞–±–ї. 1) [8–10].
–°—В–Њ–ї—М —И–Є—А–Њ–Ї–∞—П –Њ–±–ї–∞—Б—В—М –і–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–Р–Я–§ –ї–Њ–≥–Є—З–љ–Њ –Њ–±—К—П—Б–љ—П–µ—В—Б—П —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є —А–Њ–ї—М—О –∞–Ї—В–Є–≤–∞—Ж–Є–Є —А–µ–љ–Є–љ––∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ––∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л (–†–Р–Р–°) –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–∞ –≤—Б–µ—Е —Н—В–∞–њ–∞—Е –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–≥–Њ –Є –њ–Њ—З–µ—З–љ–Њ–≥–Њ –Ї–Њ–љ—В–Є–љ—Г—Г–Љ–Њ–≤, –љ–∞—З–Є–љ–∞—П –Њ—В –њ–µ—А–≤—Л—Е —Н–њ–Є–Ј–Њ–і–Њ–≤ –њ–Њ–≤—Л—И–µ–љ–Є—П –Р–Ф –Є –Ї–Њ–љ—З–∞—П —А–∞–Ј–≤–Є—В–Є–µ–Љ —В–µ—А–Љ–Є–љ–∞–ї—М–љ—Л—Е —Б—В–∞–і–Є–є –±–Њ–ї–µ–Ј–љ–Є –≤ –≤–Є–і–µ –•–°–Э –Є–ї–Є –•–Я–Э. –Т —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е in vitro, –љ–∞ –ґ–Є–≤–Њ—В–љ—Л—Е –Љ–Њ–і–µ–ї—П—Е in vivo –Є –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Г —З–µ–ї–Њ–≤–µ–Ї–∞ –і–Њ–Ї–∞–Ј–∞–љ–∞ —А–Њ–ї—М –†–Р–Р–° (–њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –µ–µ —В–Ї–∞–љ–µ–≤–Њ–≥–Њ –Ј–≤–µ–љ–∞) –≤ —А–∞–Ј–≤–Є—В–Є–Є —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –Є –≤—В–Њ—А–Є—З–љ—Л—Е –Р–У, —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є, —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П –∞—А—В–µ—А–Є–є –Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞, –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ (–У–Ы–Ц), –Є—И–µ–Љ–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞, —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П —Б–µ—А–і—Ж–∞ –њ–Њ—Б–ї–µ –Ш–Ь, –•–°–Э, –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –Є –љ–µ–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (–•–Я–Э). –Т —Ж–µ–ї–Њ–Љ –≤—Л—А–∞–ґ–µ–љ–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –†–Р–Р–° (–Ї–∞–Ї –∞–Ї—В–Є–≤–∞—Ж–Є—П, —В–∞–Ї –Є –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ) –≤—Л—П–≤–ї–µ–љ—Л –њ—А–Є –±–Њ–ї–µ–µ —З–µ–Љ 30 –љ–Њ–Ј–Њ–ї–Њ–≥–Є—П—Е –Є —Б–Є–љ–і—А–Њ–Љ–∞—Е [11]. –£—З–Є—В—Л–≤–∞—П –≤–∞–ґ–љ–µ–є—И—Г—О —А–Њ–ї—М –†–Р–Р–° –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є –Р–У –Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –Њ—А–≥–∞–љ–Њ–≤––Љ–Є—И–µ–љ–µ–є, –∞ —В–∞–Ї–ґ–µ —А–∞–Ј–≤–Є—В–Є–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Р–У, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –±–ї–Њ–Ї–Є—А—Г—О—Й–Є—Е —Н—В—Г —Б–Є—Б—В–µ–Љ—Г, –≤—Л–≥–ї—П–і–Є—В –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ—Л–Љ.
–Э–∞ —Б–µ–≥–Њ–і–љ—П –Є–Љ–µ—О—В—Б—П —В—А–Є –≥—А—Г–њ–њ—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –љ–∞–њ—А—П–Љ—Г—О –±–ї–Њ–Ї–Є—А—Г—О—Й–Є—Е –†–Р–Р–°: –Є–Р–Я–§, –±–ї–Њ–Ї–∞—В–Њ—А—Л –Р–Ґ1–—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–∞ (–С–†–Р) –Є –њ—А—П–Љ–Њ–є –Є–љ–≥–Є–±–Є—В–Њ—А —А–µ–љ–Є–љ–∞ –∞–ї–Є—Б–Ї–Є—А–µ–љ. –Я–µ—А–≤—Л–Љ —Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ, –±–ї–Њ–Ї–Є—А—Г—О—Й–Є–Љ –†–Р–Р–°, —Б—В–∞–ї –С–†–Р —Б–∞—А–∞–ї–∞–Ј–Є–љ, —Б–Њ–Ј–і–∞–љ–љ—Л–є –≤ 1971 –≥–Њ–і—Г [12]. –Ю–і–љ–∞–Ї–Њ –Њ–љ –љ–µ –±—Л–ї –≤–љ–µ–і—А–µ–љ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –њ—А–∞–Ї—В–Є–Ї—Г –≤ —Б–≤—П–Ј–Є —Б —В–µ–Љ, —З—В–Њ –Њ–±–ї–∞–і–∞–ї —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є —З–∞—Б—В–Є—З–љ–Њ–≥–Њ –∞–≥–Њ–љ–Є—Б—В–∞ –Є –±—Л–ї –њ—А–Є–≥–Њ–і–µ–љ –ї–Є—И—М –і–ї—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П. –Я–Њ—Н—В–Њ–Љ—Г –њ–∞–ї—М–Љ–∞ –њ–µ—А–≤–µ–љ—Б—В–≤–∞ –±—Л—Б—В—А–Њ –њ–µ—А–µ—И–ї–∞ –Ї –Є–Р–Я–§, –њ–µ—А–≤—Л–є –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї—М –Ї–Њ—В–Њ—А—Л—Е – –Ї–∞–њ—В–Њ–њ—А–Є–ї –±—Л–ї —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–љ –њ–Њ–і —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ–Љ D. Cushman –Є M. Ondetti –≤ 1975 –≥. –Ъ –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –Љ–Њ–Љ–µ–љ—В—Г —Б–Њ–Ј–і–∞–љ–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –і–µ—Б—П—В–Ї–Њ–≤ —Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є, —Б–њ–Њ—Б–Њ–±–љ—Л—Е –±–ї–Њ–Ї–Є—А–Њ–≤–∞—В—М –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Р–Я–§, –±–Њ–ї–µ–µ –і–µ—Б—П—В–Ї–∞ –Є–Р–Я–§ –≤–љ–µ–і—А–µ–љ—Л –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –њ—А–∞–Ї—В–Є–Ї—Г. –° –Љ–Њ–Љ–µ–љ—В–∞ –њ—Г–±–ї–Є–Ї–∞—Ж–Є–Є IV –і–Њ–Ї–ї–∞–і–∞ –Ю–±—К–µ–і–Є–љ–µ–љ–љ–Њ–≥–Њ –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –Ї–Њ–Љ–Є—В–µ—В–∞ –°–®–Р –њ–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є—О –Р–У –≤ 1988 –≥. [13] –Є–Р–Я–§ –љ–µ–Є–Ј–Љ–µ–љ–љ–Њ –≤—Е–Њ–і—П—В –≤ —З–Є—Б–ї–Њ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ–µ—А–≤–Њ–≥–Њ —А—П–і–∞ –≤–Њ –≤—Б–µ—Е –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л—Е –Є –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е –њ–Њ –ї–µ—З–µ–љ–Є—О –Р–У.
–Ь–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –Є–Р–Я–§ –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ –Ї–Њ–љ–Ї—Г—А–µ–љ—В–љ–Њ–Љ –њ–Њ–і–∞–≤–ї–µ–љ–Є–Є –Р–Я–§, —З—В–Њ, —Б –Њ–і–љ–Њ–є —Б—В–Њ—А–Њ–љ—Л, –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–∞ II – –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–Њ—А–∞ –†–Р–Р–°, –∞ —Б –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, —Г–Љ–µ–љ—М—И–∞–µ—В –і–µ–≥—А–∞–і–∞—Ж–Є—О –±—А–∞–і–Є–Ї–Є–љ–Є–љ–∞, –Ї–∞–ї–ї–Є–Ї—А–µ–Є–љ–∞, —Б—Г–±—Б—В–∞–љ—Ж–Є–Є –†. –≠—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л –Є–Р–Я–§: —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П, —Г–ї—Г—З—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є —Н–љ–і–Њ—В–µ–ї–Є—П, –∞–љ—В–Є–њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ, –≤–ї–Є—П–љ–Є–µ –љ–∞ —Б–Є—Б—В–µ–Љ—Г —Б–≤–µ—А—В—Л–≤–∞–љ–Є—П –Ї—А–Њ–≤–Є, —Г–ї—Г—З—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї.
–Т—Б–µ –Є–Р–Я–§ –Њ–±–ї–∞–і–∞—О—В –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О, –љ–µ –≤—Л–Ј—Л–≤–∞—О—Й–µ–є —Б–Њ–Љ–љ–µ–љ–Є–є. –Э–µ–і–∞–≤–љ–Њ —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–∞–Љ–Є –Ъ–Њ–Ї—А–µ–є–љ–Њ–≤—Б–Ї–Њ–≥–Њ —Б–Њ—В—А—Г–і–љ–Є—З–µ—Б—В–≤–∞ –±—Л–ї –≤—Л–њ–Њ–ї–љ–µ–љ –Ї—А—Г–њ–љ—Л–є –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј 92 –†–Ъ–Ш, –≤–Ї–ї—О—З–∞–≤—И–Є—Е 12 954 –њ–∞—Ж–Є–µ–љ—В–∞, –≤ –Ї–Њ—В–Њ—А—Л—Е –Є–Ј—Г—З–∞–ї–∞—Б—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М 14 —А–∞–Ј–ї–Є—З–љ—Л—Е –Є–Р–Я–§ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –њ–ї–∞—Ж–µ–±–Њ. –С—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–Р–Я–§ –≤ –њ–Њ–ї–Њ–≤–Є–љ–љ—Л—Е –і–Њ–Ј–∞—Е –Њ—В –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л—Е —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–љ—Л—Е, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —Б–љ–Є–ґ–µ–љ–Є–µ –Р–Ф –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 8/5 –Љ–Љ —А—В.—Б—В., –њ—А–Є—З–µ–Љ –Њ—В 60 –і–Њ 70% —Н—Д—Д–µ–Ї—В–∞ —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –і–∞–ґ–µ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–љ—Л—Е –і–Њ–Ј–Є—А–Њ–≤–Њ–Ї –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Я—А–Є —Н—В–Њ–Љ –љ–µ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤ –Є–ї–Є –љ–µ–і–Њ—Б—В–∞—В–Ї–Њ–≤ –Ї–∞–Ї–Є—Е––ї–Є–±–Њ –Ї–Њ–љ–Ї—А–µ—В–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ [14]. –Т—Л—А–∞–ґ–µ–љ–љ—Л–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –њ–Њ–Ј–≤–Њ–ї—П–µ—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Є–Р–Я–§ –і–ї—П —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф –њ—А–Є –Р–У, –Ї–∞–Ї –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ —Б —Г—А–Њ–≤–љ–µ–Љ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є «–Р» [8]. –Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –њ–ї–µ–є–Њ—В—А–Њ–њ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Є–Р–Я–§ –≤–Ї–ї—О—З–∞—О—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г–Љ–µ–љ—М—И–∞—В—М –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –У–Ы–Ц, —Б–љ–Є–ґ–∞—В—М —Н–Ї—Б–Ї—А–µ—Ж–Є—О –∞–ї—М–±—Г–Љ–Є–љ–∞ —Б –Љ–Њ—З–Њ–є, –Ј–∞–Љ–µ–і–ї—П—В—М –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –Є –љ–µ–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є, –Є—Б–њ—А–∞–≤–ї—П—В—М —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–µ —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є–µ –Є –і—А. (—В–∞–±–ї. 2)
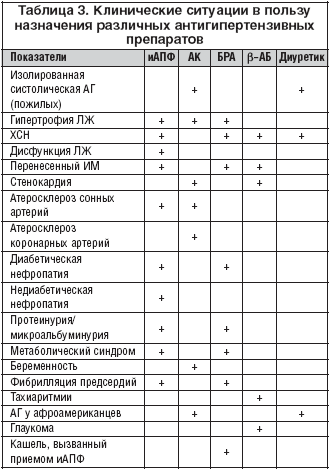
–Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –≤ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е –њ–Њ –ї–µ—З–µ–љ–Є—О –Р–У –љ–∞–Є–±–Њ–ї—М—И–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞–љ–Є–є —Б—Г—Й–µ—Б—В–≤—Г–µ—В –Є–Љ–µ–љ–љ–Њ –і–ї—П –Є–Р–Я–§ (—В–∞–±–ї. 3).
–Ю–і–љ–∞–Ї–Њ –Є–Р–Я–§ –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є –≥–µ—В–µ—А–Њ–≥–µ–љ–љ—Г—О –≥—А—Г–њ–њ—Г –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Њ—В–ї–Є—З–∞—О—Й–Є—Е—Б—П –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є –Ї–∞–Ї –њ–Њ —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–µ, –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є –Є —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є–Ї–Є, —В–∞–Ї –Є –њ–Њ –љ–∞–ї–Є—З–Є—О –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –±–∞–Ј—Л –і–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ–Њ —А–∞–Ј–ї–Є—З–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ. –Т–∞–ґ–љ–Њ –њ–Њ–љ–Є–Љ–∞—В—М, —З—В–Њ —Е–Њ—В—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Є–Р–Я–§ —Б–љ–Є–ґ–∞—В—М –Р–Ф –Є –Ј–∞–Љ–µ–і–ї—П—В—М –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –•–°–Э —А–∞—Б—Ж–µ–љ–Є–≤–∞–µ—В—Б—П –Ї–∞–Ї –Ї–ї–∞—Б—Б–—Н—Д—Д–µ–Ї—В—Л [8], –Љ–љ–Њ–≥–Є–µ –Њ—А–≥–∞–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Њ—В–і–µ–ї—М–љ—Л—Е –Є–Р–Я–§ –љ–µ –Љ–Њ–≥—Г—В –±—Л—В—М —Б –њ–Њ–Ј–Є—Ж–Є–є –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л –њ–µ—А–µ–љ–µ—Б–µ–љ—Л –љ–∞ –≤–µ—Б—М –Ї–ї–∞—Б—Б –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
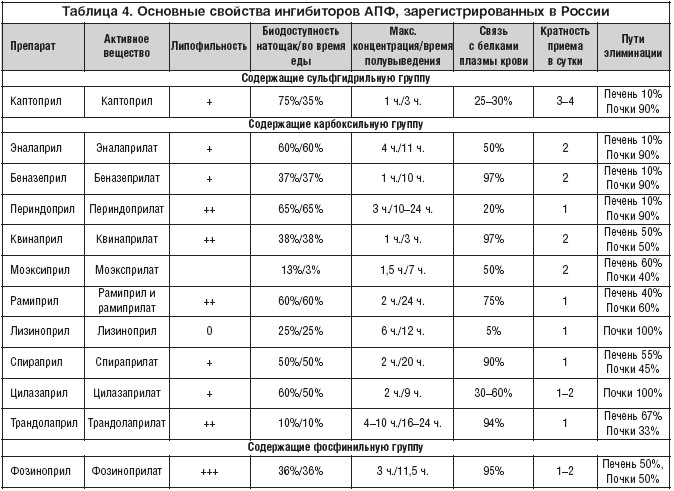
–Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —А–∞–Ј–ї–Є—З–∞—О—В—Б—П –њ–Њ —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–µ (–љ–∞–ї–Є—З–Є—О —Б—Г–ї—М—Д–≥–Є–і—А–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л –Є –і—А.), –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ (–љ–∞–ї–Є—З–Є–µ —Н—Д—Д–µ–Ї—В–∞ –њ–µ—А–≤–Њ–≥–Њ –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є—П —З–µ—А–µ–Ј –њ–µ—З–µ–љ—М), –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ –≤—Л–≤–µ–і–µ–љ–Є—П –Є–Ј –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ (—В–Њ–ї—М–Ї–Њ –њ–Њ—З–Ї–∞–Љ–Є –Є–ї–Є –њ–Њ—З–Ї–∞–Љ–Є —Б–Њ–≤–Љ–µ—Б—В–љ–Њ —Б –њ–µ—З–µ–љ—М—О), –ї–Є–њ–Њ—Д–Є–ї—М–љ–Њ—Б—В–Є, —В–Ї–∞–љ–µ–≤–Њ–є —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В–Є (—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –±–ї–Њ–Ї–Є—А–Њ–≤–∞—В—М —В–Ї–∞–љ–µ–≤—Л–µ –†–Р–Р–°) –Є –њ–Њ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –і–µ–є—Б—В–≤–Є—П (—В–∞–±–ї. 4).
–С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Є–Р–Я–§ —П–≤–ї—П—О—В—Б—П –њ—А–Њ–ї–µ–Ї–∞—А—Б—В–≤–∞–Љ–Є, –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г—О—Й–Є–Љ–Є—Б—П –≤ –њ–µ—З–µ–љ–Є —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –∞–Ї—В–Є–≤–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є—Е –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–µ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ. –Ъ—А–Њ–Љ–µ –њ–µ—З–µ–љ–Є, –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Г—О —А–Њ–ї—М –≤ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–є —В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–Є –њ—А–Њ–ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Д–Њ—А–Љ –Є–Р–Я–§ –Є–≥—А–∞—О—В –≥–Є–і—А–Њ–ї–∞–Ј—Л —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, –Ї—А–Њ–≤–Є –Є –≤–љ–µ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —В–Ї–∞–љ–µ–є. –Ы–Є—И—М 4 –Є–Р–Я–§ (–Ї–∞–њ—В–Њ–њ—А–Є–ї, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї, –ї–Є–±–µ–љ–Ј–∞–њ—А–Є–ї –Є —Ж–µ–љ–Њ–ї–∞–њ—А–Є–ї) –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –Њ–±–ї–∞–і–∞—О—В –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О, –њ—А—П–Љ–Њ —Б–≤—П–Ј—Л–≤–∞—П—Б—М —Б –Є–Њ–љ–Њ–Љ —Ж–Є–љ–Ї–∞ –≤ –∞–Ї—В–Є–≤–љ—Л—Е —Ж–µ–љ—В—А–∞—Е –Р–Я–§. –§–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–∞ —А–∞–Ј–ї–Є—З–љ—Л—Е –Є–Р–Я–§ –љ–µ–Њ–і–Є–љ–∞–Ї–Њ–≤–∞. –°–Є—Б—В–µ–Љ–љ–∞—П –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М –≥–Є–і—А–Њ—Д–Є–ї—М–љ—Л—Е –Є–Р–Я–§ –љ–Є–ґ–µ, —З–µ–Љ –ї–Є–њ–Њ—Д–Є–ї—М–љ—Л—Е. –Ф–ї—П –≤—Б–µ—Е –Є–Ј–≤–µ—Б—В–љ—Л—Е –Є–Р–Я–§ –Є –Є—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ –Њ—Б–љ–Њ–≤–љ—Л–Љ –њ—Г—В–µ–Љ –≤—Л–≤–µ–і–µ–љ–Є—П –Є–Ј –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ —П–≤–ї—П–µ—В—Б—П –њ–Њ—З–µ—З–љ—Л–є. –Я–Њ—Н—В–Њ–Љ—Г —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –±–Њ–ї—М–љ—Л—Е —Б –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ –Ї–Њ—А—А–µ–Ї—Ж–Є—П –і–Њ–Ј –Є–Р–Я–§. –°—А–µ–і–Є –Є–Р–Я–§ –Є–Љ–µ—О—В—Б—П –њ—А–µ–њ–∞—А–∞—В—Л, –і–Є–∞—Ж–Є–і–љ—Л–µ –Љ–µ—В–∞–±–Њ–ї–Є—В—Л –Ї–Њ—В–Њ—А—Л—Е –≤—Л–≤–Њ–і—П—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ —З–µ—А–µ–Ј –њ–Њ—З–Ї–Є, –љ–Њ –Є —Б –ґ–µ–ї—З—М—О –Є –Ї–∞–ї–Њ–Љ – —Б–њ–Є—А–∞–њ—А–Є–ї (–Ъ–≤–∞–і—А–Њ–њ—А–Є–ї), —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї, —В—А–∞–љ–і–Њ–ї–∞–њ—А–Є–ї. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —В–∞–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Љ–Њ–ґ–µ—В –±—Л—В—М –±–Њ–ї–µ–µ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ —Г –±–Њ–ї—М–љ—Л—Е –•–Я–Э.
–°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Њ–њ—А–Њ—Б–Њ–≤ –≤—А–∞—З–µ–є, –њ—А–Њ–≤–Њ–і–Є–≤—И–Є—Е—Б—П –≤ —А–∞–Љ–Ї–∞—Е –њ—А–Њ–≥—А–∞–Љ–Љ –Я–Ш–§–Р–У–Ю–† [15], —Б—А–µ–і–Є –≤—Б–µ—Е –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –Є–Р–Я–§ –љ–∞–Ј–љ–∞—З–∞—О—В—Б—П –≤—А–∞—З–∞–Љ–Є –љ–∞–Є–±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Њ – –і–Њ–ї—П –Є–Р–Я–§ —Б—А–µ–і–Є –≤—Б–µ—Е –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 32%.
–Ю–і–љ–Є–Љ –Є–Ј —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ –љ–µ–і–∞–≤–љ–Њ –њ–Њ—П–≤–Є–≤—И–Є—Е—Б—П –љ–∞ –љ–∞—И–µ–Љ —А—Л–љ–Ї–µ –Є–Р–Я–§ —П–≤–ї—П–µ—В—Б—П —Б–њ–Є—А–∞–њ—А–Є–ї (–Ъ–≤–∞–і—А–Њ–њ—А–Є–ї). –С—Г–і—Г—З–Є —В–Є–њ–Є—З–љ—Л–Љ –њ—А–Њ–ї–µ–Ї–∞—А—Б—В–≤–Њ–Љ, —Б–њ–Є—А–∞–њ—А–Є–ї –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П –≤ –њ–µ—З–µ–љ–Є –≤ —Б–њ–Є—А–∞–њ—А–Є–ї–∞—В, –Ї–Њ—В–Њ—А—Л–є –Њ–±–ї–∞–і–∞–µ—В –≤—Л—Б–Њ–Ї–Є–Љ —Б—А–Њ–і—Б—В–≤–Њ–Љ –Ї –Р–Я–§ (–њ–Њ—З—В–Є –≤ 10 —А–∞–Ј –±–Њ–ї—М—И–Є–Љ, —З–µ–Љ –Ї–∞–њ—В–Њ–њ—А–Є–ї [16]) –Є –і–ї–Є—В–µ–ї—М–љ—Л–Љ –њ–µ—А–Є–Њ–і–Њ–Љ –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П. –Я—А–µ–њ–∞—А–∞—В—Г –њ—А–Є—Б—Г—Й —Б–±–∞–ї–∞–љ—Б–Є—А–Њ–≤–∞–љ–љ—Л–є –њ—Г—В—М –≤—Л–≤–µ–і–µ–љ–Є—П: –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤ —А–∞–≤–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –Ъ–≤–∞–і—А–Њ–њ—А–Є–ї –≤—Л–≤–Њ–і–Є—В—Б—П —З–µ—А–µ–Ј –њ–Њ—З–Ї–Є –Є —Б –ґ–µ–ї—З—М—О.
–Р–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–њ–Є—А–∞–њ—А–Є–ї–∞ –±—Л–ї–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ –≤–Њ –Љ–љ–Њ–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, –њ–Њ–Ї–∞–Ј–∞–≤—И–Є—Е, —З—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф (–°–Р–Ф) —Б–Њ—Б—В–∞–≤–Є–ї–Њ –Њ—В 10 –і–Њ 18 –Љ–Љ —А—В.—Б—В., –∞ –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф (–Ф–Р–Ф) –Њ—В 7 –і–Њ 13 –Љ–Љ —А—В.—Б—В. –Я—А–Є —Н—В–Њ–Љ —З–∞—Б—В–Њ—В–∞ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–≥–Њ –Ф–Р–Ф<90 –Љ–Љ —А—В.—Б—В. —Б–Њ—Б—В–∞–≤–Є–ї–∞ –Њ–Ї–Њ–ї–Њ 50% [17]. –Я—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є 6 –Љ–≥ —Б–њ–Є—А–∞–њ—А–Є–ї–∞ —Б 5–20 –Љ–≥ —Н–љ–∞–ї–∞–њ—А–Є–ї–∞ –≤ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б –њ–∞—А–∞–ї–ї–µ–ї—М–љ—Л–Љ–Є –≥—А—Г–њ–њ–∞–Љ–Є —Г 251 –њ–∞—Ж–Є–µ–љ—В–∞ —Б –Р–У I–II —Б—В. –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –Њ–±–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є —Б—В–µ–њ–µ–љ–Є —Б–љ–Є–ґ–∞—О—В –°–Р–Ф. –Ю–і–љ–∞–Ї–Њ —Б–њ–Є—А–∞–њ—А–Є–ї –Њ–Ї–∞–Ј–∞–ї—Б—П –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–љ–Є–ґ–µ–љ–Є—П –Ф–Р–Ф –Ї–∞–Ї –љ–∞ –њ–Є–Ї–µ —Н—Д—Д–µ–Ї—В–∞, —В–∞–Ї –Є –≤ –Ї–Њ–љ—Ж–µ –Є–љ—В–µ—А–≤–∞–ї–∞ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П [18]. –Э–∞–Є–±–Њ–ї–µ–µ –Љ–∞—Б—И—В–∞–±–љ–Њ–µ –Є–Ј—Г—З–µ–љ–Є–µ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б–њ–Є—А–∞–њ—А–Є–ї–∞ –њ—А–Њ–≤–µ–і–µ–љ–Њ –≤ –У–µ—А–Љ–∞–љ—Б–Ї–Њ–Љ –Њ—В–Ї—А—Л—В–Њ–Љ, –љ–∞–±–ї—О–і–∞—В–µ–ї—М–љ–Њ–Љ, –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г 5000 –∞–Љ–±—Г–ї–∞—В–Њ—А–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–У [19]. –Я—А–µ–њ–∞—А–∞—В –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –≤ –і–Њ–Ј–µ 6 –Љ–≥/—Б—Г—В. –Њ–і–Є–љ —А–∞–Ј –≤ –і–µ–љ—М. –Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–∞ 3 –Љ–µ—Б. –°–њ–Є—А–∞–њ—А–Є–ї –≤—Л–Ј—Л–≤–∞–ї –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –°–Р–Ф –Є –Ф–Р–Ф (–Є—Б—Е–Њ–і–љ–Њ 175,5/99,8 –Љ–Љ —А—В.—Б—В., –≤ –Ї–Њ–љ—Ж–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П 146,9/85,1 –Љ–Љ —А—В.—Б—В.). –Т –Ї–Њ–љ—Ж–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г 89,4% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –°–Р–Ф –љ–µ –Љ–µ–љ—М—И–µ, —З–µ–Љ –љ–∞ 15 –Љ–Љ —А—В.—Б—В., —Г 85,4% — —Б–љ–Є–ґ–µ–љ–Є–µ –Ф–Р–Ф –љ–µ –Љ–µ–љ—М—И–µ, —З–µ–Љ –љ–∞ 10 –Љ–Љ —А—В.—Б—В., –њ—А–Є—З–µ–Љ —З–∞—Б—В–Њ—В–∞ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –Ф–Р–Ф –±—Л–ї–∞ –≤—Л—И–µ, —З–µ–Љ –°–Р–Ф. –Я–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ —Г 95,3% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—Ж–µ–љ–µ–љ–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—П–Љ–Є –Ї–∞–Ї —Е–Њ—А–Њ—И–∞—П –Є–ї–Є –Њ—З–µ–љ—М —Е–Њ—А–Њ—И–∞—П. –Ґ–Њ–ї—М–Ї–Њ —Г 2,9% –±–Њ–ї—М–љ—Л—Е –≤–Њ–Ј–љ–Є–Ї–ї–Є –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Є –ї–Є—И—М 0,88% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –ґ–∞–ї–Њ–≤–∞–ї–Є—Б—М –љ–∞ –Ї–∞—И–µ–ї—М –≤ —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–њ–Є—А–∞–њ—А–Є–ї–∞ [19].
–°—А–µ–і–Є –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л—Е –њ—А–Њ–µ–Ї—В–Њ–≤, –≤ –Ї–Њ—В–Њ—А—Л—Е –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–Р–Я–§ –≤ —А–µ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ, —Б–њ–Є—А–∞–њ—А–Є–ї –Є–Ј—Г—З–∞–ї—Б—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Ъ–Т–Р–Ф–†–Ш–У–Р [20], —Ж–µ–ї—М—О –Ї–Њ—В–Њ—А–Њ–≥–Њ –±—Л–ї–∞ –Њ—Ж–µ–љ–Ї–∞ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є —Б–њ–Є—А–∞–њ—А–Є–ї–∞ –≤ –і–Њ–Ј–µ 6 –Љ–≥ —Г –±–Њ–ї—М–љ—Л—Е –Р–У –≤ –≤–Є–і–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Є –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –і–Є—Г—А–µ—В–Є–Ї–Њ–Љ. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Ї–ї—О—З–Є–ї–Є 535 –±–Њ–ї—М–љ—Л—Е (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В 51 –≥–Њ–і) –Є–Ј 11 —А–µ–≥–Є–Њ–љ–Њ–≤ –љ–∞—И–µ–є —Б—В—А–∞–љ—Л —Б –°–Р–Ф 140–179 –Љ–Љ —А—В.—Б—В. –Є/–Є–ї–Є –Ф–Р–Ф (–Р–Ф) 100–109 –Љ–Љ —А—В.—Б—В. –Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–∞ 12 –љ–µ–і–µ–ї—М. –°–њ–Є—А–∞–њ—А–Є–ї –≤ –і–Њ–Ј–µ 6 –Љ–≥ –њ—А–Є –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–Љ –њ—А–Є–µ–Љ–µ –≤ –≤–Є–і–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Є–ї–Є –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і–Њ–Љ (—Г 52% –±–Њ–ї—М–љ—Л—Е) –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Р–Ф (–≤ —Б—А–µ–і–љ–µ–Љ —Б 160/98 –і–Њ 133/83 –Љ–Љ —А—В.—Б—В., —А<0,01). –Я–Њ –і–∞–љ–љ—Л–Љ —Б—Г—В–Њ—З–љ–Њ–≥–Њ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—П –Р–Ф –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –≤–µ–ї–Є—З–Є–љ —Б—Г—В–Њ—З–љ–Њ–≥–Њ, –і–љ–µ–≤–љ–Њ–≥–Њ –Є –љ–Њ—З–љ–Њ–≥–Њ –Р–Ф. –І–∞—Б—В–Њ—В–∞ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є —Б–Њ—Б—В–∞–≤–Є–ї–∞ 8,7%, –љ–Є –≤ –Њ–і–љ–Њ–Љ —Б–ї—Г—З–∞–µ –Њ—В–Љ–µ–љ—Л –њ—А–µ–њ–∞—А–∞—В–∞ –љ–µ —В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М.
–°–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Є–Р–Я–§ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –≤–ї–Є—П—В—М –љ–∞ –њ—А–Њ–≥–љ–Њ–Ј –±–Њ–ї—М–љ—Л—Е –Р–У —Г–±–µ–і–Є—В–µ–ї—М–љ–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є –Є –Њ–±–Њ–±—Й–µ–љ–∞ –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Ї—А—Г–њ–љ—Л—Е –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–∞—Е. –Ґ–∞–Ї, –љ–∞–њ—А–Є–Љ–µ—А, –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј, –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л–є —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–∞–Љ–Є Blood Pressure Lowering Treatment Trialists‘ Collaboration, –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –Є–Р–Я–§ –љ–µ —Г—Б—В—Г–њ–∞—О—В –і–Є—Г—А–µ—В–Є–Ї–∞–Љ –Є b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ –њ–Њ –≤–ї–Є—П–љ–Є—О –љ–∞ —З–∞—Б—В–Њ—В—Г –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є –Є —Б–Љ–µ—А—В–µ–ї—М–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ [21]. –Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ –і–∞–љ–љ—Л–µ –њ–Њ–ї—Г—З–µ–љ—Л –≤ –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–µ B. Psaty —Б —Б–Њ–∞–≤—В. [22]. –Ю–і–љ–∞–Ї–Њ –љ–∞–Є–±–Њ–ї–µ–µ –њ–Њ–ї–љ—Л–Љ –љ–∞ —Б–µ–≥–Њ–і–љ—П –Љ–Њ–ґ–љ–Њ —Б—З–Є—В–∞—В—М –љ–Њ–≤–µ–є—И–Є–є –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј M. Law —Б —Б–Њ–∞–≤—В. [23], –Њ–±–Њ–±—Й–Є–≤—И–Є–є —А–µ–Ј—Г–ї—М—В–∞—В—Л 147 —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б–њ—Л—В–∞–љ–Є–є (464164 –њ–∞—Ж–Є–µ–љ—В–∞), –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –≤ –њ–µ—А–Є–Њ–і —Б 1966 –њ–Њ 2007 –≥–≥. –Я–Њ –і–∞–љ–љ—Л–Љ —Н—В–Њ–≥–Њ –Ї—А—Г–њ–љ–µ–є—И–µ–≥–Њ –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–∞, –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –њ–ї–∞—Ж–µ–±–Њ –Є–Р–Я–§ —Г–Љ–µ–љ—М—И–∞—О—В –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е —Б–Њ–±—Л—В–Є–є –љ–∞ 17%, –∞ –Є–љ—Б—Г–ї—М—В–∞ –љ–∞ 22%. –Я—А–Є —Н—В–Њ–Љ —В–µ—А–∞–њ–Є—П –Є–Р–Я–§ –њ–Њ –≤–ї–Є—П–љ–Є—О –љ–∞ –Њ—Б–љ–Њ–≤–љ—Л–µ –і–µ—В–µ—А–Љ–Є–љ–∞–љ—В—Л –њ—А–Њ–≥–љ–Њ–Ј–∞ –Є –љ–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Г—О —Б–Љ–µ—А—В–љ–Њ—Б—В—М –љ–µ —Г—Б—В—Г–њ–∞–µ—В –і—А—Г–≥–Є–Љ –Ї–ї–∞—Б—Б–∞–Љ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–° —Н—В–Є–Љ–Є –і–∞–љ–љ—Л–Љ–Є —Б–Њ–≥–ї–∞—Б—Г—О—В—Б—П —А–µ–Ј—Г–ї—М—В–∞—В—Л –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Я–†–Ю–Ы–Ю–У [24], —Ж–µ–ї—М—О –Ї–Њ—В–Њ—А–Њ–≥–Њ –±—Л–ї–Њ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–Њ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤ –і–ї–Є—В–µ–ї—М–љ–Њ–є –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ–∞–і –Њ–±—Л—З–љ–Њ –љ–∞–Ј–љ–∞—З–∞–µ–Љ—Л–Љ –≤ —А–µ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –ї–µ—З–µ–љ–Є–µ–Љ –Р–У. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤—Л–Љ, —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–Љ, —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–Љ, –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л–Љ –Є –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –≤ –і–≤—Г—Е –њ–∞—А–∞–ї–ї–µ–ї—М–љ—Л—Е –≥—А—Г–њ–њ–∞—Е. –У—А—Г–њ–њ–∞ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ (854 –њ–∞—Ж–Є–µ–љ—В–∞) –њ–Њ–ї—Г—З–∞–ї–∞ —Б—В—А–Њ–≥–Њ —А–µ–≥–ї–∞–Љ–µ–љ—В–Є—А–Њ–≤–∞–љ–љ—Г—О —Б—В—Г–њ–µ–љ—З–∞—В—Г—О —В–µ—А–∞–њ–Є—О –Р–У, –Њ—Б–љ–Њ–≤–∞–љ–љ—Г—О –љ–∞ —Б–њ–Є—А–∞–њ—А–Є–ї–µ, –∞ –Ї–Њ–љ—В—А–Њ–ї—М–љ–∞—П –≥—А—Г–њ–њ–∞ (888 –њ–∞—Ж–Є–µ–љ—В–Њ–≤) –њ—А–Њ–і–Њ–ї–ґ–∞–ї–∞ –њ—А–Є–µ–Љ –Њ–±—Л—З–љ–Њ–є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –љ–∞–Ј–љ–∞—З–µ–љ–љ–Њ–є –≤—А–∞—З–Њ–Љ –њ–Њ–ї–Є–Ї–ї–Є–љ–Є–Ї–Є –Є–ї–Є –і—А—Г–≥–Њ–≥–Њ –ї–µ—З–µ–±–љ–Њ–≥–Њ —Г—З—А–µ–ґ–і–µ–љ–Є—П. –Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–∞ 1 –≥–Њ–і. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —Ж–µ–ї–µ–≤—Л–µ –Ј–љ–∞—З–µ–љ–Є—П –Р–Ф —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —З–∞—Й–µ —А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Є—Б—М —Г –±–Њ–ї—М–љ—Л—Е –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л, —З–µ–Љ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є: 69,4% vs 39,3% —З–µ—А–µ–Ј 3 –Љ–µ—Б—П—Ж–∞ –Є 83,6% vs 66,9% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ —З–µ—А–µ–Ј 12 –Љ–µ—Б—П—Ж–µ–≤ –ї–µ—З–µ–љ–Є—П. –°–љ–Є–ґ–µ–љ–Є–µ –≤–µ–ї–Є—З–Є–љ—Л —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —А–Є—Б–Ї–∞ –≤ –≥—А—Г–њ–њ–µ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П, –Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–≥–Њ –љ–∞ —Б–њ–Є—А–∞–њ—А–Є–ї–µ, —Б–Њ—Б—В–∞–≤–Є–ї–Њ 33% –њ—А–Њ—В–Є–≤ 22% –≤ –≥—А—Г–њ–њ–µ –Ї–Њ–љ—В—А–Њ–ї—П, —В–Њ –µ—Б—В—М –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–∞ 50% –±–Њ–ї—М—И–µ.
–Я–Њ–і–Њ–±–љ—Л–є —Н—Д—Д–µ–Ї—В —Б–њ–Є—А–∞–њ—А–Є–ї–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М –≤–Њ –Љ–љ–Њ–≥–Њ–Љ –Њ–±—К—П—Б–љ–µ–љ –њ—А–Є—Б—Г—Й–Є–Љ–Є –Є–Р–Я–§ –Њ—А–≥–∞–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є, –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –љ–∞–Є–±–Њ–ї–µ–µ –Є–Ј—Г—З–µ–љ—Л —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –≤—Л–Ј—Л–≤–∞—В—М —А–µ–≥—А–µ—Б—Б –У–Ы–Ц –Є –љ–µ—Д—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ, –њ—А–Њ—П–≤–ї—П—О—Й–µ–µ—Б—П –Ї–∞–Ї –њ—А–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є, —В–∞–Ї –Є –њ—А–Є –љ–µ–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є.
–Ф–∞–љ–љ—Л–µ –Њ –≤–ї–Є—П–љ–Є–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞ –њ—А–Њ—Ж–µ—Б—Б —А–µ–≥—А–µ—Б—Б–∞ –У–Ы–Ц –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –Њ—Б—В–∞—О—В—Б—П –≤–µ—Б—М–Љ–∞ –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤—Л–Љ–Є. –Ю–і–љ–∞–Ї–Њ —А–µ–Ј—Г–ї—М—В–∞—В—Л –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–Њ–≤ –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ –Є–Р–Я–§ –љ–µ —В–Њ–ї—М–Ї–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ —Г–Љ–µ–љ—М—И–∞—О—В –Љ–∞—Б—Б—Г –Ы–Ц —Г –±–Њ–ї—М–љ—Л—Е –Р–У, –љ–Њ –Є –Љ–Њ–≥—Г—В –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В—М –≤ —Н—В–Њ–Љ –і—А—Г–≥–Є–µ –Ї–ї–∞—Б—Б—Л –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ [25–27].
–Ф–ї—П —Б–њ–Є—А–∞–њ—А–Є–ї–∞ –њ–Њ–і–Њ–±–љ—Л–є —Н—Д—Д–µ–Ї—В –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —А–∞–±–Њ—В–∞—Е. –Ґ–∞–Ї, –≤ –Њ–і–љ–Њ–Љ –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є [28] –Є–Ј—Г—З–∞–ї–Њ—Б—М –≤–ї–Є—П–љ–Є–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ (–≤ —В–µ—З–µ–љ–Є–µ 3 –ї–µ—В) —Б–њ–Є—А–∞–њ—А–Є–ї–∞ –љ–∞ –У–Ы–Ц (–Є—Б—Е–Њ–і–љ–Њ –Љ–∞—Б—Б–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ > 240 –≥ –њ–Њ –і–∞–љ–љ—Л–Љ –≠—Е–Њ–Ъ–У) –Є –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Г 11 –Љ—Г–ґ—З–Є–љ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 41 –≥–Њ–і–∞ –і–Њ 60 –ї–µ—В —Б –Р–У (–Ф–Р–Ф –Њ—В 100 –і–Њ 120 –Љ–Љ —А—В.—Б—В.). –Т —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г–і–∞–ї–Њ—Б—М –і–Њ–±–Є—В—М—Б—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф (—Б–Њ 161/107 –і–Њ 135/87 –Љ–Љ —А—В. —Б—В.). –Ь–∞—Б—Б–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М —Б 340 –і–Њ 298 –≥ (—А<0,05). –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –±—Л–ї –і–Њ—Б—В–Є–≥–љ—Г—В —А–µ–≥—А–µ—Б—Б –У–Ы–Ц –љ–∞ 12%, –Ї–Њ—В–Њ—А—Л–є, —З—В–Њ –≤–µ—Б—М–Љ–∞ –≤–∞–ґ–љ–Њ, —Б–Њ—Е—А–∞–љ–Є–ї—Б—П –≤–Њ –≤—А–µ–Љ–µ–љ–Є. –Ю—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л–Љ–Є –∞–≤—В–Њ—А–∞–Љ–Є —В–∞–Ї–ґ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Є–љ–і–µ–Ї—Б–∞ –Љ–∞—Б—Б—Л –Љ–Є–Њ–Ї–∞—А–і–∞ –Ы–Ц –љ–∞ 10% –њ—А–Є –ї–µ—З–µ–љ–Є–Є 62 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Р–У —Б–њ–Є—А–∞–њ—А–Є–ї–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б. [29].
–Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –Њ—Б—В–∞—О—В—Б—П –Њ—Б–љ–Њ–≤–љ—Л–Љ –Ї–ї–∞—Б—Б–Њ–Љ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б–њ–Њ—Б–Њ–±–љ—Л—Е –Ј–∞–Љ–µ–і–ї–Є—В—М –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–Њ—З–µ–Ї –Ї–∞–Ї –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Г –±–Њ–ї—М–љ–Њ–≥–Њ –°–Ф, —В–∞–Ї –Є –≤–љ–µ —В–∞–Ї–Њ–≤–Њ–≥–Њ. –≠—В–Є —Н—Д—Д–µ–Ї—В—Л —Г–±–µ–і–Є—В–µ–ї—М–љ–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ—Л –≤–Њ –Љ–љ–Њ–≥–Є—Е –†–Ъ–Ш, –њ–µ—А–≤–Њ–µ –Є–Ј –Ї–Њ—В–Њ—А—Л—Е —Б —Г—З–∞—Б—В–Є–µ–Љ –Ї–∞–њ—В–Њ–њ—А–Є–ї–∞ –±—Л–ї–Њ –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–Њ –±–Њ–ї–µ–µ 15 –ї–µ—В –љ–∞–Ј–∞–і [30].
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М —Б–њ–Є—А–∞–њ—А–Є–ї–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –љ–µ—Д—А–Њ–њ–∞—В–Є–µ–є –љ–∞ —Д–Њ–љ–µ –°–Ф 2 —В–Є–њ–∞ –Є–Ј—Г—З–∞–ї–∞—Б—М –≤ —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –ѓ—А–Њ—Б–ї–∞–≤—Б–Ї–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –∞–Ї–∞–і–µ–Љ–Є–Є –Є –У–Э–Ш–¶ –Я–Ь –Ь–Ч –†–Њ—Б—Б–Є–Є [31]. –С—Л–ї–Є —Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ—Л 3 –≥—А—Г–њ–њ—Л –±–Њ–ї—М–љ—Л—Е: —Б –Р–У (40 –њ–∞—Ж–Є–µ–љ—В–Њ–≤), –Р–У –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 2 —В–Є–њ–∞ (43 –њ–∞—Ж–Є–µ–љ—В–∞), –Р–У –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –љ–µ—Д—А–Њ–њ–∞—В–Є–µ–є (37 –њ–∞—Ж–Є–µ–љ—В–Њ–≤). –Ы–µ—З–µ–љ–Є–µ —Б–њ–Є—А–∞–њ—А–Є–ї–Њ–Љ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –≤ –і–Њ–Ј–µ 6 –Љ–≥ –≤ —В–µ—З–µ–љ–Є–µ 8 –љ–µ–і–µ–ї—М. –Т–Њ –≤—Б–µ—Е —В—А–µ—Е –≥—А—Г–њ–њ–∞—Е —Б–њ–Є—А–∞–њ—А–Є–ї –Њ–Ї–∞–Ј–∞–ї –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В, –њ—А–Є —Н—В–Њ–Љ –љ–µ –≤–ї–Є—П–ї –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Г–≥–ї–µ–≤–Њ–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞. –Т –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е —Б –љ–µ—Д—А–Њ–њ–∞—В–Є–µ–є –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ –≤ –Ї—А–Њ–≤–Є —Б 1,30±0,05 –і–Њ 1,20±0,08, –∞ —В–∞–Ї–ґ–µ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–ї–Є—А–µ–љ—Б–∞ –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ —Б 65,0±2,9 –і–Њ 73,4±5,2 –Љ–ї/–Љ–Є–љ., —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ–± —Г–ї—Г—З—И–µ–љ–Є–Є –∞–Ј–Њ—В–Њ–≤—Л–і–µ–ї–Є—В–µ–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї. –Т –і—А—Г–≥–Њ–Љ –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є 27 –±–Њ–ї—М–љ—Л–Љ –Р–У –љ–∞–Ј–љ–∞—З–∞–ї–∞—Б—М —Б—В—Г–њ–µ–љ—З–∞—В–∞—П —В–µ—А–∞–њ–Є—П —Б–њ–Є—А–∞–њ—А–Є–ї–Њ–Љ –≤ –і–Њ–Ј–µ 3 –Љ–≥/—Б—Г—В, –Ј–∞—В–µ–Љ 6 –Љ–≥/—Б—Г—В. —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –і–Њ–±–∞–≤–ї–µ–љ–Є–µ–Љ –≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і–∞ –≤ –і–Њ–Ј–µ 12,5–25 –Љ–≥/—Б—Г—В. –Ы–µ—З–µ–љ–Є–µ —Б–њ–Є—А–∞–њ—А–Є–ї–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 16 –љ–µ–і. –≤—Л–Ј—Л–≤–∞–ї–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—О –Р–Ф —Г 60% –±–Њ–ї—М–љ—Л—Е, —Б–љ–Є–ґ–∞–ї–Њ —Г—А–Њ–≤–µ–љ—М –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є–Є –Є —Н–Ї—Б–Ї—А–µ—Ж–Є–Є b2––≥–ї–Њ–±—Г–ї–Є–љ–∞, –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–ї–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –љ–∞—А—Г—И–µ–љ–љ—Г—О —Д—Г–љ–Ї—Ж–Є—О —Н–љ–і–Њ—В–µ–ї–Є—П –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є–Њ–љ–љ—Л—Е –њ—А–Њ–±, –∞ —В–∞–Ї–ґ–µ –њ–Њ–≤—Л—И–∞–ї–Њ –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –±–Њ–ї—М–љ—Л—Е. –°–њ–Є—А–∞–њ—А–Є–ї –љ–µ –Є–Ј–Љ–µ–љ—П–ї –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Є —Г–≥–ї–µ–≤–Њ–і–љ–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ –≤ 1/3 —Б–ї—Г—З–∞–µ–≤ –њ—А–Є–Љ–µ–љ—П–ї—Б—П –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –≥–Є–і—А–Њ—Е–ї–Њ—А—В–Є–∞–Ј–Є–і–Њ–Љ [32].
–Ю–і–љ–Њ–є –Є–Ј –≤–∞–ґ–љ—Л—Е –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є —Б–њ–Є—А–∞–њ—А–Є–ї–∞ —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ –і–≤–Њ–є–љ–Њ–є –њ—Г—В—М –≤—Л–≤–µ–і–µ–љ–Є—П, —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Г—О –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е –•–Я–Э. –•–Њ—В—П –Є–Р–Я–§ —Б–њ–Њ—Б–Њ–±–љ—Л –Ј–∞–Љ–µ–і–ї—П—В—М –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –•–Я–Э –Є –њ–Њ–Ї–∞–Ј–∞–љ—Л —В–∞–Ї–Є–Љ –±–Њ–ї—М–љ—Л–Љ, –њ—А–Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–Љ —Б–љ–Є–ґ–µ–љ–Є–Є —Г—А–Њ–≤–љ—П –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є —В—А–µ–±—Г–µ—В—Б—П –Ї–Њ—А—А–µ–Ї—В–Є—А–Њ–≤–Ї–∞ –і–Њ–Ј –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Б–њ–Є—А–∞–њ—А–Є–ї–∞ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –і–Њ–Ј –Ј–∞—З–∞—Б—В—Г—О –љ–µ —В—А–µ–±—Г–µ—В—Б—П. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –Є–Ј—Г—З–µ–љ–Њ –≤–ї–Є—П–љ–Є–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–Њ—З–µ–Ї –љ–∞ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї—Г —Б–њ–Є—А–∞–њ—А–Є–ї–∞ —Г 34 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї–ї–Є—А–µ–љ—Б–Њ–Љ –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ 11–126 –Љ–ї/–Љ–Є–љ. –С—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Б—В–µ–њ–µ–љ—М –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є—П –Р–Я–§ –Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –њ–Њ–і–і–µ—А–ґ–Є–≤–∞–ї–Є—Б—М –≤–Њ –≤—Б–µ—Е –і–Є–∞–њ–∞–Ј–Њ–љ–∞—Е —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї –≤ —В–µ—З–µ–љ–Є–µ –≤—Б–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Т —Г—Б–ї–Њ–≤–Є—П—Е –њ–Њ—Б—В–Њ—П–љ–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ —Б–њ–Є—А–∞–њ—А–Є–ї–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–Њ–ї–µ–µ —В—П–ґ–µ–ї—Л–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –њ–Њ—З–µ–Ї –±—Л–ї –Њ—В–Љ–µ—З–µ–љ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є—П –Р–Я–§ –≤–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є, —В–∞–Ї –Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞. –Ю–і–љ–∞–Ї–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Д—Г–љ–Ї—Ж–Є–є –њ–Њ—З–µ–Ї –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ; –љ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —В–∞–Ї–ґ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є—П —З–∞—Б—В–Њ—В—Л –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Є —А–∞–Ј–ї–Є—З–Є–є –≤ –і–Њ—Б—В–Є–≥–љ—Г—В—Л—Е —Г—А–Њ–≤–љ—П—Е –Р–Ф [33]. –≠—В–Є —А–µ–Ј—Г–ї—М—В–∞—В—Л –љ–∞—И–ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ –≤ –і—А—Г–≥–Њ–Љ (–њ—А–Њ—Б—В–Њ–Љ —Б–ї–µ–њ–Њ–Љ, –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ) –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б–њ–Є—А–∞–њ—А–Є–ї–∞, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –њ—А–Є–љ–Є–Љ–∞–ї–Є —Г—З–∞—Б—В–Є–µ 49 –±–Њ–ї—М–љ—Л—Е –Р–У –Є —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є —Б—В–∞–і–Є—П–Љ–Є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –І–µ—В—Л—А–µ—Е–љ–µ–і–µ–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П —Б–њ–Є—А–∞–њ—А–Є–ї–Њ–Љ –љ–µ –њ—А–Є–≤–µ–ї–∞ –Ї —Г—Е—Г–і—И–µ–љ–Є—О –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї –њ—А–Є —Е–Њ—А–Њ—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ [34].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–є –Є–Р–Я–§ —Б–њ–Є—А–∞–њ—А–Є–ї (–Ъ–≤–∞–і—А–Њ–њ—А–Є–ї), –Њ–±–ї–∞–і–∞—П –≤—Б–µ–Љ–Є –Њ—Б–љ–Њ–≤–љ—Л–Љ–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞–Љ–Є –Ї–ї–∞—Б—Б–∞ –Є–Р–Я–§, –Є–Љ–µ–µ—В —А—П–і –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є, —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е –і–ї–Є—В–µ–ї—М–љ—Л–є –њ–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П –Є —Б–±–∞–ї–∞–љ—Б–Є—А–Њ–≤–∞–љ–љ—Л–є –њ—Г—В—М —Н–ї–Є–Љ–Є–љ–∞—Ж–Є–Є. –≠—В–Њ –і–µ–ї–∞–µ—В –њ—А–µ–њ–∞—А–∞—В –≤–µ—Б—М–Љ–∞ —Г–і–Њ–±–љ—Л–Љ –≤ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Г —А–∞–Ј–ї–Є—З–љ—Л—Е –Ї–∞—В–µ–≥–Њ—А–Є–є –±–Њ–ї—М–љ—Л—Е –Р–У, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —Б –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –њ–Њ—З–µ–Ї –љ–∞ —Б—В–∞–і–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Collins R, Peto R, MacMahon S et al. Blood pressure, stroke, and coronary heart disease. Part 2, Short–term reductions in blood pressure: overview of randomised drug trials in their epidemiological context. Lancet 1990;335(8693):827–38.
2. Lewington S., Clarke R., Qizilbash N., Peto R., Collins R. Prospective Studies Collaboration. Age–specific relevance of usual blood pressure to vascular mortality: a meta–analysis of individual data for one million adults in 61 prospective studies. Lancet 2002;360:1903–13.
3. A.V.Chobanian, G.L.Bakris, H.R.Black, et al. Seventh report of the joint national committee on prevention, detection, evaluation, and treatment of high blood pressure. Hypertension. 2003;42: 1206–1252.
4. 2007 Guedilined for the management of arterial hypertension. The task force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). Eur Heart J 2007;28:1462–1536.
5. –Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є. –†–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –†–Њ—Б—Б–Є–є—Б–Ї–Њ–≥–Њ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ –њ–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–Є –Є –Т—Б–µ—А–Њ—Б—Б–Є–є—Б–Ї–Њ–≥–Њ –љ–∞—Г—З–љ–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Њ–≤ (—В—А–µ—В–Є–є –њ–µ—А–µ—Б–Љ–Њ—В—А) // –Ъ–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–∞—П —В–µ—А–∞–њ–Є—П –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞, 2008; 7(6), –њ—А–Є–ї–Њ–ґ–µ–љ–Є–µ 2.
6. Neaton JD, Grimm RH Jr, Prineas RJ, et al. Treatment of mild hypertension study. Final results. JAMA 1993;270:713–24.
7. –Я—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞, –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є. –†–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –†–Њ—Б—Б–Є–є—Б–Ї–Њ–≥–Њ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ –њ–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–Є –Є –Т—Б–µ—А–Њ—Б—Б–Є–є—Б–Ї–Њ–≥–Њ –љ–∞—Г—З–љ–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Њ–≤. 2008 –≥.
8. Lopez–Sendon J, Swedberg K, McMurray J, et al. Expert consensus document on angiotensin converting enzyme inhibitors in cardiovascular disease. The Task Force on ACE–inhibitors of the European Society of Cardiology. Eur Heart J. 2004 Aug;25(16):1454–70.
9. The Task Force on the Management of Stable Angina Pectoris of the European Society of Cardiology. Eur Heart J 2006;27:1341–1381.
10. ESC Committee for Practice Guidelines. Guidelines on diabetes, pre–diabetes, and cardiovascular disease: executive summary: The Task Force on Diabetes and Cardiovascular Diseases of the European Society of Cardiology (ESC) and European Association for the Study of Diabetes (EASD). Eur Heart J 2007;28:88–136.
11. Paul M, Poyan Mehr A, Kreutz R. Physiology of local renin–angiotensin systems. Physiol Rev. 2006;86:747–803.
12. Pals D.T., Massucci F.D., Sipos F., Dennig Jr G.S.A specific compepitive antagonist of the vascular action of angiotensin II. Cirs Res. 1971; 29: 664–12.
13. The 1988 report of the Joint National Committee on Detection, Evaluation, and Treatment of High Blood Pressure. Arch Intern Med. 1988 May;148(5):1023–38.
14. Heran BS, Wong MM, Heran IK, Wright JM. Blood pressure lowering efficacy of angiotensin converting enzyme (ACE) inhibitors for primary hypertension. Cochrane Database Syst Rev. 2008 Oct 8;(4):CD003823.
15. –Ы–µ–Њ–љ–Њ–≤–∞ –Ь.–Т., –С–µ–ї–Њ—Г—Б–Њ–≤ –Ф.–Ѓ. –Р–љ–∞–ї–Є—В–Є—З–µ—Б–Ї–∞—П –≥—А—Г–њ–њ–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Я–Ш–§–Р–У–Ю–†. –Я–µ—А–≤–Њ–µ —А–Њ—Б—Б–Є–є—Б–Ї–Њ–µ —Д–∞—А–Љ–∞–Ї–Њ—Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–Є. –Ъ–∞—З–µ—Б—В–≤–µ–љ–љ–∞—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –њ—А–∞–Ї—В–Є–Ї–∞ вДЦ3 2002. —Б. 47–53.
16. Hot R.P., Hof–Miashita A., Evenou J.P. Hemodynamic effects of a new angiotensin converting enzyme inhibitor, spirapril, in sodium loaded and sodium depleted rabbits. J Cardiovasc Pharmacol 1987; 10: 599–606.
17. Noble S, Sorkin EM. Spirapril. A preliminary review of its pharmacology and therapeutic efficacy in the treatment of hypertension. Drugs. 1995 May;49(5):750–66.
18. Guitard C, Lohmann FW, Alfiero R, Ruina M, Alvisi V. Comparison of efficacy of spirapril and enalapril in control of mild–to–moderate hypertension. Cardiovasc Drugs Ther. 1997 Jul;11(3):449–57.
19. –Ш.–®–Љ–Є–і—В, –•.–Ъ—А–∞—Г–ї—М. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б–њ–Є—А–∞–њ—А–Є–ї–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–µ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –Њ–њ—Л—В –≤ –У–µ—А–Љ–∞–љ–Є–Є. –Ґ–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є –∞—А—Е–Є–≤ 2000; 10:14–18.
20. –Ѓ.–Р.–Ъ–∞—А–њ–Њ–≤, –Р.–Ф.–Ф–µ–µ–≤ –њ–Њ –њ–Њ—А—Г—З–µ–љ–Є—О —А–∞–±–Њ—З–µ–є –≥—А—Г–њ–њ—Л –†–Њ—Б—Б–Є–є—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Ъ–≤–∞–і—А–Њ–њ—А–Є–ї–∞® (—Б–њ–Є—А–∞–њ—А–Є–ї–∞) —Г –±–Њ–ї—М–љ—Л—Е —Б –Љ—П–≥–Ї–Њ–є –Є —Г–Љ–µ—А–µ–љ–љ–Њ–є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–µ–є (–Ъ–Т–Р–Ф–†–Ш–У–Р – –Ъ–Т–Р–Ф–†–Њ–њ—А–Є–ї –Ш –У–Є–њ–µ—А—В–Њ–љ–Є—П –Р—А—В–µ—А–Є–∞–ї—М–љ–∞—П). –°–µ—А–і—Ж–µ 2003;2(3):144–146.
21. Blood Pressure Lowering Treatment Trialists’ Collaboration. Effects of ACE inhibitors, calcium antagonists, and other blood–pressure–lowering drugs: results of prospectively designed overviews of randomized trials. Lancet. – 2000; 355: 1955–1964.
22. Psaty B.; Lumley T.; Furberg C.; et al. Health Outcomes Associated With Various Antihypertensive Therapies Used as First–Line Agents: A Network Meta–analysis. JAMA. 2003;289(19):2534–2544
23. Law M R, Morris J.K., Wald N.J. Use of blood pressure lowering drugs in the prevention of cardiovascular disease: meta–analysis of 147 randomised trials in the context of expectations from prospective epidemiological studies. BMJ 2009;338:b1665 doi:10.1136/bmj.b1665.
24. –®–∞–ї—М–љ–Њ–≤–∞ –°.–Р., –Ь–∞—А—Ж–µ–≤–Є—З –°.–Ѓ., –Ф–µ–µ–≤ –Р.–Ф., –Ъ—Г—В–Є—И–µ–љ–Ї–Њ –Э.–Я., –Ю–≥–∞–љ–Њ–≤ –†.–У. –Њ—В –Є–Љ–µ–љ–Є —Г—З–∞—Б—В–љ–Є–Ї–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–≥—А–∞–Љ–Љ—Л –Я–†–Ю–Ы–Ю–У . –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Я–†–Ю–Ы–Ю–У: —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–µ–є –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Ъ–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–∞—П —В–µ—А–∞–њ–Є—П –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞, 2005; 4(4).
25. Dahlof B., Pennert K., Hansson L. Reversal of left ventricular hypertrophy in hypertensive patients. A metaanalysis of 109 treatment studies. Am J Hypertens. 1992 Feb;5(2):95–110.
26. Schmieder R.E., Martus P., Klingbeil A. Reversal of left ventricular hypertrophy in essential hypertension. A meta–analysis of randomized double–blind studies. JAMA. 1996 May 15;275(19):1507–13.
27. Schmieder R.E., Schlaich M.P., Klingbeil A.U., Martus P. Update on reversal of left ventricular hypertrophy in essential hypertension (a meta–analysis of all randomized double–blind studies until December 1996). Nephrol Dial Transplant. 1998 Mar;13(3):564–9.
28. Otterstad J.E, Froeland G. Changes in left ventricular dimensions and haemodynamics during antihypertensive treatment with spirapril for 36 months. Blood Pressure. – 1994; 3 (Suppl. 2): 69–72.
29. –С–µ—А–∞—П –Ь.–Ь., –Я–µ—В—А–Є–є –Т.–Т., –С—Г–≤–∞–ї—М—Ж–µ–≤ –Т.–Ш., –Ь–∞–Ї–Њ–ї–Ї–Є–љ –Т.–Ш. –Т–ї–Є—П–љ–Є–µ —Б–њ–Є—А–∞–њ—А–Є–ї–∞ –љ–∞ —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є–µ —Б–µ—А–і—Ж–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ—П–≥–Ї–Њ–є –Є —Г–Љ–µ—А–µ–љ–љ–Њ–є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–µ–є // –†–Њ—Б—Б–Є–є—Б–Ї–Є–є –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї 2007; 63(1).
30. Lewis E.J., Hunsicker L.G., Bain R.P., Rohde R.D., for the Collaborative Study Group. The effect of angiotensin–converting–enzyme inhibition on diabetic nephropathy. N Engl J Med. 1993;329:1456–1462.
31. –ѓ–Ї—Г—Б–µ–≤–Є—З –Т.–Т., –Ь–Њ–ґ–µ–є–Ї–Њ –Ь.–Х., –Я–∞–ї—О—В–Є–љ –®.–•. –Є –і—А. –°–њ–Є—А–∞–њ—А–Є–ї – –љ–Њ–≤—Л–є –Є–љ–≥–Є–±–Є—В–Њ—А –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П: —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М —Г –±–Њ–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–µ–є –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –Є –љ–∞—А—Г—И–µ–љ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–µ–є –њ–Њ—З–µ–Ї. –Ґ–µ—А –∞—А—Е–Є–≤ 2000; 10: 6–9.
32. –Ь.–Т. –Ы–µ–Њ–љ–Њ–≤–∞, –Ь.–Р. –Ф–µ–Љ–Є–і–Њ–≤–∞, –Р.–Т. –Ґ–∞—А–∞—Б–Њ–≤, –Ѓ.–С. –С–µ–ї–Њ—Г—Б–Њ–≤.–У–Ш–Я–Ю–Ґ–Х–Э–Ч–Ш–Т–Э–Р–ѓ, –Ю–†–У–Р–Э–Ю–Я–†–Ю–Ґ–Х–Ъ–Ґ–Ш–Т–Э–Р–ѓ –Ш –Ь–Х–Ґ–Р–С–Ю–Ы–Ш–І–Х–°–Ъ–Р–ѓ –≠–§–§–Х–Ъ–Ґ–Ш–Т–Э–Ю–°–Ґ–ђ –°–Я–Ш–†–Р–Я–†–Ш–Ы–Р –£ –С–Ю–Ы–ђ–Э–Ђ–• –Р–†–Ґ–Х–†–Ш–Р–Ы–ђ–Э–Ю–Щ –У–Ш–Я–Х–†–Ґ–Х–Э–Ч–Ш–Х–Щ. –†–∞—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П –§–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П –≤ –Ъ–∞—А–і–Є–Њ–ї–Њ–≥–Є–Є 2005; вДЦ2.
33. Meredith P.A., Grass P., Guitard C. et al. Pharmacokinetics of spirapril in renal impairment. Blood Pressure 1994 (suppl. 2): 14–19.
34. Stem G., Sierakowski –Т., Jansa U. et al. Spirapril in chronic renal failure. Blood Pressure 1994 (suppl. 2): 54–60.












