АГ является гемодинамическим нарушением по определению, и рост периферического сосудистого сопротивления – отличительная гемодинамическая особенность повышенного уровня АД. Понимание этого факта привело к открытию и разработке специального класса вазодилататоров с целенаправленным механизмом действия, хотя многие из ранее используемых антигипертензивных средств также обладали вазодилатирующим действием, например, за счет блокады активности симпатической нервной системы. Первым неспецифическим вазодилататором был гидралазин, за ним последовали вазодилататоры, блокирующие кальциевые каналы гладкомышечных клеток сосудов (антагонисты кальция – АК), постсинаптические α–адренорецепторы периферических нейронов симпатической нервной системы (α–блокаторы) и блокаторы ренин–ангиотензин–альдостероновой системы (РААС) (ингибиторы ангиотензинпревращающего фермента (иАПФ), блокаторы рецепторов к ангиотензину (БРА); наконец, последними появились прямые ингибиторы ренина (ПИР).
Вазодилатирующий эффект присущ и тиазидным диуретикам (ТД), которые, уменьшая содержание натрия в гладкомышечных клетках сосудов, уменьшают их чувствительность к вазопрессорам – катехоламинам и др. При использовании антигипертензивных средств в разнородной популяции больных АГ селективность действующих веществ и другие их особенности приводят к непредсказуемому снижению АД у каждого конкретного больного. Например, назначение иАПФ больному с гиперактивацией РААС вследствие стеноза почечной артерии приведет к значительному снижению АД и нарушению функции почек [2]. В свою очередь, назначение иАПФ пожилым людям и лицам негроидной расы (у которых в большинстве случаев отмечается пониженный уровень активности РААС) приведет лишь к небольшому снижению АД [3]. Чаще всего «фенотип» АГ у конкретного больного остается неуточненным.
В недавно проведенном метаанализе 354 плацебо–контролируемых исследований различных режимов антигипертензивной монотерапии у специально не отбиравшихся больных АГ (n=56 000) показано среднее снижение (скорректированное с учетом плацебо) систолического АД на 9,1 мм рт.ст. и диастолического АД – на 5,5 мм рт.ст. [4]. За этими средними значениями скрывается большой разброс индивидуальных реакций на антигипертензивную терапию – от снижения САД на 20–30 мм рт.ст. и до полного отсутствия эффекта, а иногда – даже некоторого повышения АД [5].
Второй фактор, определяющий индивидуальную реакцию на антигипертензивную монотерапию, – индивидуальные различия систем контррегуляции АД, активируемых в ответ на снижение его уровня. В некоторых случаях подобная реакция может полностью компенсировать снижение АД. Таким образом, использование антигипертензивной монотерапии далеко не всегда дает удовлетворительный результат. Каким должен быть следующий шаг в подобной ситуации? Следует ли увеличить дозу, заменить препарат или использовать комбинацию антигипертензивных средств?
Обоснование применения
комбинированной антигипертензивной терапии
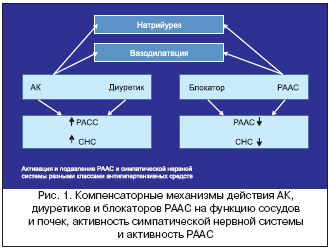
Основание для использования комбинированной терапии при АГ достаточно очевидно. Во–первых, в отличие от назначаемой вслепую монотерапии сочетание препаратов, действующих на разные системы регуляции АД, значительно повышает вероятность его эффективного снижения. Во–вторых, назначение комбинации препаратов можно расценивать как попытку заблокировать активацию контррегуляторных систем, противодействующих снижению АД на фоне применения монотерапии (рис. 1).
В–третьих, значительная часть популяции больных АГ страдает так называемой умеренной или выраженной АГ (2–й стадии) [6], к этой группе можно отнести больных с систолическим АД более 160 мм рт.ст. и/или диастолическим АД более 100 мм рт.ст., что составляет около 15–20% от всех больных АГ. Именно данные больные находятся в группе наиболее высокого риска сердечно–сосудистых событий. Повышение АД на каждые 20 мм рт.ст. удваивает риск подобных событий.
Риск АГ увеличивается с возрастом, причем также возрастает и доля больных с АГ 2–й стадии. С возрастом связано и повышение доли больных с изолированной систолической АГ, которая является причиной потери эластичности сосудов и росте сосудистого сопротивления.
Несмотря на некоторые различия в рекомендациях, в части из них комбинированное лечение относится к терапии первого ряда, правда, лишь при определенных условиях. Подобное место комбинированной терапии является закономерным ввиду рисков тяжелой АГ, признания неизбежности использования двойной (а иногда и тройной) терапии для достижения целевых значений АД менее 140/90 мм рт.ст. и необходимости быстро снизить АД до более приемлемого уровня для снижения имеющихся рисков.
При систолическом АД, превышающем целевые значения на 20 мм рт.ст., и/или диастолическом АД, превышающем целевые значения на 10 мм рт.ст., Объединенный национальный комитет по профилактике, диагностике и лечению высокого АД США (JNC–7) рекомендует начинать антигипертензивную терапию с комбинации из двух препаратов. Подобные рекомендации содержатся и в последних российских рекомендациях, причем рекомендация по применению комбинированной антигипертензивной терапии первого ряда распространяется и на больных с более низкими уровнями АД, имеющих множественные факторы риска, повреждение органов–мишеней, сахарный диабет, заболевания почек или ассоциированные сердечно–сосудистые заболевания [7].
Существуют опасения, что применение более чем одного антигипертензивного препарата в начале лечения может в ряде случаев спровоцировать клинически значимую гипотонию и повысить риск коронарных событий. Анализ исследований по лечению АГ предоставил некоторые доказательства существования J–образной связи между снижением АД и сердечно–сосудистым риском, однако, по всей видимости, это относится к больным из группы высокого риска, в том числе при наличии известной ИБС, когда выраженное снижение АД может привести к ухудшению перфузии миокарда [8]. Больные с неосложненной АГ низкие значения АД переносят удовлетворительно, как, например, в исследовании Systolic hypertension in Elderly («Систолическая гипертензия у пожилых»), где в группе активного лечения удалось снизить систолическое АД до 60 мм рт.ст. [9]. Продолжающиеся исследования, спланированные для сравнения начала антигипертензивной терапии с двойной и последовательной монотерапией, позволят оценить безопасность нового подхода.
В–четвертых, по сравнению с монотерапией комбинированная терапия позволяет добиться снижения вариабельности АД [10]. Дополнительный анализ нескольких рандомизированных исследований показал, что вариабельность систолического АД от визита к визиту является сильным и независимым от среднего АД предиктором инфаркта миокарда и инсульта [18]. Обращает на себя внимание, что наибольшую эффективность в уменьшении подобной вариабельности АД и риска инсульта проявили АК и диуретики. β–блокаторы, наоборот, дозозависимым образом увеличивали вариабельность систолического АД и показали наименьшую эффективность в профилактике инсульта. Добавление АК или, в меньшей степени, диуретика к ингибитору РААС снижает вариабельность систолического АД, что является дополнительным аргументом в поддержку комбинированной терапии.
Комбинации препаратов
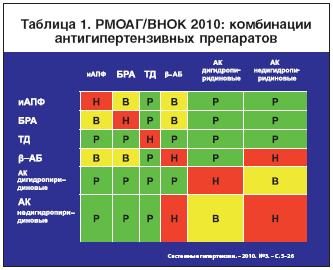
Существует 7 классов антигипертензивных препаратов, каждый из которых включает по несколько представителей, поэтому существует большое количество комбинаций (табл. 1). Ниже будут представлены комбинации в соответствии с их делением на рациональные (предпочтительные), возможные (приемлемые) и неприемлемые или неэффективные. Отнесение комбинации к той или иной группе зависит от данных по исходам, антигипертензивной эффективности, безопасности и переносимости.
Рациональные (предпочтительные) комбинации
Ингибиторы РААС и диуретики. В настоящее время данная комбинация наиболее часто используется в клинической практике. Значительное число исследований с факториальным дизайном показало дополнительное снижение АД при использовании комбинации ТД и иАПФ, БРА или ПИР. Диуретики уменьшают объем внутрисосудистой жидкости, активируют РААС, что тормозит выведение соли и воды, а также противодействует вазодилатации. Добавление к диуретику ингибитора РААС ослабляет действие этого контррегуляторного механизма. Кроме того, применение диуретика способно вызвать гипокалиемию и нарушение толерантности к глюкозе, а блокаторы РААС способны ослабить это нежелательное действие. Показано, что хлорталидон эффективнее снижает АД, чем гидрохлоротиазид, т.к. имеет бо́льшую продолжительность действия, поэтому именно хлорталидону следует отдавать предпочтение в качестве второго компонента в комбинации с ингибитором РААС. Большинство ингибиторов РААС доступны в фиксированной комбинации с гидрохлоротиазидом.
Недавно закончено исследование гипертензии у больных старческого возраста (старше 80 лет) (HYVET, Hypertension in the Very Elderly), в котором оценивалась эффективность тиазидоподобного диуретика индапамида. К этому диуретику для усиления антигипертензивного действия присоединялся иАПФ периндоприл у 75% больных. Показано 30% снижение частоты инсультов и 64% снижение сердечной недостаточности при использовании этой комбинации в сравнении с плацебо.
С применением комбинации иАПФ и диуретика был осуществлен проект ЭПИГРАФ под эгидой Всероссийского научного общества кардиологов. Этот проект состоял из двух многоцентровых исследований – ЭПИГРАФ–1 и ЭПИГРАФ–2. Данный проект ценен тем, что он способствовал созданию нефиксированной комбинации Энзикс («Штада»), содержащей два препарата в одном блистере – эналаприл (иАПФ) и индапамид (диуретик), что позволяет при необходимости менять их дозировки и соотнести время приема с циркадным ритмом АД, иметь 2 препарата в одной упаковке, а не пользоваться двумя отдельными. Препарат выпускается в трех формах: Энзикс – 10 мг эналаприла и 2,5 мг индапамида; Энзикс Дуо – 10 мг эналаприла и 2,5 мг индапамида + 10 мг эналаприла; Энзикс Дуо форте – 20 мг эналаприла и 2,5 мг индапамида + 20 мг эналаприла. Различные дозировки позволяют корригировать терапию в зависимости от степени тяжести и риска АГ, переносимости лекарственных препаратов.
В исследовании, проведенном на Украине, изучалось влияние длительной терапии нефиксированной комбинацией эналаприла и индапамида в 1 блистере (Энзикс, Энзикс Дуо) на суточный профиль АД и параметры ремоделирования ЛЖ, его систолическую и диастолическую функцию, а также качество жизни пациентов со стабильной АГ. Результаты исследования показали, что у больных АГ длительный прием комбинации эналаприла и индапамида (Энзикс, Энзикс Дуо) значительно улучшает показатели величины и скорости утреннего подъема АД и позитивно влияет на вариабельность АД. Также полученные данные свидетельствовали о том, что длительный прием нефиксированной комбинации эналаприла и индапамида в 1 блистере (Энзикс, Энзикс Дуо) оказывает отчетливый антигипертензивный эффект, приводит к обратному развитию ремоделирования ЛЖ и улучшению его диастолической функции, повышению качества жизни наряду с хорошим профилем безопасности и переносимости.
Ингибиторы РААС и антагонисты кальция. Комбинирование АК с ингибитором АПФ, АРБ или ПИР позволяет добиться дополнительного снижения АД. Периферические отеки – обычное дозозависимое нежелательное явление, наблюдаемое при монотерапии дигидропиридиновыми АК. Ослабить выраженность данного нежелательного явления можно за счет добавления к АК ингибитора РААС. Согласно результатам недавно проведенного метаанализа, иАПФ более эффективны в этом отношении, чем БРА [15]. Согласно результатам исследования ACCOMPLISH (The Avoiding Cardiovascular Events through Combination Therapy in Patients Living with Systolic Hypertension Trial, Исследование по изучению применения комбинированной терапии для предотвращения сердечно–сосудистых событий у пациентов с систолической АГ), фиксированная комбинация иАПФ беназеприла с АК амлодипином эффективнее в отношении снижения заболеваемости и смертности, чем фиксированная комбинация иАПФ с гидрохлоротиазидом [12]. В целом иАПФ и БРА показали одинаковое снижение частоты достижения конечных точек, хотя существует предположение, что иАПФ обладают несколько более выраженным кардиопротективным действием, а БРА лучше защищают от инсультов.
В международном исследовании INVEST сравнивали два режима антигипертензивной терапии: верапамил, к которому при необходимости добавлялся трандолаприл, и атенолол, к которому при необходимости добавляли гидрохлоротиазид [16]. В исследование было включено 22 576 больных АГ с установленным диагнозом ИБС, наблюдение осуществлялось на протяжении 2,7 лет. Главная комбинированная конечная точка, представленная сердечно–сосудистыми событиями, была достигнута в обеих группах с одинаковой частотой. По всей видимости, это можно объяснить тем, что недостатки схемы лечения, включавшей β–блокатор при АГ, компенсировались преимуществами β–блокаторов при ИБС.
b–блокаторы и диуретики. Эту комбинацию не все эксперты относят к числу рациональных. Вместе с тем показано, что присоединение диуретиков к β–блокаторам вызывает усиление антигипертензивного эффекта в популяциях с низкорениновой АГ. Хотя оба класса препаратов имеют схожие побочные эффекты в виде нарушения толерантности к глюкозе, развития сахарного диабета и нарушения половой функции, однако реальное клиническое значение «метаболических» побочных явлений сильно преувеличено, и исследования по изучению конечных точек показали, что применение подобной комбинации приводит к снижению сердечно–сосудистой заболеваемости и смертности [11].
Возможные (приемлемые) комбинации
Блокаторы кальциевых каналов и диуретики. Большинство врачей не всегда комбинируют АК с диуретиками. Однако в исследовании VALUE (Valsartan Antihypertensive Long–term Use Evaluation Trial) к амлодипину, при его недостаточной эффективности, добавляли гидрохлоротиазид, и подобная комбинация хорошо переносилась больными, хотя в сравнении с группой валсартана риск обнаружения сахарного диабета и гиперкалиемии повышался [13]. Тем не менее в группе амлодипина сокращение заболеваемости и смертности оказалось не меньше, чем в группе валсартана.
Блокаторы кальциевых каналов и β–блокаторы. Комбинация β–блокатора с дигидропиридиновым АК оказывает дополнительный эффект на снижение АД и в целом переносится довольно хорошо. И наоборот, β–блокаторы не следует комбинировать с недигидропиридиновыми АК, такими как верапамил и дилтиазем. Сочетание отрицательного хронотропного эффекта обоих классов препаратов может привести к развитию брадикардии или блокады сердца, вплоть до полной поперечной, и к смерти больного.
Двойная блокада кальциевых каналов. В недавно проведенном метаанализе показано, что комбинация дигидропиридинового АК с верапамилом или дилтиаземом ведет к дополнительному снижению АД без существенного увеличения частоты нежелательных явлений [17]. Подобная комбинированная терапия может быть использована у больных с документированными ангионевротическими отеками на фоне приема ингибиторов РААС, а также у больных с выраженной почечной недостаточностью, сопровождающейся риском гиперкалиемии. Однако данных об отдаленной безопасности и исходах на фоне подобной терапии на настоящий момент нет.
Двойная блокада РААС. Применение этой комбинации основано на усилении АД–снижающего действия, что было доказано в целом ряде исследований. Однако значимость этой комбинации уменьшилась в связи с неподтвержденной безопасностью по данным длительных исследований. В исследовании ONTARGET у больных, получавших комбинированную терапию телмисартаном и рамиприлом, отмечено больше нежелательных явлений, а число сердечно–сосудистых событий, несмотря на некоторое дополнительное снижение АД, не уменьшилось по сравнению с монотерапией. Таким образом, в подобной комбинации у больных с высоким риском развития неблагоприятных событий нет особого смысла. Однако в связи с тем, что блокада РААС посредством иАПФ или БРА повышает активность ренина плазмы, было высказано предположение об эффективности добавления прямого ингибитора ренина. В двойном слепом исследовании комбинации алискирена и БРА, проведенном у 1797 больных, выявлено небольшое, но статистически значимое снижение АД. Примечательно, что в открытом проспективном перекрестном исследовании больных с резистентной АГ антагонист альдостерона спиронолактон эффективнее снижал АД, чем двойная блокада РААС [18]. Применение комбинации ПИР с ингибитором АПФ или БРА в исследовании ALTITUDE (Aliskiren Trialin Type 2 Diabetes Using Cardiovascular and Renal Disease End points, Исследование алискирена у больных сахарным диабетом 2 типа с использованием сердечно–сосудистых и почечных конечных точек) по результатам промежуточного анализа в 2012 г. оказалось нецелесообразным из–за увеличения риска развития нежелательных событий, и исследование было досрочно прекращено. По–видимому, целесообразно комбинации иАПФ с БРА перевести в группу нерекомендуемых комбинаций.
Неприемлемые и неэффективные комбинации
Блокаторы РААС и β–блокаторы. Комбинацию данных классов препаратов часто используют у больных, перенесших инфаркт миокарда, а также у больных с сердечной недостаточностью, т.к. было показано, что они снижают частоту повторных инфарктов и улучшают выживаемость. Однако данная комбинация не дает какого–либо дополнительного снижения АД в сравнении с монотерапией этими препаратами. Таким образом, использовать комбинацию ингибитора РААС и β–блокатора для лечения АГ как таковой нецелесообразно.
β–блокаторы и препараты с центральным антиадренергическим действием. Комбинирование β–блокаторов с антиадренергическими препаратами центрального действия, такими как клонидин, дает минимальное дополнительное снижение АД или вообще не дает никакой пользы. Более того, при использовании подобной комбинации даже наблюдались реакции с чрезмерным повышением АД [19].
Другие классы препаратов в комбинированной терапии: α–блокаторы и спиронолактон
Антагонисты α–адренорецепторов широко используются в качестве дополнительной терапии для достижения целевых значений АД. Появление лекарственных форм с продленным высвобождением лекарственного вещества улучшило профиль переносимости этих препаратов. Данные обсервационного анализа исследования ASCOT (the Anglo–Scandinavian Cardiac Outcomes Trial, Англо–скандинавское исследование сердечных исходов) показали, что доксазозин в лекарственной форме желудочно–кишечной терапевтической системы, используемый как третий ряд терапии, снижает АД и вызывает умеренное снижение липидов сыворотки [20]. В отличие от полученных ранее в исследовании ALLHAT (Antihypertensive and Lipid–Lowering Treatment to Prevent Heart Attack Trial, Исследование по антигипертензивной и липидснижающей терапии для предотвращения сердечной атаки) данных, применение доксазозина в исследовании ASCOT не показало связи с увеличением частоты сердечной недостаточности.
Терапия, состоящая из 4 антигипертензивных препаратов, часто требуется больным с резистентной к лечению препаратами в максимальных дозах или тройной антигипертензивной терапии, включающей блокатор РААС, АК и тиазидный диуретик, АГ (невозможность достичь целевых значений <140/90 мм рт.ст.). Недавние сообщения свидетельствуют об эффективности добавления спиронолактона к тройной терапии, заключающейся в снижении АД в среднем на 22/9,5 мм рт.ст. Таким образом, спиронолактон может быть рекомендован в качестве компонента антигипертензивной терапии у больных с резистентной АГ.
Нежелательные явления. Существуют данные, свидетельствующие о том, что выраженность отеков, связанных с применением дигидропиридиновых АК, может быть уменьшена при добавлении к лечению блокаторов РААС, которые также могут снизить частоту гипокалиемии, вызываемой приемом ТД. С другой стороны, применение β–блокаторов ассоциировано с увеличением частоты выявления сахарного диабета (СД), а при использовании комбинации ТД с β–блокаторами вероятно более существенное увеличение частоты впервые выявленного СД, однако парадоксальным образом это не увеличивает частоту связанных с таким сахарным диабетом сердечно–сосудистых конечных точек, как было показано в исследовании ALLHAT. В рекомендациях NICE приводятся данные метаанализа, выявившего увеличение частоты вновь диагностированного СД при использовании β–блокаторов и ТД в сравнении с более «новыми» препаратами [11].
Полученные выводы исходят из предположения об отсутствии различий в долгосрочной заболеваемости и смертности между препаратами в рамках одного класса. Среди АК наибольшая доказательная база имеется у амлодипина. В исследованиях, посвященных изучению иАПФ и БРА в составе комбинированной терапии у больных АГ и другими сердчно–сосудистыми заболеваниями, изучались различные представители данных классов, и каких–либо различий между ними выявлено не было. Существует мнение, что среди тиазидных и тиазидоподобных диуретиков наибольшую доказательную базу в отношении долгосрочных преимуществ имеет хлорталидон в средних дозах (в сравнении с другими ТД в меньших дозах). К сожалению, проведение дальнейших исследований, направленных на сравнение препаратов данного класса, кажется маловероятным.
Самым часто используемым в исследованиях препаратом среди β–блокаторов был атенолол, и было неоднократно сказано, что если бы в испытаниях использовались другие представители данного класса, то и результаты были бы другими. Это представляется маловероятным, т.к. нежелательные явления, выявленные в исследовании ASCOT и заключавшиеся во влиянии на вариабельность АД и повышении центрального интрааортального давления по сравнению с амлодипином (и то и другое ассоциируется с повышением сердечно–сосудистого риска), вероятнее всего, возникают при использовании большинства β–блокаторов [14]. Исследования, посвященные изучению воздействия терапии β–блокаторами с дополнительными фармакологическими свойствами (например, β–1, β–2 и α–блокатора карведилола) на отдаленные исходы у больных с АГ, проведены не были.
Фиксированные комбинации
и их преимущества по влиянию на прогноз
В недавнем обзоре потенциальных преимуществ комбинаций с фиксированными дозами (КФД) над соответствующими лекарственными средствами, принимаемыми по отдельности, показано, что применение КФД ассоциируется со значительным улучшением приверженности и незначительным увеличением длительности приема препаратов. Степень приверженности к лечению с использованием КФД, по данным метаанализа 9 исследований, выше на 26% в сравнении с приемом тех же лекарственных средств по отдельности [23].
По данным исследований, содержащих информацию о значениях АД, применение КФД ассоциировано с незначительным дополнительным снижением систолического и диастолического АД (4,1 и 3,1 мм рт.ст. соответственно) [22]. В случае сохранения на протяжении длительного времени подобные различия в АД могут вылиться в реальные преимущества по сердечно–сосудистым исходам.
Заключение
Большая часть пациентов с АГ нуждаются в терапии двумя и более препаратами из разных классов антигипертензивных средств для достижения целевых значений АД. Комбинированная антигипертензивная терапия должна назначаться пациентам с АД выше целевых значений более чем на 20/10 мм рт.ст. Следует использовать рациональные (предпочтительные) и возможные (приемлемые) комбинации препаратов. Фиксированные комбинации повышают приверженность терапии, что увеличивает частоту достижения целевых цифр АД.
Литература
1. Page I.H. The MOSAIC theory // Hypertension Mechanisms. – New York: Grune and Stratton, 1987. P. 910–923.
2. Mimran A., Ribstein J., Du Cailar G. Converting enzyme inhibitors and renal function in essential and renovascular hypertension // Am. J. Hypertens. 1991. Vol. 4 (Suppl. 1). 7S–14S.
3. Dickerson J.E., Hingorani A.D., Ashby M.J. et al. Optimisation of antihypertensive treatment by cross–over rotation of four major classes // Lancet. 1999. Vol. 353. P. 2008–2013.
4. Law M.R., Wald N.J., Morris J.K., Jordan R.E. Value of low dose combination treatment with blood pressure lowering drugs: analysis of 354 randomised trials // BMJ. 2003. Vol. 326. P. 1427–1435.
5. Attwood S., Bird R., Burch K. et al. Within–patient correlation between the antihypertensive effects of atenolol, lisinoprill and nifedepin // Hypertens. 1994. Vol. 12. P. 1053–1060.
6. Chobanian A.V., Bakris G.L., Black H.R. et al. Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. National Heart, Lung, and Blood Institute; National High Blood Pressure Education Program Coordinating Committee. Seventh Report of the joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure // Hypertens. 2003. Vol. 42. P. 1206–1252.
7. Российское медицинское общество по артериальной гипертонии (РМОАГ), Всероссийское научное общество кардиологов (ВНОК). Диагностика и лечение артериальной гипертензии. Российские рекомендации (четвертый пересмотр) // Системные гипертензии. – 2010. – № 3. – C. 5–26.
8. Messerli F.H., Mancia G., Conti C.R. et al. Dogma disputed: can aggressively lowering blood pressure in hypertensive patients with artery disease be dangerous? // Ann. Intern. Med. 2006. Vol. 144. P. 884–894.
9. SHEP Cooperative Research Group. Prevention of stroke by antihypertensive drug treatment in older persons with isolated systolic hypertension. Final results of the Systolic Hypertension in the Elderly Programme (SHEP) // JAMA. 1991. Vol. 265. P. 3255–3264.
10. Rothwell P.M., Howard S.C., Dolan E. et al. Prognostic significance of visit–to–visit variability, maximum systolic blood pressure, and episodic hypertension // Lancet. 2010. Vol. 375. P. 895–905.
11. Nice guidelines. Management of hypertension in adults in primary care. 2007. www.nice.org.uk.
12. Jamerson K., Weber M.A., Bakris G.L. et al. ACCOMPLISH Trial Investigators. Benazepril plus amlodipine or hydrochlorothiazide for hypertension in high–risk patients /// NEJM. 2008.Vol. 359. P. 2417–2428.
13. Julius S., Kjeldsen S.E., Brrunner H. et al. VALUE Trial. VALUE trial: Long–term blood pressure trends in 13,449 patients with hypertension and high cardiovascular risk // Am. J. Hypertens. 2003. Vol. 7. P. 544–548.
14. Williams B., Lacy P.S., Thom S.M. et al. CAFE Investigators; Anglo–Scandinavian Cardiac Outcomes Trial Investigators; CAFE Steering Committee and Writing Committee. Differential impact of blood pressure–lowering drugs on central aortic pressure and clinical outcomes: principal results of the Conduit Artery Function Evaluation (CAFE) study // Circulation. 2006. Vol. 113. P. 1213–1225.
15. Makani H., Bangalore S., Romero J. et al. Effect of rennin–angiotensin–system blockade on calcium channel blockers associated peripheral edema // Am. J. Med. 2011. Vol. 124. P. 128–135.
16. Pepine C.J., Handberg E.M., Cooper–DeHoff R.M. et al. INVEST Investigators. A calcium antagonist vs. a non–calcium antagonist hypertension treatment strategy for patients with coronary artery disease. The International Verapamil–Trandolapril Study (INVEST): a randomized controlled trial // JAMA. 2003. Vol. 290. P. 2805–2819.
17. Alviar C.L., Devarapally S., Romero J. et al. Efficacy and Safety of Dual Calcium Channel Blocker Trerapy for the Treatment of Hypertension: A Meta–analysis // ASH. 2010.
18. Alvares–Alvares B. Management of resistant arterial hypertension: role of spironolactone versus double blockade of the rennin–angiotensin–aldosterone syste // J. Hypertens. 2010. jul 21. [Epub ahead of print].
19. Bailey R.R., Neale T.J. Rapid clonidine withdrawal with blood pressure overshoot exaggerated by beta–blockade // BMJ. 1976. Vol. 6015. P. 942–943.
20. Chapman N., Chang C.L., Dahlof B. et al. For the ASCOT Investigators. Effect of doxazosin gastrointestinal therapeutic system as third–line antihypertensive therapy on blood pressure and lipids in the Anglo–Scandinavian Cardiac Outcomes Trial // Circulation. 2008. Vol. 118. P. 42–48.
21. Chapman N., Dobson J., Wilson S. et al. On behalf of the ASCOT Trial Investigators. Effect of spironolactone on blood pressure in subjects with resistant hypertension // Hypertens. 2007. Vol. 49. P. 839–845.
22. Gupta A.K., Arshad S., Poulter N.R. Compliance, safety and effectiveness of fixed–dose combinations of antihypertensive agents: a meta–analysis // Hypertens. 2010. Vol. 55. P. 399–407.
23. Bangalore S., Kamalakkannan G., Parkar S., Messerli F.H. Fixed–dose combinations improve medication compliance: a meta–analysis // Am. J. Med. 2007. Vol. 120. P. 713–719.












