Сахарный диабет (СД) 2 типа как сопутствующее заболевание часто встречается у больных артериальной гипертонией (АГ), значительно увеличивая сердечно–сосудистую заболеваемость и смертность [1,2]. Повышенное внимание к этому заболеванию связано с тем, что эксперты предсказывают значительный рост числа больных СД во всем мире – с 250 млн. в 2007 г. до 380 млн. в 2025 г. [3]. В этой ситуации правильный выбор антигипертензивной терапии, а также учет других факторов, определяющих прогноз больных АГ и СД 2 типа, становится особенно важен.
Сахарный диабет – высокая
сердечно–сосудистая заболеваемость и смертность
Неблагоприятный прогноз у больных СД 2 типа определяется главным образом развитием макро– и микрососудистых осложнений [1,2,4,5]. Причиной развития макрососудистых осложнений является атеросклеротическое поражение основных артериальных бассейнов, приводящее к развитию ишемической болезни сердца (ИБС) и ее осложнений, церебро–васкулярной болезни и облитерирующего поражения артерий нижних конечностей. В основе развития микрососудистых осложнений лежит специфическое для СД поражение сосудов микроциркуляторного русла, связанное с утолщением базальных мембран капилляров. Важнейшими клиническими проявлениями микроангиопатии являются диабетическая нефропатия и ретинопатия. Сахарный диабет является самой частой причиной слепоты у взрослых, а среди пациентов, находящихся на хроническом гемодиализе, это заболевание встречается в 30% случаев.
Артериальная гипертония и риск
развития осложнений СД 2 типа
Наряду с другими факторами в развитии осложнений СД огромное значение придается повышенному АД. Распространенность АГ у больных СД 2 типа выше, чем в общей популяции (более чем в половине всех случаев) [6]. Наличие АГ значительно увеличивает сердечно–сосудистую заболеваемость и смертность при СД 2 типа. В исследовании MRFIT было показано, что повышенное АД ассоциируется с 2–3–кратным увеличением абсолютного риска сердечно–сосудистой смертности у больных СД 2 типа по сравнению с лицами без диабета [7]. Однако и у больных АГ вероятность заболеть СД 2 типа существенно выше. По данным длительного проспективного когортного исследования ARIC, в которое было включено 12550 взрослых, оказалось, что вероятность развития СД было в 2,5 раза выше у больных АГ, чем у индивидуумов такого же возраста без повышенного АД исходно [8].
К отличительным признакам, характеризующим течение АГ у больных СД 2 типа можно отнести более частое выявление увеличения пульсового давления (разница между систолическим и диастолическим АД), что в последние годы неизменно ассоциируется с более высокой вероятностью развития сердечно–сосудистых осложнений и в рекомендациях по АГ обозначено, как дополнительный фактор риска [5]. Для больных СД 2 типа в сочетании с АГ более характерны повышенные цифры АД в ночное время. Отсутствие снижения АД ночью является феноменом, ассоциирующимся с более частым поражением органов–мишеней (в частности, сердца и почек). Поражение почек различной степени выраженности значительно чаще встречается при сочетании АГ с СД и в конечном итоге является основной причиной терминальной почечной недостаточности и направления больных на гемодиализ.
Основной причиной смерти больных СД 2 типа является инфаркт миокарда (ИМ). Особенно часто различные появления ИБС встречаются при сочетании СД с АГ, течение которых носит безболевой характер (безболевой ИМ или безболевая ишемия миокарда). В этой ситуации необходимо проводить дополнительные обследования с целью выявления коронарной недостаточности.
Для больных СД весьма характерны значительные нарушения ауторегуляции кровяного давления, что нередко манифестируется ортостатической гипотонией, осложняющей проведение адекватного контроля за АД. У них чаще регистрируется повышенное АД во время физической нагрузки. Следует отметить, что указанные отличия могут частично объяснить более высокий риск развития сердечно–сосудистых осложнений у больных СД с АГ [5].
В плане развития сердечно–сосудистых и микрососудистых осложнений у больных СД и АГ большое значение придается и абсолютным цифрам повышения АД. По данным крупного проспективного исследования, СД 2 типа наблюдалась непрерывная прямая взаимосвязь между риском осложнений и уровнем систолического АД: различиям в 10 мм рт.ст. по уровню систолического АД соответствовали различия по риску развития ИМ в 12%, а по риску развития микрососудистых осложнений – в 13% [9]. Результаты эпидемиологического исследования не обнаружили порогового уровня АД, ниже которого не происходило бы дальнейшего снижения риска осложнений. Взаимосвязь между уровнем АД и частотой сердечно–сосудистых осложнений прослеживалась и среди больных СД с уровнем АД <130 мм рт.ст.
Антигипертензивная терапия
и сосудистые осложнения СД
В настоящее время уже окончательно установлено, что снижение уровня АД имеет решающее значение в предотвращении макро– и микрососудистых осложнений СД. В исследовании HOPE у больных СД 2 типа на фоне лечения рамиприлом отмечалось снижение риска развития основных сердечно–сосудистых осложнений (ИМ, инсульта и смертности от сердечно–сосудистых причин) на 25% [10].
По данным исследования UKPDS, у больных с более строгим контролем уровня АД (в среднем – 144/82 мм рт.ст.) по сравнению с больными с более высоким АД на фоне лечения (в среднем – 154/87 мм рт.ст.) частота развития всех осложнений СД была меньше на 24%, микрососудистых осложнений – на 37%, макрососудистых осложнений, включая ИМ, внезапную смерть, инсульт и заболевания периферических артерий – на 34%, инсультов – на 44% [11].
Результаты исследования Hypertension Optimal Treatment (НОТ) показали, что у больных СД оптимальным было снижение уровня диастолического АД до 80 мм рт.ст. и ниже [11]. В этой группе пациентов относительный риск развития сердечно–сосудистых осложнений был на 56% меньше, чем в группе, в которой было достигнуто снижение ≤85 мм рт.ст., и вдвое меньше, чем у больных, целью лечения которых было достижение уровня диастолического АД ≤90 мм рт.ст.
Большую практическую ценность более интенсивного контроля за уровнем АД у больных СД 2 типа показали результаты недавно завершившегося крупнейшего международного исследования ADVANCE. В исследование было включено 11140 больных СД 2 типа с высоким риском сердечно–сосудистых осложнений, причем участвовали больные как с АГ, так и без нее [13]. Несмотря на проводимую терапию и существующие рекомендации средний уровень АД при включении в исследование составил 145/81 мм рт.ст. В течение 6–недельного вводного периода на фоне фиксированной комбинации ингибитора АПФ периндоприла и диуретика индапамида АД снизилось до 137/78 мм рт.ст. По сравнению с больными, получавшими плацебо, те пациенты, которые принимали комбинированный препарат, имели в среднем на 5,6 мм рт.ст. (систолическое) и на 2,2 мм рт.ст. (диастолическое) ниже уровень АД на протяжении 4,5 лет наблюдения.
В результате дополнительного снижения АД на фоне применения комбинации ингибитора АПФ и нетиазидного диуретика относительный риск развития главных макрососудистых и микрососудистых событий (первичная конечная точка) достоверно снизился на 9% (р=0,04); риск смерти от сердечно–сосудистых причин на 18% (р=0,03); риск смерти от всех причин на 14% (р=0,03); коронарных осложнений на 14% (р=0,02) и почечных осложнений на 21% (р<0,0001). Эффект терапии не зависел от исходного уровня АД и используемой терапии (участники исследования получали всю современную профилактическую терапию). В этом исследовании были получены новые доказательства того, что дополнительное снижение АД у больных СД 2 типа значительно снижает риск развития основных сердечно–сосудистых событий и уменьшает смертность.
Как контролируется АД у больных СД: результаты клинических
исследований и реальной практики
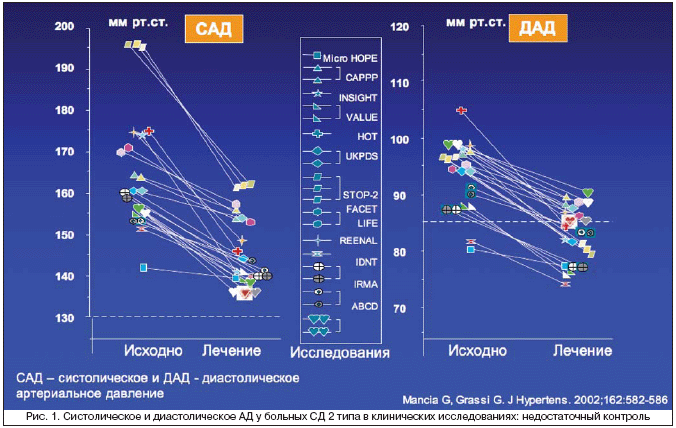
Все завершившиеся контролируемые исследования по лечению АГ у больных СД однозначно свидетельствуют о трудности контроля за уровнем АД и необходимости более частого применения комбинаций антигипертензивных препаратов [14]. Это связано, с одной стороны, с необходимостью достижения более низкого уровня АД, что возможно в большинстве случаев при использовании только нескольких препаратов, а с другой – с особенностями формирования АГ у больных СД. На рисунке 1 приведены данные о контроле за уровнем АД в наиболее крупных контролируемых исследованиях у больных СД. Видно, что особенно неблагополучно складывается ситуация с контролем систолического АД, снизить которое в среднем, в отличие от диастолического, до запланированного уровня, не удалось ни в одном из закончившихся исследований.
В исследовании UKPDS требовалось назначение 3–х и более препаратов для контроля за уровнем АД у 31% больных в группе атенолола и у 27% – в группе каптоприла [9]. По данным исследования INSIGHT, оказалось, что больные с АГ в сочетании с СД были более резистентны к лечению, у них требовалось присоединять второй и третий препараты соответственно на 40% и на 100% более часто для достижения целевого уровня АД, чем у больных без диабета [15]. Тем не менее в этом исследовании у больных СД достигнутый на фоне лечения уровень АД 141/82 мм рт.ст. оказался по величине систолического АД достоверно выше, чем у лиц без диабета – 138/82 мм рт.ст. Аналогичная картина наблюдается и в других клинических исследованиях с включением и раздельным анализом больных АГ в сочетании с СД.
Что лучше выбрать для контроля
АД у больных СД 2 типа?
В соответствии с действующими рекомендациями монотерапия одним из антигипертензивных препаратов 5 классов первой линии (диуретики, антагонисты кальция, ингибиторы АПФ, БАР и b–блокаторы) является стандартным подходом инициации контроля за АД у больных АГ [5]. Следует отметить, что эксперты рекомендуют инициировать АД–снижающую терапию у больных СД с АД>130/80 мм рт.ст. (для других категорий больных АГ при уровне более 140/90 мм рт.ст.), сразу после установления диагноза. У больных с 1 и 2 степенью повышения АД и низким или умеренным риском осложнений возможен длительный период только немедикаментозной терапии. При этом следует поддерживать АД на уровне ниже 130/80 мм рт.ст. [5,16].
Парадокс состоит в том, что установленный целевой уровень АД для больных СД согласно международным и отечественным методическим рекомендациям не базируется на доказательствах, полученных в крупномасштабных клинических исследованиях, так как для систолического АД он никогда не достигался. Что касается уровня АД, при котором у больных СД назначается антигипертензивная терапия, ситуация такая же. Данных, подтверждающих, что при АД>130/80 мм рт.ст. необходимо начинать антигипертензивное лечение, нет, так как средний уровень АД при включении в известные клинические исследования был всегда значительно выше. Поэтому эти уровни были определены на основании выраженной, положительной и постоянной ассоциации между высоким уровнем АД и риском развития клинических событий (включая терминальную почечную недостаточность), отмечаемой в эпидемиологических исследованиях [5].
В настоящее время у больного с установленным диагнозом СД 2 типа для контроля за АД нет каких–либо жестких ограничений в назначении препаратов из 5 классов антигипертензивных средств первой линии, так как эффективный контроль за АД осуществлять трудно и потенциально будет требоваться назначение комбинаций препаратов. b–блокаторы и тиазидные диуретики не следует назначать в качестве стартовой терапии, потому что они могут ухудшать инсулинорезистентность и приводить к увеличению доз и количества антидиабетических средств. В Европейских рекомендациях отмечается, что при наличии МАУ или диабетической нефропатии лечение должно начинаться или обязательно включать в себя назначение препаратов, блокирующих активность РАС [5]. Недавно было показано, что ингибиторы АПФ предупреждают появление МАУ у больных СД 2 типа; этот класс препаратов рекомендуется в качестве первичного превентивного вмешательства против нефропатии [17].
Следует напомнить, что у больных с метаболическим синдромом такие ограничения существуют: эксперты не рекомендуют инициировать лечение АГ b–блокаторами, особенно в комбинации с диуретиками, если нет на это веских дополнительных показаний [5,16]. Было показано, что такая терапия может способствовать прогрессированию нарушений углеводного обмена и повышает вероятность развития СД [18].
Рекомендуемый целевой уровень АД у больных СД ниже, чем у больных без диабета, и составляет <130/80 мм рт.ст., поэтому с помощью монотерапии далеко не всегда удается достичь заданного уровня АД. Таким образом, больные СД нуждаются в комбинированной гипотензивной терапии чаще, чем больные без диабета [11,14,15]. Если целевой уровень АД не достигается, больного переводят на комбинированную терапию (2 и более лекарственных препаратов из разных классов антигипертензивных препаратов). В Европейских рекомендациях по АГ отмечается, что у больных с высоким сердечно–сосудистым риском назначение комбинированной терапии следует иметь в виду с самого начала лечения; больные СД относятся именно к такой категории [5].
Комбинированная терапия имеет много преимуществ: усиление антигипертензивного эффекта за счет разнонаправленного действия препаратов на патогенетические механизмы развития АГ, что увеличивает число пациентов со стабильным снижением АД; уменьшение частоты возникновения нежелательных эффектов, как за счет меньших доз комбинируемых средств, так и за счет взаимной нейтрализации этих эффектов; обеспечение наиболее эффективной органопротекции и уменьшение риска и числа сердечно–сосудистых осложнений [5].
Для решения поставленных целей в лечении АГ у больных СД мы можем выбрать любую комбинацию из препаратов 5 классов, а именно – диуретики, антагонисты кальция, ингибиторы АПФ, БАР и b–блокаторы [5,16]. Вопрос состоит в том, какая из комбинаций может обеспечить максимальные преимущества в лечении этих больных.
Аргументы в пользу комбинации
препаратов, блокирующих активность РАС, и антагонистов кальция
Предпочтение до последнего времени, и вполне заслуженно, отдавалось комбинации ингибиторов АПФ с диуретиками [5]. Клиническая практика и результаты нескольких клинических исследований дают веские аргументы в пользу комбинации препаратов, ингибирующих активность ренин–ангиотензиновой системы (РАС) и антагонистов кальция. Блокада РАС уменьшает инсулинорезистентность, которая является основным механизмом развития метаболического синдрома и СД 2 типа [19]. Предполагаемыми механизмами улучшения чувствительности к инсулину являются повышение перфузии скелетных мышц, устранение микрососудистых изменений и увеличенная перфузия островковых клеток поджелудочной железы. Помимо этих гемодинамических эффектов, прямое влияние ангиотензина II на b–клетки поджелудочной железы из локальных островковых РАС может привести к потере функции b–клеток. Показано, что активация РАС ассоциируется с фиброзом островковых клеток поджелудочной железы у экспериментальных животных с СД 2 типа.
В целом ряде клинических исследований было установлено, что частота развития новых случаев СД 2 типа может быть уменьшена при назначении ингибиторов АПФ или БАР в сравнении с b–блокаторами и диуретиками [20]. В исследовании ALLHAT с общим числом участников 33357 больных АГ частота развития новых случаев СД в течение 4 лет составила 8,1% в группе ингибитора АПФ лизиноприла, 9,8% в группе антагониста кальция амлодипина и 11,6% в группе тиазидного диуретика хлорталидона [21].
Блокада РАС значительно уменьшает частоту различных диабетических осложнений, включая диабетическую нефропатию [4,16,22]. В ряде исследований были показаны нефропротективные эффекты ингибиторов АПФ и БАР как на самом начальном этапе, при наличии МАУ, так и при явной диабетической нефропатии, замедляя ее прогрессирование. В одном из клинических исследований, проведенных в условиях двойного слепого метода, изучалось влияние ингибитора АПФ лизиноприла и антагониста кальция нифедипина на МАУ у больных СД 2 типа [23]. Более 300 больных были рандомизированы в две группы и наблюдались в течение года. Несмотря на одинаковый контроль уровня АД и глюкозы крови, в группе больных, получавших лечение лизиноприлом, было более значительное снижение протеинурии по сравнению с группой нифедипина.
Комбинация ингибиторов АПФ и антагонистов кальция – это и более выраженный антигипертензивный эффект, что крайне полезно у этих больных. Действительно, во многих клинических исследованиях было показано, что антагонисты кальция (как правило, изучались амлодипин или нифедипин длительного действия) оказывают значительное АД–снижающее действие, что сопровождается дополнительными, в первую очередь вазопротективными свойствами [15,24–26]. Включение антагониста кальция в комбинированную терапию может в значительной степени усилить и антиатеросклеротическое воздействие.
Антагонисты кальция, в том числе амлодипин, быстро оказывают антигипертензивное действие. В исследовании VALUE в группе больных, получавших терапию амлодипином раньше, в сравнении с БАР валсартаном достигалось снижение повышенного АД, что в первые полгода наблюдения отражалось и на риске развития осложнений [25].
Усиление АД–снижающего действия при использовании этой комбинации сопровождается уменьшением частоты возникновения нежелательных реакций, в частности, отеков голеней, характерных для дигидропиридиновых антагонистов кальция [27]. Имеются данные о том, что кашель, ассоциированный с приемом ингибиторов АПФ, также ослабляется антагонистами кальция, включая амлодипин [28].
В настоящее время активно создаются фиксированные комбинации ингибиторов АПФ и антагонистов кальция. В разных странах на различных этапах регистрации или на рынке находятся фиксированные комбинации трандолаприла и верапамила, лерканидипина и эналаприла, периндоприла и амлодипина, беназеприла и амлодипина, амлодипина и рамиприла, лизиноприла и амлодипина (препарат Экватор) и др. Использование фиксированных комбинаций упрощает режим лечения и дополнительно решает очень важную задачу: недавний мета–анализ клинических исследований продемонстрировал увеличение приверженности больных на 25%, что также способствует улучшению контроля за АД [29]. Предлагаются, в том числе и в фиксированных формах, комбинации антагонистов кальция с БАР, которые имеют потенциально такие же преимущества.
Клинические доказательства
эффективности комбинации
ингибитор АПФ + антагонист кальция
В настоящее время мы располагаем результатами нескольких исследований, в которых изучалось влияние на прогноз комбинированной терапии. Одно из них – исследование ADVANCE, о котором упоминалось ранее в этой статье, единственное из закончившихся по оценке эффективности комбинированной терапии (ингибитор АПФ периндоприл и нетиазидный диуретик индапамид в фиксированной дозе) у больных СД 2 типа [13]. В этом исследовании с помощью комбинированного препарата впервые удалось вплотную приблизиться к рекомендуемому для больных СД 2 типа уровню систолического АД – 137/78 мм рт.ст., и это сопровождалось ощутимым результатом – снижением общей смертности.
Другое исследование, результаты которого оказали стимулирующее влияние на процесс создания фиксированных комбинаций ингибиторов АПФ и антагонистов кальция, – ASCOT [18]. Хотя в этом исследовании не предусматривалось назначение комбинации препаратов в качестве стартовой терапии, в конечном итоге в обеих группах антагониста кальция амлодипина и b–блокатора атенолола большинство больных принимали комбинированную терапию с ингибитором АПФ и тиазидным диуретиком соответственно. В этом исследовании была большая субпопуляция больных АГ и СД 2 типа (п=5137 больных), у которых было 14%–е – снижение риска развития комбинированной сердечно–сосудистой конечной точки (коронарные события, инсульт, коронарные вмешательства) (р=0,026) в пользу комбинации амлодипин/периндоприл [30]. Это сопровождалось снижением риска развития инсульта на 25% (р=0,017), поражения периферических артерий на 48% (р=0,004), некоронарных реваскуляризаций на 57% (р<0,001). Имеются предварительные данные, указывающие на большее снижение риска осложнений у больных стабильной ИБС в исследовании EUROPA на фоне ингибитора АПФ периндоприла в комбинации с антагонистами кальция по сравнению с монотерапией этими препаратами [31].
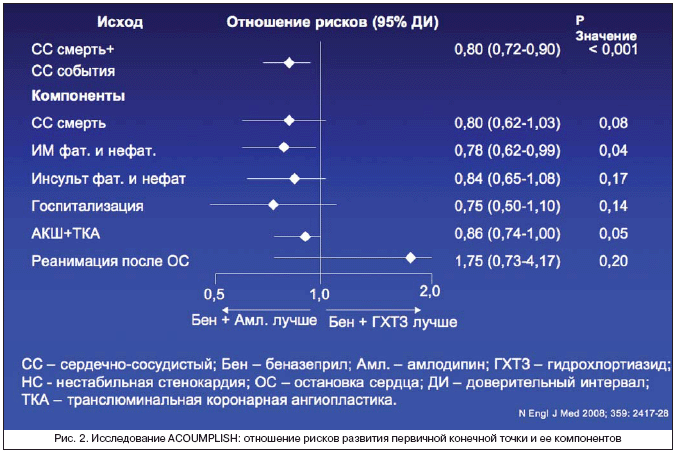
Сегодня наибольший интерес вызывают результаты клинического исследования ACCOMPLISH (the Avoiding Cardiovascular events through Combination therapy in Patients Living with Systolic Hypertension) [32]. Это единственное исследование, в котором прямо сравнивалось влияние двух режимов фиксированной комбинированной терапии ингибитора АПФ беназеприла с амлодипином либо с тиазидным диуретиком гидрохлортиазидом в качестве стартового лечения на частоту сердечно–сосудистых событий у больных АГ и высоким риском осложнений. Было включено 11506 больных (60% мужчины, средний возраст 68 лет, 71% в США и 29% в Скандинавских странах) с неконтролируемой АГ (систолическое АД >140 мм рт.ст.) на фоне лечения (97%) или без него (3%) и высоким риском осложнений (в анамнезе ИМ 23%; нестабильная стенокардия 11%; реваскуляризация миокарда 36%; инсульт 13%; заболевание почек 6%, сниженная скорость клубочковой фильтрации 18%; СД 60% больных). Больных рандомизировали на 2 группы к получению указанных комбинаций препаратов в одной капсуле с увеличением доз беназеприла до 40 мг, амлодипина до 10 мг, гидрохлортиазида до 25 мг в сутки. Предшествующая антигипертензивная терапия отменялась (периода «отмывки» не было), и со следующего дня больные принимали исследуемые комбинации. Не допускалось назначение других ингибиторов АПФ или любых БАР, тиазидных диуретиков и антагонистов кальция. Для достижения целевого уровня АД <140/90 мм рт.ст. (при СД <130/80 мм рт.ст.) при необходимости присоединялись b–блокаторы, a–блокаторы, клонидин или спиронолактон.
Исходный уровень АД составлял в среднем 145/80 мм рт.ст. без различий между группами. Было достигнуто снижение АД в обеих группах: в среднем 131,6/73,3 в группе ингибитор АПФ/антагонист кальция и 132,5/74,4 мм рт.ст. в группе ингибитор АПФ/диуретик, хотя с небольшим, но достоверным различием в пользу первой комбинации. Исследование завершилось досрочно, через 3 года, поскольку были получены четкие доказательства более высокой эффективности комбинации ингибитора АПФ с антагонистом кальция: в этой группе (события первичной конечной точки у 552 больных или 9,6%) было достоверное снижение относительного риска развития сердечно–сосудистых осложнений (первичная конечная точка) по сравнению с группой получавших комбинацию ингибитора АПФ с диуретиком (у 679 больных или 11,8%) – на 20% (рис. 2). На фоне ингибитора АПФ и антагониста кальция был достоверно ниже риск развития фатального и нефатального ИМ на 22% и потребности в проведении процедур реваскуляризации миокарда на 14% (рис. 2).
Таким образом, превосходство комбинированной терапии на основе амлодипина по отношению к клиническим исходам в этом исследовании позволяет заключить, что подход без использования тиазидных диуретиков в некоторых популяциях больных АГ может быть лучше [32]. Эти данные не ставят под сомнение эффективность диуретиков в таких исследованиях, как ADVANCE и HYVET [13,33]. Определено, что тиазидоподобные диуретики эффективны в профилактике сердечно–сосудистых осложнений, по данным мета–анализов клинических исследований с включением больных АГ [34], а их значение в составе комбинированной терапии до настоящего времени никогда не подвергалось сомнению [35]. Результаты исследования ACCOMPLISH говорят о том, что комбинация ингибитора АПФ с антагонистом кальция имеет хорошие перспективы для более широкого применения в первую очередь у больных с недостаточно контролируемой АГ и высоким сердечно–сосудистым риском или сопутствующими заболеваниями (ИБС и др.).
Заключение
Сочетание АГ и СД 2 типа значительно увеличивает риск развития сердечно–сосудистых и почечных осложнений. В условиях прогнозируемого в ближайщие десятилетия огромного роста числа больных СД 2 типа поиск оптимальных методов контроля за АГ и другими сердечно–сосудистыми заболеваниями представляется особо актуальным. Уже в современных условиях профилактика макрососудистых осложнений у этих больных вполне реальна. Она заключается в интенсивном контроле за целым рядом показателей, характеризующих тяжесть течения и повышенный риск развития осложнений (липидные показатели, уровень гликемии, инсулинорезистентность и др.), важнейщим из которых является АД. Для контроля за АД наряду с другими лекарственными средствами большое значение имеет назначение комбинированной терапии с включением препаратов, блокирующих активность РАС (препараты с фиксированной дозой приоритетны), в схему ведения больных СД 2 типа.
Литература
1. Sowers JR, Epstein M, Frohlich ED. Diabetes, hypertension, and cardiovascular disease. An Update. Hypertension 2001; 37: 1053–1059.
2. Haffner M., Lehto S., Ronnemaa T. et al. Mortality from coronary heart disease in subjects with 2 diabetes and in nondiabetic subjects with and without prior myocardial infaction. N. Engl. J. Med., 1999, 339, 229–234.
3. Wild S, Roglic G, Green A, et al. Global prevalence of diabetes: estimates for the years 2000 and projections for 2030. Diabetes Care 2004; 27: 1047–1053.
4. Дедов И.И., Шестакова М.В. Диабетическая нефропатия. Универсум Паблишинг, М., 2000, 240 с.
5. The Task Force for the management of arterial hypertension of the European Society of Hypertension and of the European Society of Cardiolody. 2007 Guidelines for the management of arterial hypertension. J Hypertens 2007; 25: 1105–1187.
6. Cooper M. The prevalence of hypertension in patients with diabetes. In: Hypertension and diabetes (Ed. Mogensen CE). Lippincott Williams & Wilkins, London, 2003, 3–9.
7. Stamler J., Vaccaro O., Neaton JD, Wentworth D., for the Multiple Risk Factor Intervention Trial Research Group. Diabetes, other risk factors, and 12–year cardiovascular mortality for men screened in the Multiple Risk Factor Intervention Trial. Diabetes Care 1993; 16: 434–444.
8. Gress TW, Nieto FJ, Shahar E, et al. Hypertension and antihypertensive therapy as risk factors for type 2 diabetes mellitus: Atherosclerosis Risk in Communities Study. N Engl J Med 2000; 342: 905–912.
9. Adler A., Stratton I.M., Neil H., et al. Assotiation of systolic blood pressure with macrovascular and microvascular complications of type 2 diabetes (UKPDS 36): prospective observational study. BMJ 2000; 321: 412–419.
10. Heart Outcomes Prevention Evaluation (HOPE) Study Investigators. Effects of ramipril on cardiovascular and microvascular outcomes in people with diabetes mellitus: results of the HOPE study and MICRO–HOPE substudy. Lancet 2000; 355: 253–258.
11. UK Prospective Diabetes Study Group. Tight blood pressure control and risk of macrovascular complications in type 2 diabetes: UKPDS 38. Br Med J 1998; 317: 703–13.
12. Hansson L., Zanchetti J.A., Carruthers S.G. Effects of intensive blood–pressure lowering and low–dose aspirin in patients with hypertension: principal results of the Hypertension Optimal Treatment (HOT) randomised trial. Lancet 1998; 351: 1756 –1762.
13. ADVANCE Collaborative Group. Effects of fixed combination of perindopril and indapamide on macrovascular and microvascular outcomes in patients with type 2 diabetes mellitus (the ADVANCE trial): a randomised controlled trial. Lancet 2007; 370: 828–840.
14. Mancia G, Grassi G. Systolic and diastolic blood pressure control in antihypertensive drug trials. J Hypertens 2002; 20: 1461–1464.
15. Brown MJ, Palmer CR, Castaigne A, et al. Morbidity and mortality in patients randomized to double–blind treatment with a long–acting calcium–channel blocker or diuretic in the international nifedipine GITS study: intervention as a Goal in Hypertension Treatment (INSIGHT). Lancet 2000; 356: 366–372.
16. The Task Fors on Diabetes and Cardiovascular Disease of the European Society of Cardiology (ESC) and of the European Association for the Study of Diabetes (EASD). Guidelines on diabetes, pre–diabetes, and cardiovascular disease: executive summary. Eur Heart J 2007; 28: 88–136.
17. Ruggenenti P, Fassi A, Bruno S, et al. Bergamo nephrologic diabetes complications trial (BENEDICT) investigators. Preventing microalbuminuria in type 2 diabetes. N Engl J Med 2004; 351; 1941–1951.
18. Sever PS, Dahlof B, Poulter NR, et al. for the ASCOT Investigators. Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required, in the Anglo–Scandinavian Cardiac Outcomes Trial (ASCOT–BPLA): a multicentre randomized controlled trial. Lancet 2005; 366: 895–906.
19. Jandeleit–Dahm KA, Tikellis C, Reid CM, et al. Why blockade of the rennin–angiotensin system reduces the incidence of new–onset diabetes. J Hypertens 2005;23: 463–73.
20. Elliot WJ, Meyer PM. Incident diabetes in clinical trials of antihypertensive drugs: a net work meta–analysis. Lancet 2007; 369: 201–207.
21. The ALLHAT Officers and Coordinators. Major outcomes in high–risk hypertensive patients randomized to ACE inhibitor or calcium channel blocker vs diuretic (ALLHAT). JAMA 2002; 288: 2981–2997.
22. Schmieder RE, Hilgers KF, Schlaich MP, et al. Renin–angiotensin system and cardiovascular risk. Lancet 2007; DOI: 10.1016|S0140–6736(07)60242–6.
23. Agardh CD, Garcia–Puig J, Charbonnel B, et al. Greater reduction of urinary albumin excretion in hypertensive type II diabetic patients with incipient nephropathy by lisinopril than by nifedipine. J Human Hypertens 1996; 10: 185–192.
24. Nissen SE, Tuzcu EM, Libby P, et al. CAMELOT Investigators. Effect of antihypertensive agents on cardiorprovascular events in patients with coronary disease and normal blood pressure: the CAMELOT study: a randomized controlled trial. JAMA 2004; 292: 2217–2225.
25. Julius S, Kjeldsen SE, Weber M, et al. Outcomes in hypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amlodipin: the VALUE randomised trial. Lancet 2004; 363: 2021–2031.
26. Weir MR. Calcium channel blockers: their pharmacologic and therapeutic role in hypertension. Am J Cardiovasc Drugs 2007; 7 (Suppl 1): 5–15.
27. Fogari R, Malamani G, Zoppi A, et al. Effect on the developrnent of ankle edema of adding delapril to manidipine in patients with mild to moderate essential hypertension: a there–way crossover study. Clin Ther 2007; 29 (3): 413–8
28. Fogari R, Zoppi A, Mugellini A, et al. Effect of amlodipine, nifedipine GITS, and indomethacin on angiotensin–converting enzyme inhibitor–induced cough: a randomized, placebo controlled, double–masked, crossover study. Curr Ther Res 1999; 60 (3):121–128.
29. Bangalore S, Kamalakkarmari G, Parkas S, et al. fixed–dose combinations improve medication compliancec a meta–analysis. Am J Med 2007: 120 (8): 713–719.
30. Ostergren J, Poulter NR, Sever PS, et al for the ASCOT investigators. The Anglo–Scandinavian Cardiac Outcomes Trial: blood pressure–lowering limb: effects in patients with type II diabetes. J Hypertens 2008; 26: 2103–2111.
31. Bertrand M, Sever P. Synergistic effect of perindopril and calcium channel blockers in prevention of cardiac events and death in coronary artery disease patients: analysis from the EUROPA study [abstract no.3267]. Congress of the European Society of Cardiology (ESC); 2008 Aug 30: Munich.
32. Jamerson KA, Weber MA, Bakris GL et al on behalf of the ACCOMPLISH investigators. Benazepril plus amlodipine or hydrochlorotiazide for hypertension in high–risk patients. N Engl J Med 2008; 359: 2417–2428.
33. Beckett NS, Peters R, Fletcher AE et al; the HYVET Study Group. Treatment of Hypertension in Patients 80 Years of Age or Older. N Engl J Med. 2008; 358: 1887–1898.
34. Turnbull F. Effects of different blood–pressure–lowering regimens on major cardiovascular events: results of prospectively–designed overviews of randomized trials. Lancet 2003; 362: 1527–1535.
35. Messerli FH, Makani H, Bangalore S, et al. Hydrochlorothiazide is inappropriate for first–line antihypertensive therapy. European Meeting on Hypertension; June 12–16, 2009; Milan, Italy. Abstract LB1.3.












