–Ы–Є–Ј–Є–љ–Њ–њ—А–Є–ї (–Ы–Є–Ј–Є–≥–∞–Љ–Љ–∞ –Є –і—А.) –≤—Л–і–µ–ї—П–µ—В—Б—П —Б—А–µ–і–Є –і–ї–Є—В–µ–ї—М–љ–Њ–і–µ–є—Б—В–≤—Г—О—Й–Є—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є–Љ–Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ–Є. –Т–Њ––њ–µ—А–≤—Л—Е, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –њ–Њ–і–∞–≤–ї—П—О—Й–µ–µ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –≤—В–Њ—А–Њ–≥–Њ –Є —В—А–µ—В—М–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П —П–≤–ї—П—О—В—Б—П –њ—А–Њ–ї–µ–Ї–∞—А—Б—В–≤–∞–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ –ї–Є—И—М –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –≥–Є–і—А–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤ –њ—А–µ–≤—А–∞—Й–∞—О—В—Б—П –≤ –∞–Ї—В–Є–≤–љ—Л–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –∞–Ї—В–Є–≤–љ–Њ–µ –≤–µ—Й–µ—Б—В–≤–Њ.
–Т–Њ––≤—В–Њ—А—Л—Е, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї (–Ы–Є–Ј–Є–≥–∞–Љ–Љ–∞ –Є –і—А.) – –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є –і–Њ—Б—В—Г–њ–љ—Л–є –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§, –Ї–Њ—В–Њ—А—Л–є –љ–µ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ, –∞ –њ–Њ–ї–љ–Њ—Б—В—М—О –≤—Л–≤–Њ–і–Є—В—Б—П –њ–Њ—З–Ї–∞–Љ–Є –≤ –љ–µ–Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–Љ –≤–Є–і–µ. –Т—Б–µ –і—А—Г–≥–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —З–∞—Б—В–Є—З–љ–Њ –Є–ї–Є –њ–Њ–ї–љ–Њ—Б—В—М—О –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г—О—В—Б—П –≤ –њ–µ—З–µ–љ–Є. –Я–Њ—Н—В–Њ–Љ—Г –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –±–Њ–ї–µ–µ –±–µ–Ј–Њ–њ–∞—Б–µ–љ, —З–µ–Љ –і—А—Г–≥–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§, —Г –±–Њ–ї—М–љ—Л—Е —Б —В—П–ґ–µ–ї—Л–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –њ–µ—З–µ–љ–Є. –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –≤—Л–≤–µ–і–µ–љ–Є—П –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –Њ–±—К—П—Б–љ—П—О—В—Б—П —В–µ–Љ, —З—В–Њ –Њ–љ —П–≤–ї—П–µ—В—Б—П –≥–Є–і—А–Њ—Д–Є–ї—М–љ—Л–Љ –≤–µ—Й–µ—Б—В–≤–Њ–Љ, —В–Њ–≥–і–∞ –Ї–∞–Ї –њ–Њ–і–∞–≤–ї—П—О—Й–µ–µ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –і—А—Г–≥–Є—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –Њ—В–љ–Њ—Б—П—В—Б—П –Ї –ї–Є–њ–Њ—Д–Є–ї—М–љ—Л–Љ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П–Љ.
–Т–—В—А–µ—В—М–Є—Е, –Ї–∞–Ї –≥–Є–і—А–Њ—Д–Є–ї—М–љ–Њ–µ –≤–µ—Й–µ—Б—В–≤–Њ, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –≤ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є –Љ–µ—А–µ —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П —Б –±–µ–ї–Ї–∞–Љ–Є (5–10%) –њ–ї–∞–Ј–Љ—Л –Ї—А–Њ–≤–Є. –Я–Њ—Н—В–Њ–Љ—Г –µ–≥–Њ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–∞ —Б—Г—И–µ—Б—В–≤–µ–љ–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ—П–µ—В—Б—П —Г –±–Њ–ї—М–љ—Л—Е —Б –≥–Є–њ–Њ–њ—А–Њ—В–µ–Є–љ–µ–Љ–Є–µ–є (–љ–∞–њ—А–Є–Љ–µ—А, –њ–µ—З–µ–љ–Њ—З–љ–Њ–≥–Њ –Є–ї–Є –њ–Њ—З–µ—З–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П), –∞ —В–∞–Ї–ґ–µ –њ—А–Є —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Б –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є, —Б–њ–Њ—Б–Њ–±–љ—Л–Љ–Є –≤—Л—В–µ—Б–љ—П—В—М –і—А—Г–≥–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л –Є–Ј —Б–≤—П–Ј–Є —Б –њ–ї–∞–Ј–Љ–µ–љ–љ—Л–Љ–Є –±–µ–ї–Ї–∞–Љ–Є (–љ–∞–њ—А–Є–Љ–µ—А, —Б—Г–ї—М—Д–Є–љ–њ–Є—А–∞–Ј–Њ–љ, –∞–Љ–Є–Њ–і–∞—А–Њ–љ –Є –і—А.) [1–5].
–Т—Б–µ —Н—В–Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –њ–Њ–Ј–≤–Њ–ї—П—О—В —Б—З–Є—В–∞—В—М –µ–≥–Њ —В–Є–њ–Є—З–љ—Л–Љ –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–µ–Љ –Њ—Б–Њ–±–Њ–≥–Њ, III –Ї–ї–∞—Б—Б–∞ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ (—В–∞–±–ї. 1).
–Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є
—Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞
–Ы–Є–Ј–Є–љ–Њ–њ—А–Є–ї –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ –Р–Я–§ III –Ї–ї–∞—Б—Б–∞ (—В–∞–±–ї. 1). –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –і—А—Г–≥–Є—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –Њ–љ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –і–µ–є—Б—В–≤–Є–µ –±–µ–Ј –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ–є –±–Є–Њ—В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–Є –≤ –њ–µ—З–µ–љ–Є. –Р–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –≤ —В–µ—З–µ–љ–Є–µ 30–60 –Љ–Є–љ. –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –≤–љ—Г—В—А—М, –і–Њ—Б—В–Є–≥–∞–µ—В –Љ–∞–Ї—Б–Є–Љ—Г–Љ–∞ —З–µ—А–µ–Ј 4–10 —З –Є –њ—А–Њ–і–Њ–ї–ґ–∞–µ—В—Б—П –і–Њ 36 —З–∞—Б–Њ–≤. –Ы–Є–Ј–Є–љ–Њ–њ—А–Є–ї – –Њ–і–Є–љ –Є–Ј –љ–µ–Љ–љ–Њ–≥–Є—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§, –Ї–Њ—В–Њ—А—Л–є —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –њ—А–Є –њ—А–Є–µ–Љ–µ 1 —А–∞–Ј –≤ —Б—Г—В–Ї–Є, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –Љ–љ–Њ–≥–Є–µ –і—А—Г–≥–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П (—Н–љ–∞–ї–∞–њ—А–Є–ї, –Ї–≤–Є–љ–∞–њ—А–Є–ї, –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї, —А–∞–Љ–Є–њ—А–Є–ї, —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї –Є –і—А.) –Є–љ–Њ–≥–і–∞ –њ—А–Є—Е–Њ–і–Є—В—Б—П –љ–∞–Ј–љ–∞—З–∞—В—М 2 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є.
–С–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –≤–љ—Г—В—А—М —Б–Њ—Б—В–∞–≤–ї—П–µ—В –≤ —Б—А–µ–і–љ–µ–Љ 25–50%. –°–Њ–≤–Љ–µ—Б—В–љ—Л–є –њ—А–Є–µ–Љ —Б –њ–Є—Й–µ–є –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –≤–ї–Є—П–љ–Є—П –љ–∞ –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞. –Я–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –≤–љ—Г—В—А—М –њ–ї–∞–Ј–Љ–µ–љ–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –і–Њ—Б—В–Є–≥–∞—О—В –Љ–∞–Ї—Б–Є–Љ—Г–Љ–∞ –≤ —В–µ—З–µ–љ–Є–µ 6 —З. –Т –Ї—А–Њ–≤–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї —Ж–Є—А–Ї—Г–ї–Є—А—Г–µ—В –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –≤–љ–µ —Б–≤—П–Ј–Є —Б –њ–ї–∞–Ј–Љ–µ–љ–љ—Л–Љ–Є –±–µ–ї–Ї–∞–Љ–Є.
–Ы–Є–Ј–Є–љ–Њ–њ—А–Є–ї –љ–µ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П –≤ –њ–µ—З–µ–љ–Є, –∞ –≤—Л–≤–Њ–і–Є—В—Б—П –њ–Њ—З–Ї–∞–Љ–Є –≤ –љ–µ–Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–Љ –≤–Є–і–µ. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –љ–µ —В—А–µ–±—Г–µ—В—Б—П —Г–Љ–µ–љ—М—И–∞—В—М –і–Њ–Ј—Г –њ—А–µ–њ–∞—А–∞—В–∞. –° –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, –њ—А–Є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Н–ї–Є–Љ–Є–љ–∞—Ж–Є—П –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –Ј–∞–Љ–µ–і–ї—П–µ—В—Б—П –Є —В—А–µ–±—Г–µ—В—Б—П –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є—Е –љ–∞—З–∞–ї—М–љ—Л—Е –і–Њ–Ј –њ—А–µ–њ–∞—А–∞—В–∞.
–Т—Л–≤–µ–і–µ–љ–Є–µ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –љ–Њ—Б–Є—В –і–≤—Г—Е—Д–∞–Ј–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А. –≠—Д—Д–µ–Ї—В–Є–≤–љ—Л–є –њ–µ—А–Є–Њ–і –µ–≥–Њ –њ–Њ–ї—Г–ґ–Є–Ј–љ–Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ–Ї–Њ–ї–Њ 13 —З–∞—Б–Њ–≤, –∞ —В–µ—А–Љ–Є–љ–∞–ї—М–љ—Л–є –њ–µ—А–Є–Њ–і – –Њ–Ї–Њ–ї–Њ 30 —З–∞—Б–Њ–≤. –Ф–ї–Є—В–µ–ї—М–љ—Л–Љ –њ–µ—А–Є–Њ–і–Њ–Љ –њ–Њ–ї—Г–ґ–Є–Ј–љ–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –Њ–±—К—П—Б–љ—П–µ—В—Б—П, –њ–Њ—З–µ–Љ—Г –µ–≥–Њ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –њ—А–µ–≤—Л—И–∞–µ—В 24 —З–∞—Б–∞ [6,7].
–Ґ–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–µ
–њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞
–Ь–µ—Е–∞–љ–Є–Ј–Љ—Л —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Е–Њ—А–Њ—И–Њ –Є–Ј—Г—З–µ–љ—Л –Є —Б–≤—П–Ј–∞–љ—Л —Б —В–Њ—А–Љ–Њ–ґ–µ–љ–Є–µ–Љ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –і–Є–њ–µ–њ—В–Є–і–Є–ї–Њ–≤–Њ–є –Ї–∞—А–±–Њ–Ї—Б–Є–њ–µ–њ—В–Є–і–∞–Ј—Л, –Ї–Њ—В–Њ—А–∞—П –Ї–∞—В–∞–ї–Є–Ј–Є—А—Г–µ—В –Њ—В—Й–µ–њ–ї–µ–љ–Є–µ –і–≤—Г—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ—Л—Е –Њ—Б—В–∞—В–Ї–Њ–≤ –Њ—В –°––Ї–Њ–љ—Ж–∞ —Н—Д—Д–µ–Ї—В–Њ—А–љ—Л—Е –њ–µ–њ—В–Є–і–Њ–≤ —А–µ–љ–Є–љ––∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤–Њ–є –Є –Ї–∞–ї–ї–Є–Ї—А–µ–Є–љ––Ї–Є–љ–Є–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ. –Т —А–µ–љ–Є–љ––∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ–µ —Н—В–∞ –і–Є–њ–µ–њ—В–Є–і–Є–ї–Њ–≤–∞—П –Ї–∞—А–±–Њ–Ї—Б–Є–њ–µ–њ—В–Є–і–∞–Ј–∞ –Ї–∞—В–∞–ї–Є–Ј–Є—А—Г–µ—В –њ—А–µ–≤—А–∞—Й–µ–љ–Є–µ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–∞ I –≤ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –∞–Ї—В–Є–≤–љ—Л–є –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ II; –њ–Њ—Н—В–Њ–Љ—Г –µ–µ —З–∞—Б—В–Њ –љ–∞–Ј—Л–≤–∞—О—В –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ I––њ—А–µ–≤—А–∞—Й–∞—О—Й–Є–Љ —Д–µ—А–Љ–µ–љ—В–Њ–Љ (—Б–Њ–Ї—А–∞—Й–µ–љ–љ–Њ: –Р–Я–§). –Т –Ї–∞–ї–ї–Є–Ї—А–µ–Є–љ––Ї–Є–љ–Є–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ–µ —Н—В–Њ—В —Д–µ—А–Љ–µ–љ—В –Ї–∞—В–∞–ї–Є–Ј–Є—А—Г–µ—В —А–∞—Б—Й–µ–њ–ї–µ–љ–Є–µ –±—А–∞–і–Є–Ї–Є–љ–Є–љ–∞ –Є –і—А—Г–≥–Є—Е –Ї–Є–љ–Є–љ–Њ–≤ –і–Њ –љ–µ–∞–Ї—В–Є–≤–љ—Л—Е –њ–µ–њ—В–Є–і–Њ–≤. –Ю—В—Б—О–і–∞ –і—А—Г–≥–Њ–µ –љ–∞–Ј–≤–∞–љ–Є–µ –і–Є–њ–µ–њ—В–Є–і–Є–ї–Њ–≤–Њ–є –Ї–∞—А–±–Њ–Ї—Б–Є––њ–µ–њ—В–Є–і–∞–Ј—Л – –Ї–Є–љ–Є–љ–∞–Ј–∞ II (–Ї–Є–љ–∞–Ј–∞ II). –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –Р–Я–§ –Є –Ї–Є–љ–Є–љ–∞–Ј–∞ II – —Н—В–Њ —А–∞–Ј–љ—Л–µ –љ–∞–Ј–≤–∞–љ–Є—П –Њ–і–љ–Њ–≥–Њ –Є —В–Њ–≥–Њ –ґ–µ —Д–µ—А–Љ–µ–љ—В–∞ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –µ–≥–Њ —Д—Г–љ–Ї—Ж–Є–Є.
–Т –Ї–Њ–љ–µ—З–љ–Њ–Љ —Б—З–µ—В–µ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ –њ–Њ–і–∞–≤–ї—П—О—В—Б—П —Н—Д—Д–µ–Ї—В—Л, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б —З—А–µ–Ј–Љ–µ—А–љ–Њ–є –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є —А–µ–љ–Є–љ––∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л, –Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —Г—Б–Є–ї–Є–≤–∞—О—В—Б—П —Н—Д—Д–µ–Ї—В—Л, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є –Ї–∞–ї–ї–Є–Ї—А–µ–Є–љ––Ї–Є–љ–Є–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л.
–С–ї–∞–≥–Њ–і–∞—А—П —Б–≤–Њ–Є–Љ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л–Љ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ —Б–≤–Њ–є—Б—В–≤–∞–Љ –Є —Е–Њ—А–Њ—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ. –Ю–±—Й–µ–њ—А–Є–Ј–љ–∞–љ–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ–Є –Ї –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ —Б—З–Є—В–∞—О—В—Б—П: (1) –і–ї–Є—В–µ–ї—М–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –Р–У; (2) –ї–µ—З–µ–љ–Є–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є –Є –љ–µ–Ї–Њ—В–Њ—А—Л—Е –і—А—Г–≥–Є—Е –њ–∞—А–µ–љ—Е–Є–Љ–∞—В–Њ–Ј–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–Њ—З–µ–Ї; (3) –ї–µ—З–µ–љ–Є–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (–•–°–Э), –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ (–Ы–Ц), –Є (4) –≤—В–Њ—А–Є—З–љ–∞—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ —Г –±–Њ–ї—М–љ—Л—Е, –њ–µ—А–µ–љ–µ—Б—И–Є—Е –Њ—Б—В—А—Л–є –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞ (–Ш–Ь). –Э–µ –≤—Б–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –Є–Ј—Г—З–∞–ї–Є—Б—М –≤ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ—А–Є —Н—В–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е. –Э–∞–њ—А–Є–Љ–µ—А, –њ—А–Є –•–°–Э —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –≤—Б–µ–≥–Њ 5 –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ (—Н–љ–∞–ї–∞–њ—А–Є–ї–∞, –Ї–∞–њ—В–Њ–њ—А–Є–ї–∞, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞, —А–∞–Љ–Є–њ—А–Є–ї–∞ –Є —В—А–∞–љ–і–Њ–ї–∞–њ—А–Є–ї–∞), —В–Њ–≥–і–∞ –Ї–∞–Ї —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–Њ—Н–Ї—Б–Є–њ—А–Є–ї–∞ –њ—А–Є –•–°–Э –љ–Є–Ї–Њ–≥–і–∞ –љ–µ –Є–Ј—Г—З–∞–ї–∞—Б—М. –Я–Њ—Н—В–Њ–Љ—Г —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –Љ–µ–і–Є—Ж–Є–љ—Л, –Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–є –љ–∞ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞—Е, –љ–µ –≤—Б–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –Љ–Њ–≥—Г—В –љ–∞–Ј–љ–∞—З–∞—В—М—Б—П –њ–Њ –≤—Б–µ–Љ —З–µ—В—Л—А–µ–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ. –Ю–і–Є–љ –Є–Ј –љ–µ–Љ–љ–Њ–≥–Є—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§, —А–∞–Ј—А–µ—И–µ–љ–љ—Л—Е –і–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–Є –Р–У, –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є, –•–°–Э –Є –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –Ш–Ь – —Н—В–Њ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї.
–Ы–Є–Ј–Є–љ–Њ–њ—А–Є–ї –њ—А–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є
–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є –Є —Б–∞—Е–∞—А–љ–Њ–Љ –і–Є–∞–±–µ—В–µ
–Ф–ї–Є—В–µ–ї—М–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –Р–У – –Њ—Б–љ–Њ–≤–љ–Њ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ –і–ї—П –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –≤–Њ–Њ–±—Й–µ –Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є.
–Т —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –і–≤–Њ–є–љ—Л–Љ —Б–ї–µ–њ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є –Ї—Г—А—Б–Њ–≤–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї (10–40 –Љ–≥/—Б—Г—В.) —Б–љ–Є–ґ–∞–µ—В –Р–Ф –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 15–20/10–15 –Љ–Љ —А—В.—Б—В. –Я–Њ –і–∞–љ–љ—Л–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ–ї—Г—З–Є—В—М —Е–Њ—А–Њ—И–Є–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В —Г 50–80% –±–Њ–ї—М–љ—Л—Е —Б –Р–У 1 –Є–ї–Є 2 —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є [6,7]. –Я–Њ –і–∞–љ–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П ALLHAT, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї, –љ–∞–Ј–љ–∞—З–∞–µ–Љ—Л–є –±–µ–Ј –і–Є—Г—А–µ—В–Є–Ї–∞, –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ —Г –Љ—Г–ґ—З–Є–љ, —З–µ–Љ —Г –ґ–µ–љ—Й–Є–љ, –Є —Г –±–µ–ї—Л—Е –±–Њ–ї—М–љ—Л—Е, —З–µ–Љ —Г –љ–µ–≥—А–Њ–≤ [8]. –Т –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б —В–Є–∞–Ј–Є–і–љ—Л–Љ –і–Є—Г—А–µ—В–Є–Ї–Њ–Љ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ —Г –Љ—Г–ґ—З–Є–љ –Є –ґ–µ–љ—Й–Є–љ, —Г –±–µ–ї—Л—Е –Є –љ–µ–≥—А–Њ–≤, —Г –±–Њ–ї—М–љ—Л—Е —Б—А–µ–і–љ–µ–≥–Њ –Є –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ [8].
–Т –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ–Њ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –љ–µ —Г—Б—В—Г–њ–∞–µ—В –љ–Є –і—А—Г–≥–Є–Љ –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ –Р–Я–§ (—Н–љ–∞–ї–∞–њ—А–Є–ї –Є –і—А.), –љ–Є —В–Є–∞–Ј–Є–і–љ—Л–Љ –і–Є—Г—А–µ—В–Є–Ї–∞–Љ (–≥–Є–і—А–Њ—Е–ї–Њ—А–Њ—В–Є–∞–Ј–Є–і), b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ (–Љ–µ—В–Њ–њ—А–Њ–ї–Њ–ї, –љ–µ–±–Є–≤–Њ–ї–Њ–ї), –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞–Љ –Ї–∞–ї—М—Ж–Є—П (–∞–Љ–ї–Њ–і–Є–њ–Є–љ, –≤–µ—А–∞–њ–∞–Љ–Є–ї–—А–µ—В–∞—А–і, –љ–Є—Д–µ–і–Є–њ–Є–љ–—А–µ—В–∞—А–і, —Д–µ–ї–Њ–і–Є–њ–Є–љ–—А–µ—В–∞—А–і) –Є –і—А—Г–≥–Є–Љ –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ –Р–Я–§ (—Н–љ–∞–ї–∞–њ—А–Є–ї –Є –і—А.). –Ы–Є–Ј–Є–љ–Њ–њ—А–Є–ї —Б—А–∞–≤–љ–Є–Љ –њ–Њ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б —В–∞–Ї–Є–Љ–Є –±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є –Р–Ґ1––∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –Ї–∞–Ї –≤–∞–ї—Б–∞—А—В–∞–љ –Є —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –Њ–љ —Б—В–Њ–ї—М –ґ–µ —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є–ї—Б—П –±–Њ–ї—М–љ—Л–Љ–Є —Б –Р–У, –Ї–∞–Ї b-–∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А —В—А–µ—В—М–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –љ–µ–±–Є–≤–Њ–ї–Њ–ї –Є –±–ї–Њ–Ї–∞—В–Њ—А—Л –Р–Ґ1––∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ [8–13]. –Ф–Є—Г—А–µ—В–Є–Ї–Є —Г—Б–Є–ї–Є–≤–∞—О—В –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞, —А–∞–≤–љ–Њ –Ї–∞–Ї –Є –і—А—Г–≥–Є—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§.
–Т–∞–ґ–љ—Л–Љ –і–Њ—Б—В–Њ–Є–љ—Б—В–≤–Њ–Љ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –њ—А–Є –њ—А–Є–µ–Љ–µ –Њ–і–Є–љ —А–∞–Ј –≤ —Б—Г—В–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ —Б–љ–Є–ґ–∞—В—М –Р–Ф –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –±–Њ–ї–µ–µ 24 —З–∞—Б–Њ–≤ –Є –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—В—М –њ–Њ–і—К–µ–Љ –Р–Ф –≤ —А–∞–љ–љ–Є–µ —Г—В—А–µ–љ–љ–Є–µ —З–∞—Б—Л.
–Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –і–ї—П –Њ–±—К–µ–Ї—В–Є–≤–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ—Б—В–Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –≤ 1988 –≥. –£–њ—А–∞–≤–ї–µ–љ–Є–µ–Љ –њ–Њ –Ї–Њ–љ—В—А–Њ–ї—О –Ј–∞ –Ї–∞—З–µ—Б—В–≤–Њ–Љ –њ–Є—Й–µ–≤—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ –Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –°–®–Р (FDA) –±—Л–ї –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ –Њ—Б–Њ–±—Л–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М – –Њ—В–љ–Њ—И–µ–љ–Є–µ –Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ (–Ї–Њ–љ–µ—З–љ–Њ–≥–Њ) —Н—Д—Д–µ–Ї—В–∞ –Ї –љ–∞–Є–±–Њ–ї—М—И–µ–Љ—Г (–њ–Є–Ї–Њ–≤–Њ–Љ—Г) —Н—Д—Д–µ–Ї—В—Г. –Ю—Б—В–∞—В–Њ—З–љ—Л–є —Н—Д—Д–µ–Ї—В (–Ю–≠) – —Н—В–Њ —Б—В–µ–њ–µ–љ—М —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф –≤ –Ї–Њ–љ—Ж–µ –Љ–µ–ґ–і–Њ–Ј–Њ–≤–Њ–≥–Њ –Є–љ—В–µ—А–≤–∞–ї–∞ (—В.–µ. —З–µ—А–µ–Ј 24 —З –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ – –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –њ—А–µ–і–љ–∞–Ј–љ–∞—З–µ–љ–љ—Л—Е –і–ї—П –њ—А–Є–µ–Љ–∞ 1 —А–∞–Ј –≤ —Б—Г—В–Ї–Є). –Э–∞–Є–±–Њ–ї—М—И–Є–є —Н—Д—Д–µ–Ї—В (–Э–≠) – —Н—В–Њ —Б—В–µ–њ–µ–љ—М —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф –љ–∞ –Љ–∞–Ї—Б–Є–Љ—Г–Љ–µ –і–µ–є—Б—В–≤–Є—П –і–∞–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞. –Т–µ–ї–Є—З–Є–љ–∞ –Ї–∞–Ї –Ю–≠, —В–∞–Ї –Є –Э–≠ —А–∞—Б—Б—З–Є—В—Л–≤–∞–µ—В—Б—П —Б –њ–Њ–њ—А–∞–≤–Ї–Њ–є –љ–∞ —Н—Д—Д–µ–Ї—В –њ–ї–∞—Ж–µ–±–Њ. –°—З–Є—В–∞–µ—В—Б—П, —З—В–Њ –≤–µ–ї–Є—З–Є–љ–∞ –Њ—В–љ–Њ—И–µ–љ–Є—П –Ю–≠/–Э–≠ –і–ї—П –љ–Њ–≤—Л—Е –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–Њ–ї–ґ–љ–∞ –±—Л—В—М –љ–µ –Љ–µ–љ–µ–µ 50% (–Є–ї–Є 0,50) [14]. –Я–Њ –і–∞–љ–љ—Л–Љ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є [15], –Ј–љ–∞—З–µ–љ–Є—П –Њ—В–љ–Њ—И–µ–љ–Є—П –Ю–≠/–Э–≠ –і–ї—П –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф —Г –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –Ї–Њ–ї–µ–±–ї—О—В—Б—П –Њ—В 40 –і–Њ 70%, —Б–Њ—Б—В–∞–≤–ї—П—П –≤ —Б—А–µ–і–љ–µ–Љ 56% (—В–∞–±–ї. 2). –≠—В–Њ –Њ–Ј–љ–∞—З–∞–µ—В, —З—В–Њ –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –њ—А–Є –њ—А–Є–µ–Љ–µ –Њ–і–Є–љ —А–∞–Ј –≤ —Б—Г—В–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ—В —Г—А–Њ–≤–µ–љ—М –Р–Ф –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є —Б—Г—В–Њ–Ї.
–Э–∞—А—П–і—Г —Б –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –≤—Л–Ј—Л–≤–∞–µ—В –Њ–±—А–∞—В–љ–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –Ы–Ц —Г –±–Њ–ї—М–љ—Л—Е –Р–У. –Х–≥–Њ –≤–ї–Є—П–љ–Є–µ –љ–∞ –≥–Є–њ–µ—А—В—А–Њ—Д–Є—О –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б —Н—Д—Д–µ–Ї—В–Њ–Љ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є –љ–Є—Д–µ–і–Є–њ–Є–љ–∞–—А–µ—В–∞—А–і –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–Њ, —З–µ–Љ —Г –∞—В–µ–љ–Њ–ї–Њ–ї–∞. –†–µ–≥—А–µ—Б—Б–Є—П –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –Ы–Ц –њ—А–Є –ї–µ—З–µ–љ–Є–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –љ–∞—Б—В—Г–њ–∞–µ—В –±—Л—Б—В—А–µ–µ, —З–µ–Љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –љ–Є—Д–µ–і–Є–њ–Є–љ–Њ–Љ–—А–µ—В–∞—А–і. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї (–≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –ї–Њ–Ј–∞—А—В–∞–љ–∞) —Г–ї—Г—З—И–∞–µ—В –њ–µ—А—Д—Г–Ј–Є—О –≥–Є–њ–µ—А—В—А–Њ—Д–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Љ–Є–Њ–Ї–∞—А–і–∞ –Є —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –Ї–Њ—А–Њ–љ–∞—А–љ—Л–є —А–µ–Ј–µ—А–≤. –≠—В–Њ –Њ–±—М—П—Б–љ—П—О—В —В–µ–Љ, —З—В–Њ –Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї (–≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –ї–Њ–Ј–∞—А—В–∞–љ–∞) —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ –≤ —В–Ї–∞–љ—П—Е –±—А–∞–і–Є–Ї–Є–љ–Є–љ–∞, –Ї–Њ—В–Њ—А—Л–є –Њ–Ї–∞–Ј—Л–≤–∞–µ—В —Б–Њ—Б—Г–і–Њ—А–∞—Б—И–Є—А—П—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ –Ї–Њ—А–Њ–љ–∞—А–љ—Л–µ –∞—А—В–µ—А–Є–Є –Є –∞—А—В–µ—А–Є–Њ–ї—Л. –Я—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї—Г—О –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї—Г—О —Д—Г–љ–Ї—Ж–Є–Є –Ы–Ц [12–16].
–Ы–Є–Ј–Є–љ–Њ–њ—А–Є–ї —Г–ї—Г—З—И–∞–µ—В –њ–Њ–і–∞—В–ї–Є–≤–Њ—Б—В—М –∞–Њ—А—В—Л –Є –Ї—А—Г–њ–љ—Л—Е –∞—А—В–µ—А–Є–є —Н–ї–∞—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ —В–Є–њ–∞. –Я—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Њ–љ —Г–Љ–µ–љ—М—И–∞–µ—В –Њ—В–љ–Њ—И–µ–љ–Є–µ –Љ–µ–і–Є—П/–њ—А–Њ—Б–≤–µ—В –∞—А—В–µ—А–Є–є —А–µ–Ј–Є—Б—В–Є–≤–љ–Њ–≥–Њ —В–Є–њ–∞ –Є —Г–ї—Г—З—И–∞–µ—В —Д—Г–љ–Ї—Ж–Є—О —Н–љ–і–Њ—В–µ–ї–Є—П —Г –±–Њ–ї—М–љ—Л—Е –Р–У, —З—В–Њ —Б–ї—Г–ґ–Є—В –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–Њ–Љ –љ–∞–ї–Є—З–Є—П —Г –љ–µ–≥–Њ –љ–µ —В–Њ–ї—М–Ї–Њ –Ї–∞—А–і–Є–Њ–, –љ–Њ –Є –≤–∞–Ј–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л—Е —Б–≤–Њ–є—Б—В–≤ [17].
–Ы–Є–Ј–Є–љ–Њ–њ—А–Є–ї –Њ–Ї–∞–Ј—Л–≤–∞–µ—В —В–∞–Ї–Њ–µ –ґ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —Д—Г–љ–Ї—Ж–Є—О –њ–Њ—З–µ–Ї, –Ї–∞–Ї –Є –і—А—Г–≥–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Є—Б—В–µ–Љ–љ–Њ–≥–Њ –Р–Ф, –њ–Њ—З–µ—З–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї –Є —Б–Ї–Њ—А–Њ—Б—В—М –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є –љ–µ —Б–љ–Є–ґ–∞—О—В—Б—П –њ—А–Є –ї–µ—З–µ–љ–Є–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ. –Ы–Є–Ј–Є–љ–Њ–њ—А–Є–ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В —Н–Ї—Б–Ї—А–µ—Ж–Є—О –∞–ї—М–±—Г–Љ–Є–љ–Њ–≤ —Б –Љ–Њ—З–Њ–є –Ї–∞–Ї —Г –±–Њ–ї—М–љ—Л—Е —Б –Р–У, —В–∞–Ї –Є —Г –ї–Є—Ж —Б –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ –Р–Ф. –Я—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–є –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ —Д—А–∞–Ї—Ж–Є—П —Д–Є–ї—М—В—А–∞—Ж–Є–Є –љ–µ –Є–Ј–Љ–µ–љ—П–µ—В—Б—П, –њ–Њ—З–µ—З–љ–Њ–µ —Б–Њ—Б—Г–і–Є—Б—В–Њ–µ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є–µ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П, –∞ –њ–Њ—З–µ—З–љ—Л–є –њ–ї–∞–Ј–Љ–Њ—В–Њ–Ї –Є —Б–Ї–Њ—А–Њ—Б—В—М –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є –Є–Љ–µ—О—В —В–µ–љ–і–µ–љ—Ж–Є—О –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О.
–Т–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —Г–Љ–µ–љ—М—И–∞—В—М —Н–Ї—Б–Ї—А–µ—Ж–Є—О –∞–ї—М–±—Г–Љ–Є–љ–Њ–≤ —Б –Љ–Њ—З–Њ–є —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 1 –Є 2 —В–Є–њ–Њ–≤, —Г –Ї–Њ—В–Њ—А—Л—Е –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є—П —П–≤–ї—П–µ—В—Б—П –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ —Б–Ї—А—Л—В–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є. –Т —А—П–і–µ –і–ї–Є—В–µ–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї —Б–љ–Є–ґ–∞–µ—В –Р–Ф –≤ —В–Њ–є –ґ–µ –Љ–µ—А–µ, —З—В–Њ –Є –≥–Є–і—А–Њ—Е–ї–Њ—А–Њ—В–Є–∞–Ј–Є–і, –∞—В–µ–љ–Њ–ї–Њ–ї, –Љ–µ—В–Њ–њ—А–Њ–ї–Њ–ї –Є–ї–Є –љ–Є—Д–µ–і–Є–њ–Є–љ–—А–µ—В–∞—А–і, –љ–Њ –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В —Н–Ї—Б–Ї—А–µ—Ж–Є—О –∞–ї—М–±—Г–Љ–Є–љ–Њ–≤ —Б –Љ–Њ—З–Њ–є (–≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 35–60%). –≠—В–Њ —П–≤–ї—П–µ—В—Б—П –љ–µ—Б–Њ–Љ–љ–µ–љ–љ—Л–Љ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–Њ–Љ –љ–∞–ї–Є—З–Є—П —Г –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —А–µ–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ–≥–Њ –Њ—В –µ–≥–Њ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–∞—А—П–і—Г —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Р–Ф –Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –Њ—Б–љ–Њ–≤–љ—Л—Е –Њ—А–≥–∞–љ–Њ–≤––Љ–Є—И–µ–љ–µ–є —Г –±–Њ–ї—М–љ—Л—Е –Р–У – —Б–µ—А–і—Ж–µ, —Б–Њ—Б—Г–і—Л –Є –њ–Њ—З–Ї–Є.
–Ъ–∞–Ї –Є –і—А—Г–≥–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –њ–Њ–≤—Л—И–∞–µ—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–Ї–∞–љ–µ–є –Ї –Є–љ—Б—Г–ї–Є–љ—Г, —З—В–Њ –і–µ–ї–∞–µ—В –µ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П –Р–У —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 2 —В–Є–њ–∞ –Є–ї–Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ.
–Ы–Є–Ј–Є–љ–Њ–њ—А–Є–ї, –Ї–∞–Ї –≥–Є–і—А–Њ—Д–Є–ї—М–љ–Њ–µ –≤–µ—Й–µ—Б—В–≤–Њ, –њ–ї–Њ—Е–Њ —А–∞—Б—В–≤–Њ—А—П–µ—В—Б—П –≤ –ґ–Є—А–∞—Е –Є –њ–Њ—Н—В–Њ–Љ—Г –љ–µ –љ–∞–Ї–∞–њ–ї–Є–≤–∞–µ—В—Б—П –≤ –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ–Є —З–µ–ї–Њ–≤–µ–Ї–∞. –Я–Њ—Н—В–Њ–Љ—Г –≤—Л—Б–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П –Љ–љ–µ–љ–Є–µ, —З—В–Њ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –±–Њ–ї–µ–µ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї–µ–љ, —З–µ–Љ –ї–Є–њ–Њ—Д–Є–ї—М–љ—Л–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§, –і–ї—П –ї–µ—З–µ–љ–Є—П –Р–У —Г –±–Њ–ї—М–љ—Л—Е —Б –Њ–ґ–Є—А–µ–љ–Є–µ–Љ.
–Т–ї–Є—П–љ–Є–µ –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –љ–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є —Г –љ–Њ—А–Љ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 1 —В–Є–њ–∞ (–°–Ф 1) –Є–Ј—Г—З–∞–ї–Њ—Б—М –≤ –Ї—А—Г–њ–љ–Њ–Љ –і–≤—Г—Е–ї–µ—В–љ–µ–Љ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є EUCLID [18,19]. –Ю–±–љ–∞—А—Г–ґ–µ–љ–Њ, —З—В–Њ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –≤ –і–Њ–Ј–µ 10–20 –Љ–≥/—Б—Г—В., –≤—Л–Ј—Л–≤–∞—П –љ–µ–±–Њ–ї—М—И–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф, –њ—А–Є–≤–Њ–і–Є—В –Ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ—Г —Г–Љ–µ–љ—М—И–µ–љ–Є—О —Н–Ї—Б–Ї—А–µ—Ж–Є–Є –∞–ї—М–±—Г–Љ–Є–љ–Њ–≤ —Б –Љ–Њ—З–Њ–є, –Ї–Њ—В–Њ—А–Њ–µ –±—Л–ї–Њ –љ–∞–Є–±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ —Г –±–Њ–ї—М–љ—Л—Е —Б –Є—Б—Е–Њ–і–љ–Њ–є –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є–µ–є (–≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 50%). –≠—В–Њ –Њ–Ј–љ–∞—З–∞–µ—В, —З—В–Њ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї —Б–њ–Њ—Б–Њ–±–µ–љ –Ј–∞–Љ–µ–і–ї–Є—В—М –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 1. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –Ј–∞–Љ–µ–і–ї—П–ї –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 1.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –і–ї–Є—В–µ–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –Љ–Њ–ґ–µ—В –Ј–∞–Љ–µ–і–ї—П—В—М —А–∞–Ј–≤–Є—В–Є–µ –Љ–Є–Ї—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 1, –њ—А–Є—З–µ–Љ –Ї–∞–Ї —Б –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ, —В–∞–Ї –Є —Б –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ –Р–Ф. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –њ–Њ –і–∞–љ–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П ALLHAT, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Б–љ–Є–ґ–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –љ–Њ–≤—Л—Е —Б–ї—Г—З–∞–µ–≤ —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ (–њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —Е–ї–Њ—А—В–∞–ї–Є–і–Њ–љ–Њ–Љ) [8].
–Т —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є BRILLIANT (1996) [7] –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 2 —В–Є–њ–∞ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї —Б–љ–Є–ґ–∞–µ—В –Р–Ф –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є, —З–µ–Љ –љ–Є—Д–µ–і–Є–њ–Є–љ–—А–µ—В–∞—А–і, –Є –≤—Л–Ј—Л–≤–∞–µ—В –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї—М—И–µ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —Н–Ї—Б–Ї—А–µ—Ж–Є–Є –∞–ї—М–±—Г–Љ–Є–љ–Њ–≤ —Б –Љ–Њ—З–Њ–є (–≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 40% –њ—А–Њ—В–Є–≤ 8%). –≠—В–Њ –Љ–Њ–ґ–µ—В —Б–ї—Г–ґ–Є—В—М –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–Њ–Љ, —З—В–Њ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –Є –і—А—Г–≥–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –±–Њ–ї–µ–µ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ—Л –і–ї—П –ї–µ—З–µ–љ–Є—П –Р–У —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 2 —В–Є–њ–∞.
–Т —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є TROPHY [9] –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б –Њ–ґ–Є—А–µ–љ–Є–µ–Љ –Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –Є –≥–Є–і—А–Њ—Е–ї–Њ—А–Њ—В–Є–∞–Ј–Є–і –≤ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є –Љ–µ—А–µ —Б–љ–Є–ґ–∞—О—В –Р–Ф, –Њ–і–љ–∞–Ї–Њ –Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§ –≥–Њ—А–∞–Ј–і–Њ —А–µ–ґ–µ –≤—Л–Ј—Л–≤–∞–µ—В —В–∞–Ї–Є–µ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л, –Ї–∞–Ї –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П –Є –≥–Є–њ–Њ–Ї–∞–ї–Є–µ–Љ–Є—П. –Ю—В–Љ–µ—З–µ–љ—Л –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П –≤ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –Є –≥–Є–і—А–Њ—Е–ї–Њ—А–Њ—В–Є–∞–Ј–Є–і–∞ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —А–∞—Б—Л –Є –≤–Њ–Ј—А–∞—Б—В–∞ –±–Њ–ї—М–љ—Л—Е. –Ґ–∞–Ї, –±–µ–ї—Л–µ –±–Њ–ї—М–љ—Л–µ –ї—Г—З—И–µ —А–µ–∞–≥–Є—А–Њ–≤–∞–ї–Є –љ–∞ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї (43% –њ—А–Њ—В–Є–≤ 20% –љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Њ—В–Є–∞–Ј–Є–і–µ), —В–Њ–≥–і–∞ –Ї–∞–Ї –љ–µ–≥—А—Л – –ї—Г—З—И–µ –љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Њ—В–Є–∞–Ј–Є–і (52% –њ—А–Њ—В–Є–≤ 33% –љ–∞ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–µ). –£ –Љ–Њ–ї–Њ–і—Л—Е –±–Њ–ї—М–љ—Л—Е (–љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В —А–∞—Б—Л) –ї—Г—З—И–µ –±—Л–ї–∞ —А–µ–∞–Ї—Ж–Є—П –љ–∞ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї (46% –њ—А–Њ—В–Є–≤ 15% –љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Њ—В–Є–∞–Ј–Є–і–µ). –£ –±–Њ–ї—М–љ—Л—Е 40 –ї–µ—В –Є —Б—В–∞—А—И–µ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –Є –≥–Є–і—А–Њ—Е–ї–Њ—А–Њ—В–Є–∞–Ј–Є–і–∞ –±—Л–ї–Є –Њ–і–Є–љ–∞–Ї–Њ–≤—Л–Љ–Є.
–Ы–Є–Ј–Є–љ–Њ–њ—А–Є–ї –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є
–Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —Б—З–Є—В–∞—О—В—Б—П –Њ–±—П–Ј–∞—В–µ–ї—М–љ—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–є —В–µ—А–∞–њ–Є–Є –•–°–Э, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –Ы–Ц. –Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–є –Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –љ–∞–Ј–љ–∞—З–∞—В—М –≤—Б–µ–Љ –±–Њ–ї—М–љ—Л–Љ –•–°–Э (–Њ—В I –і–Њ IV —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞—Б—Б–∞). –Я—А–Є —Н—В–Њ–Љ —Б–ї–µ–і—Г–µ—В –Є–Љ–µ—В—М –≤ –≤–Є–і—Г, —З—В–Њ –≤—Б–µ–≥–Њ –ї–Є—И—М –Њ 5 –Є–љ–≥–Є–±–Є—В–Њ—А–∞—Е –Р–Я–§ –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Њ–љ–Є —Б–њ–Њ—Б–Њ–±–љ—Л —Б–љ–Є–ґ–∞—В—М —Б–Љ–µ—А—В–љ–Њ—Б—В—М –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л–Љ –•–°–Э, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –Ы–Ц. –Ю–і–Є–љ –Є–Ј —В–∞–Ї–Є—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ —Б –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О – –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї. –Ф—А—Г–≥–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –ї–Є–±–Њ –≤–Њ–≤—Б–µ –љ–µ –Є–Ј—Г—З–∞–ї–Є—Б—М –≤ –Ї—А—Г–њ–љ—Л—Е –Є –і–ї–Є—В–µ–ї—М–љ—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, –ї–Є–±–Њ —А–µ–Ј—Г–ї—М—В–∞—В—Л —Н—В–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤—Л–Љ–Є. –Я–Њ —Б–≤–Њ–і–љ—Л–Љ –і–∞–љ–љ—Л–Љ 4 –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ—А–Є –•–°–Э –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї —Б–љ–Є–ґ–∞–µ—В —Б–Љ–µ—А—В–љ–Њ—Б—В—М –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 38% (—В–∞–±–ї. 3) [7].
–Т —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є ATLAS [20] –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞, —З—В–Њ –≤—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ —Г–ї—Г—З—И–∞—О—В –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М –±–Њ–ї—М–љ—Л—Е –•–°–Э, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –Ы–Ц, —З–µ–Љ –љ–Є–Ј–Ї–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞. –Т —Н—В–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б—А–∞–≤–љ–Є–≤–∞–ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ–Є–Ј–Ї–Є–Љ–Є –Є –≤—Л—Б–Њ–Ї–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —Г 3164 –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э II–IV —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –Ї–ї–∞—Б—Б–Њ–Љ (–§–Ъ) –Є —Д—А–∞–Ї—Ж–Є–µ–є –≤—Л–±—А–Њ—Б–∞ –Ы–Ц –љ–µ –±–Њ–ї–µ–µ 30%. –Ф–Њ —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є–Є –≤—Б–µ –±–Њ–ї—М–љ—Л–µ –≤ —В–µ—З–µ–љ–Є–µ 2–4 –љ–µ–і–µ–ї—М –њ–Њ–ї—Г—З–∞–ї–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –≤ –і–Њ–Ј–µ 12,5–15 –Љ–≥/—Б—Г—В. –Я–Њ—Б–ї–µ —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є–Є –≤ –Њ–і–љ–Њ–є –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е –і–Њ–Ј—Г –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Є –і–Њ 32,5–35 –Љ–≥/—Б—Г—В., –∞ –≤ –і—А—Г–≥–Њ–є – —Г–Љ–µ–љ—М—И–∞–ї–Є –і–Њ 2,5–5 –Љ–≥/—Б—Г—В. –Э–∞–±–ї—О–і–µ–љ–Є–µ –Ј–∞ –±–Њ–ї—М–љ—Л–Љ–Є –њ—А–Њ–і–Њ–ї–ґ–∞–ї–Њ—Б—М –Њ—В 39 –і–Њ 56 –Љ–µ—Б.
–С–Њ–ї–µ–µ 90% –±–Њ–ї—М–љ—Л—Е —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є–ї–Є –≤—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞. –Р—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–Њ—В–Њ–љ–Є—П –Є –љ–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —З–∞—Й–µ –≤—Б—В—А–µ—З–∞–ї–Є—Б—М –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –≤—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞. –І–∞—Б—В–Њ—В–∞ –і—А—Г–≥–Є—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е —Б—А–∞–≤–љ–Є–≤–∞–µ–Љ—Л—Е –≥—А—Г–њ–њ –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–∞—Б—М.
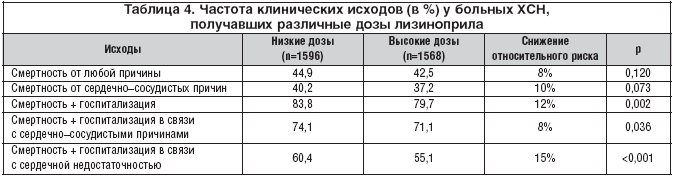
–Ч–∞ –≤—А–µ–Љ—П –љ–∞–±–ї—О–і–µ–љ–Є—П –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –≤—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞, –љ–∞–±–ї—О–і–∞–ї–∞—Б—М –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–∞—П —Б–Љ–µ—А—В–љ–Њ—Б—В—М –Њ—В –≤—Б–µ—Е –њ—А–Є—З–Є–љ (–љ–∞ 8%; —А=0,126) –Є —Б–Љ–µ—А—В–љ–Њ—Б—В—М –Њ—В —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ—А–Є—З–Є–љ (–љ–∞ 10%; —А=0,068). –Ю–±—Й–µ–µ —З–Є—Б–ї–Њ —Б–ї—Г—З–∞–µ–≤ —Б–Љ–µ—А—В–Є –Є –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –±—Л–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Љ–µ–љ—М—И–µ –≤ –≥—А—Г–њ–њ–µ –ї–µ—З–µ–љ–љ—Л—Е –≤—Л—Б–Њ–Ї–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –±–Њ–ї—М–љ—Л–Љ–Є, –њ–Њ–ї—Г—З–∞–≤—И–Є–Љ–Є –љ–Є–Ј–Ї–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ (–љ–∞ 12%; —А=0,002) (—В–∞–±–ї. 4).
–Ю—Б–Њ–±–µ–љ–љ–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ –±—Л–ї–Њ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П —Б–Љ–µ—А—В–Є —Г –±–Њ–ї—М–љ—Л—Е –•–°–Э II –§–Ъ. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —Г –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э IV –§–Ъ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤—Л—Б–Њ–Ї–Є—Е –Є –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –±—Л–ї–∞ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ, —Н—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б —В–µ–Љ, —З—В–Њ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е –•–°–Э IV –§–Ъ –≤–Љ–µ—Б—В–Њ –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –≤—А–∞—З–Є –≤—Л–љ—Г–ґ–і–µ–љ—Л –±—Л–ї–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Б—А–µ–і–љ–Є–µ –Є –≤—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞. –Т—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞–ї–Є —Б–Љ–µ—А—В—М —Г –ї–Є—Ж –Љ–Њ–ї–Њ–ґ–µ 70 –ї–µ—В –Є –Љ—Г–ґ—З–Є–љ. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —Г –ї–Є—Ж —Б—В–∞—А—И–µ 70 –ї–µ—В –Є –ґ–µ–љ—Й–Є–љ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤—Л—Б–Њ–Ї–Є—Е –Є –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –±—Л–ї–∞ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є.
–Ґ–µ—А–∞–њ–Є—П –≤—Л—Б–Њ–Ї–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –њ—А–Є–≤–µ–ї–∞ –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –≤ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ —Б–≤—П–Ј–Є —Б –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–µ–є –•–°–Э –Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Њ–±—Л—В–Є—П–Љ–Є (—В–∞–±–ї. 5). –Ґ–∞–Ї, —З–Є—Б–ї–Њ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –≤ —Б–≤—П–Ј–Є —Б –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–µ–є –•–°–Э —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 24% (—А=0,002), –∞ —З–Є—Б–ї–Њ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –≤ —Б–≤—П–Ј–Є —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Њ–±—Л—В–Є—П–Љ–Є – –љ–∞ 20% (—А=0,085). –Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –Ј–∞—В—А–∞—В—Л –љ–∞ –ї–µ—З–µ–љ–Є–µ –±–Њ–ї—М–љ–Њ–≥–Њ –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ —Б–Њ—Б—В–∞–≤–ї—П—О—В –±–Њ–ї—М—И—Г—О —З–∞—Б—В—М –≤—Б–µ—Е —А–∞—Б—Е–Њ–і–Њ–≤ –љ–∞ –ї–µ—З–µ–љ–Є–µ –±–Њ–ї—М–љ—Л—Е –•–°–Э. –Я–Њ—Н—В–Њ–Љ—Г –і–∞–љ–љ—Л–µ –Њ —Б–љ–Є–ґ–µ–љ–Є–Є –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є –±–Њ–ї—М–љ—Л—Е –•–°–Э –≤ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є ATLAS, –Љ–Њ–≥—Г—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М—Б—П, –Ї–∞–Ї –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞ —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Њ–є –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ —Г –±–Њ–ї—М–љ—Л—Е –•–°–Э, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–Њ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –Ы–Ц.
–Я—А–Є–Љ–µ—А–љ–Њ —Г 20% –±–Њ–ї—М–љ—Л—Е –•–°–Э, —Г—З–∞—Б—В–≤–Њ–≤–∞–≤—И–Є—Е –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є ATLAS, –Є–Љ–µ–ї—Б—П —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В. –Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –Њ—В–і–∞–ї–µ–љ–љ—Л–є –њ—А–Њ–≥–љ–Њ–Ј —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –±—Л–ї —Е—Г–ґ–µ, —З–µ–Љ —Г –±–Њ–ї—М–љ—Л—Е –±–µ–Ј –љ–µ–≥–Њ. –°—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –≤—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —Г–ї—Г—З—И–∞–ї–Є –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є, —З–µ–Љ —Г –±–Њ–ї—М–љ—Л—Е –±–µ–Ј –і–Є–∞–±–µ—В–∞: —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –љ–∞ 14% —Г –њ–µ—А–≤—Л—Е –Є –љ–∞ 6% —Г –≤—В–Њ—А—Л—Е. –І–Є—Б–ї–Њ –і–љ–µ–є –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –≤ —Б–≤—П–Ј–Є —Б —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –≤ –њ–Њ–і–≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –±—Л–ї–Њ –љ–∞ 27% –Љ–µ–љ—М—И–µ —Б—А–µ–і–Є –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –≤—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§, —З–µ–Љ —Б—А–µ–і–Є –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –љ–Є–Ј–Ї–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞. –Я–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –≤—Л—Б–Њ–Ї–Є—Е –Є –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –≤ —Ж–µ–ї–Њ–Љ –±—Л–ї–∞ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –Є –±–µ–Ј –љ–µ–≥–Њ, —Е–Њ—В—П –≤ –Њ–±–µ–Є—Е –њ–Њ–і–≥—А—Г–њ–њ–∞—Е –±–Њ–ї—М–љ—Л—Е –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–∞—П —З–∞—Б—В–Њ—В–∞ –≥–Є–њ–Њ—В–Њ–љ–Є–Є, –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є—П, –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї –Є –≥–Є–њ–µ—А–Ї–∞–ї–Є–µ–Љ–Є–Є —Б—А–µ–і–Є –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –≤—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ (–Њ—Б–Њ–±–µ–љ–љ–Њ —Г –±–Њ–ї—М–љ—Л—Е 70 –ї–µ—В –Є —Б—В–∞—А—И–µ).
–°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–Є—В—М –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –±–Њ–ї—М–љ—Л—Е –•–°–Э –≤ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є (–љ–∞ 24%). –Т –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –Њ–љ–Є —Б–љ–Є–ґ–∞—О—В —А–Є—Б–Ї —Б–Љ–µ—А—В–Є (–≤ —Б—А–µ–і–љ–µ–Љ –≤—Б–µ–≥–Њ –љ–∞ 8%, –∞ —Г –±–Њ–ї—М–љ—Л—Е –±–µ–Ј —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ – –љ–∞ 6%). –Я—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§, –њ–Њ––≤–Є–і–Є–Љ–Њ–Љ—Г, –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–Њ —Г –±–Њ–ї—М–љ—Л—Е –•–°–Э II –§–Ъ –Є –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–Љ —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ.
–Ы–Є–Ј–Є–љ–Њ–њ—А–Є–ї –њ–Њ—Б–ї–µ –Њ—Б—В—А–Њ–≥–Њ
–Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞
–£ 70% –±–Њ–ї—М–љ—Л—Е –•–°–Э –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ –Є–Љ–µ—О—В—Б—П —Г–Ї–∞–Ј–∞–љ–Є—П –љ–∞ –Њ—Б—В—А—Л–є –Ш–Ь. –Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –•–°–Э —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —Б–њ—Г—Б—В—П –±–Њ–ї–µ–µ –Є –Љ–µ–љ–µ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–µ –≤—А–µ–Љ—П –њ–Њ—Б–ї–µ —А–∞–Ј–≤–Є—В–Є—П —В—А–∞–љ—Б–Љ—Г—А–∞–ї—М–љ–Њ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞. –Я–Њ—П–≤–ї–µ–љ–Є—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –њ—А–µ–і—И–µ—Б—В–≤—Г–µ—В –њ–Њ—Б—В–Є–љ—Д–∞—А–Ї—В–љ–Њ–µ —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є–µ –Ы–Ц, –Ї–Њ—В–Њ—А–Њ–µ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –і–Є–ї–∞—В–∞—Ж–Є–µ–є –µ–≥–Њ –њ–Њ–ї–Њ—Б—В–Є, –Є–Ј–Љ–µ–љ–µ–љ–Є—П –µ–≥–Њ –≥–µ–Њ–Љ–µ—В—А–Є–Є –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–Є–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞.
–°–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –Њ—Б–ї–∞–±–ї—П—В—М —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є–µ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ –њ—А–Є –•–°–Э –њ–Њ–Ј–≤–Њ–ї–Є–ї–∞ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –±–Њ–ї—М–љ—Л–Љ –Њ—Б—В—А—Л–Љ –Є–љ—Д–∞—А–Ї—В–Њ–Љ –Љ–Є–Њ–Ї–∞—А–і–∞ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є. –Т –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –Є–Ј—Г—З–∞–ї–∞—Б—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –≤ –Њ—Б—В—А–Њ–Љ –њ–µ—А–Є–Њ–і–µ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞. –Ю–і–љ–Є–Љ –Є–Ј —В–∞–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –±—Л–ї–Њ GISSI–3 [21,22], –≤ –Ї–Њ—В–Њ—А–Њ–Љ —Г 19 394 –±–Њ–ї—М–љ—Л—Е –Њ—Б—В—А—Л–Љ –Є–љ—Д–∞—А–Ї—В–Њ–Љ –Љ–Є–Њ–Ї–∞—А–і–∞ –Є–Ј—Г—З–∞–ї–∞—Б—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞. –Ґ–µ—А–∞–њ–Є—О –љ–∞—З–Є–љ–∞–ї–Є –≤ –њ–µ—А–≤—Л–µ 24 —З–∞—Б–∞ –Њ—Б—В—А–Њ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –Є –њ—А–Њ–і–Њ–ї–ґ–∞–ї–Є –≤ —В–µ—З–µ–љ–Є–µ 6 –љ–µ–і–µ–ї—М.
–°—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е, –ї–µ—З–µ–љ–љ—Л—Е –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ, 6––љ–µ–і–µ–ї—М–љ–∞—П —Б–Љ–µ—А—В–љ–Њ—Б—В—М –±—Л–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–Є–ґ–µ (–љ–∞ 11%), —З–µ–Љ —Б—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е, –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ (—А=0,05). –Т –њ–µ—А–≤—Л–µ —Б—Г—В–Ї–Є —В–µ—А–∞–њ–Є–Є —Б–Љ–µ—А—В–љ–Њ—Б—В—М –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї, —Б–љ–Є–Ј–Є–ї–∞—Б—М –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 40%, —З—В–Њ —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –≤–∞–ґ–љ–Њ—Б—В—М —А–∞–љ–љ–µ–≥–Њ –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ —Г –±–Њ–ї—М–љ—Л—Е —Б –Ш–Ь. –Я–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї, –љ–∞–Ј–љ–∞—З–∞–µ–Љ—Л–є –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –Њ—Б—В—А–Њ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞, –њ–Њ –і–∞–љ–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П GISSI–3, –Њ–Ї–∞–Ј–∞–ї—Б—П –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ, —З–µ–Љ –і—А—Г–≥–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ (—В–∞–±–ї. 6).
–Э–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –±—Л–ї–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–Љ —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ, —Г –Ї–Њ—В–Њ—А—Л—Е —Б–Љ–µ—А—В–љ–Њ—Б—В—М —Б–љ–Є–Ј–Є–ї–∞—Б—М –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 32%. –°–љ–Є–ґ–µ–љ–Є–µ 6––љ–µ–і–µ–ї—М–љ–Њ–є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ —Б–Њ—Б—В–∞–≤–Є–ї–Њ –≤ —Б—А–µ–і–љ–µ–Љ 27% —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 1 —В–Є–њ–∞ –Є 44% —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 2 —В–Є–њ–∞.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї —П–≤–ї—П–µ—В—Б—П –≤—Л—Б–Њ–Ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ –Р–Я–§ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Ї–Њ—В–Њ—А–Њ–≥–Њ –љ–∞ —В–µ—З–µ–љ–Є–µ –Є –Є—Б—Е–Њ–і—Л –Р–У, —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞, –•–°–Э –Є –Њ—Б—В—А–Њ–≥–Њ –Ш–Ь —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ—Л –≤ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–∞ –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ–Њ–Љ —Д–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–Њ–Љ —А—Л–љ–Ї–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї –Ї–Њ–Љ–њ–∞–љ–Є–Є «–Т—С—А–≤–∞–≥ –§–∞—А–Љ–∞» – –Ы–Є–Ј–Є–≥–∞–Љ–Љ–∞®. –Я—А–µ–њ–∞—А–∞—В –Њ–±–ї–∞–і–∞–µ—В –≤—Б–µ–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є –≤—Л—Б–Њ–Ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Є–Р–Я–§ –Є –Љ–Њ–ґ–µ—В —И–Є—А–Њ–Ї–Њ –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –≤ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ.





–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Opie L. H. Angiotensin converting enzyme inhibitors. 3th edition. – New York, 1999.
2. Brunner H.R., Waeber B., Nussberger J. Angiotensin-converting enzyme inhibitors. – In: Messerli F. (ed.) Cardiovascular drug therapy. 2th edition. – Philadelphia, 1996. – pp. 690—711.
3. –°–Є–і–Њ—А–µ–љ–Ї–Њ –С.–Р., –Я—А–µ–Њ–±—А–∞–ґ–µ–љ—Б–Ї–Є–є –Ф.–Т. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ-–њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞. – –Ь–Њ—Б–Ї–≤–∞, 1998.
4. –°–Є–і–Њ—А–µ–љ–Ї–Њ –С.–Р., –Я—А–µ–Њ–±—А–∞–ґ–µ–љ—Б–Ї–Є–є –Ф.–Т., –С–∞—В—Л—А–∞–ї–Є–µ–≤ –Ґ.–Р. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –Є –Р–Ґ1-–±–ї–Њ–Ї–∞—В–Њ—А—Л –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ. –І–∞—Б—В—М —В—А–µ—В—М—П. – –Ь–Њ—Б–Ї–≤–∞, 2004.
5. –Я—А–µ–Њ–±—А–∞–ґ–µ–љ—Б–Ї–Є–є –Ф.–Т., –°–Є–і–Њ—А–µ–љ–Ї–Њ –С.–Р., –С–∞—В—Л—А–∞–ї–Є–µ–≤ –Ґ.–Р. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ-–њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞. – –Ь–Њ—Б–Ї–≤–∞, 2007.
6. Kostis J. B., Sginddler Lisinopril – In: Messerli F. (ed.) Cardiovascular drug therapy. 2th edition. – Philadelphia, 1996. – pp. 750—755.
7. Goa K. L., Hatua M., Wilde M. I. Lisinopril. A review of its pharmacology and use in the management of the complications of diabetes mellitus. – Drugs, 1997; 53 (6): 1081—1105.
8. The ALLHAT officers and coordinators for the ALLHAT collaborative research group. Mayor outcomes in high-risk hypertensive randomized to angiotensin-converting enzyme inhibitor or calcium channel blocker vs diuretic. – JAMA, 2002; 288: 2981—2997.
9. Weir M. R., Reisin E., Falkner B. Noctural reduction of blood pressure and the antihypertensive response to a diuretic or angiotensin-converting enzyme inhibitor in obese hypertension patients. TROPHY study group. – Amer. J. Hypertension, 1998; 11: 914—920.
10. Malacco E., Santonastaso M., Van N. A. et al. Comparison of valsartan 160 mg with lisinopril 20 mg given as monotherapy or in combination with diuretic for the treatment: the Blood Pressure Reduction and Tolerability of Valsartan in Comparison with Lisinopril (PREVAL). – Clin. Ther., 2004; 26: 855—865.
11. Rosei E. A., Rizzoni D., Comini S. et al. Evaluation of the efficacy and tolerability of nebivolol versus lisinopril in the treatment essential arterial hypertension: a randomized, multicentre, double-blind study. – Blood Pressure, 2003; supplement: 30—35.
12. Terpstra W. F., May J. F., Smit A. J. et al. Long-term effects of amlodipine and lisinopril on left ventricular mass and diastolic function in elderly, previous untreated hypertensive patients; the ELVERA trial. – J. Hypertension, 2001; 19: 303—309. 02: ,e ril
13. –¶–≤–µ—В–Ї–Њ–≤–∞ –Ю.–Р. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞. – –†–Ь–Ц, 2007; 14: 3—7.
14. Meredith P.A. Role of through to peak efficacy in the evaluation of antihypertensive efficacy – J. Hypertension, 1998; 16 (suppl. 1): S59-S64.
15. Zannad F., Matzinger A., Larche J. Through/peak rations of once daily angiotensin-converting enzyme inhibitors and calcium antagonists. — Amer. J. Hypertension, 1996; 9: 633-643.
16. Skolnik A. A. Lisinopril but not losartan boosts myocardial perfusion in hypertensives with left ventricular hypertrophy. – JAMA, 2002; 40: 703—709.
17. Rizzoni D., Muiesan M.L., Porteri E. et al. Effects of long-term antihypertensive treatment with lisinopril on resistance arteries in hypertensive patients with left ventricular hypertrophy. – J. Hypertension, 1997; 15: 197—204.
18. The EUCLID study group. Randomized placebo-controlled trial of lisinopril of normotensive patients with insulin-dependent diabetes and normoalbuminuria or microalbuminuria. – Lancet, 1997; 349: 1787—1792.
19. Chaturvedi N., Sjolie A.-K., Stephenson J. M. et al. Effect of lisinopril on progression of retinopathy in normotensive people with type 1 diabetes. – Lancet, 1998; 351: 28—31.
20. Packer M., Poole-Wilson P.A., Armstrong P. W. et al. Comparative effects of low and high doses of the angiotensin-converting enzyme inhibitor, lisinopril, on morbidity and mortality in chronic heart failure. – Circulation, 1999; 100: 2312—2318.
21. Gruppo Italiano per lo Studio della Sopravvivenza nel’Infarto miocardico-3. GISSI-3: Effects of lisinopril and transdermal glyceryl trinitate singly and together on 6-week mortality and ventricular function after myocardial infarction. – Lancet, 1994; 343: 1115—1122.
22. Zuanetti Z., Latini R., Maggioni A. P. et al. Effect of the ACE inhibitor lisinopril on mortality in diabetic patients with acute myocardial infarction. Data from the GISSI-3 study. – Circulation, 1997; 96: 4239—4245.












