Диуретики зарекомендовали себя как высокоэффективные гипотензивные препараты во многих исследованиях: ALLHAT [1], TOMHS [2], SHEP [3], LIVE [4], STOP [5], MRC [6], NESTOR [7] и др.
Значительно дольше других антигипертензивных препаратов используются тиазидные диуретики – с конца 50–х гг. прошлого века. Так, в 1956 г. был синтезирован первый пероральный тиазидный диуретик – хлортиазид. В 1957 г. был создан гидрохлоротиазид, который быстро вытеснил хлортиазид из клинической практики. В 1959 г. появился тиазидоподобный диуретик хлорталидон, a в 1974 г. – индапамид.
В 1988 г. был создан торасемид. Как убедительно продемонстрировали результаты многоцентровых испытаний, этот препарат существенно отличается от предшественников по ключевым клинико–фармакологическим характеристикам эффективности и безопасности. Одним из важных отличий торасемида является его антиальдостероновый эффект, который был доказан в ряде исследований [8,9]. Синтез препарата с дополнительным свойством антагониста альдостерона был актуален, т.к. современная волна интереса к применению антагонистов альдостерона началась в конце 1990–х гг. у пациентов с хронической сердечной недостаточностью (ХСН) в связи со значительным улучшением прогноза таких больных (снижение смертности, частоты госпитализаций и выраженности симптоматики) в контролируемом клиническом исследовании RALES [10].
Учитывая, что альдостерон способствует развитию фиброза миокарда, истощению калия, активации симпатической и торможению парасимпатической нервной системы, а также дисфункции барорецепторов [11–13], антиальдостероновые свойства торасемида могут оказывать благоприятное воздействие на состояние больных с АГ.
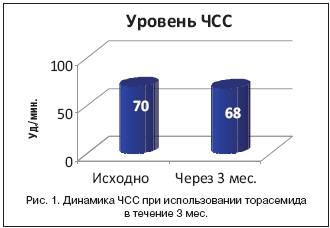
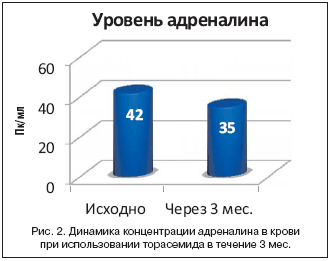
Традиционно одним из значимых недостатков использования тиазидных и петлевых диуретиков считалась избыточная активация ренин–ангиотензин–альдостероновой системы (РААС). Торасемид лишен данного недостатка. Так, в исследовании K. Harada и соавт. [14] было показано, что прием торасемида в дозе 8 мг/сут. на протяжении 3 мес. не вызывал значимого повышения уровня норадреналина, а уровень адреналина даже снижался с 42 до 35 пк/мл. При этом не наблюдалось изменения частоты сердечных сокращений (70 уд./мин. до исследования и 68 уд./ мин. – по окончании исследования) (рис. 1 и 2).
Торасемид лишен важного недостатка, присущего некоторым диуретикам, – его применение не сопровождается развитием синдрома «рикошета». Так, прием фуросемида 1 р./сут. вызывает повышенную экскрецию натрия и воды во время диуреза, а затем сменяется задержкой натрия и воды в остальное время суток. В результате этого суточная экскреция натрия и воды может увеличиваться незначительно, если только короткодействующие диуретики не назначаются в высоких дозах или 2 р./сут. В основе данного феномена «рикошета» лежат несколько внутри– и внепочечных компенсаторно–приспособительных механизмов, направленных на поддержание водно–электролитного баланса в условиях недостаточного поступления натрия хлорида в организм, и в частности активация РААС. Торасемид в отличие от других диуретиков обладает дополнительным положительным эффектом в виде блокады РААС [15,16].
У пациентов с АГ в условиях стойкой гиперактивации РААС существенно возрастает активность альдостерона как фактора, обусловливающего задержку натрия и осмотически связанной воды. Помимо этого, избыточная продукция альдостерона всегда обусловливает значительное увеличение темпа ремоделирования органов–мишеней и связанное с этим нарастание риска сердечно–сосудистых осложнений. Уникальное свойство торасемида блокировать альдостероновые рецепторы [20] стало одним из определяющих в успешности его применения как при ХСН, так и при АГ. Для лечения ХСН торасемид в дозе от 5 до 20 мг/сут. является эффективным диуретиком. В субдиуретических дозах (2,5–5 мг/сут.) торасемид используется при лечении эссенциальной АГ как в качестве монотерапии, так и в комбинации с другими антигипертензивными препаратами. Так, в мультицентровом проспективном открытом исследовании A. Coca [17] приняли участие 5102 пациента с вновь выявленной АГ или не достигшие целевых значений АД на монотерапии недиуретическими препаратами. Через 6 мес. терапии торасемидом снижение систолического АД составило 22,1 мм рт.ст. (p<0,001), а диаcтолического АД – 14,1 мм рт.ст. (p<0,001).
Для практических врачей особенно интересен факт снижения диастолического АД до уровня ниже 90 мм рт.ст. у 70–80% больных [18] при использовании торасемида в этих дозах.
Снижение интенсивности ангиотензин II–AT I–сигнализации и стимуляция активности Na+/Са2+–насоса происходят посредством угнетения Na+–2Cl––K+–котранспортной системы, что снижает цитозольную активность Na+. В отличие от других петлевых диуретиков, которые тоже ингибируют Na+–2Cl––K+–котранспортную систему, торасемид по структуре сходен с блокатором Cl––каналов. Также торасемид имеет большее сродство, чем фуросемид, к Na+–2Cl––K+–котранспортной системе. Недавно было описано, что ангиотензин II стимулирует открытие Cl––каналов, что приводит к деполяризации мембраны. Этот процесс приводит к открытию Са2+–каналов, а значительно возрастающая концентрация Са2+–приводит к вазоспазму. Торасемид подавляет открытие Cl––каналов. Наличие дополнительного угнетения Cl––каналов у торасемида, по сравнению с фуросемидом, объясняет более мощный вазодилатационный эффект торасемида. Это объясняется тем, что вторая фаза входа Са2+ в клетку связана с открытием Cl– каналов. Блокирование обоих фаз входа Са2+ приводит в значимому противодействию вазоконстрикции [19,20]. Дополнительно описана способность торасемида повышать цГМФ в стенке сосуда и стимулировать повышение секреции простациклина в эндотелии сосудов, что приводит к дополнительной вазодилатации и обеспечивает устойчивый антигипертензивный эффект.
В настоящее время имеются неоспоримый экспериментальный и клинический опыт, результаты крупных сравнительных исследований, ставящих торасемид в первые ряды выбора при фармакотерапии АГ и ХСН. Снижение интенсивности связывания альдостерона со специфическими рецепторами и уменьшение экскреции калия показаны [21] на гипертензивных крысах при применении торасемида, но не фуросемида; торасемид подавляет секрецию альдостерона в культуре клеток клубочкового слоя коры надпочечников различных млекопитающих [22].
В клинике достоверное увеличение концентрации альдостерона в сыворотке крови больных с ХСН регистрировалось под действием торасемида, но не фуросемида [23], что объяснено с позиций механизма отрицательной обратной связи, активирующегося в условиях блокады альдостероновых рецепторов торасемидом.
В исследование Х.Х. Шугушева [24] были включены больные с ХСН III–IV функционального класса (NYHA), осложнявшей течение ИБС. В качестве диуретической терапии одна группа больных получала фуросемид в дозе 20–60 мг/сут., вторая группа – торасемид 5–20 мг/сут. Авторы полагают, что снижение частоты желудочковых нарушений ритма сердца в исследуемой группе торасемида связано с отсутствием неблагоприятного влияния на электролитный состав [15], a также со способностью снижать активность РААС.
Известно также, что альдостерон потенцирует нежелательные последствия гиперактивации симпатической нервной системы, увеличивая захват катехоламинов клетками–мишенями, например кардиомиоцитами, и одновременно угнетая функцию парасимпатической нервной системы, ее участие в реализации барорефлекса [25]. Снижение показателей ВРС и смещение вегетативного баланса в сторону преобладания симпатических влияний при лечении фуросемидом, возрастание эктопической активности желудочков, по–видимому, связаны с его побочным эффектом, проявляющимся активацией РААС [16], в частности, повышением ренина плазмы, электролитными нарушениями.
Для практического врача важно знать, что у торасемида отсутствует проаритмогенный эффект, свойственный индапамиду. Известно, что индапамид может удлинять интервал Q–T и предрасполагать к развитию желудочковой тахикардии типа «пируэт», что указывается в инструкции к этому препарату [26] и объясняется исследователями его способностью тормозить активность калиевых каналов в мембранах кардиомиоцитов. Функция мембранных калиевых каналов особенно нарушается у больных, страдающих сахарным диабетом и застойной сердечной недостаточностью [27], следовательно, для данной категории пациентов особенно опасно удлинение интервала Q–T под влиянием индапамида в плане развития желудочковых аритмий.
Потенциально аритмогенное действие индапамида может проявляться при его совместном применении с препаратами из других клинико–фармакологических групп, которые также могут удлинять интервал Q–T. Поэтому при лечении индапамидом необходимо следить не только за содержанием калия в крови, но и за изменениями интервала Q–T, по крайней мере в начале лечения, что усложняет терапию и делает ее более дорогостоящей. Торасемид не инициирует рост плазменной концентрации самого агрессивного проаритмогенного медиатора – норадреналина, что выгодно отличает его от представителя того же подкласса диуретиков – азосемида [28].
Как известно, избыточный тонус симпатической нервной системы детерминирует не только АГ, но и прогрессирование ХСН. Устранением эффектов альдостерона во многом объясняется продемонстрированное в экспериментальных и клинических исследованиях торможение миокардиального фиброза при применении торасемида. Так, B. Lopez и соавт. [29] выполнили морфологическое исследование ткани миокарда межжелудочковой перегородки, полученной при биопсии у пациентов с ХСН II–IV функционального класса (NYHA). У пациентов, принимавших торасемид, было выявлено достоверное уменьшение экспрессии проколлагена I типа (PIP), маркера синтеза коллагена при сохранении скорости распада коллагена, характеризующегося постоянной концентрацией карбокситерминального телопептида проколлагена I типа (CITP). В последующем авторами было установлено, что прием торасемида сопровождается угнетением карбокситерминальной протеиназы проколлагена типа I – фермента, непосредственно участвующего в метаболическом каскаде, обусловливающем внеклеточное накопление коллагена I типа в миокарде, активируемое, в том числе, избытком альдостерона [30]. На одной из экспериментальных моделей ХСН P.T. Veeraveedu и соавт. [21] показали уменьшение площади индуцируемого избытком альдостерона миокардиального фиброза, экспрессии профиброгенного моноцитарного хемоаттрактантного протеина 1 типа (МСР–1), коллагена III типа и альдостеронсинтазы в миокарде левого желудочка под действием торасемида, но не фуросемида. Устранение тканевых эффектов альдостерона, очевидно, во многом позволяет объяснить положительное влияние торасемида на долгосрочный прогноз больных с ХСН и его способность уменьшать выраженность миокардиального ремоделирования.
Положительное влияние на ремоделирование показано в работе Е.Е. Аверина [31]. При добавлении к комбинированной терапии больных препарата Диувер через 2 года лечения произошло не только достоверно большее снижение индекса массы миокарда левого желудочка, но и изменение типов ремоделирования, выражающееся улучшением геометрии левого желудочка.
Торасемид уменьшает конечный диастолический и систолический диаметр левого желудочка [32] и индекс массы миокарда левого желудочка [31]. Способность торасемида предупреждать нарастание нарушений сократительной функции миокарда левого желудочка при ХСН подтверждало также уменьшение плазменной концентрации мозгового натрийуретического пептида [32].
Предупреждение последствий взаимодействия альдостерона с эпителиоцитами с рецепторами главных клеток собирательных трубочек предопределяет значительно меньшее, по сравнению с другими диуретиками, влияние торасемида на экскрецию калия с мочой. В исследовании TORIC [33] частота гипокалиемии, отмеченная при применении торасемида, оказалась достоверно ниже, чем при использовании фуросемида. В низких дозах торасемид оказывает длительное антигипертензивное действие, незначительно влияя на содержание калия в крови и показатели пуринового, углеводного и липидного метаболизма. Благодаря этому он в отличие от петлевых диуретиков первого поколения может более безопасно использоваться для длительного лечения АГ [14,17,34].
Все новые руководства отмечают необходимость назначения комбинированной терапии большинству пациентов с АГ. У практического врача не должно быть колебаний при назначении диуретиков больным с АГ – этот класс препаратов необходим большинству из них, а особенно «проблемным» пациентам: в сочетании с ХСН, при резистентной гипертензии [34–36]. Однако «классические» тиазидные диуретики в ряде ситуаций могут создать ненужные сложности как для врача, так и для пациента. И в этой ситуации необходимо понять, что существующие ограничения (метаболические проблемы и снижение уровня калия при применении тиазидных диуретиков) пододвигают нас к решению проблемы, а не просто лимитируют назначение диуретиков при АГ. Одним из таких решений может служить использование торасемида.
В России наиболее популярным торасемидом является Диувер (по данным Pharmexpert, 2012). Недавно появился торасемид пролонгированной формы. Гипотетически такие формы высвобождения могут обеспечивать дополнительные преимущества в сравнении с формами быстрого высвобождения. В связи с этим представляется интересным сравнить подробно препараты двух форм высвобождения – обычной (немедленного высвобождения) и пролонгированного высвобождения. У обоих препаратов с различной формой высвобождения концентрации активного вещества в крови уже через 6 ч становятся одинаковыми. Объем мочи, количество натрия, хлора и калия, выделенные за сутки, не различались у пациентов, принимавших торасемиды различных форм высвобождения [37,38].
В литературе встречаются данные, что в первый час после принятия препарата объем выделенной мочи на препарате с немедленным высвобождением больше, чем на препарате с пролонгированным высвобождением. Так, в работе M.J. Barbanoj и соавт. [37] разница в объеме мочи в первый час после приема препаратов составила 123,3 мл (578,27 против 455 мл). Учитывая, что импульсы в мозг от мочевого пузыря формируются при его наполнении более 150 мл, логично предположить, что этот объем не будет оказывать значимого влияния на количество позывов к мочеиспусканию. Это предположение нашло свое подтверждение в проведенном сравнительном исследовании M.J. Barbanoj и соавт. [37]. Так, при применении торасемида в течение 4 дней количество неотложных позывов к мочеиспусканию у разных форм высвобождения было сопоставимо. После приема пролонгированной формы отмечались 1–2 эпизода неотложного позыва к мочеиспусканию в среднем через 1,37 и 3,03 ч, а после применения обычного торасемида – 1–2 эпизода через 1,12 и 3,03 ч. При этом средние субъективные оценки интенсивности позывов, оцененные по визуально–аналоговой шкале, были 81,25 и 74,06 у пролонгированной формы и 83,87 и 77,2 у обычной формы высвобождения. Как следует из вышесказанного, ни интенсивность позывов к мочеиспусканию, ни частота мочеиспусканий не отличались у торасемидов различных форм высвобождения.
Интересная находка была сделана в исследовании S. Gropper и соавт. [39]: при назначении торасемида пролонгированного высвобождения в дозе 5 мг было больше острых мочеиспусканий, чем при принятии обычного торасемида 5 мг. Т.к. доза 5 мг рекомендована для лечения АГ, то для пациентов с АГ меньшее количество острых позывов будет субъективно переноситься лучше, т.е. применение обычного торасемида при АГ является предпочтительным. При приеме 10 мг торасемида немедленного высвобождения количество мочеиспусканий было больше по сравнению с 10 мг пролонгированного высвобождения. Учитывая, что доза 10 мг чаще используется в лечении отеков у пациентов с ХСН, то управляемый и прогнозированный диурез является положительным моментом, обусловливающим целесообразность применения обычной формы торасемида.
Между обычной формой торасемида и пролонгированного высвобождения не исключена разница в отношении их влияния на фиброз миокарда. Эта клиническая выгода, связанная с длительным применением препаратов, подтверждена для формы быстрого освобождения в исследовании B. Lоpez [29], а у пролонгированной формы этот процесс не доказан (исследование TORAFIC). Так, исходя из содержания карбокситерминального пропептида коллагена I типа в сыворотке крови, в исследовании TORAFIC долгосрочное лечение лекарственной формой торасемида с контролируемым высвобождением или фуросемидом больных с АГ, страдавших легкой клинически стабильной ХСН, не оказало достоверного влияния на развитие фиброза миокарда [37].
В проспективное наблюдательное сравнительное исследование TORIC были включены 1377 пациентов из 231 клиники Испании, страдавших ХСН II–III функциональных классов (NYНА), которые были разделены на прием торасемида или фуросемида, а также других диуретиков. Наблюдали за пациентами 12 мес. Средняя доза принимаемого торасемида обычной формы высвобождения составила 8,2±2,4 мг/сут., а фуросемида – 35,0±7,2 мг/сут. У пациентов, принимавших торасемид обычной формы высвобождения, общая смертность была ниже на 51,5% (p<0,05), сердечно–сосудистая смертность – на 59,7% (p<0,05), внезапная смертность – на 65,8%, чем у пациентов, принимавших фуросемид. За год наблюдения уровень калия изменился с 4,28 до 4,22 ммоль/л, т.е. на 0,06 ммоль/л за 12 мес. ежедневного приема в средней дозе 8,2 мг/сут.
Интересно отметить, что сопоставление инструкций к применению Диувера и бритомара на сайте Минздравсоцразвития РФ (Государственный реестр лекарственных средств) [26] по разделу «Показания» свидетельствует о полном их совпадении, по разделу «Противопоказания» в инструкции полного совпадения нет, в частности, в противопоказаниях к бритомару имеется указание на синусовую брадикардию и АВ–блокаду II–III степени, чего нет у Диувера.
С точки зрения сравнительного фармакоэкономического аспекта в доступной нам литературе данных об этих препаратах не обнаружено. Начальное сравнение прямой стоимости показывает преимущество Диувера на 18%. Так, наиболее часто используемая дозировка при лечении АГ Диувером – 5 мг № 60 стоит 536 руб., т.е. на 1 мес. терапии –268 руб. Бритомар 5 мг № 30 стоит 317 руб. (на 1 мес.) (стоимость указана на 25.09.2012 г. с сайта http://www.aptekaonline.ru). С учетом уникальности клинических эффектов торасемида и его высокой безопасности, а также расширения показаний по рекомендациям ведения АГ и ХСН экспертами ведущих отечественных и зарубежных профессиональных сообществ, с нашей точки зрения, актуально проведение полноценного проспективного длительного фармакоэкономического сравнительного исследования торасемида различных производителей.
Заключение. Торасемид – это лекарственное средство с антиальдостероновым и антигипертензивным свойствами, обладающее дозозависимым диуретическим эффектом. В дозировках 2,5–5 мг оказывает преимущественно антигипертензивное и антиальдостероное действие со слабым натрийуретическим эффектом, что позволяет использовать торасемид для ежедневной постоянной терапии АГ.
В целом, в многочисленных исследованиях на сегодняшний день доказано, что торасемид является первым представителем нового поколения петлевых диуретиков, которые по спектру фармакологических эффектов принципиально отличаются от петлевых диуретиков первого поколения. Антиальдостероновые эффекты, в основе которых лежит способность торасемида блокировать альдостероновые рецепторы в почках и сердце и тормозить секрецию альдостерона надпочечниками, обеспечивают позитивные эффекты для лечения ХСН, отеков различного генеза.
Торасемид не активирует симпатическую нервную систему (не влияет на уровень адреналина и норадреналина) и не увеличивает ЧСС. Торасемид тормозит синтез нового коллагена при сохранении скорости его распада, что выражается в снижении общей фракции коллагена в тканях, например в сердце. Клинические данные свидетельствуют об уменьшении гипертрофии левого желудочка.
Торасемид обычной формы высвобождения (немедленной) сопоставим по суточному объему выделенной мочи с пролонгированным торасемидом. При ежедневном приеме торасемидов разных форм высвобождения как количество неотложных позывов к мочеиспусканию, так и сила позывов, оцененная по визуально–аналоговой шкале, были сопоставимы. Однако у торасемида немедленной формы высвобождения доказано действие, уменьшающее фиброз миокарда, и положительное влияние на смертность пациентов, в отличие от пролонгированной формы, у которой отсутствуют доказательства влияния на эти параметры.
Литература
1. The ALLHAT officers and coordinators for the ALLHAT collaborative research group. Major outcomes in high – risk hypertensive patients randomized to angiotensin – converting enzyme inhibitor or calcium channel blocker vs diuretic // JAMA. 2002. Vol. 288. P. 2981–2997.
2. Neaton J.D., Grimm R.H., Prineas R.J. et al. Treatment of mild hypertension study // JAMA. 1993. Vol. 270. P. 713–724.
3. SHEP cooperative research group. Prevention of stroke by antihypertesive drug treatment in older persons with isolated systolic hypertension // JAMA. 1991. Vol. 265. P. 3255–3264.
4. Gosse P., Sheridan D.J., Zannad F. et al. Regression of left ventricular hypertrophy in hypertensive patients treated with indapamide SR 1.5 mg versus enalapril 20 mg: the LIVE study // J. Hypertens. 2000. Vol. 18. P. 1465–1475.
5. Dahlof B., Lindholm L.H., Hansson L. et al. Morbidity and mortality in the Swedish Trial in Old Patients with hypertension (STOP – Hypertension) // Lancet. 1991. Vol. 338. P. 1281–1285.
6. Medical research counsil working party. MRC trial of treatment of mild hypertension: principal results // BMJ. 1985. Vol. 291. P. 97–104.
7. Marre M., Puig J.G., Kokot F. et al. Equivalence of indapamide SR and enalapril on microalbuminuria reduction in hypertensive patients with type 2 diabetes: the NESTOR study // J. Hypertens. 2004. Vol. 22. P. 1613–1622.
8. Uchida T., Yamanaga K., Nishikawa M. et al. Anti–aldosteronergic effect of torasemide // Eur. J. Pharmacol. 1991. Vol. 205. P. 145–150.
9. Goodfriend T.L., Ball D.L., Oelkers W. et al. Torasemide inhibits aldosterone secretion in vitro // Life Sci. 1998. Vol. 63. PL45–PL50.
10. Pitt B., Zannad F., Remme W.J. et al. The effect of spironolactone on morbidity and mortality in patients with severe heart failure. Randomized Aldactone Evaluation Study Investigators // N. Engl. J. Med. 1999. Vol. 341. P. 709–717.
11. Francis G.S. The relationship of the sympathetic nervous system and the renin–angiotensin system in congestive heart failure // Amer. Heart J. 1989. Vol. 118. P. 642–648.
12. Wang W. Chronic administration of aldosterone depresses baroreceptor reflex function in the dog // Hypertens. 1994. Vol. 24. P. 571–575.
13. MacFadyen R.J., Barr C.S., Struthers A.D. Aldosterone blockade reduces vascular collagen turnover, improves heart rate variability and reduces early morning rise in heart rate in heart failure patients // Cardiovasc. Res. 1997. Vol. 35. P. 30–34.
14. Harada K. et al. Beneficial Effects of Torasemide on Systolic Wall Stress and Sympathetic Nervous Activity in Asymptomatic or Mildly Symptomatic Patients With Heart Failure: Comparison With Azosemide // J. Cardiovasc. Pharmacol. 2009. Vol. 53. P. 468–473.
15. Yamato M., Sasaki T., Honda K. et al. Effects of torasemide in left ventricular function and neurohumoral factors in patients with chronic heart failure // Circ. J. 2003. Vol. 67(5). P. 384–390.
16. Mуller K., Gamba G., Jaquet F., Hess B. Torasemide vs. furosemide in primary care patients with chronic heart failure NYHA II to IV – efficacy and quality of life // Eur. J. Heart Fail. 2003. Vol. 5(6). P. 793–801.
17. Coca A. Effect of torasemide in monotherapy or associated to other antihypertensive drugs on pulse pressure in essential hypertension // Amer. J. Hypertens. 2002. Vol.15. 113A–114А Р231.
18. Преображенский Д.В., Некрасова Н.И., Хосева Е.Н. и др. Торасемид – эффективный петлевой диуретик для длительной терапии артериальной гипертензии // Кардиология. –2011. – Т. 51 (4). – С. 67–73.
19. Fortuno A. Torasemide Inhibits Angiotensin II–Induced Vasoconstriction and Intracellular Calcium Increase in the Aorta of Spontaneously Hypertensive Rats // Hypertens. 1999. Vol. 34. P. 138–143.
20. Fortuno А. The loop diuretic torasemide interferes with endothelin 1 actions in the aorta of hypertensive rats // Nephrol. Dial. Transplant. 2001. Vol. 16 (Suppl 1). P. 18–21.
21. Veeraveedu P.T., Watanabe K., Ma M. et al. Comparative effects of torasemide and furosemide in rats with heart failure // Biochem. Pharmacol. 2007. Vol. 23. P. 143–148.
22. Uchida T., Yamanaga K., Nishikawa M. et al. Anti–aldosteronergic effect of torasemide // Eur. J. Pharmacol. 1991. Vol. 205(2). P. 145–150.
23. Albert N.M., Yancy C.W., Liang L. et al. Use of aldosterone antagonists in heart failure // JAMA. 2009. Vol. 302(15). P. 1658–1665.
24. Шугушев Х.Х., Гаева А. А. Влияние фуросемида и торасемида на вариабельность сердечного ритма и желудочковые аритмии у больных с хронической сердечной недостаточностью, осложнившей течение ишемической болезни сердца: сравнительное нерандомизированное исследование // Рац. фармакотерапия в кардиологии. – 2010. – Т. 6 (4). – С. 513–517.
25. Cody R.J. The sympathetic nervous system and the renin–angiotensin–aldosterone system in cardiovascular disease // Amer. J. Cardiol. 1997. Vol. 80(9B). P. 9J–14J.
26. http:www.grls.rosminzdrav.ru // Сайт Минздравсоцразвития РФ.
27. Brown N.J. Aldosterone and end–organ damage // Curr. Opin. Nephrol. Hypertens. 2005. Vol. 14(3). P. 235–241.
28. Harada K., Izawa H., Nishizawa T. et al. Beneficial effects of torasemide on systolic wall stress and sympathetic nervous activity in asymptomatic or mildly symptomatic patients with heart failure: comparison with azosemide // J. Cardiovasc. Pharmacol. 2009. Vol. 53(6). –P. 468–473.
29. Lоpez B., Querejeta R., Gonzalez A. et al. Effects of loop diuretics on myocardial fibrosis and collagen type I turnover in chronic heart failure // J. Amer. Coll. Cardiol. 2004. Vol. 43(11). P. 2028–2035.
30. Lоpez B., Gonzalez A., Beaumont J. et al. Identification of a potential cardiac antifibrotic mechanism of torasemide in patients with chronic heart failure // J. Amer. Coll. Cardiol. 2007. Vol. 50(9). P. 859–867.
31. Аверин Е.Е. Влияние торасемида на гипертрофию миокарда левого желудочка // Журнал Сердечная недостаточность. – 2012. Том 13. – № 3(71). – С.158–163.
32. Kasama S. Effects of torasemide on cardiac sympathetic nerve activity and left ventricular remodelling in patients with congestive heart failure // Heart. 2006. Vol. 92. P. 1434–1440.
33. Lopez B., Gonzalez A., Hermida N. et al. Myocardial fibrosis in chronic kidney disease: potential benefits of torasemide // Kidney Int. 2008. (Suppl. 111). S.19–S23.
34. Чазова И.Е., Фомин В.В. Резистентная артериальная гипертензия // Тер. архив. – 2008. – № 6. – С. 80–85.
35. Chapman N., Dobson J., Wilson S. et al. Effect of spironolactone on blood pressure in patients with resistant hypertension // Hypertens. 2007. Vol. 49. P. 839–845.
36. Handler J. Maximizing diuretic therapy in resistant hypertension // J. Clin. Hypertens. (Greenwich). 2007. Vol. 9(10). P. 802–806.
37. Barbanoj M.J., Ballester M.R.,Antonijoan R.M. et al. Comparison of repeated–dose pharmacokinetics of prolonged–release and immediate–release torasemide formulations in healthy young volunteers // Fundam. Clin. Pharmacol. 2009. Vol. 23 (1). P. 115–125.
38. Barbanoj M.J., Ballester M.R., Antonijoan R.M. et al. A bioavailability/bioequivalence and pharmacokinetic study of two oral doses of torasemide (5 and 10 mg): prolongedrelease versus the conventional formulation // Clin. Exp. Pharmacol. Physiol. 2009. Vol. 36 (5–6). P. 469–477.
39. Gropper S., Albet C. Single–dose, randomized, cross–over, bioavailability pilot clinical trial of torasemide immediate release compared to a new prolonged release formulation of torasemide // Basic Clin. Pharmacol. Toxicol. 2006. Vol. 99 (Suppl. 1). P. 48.
40. Gropper S., Rojas M.J. Food interaction bioavailability study of a torasemide new formulation (10 mg prolonged release) after a high fat content meal // Basic Clin. Pharmacol. Toxicol. 2006. Vol. 99 (Suppl. 1). P. 48.












