Отделение неотложной кардиологии (зав. - профессор М.Я. Руда)
Традиционная медикаментозная терапия ИБС направлена на уменьшение потребности миокарда в кислороде или на увеличение его доставки посредством вазодилатации. Метаболическая терапия нацелена на улучшение эффективности утилизации кислорода миокардом в условиях ишемии. По определению, метаболические препараты (в чистом виде) не влияют на показатели гемодинамики, основной мишенью является кардиомиоцит.
Для того чтобы представить механизм действия метаболических препаратов, рассмотрим особенности энергообеспечения миокарда в нормальных физиологических условиях и в состоянии ишемии.
Сердце можно представить в виде насоса, «топливом» для которого служат карбогидраты (в основном глюкоза) и свободные жирные кислоты (СЖК). Независимо от энергетического субстрата, в заключительной стадии распада образуется ацетил–коэнзим А, который вступает в цикл трикарбоновых кислот или цикл Кребса в митохондриях, что в конечном итоге приводит к превращению химической энергии в механическую – контрактильную работу сердца. В обычных условиях начальный этап метаболизма глюкозы – анаэробный гликолиз, в результате которого образуется пируват, приводит к синтезу незначительного (менее 10%), количества АТФ [1]. Конверсия пирувата в ацетил–коэнзим А происходит в митохондриях с помощью ферментного пируватдегидрогеназного комплекса (ПДК). Данная реакция ингибируется избыточной концентрацией ацетил–коэнзим А и СЖК [2]. При достаточном кислородном обеспечении основным энергетическим субстратом миокарда являются СЖК, которые служат источником от 60 до 80% АТФ. Важно отметить, что СЖК менее «эффективный» источник энергии по сравнению с глюкозой, т.к. требуют на 10% больше кислорода для образования эквивалентного количества АТФ. СЖК проникают в митохондрии посредством активного транспорта, за который отвечает корнитино–пальмитиновый ферментный комплекс (КПК). В митохондриях происходит b–окисление СЖК. Этот процесс строго контролируется и зависит главным образом от интенсивности транслокации СЖК в митохондрии.
В случае умеренной ишемии аэробное окисление СЖК и глюкозы снижается. Анаэробный гликолиз становится основным источником АТФ. В этих условиях запасы гликогена мобилизуются на поддержку гликолиза [3,4]. При развитии тяжелой ишемии (окклюзия коронарной артерии) анаэробный гликолиз остается единственным источником образования АТФ. При восстановлении коронарного кровотока (репефурзии) избыточное количество СЖК ингибирует ПДК, вследствие этого основной пул АТФ (около 95%) происходит за счет окисления СЖК [5]. По данным ряда исследований, резкий дисбаланс между окислением глюкозы и СЖК в сторону последних, а также повышенная концентрация СЖК в ишемизированной зоне являются основными факторами реперфузионного повреждения и дисфункции миокарда, развития опасных нарушений ритма [6,7].
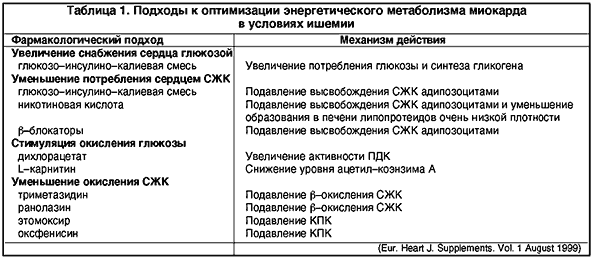
Изменения метаболизма миокарда во время ишемии и реперфузии открывают широкую возможность для медикаментозного воздействия [8]. Современные подходы включают стимуляцию внутриклеточного обмена глюкозы, а также подавление метаболизма СЖК (см. таблицу 1).
Рождение метаболического подхода в лечении ИБС традиционно связывают с глюкозо–инсулино–калиевой смесью (ГИК). В 1962 г Соди–Палларес (Sodi–Pallaris) впервые в небольшом нерандомизированном исследовании показал, что ГИК положительно влияет на динамику ЭКГ при остром инфаркте миокарда (ИМ), улучшает раннюю выживаемость [9]. Результаты последующих исследований были противоречивы, многие из них отличались неудовлетворительным дизайном. В частности, в ряде работ терапия ГИК начиналась через 48 ч после начала ангинозного приступа. Кроме того, в претромболитическую эру в большинстве работ объем выборки был недостаточным для достижения статистической достоверности [10]. Тем не менее Rackley et al. в рандомизированном исследовании показали, что введение ГИК в среднем в течение 2,5 дней после развития ИМ приводило к уменьшению смертности [11]. Использовался 30% р–р глюкозы, содержащий 50 Ед инсулина и 80 Мэкв хлорида калия на литр. По данным мета–анализа 9 исследований (n=1932), в которых ГИК использовали в первые 48 ч после развития ИМ, госпитальная смертность снижалась на 28% (p=0,004%) [10]. В настоящее время представляют интерес работы, где ГИК применяли на фоне тромболитической терапии (ТЛТ) или первичной баллонной ангиопластики. Убедительные доказательства положительного влияния ГИК на фоне реперфузионной терапии получены на основании результатов крупного проспективного рандомизированного исследования ECLA (Estudios Cardiologicos Latinoamerica) [12]. Снижение госпитальной смертности в группе, получавшей ГИК, составило 66% (p=0,008). Примечательно, что у больных, не получавших реперфузионную терапию, терапия не повлияла на уровень смертности. В большинстве работ прослеживается следующая закономерность: чем выше доза ГИК и чем раньше начиналась терапия, тем очевиднее было положительное влияние ГИК на риск осложнений ИМ. В исследовании DIGAMI (Diabetes Insulin–Glucose in Acute Myocardial Infarction) больные ИМ и сахарным диабетом (СД) были рандомизированы на две группы [13]. В первой группе коррекция уровня глюкозы была общепринятой: инсулинотерапия назначалась селективно в случае недостаточной эффективности диеты и пероральных сахар–снижающих препаратов. Во второй группе всем больным вводили глюкозо–инсулиновую смесь с последующим переходом на обычный мультидозовый режим инсулинотерапии. Во второй группе смертность через год наблюдения оказалась на 29% меньше (p=0,027). Несмотря на то, что в исследование DIGAMI включали больных СД, результаты можно экстраполировать на недиабетическую популяцию, так как преимущество активной инсулинотерапии было наиболее очевидным в подгруппе с легким и умеренным сахарным диабетом, особенно среди больных, не получавших инсулин до ИМ. В этой подгруппе госпитальная смертность снизилась на 58% (p<0,05), годичная на 58% (p<0,05). В ряде работ показано, что введение ГИК перед операцией коронарного шунтирования приводит к достоверному увеличению сердечного индекса на 40%, снижению частоты аритмий, особенно мерцания предсердий, существенному уменьшению риска развития послеоперационного кардиогенного шока.
Рождение метаболического подхода в лечении ИБС традиционно связывают с глюкозо–инсулино–калиевой смесью (ГИК). В 1962 г Соди–Палларес (Sodi–Pallaris) впервые в небольшом нерандомизированном исследовании показал, что ГИК положительно влияет на динамику ЭКГ при остром инфаркте миокарда (ИМ), улучшает раннюю выживаемость [9]. Результаты последующих исследований были противоречивы, многие из них отличались неудовлетворительным дизайном. В частности, в ряде работ терапия ГИК начиналась через 48 ч после начала ангинозного приступа. Кроме того, в претромболитическую эру в большинстве работ объем выборки был недостаточным для достижения статистической достоверности [10]. Тем не менее Rackley et al. в рандомизированном исследовании показали, что введение ГИК в среднем в течение 2,5 дней после развития ИМ приводило к уменьшению смертности [11]. Использовался 30% р–р глюкозы, содержащий 50 Ед инсулина и 80 Мэкв хлорида калия на литр. По данным мета–анализа 9 исследований (n=1932), в которых ГИК использовали в первые 48 ч после развития ИМ, госпитальная смертность снижалась на 28% (p=0,004%) [10]. В настоящее время представляют интерес работы, где ГИК применяли на фоне тромболитической терапии (ТЛТ) или первичной баллонной ангиопластики. Убедительные доказательства положительного влияния ГИК на фоне реперфузионной терапии получены на основании результатов крупного проспективного рандомизированного исследования ECLA (Estudios Cardiologicos Latinoamerica) [12]. Снижение госпитальной смертности в группе, получавшей ГИК, составило 66% (p=0,008). Примечательно, что у больных, не получавших реперфузионную терапию, терапия не повлияла на уровень смертности. В большинстве работ прослеживается следующая закономерность: чем выше доза ГИК и чем раньше начиналась терапия, тем очевиднее было положительное влияние ГИК на риск осложнений ИМ. В исследовании DIGAMI (Diabetes Insulin–Glucose in Acute Myocardial Infarction) больные ИМ и сахарным диабетом (СД) были рандомизированы на две группы [13]. В первой группе коррекция уровня глюкозы была общепринятой: инсулинотерапия назначалась селективно в случае недостаточной эффективности диеты и пероральных сахар–снижающих препаратов. Во второй группе всем больным вводили глюкозо–инсулиновую смесь с последующим переходом на обычный мультидозовый режим инсулинотерапии. Во второй группе смертность через год наблюдения оказалась на 29% меньше (p=0,027). Несмотря на то, что в исследование DIGAMI включали больных СД, результаты можно экстраполировать на недиабетическую популяцию, так как преимущество активной инсулинотерапии было наиболее очевидным в подгруппе с легким и умеренным сахарным диабетом, особенно среди больных, не получавших инсулин до ИМ. В этой подгруппе госпитальная смертность снизилась на 58% (p<0,05), годичная на 58% (p<0,05). В ряде работ показано, что введение ГИК перед операцией коронарного шунтирования приводит к достоверному увеличению сердечного индекса на 40%, снижению частоты аритмий, особенно мерцания предсердий, существенному уменьшению риска развития послеоперационного кардиогенного шока.По данным большинства исследований, несмотря на улучшение прогноза у больных ИМ, получающих ГИК, терапия ГИК не получила широкого распространения. Более того, ГИК не вошла в перечень препаратов для рутинной терапии ИМ в официальных международных рекомендациях. В самое крупное на сегодняшний день исследование ECLA было включено 407 больных, что явно недостаточно для принятия окончательного решения роли ГИК в лечении ИМ. Большинство экспертов считают необходимым проведение дополнительных крупномасштабных исследований. К недостаткам ГИК можно отнести необходимость внутривенного введения (доступ через центральную вену считается предпочтительным) и короткий курс лечения. Подобных недостатков лишены пероральные метаболические препараты.
Уменьшение потребления СЖК сердцем
ГИК обладает еще одним полезным эффектом – способностью подавлять высвобождение СЖК адипозоцитами (действие инсулина), что приводит к снижению концентрации СЖК в зоне ишемизированного миокарда. Клиническое значение ГИК рассмотрено в предыдущем разделе [7].
Никотиновая кислота (НК) снижает уровень СЖК, подавляя их освобождение адипозоцитами, а также уменьшая образование богатых триглицеридами липопротеидов очень низкой плотности в печени [14]. По данным экспериментальных исследований, НК в 2–3 раза увеличивает интенсивность окисления глюкозы в миокарде [15]. К сожалению, мы не располагаем клиническими исследованиями, способными подтвердить кардиопротективное действие НК. Ограничение применения НК в широкой практике связано в основном с серьезными побочными эффектами.
На основании многочисленных крупных рандомизированных исследований известно, что b–блокаторы значительно улучшают прогноз у больных с различными формами ИБС [16]. За счет антиадренергического действия b–блокаторы подавляют катехоламин–индуцированное высвобождение СЖК адипозоцитами во время острой ишемии [16]. По–видимому, эта способность b–блокаторов во многом определяет их клиническую эффективность.
Стимуляция окисления глюкозы
В экспериментальных работах показано, что стимуляция окисления глюкозы положительно влияет на работу сердца в условиях ишемии [4]. Фармакологически активация гликолиза возможна с помощью стимуляции ПДК либо опосредованно через подавление вунтримитохондриального ацетил–коэнзима А – основного ингибитора гликолиза.
К активаторам ПДК относится дихлорацетат, который предотвращает фосфорилирование ПДК, приводящее к его инактивации [17]. В исследованиях на животных дихлорацатат уменьшал ишемическое повреждение миокарда, ускорял восстановление сократительной функции миокарда после реперфузии [18]. У больных застойной сердечной недостаточностью дихлорацетат улучшал систолическую функцию [19].
Кроме регуляции поступления СЖК в митохондрии, L–карнитин отвечает за удаление ацетил–коэнзима А из митохондрий [5]. Аналогичным эффектом обладает пропионил L–карнитин. В эксперименте L–карнитин оказывал кардиопротективное действие, уменьшая реперфузионное повреждение и улучшая сократительную функцию миокарда [20]. В многоцентровом исследовании CEDIM (L–carnitine Ecocardiografia Digitlizzata Infarto Miocardico) L–карнитин значительно уменьшал конечное диастолическое давление в левом желудочке и предотвращал расширение камер сердца у больных, перенесших ИМ [21].
Уменьшение окисления СЖК
Окисление СЖК подавляет митохондриальное окисление глюкозы. Следовательно, блокируя окисление СЖК, можно добиться значительной активации окисления глюкозы. Такой фармакологический подход получил наибольшее распространение в метаболической терапии ИБС. Препараты этой группы можно разделить на два класса: прямые ингибиторы b–окисления СЖК и ингибиторы КПК.
К наиболее изученным и широко применяемым в клинической практике препаратам этой группы относится триметазидин (2,3,4 триметоксибензил–пиперазина дигидрохлорид) – Предуктал, разработанный французской Фармацевтической группой Сервье.
Множество экспериментальных и клинических исследований показали, что триметазидин относится к антиангинальным препаратам нового класса, реализующим свое действие на клеточном уровне, воздействуя непосредственно на ишемизированные кардиомиоциты [22]. Основные кардиальные эффекты триметазидина на клеточном, субклеточном и молекулярном уровне представлены на схеме 1. Кроме этого, препарат влияет на некоторые форменные элементы крови. В опытах in vitro отмечено дозозависимое уменьшение агрегации тромбоцитов, индуцированной арахидоновой кислотой. Показано, что препарат блокирует проникновение нейтрофилов в миокард при экспериментальном инфаркте [23]. Sentex et al. в опытах на культуре клеток отметили значительное ускорение включения фосфолипидов в клеточную мембрану, что позволяет отнести триметазидин к цитопротекторам [24]. В опытах на культуре кардиомицитов, инкубированных с триметазидином, значительно уменьшалось выведение из клеток лактатдегидрогеназы, провоцируемое свободными радикалами [25]. Представления об антиишемическом действии триметазидина претерпели определенную эволюцию. Сначала основную роль препарата видели в нейтрализации и выведении свободных радикалов. Последующие работы позволили установить механизм действия на молекулярном уровне. Kantor et al. на модели изолированных работающих сердец крыс изучали эффект триметазидина на активность ферментов, вовлеченных в окисление жирных кислот [26]. Препарат не оказывал влияния на потребление кислорода в условиях аэробной перфузии. В состоянии ишемии окисление глюкозы увеличивалось на 210%, чему способствовала активация пируватдегидрогеназы на 37%. Резко снижалось b–окисление жирных кислот за счет блокады последнего фермента цикла – 3–кетоацил коэнзим А тиолазы. Подавление b–окисления делает окисление карбогидратов (глюкозы) основным источником энергии. Следовательно, Предуктал, с одной стороны, перестраивает энергетический метаболизм, повышая его эффективность; с другой – уменьшает образование свободных радикалов, блокируя окисление жирных кислот.
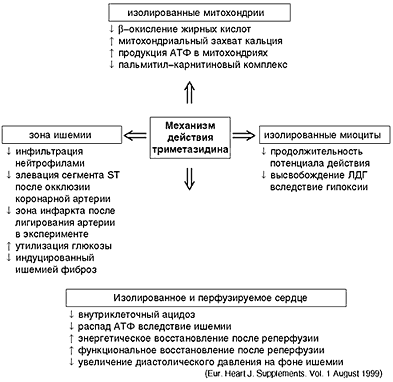
Схема 1. Антиишемические и цитопротективные эффекты триметазидина. (Eur. Heart J. Supplements. Vol. 1 August 1999)
В клинических исследованиях Предуктал зарекомендовал себя, как надежный и безопасный антиангинальный препарат. Еще в 80–х было показано, что препарат в качестве монотерапии оказывает антиишемическое действие, уменьшая количество приступов и увеличивая время нагрузки [27]. В многоцентровом европейском исследовании сравнивали эффективность триметазидина в дозе 60 мг/сут и пропранолола 120 мг/сут у больных со стабильной стенокардией [28]. Было включено 149 пациентов. Оценку проводили на основании показателей нагрузочного теста. Через 3 месяца лечения продолжительность нагрузки, время до появления депрессии сегмента ST на 1мм в обеих группах не отличались. Оба препарата в равной степени уменьшали количество ишемических эпизодов по данным суточного мониторирования ЭКГ. В представленной работе триметазидин и b–блокатор оказались одинаково эффективными у больных со стенокардией. Michaelides et al. показали, что назначение препарата больным ИБС, принимающим b–блокаторы, также заметно улучшало течение болезни [29]. Более того, в двойном слепом исследовании добавление к терапии триметазидина оказывало более выраженный эффект по сравнению с изосорбида динитратом [30]. В частности, триметазидин в большей степени увеличивал продолжительность нагрузки. В исследовании Dalla–Volta et al. триметазидин не уступал другому традиционному антиангинальному препарату – нифедипину в профилактике ангинозных приступов [31]. Монотерапия дилтиаземом уступала по влиянию на параметры нагрузочной пробы совместному приему триметазидина и дилтиазема [32]. Можно заключить, что клиническая эффективность препарата у больных со стенокардией доказана во всех исследованиях, в том числе плацебо–контролируемых.При выполнении операции коронарного шунтирования (КШ) возможно повреждение миокарда, по своим механизмам относящееся к реперфузионному. Fabiani et al. в двойном слепом исследовании проверяли кардиопротективные свойства триметазидина [33]. Препарат назначали за 3 недели до КШ и добавляли в кардиоплегический раствор. Миозин (маркер повреждения) в группе активного лечения определялся достоверно реже при сравнении с плацебо (p=0,036). Значительно увеличивался ударный сердечный индекс. Предварительная терапия триметазидином не только уменьшала повреждение миокарда, но и позволяла пациентам подойти к операции с улучшением сократительной функции левого желудочка (ЛЖ).
Kober et al. в плацебо–контролируемом исследовании показали, что при проведении баллонной ангиопластики предварительное внутрикоронарное введение триметазидина в дозе 6 мг приводило к значительному уменьшению ишемических сдвигов сегмента ST, задержке развития ангинозного приступа при раздувании баллона [34]. Таким образом продемонстрирован прямой антиишемический эффект триметазидина. В исследовании LIST (Limitation of Infarct Size by Trimetazidine) препарат назначали больным ИМ, у которых в качестве метода реваскуляризации использовали первичную баллонную ангиопластику [35]. В группе триметазидина значительно уменьшалась выраженность смещения сегмента ST по данным суточного мониторирования. Влияние на клинические исходы ИМ не изучалось в связи с небольшим объемом исследования.
В условиях хронической ишемии развивается обратимая дисфункция миокарда, которую называют гибернацией (спячкой). Наличие гибернирующего миокарда отрицательно влияет на прогноз ИБС за счет появления выраженной сердечной недостаточности. 65 больных ИБС, у которых выявлен «спящий» миокард по данным добутаминовой пробы, Маколкин В.И. и колл. разделили на 2 группы [36]. В 1–й группе проводилась обычная антиангинальная терапия, затем добавляли триметазидин в дозе 60 мг/сут. Во второй группе проведена реваскуляризация. Традиционные препараты не влияли на число асинергичных сегментов, тогда как назначение триметазидина обеспечивало восстановление сократимости в 66% сегментов со «спящим» миокардом, что сопоставимо с эффективностью реваскуляризации. В итальянском исследовании триметазидин также достоверно улучшал региональную сократимость ЛЖ у больных с ИБС при проведении добутаминовой пробы [37]. Brottier et al. проводили лечение препаратом наряду с обычной терапией в течение 6 месяцев у больных ишемической кардиопатией и тяжелой сердечной недостаточностью (III–IV класс по NYHA) [38]. По окончании курса терапии возрастала фракция выброса ЛЖ, уменьшался объем полостей сердца. Аналогичные результаты получены в работе Терещенко С.Н. и соав [39]. У больных с постинфарктной недостаточностью кровообращения терапия триметазидином в течение года приводила к увеличению фракции выброса, уменьшению переднезаднего размера ЛЖ.
К преимуществам Предуктала относится отсутствие гемодинамических эффектов, что позволяет назначать препарат независимо от уровня артериального давления, особенностей сердечного ритма и сократительной функции миокарда. Более того, препарат не влияет на показатели центральной гемодинамики. Pornin et al. измеряли сердечный индекс методом термодилюции, а также давление в ЛЖ и аорте, используя микромонометрию [40]. До и после начала терапии триметазидином изучаемые показатели не изменились.
Тромболитическая терапия (ТЛТ) считается основой консервативного лечения ИМ. Восстановление кровотока в инфаркт–связанной артерии позволяет значительно уменьшить зону поражения, сохранить функциональную способность миокарда и сохранить значительное количество жизней больных. Главная клиническая проблема, связанная с ТЛТ, – реперфузионное повреждение миокарда. Во время реперфузии резко повышается образование свободных радикалов (таких как супероксид) и уменьшается их выведение. Свободные радикалы вызывают переоксидацию клеточных мембран с последующей гибелью клеток. Триметазидин уменьшал последствия оксидативного стресса в экспериментах in vivo и ex vivo. В работе на кроликах препарат вводили внутривенно за 3 ч до легирования коронарной артерии [41]. У животных, получивших триметазидин, зона инфаркта оказалась на 42% меньше (p=0,025). Для оценки клинической эффективности терапии триметазидином у больных ИМ было проведено многоцентровое международное двойное слепое рандомизированное исследование EMIР–FR (The European Myocardial Infarction Project – Free Radicals) [42]. Исследование проводилось в 15 европейских странах, в том числе в России. Было включено 19725 пациентов. Период наблюдения составил от 35 дней до 39 месяцев, в среднем 12 месяцев. Первичной конечной точкой являлась краткосрочная смертность – 35 дней. Вторичные конечные точки – долгосрочная смертность, госпитальная смертность и комбинированная конечная точка: тяжелая сердечная недостаточность, фибрилляция желудочков, асистолия, электромеханическая диссоциация и сердечно–сосудистая смерть. Проводился отдельный анализ у больных, получавших и не получавших ТЛТ. Включение проводилось не позднее 24 ч от начала ИМ. Триметазидин вводили по следующей схеме: 40 мг болюсом перед, одновременно или в течение 15 минут после начала ТЛТ (если она проводилась) с последующей инфузией 60 мг/сут в течение 48 ч. Контрольная группа получала плацебо. У 56% включенных больных выполнена ТЛТ, соответственно, 44% больных не получили ТЛТ. Можно предположить, что в России процент пациентов, получивших ТЛТ, был ниже. Краткосрочная смертность в обеих группах не отличалась. Среди больных, которым проводилась ТЛТ, отмечалась тенденция к увеличению смертности в группе триметазидина. У больных, не получавших ТЛТ, наблюдалась обратная картина: смертность выше в группе плацебо. В обоих случаях различия статистически недостоверны. Осложнения, составляющие комбинированную конечную точку, в группе без ТЛТ на фоне активной терапии встречались достоверно реже (p=0,027). В подгруппе больных без ТЛТ, которые выполнили все требования протокола (согласно требованиям GCP, эта популяция должна быть проанализирована отдельно), краткосрочная смертность в группе триметазидина оказалась достоверно ниже на 10% по сравнению с плацебо (p=0,027). В той же подгруппе госпитальная, сердечно–сосудистая смертность, комбинированная конечная точка на фоне приема препарата снижались (p<0,05). Кривые выживаемости с поправкой на пол, возраст, особенности анамнеза, время от начала ИМ до рандомизации не внесли изменений в результаты работы. Долгосрочная и госпитальная смертность, комбинированная конечная точка были одинаковыми в обеих группах. Несмотря на то, что основная цель исследования не достигнута, триметазидин подтвердил свои антиангинальные свойства: достоверное снижение частоты затяжных ангинозных приступов и рецидивов ИМ у больных с ТЛТ. Тяжелая сердечная недостаточность, фибрилляция желудочков реже наблюдались на фоне приема триметазидина у пациентов без ТЛТ. Была подтверждена безопасность применения триметазидина и отсутствие влияния на показатели гемодинамики.
При попытке проанализировать результаты EMIР–FR прежде всего обращает на себя внимание короткий курс активной терапии. За необратимым повреждением миокарда в связи с ИМ следует длительный, продолжающийся несколько месяцев, процесс трансформации морфологических и функциональных свойств миокарда. Следовательно, вызывает интерес оценка долгосрочной терапии триметазидином у больных ИМ. Работа была спланирована в начале 90–х. На тот период механизм действия триметазидина не был охарактеризован на молекулярном уровне. В настоящее время очевидно, что Предуктал не столько элиминирует продукты окислительного стресса, сколько предотвращает их образование, блокируя окисление СЖК. Для изменения метаболизма двухдневный курс терапии может оказаться недостаточным. В этой связи профилактический, возможно длительный прием препарата мог бы повлиять на течение ИМ, уменьшая последствия оксидативного стресса. Однако это предположение нуждается в подтверждении в клинических условиях. По мнению организаторов работы, доза триметазидина могла быть недостаточной и/или препарат попадал в зону инфаркта слишком поздно. Болюс триметазидина вводили почти одновременно с ТЛТ, тогда как реперфузия не обязательно наступает сразу после начала ТЛТ. Кроме того, расширились представления о реперфузионном повреждении, большую роль в котором придают воспалительным, иммунным факторам, нарушениям кальциевых потоков. Эти данные не позволяют считать метаболическую терапию единственным направлением борьбы с нежелательными эффектами ТЛТ. Тенденция к снижению риска осложнений ИМ в группе без ТЛТ (в некоторых подгруппах статистически значимая) может быть объяснена положительным влиянием триметазидина на сократительную функцию миокарда, что подтверждается рядом работ, а также антиишемическим действием препарата. Коронарная окклюзия затрудняет доставку препарата в зону повреждения. Возможно, этим обусловлено различие результатов EMIР–FR и экспериментальных работ, где опытные животные получали триметазидин до развития ИМ. Прием препарата до ИМ относили к критериям исключения, что не позволяло провести ретроспективный анализ и могло повлиять на конечный результат. Благоприятное действие триметазидина при выполнении ТБКА и АКШ может быть связано с феноменом прекондиционирования препарата в области риска. Подводя итог EMIР–FR, можно заключить, что короткий курс внутривенной терапии триметазидином у больных ИМ не оказал положительно влияния на прогноз. Результаты EMIР–FR не должны бросать тень на основную сферу применения Предуктала – хронические формы ИБС, прежде всего стабильную стенокардию. В основе хронических и острых форм лежат разные этиологические и патогенетические факторы. Работы последних лет свидетельствуют о том, что в большинстве случаев окклюзирующий тромбоз коронарной артерии, приводящий к развитию ИМ, происходит в области «молодой», поверхностной, богатой холестерином, склонной к эрозированию и разрывам атеросклеротической бляшки [43,44]. С другой стороны, «старые» фиброзные, обтурирующие просвет сосуда бляшки, вызывающие ишемию миокарда, редко являются причиной ИМ [45]. По–видимому, основа положительного эффекта Предуктала у больных ИБС лежит в длительной, устойчивой перестройке энергетического метаболизма, что позволяет сердцу лучше переносить хронический дефицит кислорода.
Ранолазин – другой ингибитор b–окисления жирных кислот. Препарат показал свою эффективность в лечении стабильной стенокардии, снижал частоту ангинозных приступов, увеличивал время нагрузки [46]. В эксперименте препарат повышал окисление глюкозы [47]. Ранолазин оказывает аддитивное действие при комбинации с b–блокаторами и антагонистами кальция [46].
Другая возможность подавить окисление СЖК – блокада карнитино–пальмитинового комплекса. К препаратам с подобным механизмом действия относятся этомоксир, оксфенисин, метилпальмоксират. В экспериментальных работах препараты увеличивали окисление глюкозы в ишемизированном миокарде, улучшали функцию сердца после реперфузии [48]. К сожалению, этоксимер индуцировал гипертрофию миокарда, что ограничивает клиническое изучение данной группы препаратов [49].
Широкое распространение метаболических препаратов в клинической практике нашло свое отражение в последних рекомендациях Американской ассоциации кардиологов по лечению больных со стабильной стенокардией. Триметазидин, ранолазин и L–карнитин отнесены к антиангинальным препаратам [50].
В заключение важно отметить, что если клиническая эффективность метаболических препаратов (прежде всего Предуктала) не вызывает сомнений, то влияние на риск осложнений, прогноз у больных ИБС требует дальнейшего основательного изучения. Впрочем, это относится и к обычным антиангинальным препаратам: нитратам и антагонистам кальция.
Выводы
1. Результаты экспериментальных и клинических исследований позволяют рекомендовать метаболические препараты для лечения больных со стабильной стенокардией и ишемической дисфункцией ЛЖ.
2. Триметазидин (Предуктал) является наиболее изученным, эффективным и широко используемым в клинической практике метаболическим препаратом.
3. Необходимо продолжать исследования по изучению влияния метаболических препаратов на течение и прогноз различных форм ИБС.
Список литературы Вы можете найти на сайте http://www.rmj.ru
Триметазидин –
Предуктал (торговое название)
(Servier)
1. Neely J, Morgan H. Relationship between carbohydrate metabolism and energy balance of heart muscle. Ann. Rev. Physiol. 1974, 36: 413
2. Hansford R, Cohen I. Relative imortance of pyruvate dehydrogenase interconversion and feedback inhibition in the effect of fatty acids on pyruvate oxidation by rat heart mitochondria. Arch. Biochem. Byophis. 1978, 191: 65–81
3. Opie L, King L. Glucose and glycogen utilyzation in myocardial ischemia change in metabolism and consequence for myocyte. Mol. Cell. Biochem. 1998, 180: 3–26
4. Stanley W, Lopaschuk G, Hall J et al. Regulation of myocardial carbohydrate metabolism under normal and ischemic conditions. Cardiovasc. Res. 1997, 33: 243-257
5. Lopaschuk G, Belke D, Gamble J et al. Regulation of fatty acid oxidation in the mammalian heart in health and disease. Biochim. Biophys. Acta. 1994, 1213: 263-276
6. Lopaschuk G, Wambolt R, Barr L. An imbalance between glycolysis and glucose oxidation is a possible explanation for the detrimental effects of high levels of fatty acids during aerobic reperfusion of ischemic hearts. J. Pharm. Exp. Therap. 1993, 264: 135-144
7. Oliver M, Opie I. Effect of glucose and fatty acids on myocardial ischemia and arrhytmias. Lancet. 1994, 343: 155-158
8. Energy substrate metabolism as target for pharmacotherapy in ischemic and reperfused heart muscle. Heart and Metabolism. 1998, 1: 5-9
9. Sodi–Pallares D, Testelli M, Fishleder F. Effects of an intravenous infusion of a potassium–insulin–glucose solution on the electrocardiographuc signs of myocardial infarction. Am. J. Cardiol. 1962, 9: 166-181
10. Fath–Ordoubadi F, Beatt K. Glucose–Insulin–Potassium therapy for treatment of acute myocardial infarction: an overview of randomized placebo controlled trials. Circulation. 1997, 96: 1152-1156
11. Rackley C, Russel R, Rogers W et al. Clinical experience with glucose–insulin–potassium–potassium therapy in acute myocardial infarctuin. Am. Heart. J. 1981, 102: 1038-1049
12. Diaz R, Paolasso E, Piegas L et al. Metabolic modulation of acute myocardial infarction: the ECLA Glucose Insulin Potassium Pilot Trial. Circulation. 1998, 98: 2227-2234
13. Malmberg K, Ryden L, Hamsten A et al. Effects of insulin treatment on cause–specific one–year mortality in diabetic patients with acute myocardial infarction. DIGAMI study group. Eur. Heart J. 1996, 17: 1337-1344
14. Datta S, Das D, Engelman R et al. Enhanced myocardial protection by Nicitinic Acid, an antilipolytic compound: mechanism of action. Basic Res. Cardiol. 1989, 84: 63-76
15. Tateno M, Tamaki N, Yukihiro M et al. Assessment of fatty acid uptake in ischemic heart disease without myocardial infarction. N. Nucl. Med. 1996, 37:1981-1985
16. Teo K, Yusuf S, Furberg D et al. Effects of prophylactic antiarrhythmic drug therapy in acute myocardial infarction. JAMA. 1993, 270:1589-1595
17. Steapoole P. The pharmocology of dichloroacetate. Metabolism. 1989, 38: 1184-1144
18. McVeigh J, Lopaschuk G. Dichloroacetate stimulation of glucose oxidation imroves recovery of ischemic rat hearts. Am. J. Physiol. 1990, 29:1079-1085
19. Bersin R, Volfe C, Kwasman N et al. Improved hemodynamic function and mechanical efficiency in congestive heart failure with sodium dichloroacetate. J. Am. Coll. Cardiol. 1994, 23: 1617-1624
20. Russel R, Mommessin J, Taegtmeyer H. Propionyl–L–carnitine improvement in contractile function of rat hearts oxidizing acetoacetate. Am. J. Physiol. 1995, 268: 441-447
21. Hiceto S, Scrutinio D, Bruzzi P et al. Effects of L–carnitine administration on left ventricular remodeling after acute anterior myocardial infarction: the l–carnitine Ecocardiografia Digitlizzata Infarto Miocardico (CEDIM) Trial. J. Am. Coll. Cardiol. 1995, 26: 380-387
22. Cargnoni A, Pasini E, Ceconi C et al. Insight into cytoprotection with metabolic agents. Eur. Heart J. Supplements. 1999, 1: 40-48
23. Williams F, Tanda M, Kus M et al. Trimetazidine inhibits neutrophil accumulation after myocardial ischemia and reperfusion in rabbits. J. Cardiovasc. Pharm. 1993, 22: 828-833
24. Sentex E, Sergiel J, Lucien A et al. Trimetazidine increase phospholipid turnover in ventricular myocyte. Mol. Cell. Biochem. 1997, 153-162
25. Fantini E, Demaison L, Sentex E et al. Some biochemical aspects of the protective effect of trimetazidine on rat cardiomyocytes during hypoxia and reoxygenation. J. Mol. Cell. Cardiol. 1994, 26: 949-958
26. Kantor P, Lucien A, Kozak R et al. The antianginal drug trimetazidine shifts cardiac energy metabolism from fatty acid oxidation to glucose oxidation by inhibiting mitochondrial long–chain 3–ketoacyl coenzyme A thiolase. Circulation Res. 2000, 17: 580-588
27. Sellier P, Audouin P, Payen B et al. Acute effects of trimetazidine evaluated by exercize testing. Eur. J. Clin. Pharmacol. 1987, 33: 205-207
28. Detry J, Sellier P, Pennaforte S et al. Trimetazidine: a new concept in the treatment of angina. Comparison with propranolol in patients with stable angina. Br. J. Clin. Pharmac. 1994, 37: 279-288
29. Michaelides A, Vyssoulis G, Bonoris P et al. Beneficial effects of trimetazidine in men with stable angina under beta–blocker treatment. Cur. Ther. Res. 1989, 3
30. Michaelides A, Spiropoulos K, Dimopoulus K et al. Antianginal efficacy of the combination of trimetazidine–propranolol compered with isosorbide dinitrate–propranolol in patients with stable angina. Clin. Drug Invest. 1997, 13: 116-122
31. Dalla–Volta S, Maraglino G, Della–Valentina P et al. Comparison of Trimetezidine with nifedipine in effort angina: double–blind, crossover study. Cardiovasc. Drugs and Therapy. 1990, 4: 853-860
32. Levy S. Combination therapy of trimetazidine with diltiazem in patients with coronary artery disease. Am. J. Cardiol. 76:12-16
33. Fabiani J, Ponzio M, Emerit M et al. Cardioprotective effect of trimetazidine during coronary artery graft surgery. J. Cardiovasc. Surg. 1992, 33: 486-491
34. Kober G, Buck T, Sievert H et al. Myocardial protection during percutaneous transluminal coronary angioplasty: effect of trimetazidine. Eur. Heart J. 1992, 13: 1109-1115
35. Steg P, Grollier G, Gallay P et al. A randomized double–blind trial of trimetazidine as adjunctive therapy to primary PTCA for acute myocardial infarction. Evidence for improved myocardial reperfusion from ST–segment analysis. Eur. Heart J. 1998, 19: 365
36. Маколкин В.И., Бузиашвили Ю.И., Осадчий К.К. и др. Сравнение эффективности реваскуляризации и медикаментозной терапии с применением триметазидина в восстановлении функций «спящего» («гибернирующего») миокарда Кардиология. 2001, 5: 18-24
37. Чирчиа С, Фрагассо Г, Дабровски П и др. Влияние триметазидина на дисфункцию левого желудочка при ишемии у пациентов с ишемической болезнью сердца. Am. J. Cardiol. 1998, 82
38. Brottier L, Barat J, Combe C et al. Therapeutic value of a cardioprotective agent in patients with severe ischemic cardiomyopathy. Eur. Heart J. 1990, 11:207-212
39. Терещенко С.Н.,Акимова О.С., Демидова И.В. и др. Цитопротектор триметазидин в комплексной терапии тяжелой постинфарктной хронической сердечной недостаточности. Кардиология. 1999, 9: 48-52
40. Pornin M, Harpey C, Allal J et al. Lack of effects of trimetazidine on systemic heamodynamics in patients with coronary artery disease: a placebo–controlled study. Clinical trials and meta-analysis. 1994, 29:49-56
41. Noble M, Belcher P, Drake et al. Am.J. Cardiol. 1995, 76: 41-44
42. The EMIP–FR GROUP. Effect of 48–h intravenous trimetazidine on short– and long–term outcomes of patients with acute myocardial infarction, with and without thtombolytic therapy. Eur. Heart. J. 2000, 21: 1537-1546
43. Fukuda D, Kawarabayashi T, Tanaka A et al. Lesion characteristics of acute myocardial infarction: an investigation with intravascular ultrasound. Heart. 2001, 85:402-406
44. Asakura M, Ueda Y, Yamaguchi O et al. Extensive development of vulnerable plaques as a pan–coronary process in patients with myocardial infarction: an angioscopic study. J. Am. Coll. Cardiol. 2001, 37:1284-1288
45. Huang H, Virmani R, Younis H et al. The impact of calcification on the biomechanical stability of atherosclerotic plaques. Circulation. 200,103:1051-1056
46. Lopaschuk G. Optimizing cardiac energy metabolism: a new approach to treating ischemic heart disease. Eur. Heart J. Supplements. 1999, 1:32-39
47. McComack J, Barr R, Wolff A et al. Ranolazine stimulates glucose oxidation in normoxic, ischemic and reperfused ischemic rat hearts. Circulation, 1996, 93: 135-142
48. Meehan A, Higgins A. Oleate plus oxfenicine improves functional recovery assessed by an intraventricular balloon, in ischemic reperfused rat hearts. Ann. NY. Acad. Sci. 1994, 723: 343-344
49. Schulze R, Vetter R. Dietery medium chain triglycerides can prevent changes in myosine and SR due to CPT 1 inhibition by etomoxir.
50. ACC/AHA/ACP–ASIM guidlines for the management of patients with chronic stable angina.J.A.C.C. 1999, 33: 2092–2197












