Единственным доказанным способом контроля терапии АВК сегодня является протромбиновый тест с представлением результатов в виде Международного нормализованного отношения (МНО). Система МНО, разработанная ВОЗ, учитывает международный индекс чувствительности тромбопластина, используемого в каждой конкретной лаборатории, что позволяет стандартизировать результаты теста.
В настоящее время доказана эффективность АВК для профилактики тромбоэмболических осложнений у больных мерцательной аритмией (МА), после протезирования клапанов сердца, при вторичной профилактике сердечно–сосудистых эпизодов у больных, перенесших острый коронарный синдром, а также в лечении и профилактике венозных тромбозов.
Применение АВК
при мерцательной аритмии
Основной причиной смерти и инвалидизации больных МА без поражения клапанов сердца является ишемический инсульт (ИИ) и системные тромбоэмболии. По данным крупных исследований, риск инсульта у больных МА возрастает в 6 раз по сравнению с лицами, имеющими синусовый ритм, не зависит от длительности аритмии (т.е. сопоставим в дебюте заболевания и при длительном существовании аритмии) и одинаков для больных с постоянной и пароксизмальной формами МА [1–4]. Кардиоэмболические инсульты у больных МА характеризуются обширным инфарктом мозга, приводящим к выраженному неврологическому дефициту, что влечет за собой в большинстве случаев стойкую инвалидизацию больного [5].
Снижение риска ИИ при терапии Варфарином у больных МА без поражения клапанов сердца доказано крупными рандомизированными исследованиями и составляет 61% [6–10]. Определяющим в выборе тактики антитромботической терапии у каждого конкретного больного МА является наличие факторов риска тромбоэмболических осложнений (табл. 1). В рекомендациях по лечению МА, вышедших в 2006 году, при назначении Варфарина предложено использовать шкалу CHADS, где таким факторам, как недостаточность кровообращения, артериальная гипертония, возраст старше 75 лет и сахарный диабет, присвоен 1 балл, а ИИ/преходящему нарушению мозгового кровообращения или системным эмболиям в анамнезе – 2 балла. Риск инсульта составляет 2,8% в год при наличии одного балла и возрастает до 8,5% в год при наличии 4 баллов по шкале CHADS2 [11].
Эффективность ацетилсалициловой кислоты (АСК) в профилактике инсульта у больных с МА уступает Варфарину. Мета–анализ 5 рандомизированных исследований [8] установил, что назначение АСК снижает риск инсульта у больных МА на 19%. АСК может быть альтернативой АВК у больных с низким риском тромбоэмболий или у больных с противопоказаниями к непрямым антикоагулянтам.
Помимо больных с хронической фибрилляцией предсердий, назначение антикоагулянтов требуется пациентам, которым планируется восстановление синусового ритма. Риск системных тромбоэмболий при кардиоверсии без использования антикоагулянтов доходит до 5%, а использование 4–недельной терапии Варфарином до и после кардиоверсии позволяет уменьшить этот риск до 0,5–0,8% [12–13].
Длительность терапии Варфарином после кардиоверсии связана со способностью больного удерживать синусовый ритм и с наличием у него факторов риска тромбоэмболических осложнений. При частоте пароксизмов МА более одного в месяц больные должны следовать рекомендациям для пациентов с пароксизмальной формой мерцательной аритмии [12–13].
Использование чреспищеводной эхокардиографии позволяет исключить тромб в ушке левого предсердия – основной источник тромбоэмболий у больных МА, что позволяет приблизить проведение кардиоверсии. В таком случае используют гепарин (как нефракционированного, так и низкомолекулярного) или АВК не менее 5 дней (до получения двухкратных значений МНО в целевом диапазоне 2,0–3,0). После кардиоверсии терапия АВК должна быть продолжена, по меньшей мере, в течение 4 или более недель в зависимости от ритма и наличия факторов риска тромбоэмболий.
Проведение 4–недельной терапии Варфарином требуется и в случае выполнения кардиоверсии без предварительного назначения АВК (длительность пароксизма менее 48 часов или в случае остро возникшего пароксизма МА, сопровождающегося нестабильной гемодинамикой).
АВК у больных с искусственными клапанами сердца
Основную опасность для жизни больных с искусственными клапанами сердца составляют тромбоэмболические осложнения, источником которых являются тромбы, образующиеся на поверхности протеза клапана. Риск тромбоза искусственного клапана – жизнеугрожающего осложнения в отсутствие терапии АВК достигает 8–22% в год [14]. Назначение Варфарина позволяет снизить риск тромбоэмболий на 75% [15], поэтому при установке механических протезов клапанов сердца АВК обязательны и не могут быть заменены АСК. Исключение составляют больные с биопротезами без факторов риска тромбоэмболических осложнений, длительность терапии АВК у которых составляет 3 месяца. Во всех остальных случаях лечение должно быть пожизненным. Факторами риска для больных с искусственными клапанами сердца являются тромбоэмболии в анамнезе, МА, недостаточность кровообращения, атриомегалия. Уровень антикоагуляции в подавляющем большинстве случаев должен соответствовать диапазону МНО 2,5–3,5. Исключение составляют больные после имплантации протеза аортального клапана «Saint–Jude», при отсутствии у них других факторов риска тромбоэмбролий (в этом случае целевой диапазон МНО 2,0–3,0) [15].
АВК в лечении венозного тромбоза
Длительность лечения Варфарином после первого эпизода тромбоза глубоких вен составляет, как минимум, 3 месяца. При наличии высокого риска рецидива тромбоза (проксимальная локализация тромба, повторные эпизоды венозных тромбозов, перенесенная тромбоэмболия легочной артерии или ее ветвей, наличие постоянных причин для активации системы свертывания крови) – 6 месяцев, а в ряде случаев (наличие онкологического заболевания, антифосфолипидный синдром, тромбофилии) должна быть пожизненной. Уровень антикоагуляции для профилактики рецидивов венозного тромбоза соответствует МНО 2,0–3,0 [16].
АВК при вторичной
профилактике ИБС
Эффективность Варфарина при вторичной профилактике ИБС изучалась в исследованиях ASPECT–2, APRICOT–2, WARIS–II, CHAMP. Данные исследования отличались по дизайну, режимам антикоагуляции, наличию сопутствующей терапии АСК и дозой последнего. Эффективность комбинации Варфарина и АСК была выше, чем монотерапия АСК, однако риск геморрагических осложнений был выше в группе комбинированной терапии. В связи с этим в рутинной клинической практике назначение Варфарина больным после острого коронарного синдрома нашло свое применение в особых случаях – при непереносимости антиагрегантов, а также при наличии тромбофилии или дополнительных показаний к терапии АВК [16].
Практические аспекты терапии АВК
Терапия Варфарином должна отвечать двум требованиям:
1) эффективная и безопасная доза должна быть подобрана в течение первого месяца терапии;
2) поддерживающая доза должна подбираться в соответствии с возможными изменениями веса, диеты, соматического статуса и с учетом совместного назначения других лекарственных средств.
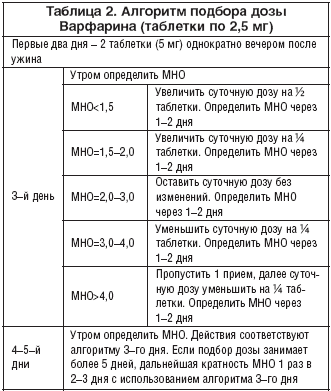
Начало терапии Варфарином предусматривает назначение насыщающей дозы 5–7,5 мг в течение первых двух дней с дальнейшим титрованием дозы, ориентируясь на достигнутый уровень МНО (табл. 2). Меньшие стартовые дозы Варфарина (5 мг и менее) рекомендуются больным старше 70 лет, имеющим низкую массу тела, хроническую сердечную или почечную недостаточность, а также при исходном нарушении функции печени, совместном приеме амиодарона, а также у больных, недавно перенесших хирургическую операцию.
Назначение сразу высоких стартовых доз Варфарина (10 мг и более) не рекомендуется, так как в начале терапии АВК происходит снижение уровня естественного антикоагулянта протеина С, что может привести к развитию венозного тромбоза.
Во время подбора дозы контроль МНО осуществляется 1 раз в 2–3 дня. После получения результатов МНО в пределах целевого диапазона дважды доза Варфарина считается подобранной, и в дальнейшем контроль МНО осуществляется 1 раз в месяц.
Целевой диапазон МНО для больных МА без поражения клапанов сердца и после перенесенного венозного тромбоза при применении Варфарина без антиагрегантов составляет 2,0–3,0, при их сочетании с одним антиагрегантом 2,0–3,0, при сочетании с двумя антиагрегантами 2,0–2,5. У больных после имплантации искусственных клапанов сердца в большинстве случаев целевое МНО составляет 2,5–3,5.
Для больных с антифосфолипидным синдромом, не имеющих дополнительных факторов риска, целевое МНО составляет 2,0–3,0. Для пациентов, перенесших тромботические осложнения, несмотря на антикоагулянтную терапию, целесообразно увеличить средние значения МНО до 3,0 [16].
В настоящее время выявлены полиморфизмы в основном гене биотрансформации Варфарина CYP2C9 и молекуле–мишени его действия VKORC1. Носителям мутантных аллелей требуется меньшая поддерживающая доза Варфарина, при этом частота кровотечений и эпизодов чрезмерной гипокоагуляции у них выше. В настоящее время проводятся исследования, цель которых – определить, имеет ли преимущество фармакогенетический подход перед стандартным эмпирическим подбором дозы Варфарина. Однако в рекомендациях АССР 2008 года говорится, что в отсутствие в настоящее время данных специальных рандомизированных исследований использование для всех больных фармакогенетического подхода к назначению АВК не оправдано [16].
Перед назначением Варфарина необходимо оценить наличие противопоказаний. Абсолютными противопоказаниями к назначению Варфарина являются аллергия на препарат, геморрагический инсульт в анамнезе, активное кровотечение, тромбоцитопения (количество тромбоцитов менее 100 тысяч). Все остальные состояния являются относительными противопоказаниями, и выбор осуществляется на основании индивидуального соотношения пользы и риска кровотечений.
Перед назначением Варфарина необходимо уточнить, были ли у больного геморрагические осложнения в анамнезе, провести обследование, направленное на уточнение состояния потенциальных источников кровотечения. При подтверждении отсутствия риска кровотечения в настоящее время Варфарин может быть назначен. План обязательного и дополнительного обследований, позволяющих определить противопоказания и уточнить состояние потенциальных источников кровотечений, представлен на рисунке 1.
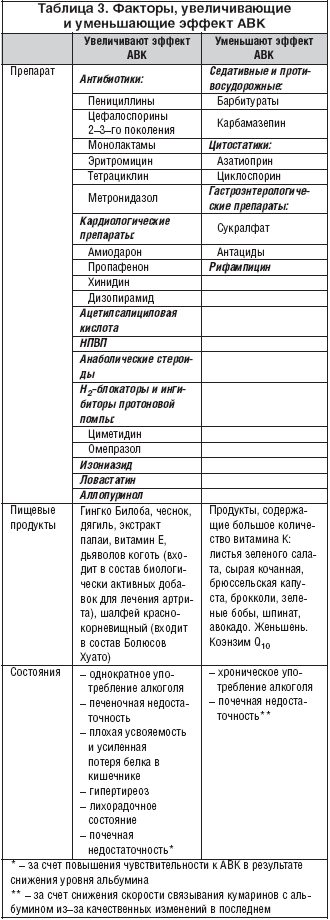
Варфарин является лекарством, для которого характерны межиндивидуальные различия в лекарственном ответе, обусловленные целым рядом факторов, как внешних (диета, лекарственные взаимодействия), так и внутренних (соматическое состояние пациента, возраст), а также генетически обусловленных. Для исключения нежелательных лекарственных взаимодействий при назначении сопутствующей терапии предпочтение следует отдавать препаратам, действие которых на антикоагулянтный эффект Варфарина незначителен (табл. 3). Использование препаратов, влияющих на метаболизм АВК, требует контроля МНО через 3–5 дней и при необходимости – коррекции дозы Варфарина.
Больные, принимающие антикоагулянты, нуждаются в системе патронажа, что обусловлено необходимостью регулярного контроля МНО, коррекции дозы препарата и оценки других факторов, влияющих на значения МНО.
Колебание значений МНО может быть обусловлено несколькими факторами:
• лабораторная погрешность
• изменение потребления витамина К с пищей
• влияние изменений соматического статуса, приема лекарственных препаратов и веществ растительного происхождения на метаболизм Варфарина
• отсутствие приверженности лечению Варфарином.
Наиболее частой причиной, объясняющей отсутствие адекватной антикоагуляции при терапии Варфарином, является плохая приверженность пациентов лечению, высокое содержание витамина К в пище и прием препаратов, повышающих активность фермента СYP2C9 (барбитураты, карбамазепин) [17–18].
Для исключения пищевых взаимодействий следует рекомендовать пациентам, принимающим Варфарин:
• придерживаться одинакового режима питания
• ограничить потребление сырых овощей (не более 250 мкг/сут. в пересчете на содержание витамина К1)
• принимая поливитамины, выбирать препарат, не содержащий витамин К1
• в случае употребления алкоголя не превышать его более 25 г в сутки в пересчете на этанол.
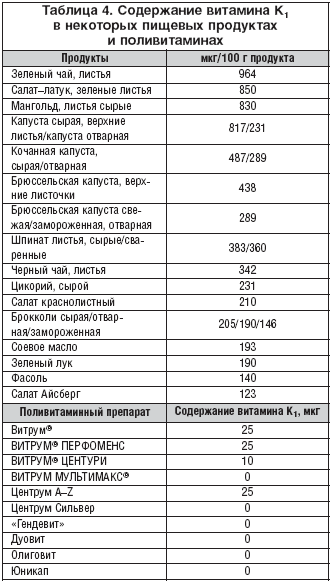
Содержание витамина К1 в некоторых пищевых продуктах и поливитаминах указано в таблице 4.
Значения МНО от измерения к измерению, у одного и того же больного могут меняться внутри терапевтического диапазона. Колебания МНО, незначительно выходящие за пределы терапевтического диапазона (1,9–3,2), не являются основанием для изменения дозы препарата. Во избежание значительных колебаний уровня антикоагуляции целесообразно уменьшение дозировки Варфарина при значениях МНО более 3,0, но менее 4,0, не пропуская при этом очередной прием препарата.
Для больных, длительно принимающих Варфарин и имеющих значительные колебания МНО, которые нельзя объяснить стандартными причинами, рекомендовано использование ежедневно небольших доз витамина К (100–200 мкг), что может способствовать стабилизации уровня МНО [16].
Вопрос о том, что считать истинной резистентностью к Варфарину, остается до настоящего времени открытым. Возможно, стоит говорить об истинной резистентности, если назначение дозы Варфарина, превышающей 20 мг в сутки, не привело к достижению терапевтического уровня антикоагуляции. Это так называемая фармакодинамическая (или истинная) резистентность, что может быть подтверждено выявлением высокой концентрации Варфарина в плазме крови при отсутствии повышения значений МНО. Число таких случаев среди больных, по данным специализированных исследований, не превышает 1% [19–21].
Риск кровотечений при терапии АВК
Развитие геморрагических осложнений является наиболее грозным осложнением терапии АВК и основной причиной неназначения препаратов этой группы. Очень редко встречаются негеморрагические побочные действия Варфарина – аллергические реакции (зуд, сыпь), желудочно–кишечные расстройства (тошнота, рвота, боли в животе), преходящее облысение [16].
Основными факторами риска геморрагических осложнений являются степень гипокоагуляции, пожилой возраст, взаимодействия с другими лекарственными препаратами и инвазиными вмешательствами, а также начало терапии [16,22–25].
Возникновение большого кровотечения (т.е. приведшего к смерти, нарушениям сердечной/дыхательной деятельности, другим необратимым последствиям, потребовавшего хирургического лечения или переливания крови) всегда требует срочной госпитализации больного для поиска причины кровотечения и его остановки. Возобновление терапии Варфарином после большого кровотечения возможно лишь в том случае, если причина кровотечения найдена и устранена. Целевой диапазон МНО при этом должен быть снижен до 2,0–2,5.
Возникновение малых геморрагических осложнений (любого внутреннего или наружного кровотечения, не потребовавшего госпитализации, дополнительного обследования и лечения) требует временной отмены Варфарина вплоть до остановки кровотечения, поиска возможной причины кровотечения и коррекции дозы Варфарина. Возобновить терапию Варфарином после остановки малого кровотечения можно при МНО<3,5. В случае рецидивирования малых геморрагий целевой уровень МНО необходимо снизить до 2,0–2,5.
Чрезмерная антикоагуляция является предиктором развития кровотечений, поэтому внимания врача требует любое, даже бессимптомное увеличение уровня МНО выше терапевтического диапазона.
Тактика врача при бессимптомном повышении МНО и развитии кровотечений определяется степенью гипокоагуляции, наличием потенциальных источников кровотечений и необходимостью инвазивных вмешательств в ближайшее время, и в соответствии с последними рекомендациями 2008 года [16] предусматривает отмену антикоагулянтов, пероральное назначение фитоменадиона (витамина К1), внутривенное введение концентрата протромбинового комплекса, рекомбинантного VII фактора, свежезамороженной плазмы (табл. 5). К сожалению, в нашей стране из предлагаемой схемы возможно осуществить лишь отмену Варфарина и введение свежезамороженной плазмы. Концентрат протромбинового комплекса и пероральная форма витамина К1 (в дозе 1–2 мг), назначение которых позволяет в течение суток снизить МНО, не зарегистрированы в России и отсутствуют на отечественном фармацевтическом рынке.
Имеющийся в России препарат викасол не является аналогом пероральной формы витамина К1. Викасол способствует синтезу витамин К–зависимых факторов свертывания de novo за счет влияния на процессы карбоксилирования, поэтому эффект после его приема наступает медленно и он бесполезен для быстрого восстановления витамин К–зависимых факторов свертывания. Имеющийся в распоряжении врачей отечественный препарат фитоменадион в капсулах по 0,1 г, содержащий 10% раствор в масле витамина К1, не может использоваться с целью снижения уровня МНО, т.к. доза витамина К1, равная 10 мг, вызывает резистентность к действию АВК в течение 7–10 дней.
Однако достаточно часто повышение МНО не сопровождается кровотечением и требует контроля МНО и коррекции дозы Варфарина. Необходимо уточнить у больного возможные причины повышения МНО, а также контролировать состояние потенциальных источников кровотечений.
Риск кровотечений возрастает при проведении любых инвазивных вмешательств – стоматологические, офтальмологические, урологические процедуры, фиброскопия с проведением биопсии, любые операции, ангиография, внутримышечные инъекции.
Мерой, позволяющей снизить риск периоперационных кровотечений, является замена АВК на терапию гепарином (как нефракционированного, так и низкомолекулярного). Для принятия решения о временной отмене Варфарина или замене его на гепарин необходимо оценить риск кровотечения во время вмешательства и тромбоэмболический риск.
У больных с низким риском тромбоэмболий (мерцательная аритмия в отсутствие факторов риска тромбоэмболических осложнений) Варфарин может быть отменен на срок 5–7 дней. Инвазивное вмешательство можно проводить при уровне МНО <1,5.
У больных высокого риска тромбоэмболий (больные с искусственными клапанами сердца, мерцательной аритмией при наличии факторов риска тромбоэмболий, перенесшие тромбоз глубоких вен или тромбоэмболию легочной артерии) при необходимости инвазивного вмешательства антикоагулянты следует заменять на гепарин (нефракционированный или низкомолекулярный) в дозах, применяемых для лечения венозного тромбоза.
Низкомолекулярный гепарин следует отменить за 24 часа до оперативного вмешательства, при этом лучше использовать половинную дозу в качестве последней инъекции. В случае использования внутривенного введения нефракциониронанного гепарина в качестве периоперационной замены Варфарину отменить гепарин необходимо, по крайней мере, за 4 часа до вмешательства.
Больным после малых хирургических вмешательств или после инвазивных процедур гепарин с низкими молекулярным весом можно возобновить через 24 часа. Больным после большого хирургического вмешательства или имеющим повышенный риск кровотечения рекомендуется отложить возобновление гепаринотерапии до 48–72 часов для обеспечения адекватного гемостаза. На основании индивидуальной оценки риска кровотечения, наличия адекватного гемостаза время возобновления гепаринотерапии в особых случаях может откладываться.
Больным перед предстоящими стоматологическими операциями можно продолжать прием Варфарина в случае использования местно гемостатической губки и обеспечении адекватного местного гемостаза. Однако, по собственному мнению автора, более безопасным для пациента является временная отмена Варфарина на 2–3 дня с возобновлением терапии сразу после процедуры.
Для домашнего контроля в настоящее время существуют портативные приборы для измерения уровня МНО. Мета–анализ, проведенный Heneghan в 2006 г. [26], показал, что самоконтроль МНО улучшает исходы больных, получающих Варфарин. Но для большинства пациентов нашей страны стоимость портативных коагулометров достаточно высока, и вряд ли они смогут заменить в ближайшее время стационарный и амбулаторный лабораторный контроль МНО.
Заключение
В настоящее время Варфарин является основным препаратом для профилактики тромбоэмболических осложнений у больных МА, после протезирования клапанов сердца, у лиц после перенесенного венозного тромбоза. Определяющим в вопросе эффективности терапии антагонистами витамина К является целевой диапазон МНО, достичь которого необходимо стараться у каждого больного. Частота геморрагических осложнений, а также необходимость постоянного лабораторного контроля является главной причиной неназначения или отмены Варфарина в реальной клинической практике. Однако отказ от антикоагулянтной терапии приводит к развитию тромбоэмболических осложнений, смерти и стойкой инвалидизации больного. Существующие алгоритмы подбора индивидуальной поддерживающей дозы Варфарина, система патронажа и регулярного лабораторного контроля МНО позволяют повысить безопасность антикоагулянтной терапии.



Литература
1. Wolf PA, Dawber TR, Thomas E Jr et al “ Epidimiologic assessment of chronic atrial fibrillation and risk of stroke: The Framingham Study” Neurology 1978; 28:973–977.
2. Onundarson PT, Thorgeirsson G, Jonmundsson E et al “Chronic atrial fibrillation – Epidimiologic features and 14 year follow–up: A case control study” Eur Heart J 1987; 3:521–27 .
3. Flegel KM, Shipley MJ, Rose G “Risk of stroke in non–rheumatic atrial fibrillation” Lancet 1987; 1:526–529.
4. Tanaka H, Hayashi M, Date C. et al “Epidemiologic studies of stroke in Shibata, a Japanese provincial city: Preliminary report on risk factors for cerebral infarction”. Stroke 1985; 16: 773–780
5. E.M. Hylek, M.D., M.P.H., Alan S. Go, M.D., Yuchiao Chang, Ph.D., et al “Effect of Intensity of Oral Anticoagulation on Stroke Severity and Mortality in Atrial Fibrillation” NEJM 2003 , N11,Vol 349:1019–1026.
6. Petersen P., Boysen G., Godtfredsen J. et al. “Placebo–controlled, randomised trial of warfarin and aspirin for prevention of thromboembolic complications in chronic atrial fibrillation. The Copenhagen AFASAK study” Lancet 1989 Jan 28;1(8631):175–9.
7. Secondary prevention in nonrheumatic atrial fibrillation and transient ischemic attack or minor stroke. EAFT (European Atrial Fibrillation Trial) Study Group. Lancet 1993; 342: 1255–1262.
8. Hart RG, Pearce LA, McBride R, et al “Factors associated with ischemic stroke during aspirin therapy in atrial fibrillation: analysis of 2012 participants in the SPAF I–III clinical trials. The Stroke Prevention in Atrial Fibrillation (SPAF) Investigators” Stroke 1999 Jun;30(6):1223–9 The effect of low–dose warfarin on the risk of stroke in patients with nonrheumatic atrial fibrillation”
9. The Boston Area Anticoagulation Trial for Atrial Fibrillation Investigators NEJM 1990 Nov 29: Vol 323:1505–1511.
10. Ezekowitz M.D., MD., Ph.D., Bridgers S.L., MD., Javes K.E., Ph.D., et al. “Warfarin in the prevention of stroke associated with nonrheumatic atrial fibrillation” NEJM 1992 Nov 12 Vol 327 N 20: 1406–13
11. ACC/AHA/ESC guidelines for the management of patients with atrial fibrillation. JACC 2006; 48:854–906
12. Manning WJ, Silverman DI, Keighley CS, et al “Transesophageal echocardiographically facilitated early cardioversion from atrial fibrillation using short term anticoagulation : final results of a prospective 4,5–year study” J Am Coll Cardiol 1995 May; 25(6):1354–61
13. Arnold AZ, Mick MJ, Mazurek RP. “Role of prophylactic anti–coagulation for direct cardioversion in patients with atrial fibrillation or atrial flutter”. J Am Coll Cardiol. 1992;19: 851–855
14. Дземешкевич С.Л, Панченко Е.П. “Антикоагулянтная терапия у пациентов с клапанными пороками сердца” РМЖ, 2001,Том 9 № 10, 427–430
15. Hirsh J., Fuster V., Ancell J., Halperin J.L. ACC/AHA/ Foundation guide to warfarin therapy Circulation 2003;107:1692–1711
16. Ansell J, Hirsh, Hylek E.M. et al “Pharmacology and Management of the vitamin K antagonists: American college of Chest Physicians Evidence–Based Clinical Practice Guidelines (8th Edition)” Chest 2008;133;160–198
17. Bolton–Smith C, Price RJ, Fenton ST, et al “ Compilation of a provisional UK database for the phylloquinone (vitamin K1) content of foods” Br J Nutr. 2000;83: 389–399.
18. Holbrook A. M., MD, PharmD, MSc, FRCPC; Jennifer A. Pereira, MSc; Renee Labiris, PhD et al “Systematic Overview of Warfarin and Its Drugand Food Interactions” Arch Intern Med, 2005, 165, 1095–1106
19. Rieder MJ, Reiner AP, Gage BF, et al “ Effect of VKORC1 haplotypes on transcriptional regulation and warfarin dose. “N Engl J Med. 2005 Jun 2;352(22):2285–93.
20. Harrington, D.J., Underwood, S., Morse, C., et al “Pharmacodynamic resistance to warfarin associatedwith a Val66Met substitution in vitamin K epoxide reductase complex subunit 1. “ Thromb. Haemost. 93, 23–6 (2005).
21. Bodin, L., Horellou, M.H., Flaujac, C.,et al “A vitamin K epoxide reductase complex subunit–1 (VKORC1) mutation in a patient with vitamin K antagonist resistance.” J. Thromb. Haemost. 3,1533–1535 (2005).
22. Fihn S.D., McDommel M., Matin D. et al “Risk factors fоr complications of chronic anticoagulation. A multicenter study. Warfarin Optimized Outpatient Follow–up Study Groop” Ann Intern Med 1993; 118(7);511–20
23. Mhairi Copland, BSc, MBChB, MRCP; Walker I.D., MD, FRCP, FRCPath; Campbell R., BSc, FRCP, MRCPath “Oral Anticoagulation and Hemorrhagic Complications in an Elderly Population With Atrial Fibrillation” Arch Inter Med Vol. 161 N17, 24, 2001
24. Levine M.N., Raskob G., Landefeld S., Kearon C. “Hemorrhagic complication of anticoagulant treatment” Chest 2001 Jan;1 19(1 Suppl):108S–121S
25. Palareti G, Leali N, Coccheri S, Poggi M, et al. “Hemorrhagic complications of oral anticoagulant therapy: results of a prospective multicenter study ISCOAT (Italian Study on Complications of Oral Anticoagulant Therapy)” G Ital Cardiol. 1997 Mar;27(3):231–43.
26. Heneghan C, Alonso–Coello P, Garcia–Alamino JM, et al “Self–monitoring of oral anticoagulation: a systematic review and meta–analysis”. The Lancet 2006; 367:404–411












