–Р–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П – –±–Њ–ї—М—И–∞—П –≥—А—Г–њ–њ–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Њ—Б–љ–Њ–≤–љ—Л–Љ —Б–≤–Њ–є—Б—В–≤–Њ–Љ –Ї–Њ—В–Њ—А—Л—Е —П–≤–ї—П–µ—В—Б—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Њ–±—А–∞—В–Є–Љ–Њ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞—В—М —В–Њ–Ї –Ї–∞–ї—М—Ж–Є—П —З–µ—А–µ–Ј —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–µ –Љ–µ–і–ї–µ–љ–љ—Л–µ –Ї–∞–ї—М—Ж–Є–µ–≤—Л–µ –Ї–∞–љ–∞–ї—Л. –≠—В–Є –њ—А–µ–њ–∞—А–∞—В—Л –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –≤ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є–Є —Б –Ї–Њ–љ—Ж–∞ 70–—Е –≥–Њ–і–Њ–≤ XX –≤–µ–Ї–∞ –Є –Ї –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є –њ—А–Є–Њ–±—А–µ–ї–Є —В–∞–Ї—Г—О –њ–Њ–њ—Г–ї—П—А–љ–Њ—Б—В—М, —З—В–Њ –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —А–∞–Ј–≤–Є—В—Л—Е —Б—В—А–∞–љ –Ј–∞–љ–Є–Љ–∞—О—В –Њ–і–љ–Њ –Є–Ј –њ–µ—А–≤—Л—Е –Љ–µ—Б—В –њ–Њ —З–∞—Б—В–Њ—В–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П —Б—А–µ–і–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Є—Б–њ–Њ–ї—М–Ј—Г—О—Й–Є—Е—Б—П –і–ї—П –ї–µ—З–µ–љ–Є—П –°–°–Ч. –≠—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ, —Б –Њ–і–љ–Њ–є —Б—В–Њ—А–Њ–љ—Л, –≤—Л—Б–Њ–Ї–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П, —Б –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л – –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–µ–±–Њ–ї—М—И–Є–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–є –Ї –Є—Е –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –Є —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ –Љ–∞–ї—Л–Љ —З–Є—Б–ї–Њ–Љ –≤—Л–Ј—Л–≤–∞–µ–Љ—Л—Е –Є–Љ–Є –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –°—А–µ–і–Є –Р–Ъ –Њ—Б–Њ–±–Њ–µ –Љ–µ—Б—В–Њ –Ј–∞–љ–Є–Љ–∞–µ—В –∞–Љ–ї–Њ–і–Є–њ–Є–љ («–Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ», Gedeon Richter), –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї—М 3––≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –Њ–±–ї–∞–і–∞—О—Й–Є–є –љ–∞–Є–±–Њ–ї–µ–µ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, –Ї–∞–Ї –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–Љ, —В–∞–Ї –Є –∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ, –Є —Г—Б–њ–µ—И–љ–Њ –њ—А–Њ—И–µ–і—И–Є–є –≤—Б–µ—Б—В–Њ—А–Њ–љ–µ–љ–љ–µ–µ –Є–Ј—Г—З–µ–љ–Є–µ –≤–Њ –Љ–љ–Њ–≥–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е.
–Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ – –∞–љ—В–∞–≥–Њ–љ–Є—Б—В –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤ –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞ —В—А–µ—В—М–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –±–ї–Њ–Ї–Є—А—Г–µ—В –Љ–µ–і–ї–µ–љ–љ—Л–µ –Ї–∞–ї—М—Ж–Є–µ–≤—Л–µ –Ї–∞–љ–∞–ї—Л (–Ї–∞–љ–∞–ї—Л L–—В–Є–њ–∞) –Є –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–Њ–є –≥–Є–њ–µ—А–Ї–∞–ї—М—Ж–Є–µ–Љ–Є–Є –Є —Б–Њ–Ї—А–∞—Й–µ–љ–Є—О –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ–Њ–є –Ї–ї–µ—В–Ї–Є, –Њ–Ї–∞–Ј—Л–≤–∞—П —Б–Њ—Б—Г–і–Њ—А–∞—Б—И–Є—А—П—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ. –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ –Њ–±–ї–∞–і–∞–µ—В –і–ї–Є—В–µ–ї—М–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–Є–Љ–µ–љ—П—В—М –µ–≥–Њ –Њ–і–Є–љ —А–∞–Ј –≤ —Б—Г—В–Ї–Є. –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ —Б–љ–Є–ґ–∞–µ—В –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ, –љ–µ –≤–ї–Є—П—П –љ–∞ —З–∞—Б—В–Њ—В—Г —Б–Њ–Ї—А–∞—Й–µ–љ–Є–є —Б–µ—А–і—Ж–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є. –Я—А–Є–Љ–µ–љ—П–µ—В—Б—П —В–∞–Ї–ґ–µ –≤ –ї–µ—З–µ–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–µ–є –љ–∞–њ—А—П–ґ–µ–љ–Є—П, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –њ—А–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ –≤–∞–Ј–Њ—Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–µ –Є—И–µ–Љ–Є–Є. –Я—А–µ–њ–∞—А–∞—В —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П, –≤—Л–Ј—Л–≤–∞—П –љ–µ–±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Я—А–Є–Љ–µ–љ—П–µ—В—Б—П –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –і—А—Г–≥–Є–Љ–Є –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ—Л–Љ–Є –Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є.
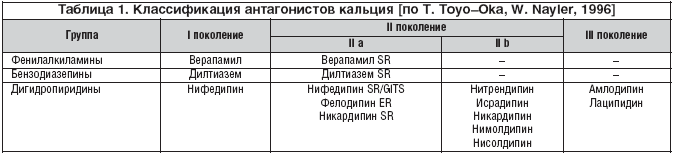
–Ъ–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П
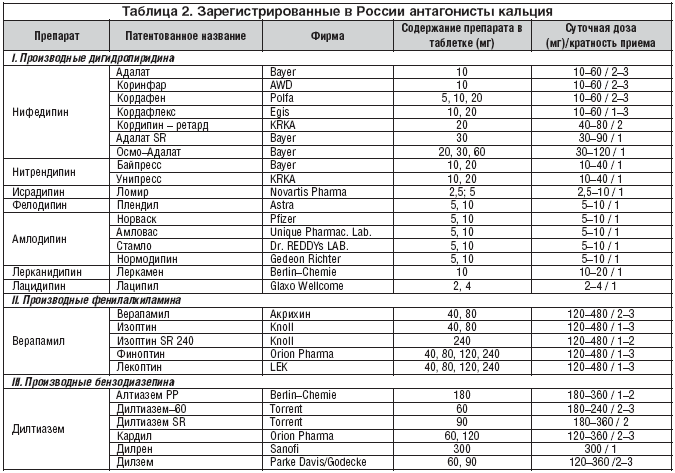
–°—Г—Й–µ—Б—В–≤—Г—О—В —А–∞–Ј–ї–Є—З–љ—Л–µ –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П. –Я–Њ —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–µ —А–∞–Ј–ї–Є—З–∞—О—В: –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–µ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П (–љ–Є—Д–µ–і–Є–њ–Є–љ, –љ–Є–Ї–∞—А–і–Є–њ–Є–љ, —Д–µ–ї–Њ–і–Є–њ–Є–љ, –ї–∞—Ж–Є–і–Є–њ–Є–љ, –∞–Љ–ї–Њ–і–Є–њ–Є–љ –Є –і—А.), –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–∞ (–і–Є–ї—В–Є–∞–Ј–µ–Љ) –Є —Д–µ–љ–Є–ї–∞–ї–Ї–Є–ї–∞–Љ–Є–љ—Л (–≤–µ—А–∞–њ–∞–Љ–Є–ї) (—В–∞–±–ї. 1, 2).
–§–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–∞
–Я—А–Є –њ—А–Є–µ–Љ–µ –≤–љ—Г—В—А—М –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ –Љ–µ–і–ї–µ–љ–љ–Њ –Є –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ–Њ–ї–љ–Њ—Б—В—М—О –≤—Б–∞—Б—Л–≤–∞–µ—В—Б—П –Є–Ј –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є. –С–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ –≤—Л—Б–Њ–Ї–∞ –Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ—В 60 –і–Њ 80%. –Ю–±—К–µ–Љ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ —А–∞–≤–µ–љ –≤ —Б—А–µ–і–љ–µ–Љ 20–21 –ї/–Ї–≥ –Љ–∞—Б—Б—Л —В–µ–ї–∞, —З—В–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –±–Њ–ї—М—И–µ, —З–µ–Љ —Г –і—А—Г–≥–Є—Е –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–µ–є –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞. –Т —Б—Л–≤–Њ—А–Њ—В–Ї–µ 95–98% –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П —Б –±–µ–ї–Ї–∞–Љ–Є –њ–ї–∞–Ј–Љ—Л. –Ь–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ –≤ –Ї—А–Њ–≤–Є –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П —З–µ—А–µ–Ј 6–12 —З –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞. –Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–µ–є—Б—В–≤–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –µ–≥–Њ –Љ–µ–і–ї–µ–љ–љ—Л–Љ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ–Љ –Є–Ј —Б–≤—П–Ј–Є —Б —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є.
–С–Є–Њ—В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є—П –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ –і–Њ –љ–µ–∞–Ї—В–Є–≤–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≤ –њ–µ—З–µ–љ–Є. –Т—Л–≤–Њ–і–Є—В—Б—П –њ—А–µ–њ–∞—А–∞—В —Б –Љ–Њ—З–Њ–є (–Њ–Ї–Њ–ї–Њ 10% –≤ –љ–µ–Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–Љ –≤–Є–і–µ –Є –Њ–Ї–Њ–ї–Њ 60% –≤ –≤–Є–і–µ –љ–µ–∞–Ї—В–Є–≤–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤) –Є —Б —Д–µ–Ї–∞–ї–Є—П–Љ–Є. –Я–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ —А–∞–≤–µ–љ 35–50 —З. –°—В–∞–±–Є–ї—М–љ–∞—П —А–∞–≤–љ–Њ–≤–µ—Б–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П (steady–state) –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П —З–µ—А–µ–Ј 7–8 –і–љ–µ–є –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞. –Я—А–Є –љ–∞—А—Г—И–µ–љ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є –≤—А–µ–Љ—П –≤—Л–≤–µ–і–µ–љ–Є—П –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П, —З—В–Њ —Е–∞—А–∞–Ї—В–µ—А–љ–Њ –Є –і–ї—П –і—А—Г–≥–Є—Е –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞. –Я—А–Є –њ—А–Є–µ–Љ–µ –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ –љ–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –љ–∞—А—Г—И–µ–љ–Є—П —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В–Є –Ї –≥–ї—О–Ї–Њ–Ј–µ, –њ–Њ—Н—В–Њ–Љ—Г –њ—А–µ–њ–∞—А–∞—В –Љ–Њ–ґ–µ—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ, –∞ —В–∞–Ї–ґ–µ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ–Њ–є –Є –њ–Њ–і–∞–≥—А–Њ–є.
–§–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є–Ї–∞
–Т–ї–Є—П–љ–Є–µ –љ–∞ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ
–Є —З–∞—Б—В–Њ—В—Г —Б–Њ–Ї—А–∞—Й–µ–љ–Є–є —Б–µ—А–і—Ж–∞
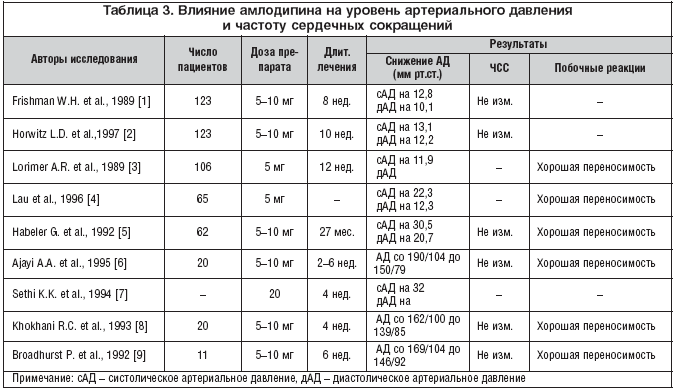
–Т —В–∞–±–ї–Є—Ж–µ 3 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ –≤–ї–Є—П–љ–Є–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –љ–∞ —Г—А–Њ–≤–µ–љ—М —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф, –І–°–° –Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞.
–Т–ї–Є—П–љ–Є–µ –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ (–≤ –≤–Є–і–µ –±–ї–Њ–Ї–Є—А–Њ–≤–∞–љ–Є—П –Љ–µ–і–ї–µ–љ–љ—Л—Е –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤ –Є —Б–љ–Є–ґ–µ–љ–Є—П –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–Њ–є –≥–Є–њ–µ—А–Ї–∞–ї—М—Ж–Є–µ–Љ–Є–Є) –≤ 80 —А–∞–Ј –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–Њ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї —Б–Њ—Б—Г–і–Њ–≤ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ—Л–Љ –Љ–Є–Њ–Ї–∞—А–і–Њ–Љ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б–љ–Є–ґ–µ–љ–Є–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Є–Љ–µ–љ–љ–Њ –≤—Б–ї–µ–і—Б—В–≤–Є–µ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є–Є. –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ –Њ–±–ї–∞–і–∞–µ—В –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Ї–∞–Ї —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ, —В–∞–Ї –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П. –Ю–і–љ–∞–Ї–Њ —Б—В–µ–њ–µ–љ—М —Б–љ–Є–ґ–µ–љ–Є—П –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П —А–∞–Ј–ї–Є—З–∞–µ—В—Б—П, –њ–Њ –і–∞–љ–љ—Л–Љ —А–∞–Ј–љ—Л—Е –∞–≤—В–Њ—А–Њ–≤. –Ґ–∞–Ї, –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Horwitz L.D. et al. [2] –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є 5–10 –Љ–≥ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –≤ —В–µ—З–µ–љ–Є–µ 10 –љ–µ–і. —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–Њ 13,1 –Љ–Љ —А—В. —Б—В., –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ – 12,2 –Љ–Љ —А—В.—Б—В., –∞ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Habeler G. et al. [5] –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —В–∞–Ї–Њ–є –ґ–µ –і–Њ–Ј—Л –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –≤ —В–µ—З–µ–љ–Є–µ 27 –Љ–µ—Б. —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ –њ–Њ–љ–Є–Ј–Є–ї–Њ—Б—М –љ–∞ 30,5 –Љ–Љ —А—В.—Б—В., –∞ —Б–љ–Є–ґ–µ–љ–Є–µ –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–∞–≤–Є–ї–Њ 20,7 –Љ–Љ —А—В.—Б—В.
–Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ –Њ–±–ї–∞–і–∞–µ—В –і–ї–Є—В–µ–ї—М–љ—Л–Љ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –Ј–∞ —Б—З–µ—В –±–Њ–ї—М—И–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П (35–50 —З), —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –µ–Љ—Г –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ –≤ —В–µ—З–µ–љ–Є–µ —Б—Г—В–Њ–Ї. –≠—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ –±–Њ–ї—М—И–µ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Ї–Њ–љ—В—А–Њ–ї—П —А–∞–љ–љ–µ–≥–Њ —Г—В—А–µ–љ–љ–µ–≥–Њ –њ–Њ–і—К–µ–Љ–∞ –Р–Ф –≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≤—А–µ–Љ–µ–љ–Є –њ—А–Є–µ–Љ–∞ (—Г—В—А–Њ–Љ –Є–ї–Є –≤–µ—З–µ—А–Њ–Љ –Њ–і–Є–љ —А–∞–Ј –≤ —Б—Г—В–Ї–Є) [10–12]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Leenen F.H. et al. –њ—А–Є –њ–µ—А–µ—А—Л–≤–µ –≤ –ї–µ—З–µ–љ–Є–Є –Р–Ф —Б–Њ—Е—А–∞–љ—П–ї–Њ—Б—М –≤ –њ—А–µ–і–µ–ї–∞—Е –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е —Ж–Є—Д—А –і–∞–ґ–µ –љ–∞ –≤—В–Њ—А—Л–µ —Б—Г—В–Ї–Є –њ–Њ—Б–ї–µ –Њ—В–Љ–µ–љ—Л –њ—А–µ–њ–∞—А–∞—В–∞ [13]. –Ь–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –њ—А–Є —В–µ—А–∞–њ–Є–Є 5 –Љ–≥ –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ –љ–∞—Б—В—Г–њ–∞–µ—В –ї–Є—И—М –љ–∞ 6––є –љ–µ–і–µ–ї–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞, —З—В–Њ –і–µ–ї–∞–µ—В –љ–µ—Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ —А–∞–љ–љ–µ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л –њ—А–Є –љ–µ–њ–Њ–ї–љ–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–µ —Г—А–Њ–≤–љ—П –Р–Ф [14]. –Я—А–µ–њ–∞—А–∞—В –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –і–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ —Г—А–Њ–≤–µ–љ—М –Р–Ф –Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –ї–Є–љ–µ–є–љ–Њ–є –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М—О «–і–Њ–Ј–∞––Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П» –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є. –Ґ–∞–Ї, –њ—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –љ–∞ –Ј–і–Њ—А–Њ–≤—Л—Е –≤–Њ–ї–Њ–љ—В–µ—А–∞—Е –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –Р–Ф —Б–љ–Є–ґ–∞–ї–Њ—Б—М –њ—А–Є –Є–Ј–Љ–µ—А–µ–љ–Є–Є —Б—В–Њ—П –љ–∞ 1,1; 4,8 –Є 8,0 –Љ–Љ —А—В.—Б—В., –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є 2,5; 5 –Є 10 –Љ–≥ –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [15].
–Я—А–Є —А–∞–Ј–≤–Є—В–Є–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ –љ–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Є–Ј–Љ–µ–љ–µ–љ–Є—П —З–∞—Б—В–Њ—В—Л —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П —Б–µ—А–і—Ж–∞, —З—В–Њ –≤—Л–і–µ–ї—П–µ—В –њ—А–µ–њ–∞—А–∞—В —Б—А–µ–і–Є –Њ—Б—В–∞–ї—М–љ—Л—Е –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–µ–є –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ—А–µ–њ–∞—А–∞—В —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є (—В–∞–±–ї. 3). –°—А–µ–і–Є –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ – –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є—П –Њ—В–µ–Ї–∞ –≥–Њ–ї–µ–љ–µ–є –Є –≥–Є–њ–µ—А–µ–Љ–Є–Є, —З—В–Њ —Б–≤–Њ–є—Б—В–≤–µ–љ–љ–Њ –≤—Б–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞.
–Р–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞
–Р–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞ –і–µ–є—Б—В–≤–Є—П –Є –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –Ї–Њ—А–Њ–љ–∞—А–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞, —З—В–Њ —В–∞–Ї–ґ–µ –Њ–њ—А–µ–і–µ–ї—П–µ—В –љ–∞–Є–±–Њ–ї–µ–µ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ—Л–є –Ї–Њ–љ—В–Є–љ–≥–µ–љ—В –±–Њ–ї—М–љ—Л—Е. –≠—Д—Д–µ–Ї—В –њ—А–µ–њ–∞—А–∞—В–∞ –Љ–∞–Ї—Б–Є–Љ–∞–ї–µ–љ –Є–Љ–µ–љ–љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ —Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Є–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –Њ–±—Б—В—А—Г–Ї—Ж–Є–Є [17]. –Ю–і–љ–∞–Ї–Њ –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ —В–∞–Ї–ґ–µ —И–Є—А–Њ–Ї–Њ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –і–ї—П –ї–µ—З–µ–љ–Є—П —Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –љ–∞–њ—А—П–ґ–µ–љ–Є—П, –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞—П —З–∞—Б—В–Њ—В—Г, –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М —Н–њ–Є–Ј–Њ–і–Њ–≤ –Є—И–µ–Љ–Є–Є [18–22]. –Ю–і–љ–Є–Љ –Є–Ј –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е –њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ –љ–∞ —Б–Њ—Б—В–Њ—П–љ–Є–µ –Љ–Є–Њ–Ї–∞—А–і–∞ –њ–Њ—Б–ї–µ —Н–њ–Є–Ј–Њ–і–∞ –Є—И–µ–Љ–Є–Є —Б—З–Є—В–∞–µ—В—Б—П –µ–≥–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Б–љ–Є–ґ–∞—В—М –Ї–∞–ї—М—Ж–Є–µ–≤—Г—О –њ–µ—А–µ–≥—А—Г–Ј–Ї—Г –Ї–ї–µ—В–Њ–Ї, —П–≤–ї—П—О—Й—Г—О—Б—П –њ—А–Є—З–Є–љ–Њ–є –Љ–Є–Њ–Ї–∞—А–і–Є–∞–ї—М–љ–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П [23]. –Т—Л–≥–Њ–і–љ—Л–Љ –Њ—В–ї–Є—З–Є–µ–Љ –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ –Њ—В –±–Њ–ї–µ–µ —А–∞–љ–љ–Є—Е –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П —Б—З–Є—В–∞–µ—В—Б—П –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Г –љ–µ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ –І–°–°, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–є –њ—А–Є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–µ —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –њ—Г—Б–Ї–Њ–≤—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –Є—И–µ–Љ–Є–Є.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є CAPE [16] –Њ—Ж–µ–љ–Є–≤–∞–ї–Њ—Б—М –≤–ї–Є—П–љ–Є–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –љ–∞ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є —З–∞—Б—В–Њ—В—Г —Н–њ–Є–Ј–Њ–і–Њ–≤ –Є—И–µ–Љ–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є –Ш–С–°. –Я—А–Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–Љ 48–—З–∞—Б–Њ–≤–Њ–Љ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є–Є –≠–Ъ–У –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Н–њ–Є–Ј–Њ–і–Њ–≤ –Є—И–µ–Љ–Є–Є. –Я—А–Є –Њ—Ж–µ–љ–Ї–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ –њ—А–Њ–∞—А–Є—В–Љ–Њ–≥–µ–љ–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –њ—А–µ–њ–∞—А–∞—В–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б–Њ —Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–µ–є –љ–∞–њ—А—П–ґ–µ–љ–Є—П –њ—А–Є –і–Њ–±–∞–≤–ї–µ–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Ї —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є ?––±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є –Є –љ–Є—В—А–∞—В–∞–Љ–Є –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –≤–Њ–Ј—А–∞—Б—В–∞–љ–Є—П —Н–њ–Є–Ј–Њ–і–Њ–≤ –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞.
–Т–ї–Є—П–љ–Є–µ —В–µ—А–∞–њ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ –љ–∞ –њ—А–Њ–≥–љ–Њ–Ј —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ—М—О —Б–µ—А–і—Ж–∞ –±—Л–ї–Њ –Њ—Ж–µ–љ–µ–љ–Њ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є PREVENT. –Э–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —З–Є—Б–ї–∞ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л—Е –і–µ—Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–µ–є —В–µ—З–µ–љ–Є—П —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (61 –≤ –≥—А—Г–њ–њ–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є 88 –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ). –Ґ–∞–Ї–ґ–µ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —З–Є—Б–ї–∞ –Њ–њ–µ—А–∞—Ж–Є–є —А–µ–≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ (53 –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б 85 –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ) –≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П b––±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤, –љ–Є—В—А–∞—В–Њ–≤ –Є–ї–Є –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є. –І–∞—Б—В–Њ—В–∞ –∞–љ–≥–Є–љ–Њ–Ј–љ—Л—Е –њ—А–Є—Б—В—Г–њ–Њ–≤ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М —Б 85 –і–Њ 60.
–°—А–∞–≤–љ–Є—В–µ–ї—М–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ –≤–ї–Є—П–љ–Є—П –љ–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Г—О –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞ —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–∞ –≤–∞–ї—Б–∞—А—В–∞–љ–∞ –Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞ –Ї–∞–ї—М—Ж–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –њ—А–Њ–≤–Њ–і–Є—В—Б—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є VALUE (Valsartan Antihypertensive Long–tern Use Evaluation), –Ї–Њ—В–Њ—А–Њ–µ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–µ –Ј–∞–≤–µ—А—И–µ–љ–Њ. –†–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–Њ 14400 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є –Є –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ (–≥–Є–њ–µ—А—Е–Њ–ї–µ—Б—В–µ—А–Є–љ–µ–Љ–Є—П >6,5 –Љ–Љ–Њ–ї—М/–ї, –Ї—А–µ–∞—В–Є–љ–Є–љ —Б—Л–≤–Њ—А–Њ—В–Ї–Є >1,2 –Љ–≥/–і–ї, –≠–Ъ–У––њ—А–Є–Ј–љ–∞–Ї–Є –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞, —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В 2 —В–Є–њ–∞, –Ш–С–° –Є–ї–Є –Є–љ—Б—Г–ї—М—В –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ). –Я–Њ–Ї–∞ –љ–µ –Ј–∞–≤–µ—А—И–µ–љ–Њ —В–∞–Ї–ґ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ
ALLHAT (Antihypertensive Lipid Lowering Heart Attack Trial) [38], –Њ–і–љ–Є–Љ –Є–Ј –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–є –Ї–Њ—В–Њ—А–Њ–≥–Њ —П–≤–ї—П–µ—В—Б—П —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ –≤–ї–Є—П–љ–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –љ–∞ —З–∞—Б—В–Њ—В—Г —А–∞–Ј–≤–Є—В–Є—П –љ–µ—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –Є –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є —Б–Љ–µ—А—В–Є. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–Њ–≤–Њ–і–Є—В—Б—П —Б—А–∞–≤–љ–µ–љ–Є–µ —З–µ—В—Л—А–µ—Е –Ї–ї–∞—Б—Б–Њ–≤ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤: –і–Є—Г—А–µ—В–Є–Ї–∞, –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞ –Ї–∞–ї—М—Ж–Є—П, ?––±–ї–Њ–Ї–∞—В–Њ—А–∞ –Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –Р–Я–§ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–љ–Є–ґ–µ–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є —Г –±–Њ–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є —Б –≥–Є–њ–µ—А—Е–Њ–ї–µ—Б—В–µ—А–Є–љ–µ–Љ–Є–µ–є.
–Т –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–µ Kloner R.A. et al. [44] –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤. –С—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–µ –Є –љ–µ—Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є –љ–Є—Д–µ–і–Є–њ–Є–љ–∞ GITS. –Я–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –∞–Љ–ї–Њ–і–Є–њ–Є–љ, –Њ–±—Й–∞—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–∞—П –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М, —З–∞—Б—В–Њ—В–∞ —А–∞–Ј–≤–Є—В–Є—П –Њ—Б—В—А–Њ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ш–С–° –±—Л–ї–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –љ–Є–ґ–µ –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –і–ї—П –і—А—Г–≥–Є—Е –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П.
–Т–ї–Є—П–љ–Є–µ –љ–∞ –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Г—О
–љ–µ—А–≤–љ—Г—О —Б–Є—Б—В–µ–Љ—Г
–Р–Ї—В–Є–≤–∞—Ж–Є—П —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л —П–≤–ї—П–µ—В—Б—П –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–Љ –њ–Њ–±–Њ—З–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –Є—Е –і–µ–є—Б—В–≤–Є—П (—А–µ—Д–ї–µ–Ї—В–Њ—А–љ–∞—П –∞–Ї—В–Є–≤–∞—Ж–Є—П). –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –њ—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –љ–Њ—А–∞–і—А–µ–љ–∞–ї–Є–љ–∞ –≤ –Ї—А–Њ–≤–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–љ–Є–Љ–∞—О—Й–Є—Е –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ, –љ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –µ–≥–Њ —Г—А–Њ–≤–љ—П –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ—Л–Љ [24–26]. –Я—А–Є —Б–њ–µ–Ї—В—А–∞–ї—М–љ–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г–≤–µ–ї–Є—З–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П LF/HF [27]. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –і–µ–є—Б—В–≤–Є—П –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ —П–≤–ї—П–µ—В—Б—П –Њ—В—Б—Г—В—Б—В–≤–Є–µ –∞–Ї—В–Є–≤–∞—Ж–Є–Є —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –Є —А–∞–Ј–≤–Є—В–Є—П —А–µ—Д–ї–µ–Ї—В–Њ—А–љ–Њ–є —В–∞—Е–Є–Ї–∞—А–і–Є–Є.
–Т–ї–Є—П–љ–Є–µ –љ–∞ –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —А–µ–љ–Є–љ–∞ –њ–ї–∞–Ј–Љ—Л
Susaguri et al. [28] –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —А–µ–љ–Є–љ–∞ –њ–ї–∞–Ј–Љ—Л –Є —Г—А–Њ–≤–µ–љ—М –љ–Њ—А–∞–і—А–µ–љ–∞–ї–Є–љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М —З–µ—А–µ–Ј 1, 4 –Є 7 —Б—Г—В. –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –≤ –Њ—В–≤–µ—В –љ–∞ —Б–љ–Є–ґ–µ–љ–Є–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –∞–Ї—В–Є–≤–∞—Ж–Є–Є —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є –Є —А–µ–љ–Є–љ–∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ –Є —Г—А–Њ–≤–љ–Є –љ–Њ—А–∞–і—А–µ–љ–∞–ї–Є–љ–∞ –Є —А–µ–љ–Є–љ–∞ –њ–ї–∞–Ј–Љ—Л –Њ—Б—В–∞–≤–∞–ї–Є—Б—М –љ–µ–Є–Ј–Љ–µ–љ–љ—Л–Љ–Є.
–Т–ї–Є—П–љ–Є–µ –љ–∞ –Љ–∞—Б—Б—Г –Љ–Є–Њ–Ї–∞—А–і–∞ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞
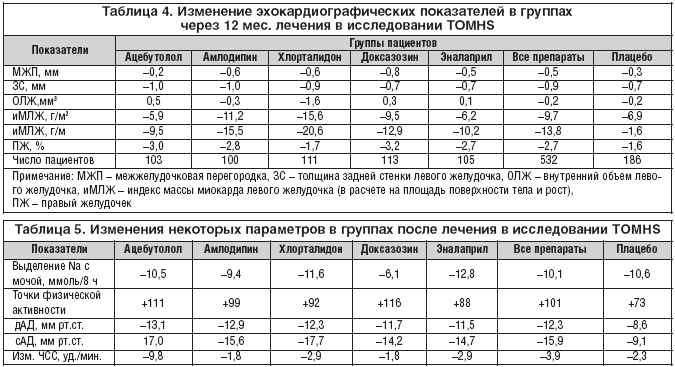
–Т —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –і–≤–Њ–є–љ–Њ–Љ —Б–ї–µ–њ–Њ–Љ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є TOMHS (Treatment of mild hypertension study) –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М —Б—А–∞–≤–љ–µ–љ–Є–µ 5 –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤: –і–Є—Г—А–µ—В–Є–Ї–∞ (—Е–ї–Њ—А—В–∞–ї–Є–і–Њ–љ), ?––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–∞ (–∞—Ж–µ–±—Г—В–Њ–ї–Њ–ї), –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞ –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤ (–∞–Љ–ї–Њ–і–Є–њ–Є–љ), –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ––Ї–Њ–љ–≤–µ—А—В–Є—А—Г—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ (—Н–љ–∞–ї–∞–њ—А–Є–ї–∞ –Љ–∞–ї–µ–∞—В), –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞ a––∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (–і–Њ–Ї—Б–∞–Ј–Њ–Ј–Є–љ) –Є –Є—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ –Љ–∞—Б—Б—Г –Љ–Є–Њ–Ї–∞—А–і–∞ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞. –Я—А–Њ–≤–µ–і–µ–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ—Б–љ–Њ–≤—Л–≤–∞–ї–Њ—Б—М –љ–∞ –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–є —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —А–∞–Ј–Љ–µ—А–Њ–≤ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ –Є –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –љ–∞ 902 –њ–∞—Ж–Є–µ–љ—В–∞—Е —Б –Љ—П–≥–Ї–Њ–є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–µ–є –≤ —В–µ—З–µ–љ–Є–µ –±–Њ–ї–µ–µ —З–µ—В—Л—А–µ—Е –ї–µ—В. –Э–∞ –њ–µ—А–≤–Њ–є —Б—В—Г–њ–µ–љ–Є –њ–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–µ–і–ї–∞–≥–∞–ї—Б—П –Њ–і–Є–љ –Є–Ј 5 –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–≤ —В–Њ–Љ —З–Є—Б–ї–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ –≤ –і–Њ–Ј–µ 5 –Љ–≥/—Б—Г—В.) –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ, –∞ –Ј–∞—В–µ–Љ –љ–∞ –≤—В–Њ—А–Њ–є —Б—В—Г–њ–µ–љ–Є –њ—А–Є –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –њ—А–Є—Б–Њ–µ–і–Є–љ—П–ї—Б—П –≤—В–Њ—А–Њ–є –њ—А–µ–њ–∞—А–∞—В (—Е–ї–Њ—А—В–∞–ї–Є–і–Њ–љ –≤ 5 –≥—А—Г–њ–њ–∞—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є —Н–љ–∞–ї–∞–њ—А–Є–ї –≤ –≥—А—Г–њ–њ–µ, —А–∞–љ–µ–µ –њ–Њ–ї—Г—З–∞–≤—И–µ–є —Е–ї–Њ—А—В–∞–ї–Є–і–Њ–љ). –Т—Б–µ –њ—А–µ–њ–∞—А–∞—В—Л –љ–∞–Ј–љ–∞—З–∞–ї–Є—Б—М –Њ–і–Є–љ —А–∞–Ј –≤ —Б—Г—В–Ї–Є —Г—В—А–Њ–Љ. –Ъ–Њ–љ—В—А–Њ–ї—М–љ—Л–µ —Н—Е–Њ–Ї–∞—А–і–Є–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –Є—Б—Е–Њ–і–љ–Њ, —З–µ—А–µ–Ј 3, 12, 24, 36 –Є 48 –Љ–µ—Б. –Ч–∞ –≤—А–µ–Љ—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П, –њ—А–Є—З–µ–Љ –≤ –≥—А—Г–њ–њ–∞—Е –∞—Ж–µ–±—Г—В–Њ–ї–Њ–ї–∞ –Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –њ—А–Њ—Ж–µ–љ—В –Є–Ј–Љ–µ–љ–µ–љ–Є—П —В–µ—А–∞–њ–Є–Є –±—Л–ї –љ–∞–Є–Љ–µ–љ—М—И–Є–Љ, —В.–µ. –∞–і–µ–Ї–≤–∞—В–љ—Л–є –Ї–Њ–љ—В—А–Њ–ї—М –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –љ–∞–±–ї—О–і–∞–ї—Б—П –≤ —В–µ—З–µ–љ–Є–µ –≤—Б–µ–≥–Њ —З–µ—В—Л—А–µ—Е–ї–µ—В–љ–µ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –≤ –і–Њ–Ј–∞—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –љ–µ –њ—А–µ–≤—Л—И–∞—О—Й–Є—Е –Є—Б—Е–Њ–і–љ—Л–µ. –Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –і–Є–љ–∞–Љ–Є–Ї–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Љ–∞—Б—Б—Л –Љ–Є–Њ–Ї–∞—А–і–∞ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ –љ–∞–Є–±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –≤ –≥—А—Г–њ–њ–∞—Е –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є —Е–ї–Њ—А—В–∞–ї–Є–і–Њ–љ–∞, –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–∞–Љ–Є –∞—Ж–µ–±—Г—В–Њ–ї–Њ–ї–∞ –Є –њ–ї–∞—Ж–µ–±–Њ. –Т —Е–Њ–і–µ –≤—Б–µ–≥–Њ –љ–∞–±–ї—О–і–µ–љ–Є—П –≤—Л—П—Б–љ–Є–ї–Њ—Б—М, —З—В–Њ –∞–Љ–ї–Њ–і–Є–њ–Є–љ —Б–љ–Є–ґ–∞–µ—В –Љ–∞—Б—Б—Г –Љ–Є–Њ–Ї–∞—А–і–∞ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞, —З—В–Њ –Љ–Њ–ґ–µ—В —Г–Љ–µ–љ—М—И–∞—В—М —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е —Б –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є –Є –≥–Є-–њ–µ—А—В—А–Њ—Д–Є–µ–є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ (—В–∞–±–ї. 4, 5).
–Т–ї–Є—П–љ–Є–µ –љ–∞ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ
–∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ —Б–Њ—Б—Г–і–Њ–≤
–Т —Б–≤—П–Ј–Є —Б –љ–∞–ї–Є—З–Є–µ–Љ —А—П–і–∞ —Б–Њ–Њ–±—Й–µ–љ–Є–є –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–Љ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–Љ –≤–ї–Є—П–љ–Є–Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П –љ–∞ —Б–Њ—Б—В–Њ—П–љ–Є–µ —Н–љ–і–Њ—В–µ–ї–Є—П —Б–Њ—Б—Г–і–Њ–≤ –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–µ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ, —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –і–≤–Њ–є–љ–Њ–µ —Б–ї–µ–њ–Њ–µ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ PREVENT [42]. –Т —Е–Њ–і–µ —Н—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ—Ж–µ–љ–Є–≤–∞–ї–Њ—Б—М –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —Б—В–µ–њ–µ–љ–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –∞—А—В–µ—А–Є–є –Є —В–Њ–ї—Й–Є–љ—Л –Є–љ—В–Є–Љ–Њ––Љ–µ–і–Є–∞–ї—М–љ–Њ–≥–Њ —Б–ї–Њ—П —Б–Њ–љ–љ—Л—Е –∞—А—В–µ—А–Є–є –љ–∞ —Д–Њ–љ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –љ–∞ 825 –њ–∞—Ж–Є–µ–љ—В–∞—Е —Б –љ–∞–ї–Є—З–Є–µ–Љ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ–Њ–є —Б –њ–Њ–Љ–Њ—Й—М—О –Ї–Њ—А–Њ–љ–∞—А–Њ–≥—А–∞—Д–Є–Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ–Є —Б–µ—А–і—Ж–∞. –Я–∞—Ж–Є–µ–љ—В—Л –њ–Њ–ї—Г—З–∞–ї–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ –≤ –і–Њ–Ј–µ 5 –Љ–≥, –Ї–Њ—В–Њ—А–∞—П –њ—А–Є —Е–Њ—А–Њ—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–∞—Б—М –і–Њ 10 –Љ–≥. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–µ –±—Л–ї–Њ –њ–Њ–ї—Г—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–≥–Њ —А–∞–Ј–ї–Є—З–Є—П –≤ –Њ–±–µ–Є—Е –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –≥—А—Г–њ–њ–∞—Е – –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Є –Ї–Њ–љ—В—А–Њ–ї—П – –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В–µ–љ–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤. –Э–∞–њ—А–Њ—В–Є–≤, –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –љ–∞ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –≤ —Б–Њ–љ–љ—Л—Е –∞—А—В–µ—А–Є—П—Е, –≤—Л—П–≤–ї—П–µ–Љ–Њ–µ —Б –њ–Њ–Љ–Њ—Й—М—О —Г–ї—М—В—А–∞—Б–Њ–љ–Њ–≥—А–∞—Д–Є–Є. –Я—А–Є —Н—В–Њ–Љ –≤ –≥—А—Г–њ–њ–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —А–µ–≥—А–µ—Б—Б–Є—П –Є–љ—В–Є–Љ–Њ––Љ–µ–і–Є–∞–ї—М–љ–Њ–≥–Њ —Б–ї–Њ—П –љ–∞ 0,046 –Љ–Љ, –∞ –≤ –≥—А—Г–њ–њ–µ –Ї–Њ–љ—В—А–Њ–ї—П – —Г—В–Њ–ї—Й–µ–љ–Є–µ –љ–∞ 0,011 –Љ–Љ. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –і–Њ–Ї–∞–Ј–∞–љ–∞ –Ї–Њ—А—А–µ–ї—П—Ж–Є—П —Б—В–µ–њ–µ–љ–Є —Г—В–Њ–ї—Й–µ–љ–Є—П –Є–љ—В–Є–Љ–Њ––Љ–µ–і–Є–∞–ї—М–љ–Њ–≥–Њ —Б–ї–Њ—П —Б–Њ–љ–љ—Л—Е –∞—А—В–µ—А–Є–є —Б —З–∞—Б—В–Њ—В–Њ–є —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –Є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞. –Ґ–∞–Ї–ґ–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є PREVENT –њ–Њ–Ї–∞–Ј–∞–љ–∞ —Е–Њ—А–Њ—И–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞, —З—В–Њ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —А–∞–љ–µ–µ –і—А—Г–≥–Є–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—П–Љ–Є, –њ—А–Є —Н—В–Њ–Љ —З–∞—Б—В–Њ—В–∞ –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–∞ —Б –≥—А—Г–њ–њ–Њ–є –њ–ї–∞—Ж–µ–±–Њ (79% –і–ї—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є 83% –і–ї—П –њ–ї–∞—Ж–µ–±–Њ). –Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ––Ї–Њ–љ–≤–µ—А—В–Є—А—Г—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ –≤ –≥—А—Г–њ–њ–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –≤ –і–≤–∞ —А–∞–Ј–∞ —А–µ–ґ–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ.
–Т–ї–Є—П–љ–Є–µ –љ–∞ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ
—Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є
–Т —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –і–≤–Њ–є–љ–Њ–Љ —Б–ї–µ–њ–Њ–Љ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є PRAISE I (Prospective Randimized Amlodipine Survival Evaluation Study) [39] –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –Њ—Ж–µ–љ–Ї–∞ –≤–ї–Є—П–љ–Є—П –љ–Њ–≤–Њ–≥–Њ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞ –Ї–∞–ї—М—Ж–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –љ–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л 1153 –њ–∞—Ж–Є–µ–љ—В–∞ —Б —Д—А–∞–Ї—Ж–Є–µ–є –≤—Л–±—А–Њ—Б–∞ –Љ–µ–љ–µ–µ 30% –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –љ–µ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ–Њ–Ї–∞–Ј–∞–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –Њ–±—Й–µ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –љ–∞ 9%, —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –≤–љ–µ–Ј–∞–њ–љ–Њ–є —Б–Љ–µ—А—В–Є –љ–∞ 16% –≤ –≥—А—Г–њ–њ–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ. –Я—А–Є —Н—В–Њ–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –Ї–∞—Б–∞–ї–Њ—Б—М –Є—Б–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–µ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ –≥–µ–љ–µ–Ј–Њ–Љ —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, —Г –Ї–Њ—В–Њ—А—Л—Е –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ –Њ–±—Й–µ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –љ–∞ 31% –Є —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –≤–љ–µ–Ј–∞–њ–љ–Њ–є —Б–Љ–µ—А—В–Є –љ–∞ 46% –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ—А–Њ–≤–Њ–і–Є—В—Б—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ PRAISE II –і–ї—П –Њ—Ж–µ–љ–Ї–Є —А–Њ–ї–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –≤ —В–µ—А–∞–њ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –љ–µ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞ (–і–Є–ї–∞—В–∞—Ж–Є–Њ–љ–љ–∞—П –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є—П). –Я–Њ–Ї–∞–Ј–∞–љ–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Є —Г—А–Њ–≤–љ—П –љ–Њ—А–∞–і—А–µ–љ–∞–ї–Є–љ–∞ –њ–ї–∞–Ј–Љ—Л –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–Є–ї–∞—В–∞—Ж–Є–Њ–љ–љ–Њ–є –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є–µ–є. –†—П–і –∞–≤—В–Њ—А–Њ–≤ —Б–≤—П–Ј—Л–≤–∞—О—В —В–∞–Ї–Њ–є —Н—Д—Д–µ–Ї—В –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ —Б –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є–µ–Љ –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є–Є NO –Є —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Љ–Є–Њ–Ї–∞—А–і–∞–ї—М–љ–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П.
–°–њ–Њ—Б–Њ–± –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є –і–Њ–Ј–Є—А–Њ–≤–Ї–Є
–Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ –њ—А–Є–љ–Є–Љ–∞—О—В 1 —А–∞–Ј –≤ —Б—Г—В–Ї–Є –≤ —Б–≤—П–Ј–Є —Б –і–ї–Є—В–µ–ї—М–љ—Л–Љ –њ–µ—А–Є–Њ–і–Њ–Љ –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П –Є –і–ї–Є—В–µ–ї—М–љ—Л–Љ –∞–і–µ–Ї–≤–∞—В–љ—Л–Љ –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –Р–Ф. –Я—А–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є –Є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –Њ–±—Л—З–љ–∞—П –љ–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ –њ—А–µ–њ–∞—А–∞—В–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 5 –Љ–≥ –Њ–і–Є–љ —А–∞–Ј –≤ —Б—Г—В–Ї–Є. –С–Њ–ї—М—И–Є–љ—Б—В–≤—Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–µ —В—А–µ–±—Г–µ—В—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л, –Њ–і–љ–∞–Ї–Њ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 10 –Љ–≥/—Б—Г—В. –Э–µ —Б–ї–µ–і—Г–µ—В —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –і–Њ–Ј—Г –њ—А–µ–њ–∞—А–∞—В–∞ –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤–Њ–є –љ–µ–і–µ–ї–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–Є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–µ —Г—А–Њ–≤–љ—П –Р–Ф, —В–∞–Ї –Ї–∞–Ї –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –њ—А–µ–њ–∞—А–∞—В–∞ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –њ–Њ–Ј–і–љ–µ–µ.
–Ы–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ
–Ъ–∞–Ї–Њ–є––ї–Є–±–Њ –Ї–Њ—А—А–µ–Ї—В–Є—А–Њ–≤–Ї–Є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –љ–µ —В—А–µ–±—Г–µ—В—Б—П –њ—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —В–Є–∞–Ј–Є–і–љ—Л—Е –і–Є—Г—А–µ—В–Є–Ї–Њ–≤, ?––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤, –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§. –Я–Њ–Ї–∞–Ј–∞–љ–Њ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —Г—А–Њ–≤–µ–љ—М –Р–Ф –њ—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ —Б ?––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є [40].
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Schwartz J.B. [47] –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –Њ—Ж–µ–љ–Ї–∞ –≤–ї–Є—П–љ–Є—П –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ –љ–∞ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Д–Є–ї—М –і–Є–≥–Њ–Ї—Б–Є–љ–∞ —Г –Ј–і–Њ—А–Њ–≤—Л—Е –≤–Њ–ї–Њ–љ—В–µ—А–Њ–≤. –Э–µ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —А–∞–≤–љ–Њ–≤–µ—Б–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –і–Є–≥–Њ–Ї—Б–Є–љ–∞ (steady–state), –∞ —В–∞–Ї–ґ–µ –Р–Ф –Є–ї–Є –І–°–° –њ—А–Є —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Р–љ—В–∞–≥–Њ–љ–Є—Б—В –Љ–µ–і–ї–µ–љ–љ—Л—Е –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤ L–—В–Є–њ–∞ –Є–Ј –≥—А—Г–њ–њ—Л –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤ –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –≤ –Љ–Њ–љ–Њ– –Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є, —В–µ—А–∞–њ–Є–Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ–Є —Б–µ—А–і—Ж–∞ –њ—А–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ –Ї–Њ—А–Њ–љ–∞—А–Њ—Б–њ–∞–Ј–Љ–µ, –∞ —В–∞–Ї–ґ–µ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –≤ —В–µ—А–∞–њ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –љ–µ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞. –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ —П–≤–ї—П–µ—В—Б—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, —З—В–Њ –љ–Є–≤–µ–ї–Є—А—Г–µ—В —А–µ–Ј–Ї–Є–µ –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–µ —Б–і–≤–Є–≥–Є, —Е–∞—А–∞–Ї—В–µ—А–љ—Л–µ –і–ї—П –љ–∞—З–∞–ї—М–љ–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –≤—Б–∞—Б—Л–≤–∞–љ–Є—П –Ї–Њ—А–Њ—В–Ї–Њ–і–µ–є—Б—В–≤—Г—О—Й–Є—Е –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П. –Ф—А—Г–≥–Њ–є –≤–∞–ґ–љ–Њ–є –Њ—В–ї–Є—З–Є—В–µ–ї—М–љ–Њ–є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞ –Њ—В –і—А—Г–≥–Є—Е –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –Ї–∞–ї—М—Ж–Є—П –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞ —П–≤–ї—П–µ—В—Б—П –Њ—В—Б—Г—В—Б—В–≤–Є–µ –≤–ї–Є—П–љ–Є—П –љ–∞ —З–∞—Б—В–Њ—В—Г —Б–µ—А–і–µ—З–љ—Л—Е —Б–Њ–Ї—А–∞—Й–µ–љ–Є–є, —З—В–Њ —А–∞—Б—И–Є—А—П–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞. –Т –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —Е–Њ—А–Њ—И–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –Э–Њ—А–Љ–Њ–і–Є–њ–Є–љ–∞, –њ—А–Є—З–µ–Љ –њ—А–Њ—Ж–µ–љ—В –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –њ—А–Є –µ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–µ –њ—А–µ–≤—Л—И–∞–ї –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Frishman W.H. et al. A randomized placebo–controlled comparison of amlodipine and atenolol in mild to moderate systemic hypertension. J cardivasc Pharmacol 1988 12 Suppl 7 103–6.
2. Horwitz L.D. et al. Comparison of amlodipine and long–acting diltiazem in the treatment of mild or moderate hypertension. Am J Hypertens 1997 10(11) 1263–9.
3. Lau C.P. et al. Relative efficacy and tolerability of lacidipine and amlodipine in patients with mild–to–moderate hypertension: a randomized double–blind study. J –°ardovasc Pharmacol 1996 28(2) 328.
4. Habeler G. et al. Effectiveness and tolerance of amlodipine in treatment of patients with mild to moderate hypertension. Results of long–term study with a new calcium antagonist. Wien Klin Wochenschr 1992 104(1) 16–20.
5. Ajayi A.A. et al. The efficacy and tolerability of amlodipine and hydrochlorothiazide in Nigerians with essential hypertension. JNatl Med Assoc 1995 87(7) 485–8.
6. Sethi K.K. et al. Amlodipine monotherapy in mild to moderate hypertension. Indian Heart J 1994 46(1) 17–20.
7. Khokhani R.C. et al. Amlodipine in mild and moderate hypertension: initial Indian experiment. J Assoc Phisicians India 1993 41(10) 662–3.
8. Broadhurst P. et al. Intra–arterial monitoring of the antihypertensive effects of once–daily amlodipine. J Hum Hypertens 1992 6 Suppl 1 9–12.
9. Ishimitsi T. et al. Amlodipine, a long–acting calcium channel blocker, attenuates morning blood pressure rise in hypertensive patients. Clin Exp Pharmacol Physiol 1999 26(7) 500–4.
10. Ferrucci A. et al. 24–hour blood pressure profiles in patients with hypertension treated with amlodipine or nifedipine GITS. Clin Drug Invest 1997 13 Suppl 1 67–72.
11. Nold G. et al. Morning versus evening amlodipine treatment: Effect of circadian blood pressure profile in essential hypertensive patients. Blood Press Monit 1998 3(1) 17–25.
12. Leenen F.H. et al. Persistence of antihypertensive effect after missed doses of calcium antagonist with long (amlodipine) vs short (diltiazem) elimination half–life. British J Clin Pharmacol 1996 41(2) 83–8.
13. Hayduk K. et al. Is initial dose titration of amlodipine worthwhile in patients with mild to moderate hypertension? Current Med Res Opinion 1999 15(1) 39–45.
14. Williams D.M. et al. Amlodipine pharmacokinetics in healthy volunteers. J Clin Pharmacol 1988 28 11 990–8.
15. Lichtlen P.R., Fisher L.D. Analysis of arrhythmias in the Circadian Antiischemia Program in Europe (CAPE) study. J Cardiovasc Pharmacol 1999 33(1) 135–9.
16. Chahine R.A. et al. Randomized placebo–controlled trial of amlodipine in vasospastic angina. L Am Coll Cardiol 1993 21(6) 1365–70.
17. Petkar S. et al. Amlodipine monotherapy in stable angina pectoris. Indian Heart J 1994 46(2) 85–8.
18. Steffensen R. et al. Effects of amlodipine and isosorbide dinitrate on exercise–induced and ambulatory ischemia in patients with chronic stable angina pectoris. Cardiovasc Drug Ther 1997 11(5) 629–35.
19. Van Kham et al. Amlodipine versus diltiazem controlled release as monotherapy in patients with stable coronary artery disease. Current Ther Res Clin Exp 1998 59(3) 139–48.
20. Knight C.J. et al. Amlodipine versus diltiazem as additional antianginal treatment to atenolol. Am J Cardiol 1998 81(2) 133–6.
21. Hall R.J. A multicentral study comparing the efficacy and tolerability of nisoldipine coat–core and amlodipine in patients with chronic stable angina. Current Ther Res Clin Exp 1998 59(7) 483–97.
22. Rinaldi C.A. et al. Randomized, double–blind crossover study to investigate the effects of amlodipine and isosorbide mononitrate on the time course and severity of exercise–induced myocardial stunning. Circulation 1998 98(8) 749–56.
23. Golgsmith S.R. Effect of amlodipine and felodipine on sympathetic activity and baroreflex function in normal humans. Am J Hypertens 1995 8(9) 902–8.
24. de Champlain J. et al. Different effects of nifedipine and amlodipine on circulating catecholamine levels in essential hypertensive patients. J Hypertens 1998 16(11) 1357–69.
25. Siche J.P. et al. Effects of amlodipine on baroreflex and sympathetic nervous system activity in mild–to–moderate hypertension. Am J Hypertens 2001 14(5 Pt 1) 424–8.
26. Minami J. et al. Effects of amlodipine and nifedipine retard on autonomic nerve activity in hypertensive patients. Clin Exp Pharmacol Physiol 1998 25(7–8) 572–6.
27. Susaguri M. et al. Amlodipine lowers blood pressure without increasing sympathetic activity or activating the rennin–angiotensin system in patients with essential hypertension. Eur J Clin Pharmacol 1997 53(3–4) 197–201.
28. Frishman W.H. et al. Amlodipine versus atenolol in essential hypertension. Am J Cardiol 1994 73(3) 50–4.
29. Ding Y.A. et al. Comparison of amlodipine and quinapril on ambulatory blood pressure and platelet function in hypertension. J Hum Hypertens 1995 9(8) 637–41.
30. Errico M. et al. Evaluation of efficacy of amlodipine vs captopril/hydrochlorothiazide in the treatment of essential hypertension. Clin Drug Invest 1997 13 Suppl 1 102–7.
31. Viscoper R.J. et al. A randomized, double–blind trial comparing mibefradil and amlodipine: two long–acting calcium antagonists with similar efficacy but different tolerability profiles. Mibefradil International Study Group. J Hum Hypertens 1997 11(6) 387–93.
32. Lorimer A.R. et al. Differences between amlodipine and lisinipril in control of clinic and twenty–hour ambulatory blood pressures. J Hum Hypertens 1998 12(6) 411–6.
33. Lefebvre J. et al. Comparative effects of felodipine ER, amlodipine and nifedipine GITS on 24 blood pressure control and through to peak ratios in mild to moderate ambulatory hypertension: a forced titration study. Canadian J Cardiol 1998 14(5) 682–8.
34. Watts R.W. et al. A placebo–controlled comparison of diltiazem and amlodipine monotherapy in essentional hypertension using 24–h ambulatory monitoring. Blood Press 1998 7(1) 25–30.
35. Videbaek L.M. et al. Crossover comparison of the pharmacokinetics of amlodipine and felodipine ER in hypertensive patients. Int J Clin Pharmacol Ther 1997 35(11) 514–8.
36. Burris J.F. et al. Double–blind comparison of amlodipine and hydrochlorothiazide in patients with mild to moderate hypertension. J Cardiovasc Pharmacol 1988 12 Suppl 7 98–102.
37. Lorimer A.R. et al. A comparison of amlodipine, verapamil and placebo in the treatment of mild to moderate hypertension. Amlodipine Study Group. J Hum Hypertens 1989 3(3) 191–6.
38. Packer M. et al. Effect of amlodipine on morbidity and mortality in severe chronic heart failure. N Engl J Med 1996 335 1107–14.
39. Brown M.J. et al. Alpha–blockade and calcium antagonism: an effective and well–tolerated combination for the treatment of resistant hypertension. J Hypertens 1995 13(6) 701–7.
40. Schwartz J.B. Effects of amlodipine on steady–state digoxin concentrations and renal digoxin clearance. J Cardiovasc Pharmacol 1988 12(1) 1–5.
41. Pitt B. et al. Effect of amlodipine on progression of atherosclerosis and the occurrence of clinical events. PREVENT investigators. Circulation 2000 102(13) 1503–10.
42. Detry J.M. Amlodipine and the total ischemic burden: Circadian Anti–Ischemia Program in Europe (CAPE) trial – Methodology, safety and toleration. Cardiology 1994 85 Suppl 2 24–30.
43. Deanfield J.E. et al. Amlodipine reduces transient myocardial ischemia in patients with coronary artery disease: double–blind Circadian Anti–Ischemia Program in Europe (CAPE Trial). J Am Coll Cardiol 1994 24(6) 1460–7.
44. Kloner R.A. et al. Safety of long–acting dihydropyridine calcium channel blockers in hypertensive patients. Am J Cardiol 1998 81(2) 163–9.












