–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Н—Д—Д–µ–Ї—В—Л –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —Б—В–∞—В–Є–љ–∞–Љ–Є, —Г –ґ–µ–љ—Й–Є–љ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ –Є–Ј—Г—З–µ–љ—Л [2]. –Т—Л—П–≤–ї–µ–љ —А—П–і –Њ—В–ї–Є—З–Є–є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ —Н—В–Њ–≥–Њ –Ї–ї–∞—Б—Б–∞ –≥–Є–њ–Њ–ї–Є–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –њ–Њ–ї–∞. –≠—В–Є —А–∞–Ј–ї–Є—З–Є—П –њ—А–Є–≤–Њ–і–Є–ї–Є –Ї —В–Њ–Љ—Г, —З—В–Њ –њ—А–Њ—Д–Є–ї—М –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є —Г –ґ–µ–љ—Й–Є–љ –Є –Љ—Г–ґ—З–Є–љ —В–∞–Ї –ґ–µ —А–∞–Ј–ї–Є—З–∞–ї—Б—П. –Э–∞–Є–±–Њ–ї–µ–µ —В—А–µ–≤–Њ–ґ–љ—Л–µ –і–∞–љ–љ—Л–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Ж–µ—А–Є–≤–∞—Б—В–∞—В–Є–љ–∞. –Ґ–µ—А–∞–њ–Є—П —Ж–µ—А–Є–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ (–і–Њ –Є–Ј—К—П—В–Є—П —Б —А—Л–љ–Ї–∞) –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–ї–∞—Б—М —Б –љ–µ—А–µ–і–Ї–Є–Љ —А–∞–Ј–≤–Є—В–Є–µ–Љ –Љ–Є–Њ–њ–∞—В–Є–є –Є —А–∞–±–і–Њ–Љ–Є–Њ–ї–Є–Ј–∞ —Г –њ–Њ–ґ–Є–ї—Л—Е —Е—Г–і—Л—Е –ґ–µ–љ—Й–Є–љ [9]. –Я—А–Є –Є–Ј—Г—З–µ–љ–Є–Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є —Ж–µ—А–Є–≤–∞—Б—В–∞—В–Є–љ–∞ –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Г –њ–Њ–ґ–Є–ї—Л—Е –ґ–µ–љ—Й–Є–љ –њ–ї–∞–Ј–Љ–µ–љ–љ—Л–є —Г—А–Њ–≤–µ–љ—М –љ–∞ 30% –≤—Л—И–µ, —З–µ–Љ —Г –њ–Њ–ґ–Є–ї—Л—Е –Љ—Г–ґ—З–Є–љ [5]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –њ–ї–∞–Ј–Љ–µ–љ–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П —Б—В–∞—В–Є–љ–Њ–≤ —Г –ґ–µ–љ—Й–Є–љ –≤—Л—И–µ, —З–µ–Љ —Г –Љ—Г–ґ—З–Є–љ. –Ю–±—Л—З–љ–Њ —Г –Ј–і–Њ—А–Њ–≤—Л—Е –ї—О–і–µ–є —Н—В–Є —А–∞–Ј–ї–Є—З–Є—П –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л –Є –љ–µ —В—А–µ–±—Г—О—В –Є–Ј–Љ–µ–љ–µ–љ–Є—П —А–µ–ґ–Є–Љ–∞ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П [3–8]. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ, —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–±–Њ—З–љ—Л—Е –і–µ–є—Б—В–≤–Є–є —Б—В–∞—В–Є–љ–Њ–≤ –≤—Л—И–µ —Г –ґ–µ–љ—Й–Є–љ, –Њ–љ —В–∞–Ї–ґ–µ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –њ—А–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –Є –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –і—А—Г–≥–Є–Љ–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є [8]. –Ь–Њ–ґ–љ–Њ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞—В—М, —З—В–Њ –≤ —Н—В–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е –і–∞–ґ–µ —Б–ї–∞–±—Л–µ –Є —Г–Љ–µ—А–µ–љ–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П –≤ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–∞—Е –Љ–Њ–≥—Г—В –Є–Љ–µ—В—М –≤–∞–ґ–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ. –Т 4 –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ–Њ –њ–µ—А–≤–Є—З–љ–Њ–є –Є –≤—В–Њ—А–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –°–°–Ч –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —Б—В–∞—В–Є–љ—Л —Б–љ–Є–ґ–∞—О—В —А–Є—Б–Ї –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е —Б–Њ–±—Л—В–Є–є –≤ —А–∞–≤–љ–Њ–є —Б—В–µ–њ–µ–љ–Є —Г –Љ—Г–ґ—З–Є–љ –Є —Г –ґ–µ–љ—Й–Є–љ [10]. –Ю–і–љ–∞–Ї–Њ, –њ—А–Њ—Ж–µ–љ—В –ґ–µ–љ—Й–Є–љ, —Г—З–∞—Б—В–≤—Г—О—Й–Є—Е –≤ —Н—В–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, —Б–Њ—Б—В–∞–≤–ї—П–µ—В –≤ —Б—А–µ–і–љ–µ–Љ –ї–Є—И—М 25%. –Т –і–≤—Г—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, –≤ –Њ–і–љ–Њ–Љ –Є–Ј –Ї–Њ—В–Њ—А—Л—Е —З–Є—Б–ї–Њ –ґ–µ–љ—Й–Є–љ –і–Њ—Б—В–Є–≥–∞–ї–Њ 52%, –љ–µ –њ–Њ–ї—Г—З–µ–љ–Њ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤ –њ–Њ–ї—М–Ј—Л –њ—А–Є–µ–Љ–∞ —Б—В–∞—В–Є–љ–Њ–≤ –і–ї—П –ґ–µ–љ—Й–Є–љ. –Ь–µ—В–∞––∞–љ–∞–ї–Є–Ј, –≤–Ї–ї—О—З–Є–≤—И–Є–є 79494 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –∞–љ–∞–ї–Є–Ј–Њ–Љ 10 –Ї–Њ–љ–µ—З–љ—Л—Е —В–Њ—З–µ–Ї, –њ–Њ–Ї–∞–Ј–∞–ї –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї —В—П–ґ–µ–ї—Л—Е –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е —Б–Њ–±—Л—В–Є–є 0,73 –і–ї—П –Љ—Г–ґ—З–Є–љ –Є 0,77 –і–ї—П –ґ–µ–љ—Й–Є–љ, –њ—А–Є–љ–Є–Љ–∞—О—Й–Є—Е —Б—В–∞—В–Є–љ—Л [11]. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —Б—В–∞—В–Є–љ—Л –Є—Б–њ–Њ–ї—М–Ј—Г—О—В —Г –ґ–µ–љ—Й–Є–љ –Љ–µ–љ–µ–µ —З–∞—Б—В–Њ, —З–µ–Љ —Г –Љ—Г–ґ—З–Є–љ –Ї–∞–Ї –і–ї—П –њ–µ—А–≤–Є—З–љ–Њ–є, —В–∞–Ї –Є –і–ї—П –≤—В–Њ—А–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є [12]. –Ь–∞–ї–Њ–Є–Ј—Г—З–µ–љ–љ—Л–Љ –Њ—Б—В–∞–µ—В—Б—П –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤–Њ–њ—А–Њ—Б –Њ —Б–Њ—Б—В–Њ—П–љ–Є–Є –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ –Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –µ–≥–Њ —А–∞–љ–љ–µ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є —Г –ґ–µ–љ—Й–Є–љ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞.
–¶–µ–ї—М—О –љ–∞—И–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Њ —Б—А–∞–≤–љ–µ–љ–Є–µ –і–Є–љ–∞–Љ–Є–Ї–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ –Є —Г—А–Њ–≤–љ—П –≤—Л—Б–Њ–Ї–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ–≥–Њ –°–†–С (hs––°–†–Я), –Ї–∞–Ї –Љ–∞—А–Ї–µ—А–∞ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ —В–µ—А–∞–њ–Є–Є —Б–Є–Љ–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ (–°–Є–Љ–≥–∞–ї) —Г –ґ–µ–љ—Й–Є–љ —Б –≤—Л—Б–Њ–Ї–Є–Љ –Ї–Њ—А–Њ–љ–∞—А–љ—Л–Љ —А–Є—Б–Ї–Њ–Љ –≤ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–Љ –Є –≤ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ.
–Я–Њ –і–Є–Ј–∞–є–љ—Г —Н—В–Њ –±—Л–ї–Њ –Њ—В–Ї—А—Л—В–Њ–µ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л 45 –ґ–µ–љ—Й–Є–љ. 1 –≥—А—Г–њ–њ—Г —Б–Њ—Б—В–∞–≤–Є–ї–Є 21 –ґ–µ–љ—Й–Є–љ–∞ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ —Б —Б–Њ—Е—А–∞–љ–µ–љ–љ–Њ–є –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–µ–є –Є 2 –≥—А—Г–њ–њ—Г – 24 –ґ–µ–љ—Й–Є–љ—Л –≤ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ.
–Ъ—А–Є—В–µ—А–Є–Є –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ: –ґ–µ–љ—Й–Є–љ—Л –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 18 –ї–µ—В –і–Њ 70 –ї–µ—В —Б –ї—О–±—Л–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –Ш–С–°, –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ–Ї—А–Њ–Ј–∞, –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –Љ–Њ–Ј–≥–Њ–≤—Л—Е –∞—А—В–µ—А–Є–є, –∞–љ–µ–≤—А–Є–Ј–Љ—Л –±—А—О—И–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –∞–Њ—А—В—Л, –њ–Њ–і–њ–Є—Б–∞–≤—И–Є–µ –Є–љ—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ —Б–Њ–≥–ї–∞—Б–Є–µ. –Ъ—А–Є—В–µ—А–Є–Є –љ–µ–≤–Ї–ї—О—З–µ–љ–Є—П: –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М, –ї–∞–Ї—В–∞—Ж–Є—П, –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞, –њ—А–Є–µ–Љ –Ј–∞–Љ–µ—Б—В–Є—В–µ–ї—М–љ–Њ–є –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –њ—А–Є–µ–Љ –≥–Є–њ–Њ–ї–Є–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є–ї–Є —В—А–∞–≤–Љ—Л —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –Є/–Є–ї–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –Ј–ї–Њ—Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –∞–ї–Ї–Њ–≥–Њ–ї–µ–Љ –Є–ї–Є –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –њ—Б–Є—Е–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Њ—В–Ї–∞–Ј –њ–∞—Ж–Є–µ–љ—В–Ї–Є –Њ—В —Б–Њ—В—А—Г–і–љ–Є—З–µ—Б—В–≤–∞, –≤—Л—А–∞–ґ–µ–љ–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є –Є –њ–Њ—З–µ–Ї; –і–Њ–±—А–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –Є –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –Њ–њ—Г—Е–Њ–ї–Є, –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ––≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Є —Б–Є—Б—В–µ–Љ–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥–ї–Є –±—Л—В—М –њ—А–Є—З–Є–љ–Њ–є –њ–Њ–≤—Л—И–µ–љ–Є—П —Г—А–Њ–≤–љ—П hs––°–†–Я.
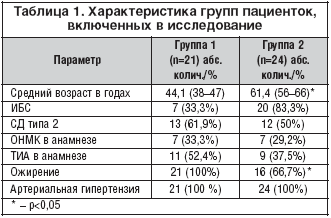
–Т —В–∞–±–ї–Є—Ж–µ 1 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –Њ—Б–љ–Њ–≤–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –і–≤—Г—Е –≤—Л–і–µ–ї–µ–љ–љ—Л—Е –≥—А—Г–њ–њ –њ–∞—Ж–Є–µ–љ—В–Њ–Ї.
–Я–µ—А–Є–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї 3 –Љ–µ—Б—П—Ж–∞ (12 –љ–µ–і–µ–ї—М). –Э–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ —Б–Є–Љ–≤–∞—Б—В–∞—В–Є–љ–∞ —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ 20 –Љ–≥/—Б—Г—В. –І–µ—А–µ–Ј 4 –љ–µ–і–µ–ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б —Г—А–Њ–≤–љ–µ–Љ –•–° –Ы–Я–Э–Я –±–Њ–ї–µ–µ 2,5 –Љ–Љ–Њ–ї—М/–ї –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –і–Њ 40 –Љ–≥. –Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є –•–° –Ы–Я–Э–Я (<2,5 –Љ–Љ–Њ–ї—М/–ї) –µ—Й–µ —З–µ—А–µ–Ј 4 –љ–µ–і–µ–ї–Є –і–Њ–њ—Г—Б–Ї–∞–ї–Њ—Б—М —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –і–Њ 80 –Љ–≥/—Б—Г—В. –Ф–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –Є –і–∞–ї–µ–µ –µ–ґ–µ–Љ–µ—Б—П—З–љ–Њ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П, –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –≤ –њ–ї–∞–Ј–Љ–µ –≤–µ–љ–Њ–Ј–љ–Њ–є –Ї—А–Њ–≤–Є –Њ–њ—А–µ–і–µ–ї—П–ї–Є—Б—М —Б–ї–µ–і—Г—О—Й–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є: –Њ–±—Й–Є–є —Е–Њ–ї–µ—Б—В–µ—А–Є–љ (–Ю–•–°), —Е–Њ–ї–µ—Б—В–µ—А–Є–љ –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і–Њ–≤ –≤—Л—Б–Њ–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є (–•–° –Ы–Я–Т–Я), —Е–Њ–ї–µ—Б—В–µ—А–Є–љ –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і–Њ–≤ –љ–Є–Ј–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є (–•–° –Ы–Я–Э–Я), —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і—Л (–Ґ–У), –≤—Л—Б–Њ–Ї–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–∞—П —Д—А–∞–Ї—Ж–Є—П –°–—А–µ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ (hs––°–†–С), –∞–ї–∞–љ–Є–љ–Њ–≤–∞—П –Є –∞—Б–њ–∞—А–∞–≥–Є–љ–Њ–≤–∞—П —В—А–∞–љ—Б–∞–Љ–Є–љ–∞–Ј–∞ (–Р–°–Ґ, –Р–Ы–Ґ), –Ї—А–µ–∞—В–Є–љ—Д–Њ—Б—Д–Њ–Ї–Є–љ–∞–Ј–∞ (–Ъ–§–Ъ), –Ї—А–µ–∞—В–Є–љ–Є–љ, –Љ–Њ—З–µ–≤–Є–љ–∞, –Љ–Њ—З–µ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, –≥–ї—О–Ї–Њ–Ј–∞ –Є –±–Є–ї–Є—А—Г–±–Є–љ.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –≤ –≥—А—Г–њ–њ–µ –ґ–µ–љ—Й–Є–љ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –≤ —Д–Њ–ї–ї–Є–Ї—Г–ї–Є–љ–Њ–≤—Г—О —Д–∞–Ј—Г –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–≥–Њ —Ж–Є–Ї–ї–∞. –Я–∞—Ж–Є–µ–љ—В–Ї–Є, –њ–Њ–ї—Г—З–∞—О—Й–Є–µ –±–∞–Ј–Є—Б–љ—Г—О –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Г—О, —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й—Г—О, –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ—Г—О —В–µ—А–∞–њ–Є—О –њ—А–Њ–і–Њ–ї–ґ–∞–ї–Є –њ–Њ–ї—Г—З–∞—В—М –µ–µ –≤ —В–Њ–Љ –ґ–µ –Њ–±—К–µ–Љ–µ –±–µ–Ј –Ї–∞–Ї–Є—Е––ї–Є–±–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є–є.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–Є –Є—Е –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ
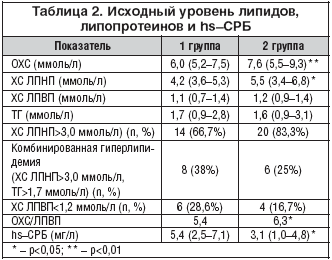
–Т —В–∞–±–ї–Є—Ж–µ 2 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Е–Њ–і–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞, —Г—А–Њ–≤–љ—П hs––°–†–С.
–£—А–Њ–≤–µ–љ—М –Ю–•–° —Г –ґ–µ–љ—Й–Є–љ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –±—Л–ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ, —З–µ–Љ —Г –ґ–µ–љ—Й–Є–љ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ (7,6 –Љ–Љ–Њ–ї—М/–ї –њ—А–Њ—В–Є–≤ 6,0 –Љ–Љ–Њ–ї—М/–ї (—А<0,05)). –Ь–µ—В–∞––∞–љ–∞–ї–Є–Ј, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л–є –Э–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –Є–љ—Б—В–Є—В—Г—В–Њ–Љ —Б–µ—А–і—Ж–∞, –ї–µ–≥–Ї–Є—Е –Є –Ї—А–Њ–≤–Є (NHLBI) –°–®–Р –≤ 1995 –Є –≤–Ї–ї—О—З–∞–≤—И–Є–є 86000 –ґ–µ–љ—Й–Є–љ –і–Њ 65 –ї–µ—В, –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –ґ–µ–љ—Й–Є–љ—Л —Б —Г—А–Њ–≤–љ–µ–Љ –Ю–•–° –≤—Л—И–µ 240 –Љ–≥/–і–ї (6,24 –Љ–Љ–Њ–ї—М/–ї) –Є–Љ–µ—О—В —А–Є—Б–Ї –Ш–С–° –≤ 2,4 —А–∞–Ј–∞ –≤—Л—И–µ, —З–µ–Љ –ґ–µ–љ—Й–Є–љ—Л —Б –Ю–•–° –Ї—А–Њ–≤–Є –љ–Є–ґ–µ 240 –Љ–≥/–і–ї [13]. –° –≤–Њ–Ј—А–∞—Б—В–Њ–Љ –Ј–љ–∞—З–µ–љ–Є–µ —Н—В–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ —А–Є—Б–Ї–∞ (–§–†) —Б–љ–Є–ґ–∞–µ—В—Б—П –Є –і–ї—П –ґ–µ–љ—Й–Є–љ —Б—В–∞—А—И–µ 65, —Б–Њ—Б—В–∞–≤–ї—П–µ—В —В–Њ–ї—М–Ї–Њ 1,12 [13]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е Framingham Study, –Є MONICA Study –њ–Њ–Ї–∞–Ј–∞–љ–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–∞—П –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Љ–µ–ґ–і—Г —Г—А–Њ–≤–љ–µ–Љ –Ю–•–° –Є —А–Є—Б–Ї–Њ–Љ –Ш–С–° —Г –ґ–µ–љ—Й–Є–љ —В–Њ–ї—М–Ї–Њ –≤ –≥—А—Г–њ–њ–µ –ґ–µ–љ—Й–Є–љ 40–50 –ї–µ—В. –£ –ґ–µ–љ—Й–Є–љ –±–Њ–ї–µ–µ —Б—В–∞—А—И–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ —Н—В–∞ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М –љ–µ –±—Л–ї–∞ –≤—Л—П–≤–ї–µ–љ–∞. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ —А–Є—Б–Ї –Ш–С–° –і–ї—П –ґ–µ–љ—Й–Є–љ —Б —Г—А–Њ–≤–љ–µ–Љ –Ю–•–°>240 –Љ–≥/–і–ї (6,24 –Љ–Љ–Њ–ї—М/–ї) –±—Л–ї –≤—Л—И–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ —Б –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ –Ю–•–°, –Њ–љ –Њ—Б—В–∞–≤–∞–ї—Б—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Љ–µ–љ—М—И–µ, —З–µ–Љ —Г –Љ—Г–ґ—З–Є–љ [14].
–Т–Њ–Ј–Љ–Њ–ґ–љ–Њ, –±–Њ–ї—М—И–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ —А–∞–Ј–≤–Є—В–Є–Є –Ш–С–° —Г –ґ–µ–љ—Й–Є–љ –Є–Љ–µ–µ—В –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В –Ю–•–°/–•–° –Ы–Я–Т–Я (–≤ –љ–Њ—А–Љ–µ –Љ–µ–љ–µ–µ 4,5) [15,16]. –Т –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Н—В–Њ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ –±—Л–ї–Њ –њ–Њ–≤—Л—И–µ–љ–Њ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е, –њ—А–Є —Н—В–Њ–Љ –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ–Њ —Г –ґ–µ–љ—Й–Є–љ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ (6,3 –Є 5,4 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ (—А<0,01)). –Я–Њ –і–∞–љ–љ—Л–Љ –Ґhe Framingham Study –Є–Љ–µ–µ—В—Б—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –Ї–Њ—А—А–µ–ї—П—Ж–Є—П –Љ–µ–ґ–і—Г —Н—В–Є–Љ –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В–Њ–Љ –Є –Ї–Њ—А–Њ–љ–∞—А–љ—Л–Љ —А–Є—Б–Ї–Њ–Љ [21,22]. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ Prospective Established Population for Epidemiologic Studies of the Elderly (EPESE), –≤ –Ї–Њ—В–Њ—А–Њ–µ –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л 2527 –ґ–µ–љ—Й–Є–љ —Б—В–∞—А—И–µ 71 –≥–Њ–і–∞ (–њ–µ—А–Є–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї –±–Њ–ї–µ–µ 4,5 –ї–µ—В) –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В–∞ –Ю–•–°/–•–° –Ы–Я–Т–Я –љ–∞ –Њ–і–љ—Г –µ–і–Є–љ–Є—Ж—Г –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —А–Є—Б–Ї –Ш–С–° –љ–∞ 17% [23].
–Т –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –љ–Є–Ј–Ї–Є–є —Г—А–Њ–≤–µ–љ—М –•–° –Ы–Я–Т–Я —З–∞—Й–µ –≤—Б—В—А–µ—З–∞–ї–Њ—Б—М –≤ –≥—А—Г–њ–њ–µ –ґ–µ–љ—Й–Є–љ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ (28,6%) , —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –ґ–µ–љ—Й–Є–љ —Б –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–Њ–є (16,7%), –њ—А–Є —Н—В–Њ–Љ —Б—А–µ–і–љ–Є–є —Г—А–Њ–≤–µ–љ—М –њ–Њ –≥—А—Г–њ–њ–∞–Љ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ –Њ—В–ї–Є—З–∞–ї—Б—П. –С–Њ–ї–µ–µ —З–∞—Б—В–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –•–° –Ы–Я–Т–Я —Г –ґ–µ–љ—Й–Є–љ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ–Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –њ—А–Є –Њ–ґ–Є—А–µ–љ–Є–Є, –Ї–Њ—В–Њ—А—Л–Љ —Б—В—А–∞–і–∞–ї–Є –≤—Б–µ –ґ–µ–љ—Й–Є–љ—Л –≤ —Н—В–Њ–є –≥—А—Г–њ–њ–µ, –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –±–Њ–ї–µ–µ —Б—В–∞—А—И–µ–є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –≥—А—Г–њ–њ–Њ–є, –≥–і–µ –Њ–ґ–Є—А–µ–љ–Є–µ –≤—Л—П–≤–ї–µ–љ–Њ —В–Њ–ї—М–Ї–Њ —Г 66,7% –њ–∞—Ж–Є–µ–љ—В–Њ–Ї [12]. –°–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П National Health And Nutrition Examination Surveys (NHANES), —Г—А–Њ–≤–µ–љ—М –•–° –Ы–Я–Т–Я —Б—А–µ–і–Є –ґ–µ–љ—Й–Є–љ —Б—В–∞—А—И–µ 20 –ї–µ—В –њ—А–Є–Љ–µ—А–љ–Њ –љ–∞ 10 –Љ–≥/–і–ї (0,26 –Љ–Љ–Њ–ї—М/–ї) –≤—Л—И–µ, —З–µ–Љ —Б—А–µ–і–Є –Љ—Г–ґ—З–Є–љ (56 –Љ–≥/–і–ї (1,46 –Љ–Љ–Њ–ї—М/–ї) –њ—А–Њ—В–Є–≤ 47 –Љ–≥/–і–ї (1,22 –Љ–Љ–Њ–ї—М/–ї)) [17]. –°–љ–Є–ґ–µ–љ–Є–µ –•–° –Ы–Я–Т–Я –љ–Є–ґ–µ 35 –Љ–≥/–і–ї (0,91 –Љ–Љ–Њ–ї—М/–ї) –і–Њ–ї–ґ–љ–Њ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М—Б—П –Ї–∞–Ї –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ—Л–є —Д–∞–Ї—В–Њ—А —А–Є—Б–Ї–∞ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞, –Є–Љ–µ—О—Й–Є–є –≤—Л—Б–Њ–Ї–Њ–µ –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ —Г –ґ–µ–љ—Й–Є–љ. –Я—А–Њ–≤–µ–і–µ–љ–љ—Л–є Gordon et al. (1989) –∞–љ–∞–ї–Є–Ј –Ї—А—Г–њ–љ—Л—Е –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –•–° –Ы–Я–Т–Я –љ–∞ 1 –Љ–≥/–і–ї (0,026 –Љ–Љ–Њ–ї—М/–ї) —Б–љ–Є–ґ–∞–ї–Њ —А–Є—Б–Ї –Ш–С–° –љ–∞ 2% –і–ї—П –Љ—Г–ґ—З–Є–љ –Є –љ–∞ 3% –і–ї—П –ґ–µ–љ—Й–Є–љ [20]. –†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П EPESE –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Г –ґ–µ–љ—Й–Є–љ —Б —Г—А–Њ–≤–љ–µ–Љ –•–° –Ы–Я–Т–Я –љ–Є–ґ–µ 35 –Љ–≥/–і–ї (0,91 –Љ–Љ–Њ–ї—М/–ї) —А–Є—Б–Ї –Ш–С–° –≤ –і–≤–∞ —А–∞–Ј–∞ –≤—Л—И–µ, —З–µ–Љ —Г –ґ–µ–љ—Й–Є–љ –≥—А—Г–њ–њ—Л –Ї–Њ–љ—В—А–Њ–ї—П —Б —Г—А–Њ–≤–љ–µ–Љ –•–° –Ы–Я–Т–Я?60 –Љ–≥/–і–ї (1,56 –Љ–Љ–Њ–ї—М/–ї) [23]. –£—А–Њ–≤–µ–љ—М –•–° –Ы–Я–Т–Я –љ–µ –Є–Ј–Љ–µ–љ—П–µ—В—Б—П, –≤–µ—А–Њ—П—В–љ–Њ, –Є –њ–Њ—Б–ї–µ –Љ–µ–љ–Њ–њ–∞—Г–Ј—Л (10]. –Ю–і–љ–∞–Ї–Њ, –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –Њ–њ–Є—Б–∞–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –•–° –Ы–Я–Т–Я —Г –ґ–µ–љ—Й–Є–љ –≤ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–µ [18,19].
–Т –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤—Л—П–≤–ї–µ–љ —В–∞–Ї–ґ–µ –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–љ–µ–љ—М –•–° –Ы–Я–Э–Я –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –≥—А—Г–њ–њ–∞—Е, –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 2 –≥—А—Г–њ–њ—Л (4,2 –Љ–Љ–Њ–ї—М/–ї –≤ 1 –≥—А—Г–њ–њ–µ –њ—А–Њ—В–Є–≤ 5,5 –Љ–Љ–Њ–ї—М/–ї –≤–Њ 2 –≥—А—Г–њ–њ–µ (—А<0,05)). –≠—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –ї–Є—В–µ—А–∞—В—Г—А–љ—Л–Љ –і–∞–љ–љ—Л–Љ. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л—Е –њ–µ—А–Є– –Є –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Г—А–Њ–≤–љ—П –•–° –Ы–Я–Т–Я, —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –•–° –Ы–Я–Э–Я –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –њ—А–Є–Љ–µ—А–љ–Њ –љ–∞ 2 –Љ–≥/–і–ї (0,05 –Љ–Љ–Њ–ї—М/–ї) –≤ –≥–Њ–і –Љ–µ–ґ–і—Г –њ—П—В—Л–Љ –Є —Б–µ–і—М–Љ—Л–Љ –і–µ—Б—П—В–Є–ї–µ—В–Є–µ–Љ –ґ–Є–Ј–љ–Є. –Т–µ–ї–Є—З–Є–љ–∞ –•–° –Ы–Я–Э–Я —Г –ґ–µ–љ—Й–Є–љ –њ—А–Є–Љ–µ—А–љ–Њ —В–∞–Ї–∞—П –ґ–µ, –Ї–∞–Ї –Є —Г –Љ—Г–ґ—З–Є–љ —В–Њ–≥–Њ –ґ–µ –≤–Њ–Ј—А–∞—Б—В–∞ [18, 22,24–28]. –Я–Њ –і–∞–љ–љ—Л–Љ –∞–љ–∞–ї–Є–Ј–∞ NHLBI, –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ–Њ–≥–Њ –≤ 1992 –≥., –њ–Њ–≤—Л—И–µ–љ–љ—Л–є —Г—А–Њ–≤–µ–љ—М –•–° –Ы–Я–Э–Я –Є–Љ–µ–µ—В –±–Њ–ї–µ–µ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ —А–∞–Ј–≤–Є—В–Є–Є –Ш–С–° —Г –ґ–µ–љ—Й–Є–љ –Љ–ї–∞–і—И–µ 65 –ї–µ—В [14].
–£—А–Њ–≤–µ–љ—М –Ґ–У –±—Л–ї –њ–Њ–≤—Л—И–µ–љ –љ–∞ 38% –≤ –≥—А—Г–њ–њ–µ 1 (–ґ–µ–љ—Й–Є–љ—Л —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞) –Є –љ–∞ 25 % –≤ –≥—А—Г–њ–њ–µ 2 (–ґ–µ–љ—Й–Є–љ—Л –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞). –Т–µ—А–Њ—П—В–љ–Њ, —Н—В–Њ —В–∞–Ї–ґ–µ —Б–≤—П–Ј–∞–љ–Њ —Б –±–Њ–ї—М—И–µ–є —З–∞—Б—В–Њ—В–Њ–є –Њ–ґ–Є—А–µ–љ–Є—П —Г –ґ–µ–љ—Й–Є–љ 1 –≥—А—Г–њ–њ—Л. –Я—А–Є —Н—В–Њ–Љ —Б—А–µ–і–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ–Њ –≥—А—Г–њ–њ–∞–Љ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–Є—Б—М. –¶–µ–ї—Л–є —А—П–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –њ–Њ–≤—Л—И–µ–љ–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Ґ–У —П–≤–ї—П–µ—В—Б—П —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е —Б–Њ–±—Л—В–Є–є –Ї–∞–Ї —Г –Љ—Г–ґ—З–Є–љ, —В–∞–Ї –Є —Г –ґ–µ–љ—Й–Є–љ, –љ–Њ —Г –ґ–µ–љ—Й–Є–љ –Њ–љ –Є–Љ–µ–µ—В –±–Њ–ї–µ–µ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ [15,29]. –Ь–µ—В–∞––∞–љ–∞–ї–Є–Ј, –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ—Л–є –≤ 1996 –≥., –Ї–Њ—В–Њ—А—Л–є –≤–Ї–ї—О—З–Є–ї –љ–µ –Љ–µ–љ–µ–µ 46000 –Љ—Г–ґ—З–Є–љ –Є 11000 –ґ–µ–љ—Й–Є–љ –Є–Ј 17 –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ–Њ–Ї–∞–Ј–∞–ї —В–∞–Ї–ґ–µ, —З—В–Њ –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М –Ґ–У –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б 30% —А–Њ—Б—В–Њ–Љ –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–≥–Њ —А–Є—Б–Ї–∞ –і–ї—П –Љ—Г–ґ—З–Є–љ –Є 75% —А–Њ—Б—В–Њ–Љ –і–ї—П –ґ–µ–љ—Й–Є–љ [30]. –†–µ–Ј—Г–ї—М—В–∞—В—Л Stockholm Prospective Study, –≤–Ї–ї—О—З–Є–≤—И–µ–≥–Њ 1500 –ґ–µ–љ—Й–Є–љ —Б –њ–µ—А–Є–Њ–і–Њ–Љ –љ–∞–±–ї—О–і–µ–љ–Є—П —Б–≤—Л—И–µ 12 –ї–µ—В, —В–∞–Ї –ґ–µ –Њ–њ—А–µ–і–µ–ї–Є–ї–Є –≥–Є–њ–µ—А—В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–µ–Љ–Є—О –Ї–∞–Ї –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–є —Д–∞–Ї—В–Њ—А —А–Є—Б–Ї–∞ –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е —Б–Њ–±—Л—В–Є–є —Б—А–µ–і–Є –ґ–µ–љ—Й–Є–љ [31,32].
–° –≤–Њ–Ј—А–∞—Б—В–∞–љ–Є–µ–Љ –њ–Њ–љ–Є–Љ–∞–љ–Є—П –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –Ї–∞–Ї –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ [33], —А–∞—Б—В–µ—В –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –і–Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є—Е –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Љ–∞—А–Ї–µ—А–Њ–≤ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, —В–∞–Ї–Є—Е –Ї–∞–Ї hs––°–†–С. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Г—А–Њ–≤–µ–љ—М –°–†–С –њ–Њ–≤—Л—И–∞–µ—В—Б—П —Б –≤–Њ–Ј—А–∞—Б—В–Њ–Љ [34,35]. –£—А–Њ–≤–µ–љ—М hs––°–†–С, –њ—А–µ–≤—Л—И–∞—О—Й–Є–є 3 –Љ–≥/–ї, —П–≤–ї—П–µ—В—Б—П –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–Љ –њ—А–Є–Ј–љ–∞–Ї–Њ–Љ, —Б–≤—П–Ј–∞–љ–љ—Л–Љ —Б —А–Є—Б–Ї–Њ–Љ —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –Ј–і–Њ—А–Њ–≤—Л—Е –ї–Є—Ж –Є –±–Њ–ї—М–љ—Л—Е —Б —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є. Women`s Health Study –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Њ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –°–†–С —Г –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ—Л—Е –ґ–µ–љ—Й–Є–љ —Б –°–°–Ч [36]. –Т –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–Љ —Б–ї—Г—З–∞–є––Ї–Њ–љ—В—А–Њ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –і–ї–Є–≤—И–µ–Љ—Б—П –±–Њ–ї–µ–µ —В—А–µ—Е –ї–µ—В, –≤–Ї–ї—О—З–Є–≤—И–µ–Љ 28000 –ґ–µ–љ—Й–Є–љ, –∞–≤—В–Њ—А—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Є –њ–Њ–Љ–Є–Љ–Њ –°–†–С –і—А—Г–≥–Є–µ –Љ–∞—А–Ї–µ—А—Л –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П (—Б—Л–≤–Њ—А–Њ—В–Њ—З–љ—Л–є –∞–Љ–Є–ї–Њ–Є–і A, –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–6). –°—А–µ–і–Є –љ–Є—Е –°–†–С –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї –љ–∞–Є–±–Њ–ї—М—И–µ–µ –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ. –Т –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г—А–Њ–≤–µ–љ—М hs––°–†–С –±—Л–ї –њ–Њ–≤—Л—И–µ–љ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е, –љ–Њ —В–∞–Ї –ґ–µ –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ–Њ —Г –ґ–µ–љ—Й–Є–љ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞: 5,4 –Љ–≥/–ї –Є 3,1 –Љ–≥/–ї —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ (—А< 0,01).
–Ф–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –≥–Є–њ–Њ–ї–Є–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є —Б–Є–Љ–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ (–°–Є–Љ–≥–∞–ї) –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –ї–Є–њ–Є–і–Њ–≤ –Ї—А–Њ–≤–Є –Є —Г—А–Њ–≤–µ–љ—М hs––°–†–С –Њ—В–Љ–µ—З–µ–љ–Њ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –њ–∞—Ж–Є–µ–љ—В–Њ–Ї (—В–∞–±–ї. 3, 4).
–Ю–і–љ–∞–Ї–Њ –≤ —Е–Њ–і–µ –њ–Њ–і–±–Њ—А–∞ –і–Њ–Ј—Л —Б–Є–Љ–≤–∞—Б—В–∞—В–Є–љ–∞ –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤—Л—Е —Г—А–Њ–≤–љ–µ–є –ї–Є–њ–Є–і–Њ–≤ –Є –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і–Њ–≤, –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ –њ–∞—Ж–Є–µ–љ—В–Ї–∞–Љ –±–Њ–ї–µ–µ —Б—В–∞—А—И–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ —В—А–µ–±—Г—О—В—Б—П –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ (—В–∞–±–ї. 5). –°—А–µ–і–љ—П—П –і–Њ–Ј–∞ —Б–Є–Љ–≤–∞—Б—В–∞—В–Є–љ–∞ –≤ –≥—А—Г–њ–њ–µ –ґ–µ–љ—Й–Є–љ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 41,9 –Љ–≥, –≤ –≥—А—Г–њ–њ–µ –ґ–µ–љ—Й–Є–љ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ – 62,8 –Љ–≥.
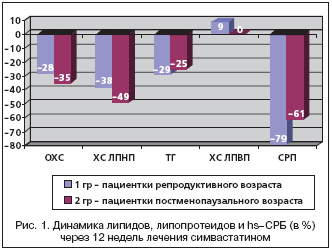
–Т –≥—А—Г–њ–њ–µ –ґ–µ–љ—Й–Є–љ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ —Г –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Г–і–∞–ї–Њ—Б—М –і–Њ–±–Є—В—М—Б—П —Ж–µ–ї–µ–≤—Л—Е —Г—А–Њ–≤–љ–µ–є –Ю–•–° –Є –•–° –Ы–Я–Э–Я (—А–Є—Б. 1). –Т —В–Њ–ґ–µ –≤—А–µ–Љ—П —Г 3 –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –љ–µ —Г–і–∞–ї–Њ—Б—М –і–Њ–±–Є—В—М—Б—П —Ж–µ–ї–µ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є –і–∞–ґ–µ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Б–Є–Љ–≤–∞—Б—В–∞—В–Є–љ–∞ –≤ –і–Њ–Ј–µ 80 –Љ–≥ –≤ —Б—Г—В–Ї–Є.
–Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –≤ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–µ (2 –≥—А—Г–њ–њ–∞) —Б–Є–Љ–≤–∞—Б—В–∞—В–Є–љ –≤ —Б—А–µ–і–љ–µ–Љ –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ–Њ, —З–µ–Љ –≤ 1 –≥—А—Г–њ–њ–µ —Б–љ–Є–ґ–∞–ї —Г—А–Њ–≤–µ–љ—М –Ю–•–° (–љ–∞ 28 % –≤ 1 –≥—А—Г–њ–њ–µ –Є –љ–∞ 35% –≤–Њ 2 –≥—А—Г–њ–њ–µ, —А<0,05), –Є –•–° –Ы–Я–Э–Я (–љ–∞ 38% –≤ 1 –≥—А—Г–њ–њ–µ –Є –љ–∞ 49% –≤–Њ 2 –≥—А—Г–њ–њ–µ, —А<0,01). –° –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, —В–µ—А–∞–њ–Є—П —Б–Є–Љ–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї–µ–µ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ–Њ–≤–ї–Є—П–ї–∞ –љ–∞ —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–µ–љ—П hs––°–†–С —Г –ґ–µ–љ—Й–Є–љ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ (–љ–∞ 79% –≤ 1 –≥—А—Г–њ–њ–µ –Є –љ–∞ 61% –≤–Њ 2 –≥—А—Г–њ–њ–µ, —А<0,05). –Э–∞–њ–Њ–Љ–љ–Є–Љ, —З—В–Њ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –≤ –≥—А—Г–њ–њ–µ –ґ–µ–љ—Й–Є–љ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –±—Л–ї–∞ –Є—Б—Е–Њ–і–љ–Њ –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є. –Я–Њ –і–∞–љ–љ—Л–Љ Ridker et al, 2001, —Б—В–∞—В–Є–љ—Л —Б–љ–Є–ґ–∞—О—В —Г—А–Њ–≤–µ–љ—М –°–†–Я –Ї—А–Њ–≤–Є —Г –±–Њ–ї—М–љ—Л—Е –Ш–С–° –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –Є—Б—Е–Њ–і–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –ї–Є–њ–Є–і–Њ–≤ –Ї—А–Њ–≤–Є –Є —Б—В–µ–њ–µ–љ–Є —Б–љ–Є–ґ–µ–љ–Є—П –•–° –Ы–Я–Э–Я. –Ю–і–љ–∞–Ї–Њ, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В —Б—В–∞—В–Є–љ–Њ–≤ —В–µ–Љ –ї—Г—З—И–µ, —З–µ–Љ –≤—Л—И–µ –Є—Б—Е–Њ–і–љ—Л–є —Г—А–Њ–≤–µ–љ—М –°–†–Я. –Я—А–µ–і–ї–∞–≥–∞–µ—В—Б—П –і–∞–ґ–µ –і–ї—П –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —Б—В–∞—В–Є–љ–Њ–≤ —Г—З–Є—В—Л–≤–∞—В—М —Г—А–Њ–≤–µ–љ—М –°–†–С.
–Т —В–µ—З–µ–љ–Є–µ 12––љ–µ–і–µ–ї—М–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ —В–µ—А–∞–њ–Є–Є —Б–Є–Љ–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ (–°–Є–Љ–≥–∞–ї) –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –љ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Б–µ—А—М–µ–Ј–љ—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є. –°–Њ–і–µ—А–ґ–∞–љ–Є–µ –Љ–Њ—З–µ–≤–Є–љ—Л, –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ –Ї—А–Њ–≤–Є, –Ї—А–µ–∞—В–Є–љ—Д–Њ—Б—Д–Њ–Ї–Є–љ–∞–Ј—Л, –∞—Б–њ–∞—А–∞–≥–Є–љ–Њ–≤–Њ–є –Є –∞–ї–∞–љ–Є–љ–Њ–≤–Њ–≤–є —В—А–∞–љ—Б–∞–Љ–Є–љ–∞–Ј, –±–Є–ї–Є—А—Г–±–Є–љ–∞ –Ї—А–Њ–≤–Є –Њ—Б—В–∞–≤–∞–ї–Њ—Б—М –≤ –њ—А–µ–і–µ–ї–∞—Е –љ–Њ—А–Љ—Л. –£ 2 –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –њ–Њ—П–≤–Є–ї–Є—Б—М –ґ–∞–ї–Њ–±—Л –љ–∞ –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В –≤ –њ—А–∞–≤–Њ–Љ –њ–Њ–і—А–µ–±–µ—А—М–µ –±–µ–Ј –њ–Њ–≤—Л—И–µ–љ–Є—П –њ–µ—З–µ–љ–Њ—З–љ—Л—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤ –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ –Њ–љ–Є –њ—А–µ–Ї—А–∞—В–Є–ї–Є –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞. 1 –њ–∞—Ж–Є–µ–љ—В–Ї–∞ –≤—Л–±—Л–ї–∞ –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ —Б–≤—П–Ј–Є —Б –љ–µ—Б–Њ–±–ї—О–і–µ–љ–Є–µ–Љ —А–µ–ґ–Є–Љ–∞ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤—Л—П–≤–ї–µ–љ—Л —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П —Г—А–Њ–≤–љ—П –ї–Є–њ–Є–і–Њ–≤ –Є –ї–Є–њ–Њ—А–Њ—В–µ–Є–і–Њ–≤, –∞ —В–∞–Ї–ґ–µ hs––°–†–С —Г –ґ–µ–љ—Й–Є–љ —Б –≤—Л—Б–Њ–Ї–Є–Љ –Ї–Њ—А–Њ–љ–∞—А–љ—Л–Љ —А–Є—Б–Ї–Њ–Љ –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ–∞—Е (–≤ –≥—А—Г–њ–њ–∞—Е –ґ–µ–љ—Й–Є–љ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –Є –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞). –£ –ґ–µ–љ—Й–Є–љ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–µ —Г—А–Њ–≤–љ–Є –Њ–±—Й–µ–≥–Њ –Ю–•–°, –•–° –Ы–Я–Э–Я. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –љ–µ —А–∞–Ј–ї–Є—З–∞—О—В—Б—П —Г—А–Њ–≤–љ–Є –Ґ–У –Є –•–° –Ы–Я–Т–Я –≤ –Њ–±–µ–Є—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ–∞—Е. –Ш–љ—В–µ—А–µ—Б–љ–Њ, —З—В–Њ —Г –ґ–µ–љ—Й–Є–љ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –≤—Л—П–≤–ї–µ–љ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М hs––°–†–С, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –±–Њ–ї—М—И–µ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ —Г —Н—В–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–Ї.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–°–Є–Љ–≤–∞—Б—В–∞—В–Є–љ (–°–Є–Љ–≥–∞–ї, –Ї–Њ–Љ–њ–∞–љ–Є—П TEVA) —Г–ї—Г—З—И–∞–µ—В –ї–Є–њ–Є–і–љ—Л–є –њ—А–Њ—Д–Є–ї—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є–µ–є, –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В —Г—А–Њ–≤–љ–Є –Њ–±—Й–µ–≥–Њ –•–°, –•–° –Ы–Я–Э–Я –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е, –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ. –Я—А–Є–µ–Љ –°–Є–Љ–≥–∞–ї–∞ –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ–Љ —Б–µ—А—М–µ–Ј–љ—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є. –Т –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є –ї–Є–њ–Є–і–Њ–≤ –Є –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і–Њ–≤ —Г –ґ–µ–љ—Й–Є–љ –≤ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–µ –±—Л–ї–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ, —Н—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ —В–Њ–Љ, —З—В–Њ –њ—А–Є –њ–Њ–і–±–Њ—А–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –і–Њ–Ј—Л —Б—В–∞—В–Є–љ–Њ–≤ —Г –ґ–µ–љ—Й–Є–љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М –≤–Њ–Ј—А–∞—Б—В –њ–∞—Ж–Є–µ–љ—В–Ї–Є.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Nicoline Jochmann, Karl Stangl et aL. Female–specific aspects in the pharmacotherapy of chronic cardiovascular diseases, Eur Heart J 2005 26: 1585–1595
2. Gibson DM, Bron NJ, Richens A, Hounslow NJ, Sedman AJ, Whitfield LR. Effect of age and gender on pharmacokinetics of atorvastatin in humans. J Clin Pharmacol 1996;36:242–246.[Abstract/Free Full Text]
3. Cheng H, Rogers JD, Sweany AE, Dobrinska MR, Stein EA, Tate AC, Amin RD, Quan H. Influence of age and gender on the plasma profiles of 3–hydroxy–3–methylglutaryl–coenzyme A (HMG–CoA) reductase inhibitory activity following multiple doses of lovastatin and simvastatin. Pharm Res 1992;9:1629–1633.[CrossRef][ISI][Medline]
4. Isaacsohn J, Zinny M, Mazzu A, Lettieri J, Heller AH. Influence of gender on the pharmacokinetics, safety, and tolerability of cerivastatin in healthy adults. Eur J Clin Pharmacol 2001;56:897–903.[CrossRef][ISI][Medline]
5. Martin PD, Dane AL, Nwose OM, Schneck DW, Warwick MJ. No effect of age or gender on the pharmacokinetics of rosuvastatin: a new HMG–CoA reductase inhibitor. J Clin Pharm 2002;42:1116–1121.[CrossRef][ISI]
6. Scripture CD, Pieper JA. Clinical pharmacokinetics of fluvastatin. Clin Pharmacokinet 2001;40:263–281.[ISI][Medline]
7. Smith HT, Jokubaitis LA, Troendle AJ, Hwang DS, Robinson WT. Pharmacokinetics of fluvastatin and specific drug interactions. Am J Hypertens 1993;6:375–382.
8. FDA. CDER. Report no.: http:www.fda.gov/cder/foi/label2001/207S6lbl.pdf.
9. Shepard DR, Jenid H, Thacker HL. Gender, hyperlipidemia, and coronary artery disease. Compr Ther 2003;29:7–17.[CrossRef][Medline]
10. Cheung BMY, Lauder IJ, Lau C–P, Kumana CR. Meta–analysis of large randomized controlled trials to evaluate the impact of statins on cardiovascular outcomes. Br J Clin Pharmacol 2004;57:640–651.[CrossRef][ISI][Medline]
11. Berra K. Women, coronary heart disease, and dyslipidemia: does gender alter detection, evaluation, or therapy? J Cardiovasc Nurs 2000;14:59–78.[Medline]
12. Stangl V., Baumann G., and Stangl K. Coronary aterogenetic risk factors in women European Heard Journal (2002) 23, 1738–1752.
13. Garber AM, Browner WS, Hulley SB, Cholesterol screening in asymptomatic adults, revisited. Ann Intern Med 1996; 124:518–31.
14. Keil U. Coronary artery disease: the role of lipids, hypertension and smoking. Basic Res Cardiol 2000; 95: I/52–I/58.
15. Castelly WP. Cholesterol and lipids in the risk of coronary artery disease: the Framingham Heart Study. Can J Cardiol 1988; 4: 5A–10A.
16. Keil U, Liese AD, Hens HW et al. Classical risk factors and their impact on incident non–fatal and fatal myocardial infarction and all cause mortality in southern Germany. Results from the MONICA Augsburg cohort study 1984–1992. monitoring Trends and Determinants in Cardiovascular Diseases. Eur Hart J 1998; 19: 1197–207.
17. Maron DJ. The epidemiology of low levels of high–density lipoprotein cholesterol in patients with and without coronary artery disease. Am J Cardiol 2000; 86: 11L–14L.
18. Johnson CVL, Rifkind BM, Sempos CT et al. Declining serum total cholesterol levels among US adults: the National Health and Nutrition Examination Surveys. JAMA 1993; 269: 3002–8.
19. Matthews KA, Meilahn E, Killer LH, Kelsey SF, Caggiula AW, Wing RR. Menopause and risk factors for coronary heart disease. N Engl J Med 1989; 321: 641–6.
20. Gordon DJ, Probsfield JL, Garrison RJ et al. High–density lipoprotein cholesterol and cardiovascular disease: for prospective American studies. Circulation 1989; 79: 8–15.
21. Kannel WB, Wilson PW. Risk factors that attenuate the female coronary disease advantage. Arch Intern Med 1995; 155: 57–61.
22. Welty FK. Cardiovascular disease and dyslipidemia in women. Arch Intern Med 2001; 161: 514–22.
23. Corti MC, Guralnik JM, Salive et al. HDL cholesterol predicts coronary heart disease mortality in older persons. JAMA 1995; 274: 539–44.
24. Kannel WB. Contributions of the Framingham Heart Study of conquest of coronary artery disease. Am J Cardiol 1988; 62: 1109–12.
25. Packard C, Caslake M, Shepherd J. The role of small, dense low density lipoprotein (LDL): a new look. Int J Cardiol 2000: 74: S17–S22.
26. Krauss RM, Blanch PJ. Detection and quantification of LDL subfractions. Curr Opin Lipidol 1992; 3: 377–83.
27. Carr MC, Kim KH, Zambon A et al. Changes in LDL density across the menopause transition. J Investig Med 2000; 48: 245–50.
28. Anber V, Griffin BA, McConnell M et al. Influence of plasma lipid LDL–subfraction profile on the interaction between low density lipoprotein with human arterial wall proteoglycans. Atherosclerosis 1996; 124: 261–71.
29. Assman G, Schulte H, Relation of high–density lipoprotein cholesterol and triglycerides to incidence of atherosclerotic coronary artery disease (the PROCAM experience). Am J Cardiol 1992; 70: 70 733–7.
30. Hokanson JE, Austin MA. Plasma triglyceride level is risk factor for cardiovascular disease in independent of high–density lipoprotein cholesterol level: a meta–analysis of population–based prospective studies. J Cardiovasc Risk 1996; 3: 213–19.
31. Lapidus L, Bengtsson C, Lindquist O, Sigurdsson JA, Ryboe E. Triglycerides – main lipid risk factor for cardiovascular disease in women? Acta Med Scand 1985; 217: 481–9.
32. D’Agostio RB, Russell MW, Huse DM et al. Primary and subsequent coronary risk appraisal: New results from the Framingham Study. Fm Heart J 2000; 139: 272–81.
33. Ross R. Atherosclerosis – an inflammatory disease. N Engl J Med 1999; 340: 115–26.
34. ECAT angina pectoris study. Baseline associations of haemostatic factors with extent coronary arteriosclerosis and risk factors in 3000 patients with angina pectoris undergoing coronary arteriography. Eur Heart J 1993; 14:8–17.
35. Tatary MC, Heinrich J, Junker R et al. C–reactiv protein and the severity of atherosclerosis myocardial infarction patients with stable angina pectoris. Eur Heart J 2000; 21:1000–8.
36. Ridker PM, Buring JE, Shih H, Matias M, Hennekens CH. Prospective study of C–reactive protein and the risk future cardiovascular events among healthy woman. Circulation 1998; 98: 731–3.
37. Mettinen TA, Pyorala K, Olsson AG, et al., for the Scandinavian Simvastatin Study Group. Cholesterol–lowering therapy in women early patients with myocardial infarction or angina pectoris. Findings from the Scandinavian Simvastatin Study (4S). Circulation 1997; 96:4211–18
38. Heart Protection Group. MRC/BHF Heart Protection Study of cholesterol lowerind with simvastatin in 20 536 high–risk individuals: a randomized placedo–controlled trial. Lancet 2002; 360:7–22.
39. Lewis SJ, Sacks FM, Mitchell JS, et al., for the CARE Investigators. Effect of pravastatin on cardiovascular events in women after myocardial infarction: The Cholesterol and Recurrent Events (CARE) Trial. J Am Coll Cardiol 1998; 32:130–6
40. The long–Term Investigators with Pravastatin in Ischaemic Disease (LIPID) Study Group. Prevention of cardiovascular events and death with pravastatin in patients with coronary heart disease and broad range of cholesterol levels. N Engl J Med 1998; 339:1349–57
41. –Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –Ї–Њ—А—А–µ–Ї—Ж–Є—П –љ–∞—А—Г—И–µ–љ–Є–є –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ —Б —Ж–µ–ї—М—О –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞. –†–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –ї–µ—З–µ–љ–Є—О. –Ъ–Њ–Љ–Є—В–µ—В —Н–Ї—Б–њ–µ—А—В–Њ–≤ –Т—Б–µ—А–Њ—Б—Б–Є–є—Б–Ї–Њ–≥–Њ –љ–∞—Г—З–љ–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Њ–≤.












