–С–Њ–ї—М—И–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –і–ї—П –Њ—Ж–µ–љ–Ї–Є —В—П–ґ–µ—Б—В–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞ —Б –Э–° –Є –њ—А–Њ–≥–љ–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П —А–∞–Ј–≤–Є—В–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ—А–µ–і–Њ—Б—В–∞–≤–ї—П—О—В —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є–µ –Њ—Ж–µ–љ–Є—В—М —Д—Г–љ–Ї—Ж–Є—О —Н–љ–і–Њ—В–µ–ї–Є—П.
–Т–њ–µ—А–≤—Л–µ –Њ —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ–є —А–Њ–ї–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Н–љ–і–Њ—В–µ–ї–Є—П –≤ —А–µ–≥—Г–ї—П—Ж–Є–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —В–Њ–љ—Г—Б–∞ –±—Л–ї–Њ –Ј–∞—П–≤–ї–µ–љ–Њ –≤ —Б—В–∞—В—М–µ R. Furchgott –Є J. Zawadzki –≤ 1980 –≥–Њ–і—Г. –У–ї–∞–≤–љ–∞—П —А–Њ–ї—М –≤ —Н—В–Њ–Љ –Њ—В–≤–Њ–і–Є–ї–∞—Б—М —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л–Љ –Ї–ї–µ—В–Ї–∞–Љ, –Ї–Њ—В–Њ—А—Л–µ –±—Л–ї–Є –Њ—Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–љ—Л –∞–≤—В–Њ—А–∞–Љ–Є, –Ї–∞–Ї «—Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–є —Н–љ–і–Њ–Ї—А–Є–љ–љ—Л–є –Њ—А–≥–∞–љ, –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—О—Й–Є–є —Б–≤—П–Ј—М –≤ –Ї—А–Є—В–Є—З–µ—Б–Ї–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е –Љ–µ–ґ–і—Г –Ї—А–Њ–≤—М—О –Є —В–Ї–∞–љ—П–Љ–Є» [4]. –Т–њ–Њ—Б–ї–µ–і—Б—В–≤–Є–Є –±—Л–ї–Њ –і–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Н–љ–і–Њ—В–µ–ї–Є–є —П–≤–ї—П–µ—В—Б—П –∞–Ї—В–Є–≤–љ—Л–Љ –Њ—А–≥–∞–љ–Њ–Љ, –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П –Ї–Њ—В–Њ—А–Њ–≥–Њ –Њ–±—П–Ј–∞—В–µ–ї—М–љ–∞ –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤—Б–µ—Е —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –≤–Ї–ї—О—З–∞—П –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј, –≥–Є–њ–µ—А—В–Њ–љ–Є—О, –Ш–С–°, –•–°–Э –Є —В.–і.
–£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —Н–љ–і–Њ—В–µ–ї–Є–є –≤–ї–Є—П–µ—В –љ–∞ —Б–Њ—Б—Г–і–Є—Б—В—Л–є —В–Њ–љ—Г—Б –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ–Њ —З–µ—А–µ–Ј –Њ—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ —Б–Њ—Б—Г–і–Њ—А–∞—Б—И–Є—А—П—О—Й–Є—Е –Є —Б–Њ—Б—Г–і–Њ—Б—Г–ґ–Є–≤–∞—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –Є –Љ–Њ–і—Г–ї–Є—А—Г–µ—В —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї [1,2]. –Ю–≥—А–Њ–Љ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ —Н–љ–і–Њ—В–µ–ї–Є—П –≤ —А–∞–Ј–≤–Є—В–Є–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≤—Л—В–µ–Ї–∞–µ—В —Г–ґ–µ –Є–Ј —В–Њ–≥–Њ, —З—В–Њ –Њ—Б–љ–Њ–≤–љ–∞—П —З–∞—Б—В—М –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ (–Р–Я–§) —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–∞ –љ–∞ –Љ–µ–Љ–±—А–∞–љ–µ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї. –Я–Њ –і–∞–љ–љ—Л–Љ V. Dwu [3], 90% –≤—Б–µ–≥–Њ –Њ–±—К–µ–Љ–∞ —А–µ–љ–Є–љ––∞–љ–≥–Є—В–µ–љ–Ј–Є–љ––∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л (–†–Р–Р–°) –њ—А–Є—Е–Њ–і–Є—В—Б—П –љ–∞ –Њ—А–≥–∞–љ—Л –Є —В–Ї–∞–љ–Є (10% – –љ–∞ –њ–ї–∞–Ј–Љ—Г), —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е —Б–Њ—Б—Г–і–Є—Б—В—Л–є —Н–љ–і–Њ—В–µ–ї–Є–є –Ј–∞–љ–Є–Љ–∞–µ—В –њ–µ—А–≤–Њ–µ –Љ–µ—Б—В–Њ, –њ–Њ—Н—В–Њ–Љ—Г –≥–Є–њ–µ—А–∞–Ї—В–Є–≤–∞—Ж–Є—П –†–Р–Р–° —П–≤–ї—П–µ—В—Б—П –љ–µ–њ—А–µ–Љ–µ–љ–љ—Л–Љ —Г—Б–ї–Њ–≤–Є–µ–Љ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є. –Ю–і–љ–Є–Љ –Є–Ј –Љ–Њ—Й–љ–µ–є—И–Є—Е –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—В–Њ—А–Њ–≤, –≤—Л–і–µ–ї—П–µ–Љ—Л—Е —Н–љ–і–Њ—В–µ–ї–Є–µ–Љ —Б–Њ—Б—Г–і–Њ–≤, —П–≤–ї—П–µ—В—Б—П —Н–љ–і–Њ—В–µ–ї–Є–љ–1 (–≠–Ґ–1).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤—Л—П–≤–ї–µ–љ–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –Э–° –Є —Г—А–Њ–≤–љ–µ–Љ –≠–Ґ–1 –≤ –Ї—А–Њ–≤–Є –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –љ–µ—Б–Њ–Љ–љ–µ–љ–љ—Л–є –Є–љ—В–µ—А–µ—Б. –Ш–Ј—Г—З–µ–љ–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –Є–Р–Я–§ (—З–µ—А–µ–Ј –†–Р–Р–° –Є –±—А–∞–і–Є–Ї–Є–љ–Є–љ) –љ–∞ —Г—А–Њ–≤–µ–љ—М –Њ–і–љ–Њ–≥–Њ –Є–Ј –Љ–Њ—Й–љ–µ–є—И–Є—Е –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—В–Њ—А–Њ–≤ – –≠–Ґ–1, –≤—Л—А–∞–±–∞—В—Л–≤–∞–µ–Љ–Њ–≥–Њ —Б–Њ—Б—Г–і–Є—Б—В—Л–Љ —Н–љ–і–Њ—В–µ–ї–Є–µ–Љ –≤ –Ї—А–Њ–≤–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ —Г—Б–ї–Њ–≤–Є—П—Е –≥–Є–њ–Њ–Ї—Б–Є–Є, —П–≤–ї—П–µ—В—Б—П –≤–∞–ґ–љ—Л–Љ —Б –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П. –≠—В–Њ –≤–ї–Є—П–љ–Є–µ –Є–Р–Я–§ –Љ–Њ–ґ–µ—В –Њ—В—А–∞–ґ–∞—В—М—Б—П –Є –љ–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ —В–µ—З–µ–љ–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
–Т –і–∞–љ–љ–Њ–є –њ—Г–±–ї–Є–Ї–∞—Ж–Є–Є –Љ—Л –њ—А–µ–і—Б—В–∞–≤–ї—П–µ–Љ —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤—Л–њ–Њ–ї–љ–µ–љ–љ–Њ–≥–Њ –љ–∞ –Ї–∞—Д–µ–і—А–µ —В–µ—А–∞–њ–Є–Є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л –У–Ю–£ –Ф–Я–Ю –†–Ь–Р–Я–Ю –љ–∞ –±–∞–Ј–µ –У–Ъ–С –Є–Љ. –°.–Я. –С–Њ—В–Ї–Є–љ–∞, —Ж–µ–ї—М—О –Ї–Њ—В–Њ—А–Њ–≥–Њ —П–≤–Є–ї–Њ—Б—М –Є–Ј—Г—З–Є—В—М –і–Є–љ–∞–Љ–Є–Ї—Г –Є –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї—Г—О —Ж–µ–љ–љ–Њ—Б—В—М –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≠–Ґ–1 –≤ –Ї—А–Њ–≤–Є –±–Њ–ї—М–љ—Л—Е –Э–° –Є –Њ—Ж–µ–љ–Є—В—М –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –≠–Ґ–1 —Б –њ–Њ–Љ–Њ—Й—М—О –Є–Р–Я–§.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л 79 —З–µ–ї–Њ–≤–µ–Ї, –Є–Ј –љ–Є—Е 51 —З–µ–ї–Њ–≤–µ–Ї – —Н—В–Њ –±–Њ–ї—М–љ—Л–µ, —Б–Њ—Б—В–∞–≤–Є–≤—И–Є–µ –≥—А—Г–њ–њ—Г —Б –љ–µ—Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–µ–є, 20 —З–µ–ї–Њ–≤–µ–Ї – –Ј–і–Њ—А–Њ–≤—Л–µ –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж—Л, 8 —З–µ–ї–Њ–≤–µ–Ї – –±–Њ–ї—М–љ—Л–µ –Ш–С–°, –њ–µ—А–µ–љ–µ—Б—И–Є–µ —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—В–Є–≤–љ—Л–µ –Њ–њ–µ—А–∞—В–Є–≤–љ—Л–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –љ–∞ –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –∞—А—В–µ—А–Є—П—Е.
–Ъ—А–Є—В–µ—А–Є—П–Љ–Є –≤–Ї–ї—О—З–µ–љ–Є—П —П–≤–Є–ї–Є—Б—М: –љ–∞–ї–Є—З–Є–µ —В–Є–њ–Є—З–љ–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ –∞–љ–≥–Є–љ–Њ–Ј–љ–Њ–≥–Њ –њ—А–Є—Б—В—Г–њ–∞, –≤–Њ–Ј–љ–Є–Ї—И–µ–≥–Њ –≤–њ–µ—А–≤—Л–µ –њ—А–Є –љ–∞–≥—А—Г–Ј–Ї–µ –Є–ї–Є –≤ –њ–Њ–Ї–Њ–µ; —Г—З–∞—Й–µ–љ–Є–µ (–њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ) –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –љ–∞–њ—А—П–ґ–µ–љ–Є—П –Є–ї–Є –њ–Њ–Ї–Њ—П, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–µ–і—Л–і—Г—Й–Є–Љ–Є –≤ —В–µ—З–µ–љ–Є–µ –љ–µ –±–Њ–ї–µ–µ 30 –њ–Њ—Б–ї–µ–і–љ–Є—Е –і–љ–µ–є –і–Њ –Љ–Њ–Љ–µ–љ—В–∞ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є; –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –љ–∞ –≠–Ъ–У –≤ –≤–Є–і–µ –њ—А–µ—Е–Њ–і—П—Й–µ–є –і–µ–њ—А–µ—Б—Б–Є–Є —Б–µ–≥–Љ–µ–љ—В–∞ ST –Є/–Є–ї–Є –Є–љ–≤–µ—А—Б–Є–Є –Ј—Г–±—Ж–∞ –Ґ –±–µ–Ј –њ–Њ–і—К–µ–Љ–∞ —Б–µ–≥–Љ–µ–љ—В–∞ ST –Є —Б–≤–µ–ґ–Є—Е –Ј—Г–±—Ж–Њ–≤ Q; –Њ—В—Б—Г—В—Б—В–≤–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –Њ—Б—В—А–Њ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞, —В–∞–Ї–Є—Е –Ї–∞–Ї —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Ї–∞—А–і–Є–Њ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤ –Ї—А–Њ–≤–Є (–Ъ–§–Ъ, –Ь–Т —Д—А–∞–Ї—Ж–Є–Є –Ъ–§–Ъ, –Р–°–Ґ, –Р–Ы–Ґ, –Ы–Ф–У, —В—А–Њ–њ–Њ–љ–Є–љ–∞ –Ґ), –Њ—В—Б—Г—В—Б—В–≤–Є–µ –≠–Ъ–У––њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –љ–µ–Ї—А–Њ–Ј–∞ –Љ–Є–Њ–Ї–∞—А–і–∞).
–Ъ—А–Є—В–µ—А–Є—П–Љ–Є –Є—Б–Ї–ї—О—З–µ–љ–Є—П –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —П–≤–ї—П–ї–Њ—Б—М —Б–ї–µ–і—Г—О—Й–µ–µ: –±–Њ–ї—М–љ—Л–µ —Б –≤—Л—Б–Њ–Ї–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–µ–є (–Р–Ф >170/110 –Љ–Љ —А—В.—Б—В.); –±–Њ–ї—М–љ—Л–µ —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є II–IV –Ї–ї–∞—Б—Б–∞ –њ–Њ NYHA; –±–Њ–ї—М–љ—Л–µ —Б –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М—О –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –≤ —В–µ—А–∞–њ–Є–Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ (–≥–Є–њ–Њ—В–Њ–љ–Є—П – –Р–Ф<90/60 –Љ–Љ —А—В.—Б—В.); –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞ –Є–ї–Є –Є–љ—Б—Г–ї—М—В –Љ–µ–љ–µ–µ —З–µ–Љ –Ј–∞ 3 –Љ–µ—Б—П—Ж–∞ –і–Њ –љ–∞—З–∞–ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П; –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ –љ–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є –Є –њ–Њ—З–µ–Ї (–Р–°–Ґ, –Р–Ы–Ґ –≤—Л—И–µ –љ–Њ—А–Љ—Л –≤ 2,5 —А–∞–Ј–∞, –Ї—А–µ–∞—В–Є–љ–Є–љ >2,0 –Љ–≥/–і–ї, —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–∞—П –Љ–Њ—З–µ–≤–Є–љ–∞ >5,0 –Љ—Н–Ї–≤/–ї, –Ї–∞–ї–Є–є –≤—Л—И–µ 5,5 –Љ–Љ–Њ–ї—М/–ї); —Г—А–Њ–≤–µ–љ—М –°–†–С –≤ –Ї—А–Њ–≤–Є –≤—Л—И–µ 10 –Љ–≥/–ї (–њ–Њ—Б–Ї–Њ–ї—М–Ї—Г —Н—В–Њ –љ–µ –Љ–Њ–≥–ї–Њ –≥–∞—А–∞–љ—В–Є—А–Њ–≤–∞—В—М –Њ—В—Б—Г—В—Б—В–≤–Є–µ –Ї–∞–Ї–Є—Е––ї–Є–±–Њ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –Ї—А–Њ–Љ–µ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л—Е –Э–°); –ї—О–±—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є–ї–Є —Б–Њ—Б—В–Њ—П–љ–Є—П, –Ї–Њ—В–Њ—А—Л–µ –љ–∞—А—Г—И–∞—О—В —Д—Г–љ–Ї—Ж–Є—О —Б–Є—Б—В–µ–Љ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Є/–Є–ї–Є –Љ–Њ–≥—Г—В –њ—А–Є–≤–µ—Б—В–Є –Ї –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –∞–±—Б–Њ—А–±—Ж–Є–Є, —З—А–µ–Ј–Љ–µ—А–љ–Њ–Љ—Г –љ–∞–Ї–Њ–њ–ї–µ–љ–Є—О, –љ–∞—А—Г—И–µ–љ–Є—О –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Є–ї–Є –љ–∞—А—Г—И–µ–љ–Є—О —Н–Ї—Б–Ї—А–µ—Ж–Є–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤; —Б–Є—Б—В–µ–Љ–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥–ї–Є –љ–∞—А—Г—И–∞—В—М —Е–Њ–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є–ї–Є –Є–љ—В–µ—А–њ—А–µ—В–∞—Ж–Є—О —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ (–љ–∞–њ—А–Є–Љ–µ—А, —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–µ—З–µ–љ–Є, –њ–Њ—З–µ–Ї); –љ–µ—Б—В–∞–±–Є–ї—М–љ—Л–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (–љ–∞–њ—А–Є–Љ–µ—А, –љ–µ–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Й–Є—В–Њ–≤–Є–і–љ–Њ–є –ґ–µ–ї–µ–Ј—Л, —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В —Б HbA1c –±–Њ–ї–µ–µ –ї–Є–±–Њ —А–∞–≤–љ–Њ–Љ 10%); –Є–Љ–µ—О—Й–Є–µ—Б—П –∞–ї–Ї–Њ–≥–Њ–ї—М–љ—Л–µ –Є–ї–Є –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–µ –∞–±—Б—В–Є–љ–µ–љ—Ж–Є–Є; –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М –Є –ї–∞–Ї—В–∞—Ж–Є—П, –њ—Б–Є—Е–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П; —Г—З–∞—Б—В–Є–µ –≤ –і—А—Г–≥–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –Ј–∞ 30 –і–љ–µ–є –і–Њ –љ–∞—З–∞–ї–∞ —Г—З–∞—Б—В–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є.
–°—В–∞–љ–і–∞—А—В–љ–∞—П –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –≤–Ї–ї—О—З–∞–ї–∞ –≤ —Б–µ–±—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ: –љ–Є—В—А–∞—В–Њ–≤ –≤/–≤ –Ї–∞–њ–µ–ї—М–љ–Њ –≤ —В–µ—З–µ–љ–Є–µ 1–2 —Б—Г—В–Њ–Ї (–њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є) —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –њ–µ—А–µ—Е–Њ–і–Њ–Љ –љ–∞ –њ–µ—А–Њ—А–∞–ї—М–љ—Л–є –њ—А–Є–µ–Љ, –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–Њ–≤, ?––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤, –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–Њ–≤ –≤ –њ–µ—А–≤—Л–µ —Б—Г—В–Ї–Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ, –Ј–∞—В–µ–Љ –њ–Њ–і –Ї–Њ–ґ—Г –ґ–Є–≤–Њ—В–∞ –њ–Њ —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —Б—Е–µ–Љ–µ. –Я—А–Є –љ–∞–ї–Є—З–Є–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є –Ї —В–µ—А–∞–њ–Є–Є –і–Њ–±–∞–≤–ї—П–ї–Є—Б—М –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞ (–∞–Љ–ї–Њ–і–Є–њ–Є–љ –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ 5–10 –Љ–≥). –Т –Ї–∞—З–µ—Б—В–≤–µ –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є –њ–Њ –Љ–µ—А–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–µ –Є –љ–µ–љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–µ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Є –Є –љ–µ–є—А–Њ–ї–µ–њ—В–Є–Ї–Є.
–Т—Б–µ–Љ –±–Њ–ї—М–љ—Л–Љ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –±—Л–ї–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–Њ —Б–Њ–±–ї—О–і–µ–љ–Є–µ –≥–Є–њ–Њ—Е–Њ–ї–µ—Б—В–µ—А–Є–љ–Њ–≤–Њ–є –і–Є–µ—В—Л. –Я–Њ –Њ–Ї–Њ–љ—З–∞–љ–Є–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤—Б–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –±—Л–ї —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ –њ—А–Є–µ–Љ —Б—В–∞—В–Є–љ–Њ–≤. –Ф–ї—П –Є—Б–Ї–ї—О—З–µ–љ–Є—П –≤–ї–Є—П–љ–Є—П –љ–∞ —Н–љ–і–Њ—В–µ–ї–Є–є —Б–Њ—Б—Г–і–Њ–≤ –њ–∞—Ж–Є–µ–љ—В—Л –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –љ–µ –њ–Њ–ї—Г—З–∞–ї–Є –≤ —В–µ—А–∞–њ–Є–Є –Р–†–Р–II –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є —Б—В–∞—В–Є–љ—Л.
–У—А—Г–њ–њ–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–° –±—Л–ї–∞ —А–∞–Ј–і–µ–ї–µ–љ–∞ –љ–∞ 2 –≥—А—Г–њ–њ—Л.
–У—А—Г–њ–њ–∞–1 – –≥—А—Г–њ–њ–∞ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Б—В–∞–љ–і–∞—А—В–љ—Г—О —В–µ—А–∞–њ–Є—О —Б –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ –Р–Я–§ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ (—В–Њ—А–≥–Њ–≤–Њ–µ –љ–∞–Ј–≤–∞–љ–Є–µ «–Ф–Є—А–Њ—В–Њ–љ», –Ї–Њ–Љ–њ–∞–љ–Є—П –У–µ–і–µ–Њ–љ –†–Є—Е—В–µ—А) –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ 5–40 –Љ–≥ (35 —З–µ–ї–Њ–≤–µ–Ї).
–У—А—Г–њ–њ–∞–2 – –≥—А—Г–њ–њ–∞ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Б—В–∞–љ–і–∞—А—В–љ—Г—О —В–µ—А–∞–њ–Є—О –±–µ–Ј –Ї–∞–Ї–Є—Е––ї–Є–±–Њ –Є–Р–Я–§ – 16 —З–µ–ї–Њ–≤–µ–Ї. –Я–∞—Ж–Є–µ–љ—В—Л —Н—В–Њ–є –≥—А—Г–њ–њ—Л –љ–µ –њ–Њ–ї—Г—З–∞–ї–Є –Є–Р–Я–§ –≤–≤–Є–і—Г –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–є –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є, –љ–∞–ї–Є—З–Є—П –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ –Є–ї–Є –њ–Њ–љ–Є–ґ–µ–љ–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Р–Ф –Є —В.–і. –Ґ–∞–Љ, –≥–і–µ —Н—В–Њ –±—Л–ї–Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –Є–Р–Я–§ –Ј–∞–Љ–µ–љ—П–ї–Є—Б—М –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞–Љ–Є –Ї–∞–ї—М—Ж–Є—П –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞.
–Т—Б–µ–Љ –±–Њ–ї—М–љ—Л–Љ –Э–° –≤–Њ –≤—А–µ–Љ—П –љ–∞—Е–Њ–ґ–і–µ–љ–Є—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –њ–Њ–і—А–Њ–±–љ–Њ–µ –Ї–ї–Є–љ–Є–Ї–Њ––Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ: –Њ—Б–Љ–Њ—В—А, –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Є–љ–і–µ–Ї—Б–∞ –Љ–∞—Б—Б—Л —В–µ–ї–∞ (–Ш–Ь–Ґ), –Њ—Ж–µ–љ–Ї–∞ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞, —А–µ–≥–Є—Б—В—А–∞—Ж–Є—П —Б—В–∞–љ–і–∞—А—В–љ–Њ–є –≠–Ъ–У –µ–ґ–µ–і–љ–µ–≤–љ–Њ –≤ —В–µ—З–µ–љ–Є–µ 3–4 –і–љ–µ–є, –Ј–∞—В–µ–Љ 1–2 —А–∞–Ј–∞ –≤ –љ–µ–і–µ–ї—О; –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –∞–љ–∞–ї–Є–Ј—Л –Ї—А–Њ–≤–Є, –Љ–Њ—З–Є, –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ї—А–Њ–≤–Є, –≤–Ї–ї—О—З–∞—О—Й–Є–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Д–µ—А–Љ–µ–љ—В–Њ–≤ –Р–Ы–Ґ, –Р–°–Ґ, –Ы–Ф–У, –Ъ–§–Ъ, –Ь–Т––Ъ–§–Ъ, –Ї—А–µ–∞—В–Є–љ–Є–љ–∞, –Љ–Њ—З–µ–≤–Є–љ—Л, —Н–ї–µ–Ї—В—А–Њ–ї–Є—В–Њ–≤, –Ї–Њ–∞–≥—Г–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї—А–Њ–≤–Є. –°–Њ–≤–Љ–µ—Б—В–љ–Њ —Б —Б–Њ—В—А—Г–і–љ–Є–Ї–∞–Љ–Є –Ї–∞—Д–µ–і—А—Л –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –†–Ь–Р–Я–Ю –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М —Б–ї–µ–і—Г—О—Й–Є–µ –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Њ–њ—А–µ–і–µ–ї—П–ї–Є—Б—М –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ (–Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Ю–•–°, –•–° –Ы–Я–Т–Я, –•–° –Ы–Я–Э–Я, –Ґ–У); —Г—А–Њ–≤–µ–љ—М –°–—А–µ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ (–°–†–С); –Є–Љ–Љ—Г–љ–Њ—Д–µ—А–Љ–µ–љ—В–љ–Њ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≠–Ґ–1.
–Я–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞, –°–†–С –Є –≠–Ґ–1 –Њ–њ—А–µ–і–µ–ї—П–ї–Є –љ–∞ 1–3––Є —Б—Г—В–Ї–Є –њ—А–µ–±—Л–≤–∞–љ–Є—П –±–Њ–ї—М–љ–Њ–≥–Њ –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ, –∞ —В–∞–Ї–ґ–µ —З–µ—А–µ–Ј 14 –і–љ–µ–є –Є 16 –љ–µ–і–µ–ї—М –Њ—В –љ–∞—З–∞–ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Ф–ї—П –∞–љ–∞–ї–Є–Ј–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–∞—Б—М –≤–µ–љ–Њ–Ј–љ–∞—П –Ї—А–Њ–≤—М, –≤–Ј—П—В–∞—П –Є–Ј –Ї—Г–±–Є—В–∞–ї—М–љ–Њ–є –≤–µ–љ—Л –љ–∞—В–Њ—Й–∞–Ї –њ–Њ—Б–ї–µ 14–—З–∞—Б–Њ–≤–Њ–≥–Њ –≥–Њ–ї–Њ–і–∞–љ–Є—П.
–Ю—Ж–µ–љ–Ї–∞ –Њ—Б–љ–Њ–≤–љ—Л—Е –Ї—А–Є—В–µ—А–Є–µ–≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –±–Њ–ї—М–љ–Њ–≥–Њ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –≤ –і–µ–љ—М –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П –≤ –Ї–ї–Є–љ–Є–Ї—Г, –≤ –Ї–Њ–љ—Ж–µ —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞ (–љ–∞ 14–16 —Б—Г—В–Ї–Є) –ї–µ—З–µ–љ–Є—П –Є —З–µ—А–µ–Ј 4 –Љ–µ—Б—П—Ж–∞ –Њ—В –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А. –Ю–љ–∞ –≤–Ї–ї—О—З–∞–ї–∞ –≤ —Б–µ–±—П: 1) –≤ –і–µ–љ—М –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П –Њ—Ж–µ–љ–Ї—Г –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є—В–Є—З–µ—Б–Ї–Є—Е –њ—А–Є—Б—В—Г–њ–Њ–≤ –≤ —Б—А–µ–і–љ–µ–Љ –Ј–∞ —Б—Г—В–Ї–Є, –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–Є–µ–Љ–µ –љ–Є—В—А–Њ–≥–ї–Є—Ж–µ—А–Є–љ–∞ (–Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —В–∞–±–ї–µ—В–Њ–Ї –≤ —Б—А–µ–і–љ–µ–Љ –Ј–∞ —Б—Г—В–Ї–Є); 2) –љ–∞ 2–3––Є —Б—Г—В–Ї–Є –Њ—В –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П, –∞ —В–∞–Ї–ґ–µ —З–µ—А–µ–Ј 4 –Љ–µ—Б—П—Ж–∞ –Њ—В –љ–∞—З–∞–ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М —Б—Г—В–Њ—З–љ–Њ–µ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є–µ –≠–Ъ–У –њ–Њ –•–Њ–ї—В–µ—А—Г, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–Љ –Њ–њ—А–µ–і–µ–ї—П–ї–Њ—Б—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М (–≤ –Љ–Є–љ—Г—В–∞—Е) –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Б–µ–≥–Љ–µ–љ—В–∞ ST. –°–њ—Г—Б—В—П 14 –і–љ–µ–є –Є 4 –Љ–µ—Б—П—Ж–∞ —В–µ—А–∞–њ–Є–Є –Њ—Ж–µ–љ–Є–≤–∞–ї–Њ—Б—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є —Г –±–Њ–ї—М–љ—Л—Е –Э–°, –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –њ—А–Є–µ–Љ–µ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –љ–Є—В—А–∞—В–Њ–≤ –Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–Њ–≤—В–Њ—А–љ—Л—Е –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є, —Б–Љ–µ—А—В–µ–ї—М–љ—Л–µ –Є—Б—Е–Њ–і—Л, –љ–∞–ї–Є—З–Є–µ –Ї–∞–Ї–Є—Е––ї–Є–±–Њ —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—В–Є–≤–љ—Л—Е –Њ–њ–µ—А–∞—Ж–Є–є –љ–∞ –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е —Б–Њ—Б—Г–і–∞—Е.
–Ъ—А–Њ–Љ–µ –≤—Л—И–µ–њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ–Њ–≥–Њ, –і–ї—П –Њ—Ж–µ–љ–Ї–Є –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞ –Ї–∞–ґ–і–Њ–Љ –≤–Є–Ј–Є—В–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –∞–љ–Ї–µ—В–Є—А–Њ–≤–∞–љ–Є–µ —Б –њ–Њ–Љ–Њ—Й—М—О –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є SF–36.
–Т—Л–і–µ–ї–µ–љ–љ—Л–µ –≥—А—Г–њ–њ—Л –±–Њ–ї—М–љ—Л—Е –Э–° —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–µ –Њ—В–ї–Є—З–∞–ї–Є—Б—М –њ–Њ –њ–Њ–ї—Г, –≤–Њ–Ј—А–∞—Б—В—Г, –љ–∞–ї–Є—З–Є—О —В–∞–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞, –Ї–∞–Ї –Ї—Г—А–µ–љ–Є–µ –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П, –љ–∞–ї–Є—З–Є—О —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ—Г —В–µ—З–µ–љ–Є—О —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –і–Њ –Љ–Њ–Љ–µ–љ—В–∞ —А–∞–Ј–≤–Є—В–Є—П –љ–µ—Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є (–њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Є–ї–Є –≤–њ–µ—А–≤—Л–µ –≤–Њ–Ј–љ–Є–Ї—И–µ–≥–Њ –њ—А–Є—Б—В—Г–њ–∞) (—В–∞–±–ї. 1).
–Ю–±—А–∞–±–Њ—В–Ї–∞ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ—А–Є –Њ—Ж–µ–љ–Ї–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –і–∞–љ–љ—Л—Е –Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–≥–Њ –Є –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –Њ–±—Й–µ–њ—А–Є–љ—П—В—Л–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –≤–∞—А–Є–∞—Ж–Є–Њ–љ–љ–Њ–є —Б—В–∞—В–Є—Б—В–Є–Ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ—Л –і–ї—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Њ–±—А–∞–±–Њ—В–Ї–Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Є –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є «Biostat» (Primer of Biostatistics, –Љ.5.0.0.0, S.A.Glantz, McGraw–Hill). –Ф–Њ—Б—В–Њ–≤–µ—А–љ–Њ—Б—В—М —А–∞–Ј–ї–Є—З–Є–є –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –њ–Њ t––Ї—А–Є—В–µ—А–Є—О –°—В—М—О–і–µ–љ—В–∞ –Є–ї–Є –љ–µ–њ–∞—А–∞–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є. –°—А–µ–і–љ–Є–µ –≤–µ–ї–Є—З–Є–љ—Л –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ –≤–Є–і–µ X±m.
–Ъ–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В –Ї–Њ—А—А–µ–ї—П—Ж–Є–Є –≤—Л—Б—З–Є—В—Л–≤–∞–ї–Є –Љ–µ—В–Њ–і–Њ–Љ –Я–Є—А—Б–Њ–љ–∞. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ–Є —Б—З–Є—В–∞–ї–Є —А–∞–Ј–ї–Є—З–Є—П –њ—А–Є –Ј–љ–∞—З–µ–љ–Є—П—Е p<0,05.
–С—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л —Б–ї–µ–і—Г—О—Й–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л. –Э–∞ –Љ–Њ–Љ–µ–љ—В –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А —Б—А–µ–і–љ–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –≤ –љ–µ–і–µ–ї—О –Є –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –љ–Є—В—А–Њ–≥–ї–Є—Ж–µ—А–Є–љ–µ –≤ —В–∞–±–ї–µ—В–Ї–∞—Е –≤ –≥—А—Г–њ–њ–µ 1 (–њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Є–Р–Я–§) —Б–Њ—Б—В–∞–≤–Є–ї–Є 6,543±0,66 –њ—А–Є—Б—В—Г–њ–Њ–≤ –Є 4,514±0,629 —В–∞–±–ї–µ—В–Њ–Ї –≤ –љ–µ–і–µ–ї—О —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —З–µ—А–µ–Ј 14 –і–љ–µ–є – 1,912±0,23 –њ—А–Є—Б—В—Г–њ–∞ –Є 1,176±0,21 —В–∞–±–ї–µ—В–Ї–Є –љ–Є—В—А–Њ–≥–ї–Є—Ж–µ—А–Є–љ–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —З–µ—А–µ–Ј 4 –Љ–µ—Б—П—Ж–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П – 3,46±0,58 –њ—А–Є—Б—В—Г–њ–∞ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –Є 2,87±0,57 —В–∞–±–ї–µ—В–Ї–Є –љ–Є—В—А–Њ–≥–ї–Є—Ж–µ—А–Є–љ–∞ –≤ –љ–µ–і–µ–ї—О —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥—А—Г–њ–њ—Л–2 (–љ–µ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Є–Р–Я–§) —Б—Е–Њ–і–љ—Л —Б –і–Є–љ–∞–Љ–Є–Ї–Њ–є –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ –≥—А—Г–њ–њ–µ–1. –Э–∞ –Љ–Њ–Љ–µ–љ—В –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А —Б—А–µ–і–љ–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –≤ –љ–µ–і–µ–ї—О –Є –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –љ–Є—В—А–Њ–≥–ї–Є—Ж–µ—А–Є–љ–µ –≤ —В–∞–±–ї–µ—В–Ї–∞—Е —Б–Њ—Б—В–∞–≤–Є–ї–Є 7±1,085 –њ—А–Є—Б—В—Г–њ–Њ–≤ –Є 4,438±1,092 —В–∞–±–ї–µ—В–Ї–Є –≤ –љ–µ–і–µ–ї—О —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —З–µ—А–µ–Ј 14 –і–љ–µ–є – 2,17±0,62 –њ—А–Є—Б—В—Г–њ–∞ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –Є 1,5±0,66 —В–∞–±–ї–µ—В–Ї–Є –љ–Є—В—А–Њ–≥–ї–Є—Ж–µ—А–Є–љ–∞ –≤ –љ–µ–і–µ–ї—О, —З–µ—А–µ–Ј 4 –Љ–µ—Б—П—Ж–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П – 3,97±1,03 –њ—А–Є—Б—В—Г–њ–∞ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –≤ –љ–µ–і–µ–ї—О –Є 2,43±0,78 —В–∞–±–ї–µ—В–Ї–Є –љ–Є—В—А–Њ–≥–ї–Є—Ж–µ—А–Є–љ–∞ –≤ –љ–µ–і–µ–ї—О. –Ф–∞–љ–љ—Л–µ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –љ–∞ —А–Є—Б—Г–љ–Ї–∞—Е 1 –Є 2. –Т–µ—А–Њ—П—В–љ–µ–µ –≤—Б–µ–≥–Њ, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –Є –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є –≤ –њ—А–Є–µ–Љ–µ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –љ–Є—В—А–∞—В–Њ–≤ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–µ–є —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ј–∞ 2 –љ–µ–і–µ–ї–Є –ї–µ—З–µ–љ–Є—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ, –Њ–і–љ–∞–Ї–Њ –њ—А–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –Є –њ—Б–Є—Е–Њ—Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –љ–∞–≥—А—Г–Ј–Њ–Ї –≤–љ–µ —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞ (—З–µ—А–µ–Ј 4 –Љ–µ—Б—П—Ж–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П) –≤—Л—И–µ—Г–Ї–∞–Ј–∞–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≤–љ–Њ–≤—М –≤–Њ–Ј—А–∞—Б—В–∞–ї–Є, –Њ—Б—В–∞–≤–∞—П—Б—М –љ–Є–ґ–µ –Є—Б—Е–Њ–і–љ—Л—Е –Ј–љ–∞—З–µ–љ–Є–є.
–Ш–Ј –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е –≤–Є–і–љ–Њ, —З—В–Њ –≥—А—Г–њ–њ–∞ 1 –Є –≥—А—Г–њ–њ–∞ 2 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–° –≤ –Љ–Њ–Љ–µ–љ—В –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Є —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л –њ–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –Є –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є –≤ –њ—А–Є–µ–Љ–µ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–Є—В—А–Њ–≥–ї–Є—Ж–µ—А–Є–љ–∞ –і–ї—П –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є (—А–Є—Б. 1 –Є 2).
–Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤—Б–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –≤ –њ–µ—А–≤—Л–µ –і–љ–Є –Њ—В –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П –Є —З–µ—А–µ–Ј 4 –Љ–µ—Б—П—Ж–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П (±5 –і–љ–µ–є) –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М —Б—Г—В–Њ—З–љ–Њ–µ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є–µ –≠–Ъ–У –њ–Њ –•–Њ–ї—В–µ—А—Г. –°—А–µ–і–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є—И–µ–Љ–Є–Є –і–ї—П –≥—А—Г–њ–њ—Л–1 –Є –≥—А—Г–њ–њ—Л–2 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –љ–∞—З–∞–ї–µ –Є –≤ –Ї–Њ–љ—Ж–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ –Њ—В–ї–Є—З–∞–ї–Є—Б—М (—А>0,05). –Ю—В—Б—Г—В—Б—В–≤–Є–µ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ—Б—В–Є, —Б–Ї–Њ—А–µ–µ –≤—Б–µ–≥–Њ, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –±–Њ–ї—М—И–Є–Љ —Б—В–∞–љ–і–∞—А—В–љ—Л–Љ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є–µ–Љ –≤ –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–∞—Е.
–Ф–∞–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–і–Њ—А–Њ–≤—М—П –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є SF–36 –≤ –і–Є–љ–∞–Љ–Є–Ї–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ —В–∞–Ї–ґ–µ –Є–Љ–µ–ї–Є —Б—Е–Њ–і–љ—Г—О –Ї–∞—А—В–Є–љ—Г, –Є–Љ–µ—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–µ –Ј–љ–∞—З–µ–љ–Є—П –±–∞–ї–ї–Њ–≤ —З–µ—А–µ–Ј 2 –љ–µ–і–µ–ї–Є –ї–µ—З–µ–љ–Є—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ, —З—В–Њ –≥–Њ–≤–Њ—А–Є—В –Њ–± —Г–ї—Г—З—И–µ–љ–Є–Є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–і–Њ—А–Њ–≤—М—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –†–∞–Ј–ї–Є—З–Є—П –Ї–∞–Ї –≤–љ—Г—В—А–Є, —В–∞–Ї –Є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –љ–µ–і–Њ—Б—В–Њ–≤–µ—А–љ—Л. –Ф–Є–љ–∞–Љ–Є–Ї–∞ –Њ–±—Й–Є—Е –±–∞–ї–ї–Њ–≤ —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–і–Њ—А–Њ–≤—М—П –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –љ–∞ —А–Є—Б—Г–љ–Ї–∞—Е 3 –Є 4.
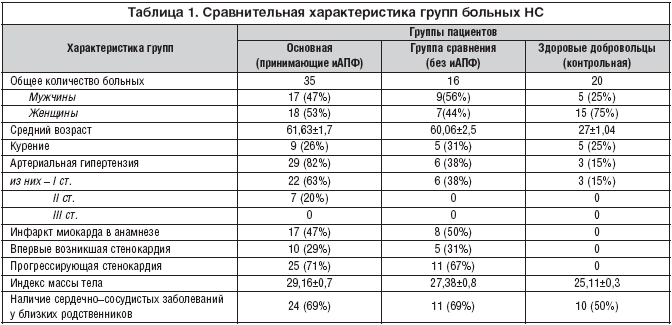
–Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П –і–Є–љ–∞–Љ–Є–Ї–Є —Г—А–Њ–≤–љ—П –°–†–С –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е —В–∞–Ї–ґ–µ –љ–µ–і–Њ—Б—В–Њ–≤–µ—А–љ—Л, –Њ–і–љ–∞–Ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ —Г—А–Њ–≤–љ—П –°–†–С –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ (—А–Є—Б. 5).
–Э–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ—Е 4–—Е –Љ–µ—Б—П—Ж–µ–≤ –љ–∞–±–ї—О–і–µ–љ–Є—П —Г—А–Њ–≤–µ–љ—М –°–†–С –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –±—Л–ї –≤—Л—И–µ 1 –Љ–≥/–ї, —З—В–Њ, –њ–Њ –ї–Є—В–µ—А–∞—В—Г—А–љ—Л–Љ –і–∞–љ–љ—Л–Љ, —П–≤–ї—П–µ—В—Б—П –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ –Њ—В–Љ–µ—З–∞–µ—В—Б—П –Њ—В—З–µ—В–ї–Є–≤–∞—П, —Е–Њ—В—П –Є –љ–µ –і–Њ—Б—В–Њ–≤–µ—А–љ–∞—П —В–µ–љ–і–µ–љ—Ж–Є—П –Ї —Б–љ–Є–ґ–µ–љ–Є—О —Г—А–Њ–≤–љ—П –°–†–С –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Є–Р–Я–§ (–≥—А—Г–њ–њ–∞ 1).
–Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤ –і–Є–љ–∞–Љ–Є–Ї–µ —В–∞–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –ї–Є–њ–Є–і–Њ–≤ –Ї—А–Њ–≤–Є, –Ї–∞–Ї –Ю–•–°, –•–° –Ы–Я–Э–Я, –•–° –Ы–Я–Т–Я –Є –Ґ–У –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ, –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е –Њ—В–ї–Є—З–Є–є –Ї–∞–Ї –≤–љ—Г—В—А–Є –≥—А—Г–њ–њ, —В–∞–Ї –Є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є —В–∞–Ї–ґ–µ –љ–µ –њ–Њ–ї—Г—З–µ–љ–Њ.
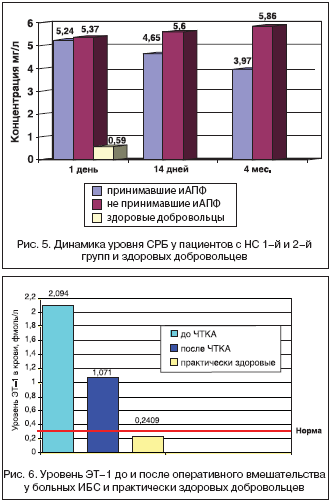
–Т —Б–≤—П–Ј–Є —Б –Љ–∞–ї–Њ—З–Є—Б–ї–µ–љ–љ—Л–Љ–Є –ї–Є—В–µ—А–∞—В—Г—А–љ—Л–Љ–Є –і–∞–љ–љ—Л–Љ–Є –Є «—А–∞–Ј–±—А–Њ—Б–Њ–Љ» –љ–Њ—А–Љ —Г—А–Њ–≤–љ—П –≠–Ґ–1, –њ—А–Є–љ—П—В—Л—Е –і–ї—П —А–∞–Ј–ї–Є—З–љ—Л—Е –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –љ–∞–±–Њ—А–Њ–≤ –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –Ј–љ–∞—З–µ–љ–Є–є –≠–Ґ–1, –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –љ–Њ—А–Љ—Л –љ–∞–Љ–Є –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≥—А—Г–њ–њ—Л –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤, –∞ —В–∞–Ї–ґ–µ –≥—А—Г–њ–њ—Л –±–Њ–ї—М–љ—Л—Е –Ш–С–° —Б –љ–∞–ї–Є—З–Є–µ–Љ –і–Њ–Ї–∞–Ј–∞–љ–љ—Л—Е –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е —Б—В–µ–љ–Њ–Ј–Њ–≤ –њ–Њ –і–∞–љ–љ—Л–Љ –Ї–Њ—А–Њ–љ–∞—А–Њ–∞–љ–≥–Є–Њ–≥—А–∞—Д–Є–Є –Є –њ—А–Њ–≤–µ–і–µ–љ–Є–µ–Љ –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ —Б—В–µ–љ—В–Є—А–Њ–≤–∞–љ–Є—П –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –∞—А—В–µ—А–Є–є. –£—А–Њ–≤–µ–љ—М –≠–Ґ–1 –≤ –Ї—А–Њ–≤–Є –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –Ј–і–Њ—А–Њ–≤—Л—Е —Б–Њ—Б—В–∞–≤–Є–ї 0,2409 —Д–Љ–Њ–ї—М/–Љ–ї, –∞ –≤ –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–µ—А–µ–љ–µ—Б—И–Є—Е —З—А–µ—Б–Ї–Њ–ґ–љ—Г—О —В—А–∞–љ—Б–ї—О–Љ–Є–љ–∞–ї—М–љ—Г—О –Ї–Њ—А–Њ–љ–∞—А–љ—Г—О –∞–љ–≥–Є–Њ–њ–ї–∞—Б—В–Є–Ї—Г (–І–Ґ–Ъ–Р), –≤ —Б—А–µ–і–љ–µ–Љ 2,094 –Є 1,071 —Д–Љ–Њ–ї—М/–Љ–ї —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –і–Њ –Є –њ–Њ—Б–ї–µ —Б—В–µ–љ—В–Є—А–Њ–≤–∞–љ–Є—П –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –∞—А—В–µ—А–Є–є, —З—В–Њ –±—Л–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ –≤–µ—А—Е–љ–µ–є –≥—А–∞–љ–Є—Ж—Л –љ–Њ—А–Љ—Л –Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤ –≥—А—Г–њ–њ–µ –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ (—А–Є—Б. 6).
–Я–Њ —Г—А–Њ–≤–љ—О –≠–Ґ–1 –љ–∞ –Љ–Њ–Љ–µ–љ—В –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П –Њ–±–µ –≥—А—Г–њ–њ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–° –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –Њ—В–ї–Є—З–∞–ї–Є—Б—М – 0,7755 —Д–Љ–Њ–ї—М/–Љ–ї –і–ї—П –≥—А—Г–њ–њ—Л–1 –Є 0,7737 —Д–Љ–Њ–ї—М/–Љ–ї –і–ї—П –≥—А—Г–њ–њ—Л–2. –І–µ—А–µ–Ј 2 –љ–µ–і–µ–ї–Є –ї–µ—З–µ–љ–Є—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –≠–Ґ–1 –≤ –Ї—А–Њ–≤–Є, –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ –≤ –≥—А—Г–њ–њ–µ–2. –І–µ—А–µ–Ј 4 –Љ–µ—Б—П—Ж–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≠–Ґ–1 –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –≤–Њ–Ј–≤—А–∞—Й–∞–ї–∞—Б—М –Ї –њ–µ—А–≤–Њ–љ–∞—З–∞–ї—М–љ–Њ–є: –≤ –≥—А—Г–њ–њ–µ–1 –і–Њ 0,7464 —Д–Љ–Њ–ї—М/–Љ–ї, –∞ –≤ –≥—А—Г–њ–њ–µ–2 –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —В–µ–љ–і–µ–љ—Ж–Є—П –Ї –µ–≥–Њ –њ–Њ–≤—Л—И–µ–љ–Є—О –і–Њ 0,8787 —Д–Љ–Њ–ї—М/–Љ–ї. –Ф–∞–љ–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –љ–∞ —А–Є—Б—Г–љ–Ї–µ 7.
–Э–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ—Е 4–—Е –Љ–µ—Б—П—Ж–µ–≤ –љ–∞–±–ї—О–і–µ–љ–Є—П —Г—А–Њ–≤–µ–љ—М –≠–Ґ–1 –≤ –Ї—А–Њ–≤–Є –±–Њ–ї—М–љ—Л—Е –Э–° –±—Л–ї –≤—Л—И–µ –≤–µ—А—Е–љ–µ–є –≥—А–∞–љ–Є—Ж—Л –љ–Њ—А–Љ—Л –Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤.
–Э–µ –љ–∞–є–і—П –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –≤ —Г—А–Њ–≤–љ–µ –≠–Ґ–1 –Є –µ–≥–Њ –і–Є–љ–∞–Љ–Є–Ї–µ –≤ —В–µ—З–µ–љ–Є–µ 4 –Љ–µ—Б—П—Ж–µ–≤ –љ–∞–±–ї—О–і–µ–љ–Є—П –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–Њ–є –њ—А–Є–љ–Є–Љ–∞—О—Й–Є—Е –Є –љ–µ –њ—А–Є–љ–Є–Љ–∞—О—Й–Є—Е –Є–Р–Я–§, –±—Л–ї–Њ —А–µ—И–µ–љ–Њ –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞—В—М –і–∞–љ–љ—Л–µ –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–° –њ–Њ —А–∞–Ј–ї–Є—З–Є—П–Љ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ —В–µ—З–µ–љ–Є–Є –Є –Є–Ј—Г—З–Є—В—М –і–Є–љ–∞–Љ–Є–Ї—Г –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤ —Н—В–Є—Е –њ–Њ–і–≥—А—Г–њ–њ–∞—Е.
–Т—Б–µ –±–Њ–ї—М–љ—Л–µ –Э–° –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ 3 –њ–Њ–і–≥—А—Г–њ–њ—Л: «–Р» – –њ–∞—Ж–Є–µ–љ—В—Л —Б–Њ —Б—В–∞–±–Є–ї—М–љ—Л–Љ —В–µ—З–µ–љ–Є–µ–Љ (–±–µ–Ј —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Г–ї—Г—З—И–µ–љ–Є—П –Є–ї–Є —Г—Е—Г–і—И–µ–љ–Є—П) –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤ —В–µ—З–µ–љ–Є–µ –≤—Б–µ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П – 11 —З–µ–ї–Њ–≤–µ–Ї; –њ–Њ–і–≥—А—Г–њ–њ–∞ «–Т» – –њ–∞—Ж–Є–µ–љ—В—Л —Б —Г–ї—Г—З—И–µ–љ–Є–µ–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –Ј–∞ 4 –Љ–µ—Б—П—Ж–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П – 10 —З–µ–ї–Њ–≤–µ–Ї; –њ–Њ–і–≥—А—Г–њ–њ–∞ «–°» – –њ–∞—Ж–Є–µ–љ—В—Л, –Є–Љ–µ–≤—И–Є–µ –њ–Њ–≤—В–Њ—А–љ—Л–µ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–Њ –њ–Њ–≤–Њ–і—Г –Э–° –Є–ї–Є –Ю–Ш–Ь, –Є–ї–Є —Г–Љ–µ—А—И–Є–µ –Њ—В —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –Є–ї–Є –њ–µ—А–µ–љ–µ—Б—И–Є–µ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –љ–∞ –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –∞—А—В–µ—А–Є—П—Е (–І–Ґ–Ъ–Р, –Р–Ъ–®) – 30 —З–µ–ї–Њ–≤–µ–Ї.
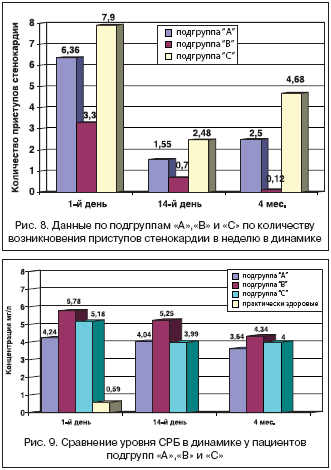
–Я–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –њ–Њ –≤—Б–µ–Љ 3––Љ –њ–Њ–і–≥—А—Г–њ–њ–∞–Љ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ (—А<0,05) –љ–∞–Є–±–Њ–ї—М—И–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –Є–Љ–µ–ї–Є –њ–∞—Ж–Є–µ–љ—В—Л –њ–Њ–і–≥—А—Г–њ–њ—Л «–°» –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ—Е —З–µ—В—Л—А–µ—Е –Љ–µ—Б—П—Ж–µ–≤ –љ–∞–±–ї—О–і–µ–љ–Є—П, —З—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї–Њ —В—П–ґ–µ—Б—В–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П –≤ —Н—В–Є—Е –њ–Њ–і–≥—А—Г–њ–њ–∞—Е (—А–Є—Б. 8).
–Я–Њ—Е–Њ–ґ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –њ–Њ–ї—Г—З–µ–љ–∞ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є –≤ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –љ–Є—В—А–∞—В–∞—Е –і–ї—П –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є.
–Я—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є –Њ–±—Й–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–і–Њ—А–Њ–≤—М—П –≤—Б–µ—Е —В—А–µ—Е –њ–Њ–і–≥—А—Г–њ–њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —В–Њ–ї—М–Ї–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–і–≥—А—Г–њ–њ—Л «–Т» –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —В–µ–љ–і–µ–љ—Ж–Є—П (—А>0,05) –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Њ–±—Й–Є—Е –±–∞–ї–ї–Њ–≤ –≤ —В–µ—З–µ–љ–Є–µ 4 –Љ–µ—Б—П—Ж–µ–≤ –љ–∞–±–ї—О–і–µ–љ–Є—П, —З—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї–Њ –Ї–ї–Є–љ–Є–Ї–µ, —В–Њ–≥–і–∞ –Ї–∞–Ї –≤ –њ–Њ–і–≥—А—Г–њ–њ–∞—Е «–Р» –Є «–°» —З–µ—А–µ–Ј 4 –Љ–µ—Б—П—Ж–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Ї–∞–Ї –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–≥–Њ, —В–∞–Ї –Є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–і–Њ—А–Њ–≤—М—П –≤–Њ–Ј–≤—А–∞—Й–∞–ї–Є—Б—М (—А>0,05) –Ї –Є—Б—Е–Њ–і–љ—Л–Љ (–њ—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є), —З—В–Њ —В–∞–Ї–ґ–µ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ—Г —В–µ—З–µ–љ–Є—О –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤ —Н—В–Є—Е –њ–Њ–і–≥—А—Г–њ–њ–∞—Е.
–Ч–∞ 4 –Љ–µ—Б—П—Ж–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –≤–Њ –≤—Б–µ—Е —В—А–µ—Е –њ–Њ–і–≥—А—Г–њ–њ–∞—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–µ –њ—А–Њ–Є–Ј–Њ—И–ї–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞, —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ –≤ —В–µ—А–∞–њ–Є–Є –≥–Є–њ–Њ–ї–Є–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–Я—А–Є –Њ—Ж–µ–љ–Ї–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –°–†–С –≤—Л—П–≤–ї–µ–љ–∞ –Њ–і–љ–Њ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–∞—П —В–µ–љ–і–µ–љ—Ж–Є—П –≤–Њ –≤—Б–µ—Е –њ–Њ–і–≥—А—Г–њ–њ–∞—Е –Ї —Б–љ–Є–ґ–µ–љ–Є—О —Г—А–Њ–≤–љ—П –°–†–С –≤ —В–µ—З–µ–љ–Є–µ 4–—Е –Љ–µ—Б—П—Ж–µ–≤ –љ–∞–±–ї—О–і–µ–љ–Є—П. –Ф–∞–љ–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –љ–∞ —А–Є—Б—Г–љ–Ї–µ 9.
–†–∞–Ј–ї–Є—З–Є—П –≤–Њ –≤—Б–µ—Е –њ–Њ–і–≥—А—Г–њ–њ–∞—Е —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –љ–µ–і–Њ—Б—В–Њ–≤–µ—А–љ—Л (—А>0,05), –Њ–і–љ–∞–Ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ —Г—А–Њ–≤–љ—П –°–†–С –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ (0,59 –Љ–≥/–ї).
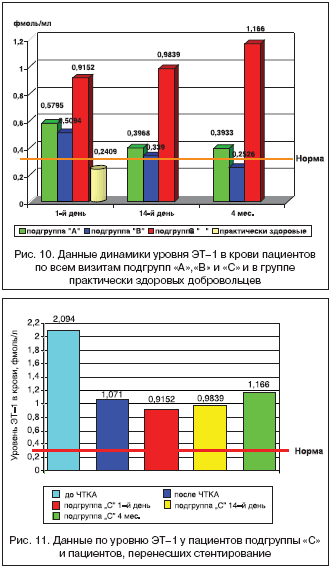
–Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б—А–µ–і–љ–µ–≥–Њ —Г—А–Њ–≤–љ—П –≠–Ґ–1 –≤ –Ї—А–Њ–≤–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–і–≥—А—Г–њ–њ—Л «–°» –≤–Њ –≤—А–µ–Љ—П –≤—Б–µ—Е –≤–Є–Ј–Є—В–Њ–≤ –Њ—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–і–≥—А—Г–њ–њ—Л «–Т», –Њ—В –≥—А—Г–њ–њ—Л –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –Є –≤–µ—А—Е–љ–µ–є –≥—А–∞–љ–Є—Ж—Л –љ–Њ—А–Љ—Л (—А<0,05). –°—В–Њ–Є—В –Њ—В–Љ–µ—В–Є—В—М —В–∞–Ї–ґ–µ, —З—В–Њ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Б—А–µ–і–љ–µ–≥–Њ —Г—А–Њ–≤–љ—П –≠–Ґ–1 –≤ –Ї—А–Њ–≤–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–і–≥—А—Г–њ–њ—Л «–°» –Њ—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–і–≥—А—Г–њ–њ—Л «–Р» –±—Л–ї–Њ –Њ—З–µ–љ—М –±–ї–Є–Ј–Ї–Њ –Ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ—Г –љ–∞ 14––є –і–µ–љ—М –Є —З–µ—А–µ–Ј 4 –Љ–µ—Б—П—Ж–∞ —В–µ—А–∞–њ–Є–Є (—А–Є—Б. 10).
–°—А–µ–і–љ–Є–є —Г—А–Њ–≤–µ–љ—М –≠–Ґ–1 –≤ –Ї—А–Њ–≤–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–і–≥—А—Г–њ–њ—Л «–°» —З–µ—А–µ–Ј 4 –Љ–µ—Б—П—Ж–∞ —В–µ—А–∞–њ–Є–Є –±—Л–ї —Б—Е–Њ–і–µ–љ —Б –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–µ–є –≠–Ґ–1 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Є–Љ–µ–≤—И–Є—Е –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–µ —Б—В–µ–љ–Њ–Ј—Л –њ–Њ –і–∞–љ–љ—Л–Љ –Ї–Њ—А–Њ–љ–∞—А–Њ–∞–љ–≥–Є–Њ–≥—А–∞—Д–Є–Є –Є –њ–µ—А–µ–љ–µ—Б—И–Є—Е –≤–њ–Њ—Б–ї–µ–і—Б—В–≤–Є–Є —Б—В–µ–љ—В–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –∞—А—В–µ—А–Є–є, –Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –љ–µ –Њ—В–ї–Є—З–∞–ї—Б—П –Њ—В –љ–µ–≥–Њ (—А>0,05). –Ф–∞–љ–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –љ–∞ —А–Є—Б—Г–љ–Ї–µ 11.
–£ –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–° –±—Л–ї–∞ –≤—Л—П–≤–ї–µ–љ–∞ –њ—А—П–Љ–∞—П –Ї–Њ—А—А–µ–ї—П—Ж–Є—П –Љ–µ–ґ–і—Г –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –Є —Г—А–Њ–≤–љ–µ–Љ –≠–Ґ–1 –≤ –Ї—А–Њ–≤–Є: —Б—А–µ–і–љ–µ–є —Б–Є–ї—Л (r=0,52) –њ—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А –Є –≤—Л—Б–Њ–Ї–Њ–є —Б–Є–ї—Л (r=0,71) —З–µ—А–µ–Ј 4 –Љ–µ—Б—П—Ж–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П. –Я—А–Є —Н—В–Њ–Љ –Ї–Њ—А—А–µ–ї—П—Ж–Є—П –Љ–µ–ґ–і—Г –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–µ–є –°–†–С –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –±—Л–ї–∞ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є (r=0,24), —З—В–Њ –≥–Њ–≤–Њ—А–Є—В –Њ —В–Њ–Љ, —З—В–Њ —Г—А–Њ–≤–µ–љ—М –≠–Ґ–1 –±–Њ–ї–µ–µ —В–Њ—З–љ–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ –Э–°.
–Ф–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ —Г—А–Њ–≤–µ–љ—М –≠–Ґ–1 –≤ –Ї—А–Њ–≤–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–° —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –≤–∞–ґ–љ–µ–є—И–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є —Н–љ–і–Њ—В–µ–ї–Є—П, –∞ —В–∞–Ї–ґ–µ –Њ–і–љ–Є–Љ –Є–Ј –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –њ—А–Њ–≥–љ–Њ–Ј–∞ —В–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Г —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –£—Е—Г–і—И–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ—Л–Љ –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —Г—А–Њ–≤–љ—П –≠–Ґ–1. –Ю—В—Б—Г—В—Б—В–≤–Є–µ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≠–Ґ–1 —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Є–Р–Я–§ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї (–Ф–Є—А–Њ—В–Њ–љ), —Б–Ї–Њ—А–µ–µ –≤—Б–µ–≥–Њ, —Б–≤—П–Ј–∞–љ–Њ —Б –±–Њ–ї–µ–µ —В—П–ґ–µ–ї—Л–Љ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Ї–Њ–љ—В–Є–љ–≥–µ–љ—В–Њ–Љ –±–Њ–ї—М–љ—Л—Е – –њ–Њ—З—В–Є 2/3 –≤–Њ—И–µ–і—И–Є—Е –≤ —Н—В—Г –≥—А—Г–њ–њ—Г –Є–Љ–µ–ї–Є –±–Њ–ї–µ–µ —В—П–ґ–µ–ї–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ —В–µ—З–µ–љ–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –≤—Л—А–∞–ґ–∞–≤—И–µ–µ—Б—П –≤ –±–Њ’–ї—М—И–µ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –Є –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є –≤ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –љ–Є—В—А–∞—В–∞—Е –і–ї—П –Є—Е –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П, –љ–∞–ї–Є—З–Є—О –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–є –Є—И–µ–Љ–Є–Є –њ–Њ –і–∞–љ–љ—Л–Љ —Б—Г—В–Њ—З–љ–Њ–≥–Њ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—П –≠–Ъ–У –Є —В.–і. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–є –Ї–Њ–љ—В–Є–љ–≥–µ–љ—В –±–Њ–ї—М–љ—Л—Е –Э–° –≤ –≥—А—Г–њ–њ–µ –љ–µ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Є–Р–Я–§ —Б–Њ—Б—В–∞–≤–Є–ї –Љ–µ–љ–µ–µ 1/2. –£—З–Є—В—Л–≤–∞—П –≤—Л—И–µ–Є–Ј–ї–Њ–ґ–µ–љ–љ–Њ–µ, –Љ–Њ–ґ–љ–Њ —Б–і–µ–ї–∞—В—М –≤—Л–≤–Њ–і –Њ –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–Љ –Ј–љ–∞—З–µ–љ–Є–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П —Г—А–Њ–≤–љ—П –≠–Ґ–1. –•–Њ—В—П –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –Є–Р–Я–§ –Є —Г–ї—Г—З—И–∞–µ—В—Б—П —Д—Г–љ–Ї—Ж–Є—П —Н–љ–і–Њ—В–µ–ї–Є—П, –Њ–і–љ–∞–Ї–Њ –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –≠–Ґ–1 –і–ї—П –њ—А–Њ–≥–љ–Њ–Ј–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ—А–µ–≤—Л—И–∞–µ—В –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М –µ–≥–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –Є–Р–Я–§.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–Р–Я–§ —Г –±–Њ–ї—М–љ—Л—Е –Э–° –Њ–њ—А–∞–≤–і–∞–љ–Њ –Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г —Б–љ–Є–ґ–∞–µ—В –≠–Ф, —Г–Љ–µ–љ—М—И–∞–µ—В –њ—А–Є–Ј–љ–∞–Ї–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –њ—А–Є–≤–Њ–і–Є—В –Ї —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–є –±–ї—П—И–Ї–Є. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ –≤ —Б–ї—Г—З–∞—П—Е –Њ—В—Б—Г—В—Б—В–≤–Є—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Є –љ–∞—А–∞—Б—В–∞–љ–Є—П —Г—А–Њ–≤–љ—П –≠–Ґ–1 –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –≤–∞–ґ–љ—Л–Љ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —В–∞–Ї—В–Є–Ї–Є –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –≤–µ–і–µ–љ–Є—П —В–∞–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е: –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≠–Ґ–1 –љ–µ –Љ–µ–љ–µ–µ —З–µ–Љ –≤ 2–3 —А–∞–Ј–∞ –Њ—В –≤–µ—А—Е–љ–µ–є –≥—А–∞–љ–Є—Ж—Л –љ–Њ—А–Љ—Л —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є —Б–Ї–Њ—А–µ–є—И–µ–≥–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Ї–Њ—А–Њ–љ–∞—А–Њ–∞–љ–≥–Є–Њ–≥—А–∞—Д–Є–Є –і–ї—П —А–µ—И–µ–љ–Є—П –≤–Њ–њ—А–Њ—Б–∞ –Њ–± –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є.



–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Р—А–Њ–љ–Њ–≤ –Ф.–Ь., –Ц–Є–і–Ї–Њ –Э.–Ш., –Я–µ—А–Њ–≤–∞ –Э.–Т. –Є –і—А. –Т–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Е–Њ–ї–µ—Б—В–µ—А–Є–љ—В—А–∞–љ—Б–њ–Њ—А—В–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –Ї—А–Њ–≤–Є —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М—О –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞. //–Ъ–∞—А–і–Є–Њ–ї–Њ–≥–Є—П. 1995; 35 (11): 39–45.
2. –Р—Б–ї–∞–љ—П–љ –Э.–Ы., –У–∞–љ–µ–ї–Є–љ–∞ –Ш.–Х., –С–∞–±–∞—П–љ –Ы.–Р. –Є –і—А. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б—Г—В–Њ—З–љ—Л—Е —А–Є—В–Љ–Њ–≤ –ї–Є–њ–Є–і–Њ–≤ –Ї—А–Њ–≤–Є –њ—А–Є –Ш–С–°. //–Ы–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–µ –і–µ–ї–Њ. 1984; 7: 387–389.
3. Dwu V.J. Tissue renin–angiotensin system in myocardial hypertrophy and failure. Arch lnten Med 1993,153:937–942.
4. Furchgott R. F., Zawadfki J. V. The obligatory role of the endothelial cells in relaxation of arterial smooth muscle by acetylcholine. Nature 1980:288:373–376.
5. Robert J Kaplan, Francisco Talavera, Richard Salcido, Kelly L Allen, Denise I Campagnolo, Barrow Neurological Institute, St Joseph’s Hospital; Vascular Diseases and Rehabilitation–Vascular Medicine, 2006, 1: 3–7.












