1. Проведение общепопуляционных скрининговых программ, в т.ч. реализуемых благодаря организации в учреждениях первичного звена здравоохранения «центров здоровья», позволяющих проводить выявление и повышать осведомленность пациентов о наличии у них основных факторов риска (ФР) развития ССЗ (повышенное АД, уровень холестерина и глюкозы крови, ожирение, нарушения функции внешнего дыхания) (рис. 1).
2. Создание национальных и международных регистров для уточнения распространенности тех или иных форм АГ, в т.ч. завершенный недавно в России регистр резистентной АГ (РЕГАТА–ПРИМА) [7].
3. Пропаганда здорового образа жизни на популяционном уровне позволяет достичь значительных успехов, что мы видим на примере США, где существенное снижение смертности от ишемической болезни сердца достигнуто на 24% за счет рационального питания и снижения уровня холестерина, на 12% – за счет прекращения табакокурения, на 5% – повышения физической активности и на 20% – улучшения контроля уровня АД. Эти популяционные наблюдения согласуются с результатами клинических исследований. По данным исследования TOMHS (Treatment Of Mild Hypertension Study), только модификация образа жизни без лекарственной терапии позволяет снизить АД в среднем на 9,1/8,6 мм рт.ст. [8]. Эта стратегия весьма актуальна и для нашей страны, поскольку, по данным Росстата, распространенность потенциально модифицируемых ФР развития основных неинфекционных заболеваний крайне высока. Так, гиперхолестеринемия встречается у 50% населения, ожирение – у 25%, низкая физическая активность – у 40%, избыточное потребление соли – у 50%, недостаточное потребление фруктов и овощей – у 75%, курение – у 39,1% [9].
4. Разработка стратегий диагностики, лечения и профилактики АГ и ее осложнений, что находит свое отражение в систематическом обновлении международных и национальных рекомендаций, в т.ч. Европейского общества кардиологов 2009 г. [10], Российского медицинского общества по артериальной гипертонии и Всероссийского научного общества кардиологов 2010 г. [11]. Основными достижениями в этой области стали:
• внедрение в течение последних 10–15 лет четких пороговых значений уровня АД, позволяющих диагностировать АГ и ее степени, а также описание диагностических критериев специфических нарушений регуляции АД, таких как изолированная систолическая АГ, изолированная клиническая АГ (гипертония «белого халата»), изолированная амбулаторная АГ («маскированная» АГ). Это позволяет практически безошибочно выделять группы лиц с более высоким, чем общепопуляционный, уровнем сердечно-сосудистого риска;
• разработка принципов, показаний и ограничений к использованию методик контроля АД, предоставляющих дополнительную к рутинному офисному измерению АД информацию, существенным способом повышающих информированность о наличии АГ и эффективности проводимой АГТ. К таким методам следует отнести суточное мониторирование и самоконтроль АД, апланационную тонометрию сонной и лучевой артерии для определения центрального АД, позволяющую исключать наличие «псевдогипертонии», оценку внутривизитной и межвизитной вариабельности АД, на которой основано выявление эпизодической АГ [12];
• разработка методик генетического анализа у больных АГ, позволяющих оценивать генетическую предрасположенность к АГ, эффективности и переносимости конкретных антигипертензивных препаратов (АГП), обнаруживать редкие формы наследственной АГ;
• описание целевых цифр АД, темпов снижения АД при проведении АГТ и нижнего уровня безопасного снижения АД. Отечественные рекомендации указывают на необходимость достижения уровня 130–139/80–89 мм рт.ст. у всех пациентов с АГ при условии хорошей переносимости снижения АД [11]. Указаны и конкретные сроки снижения АД. Так, АД у пациентов с высоким и очень высоким риском развития сердечно-сосудистых осложнений должно быть снижено до уровня 140/90 мм рт.ст. в течение 4 нед. Эти рекомендации базируются на результатах исследования VALUE, в котором было показано, что быстрое достижение целевых цифр АД в течение 1 мес. у ранее нелеченных больных позволяет достоверно улучшить прогноз в отношении большинства сердечно-сосудистых осложнений: снижение комбинированного показателя сердечных событий – на 12%, инсульта – на 17%, летальных исходов – на 10% по сравнению с пациентами с более медленным ответом на АГТ [13]. При плохой переносимости снижения АД его темпы могут быть замедлены. Рекомендуется снижение на 10–15% от исходного уровня АД в течение 2–4 нед. Чрезвычайно важным для понимания тактики АГТ является и внедрение нижнего порога безопасного снижения АД, который составляет 110–115 и 70–75 мм рт.ст.;
• создание алгоритма АГТ, базирующегося на учете уровня риска развития сердечно-сосудистых осложнений, а также выделение особых показаний для выбора тех или иных АГП и их комбинаций.
5. Создание национальных и региональных специализированных центров по лечению АГ и внедрение новых высокотехнологичных методов лечения АГ и модификации сопутствующих сердечно-сосудистых ФР, что особенно актуально при резистентной АГ. К подобным методам следует отнести медикаментозное и оперативное лечение ожирения, применение CPAP-терапии (Continuous Positive Airways Pressure) при синдроме обструктивного апноэ, радиочастотной денервации почечных артерий, имлантации стимулятора каротидных барорецепторов при резистентной АГ и т.д.
6. Обучение врачей и пациентов технологии диагностики, лечения и профилактики АГ и ее осложнений является основополагающим принципом лечения в современных условиях, который позволяет повысить приверженность терапии (рис. 1).
Несмотря на существенные достижения в области организации лечения больных АГ, реальная клиническая практика зачастую сталкивается с недостаточной приверженностью врачей рекомендациям и пациентов – лечению. Долгосрочная приверженность лечению при АГ не превышает 50% [14]. При этом в 25% случаев пациенты самостоятельно прекращают АГТ в течение первых 6 мес. лечения. Проблема низкой приверженности пациента лечению складывается из комплекса его личных особенностей и степени выполнения врачом существующих рекомендаций по проведению АГТ (табл. 1). Большое влияние на приверженность больного имеют особенности заболевания и его влияние на качество жизни пациента. В межкризовый период и до появления сердечно-сосудистых осложнений АГ практически не нарушает качество жизни, что не способствует формированию высокой приверженности терапии.
Сегодня в арсенале врача имеется пять классов препаратов с равной антигипертензивной эффективностью, рекомендуемых в качестве средств первого ряда: ингибиторы ангиотензинпревращающего фермента (иАПФ), блокаторы рецепторов к ангиотензину II 1-го типа (БРА), антагонисты кальция, β-адреноблокаторы, тиазидные диуретики [10, 11]. Помимо этого существуют три дополнительных класса для комбинированной терапии: α-адреноблокаторы, агонисты имидазолиновых рецепторов и прямые ингибиторы ренина.
Еще одной детерминантой повышения приверженности и эффективности АТГ является своевременное назначение комбинированной терапии. Согласно Российским рекомендациям 2010 г. [11], монотерапия показана для лечения только пациентов с низким и умеренным сердечно-сосудистым риском. В исследовании ПРЕМИЯ, в котором участвовали 2200 пациентов с АГ, была изучена распространенность сердечно-сосудистых ФР и поражений органов-мишеней, которые используются для оценки уровня риска. Частота ожирения в обследованной группе больных АГ составила 70,9%, гиперхолестеринемии – 67,1%, гипергликемии – 17,2%, отягощенного семейного анамнеза – 18,3%, гипертрофии левого желудочка – 33%, поражения сосудов – 4,3%, нарушения функции почек – 1% [15]. Эти результаты свидетельствуют о невысокой распространенности в российской популяции больных АГ лиц с низким и умеренным сердечно-сосудистым риском, а соответственно, о высокой потребности в комбинированной АГТ. Действительно, по данным проф. Ю.А. Карпова и соавт., частота использования комбинированной АГТ в России составляет 75% [16].
При неэффективности АГТ тактика ведения пациентов с низким и умеренным риском предусматривает переход с низкодозированной терапии на высокодозированную, что повышает вероятность развития дозозависимых побочных реакций и, соответственно, снижения приверженности АГТ. В метаанализе 190 исследований, в которых проводилось лечение АГ в режиме монотерапии, было показано, что прекращение приема АГП вследствие побочных эффектов наблюдалось у 6,7% пациентов на фоне приема АК и у 3,1% – на фоне приема как диуретиков, так и БРА [17].
Альтернативой переходу на высокодозированную монотерапию является перевод пациента на низкодозированную комбинацию АГП. Однако длительный поиск оптимальной схемы АГТ чреват существенными проблемами. Во-первых, снижением протективной эффективности АГТ, которая реализуется, как было описано выше, при быстром достижении целевого АД. Во-вторых, частая смена схемы АГТ сопровождается снижением приверженности пациента терапии и доверия врачу. Эти соображения позволяют предположить необходимость более частого применения комбинированной АГТ как стартовой терапии, в т.ч. у лиц с низким и умеренным сердечно-сосудистым риском.
Сложность достижения целевого АД при проведении монотерапии доказана результатами многих исследований. Так, в исследовании HOT комбинированная АГТ потребовалась в 63% случаев при целевом ДАД <90 мм рт.ст., в 68% – при целевом ДАД <85 мм рт.ст. и в 74% – при целевом ДАД <80 мм рт.ст. [18]. Частота назначения комбинированной АГТ в исследовании SHEP составила 45%, ALLHAT – 62%, STOP–Hypertension – 66%, INVEST – 84%, LIFE – 92%, COOPE – 93%.
Комбинированная АГТ имеет большие преимущества перед монотерапией:
1. Усиление антигипертензивного действия за счет взаимного потенцирования эффектов каждого из препаратов, входящих в комбинацию. Этот так называемый аддитивный эффект связан с подавлением разных механизмов, участвующих в повышении АД, а также с устранением контррегуляторных механизмов, уменьшающих эффективность АГП. Назначение комбинированной АГТ повышает в 2 раза вероятность ответа на лечение.
2. Уменьшение частоты побочных эффектов обусловлено как возможностью использовать при комбинированной АГТ препараты в меньших дозах, что снижает вероятность развития дозозависимых побочных реакций, так и взаимной нейтрализацией побочных эффектов отдельных препаратов при использовании рациональных комбинаций.
3. Более эффективная защита органов-мишеней АГ и, соответственно, более выраженное снижение риска развития сердечно-сосудистых осложнений.
4. Повышение приверженности пациента лечению за счет повышения эффективности и темпов достижения целевого АД.
К наиболее рациональным относятся комбинации иАПФ с тиазидным диуретиком, иАПФ с антагонистом кальция, БРА с тиазидным диуретиком, БРА с антагонистом кальция, дигидропиридинового антагониста кальция с β-адреноблокатором и антагониста кальция с тиазидным диуретиком [11]. Помимо этого к рациональным комбинациям относится и сочетание β-адреноблокаторов небиволола, бисопролола, метопролола сукцината или карведилола с низкими дозами гидрохлоротиазида (не более 6,25 мг/сут.) или индапамида. Однако комбинаций β-адреноблокаторов с диуретиками следует избегать при лечении пациентов с метаболическим синдромом или сахарным диабетом (СД).
По данным опроса врачей, проведенного в ходе исследования ПИФАГОР III, сочетание иАПФ и диуретика используется в 90% случаев, β-адреноблокатора и диуретика – в 52%, антагониста кальция и β-адреноблокатора или иАПФ – в 50% [19].
Популярность сочетания иАПФ с диуретиками связана с тем, что она отвечает всем требованиям, предъявляемым с комбинированной АГТ. Прежде всего, эта комбинация оправданна с патогенетической точки зрения, поскольку иАПФ и диуретик действуют синергично и эффективность этой пары выше, чем у каждого из препаратов по отдельности. Антигипертензивный эффект диуретиков заключается в уменьшении объема циркулирующей крови, что в свою очередь вызывает компенсаторную активацию ренин-ангиотензин-альдостероновой системы (РААС), которая играет роль контррегуляторного фактора, снижающего эффективность диуретиков. Добавление иАПФ позволяет преодолеть активацию РААС и таким образом усиливает эффект диуретиков. Применение комбинации иАПФ и диуретика позволяет устранить побочные эффекты обоих препаратов. Диуретики вызывают повышение экскреции калия, тогда как иАПФ – задержку, в результате чего комбинация предотвращает развитие и индуцированной диуретиками гипокалиемии, и возможной на фоне иАПФ гиперкалиемии. Для тиазидных диуретиков характерно развитие гиперурикемии, в то время как иАПФ способствуют ее уменьшению вследствие усиления кровотока в кортикальном слое почек и повышения экскреции мочевой кислоты. Существенным недостатком тиазидных диуретиков является их неблагоприятное влияние на углеводный и липидный обмен, обусловленный стимуляцией инсулинорезистентности, однако их сочетание с иАПФ позволяет ослабить эти нежелательные эффекты.
Влияние АГП на углеводный обмен и риск развития СД 2 типа изучались во многих исследованиях. Так, в исследовании ALLHAT риск развития новых случаев СД оценивался через 2 и 4 года наблюдения. При этом в группе, получавшей тиазидный диуретик хлорталидон, частота возникновения СД была выше на 65% через 2 года и на 43% – через 4 года, чем в группе лизиноприла, и соответственно на 30 и 18% выше по сравнению с группой амлодипина [20]. В метаанализе 22 рандомизированных клинических исследований, включавших 143 153 пациента, была проведена оценка влияния различных классов АГП на возникновение СД у больных АГ [21]. В качестве референтного агента были выбраны диуретики, для которых отношение шансов (ОШ) возникновения СД было принято за 1. По влиянию на частоту новых случаев СД 2 типа АГП и плацебо оказались в следующем порядке: БРА (ОШ=0,57), иАПФ (ОШ=0,67), антагонисты кальция (ОШ=0,75), плацебо (ОШ=0,77), β–адреноблокаторы (ОШ=0,90). Таким образом, БРА, иАПФ и антагонисты кальция достоверно уменьшают заболеваемость СД по сравнению с плацебо, а диуретики и β-адреноблокаторы – увеличивают.
В связи с этим безусловными преимуществами обладает тиазидоподобный диуретик индапамид, диуретический эффект которого крайне слаб, что способствует его хорошей переносимости. В отличие от других диуретиков индапамид метаболически нейтрален. Он не влияет на липидный обмен, практически не вызывает гипокалиемии, не нарушает метаболизм углеводов [22], поэтому рекомендуется для лечения больных АГ с метаболическим синдромом и/или СД. Важнейшей особенностью индапамида является его кардио- и нефропротективная активность.
В многоцентровом исследовании Left ventricle hypertrophy: Indapamide Versus Enalapril (LIVE) на примере группы из 505 пациентов с мягкой и умеренной АГ и повышенной массой миокарда левого желудочка индапамид в дозе 1,5 мг достоверно эффективнее снижал индекс массы миокарда левого желудочка, чем эналаприл в дозе 20 мг (-6,5 г/м2, р=0,013, против -4,3 г/м2, р=0,049) [23]. Антипротеинурический эффект индапамида с замедленным высвобождением был продемонстрирован в ходе исследования NESTOR, в котором участвовали 570 больных АГ и СД 2 типа. Пациенты были рандомизированы в группы, принимающие индапамид ретард в дозе 1,5 мг/сут. или эналаприл в дозе 10 мг/сут. Снижение уровня экскреции альбумина в группе эналаприла достигло 37%, а в группе индапамида – 45% [24]. В исследовании X-CELLENT при сопоставлении эффектов индапамида замедленного высвобождения с амлодипином и кандесартаном у пациентов с изолированной систолической гипертензией были выявлены преимущества индапамида в отношении его влияния на пульсовое давление [25].
Важным компонентом антигипертензивного профиля индапамида является его эффективность при изолированной систолической АГ, в т.ч. у лиц пожилого и старческого возраста, что было продемонстрировано результатами исследования HYVET, в котором приняли участие 3845 больных, 60,5% из которых составили женщины в возрасте 83,5±3,1 года. Результаты данного исследования показали, что АГТ, базирующаяся на индапамиде ретард, приводит к выраженному снижению систолического АД (САД) на 29,5 мм рт.ст. и диастолического АД (ДАД) на 12,9 мм рт. ст. Через 2 года наблюдения в группе индапамида ретард было достигнуто достоверное снижение на 30% частоты всех случаев инсультов, на 39% – фатальных инсультов и на 64% – случаев сердечной недостаточности [26].
Результаты эпидемиологического исследования ПИФАГОР III показали, что эналаприл и индапамид являются наиболее часто используемыми в России иАПФ и диуретиком [19], на долю которых приходится 21% назначений иАПФ и 33% – диуретиков.
С учетом этого комбинация эналаприла и индапамида была выбрана для использования в отечественном исследовании ЭПИГРАФ [28], в которое были включены 550 больных со средним возрастом 55,3±0,4 года и примерно одинаковым количеством мужчин и женщин (42 и 58% соответственно). Исходное АД составляло в среднем 174,1 и 100,6 мм рт.ст., АГ II степени регистрировалась у 82%, III степени – у 18% пациентов. В течение двухнедельного вводного периода был запрещен прием иАПФ и диуретиков, а АД контролировали приемом β–адреноблокаторов или агонистов имидазолиновых рецепторов. Активная терапия проводилась в течение 12 нед., на протяжении которых всем больным назначали индапамид в дозе 2,5 мг/сут. Затем всех участников исследования разделили на три группы по уровню САД: в 1-ой группе (124 пациента) САД 160–170 мм рт.ст., во 2-ой (328 больных) – 170–180 мм рт.ст., в 3-ей (98 больных) > 180 мм рт.ст. Пациенты 1-ой группы получали эналаприл в дозе 5 мг/сут., 2-ой – 10 мг/сут., в 3-ей – 20 мг/сут. У 22% больных целевое АД не было достигнуто, что потребовало повышения дозы эналаприла. В итоге средняя суточная дозировка эналаприла к концу исследования составила 15,2 мг в комбинации с индапамидом в дозе 2,5 мг.
Через 12 нед. терапии САД в целом по группе снизилось до 137,3 мм рт.ст. (р < 0,001), т.е. до целевых цифр АД. Средний уровень ДАД также достиг целевого (83,1±7,4 мм рт.ст., р<0,001). При этом целевое АД было зафиксировано у 70% пациентов. Комбинированная терапия эналаприлом и индапамидом хорошо переносилась: побочные явления выявлены у 45 (8,1%) больных, причем преобладали симптомы, связанные с чрезмерным снижением АД (5,4%), и лишь у 15 (2,7%) пациентов отмечен сухой кашель, вызванный приемом эналаприла.
Таким образом, результатом исследования ЭПИГРАФ стала высокая эффективность комбинации эналаприла с индапамидом, сочетавшаяся с хорошей переносимостью терапии. При этом установлено, что эффективность комбинированной терапии эналаприлом и индапамидом существенно не зависит от пола и возраста, а также от типа АГ (эссенциальная или симптоматическая). Предложенные дозировки эналаприла и индапамида обеспечивали достаточную степень эффективности при АГ различной тяжести.
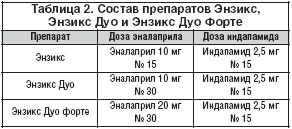
На основании результатов исследования ЭПИГРАФ было предложено создание комбинированного АГП, содержащего эналаприл и индапамид, что и было реализовано. При этом выбор был сделан в пользу нефиксированной комбинации, а комбинации двух препаратов в одном блистере. Достоинства фиксированных комбинаций АГП хорошо известны и продемонстрированы результатами рандомизированных клинических исследований, в т.ч. ACCOMPLISH [29]. Несмотря на это, частота применения фиксированных комбинаций АГП существенно ниже, чем свободных (43 и 69% соответственно) [19]. Это обусловлено рядом факторов, в т.ч. и недостатками фиксированных комбинаций, к которым относятся сложность подбора индивидуальной дозировки препаратов, входящих в комбинацию, трудности при выявлении причины побочного эффекта. В результате для преодоления имеющихся недостатков и создания альтернативы были разработаны препараты Энзикс, которые содержат в одном блистере таблетки индапамида и эналаприла в различных дозировках (табл. 2).
Нефиксированная комбинация АГТ в одном блистере имеет преимущества, поскольку дает возможность титрования дозы эналаприла в различных клинических ситуациях, отмены препарата или уменьшения дозы при развитии нежелательных явлений, повышения дозы для усиления антигипертензивного эффекта путем замены такой же формой препарата с большей дозировкой эналаприла, что не вызывает снижения приверженности лечению [30].
Эффективность и безопасность новой лекарственной формы, включающей нефиксированную комбинацию эналаприла и индапамида в одном блистере (Энзикс), изучалась в рандомизированном сравнительном контролируемом испытании ЭПИГРАФ-2 [31]. В исследовании приняли участие 313 больных АГ I–II степени, которые были рандомизированы в две группы – активного лечения и контроля. В группе активного лечения пациенты с АГ I степени получали Энзикс, при необходимости титрования дозы – Энзикс Дуо, больные АГ II степени – Энзикс Дуо, а при необходимости – Энзикс Дуо форте. В группе контроля проводилась терапия другими классами АГП: β-адреноблокаторами, тиазидными диуретиками, антагонистами кальция, БРА, агонистами имидазолиновых рецепторов. В качестве целевого уровня протоколом исследования предусматривалось снижение АД <140 и 90 мм рт.ст. у всех больных АГ и <130 и 80 мм рт.ст. – у больных АГ и СД. В случае, когда целевые значения АД не были достигнуты через 2, 4 и 6 нед. лечения, проводилось титрование доз АГТ с удвоением их в группе активного лечения и коррекцией – в группе контроля. Общая продолжительность наблюдения составила 14 нед. Оценивались динамика АД по данным офисного измерения и суточного мониторирования АД, протеинурии, качества жизни (по опроснику SF-36), распространенность побочных эффектов и фармакоэкономические показатели.
Пациенты группы активного лечения и контроля достоверно не различались по большинству параметров. Средний возраст составил около 57 лет, 60% пациентов составили мужчины с избыточной массой тела, почти половина больных имели поражения органов-мишеней (прежде всего сердца и почек), 15–19% пациентов до включения в исследование не принимали АГТ, несмотря на установленный диагноз АГ, что отражает уровень приверженности этой группы больных.
В ходе исследования в обеих группах зарегистрировано достоверное снижение АД. Степень снижения САД была достоверно выше в группе активного лечения (–26,1 мм рт. ст.), чем в группе контроля (-20,1 мм рт.ст.), ДАД также достоверно больше снижалось в группе пациентов, получавших Энзикс (-13,2 мм рт.ст. по сравнению с -11,7 мм рт.ст. в группе контроля) (рис. 2).
Частота достижения целевого АД в группе, получавшей Энзикс, через 4 нед. лечения была несколько выше, чем в группе контроля, хотя эта разница не достигала уровня статистической достоверности. Тем не менее, через 14 нед. эти различия были уже достоверны с преимуществом в пользу терапии Энзиксом (рис. 3). Результаты суточного мониторирования АД согласовались с результатами офисного изменения, но кроме снижения АД выявлено достоверное снижение вариабельности АД на 20% в группе активного лечения по сравнению с группой контроля, что сегодня рассматривается в качестве существенного критерия эффективности АГТ, особенно при достижении целевых цифр АД (рис. 3).
Помимо этого в исследовании была выявлена более выраженная нефропротективная активность комбинации эналаприла и индапамида, которая проявилась в снижении частоты протеинурии на 4,6% к 14 нед. лечения Энзиксом, а в подгруппе больных АГ II степени, получавших Энзикс Дуо или Энзикс Дуо форте, – на 10,5%. Немаловажным фактом оказалась и меньшая стоимость лечения пациентов Энзиксом по сравнению с контрольными видами лечения (рис. 4).
Переносимость терапии в обеих группах была хорошей. Досрочное прекращение лечения было зарегистрировано у 11 (5,2 %) пациентов группы активного лечения и 5 (4,9 %) из группы контроля. Из 11 больных основной группы у 3 (1,4%) развился сухой кашель, у 2 (0,9%) отмечалась недостаточная антигипертензивная эффективность, повлекшая за собой отмену препарата, у 1 (0,5%) – головная боль, у 5 (2,4%) поводом для досрочного прекращения участия в исследовании стали причины немедицинского характера.
Многоцентровое рандомизированное исследование ЭПИГРАФ-2 продемонстрировало эффективность и безопасность нефиксированной комбинации эналаприла и индапамида в одном блистере (Энзикс, Энзикс Дуо, Энзикс Дуо форте) при лечении больных АГ I–II степени. Препараты Энзикс обладают нефропротективной активностью, характеризуются хорошей переносимостью и фармакоэкономическими преимуществами перед другими свободными комбинациями АГП.
Таким образом, нефиксированная комбинация эналаприла и индапамида в одном блистере, характеризующаяся доказанной эффективностью, переносимостью и безопасностью, представляет собой еще один путь преодоления проблемы недостаточной эффективности АГТ за счет повышения приверженности терапии. Благодаря своей форме выпуска препарат Энзикс обладает, с одной стороны, преимуществами фиксированных комбинаций, с другой, предлагая разнообразие дозировок (Энзикс, Энзикс Дуо, Энзикс Дуо форте), обеспечивает возможность индивидуализации АГТ на старте лечения и при необходимости – усиления антигипертензивного эффекта. Это способствует ускорению темпов и увеличению частоты достижения целевого АД, а, соответственно, и степени органопротекции и сопровождается экономически выгодными характеристиками, что также оказывает существенное влияние на приверженность пациентов терапии.


![Рис. 2. Динамика систолического АД (по данным офисного измерения) в исследовании ЭПИГРАФ-2 [31]](/data/articles/Image/t21/n12/641-3.gif)
![Рис. 3. Эффективность лечения (процент больных, достигших целевого АД или снижения систолического АД > 20 мм рт.ст) [31]](/data/articles/Image/t21/n12/641-4.gif)
![Рис. 4. Затраты на лечение больных АГ (в расчете на одного пациента в месяц) в группах активного лечения (Энзикс) и контроля [31]](/data/articles/Image/t21/n12/641-5.gif)
Литература
1. www.who.int/mediacentre/factsheets/fs317/en/index.html
2. Шальнова С., Кукушкин С., Маношкина Е., Тимофеева Т. Артериальная гипертензия и приверженность терапии // Врач. 2009. № 12. С. 39–42.
3. www.who.int/gho/ncd/risk_factors/blood_pressure_prevalence_text/en/index.html
4. Шальнова С.А., Баланова Ю.А., Константинов В.В. и др. Артериальная гипертония: распространенность, осведомленность, прием антигипертензивных препаратов и эффективность лечения среди населения Российской Федерации // Рос. кардиол. журнал. 2006. № 4. С. 45–50.
5. Chobanian A.V., Bakris G.L., Black H.R. et al. Seventh report of the joint national committee on prevention, detection, evaluation, and treatment of high blood pressure // Hypertension. 2003. Vol. 42. P.1206–1252.
6. www.cdc.gov/nchs/data_access/Vitalstatsonline.html.
7. Чазова И.Е., Фомин В.В., Разуваева М.А., Вигдорчик А.В. Эпидемическая характеристика резистентной и неконтролируемой артериальной гипертонии РЕГАТА-ПРИМА // Системные гипертензии. 2010. №.3. С.34–41.
8. Neaton J.D., Grimm R.H. Jr, Prineas R.J. et al. Treatment of mild hypertension study. Final results // JAMA. 1993. Vol. 270. P. 713–724.
9. www.gks.ru/free_doc/200/demo/zdr08.htm.
10. Reappraisal of European guidelines on hypertension management: a European society of hypertension task force document // J. Hypertens. 2009. Vol. 27. P. 2121–2158.
11. Чазова И.Е., Ратова Л.Г., Бойцов С.А., Небиеридзе Д.В. Диагностика и лечение артериальной гипертензии (Рекомендации Российского медицинского общества по артериальной гипертонии и Всероссийского научного общества кардиологов) // Системные гипертензии. 2010. № 3. С. 5–26.
12. Rothwell P.M. Limitation of the usual blood pressure hypothesis and importance of variability, instability, and episodic hypertension // Lancet. 2010. Vol. 375(9718). P. 938–948.
13. Weber M.A. et al. Blood pressure dependent and independent effects of antihypertensive treatment on clinical values in the VALUE trial // Lancet. 2004. Vol. 363. P. 2047–2049.
14. Loghman-Adham M. Medication noncompliance in patients with chronic disease: issues in dialysis and renal transplantation // Am. J. Manag. Care. 2003. Vol. 9(2). P. 155–171.
15. Мычка В.Б., Жернакова Ю.В., Чазова И.Е. Улучшенная форма периндоприла – престариум А – в лечении больных артериальной гипертонией в различных клинических ситуациях (ПРЕМИЯ) // Системные гипертензии. 2009. № 4. С. 50–52.
16. Карпов Ю.А., Деев А.Д. от имени врачей участников программы ПРОРЫВ Неконтролируемая артериальная гипертония – новые возможности в решении проблемы повышения эффективности лечения // Кардиология. 2012. Т. 52(2). С. 29–35.
17. Ross S.D., Akhras K.S., Zhang S. et al. Discontinuation of antihypertensive drug due to adverse events: a systematic review and meta-analysis // Pharmacother. 2001. Vol. 21. P. 940–953.
18. Hansson L., Zanchetti A., Carruthers S.G. et al. Effects of intensive blood-pressure lowering and low-dose aspirin in patients with hypertension: principal results of the Hypertension Optimal Treatment (HOT) randomised trial // Lancet. 1998. Vol. 351. P. 1755–1762.
19. Леонова М.В., Белоусов Д.Ю., Штейнберг Л.Л. и др. Анализ врачебной практики проведения антигипертензивной терапии в России (по данным исследования ПАФАГОР III) // Фарматека. 2009. № 12. С. 114–119.
20. ALLHAT Collaborative Research Group. Major outcomes in high-risk hypertensive patients randomized to angiotensinconverting enzyme inhibitor or calcium channel blocker versus diuretic: the Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial (ALLHAT) // JAMA. 2002. Vol. 288. P. 2981–2997.
21. Elliott W.J., Meyer P.M. Incident diabetes in clinical trials of antihypertensive drugs: a network meta-analysis // Lancet. 2007. Vol. 369. P. 201–207.
22. Ambrosioni E., Safar M., Degaute J.P. et al. Low-dose antihypertensive therapy with 1.5 mg sustained-release indapamide: results of randomised double-blind controlled studies European study group // J. Hypertens. 1998. Vol. 16(11). P. 1677–1684.
23. Gosse P., Sheridan D. J., Zannad F. et al. Regression of left ventricular hypertrophy in hypertensive patients treated with indapamide SR 1.5 mg versus enalapril 20 mg: the LIVE study // J. Hypertens. 2000. Vol. 18. P. 1465–1475.
24. Marre M., Puig J. G., Kokot F. еt al. Equivalence of indapamide SR and enalapril on microalbuminuria reduction in hypertensive patients with type 2 diabetes: the NESTOR study // J. Hypertens. 2004. Vol. 22. P. 1613–1622.
25. London G., Asmar R., Schmieder R., Calvo C. Antihypertensive efficacy of Indapamide SR vs candesartan and amlodipine in hypertensive patients in isolated hypertensive patients // Am. J. Hypertens. 2004. Vol. 17(5). P. 183А.
26. Beckett N.S., Peters R., Fletcher A.E., et al. Treatment of hypertension in patients 80 years of age or older // N. Engl. J. Med. 2008. Vol. 358. P. 1887–1898.
27. Chalmers J., Perkovic V., Joshi R., Patel A. ADVANCE: breaking new ground in type 2 diabetes // J. Hypertens. 2006. Vol. 24 (Suppl. 5). S. 22–28.
28. Беленков Ю.Н., Мареев В.Ю. от имени рабочей группы исследования ЭПИГРАФ. Эналаприл Плюс Индапамид в лечении стабильной артериальной Гипертонии: оценка эффективности и безопасности РАциональной комбинированной Фармакотерапии (ЭПИГРАФ). Первые результаты Российского многоцентрового исследования // Сердце. 2003. № 2(4).
29. Jamerson K., Weber MA, Bakris G L, Dahlöf B. et al. For the ACCOMPLISH Trial Investigators. Benazepril plus Amlodipine or Hydrochlorothiazide for Hypertension in High-Risk Patients // N. Engl. J. Med. 2008. Vol. 359. P. 2417–2428.
30. Подзолков В.И., Осадчий К.К. Новый подход к терапии артериальной гипертензии: нефиксированные комбинации в одном блистере // Фарматека. 2008. № 5. С. 20–27.
31. Беленков Ю.Н. и рабочая группа исследования ЭПИГРАФ-2. Эналаприл Плюс Индапамид в лечении АГ: оценка эффективности и безопасности рациональной фармакотерапии. Применение нефиксированной комбинации Эналаприла и Индапамида (Энзикс). Дизайн и основные результаты исследования ЭПИГРАФ-2 // Сердце. 2005. № 4(5). С. 277–286.












