Реальная распространенность ИБС, особенно ее начальных форм, намного больше, чем показывает статистика. Основная причина смерти и инвалидизации во всем мире – это острый инфаркт миокарда (ОИМ), который может как манифестировать ИБС, так и неоднократно возникать у пациентов на фоне уже имеющейся ИБС. Так, по данным American Heart Association, в США ежегодно от ОИМ умирает около трети заболевших, причем порядка половины смертей приходится на первый час от начала заболевания. Неутешительна статистика и чрезвычайно актуальна проблема ОИМ и в Российской Федерации. По данным Московского городского центра патолого–анатомических исследований [Зайратьянц О.В., Ковальский Г.Б., Рыбакова М.Г., 2005], в столице от ОИМ ежегодно умирает примерно 10 тыс. человек.
Принято считать, что ОИМ развивается у женщин на 10–15 лет позже, чем у мужчин. Это может быть обусловлено более поздним развитием коронарного атеросклероза у женщин и меньшим распространением курения среди них по сравнению с мужчинами. После наступления менопаузы ассоциированные с полом различия в заболеваемости и смертности постепенно уменьшаются, а в возрасте старше 70 лет – вообще исчезают. Хорошо известно, что коронарный атеросклероз является хроническим заболеванием со стабильными и нестабильными периодами. Во время последних происходит активация воспалительных процессов в сосудистой стенке, повышается вероятность развития ОИМ.
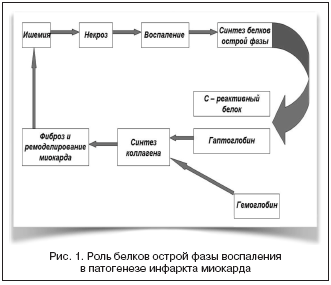
Роль воспаления при ОИМ обсуждается в течение многих лет, а в последние годы с помощью оценки уровней вырабатываемых белков острой фазы воспаления (БОФ), таких как C–реактивный белок (СРБ), гаптоглобин и т.д., подтверждено их участие и в определении прогноза. Выявлены взаимосвязи концентрации ряда БОФ и параметров, характеризующих дисфункцию левого желудочка (ЛЖ), что подтверждает роль воспаления в ремоделировании миокарда у больных с ОИМ [1].
Установлено, что гаптоглобин, связываясь с гемоглобином, стимулирует синтез коллагена в сердечной мышце, участвуя таким образом в деструктивных и репаративных процессах при ОИМ. Уровень гаптоглобина в плазме у больных, перенесших ОИМ, зависит от характера поражения миокарда и наличия осложнений (рис. 1).
Резорбционно–некротический синдром является одним из основных проявлений острого периода ИМ. Он обусловлен резорбцией некротических масс и развитием асептического воспаления в зоне некроза. Важнейшими признаками этого синдрома являются:
• повышение температуры тела;
• лейкоцитоз;
• увеличение СОЭ;
• появление биохимических признаков воспаления;
• появление биохимических маркеров гибели кардиомиоцитов.
При вовлечении в некротический процесс 10% массы миокарда начинает страдать функция сердца, в том числе систолическая – возникают нарушение сократительной функции сердца, десинхрония (замедление сокращения по сравнению со здоровым миокардом), диастолическая – отмечаются снижение эластичности и растяжимости миокарда и ремоделирование ЛЖ – растяжение миокарда в области некроза. В исходе этих нарушений развиваются острая сердечная недостаточность и кардиогенный шок, что приводит к полиорганной недостаточности и смерти.
СРБ получил свое название из–за способности вступать в реакцию преципитации с С–полисахаридом пневмококков (один из механизмов ранней защиты организма от инфекции). СРБ стимулирует иммунные реакции, в том числе фагоцитоз, участвует во взаимодействии Т– и В–лимфоцитов, активирует классическую систему комплемента. Синтезируется преимущественно в гепатоцитах, его синтез инициируется антигенами, иммунными комплексами, бактериями, грибами, при травме (через 4–6 ч после повреждения). В сыворотке здорового человека отсутствует. Концентрация СРБ в крови имеет высокую корреляцию с активностью заболевания, стадией процесса [2]. Уровень СРБ быстро и многократно повышается при воспалениях различной природы и локализации, паразитарных инфекциях, травмах и опухолях, сопровождающихся воспалением и некрозом тканей. Повышение уровня СРБ наблюдается при:
• системных ревматических заболеваниях;
• болезнях желудочно–кишечного тракта;
• реакции отторжения трансплантата;
• злокачественных опухолях;
• вторичном амилоидозе;
• инфаркте миокарда (появляется на 2–й день заболевания);
• сепсисе новорожденных;
• менингите;
• туберкулезе;
• послеоперационных осложнениях;
• нейтропении;
• приеме эстрогенов, оральных контрацептивов.
Повышение уровня СРБ является единственным маркером воспаления, обладающим предсказательной ценностью в отношении ИМ [3].
В настоящее время широко обсуждается значение БОФ как важных медиаторов, модулирующих развитие воспаления. Проведены многочисленные параллели между синтезом этих белков и противовоспалительным действием лекарственных препаратов, обладающих протективным действием на миокард [4]. Таким образом, ингибирование СРБ является перспективным новым подходом в кардиопротекции при ОИМ и инсульте. Препарат, обладающий протективным действием на миокард, следует назначать сразу же при госпитализации, до начала острой фазы ответа СРБ. Этот ответ проявляется через 6 ч от начала болевого синдрома и достигает максимума спустя 50 ч.
Одной из групп таких лекарств являются ингибиторы ангиотензинпревращающего фермента (АПФ) [5]. Доказано, что последние влияют на синтез БОФ воспаления и регулируют их взаимодействие при ОИМ [6], а поэтому должны назначаться в первые минуты госпитализации, т.е. как можно раньше [7]. Оказывая влияние на структурные нарушения в миокарде, ингибиторы АПФ препятствуют развитию гипертрофии кардиомиоцитов и средней оболочки сосудов, а также периваскулярного фиброза и увеличению общего содержания коллагена в миокарде. Долговременные эффекты ингибиторов АПФ, таким образом, в большей мере связаны с пролиферацией, фиброзом и другими процессами, представляющими воспаление [8]. Среди множества ингибиторов АПФ особого внимания заслуживает рамиприл (Дилапрел®).
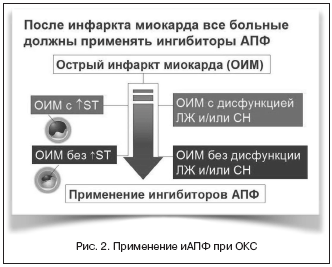
Согласно Европейским рекомендациям по диагностике и лечению острого коронарного синдрома (ОКС) (2007), после перенесенного ИМ больные должны получать ингибиторы АПФ (рис. 2). Эти препараты предупреждают ремоделирование ЛЖ и уменьшают летальность [9]. Ингибиторы АПФ следует применять с первых суток заболевания, титруя их дозу до рекомендуемой или максимально переносимой, и принимать неопределенно долго. Препараты этой группы вызывают уменьшение тонуса сосудов, главным образом артериол, вследствие чего снижаются АД, ОПСС и, соответственно, постнагрузка, что способствует увеличению сердечного выброса. Снижение содержания альдостерона приводит к выделению из организма Na и задержке K (особенно при применении больших доз препаратов). В отличие от многих вазодилататоров, ингибиторы АПФ, как правило, не вызывают рефлекторную тахикардию. Одновременно происходит увеличение концентрации брадикинина (активный вазодилататор). В результате сложного механизма сосудорасширяющего действия ингибиторы АПФ расширяют и венозные сосуды, в связи с чем уменьшают возврат крови к сердцу (преднагрузку) и давление в малом круге кровообращения. На фоне применения ингибиторов АПФ у пациентов с АГ и нормальной функцией почек практически не изменяются или иногда увеличиваются почечный кровоток и клубочковая фильтрация. Уменьшая образование ангиотензина II не только в плазме крови, но и, например, в сердце, ингибиторы АПФ препятствуют прогрессированию дилатации ЛЖ и вызывают обратное развитие его гипертрофии.
Препараты этой группы благоприятно влияют на коронарный кровоток, увеличивая его объемную скорость и уменьшая напряжение стенок желудочков. Они могут оказать противоаритмическое действие, связанное с влиянием на трофические процессы в миокарде, увеличением содержания K и Mg в крови, снижением содержания адреналина. В связи с тем, что ангиотензин II активирует симпатические центры продолговатого мозга, усиливая симпатическое влияние на сердце и сосуды, а также стимулирует передачу импульсов в симпатических нервных окончаниях, вегетативных ганглиях и секрецию адреналина в мозговом слое надпочечников, введение ингибиторов АПФ приводит к уменьшению влияния симпатической нервной системы на тонус сосудов. Ингибиторы АПФ не оказывают воздействия на мозговое кровообращение. Кровоток в сосудах мозга поддерживается на достаточном уровне и на фоне снижения АД.
Элиминация ингибиторов АПФ осуществляется двумя путями. Большинство иАПФ выводится главным образом почками (75–95%). Зачастую данный путь выведения препарата является нежелательным, т.к. при нарушении функции почек может происходить накопление лекарственного вещества в организме, а время его полувыведения увеличивается до 21–32 ч. В этой связи особого внимания заслуживает рамиприл (Дилапрел®), который обладает двойным путем выведения: 60% – через почки и 40% – через кишечник. Рамиприл разрешен к применению в том числе у сосудистых больных с латентной и компенсированной хронической почечной недостаточностью (ХПН) в исходе нефроангиосклероза и/или диабетической нефропатии, частота встречаемости которых, по данным различных авторов, достигает 68% от числа всех пациентов с кардио– и цереброваскулярной патологией.
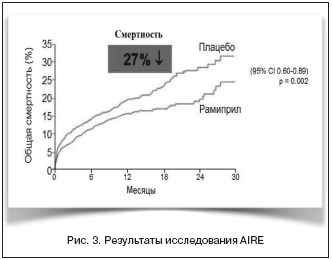
Рамиприл обладает обширной доказательной базой. Так, в исследовании AIRE [10], посвященном изучению эффективности и безопасности рамиприла у пациентов с ОИМ, было показано достоверное снижение риска смерти на 27% (95% ДИ 11–40%; р=0,002) (рис. 3): в группе принимавших рамиприл умерли 170 (17%) больных, а в группе принимавших плацебо — 222 (23%).
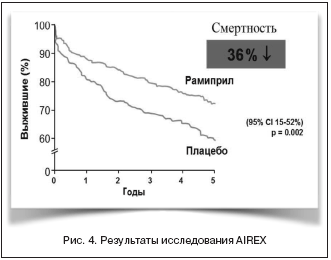
В исследовании AIREX [11], оценивавшем эффективность длительной терапии рамиприлом у пациентов после ОИМ в течение 59 мес., установлено, что лечение рамиприлом позволяло сохранить жизнь 114 больным на каждую тысячу пациентов, начавших терапию (рис. 4).
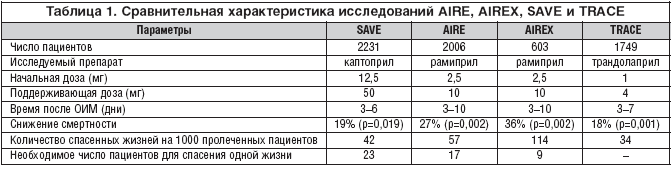
В группе плацебо умерли 117 (38,9%) из 301, а в группе рамиприла – 83 (27,5%) из 302 больных. Относительный риск смерти в группе рамиприла снизился на 36% (95% ДИ 15–52%; p=0,002). Рамиприл при ОКС продемонстрировал эффективность перед каптоприлом (SAVE) [12] и трандолаприлом (TRACE) [13] (табл. 1).
В исследовании HOPE [14], проводившемся в 267 центрах в 19 странах мира в течение 4,5 года (исследование было прекращено досрочно через 4,5 года ввиду явных преимуществ рамиприла), приняли участие около 9500 пациентов. Критериями включения пациентов в исследование были: коронарное заболевание артерий, заболевания периферических сосудов, инсульт в анамнезе или сахарный диабет с высоким риском сердечно–сосудистых осложнений. Исследование проводилось под контролем плацебо. Его целью было изучить действие ингибитора АПФ рамиприла относительно снижения сердечно–сосудистых заболеваний и приступов, а также влияние витамина Е на развитие сердечно–сосудистых и онкологических заболеваний. Часть исследования, касающаяся изучения витамина Е, до сих пор продолжается. Главным результатом исследования стало предотвращение новых случаев смерти, инфаркта миокарда и инсульта у 22% пациентов с риском развития сердечно–сосудистых заболеваний под влиянием рамиприла. Общая частота инфарктов миокарда и случаев смерти от сердечно–сосудистых причин составила в группе, принимавшей рамиприл, 13,9%, а в группе плацебо – 17,5%. Рамиприл снижал риск случаев смерти, обусловленных сердечно–сосудистыми причинами, на 26%, риск несмертельных инфарктов миокарда – на 20%, а риск несмертельных инсультов – на 31%. Частота вмешательств по поводу реваскуляризации (коронарная ангиопластика, аортокоронарное шунтирование, периферическая ангиопластика) в группе пациентов, принимавших рамиприл, была на 15% ниже. Риск развития сахарного диабета и первых его проявлений в группе пациентов, получавших рамиприл, снизился на 30%, при этом частота диабетических осложнений снизилась на 17%. Преимущества рамиприла наблюдались в равной степени в группе пациентов с нормальным давлением крови и у пациентов, страдавших артериальной гипертензией (54 и 46% соответственно). «Принимая во внимание результаты исследования HOPE, мы убеждены, что теперь имеется возможность предотвратить более миллиона преждевременных смертельных случаев инфаркта миокарда и инсульта, если соответствующие пациенты будут получать рамиприл», – сказал руководитель исследования HOPE профессор Salim Yusuf. Таким образом, данные результаты показывают, что рамиприл может оказаться жизненно важным лекарственным средством для многих «сосудистых» больных, и поэтому он должен быть назначен каждому пациенту с высоким риском развития неблагоприятных событий.
В субисследовании SECURE [15] (часть проекта НОРЕ) производили ультразвуковую оценку толщины комплекса интима–медиа сонных артерий на фоне терапии рамиприлом. В результате проведенной работы было показано, что антисклеротическое действие рамиприла не коррелировало с его влиянием на уровень артериального давления (АД). Максимальное снижение АД достигалось уже при дозе 2,5 мг/сут., а дальнейшее увеличение дозы не приводило к нарастанию гипотензивного эффекта, но значительно увеличивало антисклеротическое действие. Так, в дозе 10 мг/сут. рамиприл снижал прогрессирование атеросклероза на 37% по сравнению с плацебо. Таким образом, был сделан вывод о наиболее эффективной антиатеросклеротической и гипотензивной дозах рамиприла, равных 10 мг и 2,5 мг/сут. соответственно.
Метаболическому нейтралитету препаратов в настоящее время уделяется пристальное внимание. Это объясняется широким распространением среди пациентов инсулинорезистентности и сахарного диабета (СД), который, по нашим данным, у сосудистых больных в 81% случаев имеет осложненное течение.
Так, в исследовании MICRO–HOPE [16], направленном на изучение эффективности рамиприла в профилактике сердечно–сосудистых и микрососудистых осложнений у пациентов с СД, рамиприл продемонстрировал снижение частоты новых случаев ХПН на 24%, уменьшение других микрососудистых осложнений СД – на 16%, при безоговорочном снижении сердечно–сосудистой смертности по причине ИМ и инсульта (на 25%).
Целью исследования CARE [17] было определение эффективности и безопасности данного препарата в обычной клинической практике у пациентов с легкой и умеренной АГ (86% пациентов достигли целевого уровня АД, применяя для его снижения рамиприл в дозе 2,5–10 мг/сут.).
С целью определения эффективности и безопасности рамиприла у коморбидных больных, перенесших ИМ, авторами было проведено исследование рамиприла, субъектами которого явились 60 пациентов (34 мужчины и 26 женщин) в возрасте от 49 до 76 лет включительно (в среднем 62±7 лет), госпитализированные в отделение неотложной кардиологии [18]. У всех больных в первые 24 ч с момента госпитализации, а также через 3 мес. лечения определяли уровни СРБ, общего холестерина (ОХС), холестерина липопротеинов высокой (ХС–ЛПВП) и низкой (ХС–ЛПНП) плотности. За время госпитализации всем больным однократно выполнялась Эхо–КГ с целью оценки фракции выброса, массы миокарда левого желудочка (ММЛЖ) и размеров полостей сердца.
Все пациенты были разделены на 2 группы по 30 человек в каждой (табл. 2). Пациентам 1–й группы в первые 24 ч с момента развития ангинозного приступа назначался рамиприл внутрь в стартовой дозе 2,5 мг 2 раза/сут. Если пациенты не переносили начальную дозу препарата (артериальная гипотензия), то доза уменьшалась до 1,25 мг 2 раза/сут. Спустя 2 дня доза вновь увеличивалась до 2,5 мг 2 раза/сут., а спустя еще 2 дня – до 5 мг 2 раза/ сут. Максимальная суточная доза не превышала 10 мг. Ежедневно оценивались АД и ЧСС. После выписки из стационара предпочтительным был переход на однократный прием суточной дозы рамиприла, равной 5 или 10 мг в зависимости от переносимости лечения. Лечение продолжалось 90 дней. Пациенты 2–й группы получали стандартную терапию основного заболевания, включающую в себя прием какого–либо другого ингибитора АПФ.
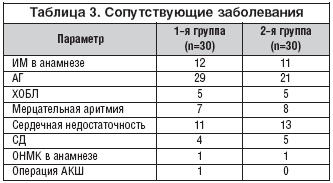
На этапе скрининга было выявлено, что у 37 пациентов ИМ развился впервые в жизни, а 23 пациента когда–либо ранее уже переносили ИМ. У 50 пациентов была диагностирована АГ, также было выявлено 10 случаев хронического обструктивного бронхита, 15 случаев мерцательной аритмии, у 24 больных имелась сердечная недостаточность. Из 60 включенных в исследование больных 9 пациентов страдали СД 2–го типа. У 2 больных в анамнезе было острое нарушение мозгового кровообращения (ОНМК). 1 пациент перенес операцию аортокоронарного шунтирования (АКШ). У всех пациентов и ранее до развития ОКС с различной частотой возникали загрудинные боли (табл. 3).
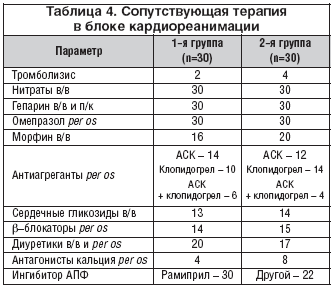
Пациенты с первых минут пребывания в кардиореанимационном отделении получали нитраты в/в (60 человек; далее в скобках указано число человек), гепарин в/в, п/к (60), омепразол per os (60), морфин в/в (36), сердечные гликозиды в/в (27), антиагреганты (60) – ацетилсалициловую кислоту (АСК) per os (26), клопидогрел per os (24), АСК per os + клопидогрел per os (10), диуретики в/в и per os (37), β–блокаторы per os (29), антагонисты кальция per os (12), ингибиторы АПФ, кроме рамиприла (22), 6 пациентам выполнен тромболизис (табл. 4).
Терапия рамиприлом в течение 3 мес. привела к значительному (на 65%) уменьшению частоты возникновения стенокардии в раннем постинфарктном периоде. Так, у 6 пациентов загрудинные боли исчезли, единичные эпизоды стенокардии случались у 21 пациента, и лишь 3 больных грудная жаба продолжала беспокоить 3 раза в неделю. Суммарное количество приступов сжимающей боли в груди уменьшилось со 106 до 37 в неделю (p<0,001). В группе контроля стенокардия исчезла только у 2 человек, 1–2 приступа загрудинных болей в неделю сохранялись у 17 пациентов, а остальные 11 больных прибегали к незапланированному приему нитратов 3–4 раза в неделю. Безусловно, в этой группе стенокардия также стала возникать реже, но суммарное количество ангинозных болей уменьшилось всего на 36% (с 98 до 63%).
У некоторых включенных в исследование пациентов на этапе СМП и в приемном отделении стационара были диагностированы высокие цифры АД. Возможно, что ИМ у этой подгруппы больных явился именно осложнением гипертонического криза. Таким образом, терапия сопутствующей АГ у пациентов, перенесших ИМ, является неотъемлемой частью профилактики повторных ишемических событий и улучшает их прогноз.
На фоне терапии АГ с использованием рамиприла было выявлено достоверное снижение как систолического, так и диастолического АД. Средний уровень САД снизился на 13,2% и составил 137 мм рт. ст. Уровень ДАД достиг 89 мм рт. ст., уменьшившись на 9,7% (p<0,001). При этом целевого уровня АД (120–139/80–89 мм рт.ст.) достигли 18 (62%) больных. Пациентов с тяжелой АГ зарегистрировано не было. Больные, которые на этапе скрининга имели тяжелую гипертензию, перешли в группу умеренной АГ.
В контрольной группе на фоне стандартной гипотензивной терапии также отмечалось достоверное эквивалентное снижение АД, но достичь целевого уровня смогли лишь 9 (43%) пациентов, при этом средний уровень САД составил 141 мм рт. ст., а ДАД – 91 мм рт. ст., снизившись на 11,9 и 9,1% соответственно.
Уровень CРБ в группе рамиприла за 3 мес. терапии снизился на 87,6% (p<0,001) по сравнению с 36,4% в группе контроля. Необходимо также отметить, что интенсивность уменьшения концентрации CРБ в крови в группе рамиприла была намного выше, чем в группе контроля. Уже через 1 мес. терапии рамиприлом уровень основного биохимического маркера воспаления в миокарде снизился на 51,3% и на 8,3% – в группе контроля.
Результаты нашего исследования продемонстрировали, что рамиприл снижает уровень ОХС и его атерогенных фракций, уменьшая прогрессирование ИБС. За 3 мес. лечения в обеих группах концентрация в крови ОХС у больных уменьшилась. В группе рамиприла уровень ОХС снизился на 8,1%, уровень ХС ЛПНП – на 7,8%, а уровень ХС ЛПВП вырос на 8,4% (p=0,01). В контрольной группе уровень ОХС снизился на 4,98%, уровень ХС ЛПНП – на 9,8%, а уровень ХС ЛПВП повысился на 2,9%.
Доказано, что добавление к стандартной терапии ингибиторов АПФ больным с ОКС позволяет снизить количество случаев развития клинически значимой сердечной недостаточности, смертельных исходов и улучшить прогноз у данной категории больных [13]. Систематический прием ингибитора АПФ показан больным с дисфункцией ЛЖ или с сердечной недостаточностью, а также после обширного ИМ, даже без нарушения функции сердца. Ремоделирование постинфарктного сердца (дилатация, деформация, развитие относительной митральной недостаточности, гипертрофия сохранного миокарда), которое развивается в условиях активации ренин–ангиотензин–альдостероновой системы (РААС), катехоламинов и т.д., ухудшает систолическую и диастолическую функции сердца. Патологическое изменение структуры и функции сердца у больных, перенесших ОИМ, понижает экономичность его работы, что усугубляет коронарную недостаточность и угрожает развитием сердечной недостаточности.
Ингибиторы АПФ оказывают ряд полезных первичных и вторичных эффектов, из которых наиболее понятным является снижение активности РААС. Через 90 дней терапии в группе рамиприла авторы наблюдали изменение ММЛЖ, которая наросла на 10,1% у мужчин (p=0,01) и на 5,4% регрессировала у женщин (p=0,1). В контрольной группе отмечалось значительное увеличение ММЛЖ: как в подгруппе мужчин (на 28,5%), так и в подгруппе женщин (на 19,2%) (p=0,01).
За 3 мес. терапии в группе пациентов, принимавших рамиприл, фатальных событий, а также нефатальных ИМ и инсультов зарегистрировано не было. Из 30 пациентов лишь двое были повторно госпитализированы по поводу дестабилизации стенокардии, в то время как в контрольной группе было зарегистрировано 4 случая повторного ИМ, в том числе 3 случая, закончившиеся смертью. По поводу дестабилизации стенокардии было госпитализировано 4 других пациента. У 1 больного через 2 мес. после выписки из стационара случился ишемический инсульт.
Таким образом, рамиприл (Дилапрел®), назначенный в первые 24 ч от начала развития ОКС и непрерывно принимаемый в последующие 3 мес., улучшает прогноз у пациентов, перенесших ОИМ. Полученные в собственном клиническом исследовании результаты позволяют рекомендовать данный препарат для широкого использования в неотложной кардиологии.

Литература
1. Ridker P.M., Hennekens C.H., Buring J.E., Rifai N. C–reactive protein and other markers of inflammation in the prediction of cardiovascular disease in women // N. Engl. J. Med. 2000 Mar 23. Vol. 342 (12). Р. 836–843.
2. Hudson M.P., Christenson R.H., Newby L.K. Cardiac markers: point of care testing // Clin. Chim. Acta. 1999. Jun; 30; Vol. 284(2). Р. 223–237.
3. Study Investigators. Effect of ramipril on mortality and morbidity of survivors of acute myocardial infarction with clinical evidence of heart failure The Acute Infarction Ramipril Efficacy // Lancet. 1993. Vol. 342. Р. 821–828.
4. Lonn E.M. Yusuf S., Jha P. Emerging role of angiotensin–converting enzyme inhibitors in cardiac and vascular protection // Circulation. 1994. Vol. 90. Р. 2056–2069.
5. Smith S.J., Bos G., Essvild R. Acute – phase proteins from the liver and enzymes from myocardial infarction, a quantitative relationship // Clin. Chem. Acta. 1977. Vol. 81. P. 75–85.
6. Барановский П.А., Куцин Н.Ф. Клиническое значение С–реактивного белка // Врач. дело. 1988. № 10. С. 75–79.
7. Ларский Э.Г., Комелькова Л.В. Белки острой фазы: современное состояние вопроса // М.Р.Ж. 1988.XXII. № 12. С. 33–37.
8. Чукаева И.И., Богова О.Т., Алешкин В.А., Новикова Л.И., Корочкин И.М. Сопоставление прогностического влияния острофазовых белков (С–РБК, орозомукоид, гаптоглобин) при инфаркте миокарда: Тез. докладов // Российский национальный конгресс «Человек и лекарство». Москва, апрель 2001. С. 500.
9. ACC/AHA 2007 Guidelines for the Management of Patients With Unstable Angina/Non–ST–Elevation Myocardial Infarction. A Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 2002 Guidelines for the Management of Patients With Unstable Angina/Non–ST–Elevation Myocardial Infarction) // JACC. 2007. Vol. 50. Р. 157.
10. Effect of ramipril on morbidity and mode of death among survivors of acute myocardial infarction with clinical evidence of heart failure. A report from the AIRE Study Investigators // Eur Heart J. 1997 Jan. Vol. 18 (1). Р. 41–51.
11. Hall A.S, Murray G.D., Ball S.G. Follow–up study of patients randomly allocated ramipril or placebo for heart failure after acute myocardial infarction: AIRE Extension (AIREX) Study. Acute Infarction Ramipril Efficacy // Lancet. 1997. Vol. 349. Р. 1493–1497.
12. Pfeffer M.A., Braunwald E.A., Moyo L.A. Effect of captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction: results of the Survival And Ventricular Enlargement trial (SAVE) // N. Engl. J. Med. 1992. Vol. 327. Р. 669–677.
13. Kobber L., Torp–Pedersen C., Carlsen J.E., Bagger H., Eliasen P., Lyngborg K., Videbaek J., Cole D.S., Auclert L., Pauly N.C. A clinical trial of the angiotensin–converting–enzyme inhibitor trandolapril in patients with left ventricular dysfunction after myocardial infarction. Trandolapril Cardiac Evaluation (TRACE) Study Group // N. Engl. J. Med. 1995. Vol. 333. Р. 1670–1676.
14. Lonn E.M., Yusuf S. Clinical, public health, and research implications of the Heart Outcomes Prevention Evaluation (HOPE) Study // Eur. Heart J. 2001 Jan. Vol. 22 (2). Р. 103–104.
15. Lonn E., Yusuf S., Dzavik V. Effects of ramipril and vitamin E on atherosclerosis: the study to evaluate carotid ultrasound changes in patients treated with ramipril and vitamin E (SECURE) // Circulation. 2001 Feb 20. Vol. 103 (7). Р. 919–925.
16. Bosch J., Yusuf S., Pogue J. MICRO–HOPE Investigators. Use of ramipril in preventing stroke: double blind randomised trial // BMJ. 2002. Vol. 324. Р. 699–702.
17. Kaplan N.M. CARE Investigators. Hypertension in the population at large // Clinical Hypertension. 6th ed. Baltimore.
18. Верткин А.Л., Скотников А.С. Исследование ингибиторов ангиотензинпревращающего фермента у пациентов, перенесших острый инфаркт миокарда // Кардиология, 2008. – Том 48, № 7. – С. 14–18.












