–У–µ—В–µ—А–Њ–≥–µ–љ–љ–Њ—Б—В—М —Н—В–Є–Њ–ї–Њ–≥–Є–Є –Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –≤—Л—Б–Њ–Ї–Є—Е —Ж–Є—Д—А –Р–Ф –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Њ–±—Й–µ–њ—А–Є–љ—П—В–∞ –Ї–ї–Є–љ–Є—Ж–Є—Б—В–∞–Љ–ЄвАУ–Ї–∞—А–і–Є–Њ–ї–Њ–≥–∞–Љ–Є. –Я–Њ –Љ–љ–µ–љ–Є—О –У.–У. –Р—А–∞¬≠–±–Є¬≠–і–Ј–µ, ¬Ђ–Љ–Њ–Ј–∞–Є—З–љ–∞—П —В–µ–Њ—А–Є—П¬ї –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г–µ—В —В–µ—Б–љ–Њ–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤, —Б–Њ—Б—В–∞–≤–ї—П—О—Й–Є—Е –Є–љ—В–µ–≥—А–∞–ї—М–љ—Г—О —Б–Є—Б—В–µ–Љ—Г —А–µ–≥—Г–ї—П—Ж–Є–Є –Р–Ф. –Ю–і–љ–∞–Ї–Њ –Њ–±—Й–µ–њ—А–Є–љ—П—В–∞—П –Ї–Њ–љ—Ж–µ–њ—Ж–Є—П –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –Р–У –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Г—З–Є—В—Л–≤–∞–µ—В –≤–Ї–ї–∞–і –љ–∞—А—Г—И–µ–љ–Є–є —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –Ї—А–Њ–≤–Є, –Њ–њ—А–µ–і–µ–ї—П–µ–Љ—Л—Е –±–µ–ї–Ї–Њ–≤–ЊвАУ–ї–Є–њ–Є–і–љ—Л–Љ —Б–Њ—Б—В–∞–≤–Њ–Љ –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ —Б–Њ—Б—В–Њ—П–љ–Є–µ–Љ —Д–Њ—А–Љ–µ–љ–љ—Л—Е —Н–ї–µ–Љ–µ–љ—В–Њ–≤ –Ї—А–Њ–≤–Є (—В—А–Њ–Љ–±–Њ—Ж–Є—В—Л, —Н—А–Є—В—А–Њ—Ж–Є—В—Л, –ї–µ–є–Ї–Њ—Ж–Є—В—Л) –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є –≤—Л—Б–Њ–Ї–Є—Е —Ж–Є—Д—А –Р–Ф –Ї–∞–Ї –Є–љ—В–µ–≥—А–∞–ї—М–љ–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –љ–∞—А—Г—И–µ–љ–Є–є —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є. –Я–Њ—Б–ї–µ–і¬≠–љ–Є–µ –≥–Њ–і—Л –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ –≤–љ–Є–Љ–∞–љ–Є–µ–Љ –Ї –Є–Ј—Г—З–µ–љ–Є—О –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –∞–≥—А–µ–≥–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В–Є –Є –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ –≤ —Б–Њ–њ–Њ—Б—В–∞–≤–ї–µ–љ–Є–Є —Б –њ–ї–∞–Ј–Љ–µ–љ–љ—Л–Љ–Є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞–Љ–Є –Ї—А–Њ–≤–Є —Г –±–Њ–ї—М–љ—Л—Е –Р–У.
–Т—Л–±–Њ—А –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Г –±–Њ–ї—М–љ—Л—Е –Р–У —Б–ї–Њ–ґ–µ–љ. –Ю–љ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М—О –Є—Б–Ї–ї—О—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є—Е –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ –њ—А–Њ—Ж–µ—Б—Б—Л –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –≥–ї—О–Ї–Њ–Ј—Л –Є –ї–Є–њ–Є–і–Њ–≤, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є–Ј–±—Л—В–Њ—З–љ–Њ–є –Љ–∞—Б—Б–Њ–є —В–µ–ї–∞ (–Ш–Ь–°>25 –Ї–≥/–Љ2). –Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –і–Њ–ї–ґ–љ—Л –Њ–±–ї–∞–і–∞—В—М –Њ—А–≥–∞–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є. –Ф–Њ –љ–µ–і–∞–≤–љ–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є bвАУ–∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А—Л (–С–Р–С) –Є –і–Є—Г—А–µ—В–Є–Ї–Є —Б—З–Є—В–∞–ї–Є—Б—М –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –њ–µ—А–≤–Њ–≥–Њ –≤—Л–±–Њ—А–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Р–У. –°–µ–є—З–∞—Б –Њ–љ–Є —Б–Њ–≤–Љ–µ—Й–∞—О—В —Н—В—Г –њ–Њ–Ј–Є—Ж–Є—О —Б –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§, –∞–љ—В–Є–Ї–∞–ї—М—Ж–Є–µ–≤—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є [4,5].
–Ш–і–µ—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –С–Р–С –≤ –Ї–∞—З–µ—Б—В–≤–µ –Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–Њ–≤ –њ—А–Є–љ–∞–і–ї–µ–ґ–Є—В –∞–љ–≥–ї–Є—З–∞–љ–Є–љ—Г J.W. Black, –∞ –≤ 1988 –≥. –µ–Љ—Г —Б —Б–Њ—В—А—Г–і–љ–Є–Ї–∞–Љ–Є –Ї–∞–Ї c–Њ–Ј–і–∞—В–µ–ї—П–Љ –Є –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—П–Љ —А–Њ–ї–Є –С–Р–С –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –±—Л–ї–∞ –њ—А–Є—Б—Г–ґ–і–µ–љ–∞ –Э–Њ–±–µ–ї–µ–≤—Б–Ї–∞—П –њ—А–µ–Љ–Є—П. –Э–Њ–±–µ–ї–µ–≤—Б–Ї–Є–є –Ї–Њ–Љ–Є—В–µ—В –Њ—Ж–µ–љ–Є–ї –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Ї–∞–Ї ¬Ђ–≤–µ–ї–Є—З–∞–є—И–Є–є –њ—А–Њ—А—Л–≤ –≤ –±–Њ—А—М–±–µ —Б –±–Њ–ї–µ–Ј–љ—П–Љ–Є —Б–µ—А–і—Ж–∞ –њ–Њ—Б–ї–µ –Њ—В–Ї—А—Л—В–Є—П –і–Є–≥–Є—В–∞–ї–Є—Б–∞ 250 –ї–µ—В –љ–∞–Ј–∞–і¬ї.
–Т –њ–Њ—Б–ї–µ–і–љ–Є–µ 40 –ї–µ—В –±—Л–ї–Њ —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–љ–Њ –±–Њ–ї–µ–µ 100 –С–Р–С. –Т –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –љ–µ –±–Њ–ї–µ–µ 30 –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–С–Р–С –Ї–ї–∞—Б—Б–Є—Д–Є—Ж–Є—А—Г—О—В—Б—П –њ–Њ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ —Б–≤–Њ–є—Б—В–≤–∞–Љ, —Е–∞—А–∞–Ї—В–µ—А–љ—Л–Љ –≤ —А–∞–Ј–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –і–ї—П –Ї–Њ–љ–Ї—А–µ—В–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ [5]:
вАУ –њ–Њ —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ї ќ≤1вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–∞–Љ;
вАУ –њ–Њ –ї–Є–њ–ЊвАУ –Є–ї–Є –≥–Є–і—А–Њ—Д–Є–ї—М–љ–Њ—Б—В–Є (—А–∞—Б—В–≤–Њ—А–Є–Љ–Њ—Б—В—М –≤ –ґ–Є—А–∞—Е –Є–ї–Є –≤–Њ–і–µ);
вАУ –њ–Њ –љ–∞–ї–Є—З–Є—О –≤–љ—Г—В—А–µ–љ–љ–µ–є —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є;
вАУ –њ–Њ –љ–∞–ї–Є—З–Є—О –Љ–µ–Љ–±—А–∞–љ–Њ—Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г—О—Й–µ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є;
вАУ –њ–Њ —Б–Є–ї–µ –±–ї–Њ–Ї–∞–і—Л —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤;
вАУ –њ–Њ —Б—В–∞–±–Є–ї—М–љ–Њ—Б—В–Є –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –і–µ–є—Б—В–≤–Є—П.
–Ь–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –С–Р–С —Б–Њ—Б—В–Њ–Є—В –≤ –Ї–Њ–љ–Ї—Г—А–µ–љ—В–љ–Њ–Љ –∞–љ—В–∞–≥–Њ–љ–Є–Ј–Љ–µ —Б –Ї–∞—В–µ—Е–Њ–ї–∞–Љ–Є–љ–∞–Љ–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є ќ≤вАУ–∞–і—А–µ–љ–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Т –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –Љ–µ—В–∞вАУ–∞–љ–∞–ї–Є–Ј–∞—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є –њ–Њ–і–≤–µ—А–≥–∞–ї–∞—Б—М —Б–Њ–Љ–љ–µ–љ–Є—О —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —Б –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —Ж–µ–ї—М—О –∞—В–µ–љ–Њ–ї–Њ–ї–∞ [6]. –Я–Њ —Н—В–Њ–є –њ—А–Є—З–Є–љ–µ –Њ—Б–њ–∞—А–Є–≤–∞–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –љ–∞—З–∞–ї–∞ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б –С–Р–С –њ—А–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е —Б–∞—Е–∞—А–љ–Њ–Љ –і–Є–∞–±–µ—В–µ (–°–Ф) –Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ. –Ю–і–љ–∞–Ї–Њ –Љ–љ–Њ–≥–Є–µ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –С–Р–С –њ—А–Є –њ—А–∞–≤–Є–ї—М–љ–Њ–Љ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є–Є –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –ї–Є—И–µ–љ—Л —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —Б–≤–Њ–є—Б—В–≤ [7]. –Ъ–∞–Ї –Њ—В–Љ–µ—З–∞–µ—В—Б—П –≤ –љ–µ–і–∞–≤–љ–µ–Љ –°–Њ–≥–ї–∞—Б–Є—В–µ–ї—М–љ–Њ–Љ –і–Њ–Ї—Г–Љ–µ–љ—В–µ —Н–Ї—Б–њ–µ—А—В–Њ–≤ –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Њ–≤ –њ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –С–Р–С, –њ—А–µ–њ–∞—А–∞—В—Л —Н—В–Њ–≥–Њ –Ї–ї–∞—Б—Б–∞ –њ–Њ–Ї–∞–Ј–∞–љ—Л –і–ї—П –ї–µ—З–µ–љ–Є—П –Р–У —Б —Г—А–Њ–≤–љ–µ–Љ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Р –Ї–∞–Ї –і–ї—П –Ї–Њ–љ—В—А–Њ–ї—П –Ј–∞ —Г—А–Њ–≤–љ–µ–Љ –Р–Ф, —В–∞–Ї –Є –і–ї—П –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –≤ —Ж–µ–ї–Њ–Љ —А—П–і–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є—В—Г–∞—Ж–Є–є [2]. –Ґ–∞–Ї, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ї–∞—А–≤–µ–і–Є–ї–Њ–ї–∞ –њ—А–Є –Р–У –љ–∞ —Д–Њ–љ–µ –°–Ф –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М –≤ —Н—В–Њ–Љ –њ–ї–∞–љ–µ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–µ–Ј–Њ–њ–∞—Б–љ–µ–µ, —З–µ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Љ–µ—В–Њ–њ—А–Њ–ї–Њ–ї–∞ (GEMINI) [8]. –С–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–Љ –°–Ф –Є –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є–Є –і–Њ–Ї–∞–Ј–∞–љ–∞ —В–∞–Ї–ґ–µ –Є –і–ї—П –Ї–∞—А–і–Є–Њ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –С–Р–С вАУ –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞ [5,9].
–Т–∞–ґ–љ—Л–Љ —Б–≤–Њ–є—Б—В–≤–Њ–Љ –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞ —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–ї–Њ–љ–≥–Є—А–Њ–≤–∞–љ–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–≥–Њ —Б—Г—В–Њ—З–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞. –С–Є—Б–Њ–њ—А–Њ–ї–Њ–ї –≤—Л–Ј—Л–≤–∞–µ—В –Ј–∞–≤–Є—Б–Є–Љ–Њ–µ –Њ—В –і–Њ–Ј—Л —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–Њ–і—К–µ–Љ–∞ –Р–Ф –Є –І–°–° –≤–Њ –≤—А–µ–Љ—П –Є –њ–Њ—Б–ї–µ —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Є, —В.–µ. —Б–њ–Њ—Б–Њ–±–µ–љ –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—В—М —Б—В—А–µ—Б—БвАУ–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ—Л–µ –њ–Њ–і—К–µ–Љ—Л –Р–Ф [10]. –Т —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–≥–Њ 24вАУ—З–∞—Б–Њ–≤–Њ–≥–Њ –Љ–Њ–љ–Є—В–Њ—А–Є–љ–≥–∞ –Р–Ф –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞ –≤ —В–µ—З–µ–љ–Є–µ 24 —З –≤—Л—И–µ, —З–µ–Љ —Г –і—А—Г–≥–Є—Е –љ–∞–Ј–љ–∞—З–∞–µ–Љ—Л—Е 1 —А–∞–Ј/—Б—Г—В. –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–љ–∞–њ—А–Є–Љ–µ—А, –∞—В–µ–љ–Њ–ї–Њ–ї–∞ –Є–ї–Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞ –Ї–∞–ї—М—Ж–Є—П вАУ –љ–Є—В—А–µ–љ–і–Є–њ–Є–љ–∞). –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ —В–∞–Ї–ґ–µ, —З—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –Р–Ф –≤ —В–µ—З–µ–љ–Є–µ —Б—Г—В–Њ–Ї –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–Њ –њ—А–Є –њ—А–Є–µ–Љ–µ –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞, —З–µ–Љ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –≤—В–Њ—А–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ—А–µ–њ–∞—А–∞—В –Њ—В–ї–Є—З–∞–µ—В—Б—П —Е–Њ—А–Њ—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О –Є —Г–ї—Г—З—И–∞–µ—В —Б–µ–Ї—Б—Г–∞–ї—М–љ—Г—О —Д—Г–љ–Ї—Ж–Є—О [11,12].
–Т –њ–µ—А–µ–Ї—А–µ—Б—В–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –і–≤–Њ–є–љ–Њ–≥–Њ —Б–ї–µ–њ–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е –Р–У –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–Њ–Љ (10 –Љ–≥/—Б—Г—В.), –њ–Њ –і–∞–љ–љ—Л–Љ –Є–Љ–њ—Г–ї—М—Б–љ–Њ–є –і–Њ–њ–ї–µ—А—Д–ї–Њ—Г–Љ–µ—В—А–Є–Є, –і–Є–∞–Љ–µ—В—А —Б–Њ–љ–љ–Њ–є –Є –њ–ї–µ—З–µ–≤–Њ–є –∞—А—В–µ—А–Є–є, –∞ —В–∞–Ї–ґ–µ –Ї—А–Њ–≤–Њ—В–Њ–Ї –Є —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є–µ –≤ —Г–Ї–∞–Ј–∞–љ–љ—Л—Е —Б–Њ—Б—Г–і–∞—Е –љ–µ –Љ–µ–љ—П–ї–Є—Б—М. –°–Ї–Њ—А–Њ—Б—В—М —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П –њ—Г–ї—М—Б–Њ–≤–Њ–є –≤–Њ–ї–љ—Л –≤ –Њ–±–Њ–Є—Е —Б–Њc—Г–і–∞—Е —Г–Љ–µ–љ—М—И–∞–ї–∞—Б—М, –∞ —А–∞—Б—В—П–ґ–Є–Љ–Њ—Б—В—М –њ–ї–µ—З–µ–≤–Њ–є –∞—А—В–µ—А–Є–Є —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–∞—Б—М. –Я–Њ–ї—Г¬≠—З–µ–љ¬≠–љ—Л–µ –і–∞–љ–љ—Л–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ —В–Њ–Љ, —З—В–Њ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –њ—А–Є –±–ї–Њ–Ї–∞–і–µ ќ≤1вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Г–ї—Г—З—И–µ–љ–Є–µ–Љ —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є, —З—В–Њ –Ї–Њ—Б–≤–µ–љ–љ–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–Є —А–µ–ї–∞–Ї—Б–∞—Ж–Є–Њ–љ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є —Н–љ–і–Њ—В–µ–ї–Є—П [13].
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Љ–љ–Њ–≥–Є–µ —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є —А–∞–Ј–≤–Є—В—Л–µ —Б—В—А–∞–љ—Л –Љ–Є—А–∞ –њ–µ—А–µ—Е–Њ–і—П—В –љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –і–ґ–µ–љ–µ—А–Є–Ї–Њ–≤—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П —Г–ї—Г—З—И–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є–Ї–Є вАУ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –љ–∞—Г–Ї–Є –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—П—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Є –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М—И–µ–≥–Њ —З–Є—Б–ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ј–∞ —Б—З–µ—В –≤—Л–≤–µ—А–µ–љ–љ–Њ–≥–Њ —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Ї —В–µ—А–∞–њ–Є–Є. –Ф–ґ–µ–љ–µ—А–Є–Ї (generic) вАУ —А–Њ¬≠–і–Њ¬≠–≤–Њ–є —Б—Е–Њ–і–љ—Л–є. –Ш–љ—Д–Њ—А–Љ–∞—Ж–Є—П –Њ ¬Ђ—Б—В–∞—В—Г—Б–µ¬ї (¬Ђ—А–Њ–і–Њ—Б–ї–Њ–≤–љ–Њ–є¬ї) –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ (–Ы–°) –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ —Б–њ—А–∞–≤–Њ—З–љ–Є–Ї–µ ¬ЂOrange Book¬ї –Є –і–Њ—Б—В—Г–њ–љ–∞ –≤—Б–µ–Љ (www.fda.gov/cder/ob).
–Ф–ґ–µ–љ–µ—А–Є–Ї–Є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–µ —В—А–µ¬≠–±–Њ–≤–∞–љ–Є—П–Љ G–°P –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–∞ (–њ—А–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –Є—Б¬≠—Б–ї–µ¬≠–і–Њ–≤–∞–љ–Є–Є –љ–∞ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї—Г—О —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ–Њ—Б—В—М –Є –Є–Љ–µ—О¬≠—Й–Є–µ –Њ—В–ї–Є—З–Є—П –њ–Њ –±–Є–Њ—Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ–Њ—Б—В–Є –Њ—В –Њ—А–Є–≥–Є–љ–∞–ї—М–љ–Њ–≥–Њ –Ы–° –љ–µ –±–Њ–ї–µ–µ 3вАУ4%) –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б–Њ —Б—В—А–Њ–≥–Є–Љ –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –Ї–∞—З–µ—Б—В–≤–∞, —П–≤–ї—П—О—В—Б—П —Г–і–∞—З–љ–Њ–є –±—О–і–ґ–µ—В–љ–Њ–є –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–Њ–є –њ—А–Є –Є—Б¬≠–њ–Њ–ї—М¬≠–Ј–Њ–≤–∞–љ–Є–Є —Г —И–Є—А–Њ–Ї–Є—Е —Б–ї–Њ–µ–≤ –љ–∞—Б–µ–ї–µ–љ–Є—П [14вАУ16].
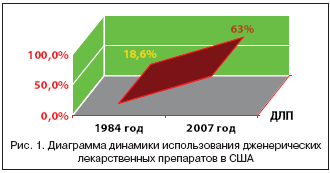
–Ф–ґ–µ–љ–µ—А–Є—З–µ—Б–Ї–∞—П –Ј–∞–Љ–µ–љ–∞ –Ы–° вАУ –Њ–і–Є–љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ—Л—Е (–Њ—З–µ–≤–Є–і–љ—Л—Е) —Б–њ–Њ—Б–Њ–±–Њ–≤ —Б–љ–Є–ґ–µ–љ–Є—П —Б—В–Њ–Є–Љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –Є —Г–≤–µ–ї–Є—З–µ–љ–Є—П –і–Њ—Б—В—Г–њ–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є, –∞–Ї—В–Є–≤–љ–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–є –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е —Б—В—А–∞–љ–∞—Е –Љ–Є—А–∞. –Т –°–®–Р вАУ –і–Њ–ї—П –і–ґ–µ–љ–µ—А–Є—З–µ—Б–Ї–Є—Е –Ы–° (–Ф–Ы–°) –≤ 1984 –≥. —Б–Њ—Б—В–∞–≤–Є–ї–∞ 18,6% –Њ—В –≤—Б–µ—Е —А–µ—Ж–µ–њ—В—Г—А–љ—Л—Е –љ–∞–Ј–љ–∞—З–∞–µ–Љ—Л—Е –Ы–Я, –∞ –≤ 2007 –≥. вАУ —Г–ґ–µ 63% (—А–Є—Б. 1).
–Ю—Б–Њ–±–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ –Ј–∞—Б–ї—Г–ґ–Є–≤–∞—О—В –Ї–Њ–Љ–њ–∞–љ–Є–Є, –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—О—Й–Є–µ ¬Ђ–±—А–µ–љ–і–Є—А–Њ–≤–∞–љ–Є–µ¬ї (–њ—А–Њ–і–≤–Є–ґ–µ–љ–Є–µ) –і–ґ–µ–љ–µ—А–Є–Ї–Њ–≤, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—П —В–µ–Љ —Б–∞–Љ—Л–Љ –Є—Е —Г–Ј–љ–∞–≤–∞–µ–Љ–Њ—Б—В—М, –∞ –Ј–љ–∞—З–Є—В, –Є–Љ–µ—О—Й–Є–µ –≤—Б–µ –Њ—Б–љ–Њ–≤–∞–љ–Є—П –Є —Б–њ–Њ—Б–Њ–±–љ—Л–µ –Њ—В–≤–µ—З–∞—В—М –Ј–∞ –≤—Л—Б–Њ–Ї–Њ–µ –Ї–∞—З–µ—Б—В–≤–Њ —В–∞–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
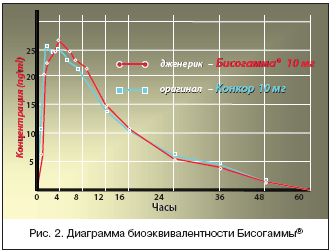
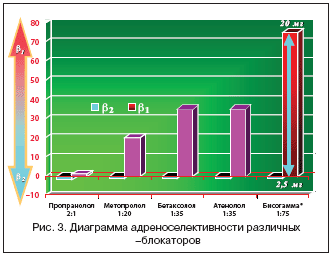
–С–Є—Б–Њ–≥–∞–Љ–Љ–∞¬Ѓ (W√ґrwag Pharma, –У–µ—А–Љ–∞–љ–Є—П) вАУ –і–ґ–µ–љ–µ—А–Є–Ї —Б –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–є –±–Є–Њ—Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ–Њ—Б—В—М—О –Њ—А–Є–≥–Є–љ–∞–ї—Г (—А–Є—Б. 2), –≤—Л—Б–Њ–Ї–Њ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–є b1вАУ–∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А —Б —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ–Љ b1/b2вАУ–±–ї–Њ–Ї–Є—А—Г—О—Й–µ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є 1/75. –Т —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ј–∞—Е –Њ—В 2,5 –і–Њ 10 –Љ–≥ –њ—А–µ–њ–∞—А–∞—В –њ–Њ—З—В–Є –љ–µ –њ—А–Њ—П–≤–ї—П–µ—В –±–ї–Њ–Ї–Є—А—Г—О—Й–µ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є b2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –њ–Њ—Н—В–Њ–Љ—Г –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –∞–љ–≥–Є–Њ—Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –љ–∞ –∞—А—В–µ—А–Є–Є, –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В —В–∞–Ї–Є—Е –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –Ї–∞–Ї –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П, –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є—П –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –±–ї–Њ–Ї–∞–і—Л b2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –±—А–Њ–љ—Е–Њ–≤, –і–∞–ґ–µ –љ–∞ —Д–Њ–љ–µ –љ–∞–Є–±–Њ–ї—М—И–µ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є вАУ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –і–Њ–Ј—Л 20 –Љ–≥ (—А–Є—Б. 3). –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М —В–∞–Ї–ґ–µ –љ–∞–ї–Є—З–Є–µ —Г –С–Є—Б–Њ–≥–∞–Љ–Љ—Л¬Ѓ –Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л—Е —Б–≤–Њ–є—Б—В–≤ [17].
–§–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ–Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞ —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ –≤—Л—Б–Њ–Ї–∞—П –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М (>90%), —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —А–∞—Б—В–≤–Њ—А—П—В—М—Б—П –Ї–∞–Ї –≤ –ї–Є–њ–Є–і–∞—Е, —В–∞–Ї –Є –≤ –≤–Њ–і–µ, —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –і–≤–Њ–є–љ–Њ–є –њ—Г—В—М –µ–≥–Њ —Н–ї–Є–Љ–Є–љ–∞—Ж–Є–Є вАУ —З–µ—А–µ–Ј –њ–µ—З–µ–љ—М –Є –њ–Њ—З–Ї–Є, –њ–Њ—Н—В–Њ–Љ—Г –±–Њ–ї—М–љ—Л–Љ —Б –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —Н—В–Є—Е –Њ—А–≥–∞–љ–Њ–≤ –љ–µ —В—А–µ–±—Г–µ—В—Б—П –Ї–Њ—А—А–µ–Ї—Ж–Є—П –і–Њ–Ј—Л –С–Є—Б–Њ–≥–∞–Љ–Љ—Л¬Ѓ.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л 48 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–У 1вАУ2вАУ–є —Б—В–µ–њ–µ–љ–Є, —А–Є—Б–Ї–Њ–Љ 1вАУ3 (–Т–Ю–Ч/–Ь–Ю–У 1999 –≥.), –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 45 –і–Њ 65 –ї–µ—В (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В вАУ 51,41¬±6,3 –≥–Њ–і–∞), 29 –Љ—Г–ґ—З–Є–љ –Є 19 –ґ–µ–љ—Й–Є–љ. –Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Р–У –≤ —Б—А–µ–і–љ–µ–Љ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 5,4¬±2,1 –≥–Њ–і–∞. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Є —Г –≤—Б–µ—Е –њ–∞¬≠—Ж–Є¬≠–µ–љ—В–Њ–≤ –±—Л–ї–∞ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–∞—П –Є—И–µ–Љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–Ј–љ—М —Б–µ—А–і—Ж–∞. –Ъ–Њ–љ—В—А–Њ–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г —Б–Њ—Б—В–∞–≤–Є–ї–Є 20 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ вАУ –љ–Њ—А–Љ–Њ—В–Њ–љ–Є–Ї–Є: —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В вАУ 53,1¬±5,8 –≥–Њ–і–∞, —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –љ–µ –Њ—В–ї–Є—З–∞–ї—Б—П –Њ—В –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ—Л (—А>0,05); 11 –Љ—Г–ґ¬≠—З–Є–љ, 9 –ґ–µ–љ—Й–Є–љ. –°–µ–ї–µ–Ї—В–Є–≤–љ—Л–є ќ≤1вАУ–±–ї–Њ–Ї–∞—В–Њ—А вАУ –С–Є—Б–Њ–≥–∞–Љ–Љ–∞¬Ѓ (Worwag Pharma) вАУ –њ—А–Є–Љ–µ–љ—П–ї—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –њ–Њ –љ–∞—А–∞—Б—В–∞—О—Й–µ–є —Б—Е–µ–Љ–µ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Њ—В 2,5 –і–Њ 10 –Љ–≥ (–≤ —Б—А–µ–і–љ–µ–Љ вАУ 7,5¬±0,15 –Љ–≥) –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ –≤ —Б—Г—В–Ї–Є –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б. —Г 48 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Р–У.ћИћИ
–£ –≤—Б–µ—Е –љ–∞–±–ї—О–і–∞–µ–Љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–У –і–Њ –Є –њ–Њ—Б–ї–µ 4вАУ–љ–µ–і–µ–ї—М–љ–Њ–є –Є 6вАУ–Љ–µ—Б—П—З–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є–Ј—Г—З–∞–ї–Є –∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ (–Р–Ґ—А), —Н–ї–µ–Ї—В—А–Њ—Д–Њ—А–µ—В–Є—З–µ—Б–Ї—Г—О –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В—М —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ (–≠–§–Я–≠), –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Ї—А–Њ–≤–Є: Ht, –ї–Є–њ–Є–і–љ—Л–є –њ—А–Њ—Д–Є–ї—М, —Д–Є–±—А–Є–љ–Њ–≥–µ–љ, –≥–ї—О–Ї–Њ–Ј—Г, –Њ–њ—А–µ–і–µ–ї—П–ї–Є –≤–µ–ї–Є—З–Є–љ—Г –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –Є–љ—В–Є–ЉвАУ–Љ–µ–і–Є–∞ –Є —А–∞—Б—Б—З–Є—В—Л–≤–∞–ї–Є –Љ–Њ–і—Г–ї—М –Ѓ–љ–≥–∞ –і–ї—П –Њ–±—Й–µ–є —Б–Њ–љ–љ–Њ–є –Є –Њ–±—Й–µ–є –±–µ–і—А–µ–љ–љ–Њ–є –∞—А—В–µ—А–Є–Є.
–Э–Њ—А–Љ–∞—В–Є–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —А–µ–Њ–ї–Њ–≥–Є–Є –Ї—А–Њ–≤–Є –±—Л–ї–Є –Њ–њ—А–µ–і–µ–ї–µ–љ—Л —Г –љ–Њ—А–Љ–Њ—В–Њ–љ–Є–Ї–Њ–≤ (20 –њ–∞—Ж–Є–µ–љ—В–Њ–≤), –њ—А–Њ—Е–Њ–і—П—Й–Є—Е –Њ—З–µ—А–µ–і–љ–Њ–µ –і–Є—Б–њ–∞–љ—Б–µ—А–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ. –Ґ—А–Њ–Љ–±–Њ¬≠—Ж–Є¬≠—В–∞—А–љ—Л–є –≥–µ–Љ–Њ—Б—В–∞–Ј –Є–Ј—Г—З–∞–ї–Є –њ—Г—В–µ–Љ –Ј–∞–њ–Є—Б–Є –∞–≥—А–µ–≥–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –љ–∞ –ї–∞–Ј–µ—А–љ–Њ–Љ –∞–≥—А–µ–≥–Њ–Љ–µ—В—А–µ вАУ Aggregation Analyser вАУ Biola Ltd (–Ѓ–љ–Є–Љ–µ–і, –Ь–Њ—Б–Ї–≤–∞) –њ–Њ –Љ–µ—В–Њ–і—Г Born –≤ –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є OвАЩBrien. –Т –Ї–∞—З–µ—Б—В–≤–µ –Є–љ–і—Г–Ї—В–Њ—А–∞ –∞–≥—А–µ–≥–∞—Ж–Є–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –Р–Ф–§ (—Д–Є—А–Љ–∞ Serva, –§—А–∞–љ—Ж–Є—П) –≤ –Ї–Њ–љ–µ—З–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є 0,1 –Љ–Ї–Љ.
–≠–ї–µ–Ї—В—А–Њ—Д–Њ—А–µ—В–Є—З–µ—Б–Ї—Г—О –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В—М —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ (–≠–§–Я–≠) –Њ–њ—А–µ–і–µ–ї—П–ї–Є –љ–∞ —Ж–Є—В–Њ—Д–Њ—В–Њ–Љ–µ—В—А–µ Opton –≤ —А–µ–ґ–Є–Љ–µ I=5 –Љ–Р, V=100 B, t=25¬∞. –Я–µ—А–µ–і–≤–Є–ґ–µ–љ–Є–µ —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ —А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Є –≤ —Д–∞–Ј–Њ–≤–ЊвАУ–Ї–Њ–љ—В—А–∞—Б—В–љ–Њ–Љ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–µ –њ—А–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –≤ 800 —А–∞–Ј. –≠–§–Я–≠ –≤—Л—З–Є—Б–ї—П–ї–Є –њ–Њ —Д–Њ—А–Љ—Г–ї–µ: B=I/(t вАҐ E), –≥–і–µ I вАУ –њ—Г—В—М —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ –≤ —Б–µ—В–Ї–µ –Њ–Ї—Г–ї—П—А–∞ вАУ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–∞ –≤ –Њ–і–љ—Г —Б—В–Њ—А–Њ–љ—Г (—Б–Љ), t вАУ –≤—А–µ–Љ—П –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є—П (—Б), E вАУ –љ–∞–њ—А—П–ґ–µ–љ–љ–Њ—Б—В—М —Н–ї–µ–Ї—В—А–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ–ї—П (B/—Б–Љ). –Т –Ї–∞–ґ–і–Њ–Љ —Б–ї—Г—З–∞–µ —А–∞—Б—З–Є—В—Л–≤–∞–ї–∞—Б—М —Б–Ї–Њ—А–Њ—Б—В—М –Љ–Є–≥—А–∞—Ж–Є–Є 20вАУ30 —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤. –Э–Њ—А–Љ–∞–ї—М–љ–∞—П –≤–µ–ї–Є—З–Є–љ–∞ –≠–§–Я–≠ вАУ 1,128¬±0,018 –Љ–Ї–Љ/c–Љ/—БвАУ1 /BвАУ1.
–£—А–Њ–≤–µ–љ—М –Њ–±—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ (–Ю–•–°), —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і–Њ–≤ –≤—Л—Б–Њ–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є (–•–° –Ы–Я–Т–Я) –Є —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –Њ–њ—А–µ–і–µ–ї—П–ї–Є —Н–љ–Ј–Є–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ –Љ–µ—В–Њ–і–Њ–Љ –љ–∞ –∞–≤—В–Њ–∞–љ–∞–ї–Є–Ј–∞—В–Њ—А–µ FMвАУ901 (Labsystems вАУ –§–Є–љ–ї—П–љ–і–Є—П) —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —А–µ–∞–Ї—В–Є–≤–Њ–≤ —Д–Є—А–Љ—Л Randox (–§—А–∞–љ—Ж–Є—П). –Ъ–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і–Њ–≤ –Њ—З–µ–љ—М –љ–Є–Ј–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є (–•–° –Ы–Я–Ю–Э–Я) –Є —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і–Њ–≤ –љ–Є–Ј–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є (–•–° –Ы–Я–Э–Я) –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ —А–∞—Б—Б—З–Є—В—Л–≤–∞–ї–Є –њ–Њ —Д–Њ—А–Љ—Г–ї–µ Friedewald W.T. (1972):
–•–° –Ы–Я–Ю–Э–Я = –Ґ–У/2,2
–•–° –Ы–Я–Э–Я = –Ю–•–° вАУ (–•–° –Ы–Я–Ю–Э–Я + –•–° –Ы–Я–Т–Я).
–†–∞—Б—З–µ—В –Є–љ–і–µ–Ї—Б–∞ –∞—В–µ—А–Њ–≥–µ–љ–љ–Њ—Б—В–Є (–Ш–Р) –њ—А–Њ–≤–Њ–і–Є–ї–Є –њ–Њ —Д–Њ—А–Љ—Г–ї–µ –Р.–Ш. –Ъ–ї–Є–Љ–Њ–≤–∞ (1977):
–Ш–Р = (OXC вАУ –•–° –Ы–Я–Т–Я) /–•–° –Ы–Я–Т–Я.
–Ъ–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О —Д–Є–±—А–Є–љ–Њ–≥–µ–љ–∞ –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є –Њ–њ—А–µ–і–µ–ї—П–ї–Є —Д–Њ—В–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є —Б —В—Г—А–±–Њ–і–Є–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–Љ –Љ–µ—В–Њ–і–Њ–Љ —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є ¬ЂFibrintimer¬ї (–У–µ—А–Љ–∞–љ–Є—П), —Б –њ–Њ–Љ–Њ—Й—М—О –Ї–Њ–Љ¬≠–Љ–µ—А—З–µ—Б–Ї–Є—Е –љ–∞–±–Њ—А–Њ–≤ ¬ЂMultifibrin Test вАУ Kit¬ї (Behring AG).
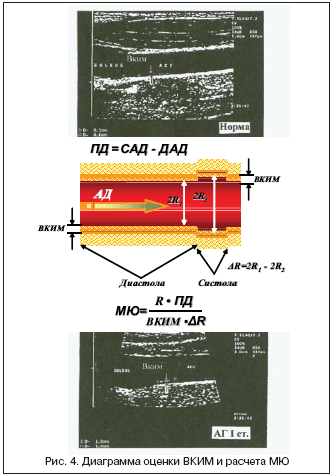
–Т–µ–ї–Є—З–Є–љ—Г –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –Є–љ—В–Є–ЉвАУ–Љ–µ–і–Є–∞ (–Т–Ъ–Ш–Ь) –і–Є—Б—В–∞–ї—М–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤ –Њ–±—Й–µ–є —Б–Њ–љ–љ–Њ–є –∞—А—В–µ—А–Є–Є (–Ю–°–Р) –Є –Њ–±—Й–µ–є –±–µ–і—А–µ–љ–љ–Њ–є –∞—А—В–µ—А–Є–Є (–Ю–С–Р) –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –і–Њ–њ–њ–ї–µ—А –£–ЧвАУ–Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ –≤ –ТвАУ—А–µ–ґ–Є–Љ–µ –њ–Њ –Љ–µ—В–Њ–і–Є–Ї–µ Pignolli (1986) –љ–∞ –∞–њ–њ–∞—А–∞—В–µ ELEGRA —Д–Є—А–Љ—Л Siemens –ї–Є–љ–µ–є–љ—Л–Љ –і–∞—В—З–Є–Ї–Њ–Љ 5вАУ10 –Љ–У—Ж. –†–∞—Б—З–µ—В –Љ–Њ–і—Г–ї—П –Ѓ–љ–≥–∞ (–Ь–Ѓ) вАУ –Њ—В–љ–Њ—И–µ–љ–Є–µ –љ–∞–≥—А—Г–Ј–Ї–Є (—Б–Є–ї–∞ –љ–∞ –µ–і–Є–љ–Є—Ж—Г –њ–ї–Њ—Й–∞–і–Є —Б–Њ—Б—Г–і–∞) –Ї —А–∞—Б—В—П–ґ–µ–љ–Є—О (–Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–µ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –ї–Є–љ–µ–є–љ–Њ–≥–Њ —А–∞—Б—Б—В–Њ—П–љ–Є—П, –Њ–њ—А–µ–і–µ–ї—П–µ–Љ–Њ–≥–Њ –≤–і–Њ–ї—М –≤–µ–Ї—В–Њ—А–∞ —Б–Є–ї–∞вАУ–≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ) –њ—А–Њ–≤–Њ–і–Є–ї–Є –њ–Њ —Д–Њ—А–Љ—Г–ї–µ:
–†–∞—Б—З—С—В –Љ–Њ–і—Г–ї—П –Ѓ–љ–≥–∞ (–Ь–Ѓ). –§–Њ—А–Љ—Г–ї–∞
–≥–і–µ R вАУ —А–∞–і–Є—Г—Б –∞—А—В–µ—А–Є–Є; –Т–Ъ–Ш–Ь вАУ –≤–µ–ї–Є—З–Є–љ–∞ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –Є–љ—В–Є–ЉвАУ–Љ–µ–і–Є–∞; –Я–Ф вАУ –њ—Г–ї—М—Б–Њ–≤–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ; –Ш–Ф–Р вАУ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –і–Є–∞–Љ–µ—В—А–∞ –∞—А—В–µ—А–Є–Є –Ј–∞ –Њ–і–Є–љ —Б–µ—А–і–µ—З–љ—Л–є —Ж–Є–Ї–ї (—А–Є—Б. 4).
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
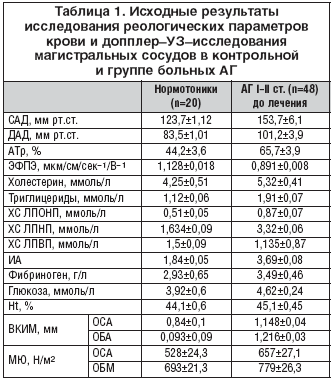
–°—Г–Љ–Љ–∞—А–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Е–Њ–і–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –Є –±–Њ–ї—М–љ—Л—Е –Р–У –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 1. –Ю–±—А–∞—Й–∞–µ—В –љ–∞ —Б–µ–±—П –≤–љ–Є–Љ–∞–љ–Є–µ –Є—Б—Е–Њ–і–љ–Њ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–µ –∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –≤ –≥—А—Г–њ–њ–µ –њ–∞¬≠—Ж–Є¬≠–µ–љ—В–Њ–≤ —Б –Р–У –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –љ–Њ—А–Љ–Њ—В–Њ–љ–Є–Ї–∞–Љ–Є: —Г –љ–Њ—А–Љ–Њ—В–Њ–љ–Є–Ї–Њ–≤ –Р–Ґ—А вАУ 44,2¬±3,6%, —Б—Г–Љ–Љ–∞—А–љ–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б –Р–У вАУ 68,5¬±6,7%, —В.–µ. –љ–∞ 55% –±–Њ–ї—М—И–µ (—А–∞–Ј–љ–Є—Ж–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–∞ –њ–Њ —В—А–µ—В—М–µ–Љ—Г –њ–Њ—А–Њ–≥—Г –≤–µ—А–Њ—П—В–љ–Њ—Б—В–Є –±–µ–Ј–Њ—И–Є–±–Њ—З–љ–Њ–≥–Њ –њ—А–Њ–≥–љ–Њ–Ј–∞ вАУ p<0,001). –Р–љ–∞–ї–Њ–≥–Є—З–љ–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –≠–§–Я–≠ –≤ –≥—А—Г–њ¬≠–њ–µ –±–Њ–ї—М–љ—Л—Е —Б –Р–У –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –љ–Њ—А–Љ–Њ—В–Њ–љ–Є–Ї–∞–Љ–Є: –≤ –≥—А—Г–њ¬≠–њ–µ –љ–Њ—А–Љ–Њ—В–Њ–љ–Є–Ї–Њ–≤ вАУ 1,128¬±0,018 –Љ–Ї–Љ/—Б–Љ/—БвАУ1/–ТвАУ1, —Б—Г–Љ¬≠–Љ–∞—А–љ–Њ –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–У вАУ 0,872¬±0,012 –Љ–Ї–Љ/—Б–Љ/—БвАУ1/–ТвАУ1 (—А–∞–Ј–љ–Є—Ж–∞ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–∞ –њ–Њ –≤—В–Њ—А–Њ–Љ—Г –њ–Њ—А–Њ–≥—Г –≤–µ—А–Њ—П—В–љ–Њ—Б—В–Є –±–µ–Ј–Њ—И–Є–±–Њ—З–љ–Њ–≥–Њ –њ—А–Њ–≥–љ–Њ–Ј–∞ вАУ —А<0,01), —В.–µ. –љ–Є–ґ–µ –љ–∞ 42,3%.
–°—Г–Љ–Љ–∞—А–љ—Л–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –ї–Є–њ–Є–і–љ–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П (–Ш–Р) —В–∞–Ї–ґ–µ –±—Л–ї –њ–Њ–≤—Л—И–µ–љ –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е —Б –Р–У –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–Њ–є –њ–Њ—З—В–Є –≤–і–≤–Њ–µ (–љ–∞ 95%): 1,84¬±0,05, 3,59¬±0,09 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ (—А<0,001). –Я–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Г—А–Њ–≤–љ–µ–є —Д–Є–±—А–Є–љ–Њ–≥–µ–љ–∞ –Є –≥–ї—О–Ї–Њ–Ј—Л –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –Є –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –љ–µ –Њ—В–ї–Є—З–∞–ї–Є—Б—М –і—А—Г–≥ –Њ—В –і—А—Г–≥–∞, —Е–Њ—В—П –Њ—В–Љ–µ—З–µ–љ–∞ —В–µ–љ–і–µ–љ—Ж–Є—П –≤ —Б—В–Њ—А–Њ–љ—Г —Г–≤–µ–ї–Є—З–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б –Р–У.
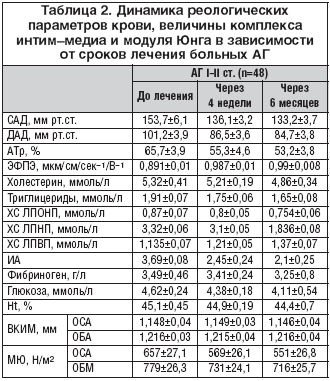
–Т —В–∞–±–ї–Є—Ж–µ 2 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –і–Є–љ–∞–Љ–Є–Ї–∞ —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –Ї—А–Њ–≤–Є –Є —Б–Њ—Б—В–Њ—П–љ–Є—П —А–µ–Ј–Є—Б—В–Є–≤–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –≤ —А–∞–Ј–ї–Є—З–љ—Л–µ —Б—А–Њ–Ї–Є –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е –Р–У –С–Є—Б–Њ–≥–∞–Љ–Љ–Њ–є¬Ѓ. –Ъ–∞–Ї –≤–Є–і–љ–Њ –Є–Ј —В–∞–±–ї–Є—Ж—Л, –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е –Р–У —З–µ—А–µ–Ј 4 –љ–µ–і. –Є 6 –Љ–µ—Б. –ї–µ—З–µ–љ–Є—П –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —Б–ї–µ–і—Г—О—Й–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ —Б–Њ —Б—В–Њ—А–Њ–љ—Л –°–Р–Ф –Є –Ф–Р–Ф: –°–Р–Ф –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–Є–ї–Њ—Б—М –љ–∞ 11,5 –Є 13,3%, –Ф–Р–Ф вАУ –љ–∞ 14,5 –Є 16,3% (—А<0,05). –Т —Б—А–µ–і–љ–µ–Љ –њ–Њ –≥—А—Г–њ–њ–µ –±—Л–ї–Є –і–Њ—Б—В–Є–≥–љ—Г—В—Л —Ж–µ–ї–µ–≤—Л–µ —Г—А–Њ–≤–љ–Є –Р–Ф: –°–Р–Ф вАУ 133,2¬±3,7 –Љ–Љ —А—В.—Б—В., –Ф–Р–Ф вАУ 84,7¬±3,8 –Љ–Љ —А—В.—Б—В.
–Р–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ–µ –≤ —А–∞–Ј–љ—Л–µ —Б—А–Њ–Ї–Є –љ–∞–±–ї—О–і–µ–љ–Є—П —Б–љ–Є–Ј–Є–ї–∞—Б—М –љ–∞ 15,8 –Є 19% (—А<0,05). –Т—Л—П–≤–ї–µ–љ–∞ —В–µ—Б–љ–∞—П –њ—А—П–Љ–∞—П –Ї–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ–∞—П —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –і–Є–љ–∞–Љ–Є–Ї–Њ–є —Г—А–Њ–≤–љ–µ–є –Р–Ґ—А –Є –Р–Ф: r–Р–Ґ—А вАУ –°–Р–Ф = 0,67 –Є r–Р–Ґ—А вАУ –Ф–Р–Ф = 0,72 (—А<0,01).
–≠–§–Я–≠ –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ–µ –њ–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ —Г–≤–µ–ї–Є—З–Є–ї–∞—Б—М –љ–∞ 10,8 –Є 11,1% (—А<0,05). –£–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–Ї–Њ—А–Њ—Б—В–Є –≠–§–Я–≠ –љ–∞—Е–Њ–і–Є—В—Б—П –≤ —В–µ—Б–љ–Њ–є –Њ–±—А–∞—В–љ–Њ–є –Ї–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ–Њ–є —Б–≤—П–Ј–Є —Б –і–Є–љ–∞–Љ–Є–Ї–Њ–є —Г—А–Њ–≤–љ—П –Р–Ф: r–≠–§–Я–≠вАУ–°–Р–Ф = вАУ0,56, r–≠–§–Я–≠вАУ–Ф–Р–Ф = вАУ0,78 (—А<0,01). –Ъ–∞—З–µ—Б—В–≤–Њ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ –љ–∞—Е–Њ–і–Є—В—Б—П –≤ —В–µ—Б–љ–Њ–є –Ї–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ–Њ–є —Б–≤—П–Ј–Є —Б –Ш–Р (—Б—Г–Љ–Љ–∞—А–љ–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –Ї—А–Њ–≤–Є): r–≠–§–Я–≠ вАУ –Ш–Р = вАУ0,74 (—А<0,01).
–Я—А–Є –ї–µ—З–µ–љ–Є–Є –С–Є—Б–Њ–≥–∞–Љ–Љ–Њ–є¬Ѓ –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –Ш–Р (—Б —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–є –≥–Є–њ–Њ–ї–Є–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–µ–є —Б—В–∞—В–Є–љ–∞–Љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Г—А–Њ–≤–љ–µ–Љ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ >5 –Љ–Љ–Њ–ї—М/–ї) –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ –љ–∞ 43,2 –Є –љ–∞ 50,6%, –Ј–∞ —Б—З–µ—В —Б–љ–Є–ґ–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –љ–∞ 12,4 –Є 15,1%, –•–Ы–Я–Э–Я вАУ –љ–∞ 34,5 –Є 40,9% –Є —Г–≤–µ–ї–Є—З–µ–љ–Є—П –•–Ы–Я–Т–Я –љ–∞ 29,7% –Є 30,6% (—А<0,01). –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Є (–≤ —Б—В–Њ—А–Њ–љ—Г —Г–Љ–µ–љ—М—И–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є) –њ–Њ —Б–Њ–і–µ—А–ґ–∞–љ–Є—О —Д–Є–±—А–Є–љ–Њ–≥–µ–љ–∞ –Є –≥–ї—О–Ї–Њ–Ј—Л –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –љ–µ –њ–Њ–ї—Г—З–µ–љ–Њ. –Ю—В–Љ–µ—З–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –љ–µ–і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є Ht —Б 45,1¬±0,45% –і–Њ 44,4¬±0,7% (—А>0,05).
–Т–Ъ–Ш–Ь –≤ –Ю–°–Р –Є –Ю–С–Р –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –љ–µ –Њ—В–ї–Є—З–∞–ї—Б—П –Њ—В –Є—Б—Е–Њ–і–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П (—А>0,05) –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –њ—А–Њ–≥—А–∞–Љ–Љ—Л –ї–µ—З–µ–љ–Є—П, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–Љ —Н—Д—Д–µ–Ї—В–µ –С–Є—Б–Њ–≥–∞–Љ–Љ—Л¬Ѓ –≤ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–Є —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П —А–µ–Ј–Є—Б—В–Є–≤–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е –Р–У.
–Ь–Ѓ вАУ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –ґ–µ—Б—В–Ї–Њ—Б—В–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є, –Ї–Њ—Б–≤–µ–љ–љ–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –і–Є–ї–∞—В–∞—Ж–Є–Њ–љ–љ–Њ–Љ —А–µ–Ј–µ—А–≤–µ —Б–Њ—Б—Г–і–Њ–≤. –Т –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ–µ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –С–Є—Б–Њ¬≠–≥–∞–Љ–Љ–Њ–є¬Ѓ –Ь–Ѓ –і–ї—П –Ю–°–Р –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–Є–ї—Б—П –љ–∞ 13,4 –Є 16,1%, –і–ї—П –Ю–С–Р вАУ –љ–∞ 6,2 –Є –љ–∞ 8,1% (—А<0,05), —З—В–Њ —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г –≤ —Б—В–Њ—А–Њ–љ—Г —Г–≤–µ–ї–Є—З–µ–љ–Є—П –і–Є–ї–∞—В–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ —А–µ–Ј–µ—А–≤–∞ –≤ —А–µ–Ј–Є—Б—В–Є–≤–љ—Л—Е –∞—А—В–µ—А–Є—П—Е.
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤
–°–Њ–≥–ї–∞—Б–љ–Њ –Э–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ –њ–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є—О –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–Є [4], –њ–µ—А–≤–Є—З–љ–∞—П —Ж–µ–ї—М –≤ –ї–µ—З–µ–љ–Є–Є –Р–У вАУ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Њ–±—Й–µ–≥–Њ —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–ЊвАУ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≤ –Њ—В–і–∞–ї–µ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ. –Ф–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Ж–µ–ї–Є —В—А–µ–±—Г–µ—В —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Р–Ф <140/90 –≤ –Њ–±—Й–µ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є –±–Њ–ї—М–љ—Л—Е –Р–У, –∞ —В–∞–Ї–ґ–µ –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –≤—Б–µ—Е –Њ–±—А–∞—В–Є–Љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –љ–∞—И–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П вАУ –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П (<135/85), —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—Й–Є–µ –Њ–± —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–Љ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–Љ —Н—Д—Д–µ–Ї—В–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–µ–є –С–Є—Б–Њ–≥–∞–Љ–Љ–Њ–є¬Ѓ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –≤ 89,6% –љ–∞–±–ї—О–і–µ–љ–Є–є (—Г 43 –Є–Ј 48 –њ–∞—Ж–Є–µ–љ—В–Њ–≤).
–°–Њ–≥–ї–∞—Б–љ–Њ —Б—Г—Й–µ—Б—В–≤—Г—О—Й–µ–є —Д–Њ—А–Љ—Г–ї–µ –Р–Ф=–Ь–Ю–°√Ч–Я–°–°, —Г—А–Њ–≤–µ–љ—М –Р–Ф –ї–Є–љ–µ–є–љ–Њ –Ј–∞–≤–Є—Б–Є—В –љ–µ —В–Њ–ї—М–Ї–Њ –Њ—В —Б–Њ—Б—В–Њ—П–љ–Є—П –љ–∞—Б–Њ—Б–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є —Б–µ—А–і—Ж–∞, –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ –Ї–Њ—В–Њ—А–Њ–є —П–≤–ї—П–µ—В—Б—П –Љ–Є–љ—Г—В–љ—Л–є –Њ–±—К–µ–Љ, –љ–Њ –Є –Њ—В –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П (–Я–°–°), –Ї–Њ—В–Њ—А–Њ–µ –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, —Б–Њ–≥–ї–∞—Б–љ–Њ —Г–њ—А–Њ—Й–µ–љ–љ–Њ–є —Д–Њ—А–Љ—Г–ї–µ –Я—Г–∞–Ј–µ–є–ї—П, –Ј–∞–≤–Є—Б–Є—В –Њ–±—А–∞—В–љ–Њ –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ–Њ –Њ—В —В–Њ–љ—Г—Б–∞ —Б–Њ—Б—Г–і–Њ–≤, –Ї–Њ—В–Њ—А—Л–є –Њ–њ—А–µ–і–µ–ї—П–µ—В –і–Є–∞–Љ–µ—В—А –њ—А–Њ—Б–≤–µ—В–∞ —Б–Њ—Б—Г–і–Њ–≤, –љ–Њ –Є –њ—А—П–Љ–Њ –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ–Њ вАУ –Њ—В –і–ї–Є–љ—Л —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —А—Г—Б–ї–∞ –Є –≤—П–Ј–Ї–Њ—Б—В–љ—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –Ї—А–Њ–≤–Є, —В.–µ. –Њ—В —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –Ї—А–Њ–≤–Є: –Ю–Я–°–° = L√ЧќЈ/S, –≥–і–µ S вАУ –њ–ї–Њ—Й–∞–і—М –њ—А–Њ—Б–≤–µ—В–∞ —Б–Њ—Б—Г–і–Њ–≤, L вАУ –і–ї–Є–љ–∞ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —А—Г—Б–ї–∞, ќЈ вАУ –≤—П–Ј–Ї–Њ—Б—В—М –Ї—А–Њ–≤–Є. –†–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –Ї—А–Њ–≤–Є –≤–Ї–ї—О—З–∞—О—В –≤ —Б–µ–±—П –≥–ї—О–Ї–Њ–Ј–ЊвАУ–±–µ–ї–Ї–Њ–≤–ЊвАУ–ї–Є–њ–Є–і–љ—Л–є —Б–Њ—Б—В–∞–≤, –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ (Ht) –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ —Д–Њ—А–Љ–µ–љ–љ—Л—Е —Н–ї–µ–Љ–µ–љ—В–Њ–≤, –Ї–Њ–∞–≥—Г–ї—П—Ж–Є–Њ–љ–љ—Л–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї.
–Ю–±—Й–µ–Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е ќ≤вАУ–∞–і¬≠—А–µ¬≠–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –С–Є—Б–Њ–≥–∞–Љ–Љ—Л¬Ѓ, –≤ –ї–µ—З–µ–љ–Є–Є –Р–У –љ–∞–њ—А–∞–≤–ї–µ–љ–Њ –љ–∞ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ь–Ю –Ј–∞ —Б—З–µ—В –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ —Е—А–Њ–љ–Њ—В—А–Њ–њ–љ–Њ–≥–Њ –Є –Є–љ–Њ—В—А–Њ–њ–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–Њ–≤ (—В.–µ. —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –£–Ю –Є –І–°–°, —В.–Ї. –Ь–Ю = –£–Ю√Ч–І–°–°). –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –і–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–µ –∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –≤–љ–Њ—Б–Є—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–є –≤–Ї–ї–∞–і –≤ –њ–Њ–≤—Л—И–µ–љ–Є–µ –Р–Ф вАУ —З–µ—А–µ–Ј —Б–µ–Ї—А–µ—Ж–Є—О —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–∞ –Р2, –Љ–Њ—Й–љ–Њ–≥–Њ –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—В–Њ—А–∞. –Ґ—А–Њ–Љ–±–Њ—Ж–Є—В вАУ —Б–ї–Њ–ґ–љ–∞—П –њ–Њ —Б—В—А—Г–Ї—В—Г—А–µ –Є —Д—Г–љ–Ї—Ж–Є–Є –Ї—А–Њ–≤—П–љ–∞—П –Ї–ї–µ—В–Ї–∞, —А–µ–∞–ї–Є–Ј—Г–µ—В —Б–≤–Њ–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ —З–µ—А–µ–Ј –∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А—Л, –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ –Ї–∞—А–і–Є–Њ–Љ–Є–Њ—Ж–Є—В–∞–Љ –Є –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л–Љ –Ї–ї–µ—В–Ї–∞–Љ —Б–Њ—Б—Г–і–Њ–≤. –Я–Њ—Н—В–Њ–Љ—Г –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ ќ≤вАУ–∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Р–У –Њ–Ї–∞–Ј—Л–≤–∞–µ—В —Н—Д—Д–µ–Ї—В ¬Ђ—Г—Б–њ–Њ–Ї–Њ–µ–љ–Є—П¬ї —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –і–µ–ї–∞—П –Є—Е –љ–µ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ–Є –Ї –Ї–∞—В–µ—Е–Њ–ї–∞–Љ–Є–љ–∞–Љ, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —А—П–і–∞ –∞–≤—В–Њ—А–Њ–≤ –Є –љ–∞—И–Є–Љ–Є –љ–∞–±–ї—О–і–µ–љ–Є—П–Љ–Є. –Т –љ–∞—И–Є—Е –љ–∞–±–ї—О–і–µ–љ–Є—П—Е –њ–Њ—Б–ї–µ 4вАУ–љ–µ–і–µ–ї—М–љ–Њ–≥–Њ –Є 6вАУ—В–Є –Љ–µ—Б—П—З–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –С–Є—Б–Њ–≥–∞–Љ–Љ–Њ–є¬Ѓ –±–Њ–ї—М–љ—Л—Е —Б –Р–У –Њ—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ —Б—Г–Љ–Љ–∞—А–љ–Њ –њ–Њ –≤—Б–µ–є –≥—А—Г–њ–њ–µ –љ–∞ 15,8 –Є –љ–∞ 19%, –Ї–Њ—Б–≤–µ–љ–љ–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—Й–µ–µ –Њ –љ–∞–ї–Є—З–Є–Є –≤ —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ–µ ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Ю–і–љ–Њ–≤—А–µ¬≠–Љ–µ–љ–љ–Њ –≤—Л—П–≤–ї–µ–љ–∞ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–∞—П –Ї–Њ—А—А–µ–ї—П—Ж–Є–Њ–љ–љ–∞—П —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г —Г—А–Њ–≤–љ—П–Љ–Є –°–Р–Ф, –Ф–Р–Ф –Є –∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ—Л–Љ —Б–Њ—Б—В–Њ—П–љ–Є–µ–Љ —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤: r –Р–Ґ—А вАУ –Ф–Р–Ф = 0,72 (—А<0,001), r –Р–Ґ—А вАУ –°–Р–Ф = 0,67 (—А<0,01). –£–≤–µ–ї–Є—З–µ–љ–Є–µ –≠–§–Я–≠ —Б—Г–Љ–Љ–∞—А–љ–Њ –њ–Њ –≤—Б–µ–є –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е –Р–У –љ–∞ 14,6% –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –С–Є—Б–Њ–≥–∞–Љ–Љ–Њ–є¬Ѓ, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–Њ —З–µ—А–µ–Ј –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—О –ї–Є–њ–Є–і–љ–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П –≤ —Б—В–Њ—А–Њ–љ—Г –∞–љ—В–Є–∞—В–µ—А–Њ–≥–µ–љ–љ–Њ—Б—В–Є.
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –љ–∞—А—Г—И–µ–љ–Є—П –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–Њ—Б—В–∞–≤–∞ —Н—А–Є—В—А–Њ—Ж–Є—В–∞—А–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ —П–≤–ї—П—О—В—Б—П –Њ–і–љ–Њ–є –Є–Ј –њ—А–Є—З–Є–љ —Б–љ–Є–ґ–µ–љ–Є—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ –Ї –і–µ—Д–Њ—А–Љ–∞—Ж–Є–Є, –∞ —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –Ї –љ–∞—А—Г—И–µ–љ–Є—О –Є—Е –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –Є –≤ —Ж–µ–ї–Њ–Љ вАУ —В–µ–Ї—Г—З–µ—Б—В–Є –Ї—А–Њ–≤–Є, —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –њ–Њ–≤—Л—И–µ–љ–Є—О –Я–°–° –Є –Р–Ф. –Э–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П –ї–Є–њ–Є–і–љ–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П —Г –±–Њ–ї—М–љ—Л—Е –Р–У –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –С–Є—Б–Њ–≥–∞–Љ–Љ–Њ–є¬Ѓ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –љ–∞—И–Є—Е –љ–∞–±–ї—О–і–µ–љ–Є–є: –Ш–Р —Б–љ–Є–Ј–Є–ї—Б—П –љ–∞ 43,1% (—А<0,001) –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Ј–∞ —Б—З–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—П –•–Ы–Я–Т–Я –љ–∞ 29,7% –Є —Б–љ–Є–ґ–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –•–° –Ы–Я–Э–Я –љ–∞ 34,5% (—А<0,001). –Р–љ–∞–ї–Њ–≥–Є—З–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –њ–Њ–ї—Г—З–µ–љ–∞ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –і—А—Г–≥–Є—Е –∞–≤—В–Њ—А–Њ–≤ [18,19], —З—В–Њ —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –≤ –ї–µ—З–µ–љ–Є–Є –Р–У –С–Є—Б–Њ–≥–∞–Љ–Љ—Л¬Ѓ (–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є –љ–µ–є—В—А–∞–ї–µ–љ), –і–µ–є—Б—В–≤—Г—О—Й–Є–Љ –љ–∞—З–∞–ї–Њ–Љ –Ї–Њ—В–Њ—А–Њ–≥–Њ —П–≤–ї—П–µ—В—Б—П –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї, –њ–µ—А–µ–і –і—А—Г–≥–Є–Љ–Є ќ≤вАУ–∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –Є–Ј–Љ–µ–љ—П—В—М –ї–Є–њ–Є–і–љ—Л–є –њ—А–Њ—Д–Є–ї—М –≤ —Б—В–Њ—А–Њ–љ—Г –∞—В–µ—А–Њ–≥–µ–љ–љ–Њ—Б—В–Є. –Ч–∞ –њ–µ—А–Є–Њ–і 6вАУ–Љ–µ—Б—П—З–љ–Њ–≥–Њ –љ–∞–±–ї—О–і–µ–љ–Є—П –љ–µ –±—Л–ї–Њ —В–∞–Ї–ґ–µ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ —Б–ї—Г—З–∞–µ–≤ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Г–≥–ї–µ–≤–Њ–і–љ–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П –Ї—А–Њ–≤–Є (—Б—А–µ–і–љ–Є–є —Г—А–Њ–≤–µ–љ—М –≥–ї—О–Ї–Њ–Ј—Л –і–Њ –ї–µ—З–µ–љ–Є—П 4,62¬±0,24 –Љ–Љ–Њ–ї—М/–ї, –њ–Њ—Б–ї–µ 6 –Љ–µ—Б. –ї–µ—З–µ–љ–Є—П 4,11¬±0,54 –Љ–Љ–Њ–ї—М/–ї).
–Т –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —З–µ—А–µ–Ј 6 –Љ–µ—Б—П—Ж–µ–≤ –ї–µ—З–µ–љ–Є—П –С–Є—Б–Њ–≥–∞–Љ–Љ–Њ–є¬Ѓ –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–Њ–і—Г–ї—П –Ѓ–љ–≥–∞ –≤ –Ю–°–Р –Є –Ю–С–Р, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В —Г–ї—Г—З—И–µ–љ–Є–µ —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є –Є –Ї–Њ—Б–≤–µ–љ–љ–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–Є —А–µ–ї–∞–Ї—Б–∞—Ж–Є–Њ–љ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є —Н–љ–і–Њ—В–µ–ї–Є—П.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –С–Є—Б–Њ–≥–∞–Љ–Љ–∞¬Ѓ –≤ –њ—А–Њ–≥—А–∞–Љ–Љ–µ –ї–µ—З–µ–љ–Є—П –Р–У –Њ–±–ї–∞–і–∞–µ—В –Љ–љ–Њ–≥–Њ–њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ: –њ–Њ–Љ–Є–Љ–Њ –њ—А—П–Љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ —Б—В—А—Г–Ї—В—Г—А—Л –°–°–° –љ–Њ—А–Љ–∞–ї–Є–Ј—Г–µ—В —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –Ї—А–Њ–≤–Є, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Б–љ–Є–ґ–µ–љ–Є—О –Є–љ–і–µ–Ї—Б–∞ –∞—В–µ—А–Њ–≥–µ–љ–љ–Њ—Б—В–Є, —Г–ї—Г—З—И–µ–љ–Є—О —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є, —З—В–Њ —Б—Г–Љ–Љ–∞—А–љ–Њ –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј—Г–µ—В —Г—А–Њ–≤–µ–љ—М –Р–Ф, –∞ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–∞—П –љ–µ–є—В—А–∞–ї—М–љ–Њ—Б—В—М –Њ–њ—А–µ–і–µ–ї—П–µ—В –≤–µ–і—Г—Й–µ–µ –Љ–µ—Б—В–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–У.