Мерцательная аритмия (МА) является одним из наиболее тяжелых и распространенных нарушений сердечного ритма, встречается у 0,4% популяции в целом (М.С. Кушаковский, 1999) и более чем у 5% людей старше 69 лет (Braunwald, 1996). У подавляющего большинства МА приводит к появлению (или усугублению) сердечной недостаточности, которая, помимо исчезновения предсердной систолы, обусловлена собственно тахиаритмией, т.е. двумя слагаемыми: тахикардией и аритмией работы сердца (непродуктивные – слишком длинные и слишком короткие – диастолические паузы). При лечении МА общепринятой является необходимость уредить работу сердца (вторая составляющая – собственно аритмия – обычно, к сожалению, не учитывается). Известно, что урежение ритма сердца, действительно, сопровождается заметным уменьшением признаков СН. Имеются даже исследования (PIAF, 2000; AFFIRM, 2002), в которых показано, что с учетом таких конечных точек, как частота инсультов, инфарктов, тромбоэмболических и геморрагических осложнений, смертность, а также качество жизни, эффективное консервативное лечение МА (а это, в первую очередь, урежающая ритм терапия) не уступает тактике восстановления и сохранения синусового ритма. Однако эти данные получены на достаточно конкретной группе больных (пожилые люди со снижением сократительной функции сердца, с заведомо плохими шансами на стабильное поддержание синусового ритма и повышенным риском развития осложнений основного заболевания – распространенного атеросклероза и антиаритмической терапии), и их нельзя распространять на весь массив больных, страдающих МА.
Для урежения ритма при МА используют прежде всего препараты наперстянки, как наиболее эффективные и, казалось бы, достаточно изученные. Кроме того, применяются b-блокаторы, блокаторы кальциевых каналов, реже – препараты III класса антиаритмиков (амиодарон, d,l–соталол). В настоящее время некоторые авторы считают, что возможна даже монотерапия b-блокаторами или антагонистами кальция, как наиболее жесткими средствами урежения ритма. Чаще их все же рекомендуют добавлять к дигиталисным препаратам при недостаточном урежающем эффекте последних. При этом учитывают лучшую по сравнению с наперстянкой способность b-блокаторов и антагонистов кальция урежать ритм не только в покое, но и при физической нагрузке, а также возможность с помощью такой комбинированной терапии назначать меньшие дозы сердечных гликозидов с соответственно меньшим риском получить дигиталисную интоксикацию.
Подбор препаратов производят эмпирически, основываясь на существующих на сегодняшний день представлениях, что единственным патогенетическим механизмом урежающего действия этих средств является торможение проведения волн ff через атрио–вентрикулярную (АВ) систему (влияние на степень аритмии ритма сердца, как было сказано выше, вообще не учитывается).
К настоящему времени нами получены данные, позволяющие дополнить существующие представления о механизмах урежающего действия наперстянки и других препаратов. Начало этих работ было положено нами (А.В. Недоступ, Э.А. Богданова, А.А. Платонова) в середине 70–х годов [1–4] и продолжено (в соавт. с О.В. Благовой) в последние годы [5–9]. В соответствии с этим стал возможен более объективный подход к тактике урежающей ритм терапии при МА. Ниже приводим перечень новых положений, которые следует учитывать при урежающей ритм терапии у больных с МА.
1. При воздействии на сердце больного с МА сердечные гликозиды оказывают существенное влияние не только на проведение в АВ–системе, но также и на сам процесс мерцания предсердий, который характеризуется определенной величиной периода волн ff и обратной ему частоты. При этом у подавляющего большинства больных (около 80%) на первой стадии дигитализации происходит «измельчение» волн ff, т.е. уменьшение их периода с исходного 0,15–0,20 с. до 0,12–0,14 с. с соответствующим увеличением частоты мерцания. Этот процесс предшествует по времени воздействия наперстянки на АВ–систему и является ведущим механизмом урежения при среднем темпе дигитализации: поток более частых волн мерцания по закону парабиоза с бoльшим затруднением проходит через АВ–систему к желудочкам, следствием чего является замедление ритма сердца, прямо пропорциональное по степени исходному периоду волн ff.
2. Замедление АВ–проводимости при воздействии гликозидов достигается у большинства больных лишь на втором (более позднем) этапе и совпадает с появлением характерной «дигиталисной» кривой на ЭКГ, а затем желудочковой экстрасистолии и других проявлений гипердигитализации. Лишь у 20% больных, имеющих, как правило, исходно мелкие волны ff (с периодом 0,12–0,14 c.), их дальнейшего «измельчения» не происходит и прямое замедление АВ проводимости развивается на ранних этапах дигитализации.
3. Урежение желудочкового ритма у больных с МА под воздействием b-блокаторов и блокаторов кальциевых каналов достигается лишь благодаря их тормозящему эффекту на АВ проводимость (более сильному у b-блокаторов, которые дополнительно усиливают скрытое проведение через АВ соединение) – при этом отмечается значительное нарастание минимального интервала RR (RRmin), прямо отражающего при МА рефрактерность АВ узла. На предсердную активность эти препараты не влияют.
4. Антиаритмики III класса (амиодарон, d,l–соталол) урежают волны ff, вплоть до трансформации мерцания предсердий в трепетание, что облегчает их проведение через АВ систему, а с другой стороны, тормозят АВ проведение. Благодаря этим двум противонаправленным процессам урежение желудочкового ритма под воздействием этих препаратов умеренно выражено (сильнее – при назначении d,l–соталола ввиду его b-блокирующего действия, приводящего не только к возрастанию рефрактерности АВ–соединения, но и к усилению скрытого проведения в нем).
5. При МА монотерапия b-блокаторами или верапамилом приводит, наряду с урежением ритма, к отрицательным изменениям его структуры (нарастанию аритмичности, чередованию коротких и длинных интервалов RR, что субъективно плохо переносится больными). Эти изменения несколько менее выражены при назначении верапамила благодаря отсутствию у него влияния на скрытое проведение в АВ–узле. Благодаря более равномерному перераспределению интервалов RR в результате проведения на желудочки «измельченных» волн мерцания, назначение препаратов наперстянки сопровождается меньшим разбросом значений RR, структура желудочкового ритма при этом близка к оптимальной (симметричная мономодальная гистограмма интервалов RR).
6. У ряда больных со стойкой тахиаритмией, плохо поддающейся дигиталисной терапии, тахикардия бывает обусловлена наложением периодов частого, достаточно регулярного ритма («тахикардитические цепи»), которым на гистограмме интервалов RR соответствует пик в зоне коротких распределений RR («ранний» пик RR). Вероятно, при этом имеет место периодическое аномально быстрое проведение волн ff на желудочки или наличие периодов частого наджелудочкового ритма (эктопического или вследствие re–entry в АВ–узле и др. миокардиальных структурах). В таких случаях эффективное урежение ритма достигается амиодароном, воздействующим на все возможные механизмы формирования «раннего» пика; также могут оказаться эффективными d,l–соталол и b-блокаторы.
Из перечисленного выше при начале терапии МА очевидна необходимость учета исходных данных не только о частоте (и структуре) желудочкового ритма, но и о частоте волн ff. Ориентировочные данные о ней можно получить уже при анализе обычной ЭКГ в отведении V1 где хорошо видны волны мерцания. Период волн ff 0,15–0,20 с соответствует при записи со скоростью 25 мм/с ширине волн 3,5–5,0 мм. Точные данные можно получить с помощью специальной компьютерной программы, созданной для работы в среде Matlab 5,3 и позволяющей проводить анализ ЭКГ высокого разрешения в ортогональных отведениях по Франку (X, Y, Z). С помощью этой программы можно получить периодограмму волн ff, построить автокорреляционную функцию периодов волн ff, гистограмму интервалов RR, кардиоинтервалограмму и скатерограмму интервалов RR, рассчитать статистические параметры вариабельности желудочкового ритма.
Для практической работы (назначение терапии) достаточно периодограммы волн ff и гистограммы интервалов RR. Повторяем, что ориентировочный анализ предсердных волн ff может быть сделан по обычной ЭКГ; по ней же можно определить рефрактерность АВ–узла, соответствующую минимальному интервалу RR, и оценить структуру ритма – степень «разброса» интервалов RR и характер их чередования с выявлением периодов частого относительно регулярного ритма (лучше по данным Холтеровского мониторирования). Безусловно, при подборе терапии сохраняют свое значение широко известные клинические критерии – характер основного заболевания, сопутствующая патология, опыт предшествующей терапии и др. Однако без анализа особенностей самой МА терапия не может быть по–настоящему индивидуальной.
Наиболее общие принципы назначения урежающих ритм препаратов в зависимости от характера предсердной активности и желудочкового ритма таковы:
1. Наиболее рациональным является комбинированное назначение препаратов с различными механизмами урежающего действия: уменьшающего период волн ff дигоксина и лишь позднее тормозящего АВ–проведение – с препаратами, исключительно блокирующими АВ–проводимость (b-блокаторами, верапамилом), в отдельных случаях – с подавляющими желудочковую эктопию, нормальное и аномально быстрое АВ–проведение и эктопические наджелудочковые ритмы, амиодарона и d,l–соталола, хотя следует учитывать их одновременный нежелательный «укрупняющий» эффект на волны ff. Возможна и комбинация амиодарона с b-блокаторами, углубляющими замедление АВ–проводимости и снижающими риск развития желудочковых аритмий.
2. При наличии (или появлении на любом этапе терапии) волн ff крупных и средних периодов не удается достичь стабильного урежающего эффекта с получением оптимального по структуре ритма без «измельчения» волн ff с помощью препаратов наперстянки.
3. При наличии периодов частого относительно правильного ритма («тахикардитических цепей», которым соответствует «ранний» пик на гистограмме интервалов RR) урежающий эффект достигается лишь с помощью комбинированной терапии, включающей, как правило, дигоксин и антиаритмик III класса или b-блокатор.
На рисунке 1 представлен алгоритм индивидуального подбора урежающей терапии при постоянной форме МА в зависимости от ее исходных параметров. Прокомментируем этот алгоритм.
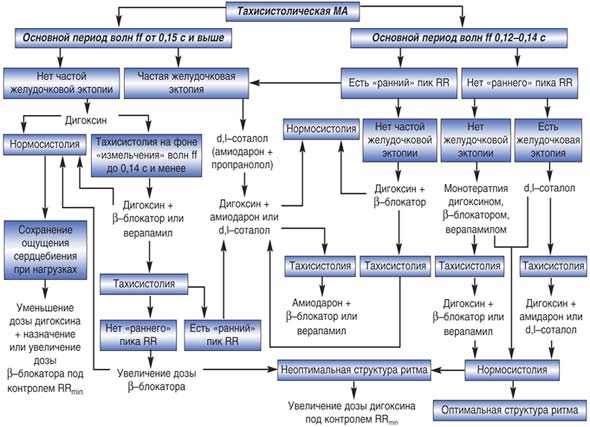
Рис. 1. Алгоритм подбора урежающей ритм терапии в зависимости от исходных параметров мерцательной аритмии
Как видно, при подборе терапии больным с тахисистолической формой МА прежде всего следует определить исходную величину периода волн ff.При ее значениях от 0,15 с и выше (средние и крупные волны ff) всем больным показано назначение сердечных гликозидов, которое в зависимости от наличия или отсутствия желудочковой экстрасистолии проводится сразу или после ее подавления. При этом важным фактором, определяющим успех монотерапии гликозидами, является (наряду со степенью исходной тахикардии) наличие «раннего» пика RR и его устойчивость к дигоксину.
А. При наличии крупных и средних волн ff (от 0,15 с) и отсутствии частой желудочковой экстрасистолии назначают дигоксин (средний темп дигитализации – 0,5 мг в сутки). При достижении нормосистолии (что сопровождается уменьшением периода волн ff, т. е. их учащением) и хорошем субъективном состоянии цель лечения достигнута. Если (что бывает чаще) сохраняется ощущение сердцебиения при нагрузках, к дигоксину добавляют b-блокатор (предварительно снизив дозу дигоксина), контролируя по динамике минимального интервала RR рефрактерность АВ–узла (RRmin должен находиться в пределах 50 мс и менее).
Если на фоне лечения дигоксином произошло уменьшение периода волн ff до 0,14 с и ниже, но сохраняется тахисистолия, к дигоксину (не уменьшая его дозы) добавляют также b-блокатор или верапамил, после чего можно получить хороший результат.
Если и после этого сохраняется тахисистолия и на этом фоне нет зон относительно ритмичной тахикардии («тахикардитических цепей», дающих «ранний» пик на гистограмме интервалов RR), следует увеличить дозу b-блокатора (не дигоксина). При хорошем эффекте (нормосистолия), но сохранении чувства сердцебиения при нагрузке можно еще раз осторожно увеличить дозу b-блокатора. При этом, однако, следует обращать внимание на ощущение больным «аритмичности» сердцебиения, свойственное терапии достаточно высокими дозами b-блокаторов. Если такое чувство имеется (лучше это подтвердить анализом гистограммы интервалов RR, на которой выявляется большой «разброс» значений RR), осторожно увеличивают дозу дигоксина, рассчитывая на этой стадии его назначения уже на замедление им АВ–проводимости (и, соответственно, контролируя значение RRmin, увеличение которого до 55–60 мс сигнализирует о глубоком торможении АВ–проводимости с угрозой развития полной АВ–блокады на фоне МА, т.е. синдрома Фридерика). Как правило, таким образом удается добиться достаточно регулярного нормосистолического ритма.
Если на фоне терапии дигоксином и b-блокатором сохраняется тахиаритмия и просматриваются участки «тахикардитических цепей» с соответствующим «ранним» пиком на гистограмме интервалов RR, не отменяя дигоксин, заменяют b-блокатор на амиодарон или d,l–соталол, обычно устраняющие участки ритмической тахикардии (при недостаточном на фоне лечения дигоксином и амиодароном урежении ритма вновь добавляют b-блокатор). При лечении дигоксином и амиодароном это обычно не требуется; если больной страдает бронхообструктивным синдромом, то вместо d,l–соталола или b-блокатора добавляют верапамил или дилтиазем.
Б. В случае исходной частой желудочковой экcтрасистолии у больных с исходной тахисистолией и периодом волн ff 0,15 с и выше назначают d,l–соталол или амиодарон (последний в сочетании с b-блокаторами). Лишь добившись исчезновения экстрасистолии, следует добавить дигоксин, который назначают обязательно, учитывая его способность «измельчать» волны ff и оптимизировать структуру ритма. При наличии частой желудочковой экстрасистолии на фоне уже проводящейся дигитализации, не приводящей к нормосистолии, отменяют препараты наперстянки, назначают d,l–соталол или амиодарон и, подавив желудочковую экстрасистолию, осторожно добавляют к лечению дигиталисные препараты.
Этими вариантами обычно исчерпываются ситуации, с которыми сталкивается врач, начинающий терапию при исходных волнах ff крупных и средних (0,15–0,20 с.) периодов (и, соответственно, небольшой и средней частоте предсердной активности).
При тахисистолии и исходном периоде волн ff 0,12–0,14 с («измельченных» волнах ff), что иногда бывает изначально свойственно ряду больных с МА, но чаще отмечается при уже проводимом лечении дигоксином, очевидно, что добиться необходимого урежения ритма назначением дигоксина (или наращиванием дигитализации) можно, лишь замедляя АВ–проводимость, т.к. на волны мерцания такой частоты препараты наперстянки уже не действуют. Тем не менее назначение дигоксина у большинства подобных больных является желательным:
1) для поддержания высокой частоты волн ff (особенно при одновременном назначении антиаритмиков III класса);
2) для оптимизации структуры ритма;
3) для достижения кардиотонического эффекта.
А. При наличии исходно «мелких» волн ff (0,12–0,14 с) в сочетании с отсутствием «раннего» пика RR («тахикардитических цепей» на ЭКГ) и желудочковой эктопии возможно осторожное проведение монотерапии дигоксином. Следует помнить о том, что на АВ–проводимость действуют лишь значительные дозы дигиталиса, близкие к токсичным, в связи с чем предпочтительнее комбинация дигоксина с b-блокаторами или верапамилом либо монотерапия последними. Получив нормосистолию с оптимальной структурой ритма, можно перейти к поддерживающей терапии. Если структура ритма неоптимальна (сохраняется большой «разброс» значений RR на фоне нормосистолии), осторожно увеличивают дозу дигоксина (контролируя значение RRmin и при необходимости снижая дозу b-блокаторов или верапамила).
Б. Если у больных с исходным периодом волн ff 0,12–0,14 с нет «раннего» пика RR, но есть желудочковая эктопия, лучше всего назначить d,l–соталол, который и устраняет желудочковую эктопию, и урежает ритм. Дигоксин можно добавить, лишь устранив желудочковую эктопию (если больной уже получает дигоксин, его следует отменить). Если d,l–соталол в этом отношении неэффективен, следует провести «кордаронизацию» (с возможным добавлением b-блокатора, помня о том, что амиодарон сам по себе плохо урежает ритм) и затем, устранив желудочковую эктопию, добавить дигоксин. Проведение постоянной монотерапии антиаритмиками III класса (особенно амиодароном) приведет к «укрупнению» волн ff с утратой или ослаблением урежающего эффекта, а также ухудшением структуры ритма. Еще раз напомним, что у больных с бронхообструкцией приходится «жертвовать» d,l–соталолом и b-блокаторами, заменяя их на амиодарон в сочетании с верапамилом.
В. При тахисистолии с исходным периодом волн ff 0,12–0,14 с и «ранним» пиком RR в отсутствие частой желудочковой эктопии можно попытаться осторожно наращивать дозу дигоксина в сочетании с b-блокатором. Если после этого зона ритмической тахикардии («цепи») сохраняется, дигоксин оставляют, заменяя b-блокатор на d,l–соталол или амиодарон, что, как правило, дает хороший эффект. При исчезновении «раннего» пика, но сохранении тахикардии, как уже указывалось, к комбинации «дигоксин–амиодарон» прибавляют b-блокатор (верапамил).
Г. При одновременном наличии «раннего» пика и желудочковой эктопии у больных с мелкими волнами ff имеются еще более веские основания для назначения амиодарона или d,l–соталола. При этом справедливо все вышесказанное о нежелательности монотерапии этими препаратами (при невозможности назначения дигоксина из–за неполного подавления желудочковой эктопии могут использоваться b-блокаторы).
Как видно из приведенных комментариев, несмотря на кажущуюся сложность алгоритма, количество возможных исходных вариантов МА и сопутствующих нарушений ритма не столь велико и поддается терапии в рамках более или менее стандартных правил.
В среде интернистов (еще до выделения кардиологии в отдельную дисциплину) всегда считалось, что лечение препаратами дигиталиса – одна из самых трудных терапевтических задач. Существовал даже афоризм: «Кто умеет лечить наперстянкой – тот может считаться врачом». Понятно, что это относилось, в особенности, к дигиталисной терапии больных с МА. Постепенно, с появлением ЭКГ, клинической фармакологии как самостоятельной дисциплины, «тайны» терапии наперстянкой стали раскрываться. Задача урежения ритма при мерцательной тахиаритмии еще более упростилась с введением в клинический обиход b-блокаторов, блокаторов кальциевых и калиевых каналов, хотя их появление поставило новые задачи – предпочтительной терапии для тех или иных больных, комбинирования медикаментов и т.д. И все же терапия мерцательной тахиаритмии до сих пор носит достаточно эмпирический характер.
Мы надеемся, что приведенные нами новые данные о механизме действия наперстянки при МА, как и другие наблюдения, лежащие в основе приведенных выше рекомендаций, послужат еще одной ступенью на пути оптимизации и научного подхода к терапевтической тактике при урежающей ритм терапии у больных с МА.
1. Егоров Д.Ф., Лещинский А.А., Недоступ А.В., Тюлькина Е.Е. Мерцательная аритмия (стратегия и тактика лечения на пороге XXI века). – Ижевск: Алфавит, 1998. – 413 с.
2. Недоступ А.В., Богданова Э.А., Михновский Е.И. Анализ структуры сердечного ритма при мерцании предсердий с помощью специализированной ЭВМ. Кардиология, 1975, №1: с.64–69.
3. Недоступ А.В., Богданова Э.А., Платонова А.А. и др.: Анализ структуры сердечного ритма при дигиталисной терапии больных с мерцательной аритмией. Кардиология, 1977, №4: с. 85–90.
4. Недоступ А.В., Богданова Э.А., Платонова А.А. Изучение процесса фибрилляции предсердий в клинической практике с применением статистических методов анализа. Кардиология, 1980, №10: с. 73–78.
5. Недоступ А.В., Благова О.В., Богданова Э.А., Платонова А.А. Значение анализа электрической активности предсердий при мерцательной аритмии для подбора урежающей ритм терапии // Тезисы конгресса «Кардиостим–2000». «Вестник аритмологии», 2000, №15: с. 53
6. А.В.Недоступ, О.В.Благова, Э.А.Богданова, А.А.Платонова. Возможности применения сочетанного анализа электрической активности предсердий и структуры желудочкового ответа у больных с постоянной формой мерцательной аритмии для контроля урежающей ритм терапии // «Progress in Biomedical Research», 2001, декабрь, Т.6, №1, Suppl. А: с. 26–35
7. А.В.Недоступ, О.В.Благова, Э.А.Богданова, А.А.Платонова. Медикаментозная урежающая терапия при мерцательной аритмии: новый подход к старой проблеме // «Терапевтический архив», 2002, №8: с. 35–42
8. А.В.Недоступ, О.В.Благова. Новый патогенетический подход к урежающей ритм терапии при мерцательной аритмии // «Врач», 2002, №12: с.12–16
9. А.В.Недоступ, О.В.Благова, Э.А.Богданова, А.А.Платонова. Коррекция частоты и структуры желудочкового ритма при постоянной форме мерцательной аритмии: комплексный патогенетический подход. «Кардиология», 2003, №12, с.












